预约演示
更新于:2026-06-06
ARO-INHBE
更新于:2026-06-06
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
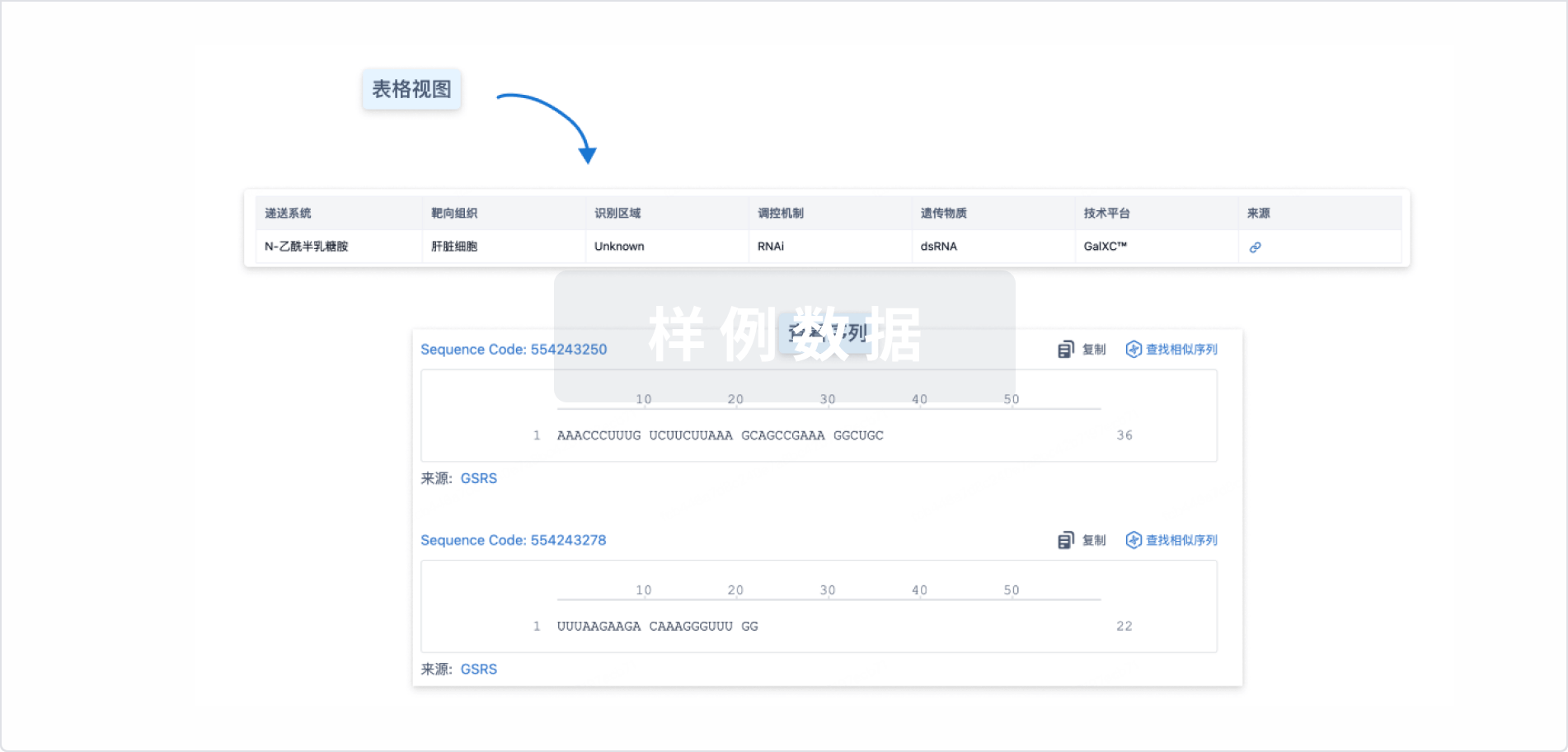
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
1
项与 ARO-INHBE 相关的临床试验NCT06700538
A Phase 1/2a Study to Evaluate the Safety, Tolerability, Pharmacokinetics, and Pharmacodynamics of ARO-INHBE in Adult Volunteers With Obesity With and Without Diabetes Mellitus
This is a Phase 1/2a double-blind dose-escalating study to evaluate the safety, tolerability, pharmacokinetics (PK), and pharmacodynamics (PD) of single and multiple doses of ARO-INHBE in adult participants with obesity (in Part 1), the safety, tolerability, PK, and PD of multiple doses of ARO-INHBE either as monotherapy, or in combination with tirzepatide, in adult participants with obesity with and without type 2 diabetes mellitus (in Part 2 and Part 3).
开始日期2024-12-04 |
100 项与 ARO-INHBE 相关的临床结果
登录后查看更多信息
100 项与 ARO-INHBE 相关的转化医学
登录后查看更多信息
100 项与 ARO-INHBE 相关的专利(医药)
登录后查看更多信息
125
项与 ARO-INHBE 相关的新闻(医药)2026-06-04
本文涉及大量转载内容,版权归属原作者,如涉侵权,请联系删除。
兆维
事业发展部
——
Hongene
Biotech B&D
INDUSTRY NEWS
核酸产业要闻半月报
01 国内药物研发进展
<
纳美信生物冻干呼吸道合胞病毒 mRNA 疫苗启动 II 期临床
5 月 20 号,药物临床试验登记与信息公示平台数据显示,纳美信(上海)生物科技有限公司的冻干呼吸道合胞病毒 mRNA 疫苗在 60 周岁及以上人群中接种的免疫原性及安全性的随机、盲法、安慰剂对照的 II 期临床试验已启动,临床试验登记号为 CTR20261965。
该药物剂型为粉针,用法为上臂三角肌肌内注射 1 剂,用药时程为接种1剂。本次试验主要目的为评价冻干呼吸道合胞病毒 mRNA 疫苗在 60 周岁及以上人群中接种的免疫原性。
本次试验主要终点指标包括疫苗接种后第 14 天和 30 天血清抗 RSV A 型和 B 型中和抗体阳转率、几何平均滴度、几何平均增长倍数;次要终点指标包括疫苗接种后 0-14 天征集性(局部和全身)不良事件发生率,疫苗接种后 0-30 天非征集性不良事件发生率,疫苗接种后 12 个月内严重不良事件、特殊关注的不良事件发生情况,疫苗接种后第 6 个月和 12 个月血清抗 RSV A 型和 B 型中和抗体阳性率、GMT、GMFR,疫苗接种后第 14 天、30 天、第 6 个月和 12 个月 preF 蛋白结合抗体的几何平均浓度、GMFR 和 SCR/阳性率。
参考资料:
https://www.cde.org.cn/
恒瑞医药:乙肝 siRNA 启动 III 期临床
5 月 26 日,恒瑞医药在 Clinicaltrials.gov 网站上注册了乙肝 siRNA 新药 HRS-5635 治疗慢性乙肝感染的 III 期临床试验。注册号为 NCT07606950。
该 III 期临床计划入组 540 例慢性乙肝受试者,预计 2028 年 6 月完成。该 III 期临床主要终点为功能性治愈率,即治疗 24 周停药 24 周后 HBV DNA 持续抑制且 HBsAg 转阴的比例。
参考资料:
https://clinicaltrials.gov/
浩博医药 AHB-137:公布 II 期临床试验数据
5 月 27 号,浩博医药(AusperBio)公布了其自主研发的 ASO 药物 AHB-137 用于初治 CHB 患者的 II 期临床研究随访结束数据。AHB-137 是一款新型非偶联 ASO 药物,该药物通过精准靶向肝细胞内 HBV 转录本,从源头阻断病毒蛋白合成,实现病毒深度压制与抗原快速清除;同时,其独特的免疫调节机制有助于实现持久的病毒学清除。
此次公布的数据显示,AHB-137 单药在未经治疗的 CHB 患者中展现出较强的 HBV DNA 抑制和 HBsAg 下降能力。研究结果显示,停药 24 周后,在总体人群中有 32% 患者实现功能性治愈。在基线 HBsAg 水平为 100-1000IU/mL 的患者中,功能性治愈率为 70%。
参考资料:
https://mp.weixin.qq.com/s/i7cXB_QpeQuVB_Qp0GtpRA
https://mp.weixin.qq.com/s/FrnZbexlI-U6km2YgS3Vyw
瑞博生物 siRNA 新药递交 II 期临床申请
5 月 28 号,瑞博生物已向欧洲药品管理局(EMA)提交用于治疗冠状动脉疾病的小核酸药物 RBD1119 的 II 期临床试验申请(CTA)。
近期,基于 RiboGalSTAR™ 肝脏靶向 siRNA 平台,瑞博生物已在包括房颤和静脉血栓栓塞等细分领域同步推进了多项 siRNA 药物的临床开发,打造了全球领先的抗凝/抗血栓小核酸版图,旨在系统性地解决血栓栓塞性疾病的根源治疗缺口。本次针对冠状动脉疾病的 CTA 递交标志着瑞博生物在抗血栓领域的重磅布局再获重要进展,以及持续拓展小核酸在该领域广阔应用的的信心。
参考资料:
https://www.ribolia.com/media-center/our-products-news/168
荣灿生物个体化 mRNA 肿瘤新抗原免疫疗法 IIT 研究取得阶段性临床结果
6 月 1 号,荣灿生物在研的一项个体化 mRNA 肿瘤新抗原免疫疗法取得阶段性临床研究进展。该研究为国内首次将个体化 mRNA 肿瘤免疫疗法应用于骨肉瘤患者的临床探索,也是全球第二例相关临床实践。初步研究结果显示,该 mRNA 新抗原疫苗在受试者体内成功诱导出积极的特异性免疫应答信号,并展现出良好的安全性与耐受性,显示出其在实体肿瘤精准免疫治疗领域的潜在应用价值。
此次 IIT 试验计划纳入 9-18 例晚期实体瘤患者,均为经标准治疗失败、目前无标准治疗方案或标准治疗不耐受的患者人群。前期入组的若干受试者均为骨肉瘤患者。初步随访数据显示,多名受试者在接受个体化 mRNA 肿瘤新抗原免疫药物治疗后,均出现明显的免疫应答,表现为 CD8+ T 细胞活化及 IFN-γ 分泌水平升高,该应答在安全性随访期内仍维持在高于基线的水平。其中 2 例患者的影像学评估显示,原发病灶及转移病灶均有不同程度缩小;其余患者肿瘤维持稳定状态,且未见新发病灶——对于晚期肿瘤快速进展的患者而言,这一控制效果具有临床意义。截至目前,已入组的受试者,均未出现与疫苗相关的 2 级及以上不良反应,安全性与耐受性表现优异,患者整体反馈良好。
该 IIT 结果为骨肉瘤这一"冷肿瘤"领域的创新治疗性药物研发提供了具有启发意义的早期临床证据,提示该候选产品在激活抗肿瘤免疫方面具有优异的潜在临床价值,为后续注册临床开发及商业转化奠定了良好基础。
参考资料:
http://rc-rna.com/cn/home/news/id/1003
02 国内投融资及合作信息
<
臻愈生物完成近亿元 A 轮融资
5 月 27 日,成都臻愈生物医药科技有限公司(以下简称"臻愈生物")宣布完成近亿元 A 轮融资。本轮融资由成都未来产业基金和元生创投联合领投,仁佑投资、盛景嘉成等机构联合参与,老股东君联资本追加投资。所募资金将主要用于拓展公司核心管线的临床推进。
这是继 2023 年种子轮由君联资本独家投资之后,臻愈生物首次引入外部机构股东,也标志着这家成立于 2023 年 7 月的公司正式从"概念验证"阶段迈入"临床推进"阶段的深水区,成立之初即聚焦下一代通用型细胞治疗产品的研发,确立 In vivo CAR-T 与全新成药形式的治疗性疫苗两大平台技术,攻坚传统细胞治疗应用难点。
参考资料:
https://news.pedaily.cn/202605/564494.shtml
星曜坤泽完成超 6.3 亿元人民币 B 轮融资
5 月 28 日,星曜坤泽正式宣布完成超 6.3 亿元人民币 B 轮融资。本轮融资由上海复星医药产业发展有限公司、杭州凯泰资本、珠海华金投资,TG Sino-Dragon Fund II L.P.、谦和资本、得时资本、太浩创投等机构及个人共同参与完成。
参考资料:
http://static.sse.com.cn/disclosure/listedinfo/announcement/c/new/2026-05-27/600196_20260527_CY30.pdf
尧唐生物完成近 5 亿元 C 轮融资
5 月 29 日 ,尧唐生物宣布完成近五亿元人民币 C 轮融资。本轮融资由正心谷资本领投,上海国投先导、闵金投、德岳投资等知名机构参与投资,老股东险峰淇云、远翼投资、天创资本加码跟投。
公司已有 6 条管线进入临床阶段,是全球范围内进入临床阶段体内基因编辑管线最多的公司。2024 年,其自主研发的治疗 ATTR 淀粉样变性的 YOLT-201 成为中国首款进入注册临床的基于 LNP 的体内基因编辑药物,目前已经完成 I/IIa 期临床所有患者给药。2025 年,FDA 批准其治疗原发性高草酸尿症的 YOLT-203 在美国进入确证性临床。
参考资料:
https://www.yoltx.com/cn/news/press-release/129
03 国外药物研发进展
<
Wavelife RNA 编辑寡核苷酸疗法临床结果积极
5 月 19 号,Wave Life Sciences 公布了在研疗法 WVE-006 的 RestorAATion-2 临床试验的最新数据。WVE-006 是一款 GalNAc 偶联、皮下注射给药的 RNA 编辑寡核苷酸(AIMer)疗法,用于治疗 α-1 抗胰蛋白酶缺乏症(AATD)。该疗法可通过生成健康的野生型 M 型 α-1 抗胰蛋白酶(M-AAT)、减少有害的 Z 型 α-1 抗胰蛋白酶(Z-AAT),并恢复机体在需要时动态产生功能性 α-1 抗胰蛋白酶(AAT)的能力,同时应对肺部和肝脏 AATD。
试验数据显示,单次 WVE-006 给药即可使循环中的突变型 Z-AAT 较基线出现强效、剂量依赖性下降,降幅分别达到 47.3%(200mg)、49.7%(400mg)和 59.1%(600mg)。多次给药 WVE-006 后,Z-AAT 进一步下降,在 200mg 每两周一次给药队列中降幅达到 70.5%。延长给药间隔后,Z-AAT 降幅相似,在 400mg 每月一次给药队列中达到 67.7%。
同时,单次 WVE-006 给药即可使野生型 M-AAT 蛋白在总循环 AAT 中所占比例出现强效、剂量依赖性恢复,分别达到 44.4%(200mg)、48.0%(400mg)和 52.3%(600mg)。数据支持每月一次皮下注射给药;在 200mg 和 400mg 多次给药队列中,编辑作用在最后一次给药后至少维持三个月。WVE-006 表现出良好的安全性和耐受性。所有不良事件(AE)均为轻度至中度,未发生严重不良事件(SAE),也未观察到具有临床意义的肝功能检测指标升高。
参考资料:
https://www.globenewswire.com/news-release/2026/05/18/3297034/0/en/wave-life-sciences-announces-positive-update-on-restoraation-2-trial-wve-006-galnac-rna-editing-achieves-mz-like-phenotype-across-both-biweekly-and-monthly-dosing.html
Dyne Therapeutics 向 FDA 递交 DYNE-25 的生物制品许可申请
5 月 26 号,Dyne Therapeutics 宣布向美国 FDA 递交 zeleciment rostudirsen(z-rostudirsen,也称 DYNE-251)的生物制品许可申请(BLA),用于治疗适合外显子 51 跳跃的杜氏肌营养不良症(DMD)患者。该疗法则采用磷酰二胺吗啉寡聚体(PMO)与靶向转铁蛋白受体 1(TfR1)的抗体片段偶联,以提升药物向肌肉和中枢神经系统相关组织递送的能力。
Z-rostudirsen 由 PMO 与靶向 TfR1 的抗体片段偶联而成。TfR1 在肌肉组织中具有较高表达,因此这一设计希望借助受体介导的递送机制,提高 PMO 进入相关组织和细胞的能力,并促进外显子 51 跳跃,从而产生近全长抗肌萎缩蛋白。Dyne 此次递交 BLA,申请用于治疗适合外显子 51 跳跃的 DMD 患者。
参考资料:
https://www.globenewswire.com/news-release/2026/05/26/3300969/0/en/dyne-therapeutics-announces-submission-of-biologics-license-application-bla-to-u-s-fda-for-z-rostudirsen-in-exon-51-duchenne-muscular-dystrophy-dmd.html
Arrowhead 公布了 ARO-INHBE I/IIa 期临床试验的中期结果
5 月 27 号,Arrowhead Pharmaceuticals 公布了 ARO-INHBE I/IIa 期临床试验的中期结果。ARO-INHBE 是该公司正在开发的一款在研 RNA 干扰(RNAi)疗法,有望用于治疗肥胖症和代谢功能障碍相关脂肪性肝炎(MASH)。在欧洲肝脏研究协会年会(EASL 2026)上公布的数据显示,在肥胖成人中,ARO-INHBE 作为单药治疗以及与低剂量替尔泊肽(tirzepatide)联合使用时,均可带来具有临床意义的肝脏脂肪减少。ARO-INHBE 旨在降低肝脏中 INHBE 基因及其分泌性基因产物 Activin E 的表达。
ARO-INHBE I/IIa 期部分结果:
在肥胖受试者中,单次给药 ARO-INHBE 后观察到 Activin E 呈剂量依赖性下降;在 ARO-INHBE 400mg 剂量组中,平均最大降幅达到 85.3%,且疗效持续超过 3 个月。
在合并肥胖和 2 型糖尿病(T2DM)的受试者中,接受两次 ARO-INHBE 给药(20mg 或 400mg)并联合 5mg 替尔泊肽治疗后,也观察到类似的 Activin E 下降;疗效可持续至第 24 周,并显示出未来可能实现每年两次低频给药的潜力。
在基线肝脏脂肪含量(LFC)高于 8% 的肥胖受试者中,接受 200mg 或更高剂量 ARO-INHBE 单药治疗的患者(n=10;基线 LFC 为 14.5±5.1%)在给药后实现了经安慰剂校正的 LFC 下降 44%。
在伴或不伴 T2DM 的肥胖受试者中,与单独使用替尔泊肽相比,ARO-INHBE 联合低剂量替尔泊肽(5mg)可进一步降低内脏脂肪和 LFC。
参考资料:
https://www.businesswire.com/news/home/20260527903149/en/Arrowhead-Pharmaceuticals-Presents-New-Clinical-Data-on-RNAi-based-Obesity-and-MASH-Candidate-ARO-INHBE-at-EASL-2026
GSK全球首创 ASO 疗法 III 期数据公布
5 月 28 号,葛兰素史克(GSK)在欧洲肝病学会(EASL)年会上重磅公布了反义寡核苷酸(ASO)药物贝普若韦生(bepirovirsen)两项全球 III 期临床试验(B-Well1 和 B-Well2)结果。
数据显示,整体研究人群可实现 19% 的显著功能性治愈率,病毒活性较低患者的功能性治愈率可达 26%,而仅接受标准治疗的患者为 0%;中国亚组数据表现更好,基线 HBsAg≤1000IU/mL 患者功能性治愈率高达 35%。目前的标准治疗功能性治愈不到 1%,通常需要终身服药。另外,2026 年 5 月,GSK 已与中国生物制药达成战略合作,旨在加快该产品在中国的上市进程。
核心疗效数据显示:
主要终点:整体研究人群中,bepirovirsen 组功能性治愈率达 19%(233/1220),而安慰剂组为 0%(0/614),两项试验 p 值均<0.001,具有高度统计学意义和临床意义。
关键次要终点:在基线 HBsAg≤1000IU/mL 的患者亚组(约占全球确诊病例的 45%)中,功能性治愈率进一步提升至 26%(200/768),安慰剂组为 0%。
中国亚组表现尤为突出:基线 HBsAg≤3000IU/mL 患者功能性治愈率为 24%,基线 HBsAg≤1000IU/mL 患者更是高达 35%,显著高于全球平均水平。
长期疗效持久:探索性分析显示,49% 的 bepirovirsen 受试者在结束治疗一年后定量表面抗原水平(qHBsAg)降低至≤100IU/mL。医学文献认为这种低表面抗原水平与增强免疫控制和改善患者预后相关。此外,一项关键的次要终点显示,23% 的所有受试者(283/1220 vs. 0/614 安慰剂组;两项试验 p<0.001)及 31% 的基线 HBsAg≤1000IU/mL 的受试者(237/768 vs. 0/393 安慰剂组;两项试验 p<0.001),在第 48 周停止所有治疗后,在第 72 周实现持续乙肝病毒 DNA 低于定量下限(
临床2期siRNA疫苗信使RNA临床1期
2026-06-01
PS:点击上方小程序或公众号后台回复“451”,下载原文
报告摘要
当所有人都在盯着GLP-1受体激动剂(如司美格鲁肽、替尔泊肽)如何卷价格、卷减重效果时,一家名为Arrowhead Pharmaceuticals的美国生物技术公司,正在用一种全新的技术路径,悄悄改写游戏规则。
就在本周(2026年5月27日),该公司在西班牙巴塞罗那举行的欧洲肝脏研究学会年会(EASL 2026)上,公布了一项关于其在研药物ARO-INHBE的最新临床数据。
这份刚刚出炉的海报摘要显示:单药治疗即可使肝脏脂肪减少44%,且与低剂量替尔泊肽联用时,能显著增强内脏脂肪和肝脏脂肪的减少效果。
在这个“减肥药即正义”的时代,Arrowhead似乎找到了一把专门打开“代谢健康”大门的钥匙——抑制素βE(INHBE)。
核心看点
🔬 核心机制:一把名为“INHBE”的代谢“开关”
首先,我们要搞清楚一个问题:为什么减重还要专门盯着肝脏和脂肪细胞之间的通讯?
ARO-INHBE是一款基于RNA干扰(RNAi)技术的药物。它的靶点非常精准——抑制素βE(INHBE)。
靶点身份:INHBE主要在肝细胞中表达,它编码的蛋白叫Activin E(激活素E)。这不仅仅是一个蛋白质,它是一种“肝因子”(Hepatokine),专门在肝脏和脂肪组织之间传递信号。
作恶逻辑:Activin E通过ALK7受体,促进脂肪细胞储存脂肪。简单说,它就是那个告诉身体“把能量存起来,别动”的信号兵。
破解之道:ARO-INHBE通过沉默肝细胞中的INHBE表达,阻断这个信号,从而减少脂肪堆积、改善胰岛素抵抗。
遗传学证据:自然界中,那些天生携带INHBE基因“失活”突变的人,往往拥有更好的心脏代谢指标,更低的2型糖尿病风险。
📊 数据“拆解”:44%的肝脏脂肪减少意味着什么?
这份在EASL 2026上公布的海报(编号LB26-MITT-5164),披露了1期/2a期临床试验(ARO-INHBE-1001)的最新进展。
我们需要关注三个关键数据点:
1. 单药疗效:直击“脂肪肝”痛点
实验设计:在基线肝脏脂肪含量(LFC)≥8%的肥胖患者中,使用≥200mg剂量的ARO-INHBE单药治疗。
结果:相比于安慰剂,肝脏脂肪含量(LFC)减少了44%(p < 0.01)。
意义:这是一个非常惊人的数字。目前的GLP-1类药物虽然也能改善脂肪肝,但通常需要大剂量和长时间治疗。ARO-INHBE作为单药,仅通过抑制一个靶点,就实现了如此显著的降脂效果,证明了其机制的强悍。
2. 联合疗法:与“替尔泊肽”的“1+1>2”
实验设计:ARO-INHBE(200mg或400mg)与低剂量替尔泊肽(5mg)联用。
结果:相比于单用替尔泊肽,联合治疗组在内脏脂肪组织(VAT)和肝脏脂肪的减少上表现更优。
战略意图:这说明ARO-INHBE不仅仅是一个替代品,更是一个“增效剂”。未来,它可能允许医生使用更低剂量的GLP-1药物,从而减少恶心、呕吐等副作用,同时获得更好的代谢收益。
3. 安全性:RNAi技术的“成年礼”
数据:91%的受试者报告了治疗 emergent 不良事件(TEAEs),但绝大多数为轻度。
关键指标:没有观察到与药物相关的严重不良事件(SAEs),也没有因不良事件导致停药的情况。特别是肝酶(ALT)水平没有出现不良变化趋势。
结论:这意味着ARO-INHBE在安全性上过关了,RNAi药物在代谢领域的应用潜力得到了验证。
🧩 行业深意:为什么这是一家值得关注的公司?
除了这次EASL的数据,Arrowhead Pharmaceuticals在近期的另一项动作也值得玩味。
就在几天前(5月22日),该公司宣布任命John G. McHutchison, AO, MBBS, BMedSc, MD, FRACP为首席科学官(CSO)。
人物背景:McHutchison教授是肝病和代谢领域的泰斗级人物,曾任Gilead Sciences的首席科学官和研发总裁,在丙肝和NASH药物研发上拥有传奇履历。
信号:一家公司高管的任命,往往预示着其战略重心。Arrowhead正在从一家单纯的RNAi技术平台公司,转型为一家专注于代谢疾病(尤其是肝脏-脂肪轴)的生物制药巨头。
💡 结语:代谢疾病治疗的“第三条路”
2026年的减肥药市场,已经变成了诺和诺德和礼来的“二人转”。然而,ARO-INHBE的出现,提醒了我们一件事:GLP-1并不是代谢健康的唯一答案。
Arrowhead Pharmaceuticals正在走一条“肝脏因子调控”的第三条路。
技术优势:RNAi药物通常具有长效性(可能一个月甚至更久打一针)和高特异性。
临床价值:专门解决GLP-1药物可能存在的短板,如脂肪肝改善不彻底、肌肉流失等。
虽然目前的数据还处于早期(1期/2a期),但44%的肝脏脂肪减少率,已经足够让市场听到“硬币落地”的声音。
报告免费下载方式
▲点击上方小程序
▲或在公众号消息框发送:
451,即可免费下载原文
往期相关资料推荐:76份药企PPT下载丨2025 JPM 大会亮点回顾:制药巨头战略布局与前沿动态第一期
76份药企PPT下载第二期丨2025 JPM 大会亮点回顾:制药巨头战略布局与前沿动态
76份药企PPT下载第三期丨2025 JPM 大会亮点回顾:制药巨头战略布局与前沿动态
200+份药企PPT下载丨2025 JPM 大会亮点回顾:制药巨头战略布局与前沿动态
免责声明:所载内容、图片来源互联网,微信公众号等公开渠道,我们对文中观点保持中立,仅供参考、交流之目的。转载的稿件版权归原作者和机构所有,如有侵权,请联系我们删除。本公众号原创文章,欢迎转载,转载时请注明出处。
2026-05-29
·生物经纬
01
2026年5月29日,基石药业在ASCO大会上公布CS2009在NSCLC患者(前线/后线)中的I/II期临床试验数据和在晚期实体瘤患者中的I期临床试验数据。结果显示,在多种肿瘤类型中均观察到了令人鼓舞的抗肿瘤活性,在无已知可操作致癌基因改变的非小细胞肺癌 (n = 27)、软组织肉瘤 (n = 9)、非透明细胞肾细胞癌 (n = 5) 和三阴性乳腺癌 (n = 6),其ORR分别为 18.5%、33.3%、20.0% 和 16.7%,DCR分别为74.1%、66.7%、100.0%和50.0%。安全性方面,未发生剂量限制性毒性;未达到最大耐受剂量。
02
2026年5月28日,Arrowhead Pharmaceuticals公布了ARO-INHBE 1/2a期临床试验的中期结果。ARO-INHBE是该公司正在开发的一款在研RNA干扰(RNAi)疗法,有望用于治疗肥胖症和代谢功能障碍相关脂肪性肝炎(MASH)。数据显示,在肥胖成人中,ARO-INHBE作为单药治疗以及与低剂量替尔泊肽(tirzepatide)联合使用时,均可带来具有临床意义的肝脏脂肪减少。
03
2026年5月28日,Biohaven公布了其专有细胞外MoDE(BHV-1300)和TRAP(BHV-1400)降解剂平台的结果,包括BHV-1300 MoDE降解剂治疗Graves病和BHV-1400 TRAP降解剂治疗IgA肾病的新患者数据。结果显示,每周给药BHV-1300(1000 mg)后,在Graves甲亢患者中,到第12周时致病性TSHR-IgG1平均降低幅度超过80%,这一致病性TSHR-IgG1降幅超过新生儿Fc受体(FcRn)抑制剂已显示的结果。此外,在IgAN患者中,皮下注射BHV-1400后48小时内,致病性Gd-IgA1平均降低超过60%;给药1个月内降低70%。
04
2026年5月27日,浩博医药(AusperBio)公布了其自主研发的ASO药物AHB-137在中国大陆地区用于未经治疗的‘初治’慢性乙型肝炎(CHB)患者的II期临床研究随访结束数据。结果显示,AHB-137在未经治疗的初治慢乙肝患者中展现出强效且持久的抗病毒活性,并在基线HBsAg 100 – 1000 IU/mL的人群中实现了70%的临床治愈(Functional Cure,FC),同时整体安全性符合预期。
05
2026年5月27日,Kura Oncology公布了FIT-001临床试验中darlifarnib联合KRAS G12C抑制剂adagrasib的首次人体研究数据。Darlifarnib(KO-2806)是一款下一代法尼基转移酶抑制剂(FTI)。数据显示,darlifarnib与adagrasib联合疗法在这些患者中展现出具有意义的抗肿瘤活性,为Kura的FTI平台提供了临床机制验证依据。77%(20/26)的可评估患者出现肿瘤缩小;在未接受过KRAS抑制剂治疗的可评估患者中,这一比例达到94%(15/16)。按瘤种来看,PDAC、NSCLC和KRAS抑制剂初治CRC患者的客观缓解率分别为67%、50%和29%。该联合方案整体耐受性良好,安全性可控。
06
2026年5月27日,恒瑞医药与Kailera共同宣布,口服小分子GLP-1受体激动剂HRS-7535在中国284名成人2型糖尿病受试者中开展的Ⅲ期临床试验(OUTSTAND-1)取得积极顶线结果。32周主要终点数据显示,HRS-7535三个剂量组(30 mg、60 mg、90 mg)HbA1c降幅达1.40%~1.68%;关键次要终点HbA1c<7.0%的达标率达83.5%~89.6%。HRS-7535展现了良好的安全性和耐受性。
1
为了落实国家药监局“提前介入、一企一策、全程指导、研审联动”的要求,加强申请人与药审中心的沟通交流,聚焦并解决源头性创新罕见疾病药物研发中的科学问题,提升罕见疾病药物研发效率,药审中心组织制定了罕见疾病创新药物研发鼓励试点计划(“关爱计划-延伸”),经国家药品监督管理局审核同意,现予发布,自发布之日起启动。
详情网址:
https://www.cde.org.cn/main/news/viewInfoCommon/3a028dc5479e8098013b33a83296ac3f
往期回顾
医药科技简讯 | 卵巢癌免疫治疗历史性破局!Keytruda联合疗法3期结果公布
医药科技简讯 | 首个全能PCSK9抑制剂!显著降低MACE风险
医药科技政策简讯 | 体重下降约25斤!诺和诺德长效胰淀素3期结果亮眼公布
医药科技政策简讯 | 100%疾病控制率,近90%患者肿瘤缩小!双抗亮眼结果公布
医药科技政策简讯 | 史无前例!持久降血脂,反义寡核苷酸疗法3期亮眼结果公布
综合整理 | 史卓琳、王演鑫(NO.826期)
图文编辑 | 王小雨
商务合作丨马经理 15850522742
新闻投稿/访谈邀约
彭经理 18012921198
100 项与 ARO-INHBE 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肥胖 | 临床2期 | 新西兰 | 2024-12-04 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用