预约演示
更新于:2026-04-24
Pan-RAS (Fog Pharma)
更新于:2026-04-24
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段药物发现 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 Pan-RAS (Fog Pharma) 相关的临床结果
登录后查看更多信息
100 项与 Pan-RAS (Fog Pharma) 相关的转化医学
登录后查看更多信息
100 项与 Pan-RAS (Fog Pharma) 相关的专利(医药)
登录后查看更多信息
53
项与 Pan-RAS (Fog Pharma) 相关的新闻(医药)2026-04-21
SAN DIEGO
— Since Herceptin’s approval in 1998, breast cancer has been reshaped from a near-term death sentence into — in many cases — a chronic disease. Now, researchers hope daraxonrasib from Revolution Medicines will launch the same type of transformation in pancreatic cancer.
A recent Phase 3 finding on daraxonrasib “is one of the most important things that’s happened in cancer therapeutics in the last 30 to 40 years,” Stifel healthcare director Tim Opler said. “This is very much a Herceptin-type moment.”
Before Herceptin’s approval, chemotherapy was often the only treatment for breast cancer, potentially keeping the cancer at bay for a few months. But the tumors would recur in most cases, leaving patients without further options.
Herceptin, the first targeted cancer therapy,
extended response rates
by three months. Now, almost three decades later, many patients respond to targeted breast cancer therapies for multiple years. The most impressive figure comes from an Enhertu-Perjeta combination that recorded a 40.7-month progression-free survival mark and was approved late last year.
Cancer outcomes broadly have improved in the same period, and even dating back to the 1970s. About 70% of individuals diagnosed with cancer between 2015 and 2021
lived for at least five years after their diagnosis
, up from 63% in the three years before Herceptin’s approval. Between 1975 and 1977, only 49% of cancer patients reached the five-year mark.
But pancreatic cancer outcomes remain poor, with five-year survival rates sitting at 13%,
according to the American Cancer Society
, among the lowest in major cancers. That figure drops to 3% for patients whose tumors have metastasized.
The stunning success of Revolution Medicines’ daraxonrasib in a Phase 3 study, where it doubled patients’ survival times, is expected to shake up that dynamic — and shake it up robustly. The data represent a transformative moment on a scale similar to Herceptin’s impact on breast cancer.
Prior to the Phase 3 trial success announced last week, only a mere handful of past late-stage pancreatic cancer trials had succeeded.
“It reinvigorates the whole field,” said Daniel Von Hoff of the Translational Genomics Research Institute and City of Hope. Von Hoff, who led trials of the current chemotherapy regimen for pancreatic cancer, was not involved in the daraxonrasib trial.
The once-a-day pill is a “pan-RAS” inhibitor, targeting cancer-driving mutants of RAS — long believed to be undruggable — that underlie more than 90% of pancreatic cancer cases.
And physicians and scientists are eagerly awaiting the first-line results for daraxonrasib from a large, Phase 3 trial. In early-stage data
shared
at AACR, daraxonrasib alongside chemotherapy resulted in a 58% response rate across 40 patients after at least 18 weeks (just over 4 months). However, the data are still early, with a median follow-up time of just under 10 months.
Meanwhile, in 38 first-line patients who received daraxonrasib alone, the response rate was 47% at a median follow-up of 13.7 months, according to
results
that will be shared Tuesday at AACR.
The Phase 3 trial
RASolute 303
will compare daraxonrasib alone and daraxonrasib plus chemotherapy versus chemotherapy alone, with an expected primary result in mid-2028.
“Everybody’s hoping those will really come quickly,” Von Hoff said of the first-line readout.
While some Wall Street analysts predict the drug could bring in over $10 billion one day, it remains to be seen how broadly daraxonrasib will be used. RevMed and many other companies are also developing mutation-specific KRAS inhibitors and degraders. Researchers say more work needs to be done to see which drugs come out on top, and where and how each drug should be used.
The true payoff for Herceptin has come in the decades since its first approval. It got the ball rolling on HER2-positive breast cancer, especially in the advanced and metastatic settings. Combinations are now the norm and continue to improve outcomes. Daraxonrasib provides hope that something similar is in store for pancreatic cancer as well.
“It’s just the beginning of the role of all types of inhibitors of the RAS pathway in making major impacts in the clinic,” said Robert Vonderheide of the University of Pennsylvania and AACR president-elect.
Endpoints is fielding the next Biopharma Sentiment Index (BPSI) — a concise, three-minute survey that distills thousands of industry views into a clear quarterly benchmark. This year is pivotal for biopharma, and we need your perspective on where things are going.
Take the survey here.
临床3期临床结果AACR会议
2026-04-16
4月16日,阿诺医药(NASDAQ:ANL)宣布已就一项上市公司私募股权融资(PIPE)签署证券购买协议,预计融资总额约为1.5亿美元(未扣除配售代理及其他相关费用)。2月3日,阿诺医药完成1.4亿美元PIPE融资。两次PIPE累计融资2.9亿美元。阿诺医药凭借AN9025一款临床阶段的 pan-RAS(ON) 分子胶成功完成逆转,尤其是最近Revolution的RMC-6236的3期临床成功。(阿诺医药完成1.4亿美元配售融资;16.33亿元!奥赛康引进一款pan-RAS(ON) 分子胶;市值增加100亿美元!Revolution完成20亿美元超额融资,准备自己干商业化)
本次超额认购的交易吸引了多元化的新老机构投资者共同参与。新投资者包括Soleus Capital,Perceptive Advisors,ADAR1 Capital Management,MPM BioImpact,Octagon Capital,Eventide Asset Management ,Kalehua Capital和DAFNA Capital Management。同时,部分现有投资者亦追加参与此次融资,包括Cormorant Asset Management,Columbia Threadneedle Investments,Balyasny Asset Management,Casdin Capital,Squadron Capital Management和Superstring Capital Management,彰显对公司长期价值的坚定信心。
在本次私募融资中,公司拟以每美国存托股份(ADS)13.25 美元的价格,向投资者发行11,320,755股ADS, 该定价与公司 ADS 于 2026 年 4 月 15 日在纳斯达克的收盘价持平。本次定向增发预计于2026 年 4 月 17 日完成交割,前提是满足惯常的交割条件。
关注下方公众号,带你看世界!
2026-04-15
Revolution Medicines is capitalizing on its recent clinical trial success, putting together the biotech industry’s largest public raise since the Covid-19 pandemic.
The company
priced
its stock and debt offering at $2 billion, doubling the
amount it expected to raise
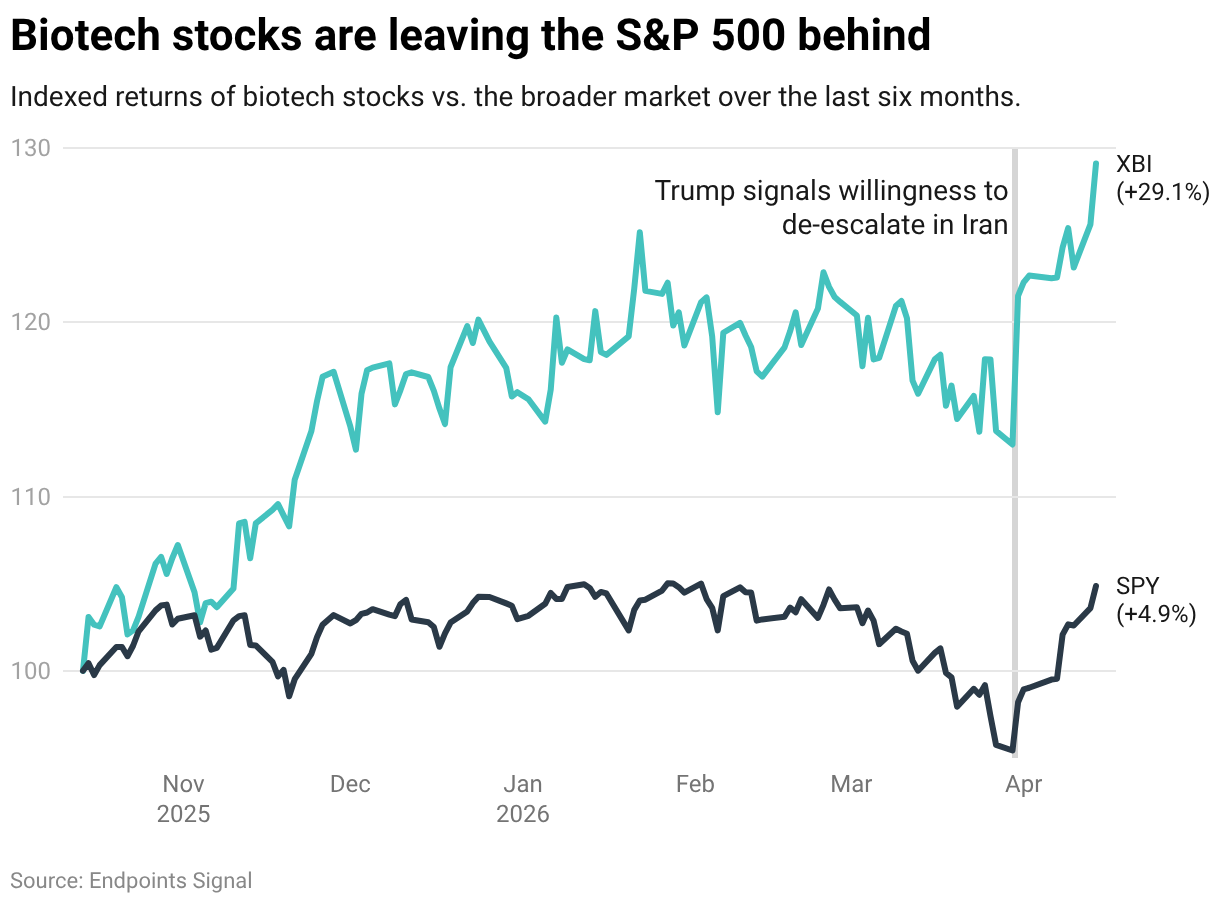
after a Phase 3 win in pancreatic cancer. The colossal figure comes as the XBI, biotech’s closely watched industry barometer, topped $135 on Tuesday — its highest point since the summer of 2021, when pandemic-era vibes still dominated.
Over the last six months, the XBI has risen 29.1%, compared to a 4.9% increase in the S&P 500. It’s been powered by a wave of public offerings and heightened M&A activity. Along with Revolution, Spyre Therapeutics and Allogene Therapeutics also put together raises this week, pricing theirs at $403 million and $175 million, respectively.
As of Tuesday’s market close, Revolution’s market capitalization sat just above $29 billion.
Revolution’s raise is made up of a $1.5 billion stock offering and $500 million in convertible senior notes. It initially sought $750 million in stock and $250 million in notes.
The success of daraxonrasib, Revolution’s RAS inhibitor, is driving the excitement on Wall Street. Daraxonrasib
cut the risk of death by 60%
versus chemotherapy in a Phase 3 pancreatic cancer trial, an outcome previously unheard of in patients with such tumors. The result caused Revolution’s stock price
$RVMD
to jump 40% earlier this week.
Daraxonrasib was designed as a “pan-RAS” drug, which is unlike the two previously approved KRAS drugs that only addressed one disease-causing mutation. That could offer potential in other kinds of tumors where immunotherapy has thus far proven to yield relatively lackluster results, such as colorectal cancer.
Revolution was the subject of buyout rumors earlier this year, with Merck reportedly in discussions for a deal worth about $30 billion. But no acquisition ever materialized.
临床3期并购免疫疗法临床结果IPO
100 项与 Pan-RAS (Fog Pharma) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 结直肠癌 | 药物发现 | 美国 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用