预约演示
更新于:2026-03-21
REC-163964
更新于:2026-03-21
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
关联
2
项与 REC-163964 相关的临床试验NCT06536465
A Phase 2 Clinical Study of REC-3964 in Adults for the Reduction of Recurrent Clostridioides Difficile Infection (CDI)
This is a multi-center, open-label study to investigate the safety, tolerability, pharmacokinetics (PK) and efficacy of REC-3964 (doses of either 250 mg or 500 mg PO every 12 hours) for the reduction of Clostridioides difficile infection (CDI).
开始日期2024-10-14 |
NL-OMON53684
A Randomized, Double-blind, Placebo-controlled, Single Ascending Dose and Multiple Ascending Dose Study to Investigate the Safety, Tolerability, and Pharmacokinetics of REC-3964 in Healthy Subjects - SAD PK study with REC-3964
开始日期2022-08-17 |
100 项与 REC-163964 相关的临床结果
登录后查看更多信息
100 项与 REC-163964 相关的转化医学
登录后查看更多信息
100 项与 REC-163964 相关的专利(医药)
登录后查看更多信息
22
项与 REC-163964 相关的新闻(医药)2026-03-11
·创药网
当前,人工智能技术已深入渗透到药物研发的各个环节,从靶标发现、化合物筛选到临床试验设计优化,形成了全流程赋能新范式,为加速药物研发与上市带来了前所未有的机遇。本文对2025年AI药物研发领域的临床进展进行简要梳理,以期为相关研发人员提供参考与启示。
近年来,人工智能(AI)技术迅速发展,并加速向生物医药领域深度融合,正在重塑传统药物研发模式。当前,AI已全面渗透至药物研发的关键环节,从疾病机制解析与靶标发现、先导化合物的高通量筛选与结构优化,到药效毒性预测、临床试验设计及患者分层等阶段,逐步形成覆盖研发全流程的智能化赋能新范式。相较于传统依赖经验和试错的研发路径,AI技术在提升研发效率、降低成本、缩短研发周期以及提高成功率方面展现出显著优势,为创新药物的快速转化与上市带来了前所未有的发展机遇。
全球范围内,AI药物研发加速发展。据Precedence Research发布的研究报告显示,全球AI在药物发现市场的规模在2025年达到69.3亿美元,预计到2035年将达到约178.1亿美元。中国市场同样表现亮眼,伴随资本、技术与人才的持续涌入,中国AI制药企业数量快速增长。据不完全统计,截至2026年1月,中国AI制药公司已达到了113家,企业密集分布于北京、长三角与大湾区,北京、上海、深圳三城集聚效应显著,形成“三足鼎立”之势。在研发层面,AI赋能药物研发已从早期探索逐步迈向临床验证阶段。当前,已有多条管线推进至Ⅲ期临床,标志着AI参与药物研发的成熟度不断提升。
以下,对2025年AI药物研发领域的临床积极与消极进展进行概述。
临床积极进展
首个“AI药物”临床概念验证结果发布
01
2025年6月,AI制药公司英矽智能的在研药物——业界首个完成临床药效概念验证的AI药物Rentosertib(ISM001-055)取得新突破:其Ⅱa期临床研究结果被刊登于全球顶尖学术期刊Nature Medicine,论文题名为“A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial”。Ⅱa期数据初步验证了该药物的安全性和有效性。Rentosertib是通过英矽智能生成式AI平台Pharma.AI发现和设计的用于治疗特发性肺纤维化(IPF)的潜在全球首创小分子药物,靶向AI赋能发现的新颖靶标TNIK。通过抑制TNIK信号传导,Rentosertib旨在阻止或逆转纤维化过程,有望为全球500万受IPF影响的患者提供一种改善疾病的治疗方法,打破现有疗法无法停止甚至逆转疾病进程的困局。
该论文主要报道了一项名为GENESIS-IPF的Ⅱa期研究(NCT05938920)结果,这是针对Rentosertib的一项双盲、安慰剂对照临床试验,在中国22个中心共入组71例IPF患者,受试者被随机分配接受安慰剂、每日一次30mg、每日两次30mg或每日一次60mg,持续12周的用药观察。结果显示,Rentosertib达到主要研究终点,即具有可控的安全性和耐受性。从数据来看,各治疗组中与治疗相关的不良事件(TEAEs)发生率相似,大多数不良事件(AEs)为轻度或中度,严重不良事件(SAEs)发生率罕见,且所有不良事件在停药后均可恢复。
在次要疗效终点方面,Rentosertib同样取得了令人鼓舞的结果。为期12周的试验中,以用力肺活量(FVC)这一评价IPF患者肺功能的金标准来看,在接受治疗的患者中观察到剂量依赖性的肺功能改善。在每日一次60mg的最高用药剂量组中,患者的FVC与基线水平相比,平均提高98.4mL,而安慰剂组患者的FVC与基线水平相比,平均下降20.3mL。
2025年12月,英矽智能在港交所成功挂牌上市,成为首家通过联交所主板上市规则8.05条上市的AI生物医药科技公司。
全球首款AI优化单抗进入Ⅲ期临床
02
2025年12月,AI驱动的生物技术公司Generate : Biomedicines宣布,其抗TSLP(Thymic Stromal Lymphopoietin)长效抗体GB-0895启动两项全球Ⅲ期临床试验,SOLAIRIA-1和SOLAIRIA-2。该试验将在全球40多个国家,评估该药在约1600名严重哮喘成人和青少年的疗效与安全性,标志着GB-0895在推进可编程生物学应用方面迈出了关键一步,并且GB-0895展现出了惊人的研究速度,从2021年GB-0895第一次在实验室内合成,到如今进入Ⅲ期临床仅仅只过了4年时间。
GB-0895是一种通过AI优化的抗体,旨在实现超高亲和力TSLP结合、延长半衰期和高特异性。TSLP是多种炎症级联反应的关键上游细胞因子,在哮喘、特应性皮炎、慢性鼻窦炎等过敏性疾病中发挥核心作用。值得注意的是,GB-0895不是一款从头设计的抗体,而是根据安进的重磅药物Tezspire(Tezepelumab)的基础上优化而来。目前Tezspire被批准用于治疗重度哮喘和鼻窦炎,要求患者一个月注射一次。
在针对96名轻度至中度哮喘患者的I期研究中,GB-0895在10mg至1200mg的广泛剂量范围内总体耐受良好,显示出剂量比例的药代动力学,半衰期约为89天,并且关键生物标志物持续减少,符合阻断TSLP至少六个月。此外,GB-0895还正在慢性阻塞性肺疾病(COPD)的Ⅰ期临床试验中接受评估。
AI设计的药物Ⅲ期临床试验积极
03
Zasocitinib(TAK-279)是一款AI设计的分子,由Nimbus Therapeutics和AI制药公司薛定谔共同开发,由此获得了靶向TYK2(酪氨酸激酶2)的高选择性药物。2022年底,武田以40亿美元的首付款从Nimbus Therapeutics手中收购了Zasocitinib。
2025年12月,武田宣布,Zasocitinib在两项关键Ⅲ期临床试验中取得积极结果。数据显示,Zasocitinib在第16周显著优于安慰剂,达到共同主要终点,即静态临床医生整体评估(sPGA)评分为0或1的参与者比例均优于安慰剂。银屑病面积及严重程度指数(PASI)较基线改善至少75%的参与者比例也优于安慰剂,且早在第4周即可观察到显著更高的PASI 75应答率,并持续提高至第24周。这些研究还达到了全部44项排序次要终点,包括与安慰剂和阿普米司特(Apremilast)相比的PASI 90、PASI 100以及sPGA 0,显示这种便捷的每日一次口服方案具有实现皮损完全清除的潜力。基于Zasocitinib强效和安全性表现,武田计划2026财年提交新药上市申请。该药物有望挑战百时美施贵宝的TYK2抑制剂Sotyktu的市场地位。
MTS-004成为国内首款完成Ⅲ期临床的AI赋能制剂新药
04
2025年10月,剂泰科技宣布,其自研AI驱动小分子制剂优化平台AiTEM候选药物MTS-004已顺利达到Ⅲ期临床研究主要终点,成为目前国内首款完成Ⅲ期临床的AI赋能制剂新药。MTS-004也是中国首款且目前唯一完成Ⅲ期临床试验的PBA(Pseudobulbar Affect,假性延髓情绪失控)药物,有望填补国内PBA治疗领域尚无获批药物的空白。
MTS-004是一款新型PBA口服治疗候选药物,采用剂泰科技AiTEM自研口腔崩解片(ODT)剂型设计。该制剂针对PBA患者常见吞咽困难问题,无需用水即可在口腔中迅速溶解,口感良好,显著改善了患者服药体验和治疗依从性。
研究结果显示,MTS-004整体安全性良好,在治疗继发于神经系统疾病的PBA方面展现出明确疗效与良好耐受性。经过12周治疗,MTS-004显著减少PBA的平均发作次数,差异具有统计学意义,并在多项敏感性与亚组分析中得到一致验证。自第2周起即观察到疗效,治疗持续期间无发作日显著增加,且改善幅度随时间延长而增加。除主要终点外,MTS-004在CNS-LS评分、CGI-C和PGI-C评估以及SF-36心理健康指数上均显著优于安慰剂,提示其可明显改善患者情绪控制和生活质量。MTS-004亦显著改善CNS-BFS总分及吞咽、流涎症状。
MTS-004计划于2026年向国家药品监督管理局(NMPA)提交用于PBA适应症的新药上市申请(NDA),并在获批后启动临床研究,评估其在吞咽障碍治疗中的潜在拓展适应症。
国内首款AI设计新药进入Ⅲ期临床
05
2025年12月,德睿智药宣布,已正式启动其自主研发的AI辅助设计小分子GLP-1受体激动剂MDR-001的Ⅲ期中国临床试验MOBILE。该研究计划在全国范围内招募约750名超重或肥胖受试者,进行长达52周的系统性评估。这是中国第一个AI设计的药物分子进入Ⅲ期确证性临床研究试验。MDR-001仅用时四年半,便高效推进至Ⅲ期临床,这不仅是德睿智药的关键里程碑,更是中国AI制药领域的重大突破。
此外,基于MDR-001在已有的临床研究中展示的优异的治疗潜力与卓越的安全性优势,这也是中国创新药企业在口服小分子GLP-1药物领域一次极有希望冲击全球“Best-in-class”地位的努力。
临床消极进展
2025年,多个AI药物研发进展不佳。
2025年8月,薛定谔宣布停止CDC7抑制剂SGR-2921的临床开发计划,该药物是一款针对复发/难治性急性髓性白血病(AML)或高危骨髓增生异常综合征(MDS)患者的小分子抑制剂。该研究(NCT05961839)是一项在成人中进行的剂量递增研究,旨在测量药物的安全性和耐受性,并确定未来试验的最大耐受剂量和推荐剂量。尽管在Ⅰ期研究中观察到单药治疗活性的早期证据,但包括SGR-2921被认为导致两名AML患者死亡的紧急事件,还是促使薛定谔最终放弃了该药物。
2025年12月,AI制药公司Verge Genomics亦终止了其唯一临床资产VRG50635的开发。根据clinicaltrials.gov披露的信息,研究终止原因是“因缺乏风险-收益数据,发起人终止了研究”。VRG50635是一种强效、可口服的PIKfyve抑制剂。PIKfyve是Verge基于专有的AI平台CONVERGE平台发现的肌萎缩侧索硬化症(ALS)潜在治疗靶标。VRG50635有望改善ALS患者神经元的存活率,并在ALS相关运动神经元变性模型的多项临床前研究中显示出疗效。值得注意的是,VRG50635是首批完全由AI平台开发并进入临床试验的药物之一,从发现到临床仅用了4年时间。Verge公司在2024年3月将VRG50635除美国以外多个国家/地区的独家权益授权给了Ferrer,该协议总价值超过1.125亿欧元(约合1.217亿美元)。
AI制药上市公司Recursion发布了其2025年一季报,并宣布了一项重磅且艰难的决定。公司的5款药物(REC-994、REC-2282、REC-3964、REC-4539和REC-4209)宣布暂停或取消优先开发。其中,REC-994是一种超氧化物清除剂小分子,用于治疗脑海绵状血管畸形。该药物的临床数据是Recursion有史以来第一个Ⅱ期数据,然而,该数据显示疗效指标的数据好坏参半,公司只好放弃该药物的开发。
【参考资料】
1. Precedence Research、医药地理、财联社、德睿智药、智药局、药渡等网络公开资源.
本文其它内容请见《全球药物创新快讯》2026年第1期(总第158期)。
2025-12-27
·制药网
【制药网 行业动态】随着人工智能和计算机技术的发展, AI技术在药物研发上的应用价值正不断释放,当前众多药企都在利用AI技术加速新药的开发,但与此同时,有不少基于AI开发的药物管线也在这几年陆续宣告失败。 近日,AI制药公司Verge Genomics宣布终止其进入临床阶段的候选AI药物VRG50635的开发,因“缺乏风险收益数据”而终止。 据了解,VRG50635是公司利用AI平台——CONVERGE端到端药物发现平台发现的PIKfyve抑制剂,旨在治疗肌萎缩侧索硬化症(ALS,俗称渐冻症)。该药物是Verge Genomics唯一进入临床阶段的资产,自2022年10月启动人体给药以来,被视为公司核心项目。 但近期其在肌萎缩侧索硬化症患者1b期的疗效方面未达到标准,临床试验已终止。公司表示,未来将转型为以人工智能平台和专有数据库为基础的合作模式,协助外部伙伴提升药物发现效率。值得注意的是,在药物失败的同时,Verge还经历了管理层的大换血。自去年起,公司大部分高管已离职,包括总裁兼首席商务官、首席财务官、首席科学官和首席医疗官。 实际上,近年来全球多家AI制药公司都进行了临床管线的战略性缩减与调整,除了Verge Genomics的 VRG50635,也有不少AI 药物在今年宣布终止或暂停,涉及肿瘤、神经退行性疾病、纤维化等领域。 如AI制药企业薛定谔在今年8月宣布停止CDC7抑制剂SGR-2921的临床开发计划。该药物是一款针对复发/难治性急性髓性白血病(AML)或高危骨髓增生异常综合征(MDS)患者的小分子抑制剂。这项开放标签、剂量递增研究于2023年开始,旨在评估SGR-2921的安全性和药代动力学,并探索性地计划测试其与其他AML/MDS治疗联合使用的初步抗肿瘤活性。 此外,AI药物研发上市公司Recursion近一年来也经历了一系列管线失败和大调整。首先,一款针对罕见病小分子药物REC-994 的 2 期数据,该药物尽管耐受性和安全性良好,但疗效有限。紧接着,公司又砍掉一半临床管线,五款药物宣布暂停或取消优先开发,包括REC-2282(2型神经纤维瘤病)、REC-994(脑海绵状血管畸形)、REC-3565(MALT1 抑制剂,B 细胞恶性肿瘤)、REC-3964(艰难梭菌感染)、REC-4209(特发性肺纤维化)。 尽管面临诸多挑战与失败,但AI制药行业的未来依然充满希望。未来,随着AI 技术的加速进化,AI有望更精准地预测药物分子的生物活性和安全性,大幅缩短研发周期。业内认为,将来那些构建 “AI + 实验验证” 闭环、聚焦高壁垒靶点、重视临床数据与商业化的企业,才能在医药创新大势下脱颖而出。 尽管面临诸多挑战,AI制药行业的未来依然充满希望。行业内的合作与整合已成为推动AI制药发展的重要驱动力,大型药企与AI公司的协同将更加紧密,共同推动创新药从研发到商业化的全链条进化,而商业模式也将向多元化延伸,从单一“技术采购”转向“风险共担”等深度合作模式。 免责声明:在任何情况下,本文中的信息或表述的意见,均不构成对任何人的投资建议。
临床1期临床2期
2025-12-09
医道社:传承和发展民间中医
来源:海外网站 作者:医道社整理
版权归原作者所有,如有违规、侵权请联系我们删除!
👆关注不迷路,更多创新药前沿资讯
大家好,我是你们的创新药专业博主。今天咱们来聊聊Recursion Pharmaceuticals(纳斯达克:RXRX),这家AI制药领域的“黑马”。不是空谈概念,而是围绕他们最新公布的REC-4881在家族性腺瘤性息肉病(FAP)TUPELO 1b/2期试验数据,深入剖析一下。这项数据于2025年12月8日发布,股价应声上涨,但更重要的是,它标志着AI药物发现从实验室走到真实患者身上的关键一步。作为临床医生和药品研发人员,你们肯定对罕见病的治疗瓶颈和AI在机制探索中的潜力特别感兴趣。这篇文章会用硬核事实和数据,帮大家梳理清楚Recursion的平台逻辑,为什么它可能重塑我们对药物研发的认知。走起,一起看看这个“漂亮一拳”背后的故事。一、临床数据详解:REC-4881在FAP患者身上的“不寻常”表现
先直奔主题:FAP是一种残酷的遗传性疾病,由APC基因突变引起,导致肠道长出数百到上千个腺瘤性息肉。如果不干预,患者40岁前结直肠癌风险接近100%。目前没有获批药物,患者只能靠频繁内镜下息肉电切除和预防性结肠切除术“维持”,这往往在20多岁就永久影响生活质量。Recursion的REC-4881是一款口服MEK1/2抑制剂,通过AI平台发现并重定位到FAP适应症。这次TUPELO试验(开放标签,4mg QD剂量)的中期结果,让人眼前一亮。疗效数据:快速减轻+停药后持久响应
·第13周(治疗12周时):在12名疗效可评估患者(≥55岁队列)中,息肉总负荷中位数减少43%,75%患者息肉负担减轻,40%患者Spigelman分期(上消化道严重度指标,直接影响随访和手术决策)改善≥1分。
·第25周(停药12周后随访):11名患者中,82%维持响应,中位数减少进一步升至53%,73%实现≥30%的持久减轻。患者在第13周后停药,仅观察,这意味着疗效有“后劲”。
对比自然史数据(Recursion与阿姆斯特丹大学医学中心合作,分析n=55符合标准患者):87%未治疗患者息肉负荷年化增加(平均+60%,中位数+28%),仅3%自发轻微下降。REC-4881完全逆转了这一轨迹,在一个“默认只会恶化”的疾病中,实现器官层面(内镜可见)的结构改善。这在癌前病变或肿瘤前综合征的试验中,非常罕见。
临床医生视角:犹他大学医学院的TUPELO首席研究者Jessica Stout博士评论道,“在一个结直肠癌终生风险接近100%、没有获批药物、只能靠手术维持生命的疾病里,看到停药12周后依然持续减负的药物效果,对患者来说意义非常大。”这不只是数字,而是潜在的非手术希望——减少手术频率,提升生活质量。安全性:MEK抑制剂类的一致性
合并1b+2期安全性队列(n=19):94.7%患者有治疗相关不良事件(TRAE),但绝大多数为1-2级(如痤疮样皮疹、CK升高)。3级TRAE发生率约15.8%,无≥4级事件,仅2人因AE短暂中断,无永久停药。整体可控,符合MEK抑制剂预期。
外部补充:BioSpace 2024年报道类似AI驱动罕见病试验(如Biodexa的eRapa II期,息肉减少17-29%,但无停药耐久数据),REC-4881的“快速+持久”信号更优。Evaluate Pharma 2024分析指出,FAP市场虽小(美欧>5万患者),但孤儿药地位+快速通道可带来高定价,峰值销售>5亿美元。更关键的是,这验证了AI在“无药可医”领域的突破。传统药物发现成功率<10%、周期15年、成本26亿美元(Tufts CSDD数据),Recursion用AI从数千化合物中“钓”出REC-4881,仅几年就进入临床,成本降至传统1/10。
为什么震撼?样本虽小(单臂设计),但在FAP这种机制明确的罕见病中,它提供了强信号:REC-4881已获FDA快速通道、孤儿药认定及欧盟孤儿药资格,计划2026年上半年讨论注册路径(可能单臂+自然史对比,或小型对照)。乐观情景下,商业化或在2028年后实现。二、技术护城河:Recursion OS——从细胞图像到患者获益的完整闭环
REC-4881不是运气,而是Recursion OS平台的产物。这套“制药操作系统”把生物学从“艺术”变成“工程”,融合数据、模型和计算,形成闭环反馈。不同于传统“靶点优先”的老路,Recursion用无偏表型筛查+机器学习,直接从“病态 vs 健康”细胞中破解谜题。1. 数据壁垒:65PB的“生物石油”,每周百万级实验反馈
Recursion构建了全球最大专有生物数据集——65PB多模态数据(截至2025年中),包括表型组学、转录组学、蛋白质组学、ADME、去标识患者EHR(电子健康记录)。自动化湿实验室(机器人+计算机视觉)每周生成数百万细胞实验数据,形成“飞轮效应”。
事实:2023年Recursion年报显示,这个数据集比辉瑞或罗氏内部数据大10倍。Nature Reviews Drug Discovery 2024(基于McKinsey报告)指出,AI制药需海量数据,Recursion模型准确率达85%以上,而传统仅50%。ClinTech子模块分析>1000名FAP患者EHR+25万条临床笔记,用定制LLM结构化医生自由文本,优化试验设计(如扩展至≥18岁)。
在REC-4881发现中:AI从APC缺陷模型中提取>1000个细胞形态特征,一键评分化合物“拯救”能力。平台优先标记MEK1/2抑制为“拯救机制”,逆转ERK/MAPK过度激活。从武田(Takeda)授权的实体瘤分子,重定位到FAP,仅用1年。2. 模型创新:无偏表型筛查,零假设驱动的“黑箱破解”
高内涵成像+ML模型:不预设机制,直接比较病态/健康细胞,识别逆转表型的化合物。Recursion OS v2.0(2024更新)训练数万亿生物-化学关系,在FAP中从纯数据得出MEK1/2抑制的结论——不是人类先验,而是AI主导。
外部观点:Forbes 2024专访CEO Chris Gibson,强调ML模型在罕见病“机制发现”率是传统3倍。MIT Technology Review报告:AI表型筛查缩短早期发现时间50%。REC-4881高度匹配APC丢失场景:在其他肿瘤模型中不表现出类似效果,证明平台精准性。3. 计算引擎:BioHive-2,NVIDIA的“制药超级计算机”
2023年NVIDIA投资7000万美元(持股~4%),共建BioHive-2——生物制药最强AI超级计算机,每周模拟>1亿实验,成本降至传统1/5。NVIDIA GTC 2024演示:Recursion模型训练速度是竞品2倍,帮助发现>20个新靶点。
震撼思考:制药业计算力短缺导致90%项目失败(Deloitte 2023报告)。Recursion的闭环(数据→模型→实验→反馈)迭代速度是传统10倍。FAP试验是首个完整“验证周期”:无偏AI洞察→机制明确→分子引入→临床获益。这证明OS不是“PPT”,而是“疾病操作系统”——上游机制探索、中游筛选生成、下游临床设计。
深度观点:平台通用性强,已延伸到肿瘤/罕见病(如HPP低磷酸酶症)。Statista 2024预测:AI药物市场到2030年达500亿美元,Recursion占10%份额可期。三、公司战略:伙伴生态+财务韧性,构建“TechBio”帝国
技术牛,但执行力决定一切。Recursion不是“单药赌命型”biotech,而是“基础设施公司”,用战略布局筑护城河。1. 管线策略:敢于“砍”,聚焦AI信号最强方向
2024年收购Exscientia部分资产(真实整合AI能力)后,2025年5月清理管线:降低REC-2282(NF2)、REC-994(脑海绵状畸形)、REC-3964(艰难梭菌感染)优先级,暂停REC-4539(肿瘤)。聚焦6大项目:4肿瘤、2罕见病(FAP+REV-102 HPP,2025年中从Rallybio收购的口服ENPP1抑制剂)。
这释放信号:用数据“砍”项目,不是堆砌刷存在感。REV-102将是下一个“口服疾病修饰疗法”验证点。2. 伙伴网络:大药企+科技巨头的金矿
与罗氏/基因泰克(全基因组敲除,2025 Q3获3000万美元里程碑)、拜耳(纤维化)、默克KGaA、赛诺菲深度绑定,前期+里程碑>5亿美元。NVIDIA的BioNeMo推动OS商业化。Bloomberg 2024报道:此类伙伴让非稀释融资达2亿美元,远超同规模AI Bio公司。3. 财务韧性:7.85亿美元现金,跑道至2027
2025 Q3财报:收入520万美元(合作里程碑缓冲),研发1.211亿美元/季,净亏损1.623亿美元/季。现金6.671亿美元(9月底),调整后约7.85亿美元,烧钱率1.2亿美元/季,支撑至2027年底无稀释。Yahoo Finance分析:现金/烧钱比是AI Bio中位数1.5倍。相比现金告急竞品,Recursion有“耐力赛”优势。高烧钱投资平台,回报是管道价值(Clarivate 2024估FAP峰值>5亿)。4. 领导交接:从创始人驱动到R&D+BD一体
2026年1月1日起,Najat Khan博士(现首席研发及商务官)接任CEO,Chris Gibson转董事长。Khan的AI+商务背景,确保平台商业化。Seeking Alpha 2024报告:风险低,Khan的“绿色芽”言论提振信心。TipRanks共识:中等买入,目标价8美元(从4.71美元涨70%)。
护城河是“生态”:技术+伙伴+现金,正反馈。Motley Fool 2024称:Recursion是“AI制药的NVIDIA”,高风险高回报。四、行业对比与深度思考:Recursion的差异化位置
与其他AI制药公司比,Recursion的独特在于完整闭环和落地证据。
维度
Recursion Pharmaceuticals
其他AI制药公司典型模式
数据规模
自建65PB专有数据集,每周数百万湿实验
多依赖公共数据或有限合作数据
技术栈
全栈式:湿实验自动化+超级计算+AI模型+临床洞察
侧重算法或单一环节(如分子生成)
临床验证
REC-4881提供从发现到临床的完整案例
多处于临床前或早期,缺乏完整验证
生态位
聚焦罕见病及遗传驱动肿瘤,生物学清晰
部分尝试复杂常见病,机制模糊
商业化路径
自主推进核心管线+大型药企合作授权
多数依赖授权,缺乏自主能力
如Insilico(NASH/IPF II期,但无明确获益验证)、Exscientia(传统+AI优化,无平台闭环)、BenevolentAI(管线失败调整)、Relay/Schrödinger(物理建模,非表型AI)。Recursion在FAP做到:AI主导机制(MEK抑制非主流假说)+重定位+人体器官改善。
为什么重要?
·回答质疑:AI不是优化已知靶点,而是发现全新机制(表型优先跳出人类先验)。
·平台可重复性:首个“验证周期”,有望复制到HPP等。价值从“项目”转向“操作系统”。
·产业启示:AI表型平台在罕见遗传病中给出“器官结构改变”证据(息肉下降40-50%),打开非直观靶点空间。类似2010年代云计算,Recursion OS或成2030医药基础设施。
·斯普特尼克时刻:在万亿美元制药业,90%失败率,Recursion用AI拉成功率至30%以上(内部数据),为患者带来非手术希望。五、市场反应、风险与挑战:冷静背后的现实考量
数据亮眼,但RXRX股价仅盘前涨6%,收盘4-5美元(低于52周高点和200日均线)。原因:
·样本小(12-19人,单臂,无随机对照),只是“强信号”,非注册证据。
·上市路径长(2026 FDA讨论,2028+商业化)。
·高烧钱(季度>1.2亿R&D),AI Bio估值重估,市场对“科技感”容忍低。
·空头高(Benzinga名单),竞争加剧(大药企自建AI,Google/Meta工具释放)。
·华尔街分裂:MarketBeat持平,6分析师平均7.25美元目标。
风险:
·临床:需更大规模验证疗效/长期安全,尤其年轻患者。
·商业:FAP市场小,需证明优于手术,说服支付方。
·财务:2027后或需融资/合作。
·竞争:若无多闭环,领先稀释。
投资视角(DYOR):对长线玩家,卫星仓值得(当前4美元,潜力翻倍);保守者,等III期。但对医生/研发者,这是跟踪AI转化的绝佳案例。结语:AI制药的曙光已现,Recursion值得我们持续关注
Recursion的REC-4881/FAP数据,不是小新闻,而是AI制药的“iPhone时刻”起点:从65PB数据诞生首创药,逆转癌症宿命,成本效率碾压传统。技术领先5年,公司生态筑牢根基。它证明机器能学习生命的语言,在棘手疾病中找到突破——但需复制多次,才成基础设施。
作为医生和研发者,你们或许在想:这对临床实践和机制研究意味着什么?它打开了表型AI在罕见病中的大门,或许很快会影响你们的患者管理。未来催化剂:2026 FDA讨论、HPP进展、合作里程碑。AI不是万能,但给它数据+算力+勇气,它确实能打出“漂亮一拳”。
欢迎评论你的看法:作为一线医生,你怎么看这种停药后持久疗效?研发者们,表型筛查会改变你的工作流吗?关注公众号,更多深度解析。参考来源:Recursion官网新闻稿、2025 Q3财报、BioSpace、Forbes、Nature Reviews、路透社、Benzinga、Evaluate Pharma、Seeking Alpha、Yahoo Finance、学术文献(全基于2024-2025公开数据,非虚构)。投资有风险,DYOR。
临床结果临床2期
100 项与 REC-163964 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 复发性艰难梭菌感染 | 临床2期 | 美国 | 2024-10-14 | |
| 艰难梭菌感染 | 临床2期 | - | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
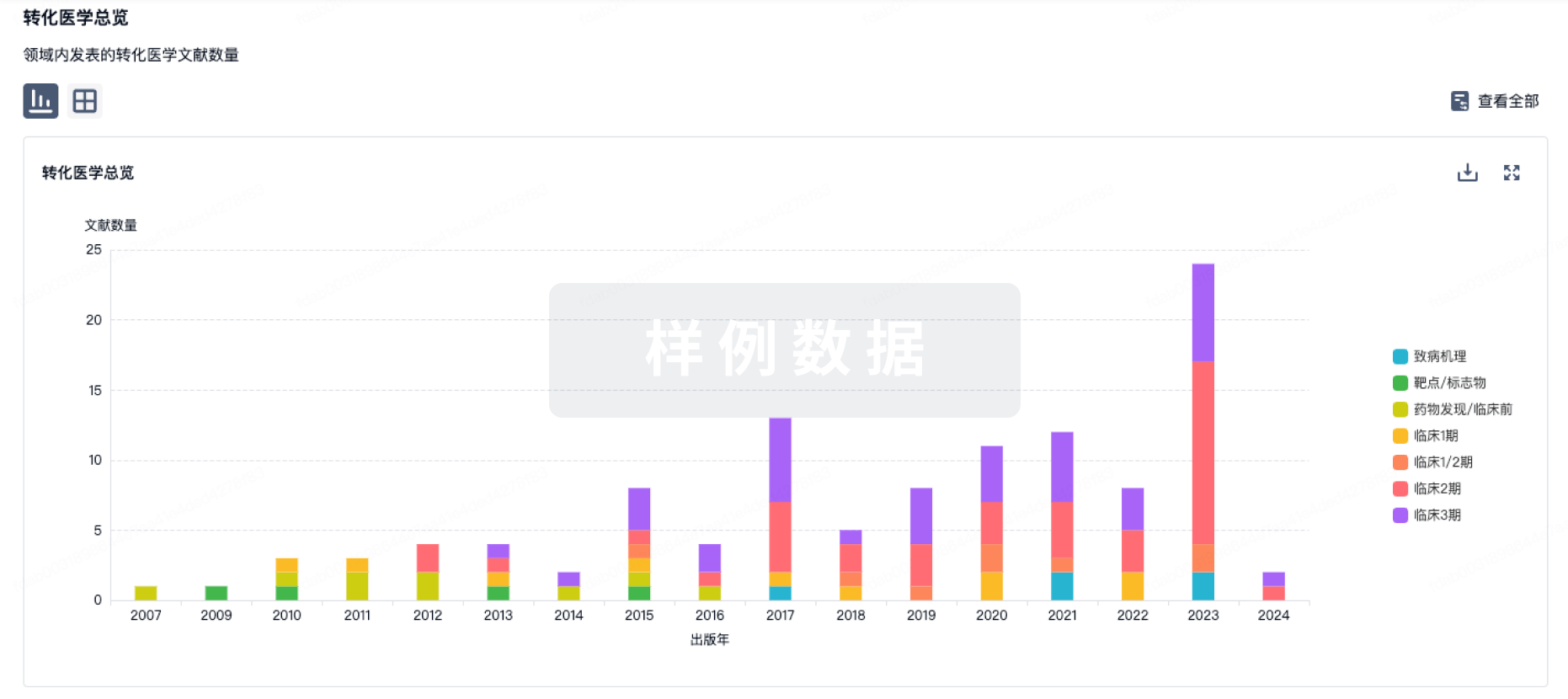
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
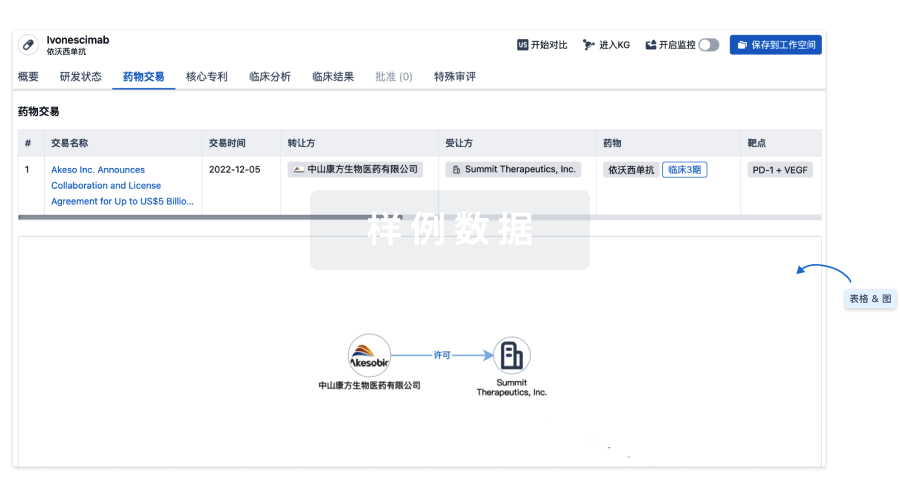
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
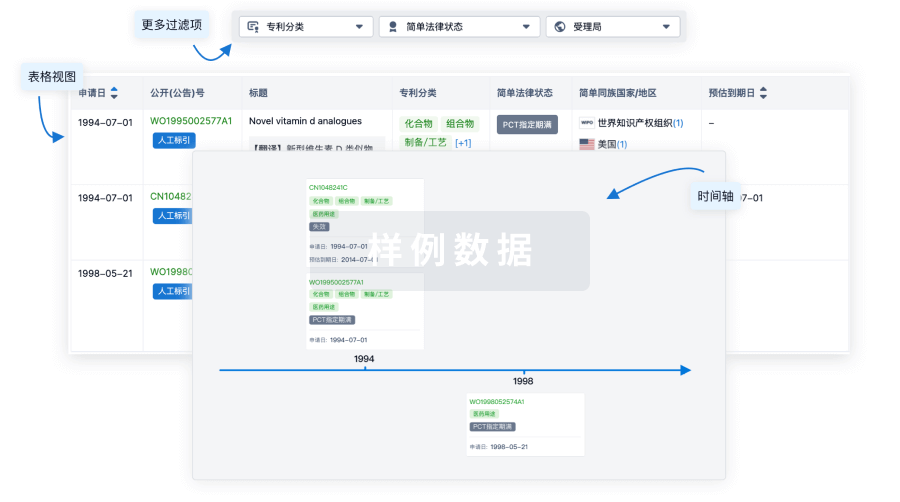
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
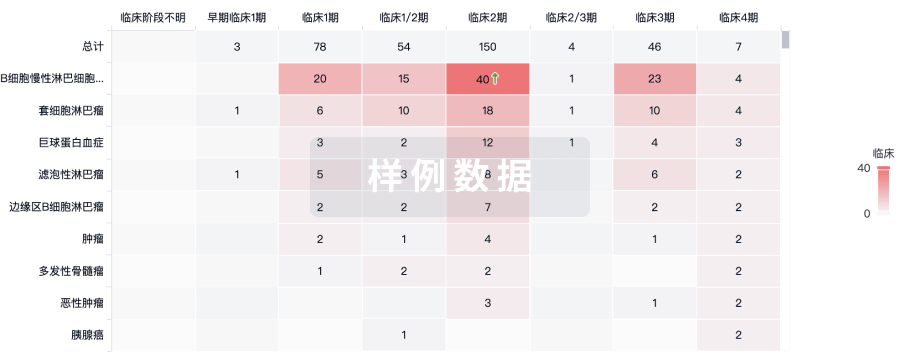
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
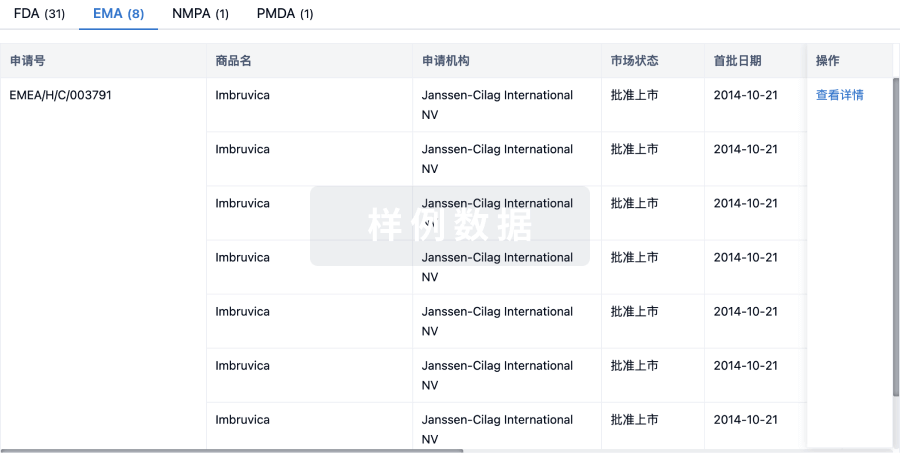
批准
利用最新的监管批准信息加速您的研究。
登录
或
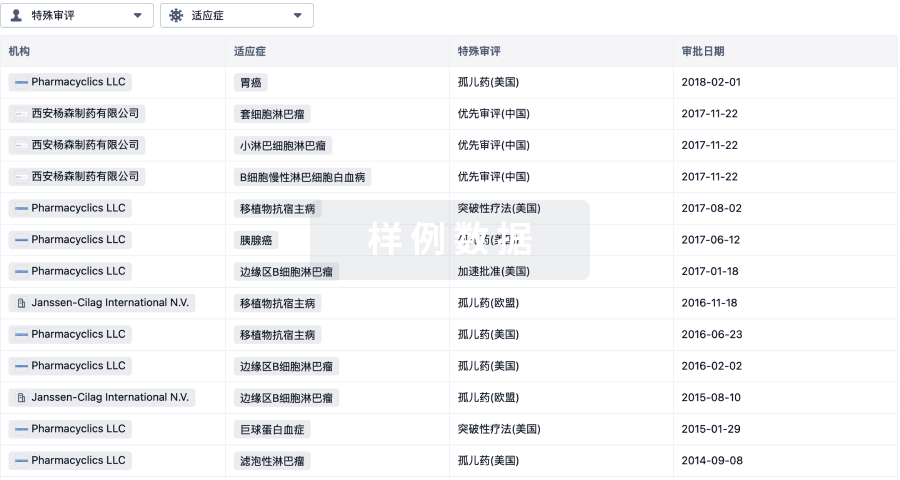
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
