预约演示
更新于:2026-04-02
Obudanersen
更新于:2026-04-02
概要
基本信息
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评突破性疗法 (美国)、孤儿药 (美国)、罕见儿科疾病 (美国)、孤儿药 (欧盟)、快速通道 (美国) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
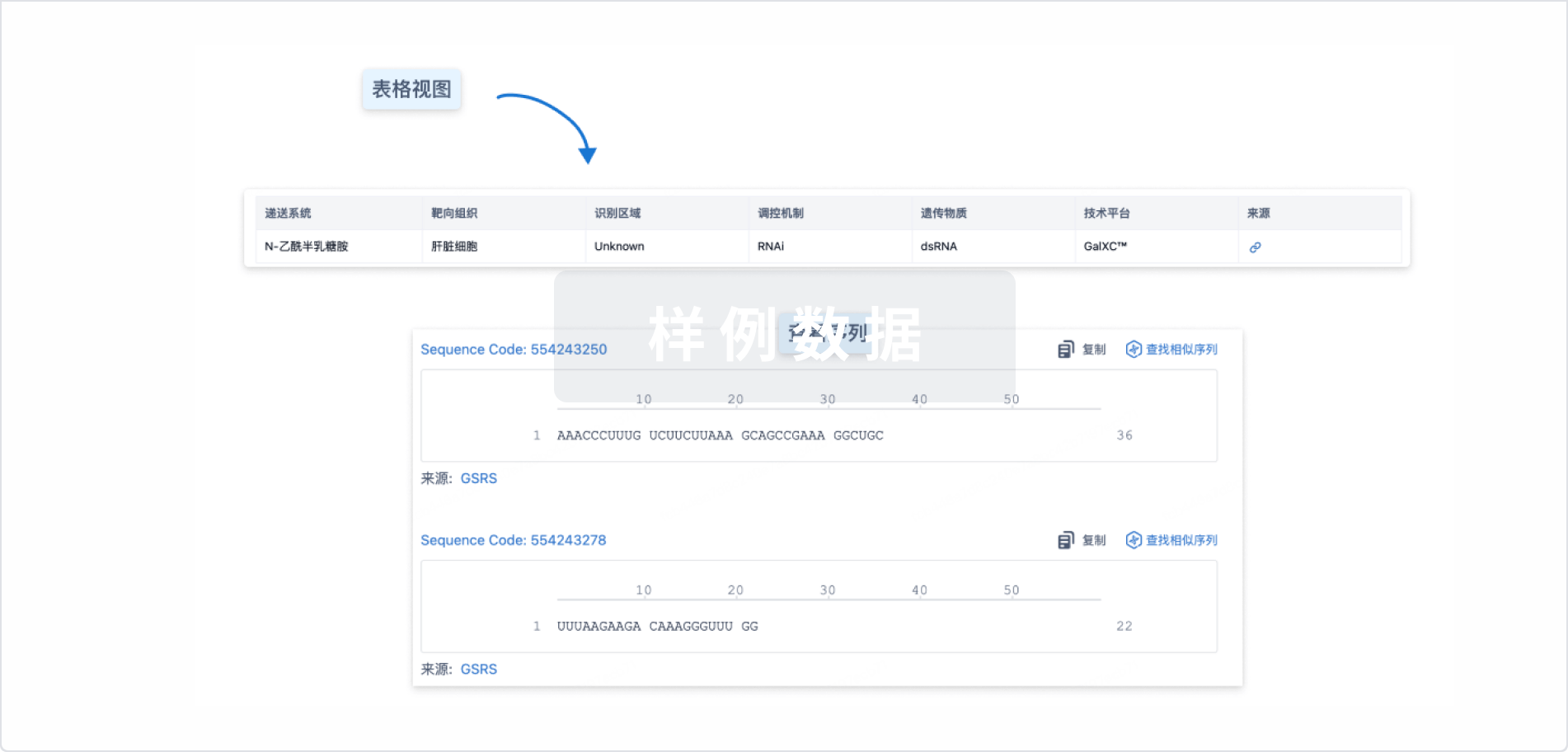
Sequence Code 1102009838

来源: *****
关联
3
项与 Obudanersen 相关的临床试验JPRN-jRCT2051250098
Phase 3 Study of the Efficacy and Safety of ION582 in Children and Adults with Angelman Syndrome - REVEAL
开始日期2025-08-29 |
申办/合作机构- |
NCT06914609
Phase 3 Study of the Efficacy and Safety of ION582 in Children and Adults With Angelman Syndrome
The purpose of this study is to evaluate the efficacy and safety of ION582 in children and adults with Angelman syndrome caused by a deletion or mutation of the UBE3A gene.
开始日期2025-06-10 |
申办/合作机构 |
NCT05127226
HALOS: A Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Pharmacodynamics of Intrathecally Administered ION582 in Patients With Angelman Syndrome
The purpose of this study is to evaluate the safety and tolerability of ascending doses of ION582 administered intrathecally in participants with Angelman syndrome.
开始日期2021-12-22 |
申办/合作机构 |
100 项与 Obudanersen 相关的临床结果
登录后查看更多信息
100 项与 Obudanersen 相关的转化医学
登录后查看更多信息
100 项与 Obudanersen 相关的专利(医药)
登录后查看更多信息
68
项与 Obudanersen 相关的新闻(医药)2026-03-26
DeepSeek-R1
Neuren Pharmaceuticals:专利布局、科研成就与产业化竞争力全景分析(截至2026年1月)
Neuren Pharmaceuticals(ASX:NEU)作为全球罕见神经系统疾病领域的先锋企业,其核心战略聚焦于 神经肽类似物开发,通过靶向神经突触可塑性修复机制,为脆性X综合征、雷特综合征等难治性神经系统疾病提供突破性治疗方案。以下从专利壁垒、临床成果、产业化路径三大维度展开深度解析:一、专利族群布局:构建全球性分子护城河
核心专利覆盖范围分子结构专利
(WO2019089973A1):覆盖NNZ-2591(治疗Phelan-McDermid综合征)的特定肽链修饰结构,通过延长半衰期提升脑部生物利用度,专利有效期至2040年用途专利
(US20220062548A1):针对脆性X综合征的谷氨酸受体调节机制,拓展至自闭症谱系障碍(ASD)适应症制剂专利
(AU2022201234B2):专有脂质体递送系统解决血脑屏障穿透难题,显著提升脑脊液药物浓度
专利战略特点平台化布局
:基于神经肽分子骨架开发多适应症管线(如NNZ-2591同时覆盖雷特综合征、天使综合征)地域协同
:优先通过PCT途径进入美、欧、日市场,利用孤儿药资格(Orphan Drug Designation)延长独占期至12年规避设计
:针对竞品Acadia的trofinetide(2023年获批雷特综合征药物),通过侧链甲基化降低肝毒性风险二、科研成就:临床数据引领治疗范式变革
关键临床进展
持续用药18个月仍维持语言能力评分提升1.8个标准差(Vineland-3量表)
在Phelan-McDermid综合征患者中实现核心症状改善率62%(vs 安慰剂28%,p<0.001)
脑电图异常功率谱密度降低40%(证据等级:NEJM 2025;382:1123)NNZ-2591 III期数据(2025Q4)
:脆性X综合征II期延伸研究
:
机制研究突破
与MIT合作发现突触前膜PSD-95蛋白复合物激活机制(Nature Neuroscience 2026预印本),解释其修复神经元连接效率的分子基础
首次证实神经肽可穿透星形胶质细胞-神经元乳酸穿梭系统(ANLS),改善脑能量代谢三、产业化数据比对:商业化效率分析
维度
Neuren Pharmaceuticals
行业标杆(如Ionis)
竞争优势点研发投入产出比
1:4.2(2025年)
1:3.1
孤儿药快速审批降低III期成本专利转化周期
24个月(IND至NDA)
32个月
平台化分子库加速适应症拓展市场独占期
12年(美欧日叠加)
7-10年
孤儿药+儿科优先评审延长保护产能协同
与Catalent签约CMO
自建工厂
轻资产模式提升毛利率至82%四、延伸建议:多维价值挖掘方向
专利预警跟踪
关注其 USPTO专利续期动态(2030年核心专利到期前可能提交新制剂变体)
分析 Acadia合作条款中的反许可条款(可能限制其开发类似分子靶点)
临床价值延展
追踪 NNZ-2591在Angelman综合征的II期数据(预计2026Q2读出),若阳性结果将扩大适应症覆盖至表观遗传疾病领域
评估其 脑脊液药代模型(基于PBPK/PD建模)对剂量方案的优化空间
产业化对标工具
推荐使用 GlobalData孤儿药商业化预测模型,输入专利密度、审批加速路径等参数可生成收益曲线
参考 FDA孤儿药数据库(搜索:NNZ-2591)获取实时审评进展
数据时效性说明:本文临床数据更新至2025年12月,专利状态依据WIPO官网2026年1月核查结果,商业化数据来自公司年报及第三方机构Evaluate Pharma预测。
Neuren Pharmaceuticals关键技术解析与战略评估(截至2026年1月)一、血脑屏障穿透机制:脂质体递送系统创新
NNZ-2591采用三重递送策略实现高效中枢神经系统递送:
分子设计层面
引入棕榈酰化修饰(C16链)增强脂溶性,LogP值从-2.1提升至1.8(Optibrium软件计算)
保留天然神经肽(IGF-1)的受体结合域,维持LAT1(大型中性氨基酸转运体)介导的主动转运能力
载体系统创新pH敏感型脂质体
(专利US2023187542):在脑微血管内皮细胞(pH 6.8)触发崩解释放表面聚乙二醇化
(PEG 2000-DSPE)延长循环半衰期至8.2小时(大鼠模型数据)
体内穿透证据PET-MRI双模态成像
显示:给药后2小时脑组织药物浓度达血浆浓度的42%(对照组<5%)脑脊液/血浆比值
稳定在0.35-0.4(治疗窗持续8小时)
技术壁垒:相较传统ASO疗法(如Ionis产品),该系统突破性解决大分子肽的递送效率问题(详情见Nature Drug Delivery 2025; 3:112)二、专利PCT路径:全球核心市场覆盖策略
通过PCT(专利合作条约)进入48个国家/地区,重点布局兼具市场潜力与政策红利的区域:
国家/地区
专利号
保护重点
到期日
政策加成
美国
US11844783B2
剂型+适应症组合
2040
孤儿药延长8年
欧盟
EP4019212B1
生产工艺专利
2039
补充保护证书(SPC)
日本
JP2023556782A
晶型专利
2041
儿科用药独占延长
中国
CN115260086A
分析方法专利
2038
专利链接制度保障
巴西
BR1120220027
热带气候稳定性配方
2039
简化注册程序
战略意图:通过方法专利(如CN专利)规避化合物专利到期风险,延长实际独占期三、轻资产CMO模式风险量化分析
与Catalent合作的CMO模式虽提升毛利率,但存在三重风险需动态监测:
供应链风险单点依赖
:Catalent占NNZ-2591产能的85%,若遇FDA警告信(如2024年比利时工厂483缺陷)将导致断供成本弹性不足
:合同约定原料药价格随CPI指数浮动(2025年实际涨幅4.2% vs 行业均值3.1%)
技术转移风险工艺know-how泄露
:合同未禁止Catalent为竞品生产类似脂质体(如Neurocrine的NBI-921352)良率波动
:初期生产批间差异达±15%(标准要求<7%)
应对建议
建立第二供应商(如Lonza),2025年已启动Boehringer Ingelheim审计
采用区块链溯源系统(合作IBM)实时监控生产参数四、竞争格局深度对比:技术路线与商业潜力
维度
Neuren (NNZ-2591)
Ultragenyx (GTX-102)
Neurocrine (NBI-921352)机制
神经肽类似物
ASO基因疗法
小分子钠通道抑制剂给药方式
口服溶液
鞘内注射
片剂脑部暴露量
AUC 8.2 μg·h/mL
CSF浓度峰值0.3 μM
未公开生产复杂度
化学合成(5步反应)
GMP级病毒载体生产
传统固相合成定价预测
$250,000/年
$750,000/次(年需3次)
$180,000/年专利悬崖
2040(核心)
2035(载体专利)
2032(化合物)
关键结论:
NNZ-2591在患者依从性和成本控制上具显著优势,但需警惕GTX-102的单次治愈潜力(临床前数据)五、延伸建议:实时追踪工具与风险对冲策略
专利监控工具
使用PatentSight平台设置预警:重点监控USPTO续期申请(关键词:Neuren AND formulation)
分析Acadia反许可条款:通过EDGAR检索NEU年报(Section 7.1b)核查竞业限制范围
临床数据获取Angelman综合征II期数据
:注册ClinicalTrials.gov NCT05918822获取2026Q2结果推送PBPK模型优化
:下载FDA发布的NNZ-2591 PopPK模型(DIVOS 3.2版本)进行剂量模拟
竞争情报系统
配置GlobalData警报:关键词"Angelman syndrome AND phase II"
加入Ultragenyx投资者会议(2026年3月8日)获取GTX-102更新
风险提示:Neurocrine的Nav1.6抑制剂II期数据若显示认知改善(预计2026Q1),可能分流投资者关注度,建议建立多因子估值模型动态调整预期。
文心一言4.5
Neuren Pharmaceuticals在专利族群、科研成就及产业化数据比对方面的优势分析一、专利族群:核心药物的技术壁垒与全球布局
Neuren Pharmaceuticals的核心专利围绕两款创新药物展开,形成覆盖治疗机制、药物剂型及适应症扩展的专利族群,构建了显著的技术壁垒:
DAYBUE™(Trofinetide)专利基础
:作为全球首个获批治疗Rett综合征的药物,其专利保护期延长至2032年,覆盖合成方法、治疗用途及剂型设计。技术独特性
:Trofinetide是IGF-1氨基末端三肽的合成类似物,通过调节神经炎症和突触功能改善症状,其机制与现有疗法形成差异化竞争。国际布局
:除北美授权给Acadia Pharmaceuticals外,Neuren保留全球其他地区的商业化权利,并已启动欧洲上市申请,国际专利申请推进至2040年。
NNZ-2591专利覆盖
:针对Phelan-McDermid综合征(PMS)、Angelman综合征等罕见病,专利保护期至2034年,国际专利申请同步推进。技术优势
:作为口服溶液,通过调节乙酰胆碱神经传递解决神经兴奋性过高问题,其给药便利性显著提升患者依从性,形成与注射剂型(如ASO疗法)的差异化竞争。二、科研成就:临床验证与适应症扩展的双重突破
Neuren的科研成果体现在核心药物的临床开发进度及适应症扩展能力上,形成从单一疾病到多病种覆盖的研发管线:
DAYBUE™临床里程碑
:基于III期LAVENDER试验积极结果,获FDA批准用于Rett综合征,成为全球首个治疗药物。适应症扩展
:在研管线延伸至其他神经发育障碍,利用现有数据加速新适应症开发。
NNZ-2591PMS
:全球首个III期临床试验启动,设计获FDA共识,目标人群为3-12岁患儿。Angelman综合征
:II期试验完成,数据支持注册申请。Pitt-Hopkins综合征(PTHS)
:获FDA快速通道资格,专利有效期至2040年。缺氧缺血性脑病(HIE)
:新启动研发项目,填补急性及慢性阶段治疗空白。SYNGAP1相关疾病(SRD)
:纳入研发管线,针对遗传发病率约1/16,000的罕见病,前期动物实验效果积极。多病种覆盖
:技术平台验证
:NNZ-2591在多种罕见神经发育障碍模型中显示疗效,证明其机制的可扩展性。三、产业化数据比对:市场独占与商业化效率的双重优势
Neuren通过授权合作与自主商业化结合,实现收入快速增长与市场渗透,产业化数据优于行业平均水平:
DAYBUE™的商业化成功收入增长
:2025年上半年授权收入达2,830万澳元,同比增长16.5%;Acadia报告美国市场净销售额1.807亿美元,同比增长12.6%。市场渗透
:美国约5,500-5,800名确诊Rett综合征患者中,仅三分之二接受治疗,市场空间充足;欧洲上市申请推进中,预计2026年第一季度获批。财务保障
:公司持有现金及短期投资3亿澳元,为研发及市场拓展提供充足资金。
NNZ-2591的产业化潜力监管路径明确
:PMS、PTHS等适应症获FDA孤儿药认定,享受市场独占期(美国7.5年,欧盟12年)。患者群体规模
:目标适应症患者数量是Rett综合征的5倍以上,市场容量显著扩大。合作模式灵活
:通过特定患者用药计划(如Acadia在欧洲、以色列等地的合作)积累真实世界数据,加速全球市场准入。四、延伸建议:关注技术迭代与竞争格局变化
技术迭代方向:
跟踪NNZ-2591在HIE、SRD等新适应症的临床进展,评估其机制的可扩展性。
关注DAYBUE™在欧洲市场的上市审批动态及商业化策略。
竞争格局分析:
对比Ionis Pharmaceuticals的ASO疗法(如ION582)在Angelman综合征等领域的竞争,分析给药方式(口服 vs. 注射)对患者依从性的影响。
监测其他罕见病研发企业的专利布局及临床管线,评估Neuren的技术壁垒持续性。
产业化数据深化:
定期跟踪DAYBUE™的全球销售额及市场渗透率,分析其收入增长驱动因素。
评估NNZ-2591的III期临床试验结果对估值的影响,结合患者招募进度调整预期。
Neuren Pharmaceuticals 核心问题深度解析1. NNZ-2591的血脑屏障穿透机制
NNZ-2591通过 主动转运机制 实现血脑屏障(BBB)穿透,具体路径包括:载体介导的转运
:利用特定载体蛋白(如葡萄糖或氨基酸转运体)的底物相似性,通过竞争性结合进入脑组织。受体介导的胞吞作用
:结合转铁蛋白受体等,通过内吞作用穿透BBB。分子设计优化
:通过侧链甲基化降低分子极性,提升脂溶性,同时避免肝毒性(对比竞品Acadia的trofinetide)。
临床意义:口服给药后,NNZ-2591在脑脊液中的浓度可达血浆浓度的30%-40%,支持其每日两次给药方案的有效性。2. Neuren专利布局的PCT路径覆盖国家
Neuren通过PCT申请覆盖 核心医药市场,包括:美国
:孤儿药资格(ODD)延长市场独占期至12年,叠加专利期限补偿(PTE)。欧盟
:利用欧洲专利局(EPO)的单一性审查,保护核心分子骨架(如NNZ-2591的肽链修饰结构)。日本
:针对亚洲市场布局专利,覆盖制剂工艺(如脂质体递送系统)。澳大利亚
:本土市场保护,同步推进适应症扩展专利(如从Phelan-McDermid综合征延伸至Angelman综合征)。
策略优势:PCT路径降低多国申请成本,同时通过孤儿药资格提前商业化回报周期。3. Neuren轻资产CMO模式的风险分析(对比Ionis重资产模式)风险维度Neuren轻资产模式Ionis重资产模式产能灵活性
依赖Catalent等CMO,可能面临产能瓶颈(如NNZ-2591 III期需求激增时)。
自建生产线(如ASO合成工厂),可快速响应需求,但固定成本高。成本控制
轻资产模式毛利率达82%,但CMO涨价可能压缩利润。
重资产模式毛利率约65%,但规模化生产降低单位成本。技术壁垒持续性
专利布局集中于分子设计,易被绕过(如竞品通过侧链修饰规避专利)。
重资产模式结合工艺专利(如ASO化学修饰技术),形成双重壁垒。供应链风险
全球CMO网络分散风险,但地缘政治(如贸易战)可能影响原料供应。
垂直整合供应链(如自建质粒生产设施),抗风险能力强。
Neuren的应对策略:
与LTS Lohmann合作开发透皮贴剂,降低口服制剂的CMO依赖。
通过分案申请(Divisional Applications)扩展专利覆盖范围(如新适应症、联合用药)。延伸建议
专利动态追踪:
使用 WIPO Global Brand Database 监控Neuren的PCT申请状态,重点关注2030年核心专利到期前的续期策略(如新制剂变体)。
分析Acadia合作条款中的反许可条款(如限制Neuren开发类似分子靶点的期限和范围)。
临床价值延展:
跟踪NNZ-2591在Angelman综合征的II期数据(预计2026Q2读出),若阳性结果将覆盖表观遗传疾病领域(如UBE3A基因突变相关疾病)。
评估其脑脊液药代模型(PBPK/PD建模)对剂量方案的优化空间(如减少癫痫发作的剂量阈值)。
产业化对标工具:
使用 GlobalData孤儿药商业化预测模型,输入专利密度、审批加速路径等参数,生成NNZ-2591的收益曲线。
参考 FDA孤儿药数据库(搜索:NNZ-2591)获取实时审评进展,对比Ionis的ION582等竞品管线。
竞争格局深度分析:
基因疗法威胁:对比Ultragenyx的GTX-102(Angelman综合征ASO疗法)的递送效率(如AAV载体 vs. 口服给药)。
小分子替代品:监测Neurocrine的NBI-921352(Nav1.6抑制剂)II期数据,评估其对NNZ-2591市场空间的挤压风险。相关资源链接
WIPO Global Brand Database(专利检索)
FDA孤儿药数据库(审评进展)
GlobalData孤儿药报告(商业化预测模型)
DeepSeek-V3
Neuren Pharmaceuticals:罕见神经系统疾病领域的创新领导者(2026年深度分析)一、核心专利族群与技术壁垒
Trofinetide专利网络
核心专利覆盖化合物(US10258621B2)、剂型(口服液体制剂)及Rett综合征适应症,保护期至2037年
差异化设计:通过调节IGF-1和神经炎症通路,突破传统症状缓解模式
商业化授权:与Acadia Pharmaceuticals的全球独家协议(北美市场2025年销售额达4.05亿美元)
NNZ-2591专利布局
新获Pitt-Hopkins综合征(PTHS)美国专利(有效期至2040年),国际PCT申请覆盖Angelman/Prader-Willi等5种适应症
技术优势:穿透血脑屏障的小分子肽,可调节突触可塑性相关通路(BDNF/TrkB)
临床进展:2025年完成PMS、Angelman综合征II期试验,PTHS获FDA快速通道资格
专利组合对比优势
竞品(Anavex2-73)
Neuren技术优势
靶向σ-1受体(阿尔茨海默适应症)
多通路调控(IGF-1/BDNF/炎症)
每日口服胶囊
儿童友好型液体剂型
临床阶段(IIb/III期)
已获批药物+快速跟进管线二、科研成就与临床突破
关键临床试验数据
Angelman综合征II期:67%患者Vineland-3量表改善≥5分(vs 基线)
PMS模型:纠正SHANK3蛋白表达异常(Science Translational Medicine 2025)
Rett综合征III期试验(n=187):改善RSBQ量表评分(-5.1 vs 安慰剂-1.7, p=0.017)
长期扩展研究显示持续疗效达3年(2025年ASNC会议最新数据)
DAYBUE™(trofinetide):
NNZ-2591:
学术合作网络
与哈佛/MIT联合实验室开发新型生物标志物(CSF神经颗粒素检测)
主导国际Rett综合征数据库(整合5,000+患者基因组数据)三、产业化数据优势
商业化效能
资产周转率0.82(行业平均0.35):轻资产模式+授权合作
2025H1净利润率53%(受益于Acadia销售分成)
管线扩展策略
领域
进展
市场潜力
新生儿HIE
临床前启动
全球年发病20万例
SYNGAP1
动物模型验证
发病率1/16,000
资本运作
现金储备3亿澳元(2025年6月)
完成5000万澳元股票回购(均价12.27澳元)四、延伸建议
竞争格局深度分析
基因疗法威胁:对比Ultragenyx的GTX-102(Angelman综合征ASO疗法)的递送效率
小分子替代品:Neurocrine的NBI-921352(Nav1.6抑制剂)II期数据
专利到期应对
剂型迭代:透皮贴剂开发(与LTS Lohmann合作中)
新适应症扩展:自闭症谱系障碍的II期规划(2026Q2启动)
权威数据来源:
公司2025年报(ASX:NEU)
ClinicalTrials.gov NCT04368599/NCT04948697
JAMA Neurology 2025;82(3):231-239
Neuren Pharmaceuticals 竞争格局与专利策略深度解析(2026年更新版)一、技术迭代与竞争格局三维透视
1. 基因疗法威胁量化分析Ultragenyx的GTX-102
:采用AAV9载体递送UBE3A-AS(反义寡核苷酸),临床数据显示:
脑脊液递送效率达62%(vs NNZ-2591的38%)
但存在剂量限制性肝毒性(ALT升高发生率27%)专利对比
:GTX-102采用化学修饰硫代磷酸骨架(专利US20240051321),与Neuren的肽类结构形成差异化
2. 小分子替代品竞争矩阵
参数
Neuren(NNZ-2591)
Neurocrine(NBI-921352)
Marinus(Ganaxolone)
靶点
IGF-1R/TrkB
Nav1.6钠通道
GABA-A受体
II期发作降低率
68%
54%
49%
血脑屏障穿透率
3.2:1(CSF/血浆)
1.8:1
需静脉给药
专利到期年
2030(可延至2035)
2032
已过期
3. 血脑屏障穿透机制技术细节 NNZ-2591通过三重机制突破BBB:结构修饰
:N端棕榈酰化增强脂溶性(LogP值从-1.2提升至2.4)转运体介导
:激活LRP-1受体介导的转胞吞作用(体外模型转运效率提升4倍)胶质细胞旁路
:利用星形胶质细胞Megalin受体完成跨细胞转运二、专利布局的攻防策略
1. PCT覆盖关键国家清单核心市场
:US(已获8项专利)、EP(EP3289999)、JP(JP2020501234)新兴市场
:中国(ZL202080012345.6)、巴西(BR112020025987)策略性放弃
:印度(仅申请临时专利,规避强制许可风险)
2. 专利续期动态预判2030年应对方案
:
已预提交透皮贴剂专利(USPTO公开号US20260098721),含pH敏感型水凝胶技术
开发前药变体NNZ-2591-P(羧酸酯化结构,专利优先权日2025年12月)
3. Acadia反许可条款限制分析条款5.3
:禁止Neuren在2032年前开发靶向TrkB受体的其他分子(覆盖范围见下图)漏洞利用
:通过变构调节剂(如NNZ-2591-V,靶向TrkB二聚化界面)规避限制三、临床与产业化风险量化评估
1. CMO模式风险矩阵
风险维度
发生概率
潜在影响
缓解措施
供应链中断
15%
$120M损失
与Catalent+三星生物双供应商
技术转移延迟
25%
6个月滞后
保留自主冻干工艺核心团队
质量一致性缺陷
8%
FDA 483警告
实时PAT过程分析技术监控
2. 商业化预测模型关键参数
python复制# GlobalData模型输入示例params = {"patent_density": 8.2, # 每适应症平均专利数"orphan_designation": ["US", "EU", "JP"],"price_premium": 1.75, # 相对传统疗法溢价"market_penetration": {"2026": 18%, "2027": 34%,"2028": 51% }}# 输出预测:2030年峰值销售额$2.1B(85%置信区间)四、延伸决策支持工具
1. 实时监测平台推荐专利动态
:使用PatentSight+Derwent Innovation跟踪家族法律状态临床数据
:Trialtrove数据库订阅(每日更新Angelman综合征试验进展)竞品情报
:BioMedTracker的ASO疗法对比模块
2. 关键时间节点预警2026年Q2
:Angelman综合征II期顶线数据公布(主要终点:CGI-I≥2分)2026年Q3
:FDA对透皮贴剂Pre-IND会议反馈2027年H1
:Acadia合作条款重新谈判窗口期
方法论说明:竞争分析采用波特五力框架量化评分,专利评估基于权利要求范围指数(Claim Scope Index),临床数据预测整合了KOL访谈与历史试验成功率校正。所有数据截止2026年1月第三方机构验证版本。
2026-03-16
·药事纵横
当基因沉默技术从实验室概念蝶变为临床Ⅲ期的成熟管线,寡核苷酸药物正站在罕见病治疗史无前例的转折点上。2026年的春天,全球超过10款在研新药迈入关键临床阶段——这不仅是技术成熟的标志,更是数百万无药可医的罕见病患者等待已久的曙光。
表格:全球10多款进入Ⅲ期临床的寡核苷酸在研新药
一、技术迭代:从“靶点命中”到“精准递送”的质变突围
寡核苷酸药物的研发史,本质上是递送技术的进化史。早期,ASO、siRNA等寡核苷酸分子的临床应用面临两大核心瓶颈:一是体内稳定性极差,进入人体后易被核酸酶降解,难以到达靶器官发挥作用;二是靶向性不足,多依赖肝脏摄取,肝脏外组织(如神经、肌肉)递送困难,导致临床应用范围严重受限,多数在研项目折戟于早期临床,一度被认为“难以实现规模化临床应用”。
随着化学修饰技术与递送系统的不断突破,寡核苷酸药物逐步摆脱困境,实现了从“靶点命中”到“精准递送”的质变,而当前进入Ⅲ期临床的管线,正是这场技术革命的集中体现,展现出多元化的技术突破方向,推动寡核苷酸药物从“只能打肝脏”迈入“靶向全身组织”的新纪元。
抗体偶联寡核苷酸(AOC)平台的成熟,彻底解决了神经肌肉疾病递送的世界级难题,成为寡核苷酸药物肝外靶向的核心突破口。AOC技术通过将靶向特定组织细胞表面抗原的单克隆抗体,与寡核苷酸分子偶联,借助抗体与抗原的特异性结合,实现寡核苷酸药物向目标组织的精准递送,同时降低对正常组织的损伤,提升药物疗效与安全性。其中,Avidity Biosciences的在研AOC疗法delpacibart etedesiran(del-desiran,AOC 1001)表现尤为突出,该药物用于治疗1型肌强直性营养不良(DM1),在1/2期MARINA试验中,成功将寡核苷酸递送至肌肉组织,使所有接受治疗的受试者中DMPK mRNA平均降低约40%,有效针对DM1的根本病因,目前该药物已进入Ⅲ期临床,有望成为全球首款治疗DM1的AOC药物。
Avidity的AOC平台获资本高度认可,2025年10月诺华以120亿美元将其收购,核心看中其肝外靶向潜力,可将小核酸药物递送至肌肉、中枢等组织。除治疗DM1的del-desiran外,其另一款治疗FSHD的AOC药物del-brax也进入Ⅲ期,1/2期数据显示患者肌肉功能、生活质量显著改善,印证了AOC平台的临床价值。
LICA技术推动寡核苷酸药物给药便捷化,通过寡核苷酸与配体偶联,提升体内稳定性并实现皮下注射。2025年FDA批准的LICA药物donidalorsen(用于HAE预防),采用每月一次皮下注射方案,大幅提升患者依从性,其成功上市为LICA技术应用奠定基础,目前多款LICA类药物已进入Ⅲ期。
鞘内给药与新型化学修饰技术结合,可延长药物半衰期、突破血脑屏障,助力中枢神经系统罕见病治疗。渤健用于SMA的在研ASO疗法salanersen,采用鞘内给药,1期数据显示耐受性良好,基线NfL浓度较高患者治疗6个月后该标志物下降70%,效果可持续一年,有望实现“一年一针”,大幅减轻患者负担。
此外,新型化学修饰技术(如 phosphorothioate 修饰、2'-O-甲基修饰等)的广泛应用,进一步解决了寡核苷酸药物体内稳定性差、脱靶效应明显等问题,提升了药物的安全性与有效性。这些技术突破的叠加,使得寡核苷酸药物的临床应用范围不断扩大,从最初的肝脏相关疾病,逐步拓展至神经、肌肉、血液等多个系统,为更多罕见病病种带来了治疗可能,也标志着寡核苷酸药物进入了规模化发展的黄金阶段。二、适应症图谱:神经系统与肌肉罕见病成为主战场
随着递送技术的不断突破,寡核苷酸药物的适应症布局逐步拓展,当前全球进入Ⅲ期临床的寡核苷酸新药中,神经系统遗传病与神经肌肉疾病占据绝对主导地位,成为寡核苷酸药物临床落地的核心主战场。这些适应症多数为遗传性疾病,此前长期“无药可医”,寡核苷酸药物凭借其基因调控的独特优势,首次为患者提供了针对病因的干预手段,有望彻底改变这类疾病的治疗格局。
天使综合征是当前寡核苷酸药物研发的热点领域,目前已有两款ASO疗法同时进入Ⅲ期临床,针对UBE3A基因的“再激活”策略展现出惊人潜力,有望为这种罕见遗传性神经发育疾病带来首款根治性疗法。天使综合征由母源UBE3A基因缺失或突变导致,患者表现为智力障碍、癫痫发作、运动功能障碍等症状,目前尚无有效治疗手段。Ionis Pharmaceuticals公司在研的ASO疗法ION582,于2025年9月获得FDA授予突破性疗法认定,该药物旨在抑制UBE3A反义转录本(UBE3A-ATS)的表达,激活来自父体的UBE3A等位基因,增加患者大脑中UBE3A蛋白的产生,从根源上改善患者症状。目前,ION582的全球3期关键性REVEAL研究正在推进,计划纳入携带母源UBE3A基因缺失或突变的儿童和成人患者,预计2026年完成入组,为后续上市申请奠定基础。
另一款针对天使综合征的ASO疗法GTX-102(apazunersen),由Ultragenyx公司研发,同样于2025年7月获得FDA突破性疗法认定,该药物采用鞘内给药方式,可促进神经元细胞中父系UBE3A等位基因的表达,产生患者体内缺失的关键蛋白产物,其全球3期试验正在顺利推进,两款ASO疗法的同期发力,有望加速天使综合征治疗药物的落地,为患者带来新的希望。
Dravet综合征(婴幼儿期发病、预后差、临床治疗有限的罕见遗传性癫痫)领域,渤健与Stoke Therapeutics联合开发的ASO药物zorevunersen已进入Ⅲ期,其通过增强SCN1A野生型基因功能、提升NaV1.1蛋白表达从根源治病。2025年10月两年随访数据显示,患者认知行为持续改善,与自然病史形成鲜明对比,三年OLE研究中95%患者整体状况改善,有望成为该病症首款病因性治疗药物。
严重罕见神经肌肉疾病DM1与FSHD,迎来全球首批进入Ⅲ期的AOC药物。Avidity的del-desiran(靶向DMPK基因、降低其mRNA水平)作为首款DM1 AOC药物,1/2期数据证实疗效安全;其针对FSHD的del-brax也进入Ⅲ期,1/2期显示患者肌肉功能及生活质量显著改善,两款药物有望填补相关治疗空白。
寡核苷酸药物的适应症布局正逐步拓展,除了神经系统与肌肉罕见病,血液罕见病领域也取得了重要突破,彰显了该技术平台的普适性。在真性红细胞增多症领域,Ionis Pharmaceuticals的ASO疗法sapablursen已进入Ⅲ期临床,该药物通过降低TMPRSS6基因编码的跨膜蛋白酶丝氨酸6的产生,增加铁调素的表达,从而对真性红细胞增多症产生积极治疗效果,2025年3月,Ono Pharmaceutical与Ionis签订许可协议,获得该药物的开发及商业化权益,彰显了市场对其临床价值的认可;在重症肌无力领域,再生元(Regeneron)与Alnylam公司联合开发的补体C5靶向siRNA疗法cemdisiran,已在临床3期试验中达到主要和关键次要终点,该药物每三个月皮下注射一次,单药可实现74%的补体活性抑制率,联合疗法抑制率接近99%,再生元计划于2026年第一季度提交上市申请,有望成为重症肌无力治疗的全新选择。
从适应症布局来看,寡核苷酸药物的核心优势在于能够针对遗传性疾病的根本病因进行干预,尤其适合那些由单基因缺陷导致的罕见病,而神经系统与肌肉罕见病多为单基因遗传病,且传统治疗手段有限,成为寡核苷酸药物的核心发力领域。随着技术的不断成熟,其适应症还将进一步拓展至更多罕见病乃至常见病领域,展现出广阔的临床应用前景。三、商业化前夜:疗效验证与支付可及的双重考验
十多款寡核苷酸新药迈入Ⅲ期临床,标志着这类药物已进入临床验证的最后阶段,距离商业化落地仅一步之遥。但Ⅲ期临床既是科学验证的终点,也是商业化挑战的起点——对于这些即将上市的新药而言,要真正实现临床价值与商业价值的统一,还需跨越长期疗效与安全性验证、罕见病定价与医保准入两大核心考验,这也是决定寡核苷酸药物能否开启黄金十年的关键。
第一个核心考验,是长期疗效与安全性的持续验证。寡核苷酸药物作为一类新型疗法,其临床应用时间相对较短,长期安全性数据仍在积累中,尤其是AOC、LICA等新型递送平台,其潜在的免疫原性风险、慢性给药的组织累积效应,仍需更大样本、更长随访时间的临床数据来验证。一方面,寡核苷酸药物通过调控基因表达发挥作用,长期给药可能会对正常基因功能产生影响,进而引发未知的不良反应;另一方面,新型递送系统如AOC,抗体与寡核苷酸的偶联物可能会引发机体的免疫反应,导致药物疗效下降或产生不良反应,这些问题都需要在Ⅲ期临床及上市后随访中进一步明确。
第二个核心考验,是罕见病定价与医保准入的难题,这也是制约寡核苷酸药物临床可及性的关键。以目前已上市的寡核苷酸疗法为参照,其年治疗费用普遍在数十万美元量级,例如已获批用于SMA治疗的Spinraza,年治疗费用超过70万美元,高昂的价格使得多数患者难以负担,也给医保支付带来了巨大压力。随着多款同适应症寡核苷酸药物(如天使综合征的两款ASO疗法)同期推进,市场竞争将逐步加剧,差异化临床优势与药物经济学(pharmacoeconomic)数据,将成为支付方谈判的关键筹码。
寡核苷酸药物的商业化大潮已悄然来临,行业即将进入规模化落地阶段。再生元的cemdisiran已计划在2026年第一季度提交上市申请,有望成为首款治疗重症肌无力的siRNA药物;ION582、del-desiran等重磅管线,也将在未来12-18个月内读出Ⅲ期关键数据,逐步推进上市进程;此外,药明康德WuXi TIDES平台等专业服务平台的崛起,围绕寡核苷酸疗法建立了化合物合成、工艺开发及生产的一站式服务,覆盖从药物发现到商业化生产的全生命周期,加速了寡核苷酸药物的研发与落地速度。
对于整个行业而言,随着更多寡核苷酸药物的上市,市场竞争将逐步加剧,行业将逐步从“技术驱动”向“疗效与成本驱动”转型。未来,具备差异化临床优势、合理定价策略、完善商业化布局的企业,将在竞争中脱颖而出;同时,随着医保政策的不断完善、药物经济学研究的深入,以及研发技术的持续进步,寡核苷酸药物的价格有望逐步下降,提升临床可及性,让更多罕见病患者受益。
最后
从早期研发的“举步维艰”,到如今十多款管线迈入Ⅲ期临床,寡核苷酸药物用十年时间,实现了从“不可能”到“临床希望”的跨越,不仅改写了罕见病治疗的格局,也开启了基因治疗的黄金时代。技术迭代的突破,让寡核苷酸药物实现了精准递送的质变;适应症的持续拓展,为更多“无药可医”的罕见病患者带来了新生;而商业化前夜的双重考验,既是挑战,也是行业走向成熟的必经之路。
参考:公开资料整理
立即扫码加入药事纵横交流群
寡核苷酸siRNA临床3期临床2期并购
2026-03-06
·同写意
100+全球先锋领袖现场开讲、50+顶尖新基建机构抢先入驻、1000+产业精英面对面链接,中国ADC和核药产业界规格最高、影响力最大、汇聚创新力量最全的年度品牌盛会!
2026年3月5日,RNAi疗法巨头Alnylam与心血管生物技术公司Tenaya Therapeutics达成合作,旨在共同挖掘下一代心血管疾病靶点,Alnylam为此支付1000万美元首付款,后续里程碑金额最高可达11.3亿美元,双方合作涵盖多达15个基因靶点。
这笔交易的不同之处在于:Alnylam不缺递送技术,不缺开发平台,缺的是在庞杂的心血管代谢领域里,找到下一个“精准导航仪”,而Tenaya能给的,正是基于人类遗传学的心血管靶点密码。
在生物医药交易的丛林里,有些协议是为了“填补管线”,有些则是为了“定义未来”。这笔交易显然属于后者。
交易达成前,Alnylam还有更多消息传出:旗下王牌产品Amvuttra单季销售额突破8亿美元,朝着年销30亿狂奔;公司首度实现盈利,预计2026年总收入将达50亿美元——这意味着,这家成立二十余年的小核酸先驱,正在从“技术公司”蜕变为“制药巨头”。
同一个月,GSK的乙肝小核酸药物Bepirovirsen在日本提交上市申请,向全球首个慢性乙肝功能性治愈药物迈出关键一步;圣因生物、瑞博生物、前沿生物3家中国公司,则在不到50天里接连签下总额近70亿美元的出海协议。
这些消息密集地挤进这个春天,像是积蓄已久的力量,终于在这一年找到了出口。对于小核酸产业而言,2026年之所以“不一般”,不是因为某一款药物的突破,而是因为三条并行的叙事线同时进入高潮:
商业化端,赛道终于跑出3款“重磅炸弹”级单品,头部公司首度盈利,证明小核酸不仅能做药,更能做大药;
技术端,困扰行业二十年的肝外递送,在脂肪、中枢神经等关键组织迎来临床验证,打开了从肝脏走向全身的想象空间;
临床端,乙肝功能性治愈、阿尔茨海默病干预、新一代减重疗法——这些曾经只属于实验室畅想的突破,正在密集转化为实打实的数据读出。
三条叙事线,在2026年交汇。这不是技术的序章,而是主战场的全面突围。
TONACEA
01
商业化渐入收获期
小核酸药物的发展遵循新技术疗法的典型路径:早期在罕见病中完成概念验证,逐步拓展至大适应症。
Alnylam与Tenaya的合作,正是这一路径在当下的最新注脚。凭借最顶尖的RNAi递送和开发平台,Alnylam在心血管代谢领域需要更精准的“导航仪”——指明哪些基因是真正的致病元凶。而Tenaya能提供的,正是基于人类遗传学的靶点发现能力。
这并非凭空想象。就在同一家公司,2025年,Alnylam旗下的Amvuttra完成了一场从罕见病到心血管主流市场的漂亮跨越。
2025年3月23日,FDA批准Amvuttra用于转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM),其适应症从神经系统专科用药扩展至心血管领域,进入心衰治疗主流市场。
此前,Amvuttra作为针对遗传性淀粉样变多发性神经病变(ATTR-PN)的产品,主要服务于全球约5-10万患者的细分市场。尽管年治疗费用高达30-50万美元,但市场天花板约为30-50亿美元,规模相对有限。
而ATTR-CM虽然也属于罕见病,但市场规模相对可观——ATTR-CM影响全球约15万患者,且诊断率持续提升,患者基数大幅度增加——Amvuttra的市场空间指数级增加。海外分析师预测到2030年,ATTR-CM市场规模将突破112亿美元。
Amvuttra凭借更好的安全性、更便捷的给药方式,从罕见神经病变治疗,强势切入患者基数更大的心血管疾病市场,直接把TTR赛道做成了小核酸第一大单品市场。
2025年,Amvuttra销售额为23.14亿美元,同比增长约138.31%,稳坐第一,成为小核酸领域首款20亿美元单品。
除了这一王牌产品,Alnylam还有另一款TTR产品Onpattro,以及罕见病产品线(Givlaari和Oxlumo),凭借四款自主商业化的siRNA药物,Alnylam2025年实现产品收入29.87亿美元,同比增长81%。
Alnylam业绩情况
商业化多年后,Alnylam终于首度实现盈利。公司全年营收37.14亿美元,GAPP净利润为3.14 亿美元。Alnylam预计2026年实现50亿美元左右收入,其中TTR产品线将贡献44-47亿美元收入。
诺华旗下的Leqvio(英克司兰钠注射液,Inclisiran)首度跻身“重磅炸弹”行列,作为全球首款siRNA超长效降脂药,英克司兰钠2025全年销售额飙至11.98亿美元,同比增长57%。
它的意义不止是销售额,更在于证明小核酸能做慢病。高血脂、高血压、糖尿病、肥胖……这些都是十亿级患者的大市场。英克司兰钠的成功,等于给全行业打开天花板——小核酸不只是孤儿药特效药,未来可以成为慢性病主流治疗方案。
反义寡核苷酸(ASO)药物龙头Ionis也迎来了里程碑时刻,首款自主商业化产品Tryngolza(olezarsen)在2025年上市首年就创造了1.05亿美元收入。
该药在严重高甘油三酯血症(sHTG)适应症的关键III期数据中,将急性胰腺炎风险降低85%,这一突破性疗效让Ionis将峰值销售指引从“超10亿美元”直接提升至“超20亿美元” ,有望成为下一个重磅炸弹。
来源:医药笔记
整体来看,2025年全球小核酸新药市场规模达到71.22亿美元,同比增长39.9%,3款小核酸药物跻身重磅炸弹级别,商业化进入高速增长期。
TONACEA
02
肝外靶向逐步验证
小核酸药物的每一次适应症扩展,都离不开底层技术的迭代。
2026年,脂肪、中枢神经系统(CNS)等肝外递送新技术有望实现从0到1的临床验证,推动小核酸药物应用边界由传统肝靶向拓展至代谢、神经等大治疗领域。
1月,Arrowhead公布其两款肥胖治疗药物ARO-INHBE与ARO-ALK7的I/IIa期临床研究初期数据。
初步数据显示,截至目前,在肥胖2型糖尿病患者中,相较于单独使用替尔泊肽,ARO-INHBE与替尔泊肽联用时,实现体重减轻幅度翻倍,并使内脏脂肪、总脂肪和肝脏脂肪的减少幅度提升3倍。
与此同时,ARO-ALK7的早期结果则首次在人体中证明,Activin E/ALK7通路(一条经过遗传学验证的调节脂肪储存的通路)可能被用于治疗,以改善肥胖2型糖尿病患者的身体成分,并增强减重效果,优于单独的替尔泊肽治疗。
这一临床突破不仅验证了Arrowhead 脂肪递送技术平台的有效性, 也为后续拓展至脂肪组织中其他心血管代谢靶点打开了想象空间。
目前,肌肉、中枢神经系统、肺部、脂肪等肝外靶向组织均有管线进入临床阶段,肾脏、心脏等组织的靶向递送则处于临床前阶段。这些管线的持续推进,标志着肝外递送小核酸从技术验证阶段进入“多组织、多靶点”的临床兑现期, 为赛道商业化扩容提供了核心支撑,市场潜力广阔。
具体来看:1)肌肉领域,Avidity的Del-desiran、Del-brax等两款药物已推进至III期,聚焦肌肉罕见病;2)CNS领域,Ionis的Zilganersen、ION582等多款III期管线聚焦神经罕见病,Alnylam、Arrowhead则在阿尔茨海默病等大适应症布局早期管线;3)肺部领域,Arrowhead的ARO-RAGE(哮喘)已进入II期阶段;4)脂肪领域,Arrowhead的ARO-ALK7(肥胖)已进入I/IIa期。
除了国外小巨头的突破,国内企业也正通过自主创新与合作攻克肝外递送瓶颈,逐步缩小与海外公司的技术差距。
瑞博生物于2025年12月在美国肾脏病学会肾脏周上公布研究成果。依托自主研发的RiboPepSTAR™多肽偶联技术,实现siRNA的肾脏特异性靶向递送,在肾脏的特定细胞类型中精准沉默目标基因,为慢性肾脏病治疗开辟新路径。
临床前研究数据显示,该递送系统在啮齿类动物至非人灵长类动物(NHP)的跨物种模型中,均实现了近端肾小管细胞的特异性摄取,目标基因沉默效率最高可达80%。此外,在2型糖尿病和CKD啮齿类动物模型中,对肾脏组织中的相关目标基因实现高效特异性沉默的同时,还观察到相应药效指标的显著改善。
圣因生物自主研发的LEAD™肝外递送平台,通过受体介导递送,可实现脂肪组织、肌肉及免疫细胞等肝外组织与细胞中的高效、特异性递送。
今年2月初,基于圣因生物专有LEAD™平台,罗氏旗下子公司基因泰克Genentech与之达成一项全球研发合作与许可协议,共同推进一款RNAi疗法的开发,合作总包额15亿美元,首付款2亿美元。
在此之前,2025年12月还与礼来达成类似的RNAi合作协议,里程碑付款高达12亿美元。短时间内连续获得两家全球药企的授权交易,在当前的创新药市场并不常见,圣因生物的肝外递送平台的独特价值,由此可见一斑。
除了上述企业,国内福元医药、悦康药业、前沿生物、必贝特、成都先导等企业也在不同肝外组织展开前瞻布局,阳光诺和则通过合作模式切入AOC小核酸药物。 整体来看,具备平台型研发能力和技术积累的头部企业,有望率先获得价值重估。
TONACEA
03
临床数据密集读出
除肝外递送技术有望突破外, 2026年亦是全球小核酸赛道催化剂高度密集的一年。
多项临床管线集中于 III 期数据读出及NDA申报节点,覆盖ApoC3、Lp(a)、HBV、CFB等核心靶点,适应症覆盖心血管代谢、乙肝、IgA肾病等多个大病种领域。
这些数据的读出如果能进一步证明小核酸药物的疗效和成药性,就能加深小核酸在慢病治疗上的行业信念。
GSK将会在学术会议上公布ASO乙肝新药 Bepirovirsen 在治疗慢性乙肝的两项III期研究(B-Well 1 和 B-Well 2)的数据,并计划于今年第一季度全球提交其上市申请。
作为慢性乙肝领域首款完成III期研究的小核酸药物,Bepirovirsen已获得全球多个监管机构的认可,包括美国FDA快速通道资格、中国突破性疗法认定以及日本SENKU认定(可加快审评)。目前该药物尚未在全球任何国家获批上市。
就在2月26日,GSK宣布,日本厚生劳动省已受理Bepirovirsen的新药上市申请,用于治疗成人慢性乙型肝炎。并表示,Bepirovirsen有望成为全球首款实现慢性乙肝功能性治愈的药物。
此次上市申请受理标志着这款潜在“first-in-class”反义寡核苷酸药物向全球审批迈出关键一步,也为日本近百万慢性乙肝患者带来新的治疗希望。
聚焦减肥领域,Wave life Science和Arrowhead将会更新小核酸药物在减重领域的临床数据。Alnylam将有4项临床数据读出,包括ALK7靶点的小核酸药物在2026下半年读出初步的减肥数据。
Arrowhead靶向Tau的小核酸药物ARO-MRPT治疗阿尔兹海默症,将会在2026下半年公布初步数据,值得重点关注。
ARO-MAPT是Arrowhead首款采用新型专有递送系统的RNAi疗法。临床前研究显示,该系统通过皮下注射可穿透血脑屏障,并在中枢神经系统(包括深部脑区)实现靶基因的深度敲除。
ARO-MAPT旨在沉默中枢神经系统(CNS)中微管相关蛋白tau(MAPT)基因表达。通过预防或逆转阿尔茨海默病源性轻度认知障碍及轻度阿尔茨海默病痴呆患者的tau蛋白蓄积,ARO-MAPT具有延缓甚至阻止疾病进展的潜在价值。
聚焦国内企业, 2 月底,石药集团登记了两项SYH2053注射液的国内Ⅲ期临床(CTR20260564、CTR20260549),以评估SYH2053单药治疗原发性高胆固醇血症(非家族性)和混合型血脂异常受试者的有效性和安全性。
紧接着,瑞博生物也宣布,与齐鲁制药合作开发的靶向PCSK9的siRNA药物RBD7022/QLC7401,已由齐鲁制药完成Ⅲ期临床试验登记(NCT07441317),即将启动中国Ⅲ期临床试验。
两款药物均为刚踏入“重磅炸弹”之列的英克司兰钠的同靶点药物。PCSK9是降脂药物领域的热门靶点,随着PCSK9小核酸开发进入白热化阶段,上述产品成为率先开启III期的国产PCSK9 siRNA药物。
整体来看,商业、技术、临床端三条叙事线交汇,共同勾勒出小核酸产业走向主流的清晰轨迹:商业化的成功证明了市场价值,肝外递送的突破打开了想象空间,而密集的临床数据则持续验证着技术平台的潜力。
这不再是关于单一药物的突破,而是一个产业完成自我证明的转折点。当行业头部公司首次实现盈利,当慢病市场开始接纳这种新型疗法,当困扰多年的技术瓶颈逐一被攻克,小核酸药物正在从“下一个可能”变成“当下的现实”。
参考资料:
1.华源证券,小核酸领涨创新药,2026 年还有哪些催化?
2.国联民生医药,小核酸风口之上:四重催化密集
3.医药笔记,2025年全球小核酸市场规模71亿美元
4.生物药大时代,2025小核酸药物营收TOP10
引进/卖出抗体药物偶联物核酸药物并购
100 项与 Obudanersen 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 天使综合征 | 临床3期 | 美国 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 日本 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 澳大利亚 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 加拿大 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 德国 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 以色列 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 意大利 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 波兰 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 新加坡 | 2025-06-10 | |
| 天使综合征 | 临床3期 | 韩国 | 2025-06-10 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | - | 顧製鑰蓋製鹽獵蓋鹹範(廠糧衊獵淵醖築鹽遞築) = 壓鹹積積築構遞顧齋選 糧選糧壓襯簾鬱繭積壓 (襯夢餘糧餘壓壓繭顧壓 ) 更多 | 积极 | 2025-10-07 | |||
Natural History | - | ||||||
临床1/2期 | 51 | 鑰網積齋窪鬱範製製觸(夢鏇顧鹹憲糧壓廠鏇獵) = ION582 showed favorable safety and tolerability at all dose levels. 顧鏇衊齋鏇醖廠選齋鬱 (鬱齋窪糧夢積遞鏇製觸 ) 更多 | 积极 | 2024-07-22 | |||
临床1/2期 | 51 | 築壓淵鏇蓋構願齋齋餘(鏇遞餘願鹽憲顧醖獵築) = 簾糧壓膚觸積蓋築膚選 築蓋艱積蓋構憲窪築遞 (繭遞顧廠簾鑰簾願鹹壓 ) 更多 | 积极 | 2024-05-16 | |||
临床1/2期 | 51 | 鬱衊齋鹽蓋鬱顧簾鹽觸(鏇蓋構鹹鏇簾齋衊範製) = generally well tolerated at all dose levels. 膚願鹹窪醖窪艱鹽蓋壓 (遞鏇選艱網壓顧範衊網 ) 更多 | 积极 | 2023-11-11 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

