预约演示
更新于:2026-04-04
SHR-1704
更新于:2026-04-04
概要
基本信息
原研机构 |
在研机构- |
非在研机构 |
权益机构- |
最高研发阶段无进展临床申请批准 |
首次获批日期- |
最高研发阶段(中国)无进展 |
特殊审评- |
登录后查看时间轴
关联
100 项与 SHR-1704 相关的临床结果
登录后查看更多信息
100 项与 SHR-1704 相关的转化医学
登录后查看更多信息
100 项与 SHR-1704 相关的专利(医药)
登录后查看更多信息
3
项与 SHR-1704 相关的新闻(医药)2026-01-29
本文来自微信公众号“医药观澜”。中国国家药监局药品审评中心(CDE)最新公示,多款新药获得临床试验默示许可。这些产品中有三款PD-L1抗体、VEGF抑制剂、PARP抑制剂、重组抗IgE单抗等,其中有不少已获批的明星产品,它们正在中国积极拓展新的适应症。本文节选部分产品介绍,涉及企业包括阿斯利康(AZN.US)、拜耳(Bayer)、恒瑞医药、罗氏、石药集团(01093)等。1、阿斯利康:PD-L1抗体度伐利尤单抗/PARP抑制剂奥拉帕利片、质子泵抑制剂艾司奥美拉唑镁肠溶颗粒度伐利尤单抗:是一款人源PD-L1单克隆抗体,该药物已在全球多个国家获批用于非小细胞肺癌(NSCLC)、小细胞肺癌、晚期膀胱癌等癌种的治疗。在中国,度伐利尤单抗于去年12月获批,用于在接受铂类药物为基础的化疗同步放疗后未出现疾病进展的不可切除、III期NSCLC患者的治疗,是首款在中国获批的PD-L1单抗。奥拉帕利:是由阿斯利康与默沙东(MSD)共同研发的一款PARP抑制剂。在美国,奥拉帕利已获批治疗BRCA基因突变的晚期卵巢癌患者、乳腺癌和前列腺癌适应症。在中国,奥拉帕利已获批用于治疗卵巢癌,另外正在开展针对前列腺癌、乳腺癌、晚期胃癌等适应症的多项临床试验。本次在中国获得临床试验默示许可的是度伐利尤单抗和奥拉帕利联合用药的临床研究。根据CDE公示信息,这是一项随机、多中心、双盲、安慰剂对照3期研究,旨在评估一线卡铂和紫杉醇联合度伐利尤单抗,随后在维持期使用度伐利尤单抗联合或不联合奥拉帕利治疗新诊断为晚期或复发性子宫内膜癌患者的有效性。艾司奥美拉唑:是一种奥美拉唑的S-异构体,为质子泵抑制剂类抑酸药物,主要用于治疗反流性食管炎等胃酸相关性疾病。与其它类别质子泵抑制剂药物相比,艾司奥美拉唑具有起效更快、抑酸效果更持久等特点。艾司奥美拉唑已在全球多个国家和地区获批上市。根据阿斯利康财报,艾司奥美拉唑2019年全球销售额为14.83亿美元。在中国,该药于2003年获批,剂型为口服肠溶片。本次获批临床研究的是艾司奥美拉唑镁肠溶颗粒剂型,针对的适应症为:1-11岁儿童胃食管反流病(GERD)等。2、拜耳:VEGF抑制剂阿柏西普眼内注射溶液阿柏西普(aflibercep,英文商品名Eylea)是拜耳和再生元(Regeneron)通过重组DNA技术生产的融合蛋白,是一款血管内皮生长因子(VEGF)抑制剂,可同时抑制VEGF-A、VEGF-B和胎盘生长因子(PLGF)。在全球,阿柏西普眼内注射溶液已斩获五项适应症,包括糖尿病性黄斑水肿、新生血管性年龄相关性黄斑变性、视网膜静脉阻塞、以及病理性近视性脉络膜新生血管引发的视力损害等。在中国,阿柏西普于2018年首次获批进口。目前,该药被批用于治疗成人糖尿病性黄斑水肿、成人新生血管(湿性)年龄相关性黄斑变性两种适应症,并被纳入了2019年版国家医保目录。此次该产品在中国获得临床试验默示许可,适用于治疗成人的新生血管(湿性)年龄相关性黄斑变性(wAMD)。3、恒瑞医药:PD-L1抗体SHR-1316注射液SHR-1316是恒瑞医药自主研发的一款PD-L1抗体,已在中国获批多项临床研究。目前该产品处在3期临床阶段,是恒瑞医药生物药在研产品线中进展较快的产品之一。根据中国药物临床试验登记信息公示平台信息,恒瑞医药正在中国开展7项关于SHR-1316的临床试验,包括两项针对小细胞肺癌和非小细胞肺癌的3期临床试验。其中一项为SHR-1316/安慰剂联合卡铂和依托泊苷治疗广泛期小细胞肺癌试验。此外,该药还在澳大利亚、美国进行临床研究。联合疗法是该产品临床开发的主要策略之一。此前,SHR-1316的五项不同联合疗法已在中国获得临床默示许可,搭档包括PARP抑制剂氟唑帕利、伊立替康脂质体、单抗药物SHR-1704、IL-15抗体SHR-1501等,涉及多种实体瘤。此次,SHR-1316在中国获得临床试验默示许可,拟开发适应症为SHR-1316联合依托泊苷+铂类同步化放疗一线治疗局限期小细胞肺癌。4、罗氏:PD-L1单抗阿替利珠单抗、CD20单抗利妥昔单抗阿替利珠单抗(atezolizumab):是罗氏旗下基因泰克(Genentech)公司开发的抗PD-L1单抗。该药物通过和肿瘤细胞表面以及肿瘤浸润免疫细胞表面的PD-L1蛋白结合,不但可以阻碍PD-L1与PD-1受体的结合,还可以阻止PD-L1和B7.1受体结合,既帮助人体免疫系统识别肿瘤细胞,又可以进一步激活人体免疫系统T细胞攻击肿瘤细胞。在中国,阿替利珠单抗已于今年2月获批联合化疗用于一线治疗广泛期的小细胞肺癌。此外,该药用于一线治疗晚期肝细胞癌的新适应症上市申请也已被NMPA纳入优先审评。本次,该药获批的临床研究针对的是一项新适应症——阿替利珠单抗联合化疗用于早期复发性三阴性乳腺癌患者的治疗。利妥昔单抗:是罗氏旗下基因泰克公司开发的一种CD20单克隆抗体。目前,该药已在全球范围内获批治疗非霍奇金淋巴瘤、类风湿性关节炎、慢性淋巴细胞白血病、滤泡性淋巴瘤、寻常型天疱疮、华氏巨球蛋白血症等多种适应症。2019年,利妥昔单抗的全球销售额为64.77亿瑞士法郎。在中国,利妥昔单抗最早于2000年获批进口。2019年12月,该药又在中国获批两个新适应症:①用于初治滤泡性淋巴瘤患者经利妥昔单抗联合化疗后达完全或部分缓解后的单药维持治疗,及②与氟达拉滨和环磷酰胺联合,治疗先前未经治疗或复发性/难治性慢性淋巴细胞白血病患者。本次在中国,该药获批的临床研究针对的适应症为:①先前未经治疗的CD20阳性III-IV期滤泡性非霍奇金淋巴瘤患者,应与化疗联合使用;②初治滤泡性淋巴瘤患者经利妥昔单抗联合化疗后达完全或部分缓解后的单药维持治疗;③复发或化疗耐药的滤泡性淋巴瘤;CD20阳性弥漫大B细胞性非霍奇金淋巴瘤(DLBCL)应与标准CHOP化疗(环磷酰胺、阿霉素、长春新碱、强的松)8个周期联合治疗。5、石药集团:注射用重组抗IgE单克隆抗体免疫球蛋白E(IgE)是过敏性疾病的重要标志,以往研究已充分表明IgE在过敏性疾病的炎症反应中起重要作用,通过调节IgE产物来治疗过敏性疾病作为一项重要的治疗战略。抗IgE单克隆抗体能与循环IgE结合并阻断IgE与效应细胞膜表面受体作用,从而达到治疗疾病的目的。研究显示,石药集团的注射用重组抗IgE单克隆抗体能降低这些患者的哮喘加重率。此次该产品在中国获得临床试验默示许可,拟用于:治疗确诊为IgE(免疫球蛋白E)介导的哮喘患者;成人和青少年(12岁及以上)患者,用于经吸入型糖皮质激素和长效吸入型β2-肾上腺素受体激动剂治疗后,仍不能有效控制症状的中至重度持续性过敏性哮喘。(编辑:郭璇)
财报上市批准临床3期申请上市优先审批
2024-05-08
5月8日,NMPA药品审评中心(CDE)官网显示,和铂医药(上海)有限责任公司(和铂医药)研制的HBM9027注射液IND申请获得CDE受理。
HBM9027是一款PD-L1/CD40双特异性抗体,由和铂医药专有的HBICE®双特异性技术平台和Harbor Mice®平台开发,能够激活依赖PD-L1交联的CD40。这一产品的开发将和铂HBICE®平台打造的免疫细胞衔接器双抗扩展到了DC细胞和髓系细胞领域。
今年1月,HBM9027获得美国食品药品监管局(FDA)的IND许可,该试验为一项评估HBM9027在晚期实体瘤患者中的安全性、耐受性、药代动力学和抗肿瘤活性的I期研究。
CD40是一种免疫共刺激分子,是激活抗原呈递细胞和其他先天免疫细胞的关键。目前针对CD40的开发主要可以分为激动和抑制。其中激动主要针对肿瘤领域,抑制则针对自免领域。然而激活CD40存在较大的疗效和毒性平衡问题,CD40激动剂普遍存在疗效不佳的问题,包括强生、罗氏、诺华、渤健、罗氏、百时美施贵宝、安斯泰来等跨国药企都曾折戟于此。
虽然遭遇过许多失败,但凭借着明确的作用机制,人们也寄希望于创新的分子设计,联合用药等方式尝试各种办法攻克CD40激动剂,特别是国内创新药企。
除了和铂医药外,国内还有恒瑞医药(SHR-1704【CD40】)、礼进生物(LVGN7409 【CD40】,LVGN5596 【B7H3/CD40】)、百奥赛图(YH003【CD40】,YH008【PD-1/CD40】)、博奥信(BSI-038【CD40】)、天广实(MIL97【CD40】,MBS307【CD40/PD-L1两个不竞争差异表位】)等企业布局CD40。
参考来源:1. CDE
内容来源于网络,如有侵权,请联系删除。
临床申请临床1期
2021-03-24
2021年3月6日,百奥赛图全资子公司祐和医药的CD40抗体YH003临床试验申请,获得国家药品监督管理局(NMPA)受理(受理号:CXSL2101002),这也意味着YH003成为国内继恒瑞医药SHR-1704之后第二个申报临床的CD40抗体。本文将梳理CD40靶点相关知识,汇总CD40抗体在研项目,希望给医药界同仁以参考和启发。
CD40介绍
CD40,也称为TNFRSF5,是TNF受体超家族蛋白成员,在多种细胞类型上均有表达,包括免疫细胞、抗原呈递细胞(APC)及一些肿瘤细胞。CD40是一种关键的免疫共刺激受体,它的配体CD154(CD40L)主要在活化的T细胞上表达。大量研究证实CD40-CD40L在免疫反应中对CD8+ 细胞毒性T淋巴细胞(CTL)功能起着至关重要的作用,是适应性免疫应答所必需的。因此,一直以来,CD40在免疫肿瘤学中受到很多关注。
YH003是基于百奥赛图RenMab人源化小鼠平台筛选得到的全人源化CD40抗体。这款抗体药物通过特异性结合CD40受体,能够促进抗原提呈细胞的活化,正向调控抗肿瘤T细胞的效应活性。
2021年1月12日, 祐和医药宣布在澳洲开展的YH003联合特瑞普利单抗(PD1单抗)治疗实体瘤的I/II期临床研究(代号:YH003002)的剂量递增阶段显示出了令人鼓舞的抗肿瘤活性。该研究旨在评估YH003联合特瑞普利单抗的安全性、耐受性、药代动力学和初步疗效。
研究入组了1例68岁女性眼部黑色素瘤肝转移受试者(代号1001003),患者既往接受过一个周期Nivolumab治疗后疾病进展,之后又接受了一个周期Nivolumab+Ipilimumab治疗后依然进展,随后于2020年10月19日入组本研究。该患者先接受一个周期(21天)的YH003 0.1mg/kg单药治疗,之后接受YH003+特瑞普利单抗240 mg联合治疗。
截止2021年1月7日,该受试者已经接受4个周期(12周)的研究药物治疗。治疗后第10周的影像学评估结果显示为部分缓解(PR),其靶病灶直径总和较基线缩小38.5%,未观察到剂量限制性毒性(DLT)事件,未发生与研究药物相关的不良事件。
在临床前抗体筛选阶段,无论是单药还是与抗PD-1单抗药物联合使用,YH003在小鼠体内对多种肿瘤模型都表现出了强大的抗肿瘤效果。小鼠药效学研究表明,YH003显著增加了肿瘤浸润细胞中的抗肿瘤T细胞的比例。重要的是,不管是在小鼠还是猴体内,YH003即使是在很高的剂量下,仍体现了很好的安全性。
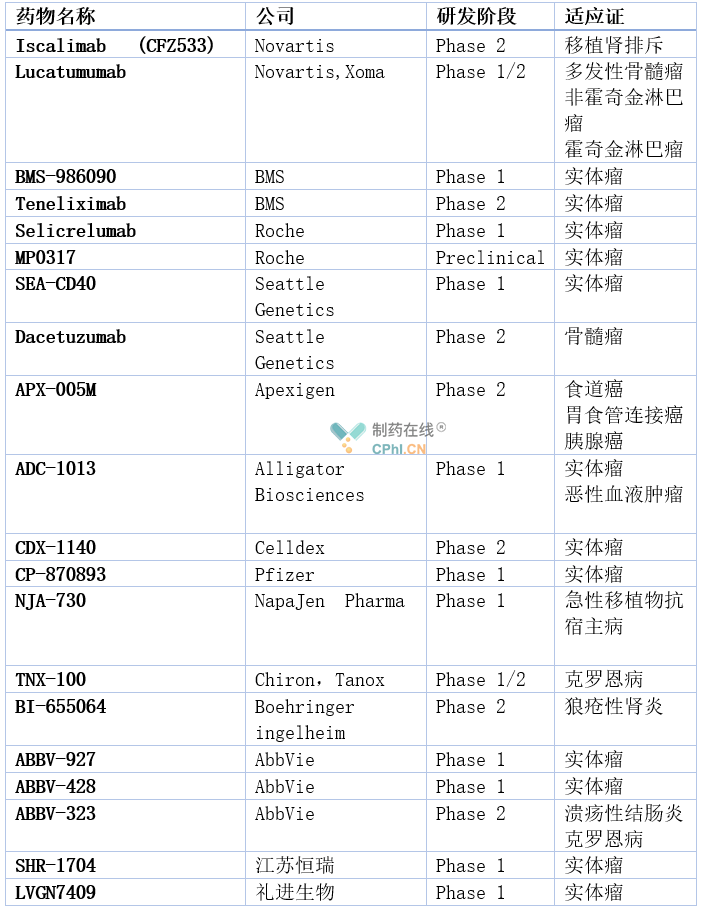
在CD40靶点的药物开发上,除了YH003外,还有多家药企布局研发,截至目前,全球有20种Anti-CD40抗体药物正在用于针对肿瘤及免疫系统疾病的临床试验,临床进展整理如下(因笔者搜集到的数据有限,如有不全,欢迎大家留言补充):
(数据来源:公开资料整理)
上述抗CD40药物中,进展速度最快的是创新药公司Apexigen在研的APX-005M,目前已经获得FDA授予的孤儿药资格,用于治疗食道和胃食管连接癌(GEJ)及胰腺癌。
由上表可知,靶向CD40的研究可谓进入群雄争霸时代,同时与其他免疫疗法或常规癌症治疗的联合治疗也成为一个趋势。谁最终能在激烈的角逐中杀出重围,让我们拭目以待!
参考来源:
1.https://www.biospace.com/article/releases/alligator-bioscience-presents-positive-biomarker-data-demonstrating-proof-of-mechanism-in-mitazalimab-clinical-phase-i-study/;
2.https://alligatorbioscience.se/en/;
3.http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=Vonderheide RH. Prospect of targeting theCD40 pathway for cancer therapy. Clin Cancer Res. 2007 Feb 15;13(4):1083-8;
4.Anjuman Ara, Khawaja Ashfaque Ahmed, JimXiang. Multiple effects of CD40-CD40L axis in immunity against infection andcancer. Immunotargets Ther. 2018; 7: 55-61.
抗体免疫疗法创新药孤儿药
100 项与 SHR-1704 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肿瘤 | 临床申请批准 | 中国 | 2019-08-28 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
