预约演示
更新于:2026-03-19
ARO-DIMER-PA
更新于:2026-03-19
概要
基本信息
药物类型 siRNA |
别名- |
作用方式 抑制剂 |
作用机制 APOC3抑制剂(载脂蛋白C-Ⅲ抑制剂)、PCSK9抑制剂(前蛋白转化酶枯草杆菌蛋白酶Kexin-9抑制剂) |
治疗领域 |
在研适应症 |
非在研适应症- |
非在研机构- |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
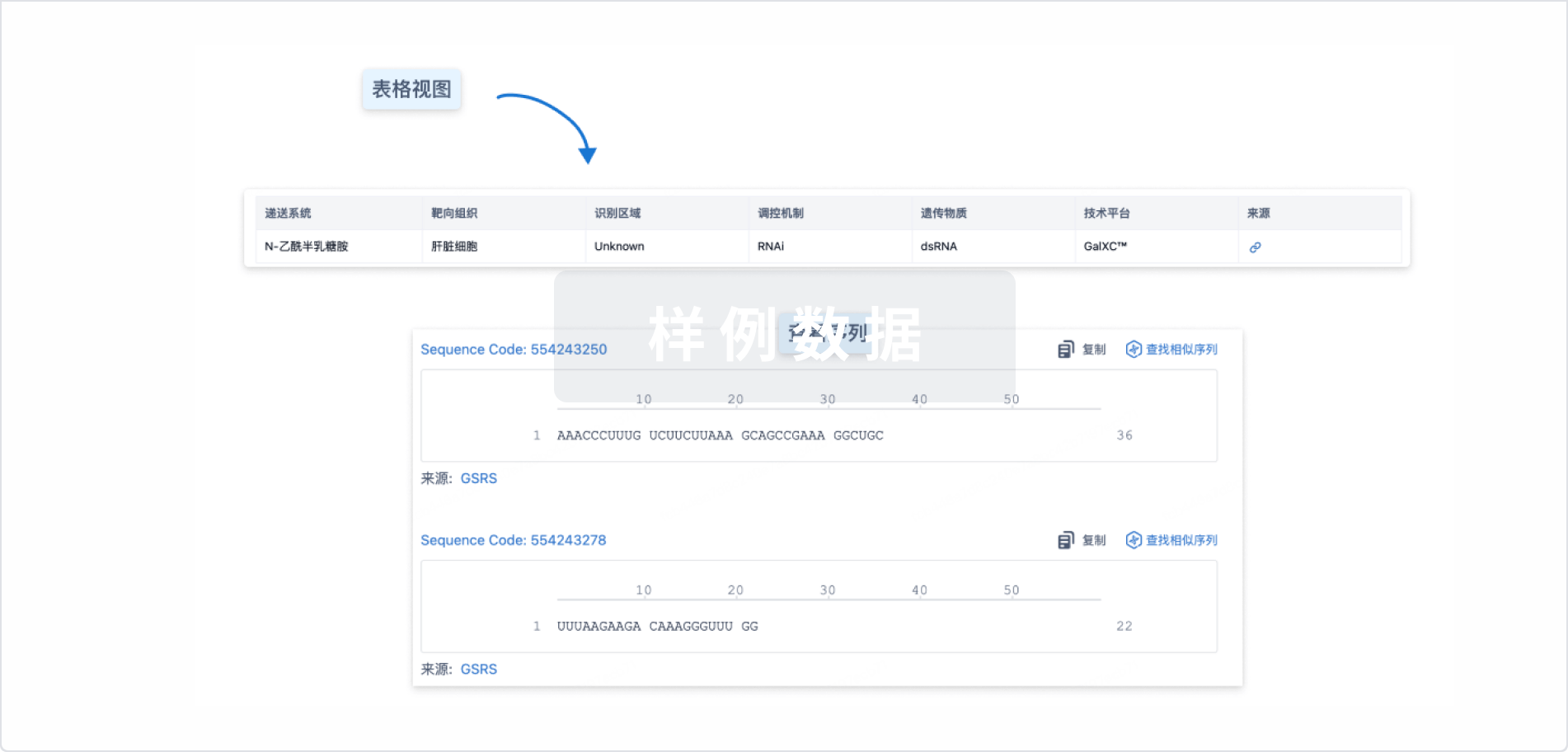
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
1
项与 ARO-DIMER-PA 相关的临床试验NCT07223658
Phase 1/2a, Double-blind, Placebo-controlled, Single and Multiple Dose-escalating Study to Evaluate the Safety, Tolerability, Pharmacokinetics, and Pharmacodynamic Effects of ARO-DIMERPA in Adult Subjects With Mixed Hyperlipidemia
Study to evaluate the safety, tolerability, pharmacokinetics (PK), and pharmacodynamics (PD), and effects on low-density lipoprotein cholesterol (LDL-C) and triglycerides (TGs) of single-dose ARO-DIMERPA and multiple doses of ARO-DIMERPA in adult participants with mixed hyperlipidemia.
开始日期2025-12-22 |
100 项与 ARO-DIMER-PA 相关的临床结果
登录后查看更多信息
100 项与 ARO-DIMER-PA 相关的转化医学
登录后查看更多信息
100 项与 ARO-DIMER-PA 相关的专利(医药)
登录后查看更多信息
19
项与 ARO-DIMER-PA 相关的新闻(医药)2026-03-11
双靶点siRNA药物是小核酸药物领域的新兴方向,目前处于快速发展阶段。双靶点siRNA药物是RNA干扰(RNAi)疗法领域的一项前沿创新。它通过精心设计的单一分子,旨在同时沉默与疾病相关的两个不同基因,为治疗复杂疾病提供了“一石二鸟”的新策略。 根据目前的研发进展,这类药物主要通过两种核心技术路径实现:一是设计可容纳两个不同siRNA序列的单分子支架;二是利用纳米载体(如多肽纳米颗粒、聚合物胶束)共递送两种靶向不同基因的siRNA。
发展现状:
1.研发活跃度高
全球范围内多家企业积极布局双靶点siRNA药物研发,涵盖海外巨头(如Alnylam、Arrowhead)和国内创新企业(如圣诺医药、迈威生物、时安生物等)。截至2026年2月,全球有多款双靶点siRNA药物进入临床阶段,适应症聚焦于心血管疾病、乙肝、肿瘤等领域。双靶点siRNA药物代表了RNAi疗法从单基因到多基因调控的范式跃迁。目前,该领域在心血管代谢疾病上进展最快,已有候选药物率先进入临床阶段。在肿瘤和中枢神经系统疾病等复杂疾病领域,多样化的创新设计也在临床前研究中展现出巨大潜力。表1汇总了目前公开披露的代表性在研双靶点siRNA项目,涵盖了其技术路径、靶点、适应症和开发阶段。
表1:目前公开披露的代表性在研双靶点siRNA项目
推荐阅读:小核酸药物三大“破局”趋势
2.技术优势明显
双靶点siRNA通过同时靶向两个致病基因,可实现协同增效,突破单靶点治疗的局限性。例如,在乙肝治疗中,同时靶向HBV病毒基因和免疫调节基因,既能抑制病毒复制,又能增强免疫清除能力;在肿瘤治疗中,针对癌细胞的多个关键通路,可更有效地抑制肿瘤生长。
长期大量供应小核酸固相合成树):聚苯乙烯(PS)氨基核酸固相合成载体,羟基固相合成载体,Unylinker 羟基载体,预载DNA碱基及RNA碱基羟基载体,GalNAC-NH固相合成载体等,同时供应各种核酸药物纯化填料,纯化工艺开发。联系:15771973009(微信同)。
1). 治疗效力的深度与广度:“1+1 > 2”的协同效应 双靶点设计最核心的优势在于能够同时作用于疾病网络中的两个关键节点,产生协同增效,这是单靶点药物难以企及的。
显著提升抗肿瘤活性:同时抑制两个致癌驱动基因,效果远优于单个抑制。例如,北卡罗来纳大学开发的靶向KRAS和MYC的双靶点分子,在实验室研究中使癌细胞活力抑制效果提升了高达40倍。在胰腺癌研究中,同时递送靶向KRAS和TP53的siRNA,体外效果提升了20倍,体内效果提升了3.5倍。
更全面的疾病干预:在心血管领域,同时抑制PCSK9(降低坏胆固醇LDL-C)和LPA(降低脂蛋白a),或PCSK9与APOC3(降低甘油三酯),可以实现对血脂谱的“综合治理”,解决单一疗法无法覆盖的残余风险。在肝癌治疗中,通过抑制GP73(与转移、免疫逃逸相关)和hTERT(与增殖、永生化相关),能同时阻断肿瘤的转移和增殖能力。
2). 递送效率与药代动力学的统一 对于联合疗法(即同时使用两种独立的siRNA药物),一个核心难题是两个药物在体内的分布、代谢和清除过程很难完全一致。双靶点siRNA作为一个单一分子,完美地解决了这一问题。
确保一致的药代动力学行为:采用一个分子结构,保证了针对两个靶点的siRNA具有完全相同的组织分布、细胞摄取和体内清除速率,避免了联合用药中因PK/PD(药代动力学/药效动力学)差异导致的疗效不稳定。
单一递送系统,降低复杂度:只需一个经过优化的递送系统(如GalNAc偶联物、脂质纳米颗粒等),即可将两个siRNA同时递送至目标细胞,提高了递送效率。例如,通过GalNAc修饰的胶束系统共递送COP1 siRNA和乐伐替尼(一种小分子药物),实现了在原位肝癌模型中对肿瘤的73%抑制率,远超单用乐伐替尼的31%。
优化载体设计,突破递送瓶颈:针对特定的递送挑战,可以进行精巧设计。例如,圣诺医药的PDoV™-GalNAc平台,通过在载体中融合具有内涵体逃逸功能的多肽,不仅提供了两个siRNA的结合位点,还解决了核酸药物入胞后“出不来”的难题,相比单独使用GalNAc平台,能更快地实现靶基因敲低(一周内达到最大敲低,而单用需三周)。
3). 协同作用机制:多维度打击疾病 双靶点策略能够通过多种机制产生协同效果,这是其疗效显著的基础。
功能通路互补:如上文所述,在肿瘤治疗中,可以同时抑制增殖(如MYC、hTERT)和转移/血管生成(如KRAS、GP73、VEGFR2)这两条不同的致癌通路,多维度抑制肿瘤发展。
克服耐药性:肿瘤细胞常常通过激活旁路信号来逃避单一药物的攻击。双靶点策略同时封锁主通路和旁路,能有效延缓或防止耐药性的产生。例如,在肝癌治疗中,通过siRNA沉默COP1(一种E3泛素连接酶),可使肝癌细胞对化疗药物乐伐替尼增敏,克服其耐药性。
改善肿瘤微环境:圣诺医药的STP355同时靶向免疫抑制因子TGFβ1和促血管生成因子VEGFR2。在黑色素瘤模型中,该疗法不仅直接抑制肿瘤生长,还使肿瘤内的T细胞和NK细胞浸润增加了近4倍,将“冷肿瘤”转化为“热肿瘤”,为联合免疫检查点抑制剂(如PD-1/PD-L1抗体)铺平了道路。
4). 开发与生产的便利性 从药物开发的全周期来看,双靶点分子也带来了显著的效率和成本优势。
简化开发流程:将一个双靶点分子推进临床,在监管沟通、CMC(化学、制造和控制)等方面,通常比同时开发两个独立的单靶点药物并将其组合要简单得多。
灵活的模块化设计:研究者已经开发出多种灵活的平台技术,使得构建双靶点siRNA变得像“搭积木”一样方便。例如,利用点击化学连接两个不同的siRNA模块,或者通过一个线性的分子内连接子将两个siRNA序列合二为一。大睿生物的"即插即用"平台也是这一优势的体现。
多样化的生物合成途径:除了化学合成,还可以利用大肠杆菌等生物系统来生产具有分支结构的双靶点多siRNA(如GT-multi-siRNA),为大规模生产提供了新的可能。
5). 改善药物安全性 降低脱靶毒性风险:在相同疗效的前提下,双靶点药物可以使用比两种单药联合更低的剂量,从而可能降低由高剂量带来的非靶点相关毒性。
靶向特定细胞,减少系统暴露:通过精心的递送系统设计(如利用GalNAc靶向肝细胞,或利用多肽靶向肿瘤细胞),可以将药物更多地富集在病灶部位,减少对正常组织的影响。例如,ASGPR靶向的胶束能特异性地被肝癌细胞摄取,而对正常肝细胞影响较小。
6). 拓展适应症范围 双靶点策略极大地拓展了siRNA药物的应用边界,使其从单基因遗传病,走向了机制更复杂的多基因疾病。
进军中枢神经系统疾病:针对阿尔茨海默病、亨廷顿舞蹈症等复杂神经退行性疾病,双靶点siRNA能够同时干预两个不同的致病通路(如同时靶向MSH3和HTT,或APOE和JAK1),在小鼠中枢神经系统中实现了长达至少2个月的有效基因沉默。
靶向“不可成药”靶点:许多关键的致癌蛋白(如KRAS、MYC)由于其蛋白结构特点,长期以来被认为“不可成药”。而siRNA直接在基因水平发挥作用,为靶向这类靶点提供了全新路径。
3.临床进展加速
部分药物已进入临床II期或III期阶段,如时安生物的SA1211(针对慢性乙肝)、必贝特的BEBT-701(针对高血压合并高血脂)等。临床前研究显示,双靶点siRNA药物在降低靶基因表达、改善疾病症状方面表现出良好效果,且安全性可控。
1). 心血管代谢领域:临床进展最快的方向 心血管疾病通常是多因素导致的,因此成为双靶点siRNA疗法最先突破的领域。
Arrowhead的ARO-DIMER-PA (PCSK9/APOC3):这是目前全球首个进入临床阶段的双功能RNAi药物。它利用其TRiM™平台设计,旨在同时抑制PCSK9(降低坏胆固醇LDL-C)和APOC3(降低甘油三酯TG)。在非人灵长类动物的临床前研究中,该药已显示出能有效降低血清PCSK9和APOC3水平,并改善混合型高脂血症相关的脂质指标-10。其1/2a期临床试验已于近期启动,旨在评估其在混合型高脂血症患者中的安全性、耐受性及药效。
大睿生物的RN5681 (PCSK9/LPA):这是另一种设计思路的双靶点siRNA,通过其专有的"即插即用"平台,将一个分子设计成可同时靶向PCSK9和LPA 。LPA基因编码脂蛋白(a),是另一个独立且难以通过现有疗法控制的心血管风险因素。该药物已递交澳大利亚临床试验申请,即将进入1期临床,目标是通过每6-12个月给药一次,同时降低LDL-C和Lp(a),以更全面地管理心血管风险。
2). 肿瘤治疗领域:侧重于改善肿瘤微环境 在肿瘤领域,双靶点策略更多用于同时攻击肿瘤细胞和其赖以生存的微环境。
圣诺医药的STP355 (TGFβ1/VEGFR2):这是一款利用多肽纳米颗粒(PNP)包装的双重siRNA疗法。它同时靶向TGFβ1(一个关键的免疫抑制分子)和VEGFR2(一个关键的血管生成因子)。在黑色素瘤小鼠模型中,STP355显示出强大的抗肿瘤效果,与化疗药顺铂相比,STP355使肿瘤重量降低70%(顺铂组为61%),且无明显毒副作用;使肿瘤内T细胞和自然杀伤细胞(NK细胞)的浸润增加近4倍;与PD-L1等免疫检查点抑制剂联用时,肿瘤抑制率最高可达73%,显示出克服免疫治疗耐药的潜力。
3). 中枢神经系统(CNS)疾病领域:突破递送与多基因设计 CNS疾病的病理机制复杂,且药物递送困难。学术界正在探索新型的分子结构来解决这一问题。
马萨诸塞大学医学院的线性二价siRNA (dual-targeting di-valent siRNA):研究人员重新设计了已有的CNS活性二价siRNA,通过一个共价连接子将两个不同的siRNA序列线性连接,形成一个可同时沉默两个靶点的单一分子。在小鼠模型中,该设计被证实能够在中枢神经系统中有效且持久地(至少2个月)沉默与疾病相关的基因对。
亨廷顿舞蹈症:同时靶向致病基因HTT和疾病加速基因MSH3。
阿尔茨海默病:同时靶向APOE和JAK1。 这一进展为治疗复杂的神经退行性疾病提供了新的药物设计框架。
4). 其他联合治疗策略:药物与基因协同 一些研究也在探索将siRNA与小分子药物联合递送,以取得协同治疗效果。
ASGPR靶向胶束(COP1 siRNA + 乐伐替尼):研究人员开发了一种GalNAc修饰的聚合物胶束,用于共递送靶向E3连接酶COP1的siRNA和肝癌治疗药物乐伐替尼。该设计通过靶向肝癌细胞表面的ASGPR受体,实现了在肝癌细胞中的富集。在原位肝癌小鼠模型中,该联合疗法使肿瘤减少了73%,远高于单用乐伐替尼的31%,效果显著。
4.产业化挑战待突破
双靶点siRNA的合成工艺复杂,正义链长度增加、 linker修饰引入等因素导致生产难度增大,规模化生产面临挑战。同时,专利壁垒较高,企业需通过技术创新或合作开发突破技术瓶颈。
发展趋势:
1.适应症拓展
未来双靶点siRNA药物的适应症将从当前的心血管疾病、乙肝、肿瘤等领域,逐步向神经系统疾病、自身免疫性疾病、代谢性疾病等复杂疾病延伸,满足更多未被满足的临床需求。
2.递送技术优化
肝外递送技术是未来发展的关键方向。随着LNP、抗体偶联、肽类递送等技术的不断进步,双靶点siRNA药物有望更高效地递送到肝脏以外的组织器官,如中枢神经系统、肌肉、肺部等,拓展治疗范围。
3.联合治疗策略
双靶点siRNA药物可能与现有药物(如小分子药物、生物制剂)联合使用,形成更强大的治疗方案。例如,在肿瘤治疗中,与免疫检查点抑制剂、化疗药物等联合,提高治疗效果,降低耐药性。
4.智能化设计与AI辅助研发
利用人工智能技术进行靶点筛选、序列优化、脱靶预测等,将提高双靶点siRNA药物的研发效率和成功率。AI驱动的药物设计平台有望加速药物发现进程,降低研发成本。
5.全球化合作与市场拓展
国际药企与国内创新企业之间的合作将更加频繁,通过技术授权、联合开发等方式共享资源,加速药物全球上市进程。同时,随着药物临床数据的积累和市场认可度的提高,双靶点siRNA药物有望在全球范围内获得更广泛的应用。总体而言,双靶点siRNA药物凭借其独特的优势,正成为小核酸药物领域的重要发展方向。尽管面临技术、产业化等挑战,但随着技术的不断进步和临床研究的深入,有望为复杂疾病的治疗带来新的突破。
参考资料:
1.A programmable dual-targeting di-valent siRNA scaffold supports potent multi-gene modulation in the central nervous system,doi: 10.1101/2023.12.19.572404
2.ASGPR-targeted micelles co-delivering lenvatinib and COP1 siRNA for hepatocellular carcinoma via dual-targeting,DOI: 10.1016/j.ejps.2025.107308
3.Development of a Dual Gene-Targeted Multi-Sirna with Branched Structure and Its Role in the Therapy of Liver Cancer,https://doi.org/10.3390/ph18121844
免责声明:本微信文章中的信息仅供一般参考之用,部分内容摘自网络及AI生成,如有侵权联系删除。此公众号任何时候都不保证文中描述内容的可靠性,不可直接作为决策内容,生物制药合伙人不对任何主体因使用本文内容而导致的任何结果承担责任。
公众号已建立“生物药工艺开发技术交流”微信群,添加小编微信514099167 加入,加微信时备注姓名-单位-岗位,非生物制药行业人员勿扰。
生物制药合伙人
扫码关注我们
ID:zpt_Partner
W:514099167
分享,点赞,在看!为生物制药人三连击!
2026-03-03
·西兰生物
CNS 递送突破:Arrowhead的 ARO-MAPT(针对阿尔茨海默病)于2月正式开始人体给药。该药采用了全新的递送系统,实现了通过皮下注射穿透血脑屏障并达到深度基因敲低。
肺部靶向:N4 Pharma与 SRI合作,通过Nuvec 平台技术成功将 siRNA 递送至非小细胞肺癌细胞,标志着肺部给药技术的突破。
双靶点 siRNA: Arrowhead 启动了 ARO-DIMER-PA临床,这是全球首个在单一分子中同时沉默PCSK9和 APOC3基因的疗法,旨在一次性解决混合型高脂血症。国内已有多家公司推进双靶点siRNA临床,新一代寡核酸设计正在崛起。
Bepirovirsen (ASO) 2月26日在日本提交上市申请。有望成为全球首个实现慢性乙肝“临床治愈”的寡核酸药物,市场潜力极大。
监管重大突破:2026年2月23日,FDA 发布了《个体化治疗的可行机制框架(Plausible Mechanism Framework)》草案。
该政策专门针对基因组编辑和 RNA 类疗法,允许针对极罕见病的药物基于“明确的生物学作用机制”而非大规模随机对照临床试验(RCT)进行审批。这极大地缩短RNA等定制化药物的上市周期,被视为“核酸药物的快速通道”,将引爆针对单基因罕见病的小众药物开发。
全球寡核酸药物(主要包括 ASO、siRNA 等 RNA 靶向疗法)2025 年销售额约 71.9 亿美元,2024 年市场规模约 59 亿美元,预计 2030 年达到约 177 亿美元(来源:MarketsandMarkets Research Pvt. Ltd.)。
随着寡核酸药物从罕见病进入慢性病和大适应症治疗阶段,行业正在进入第二轮增长周期。
葛兰素史克(GSK)正式宣布,将其与 Wave Life Sciences 共同开发的 RNA 编辑疗法 WVE-006 的全球权益退还。两年前,双方签署的 33 亿美元里程碑合作,至此结束。
CRISPR 奠基人张锋与Illumina前首席技术官 Alex Aravanis 共同创立的 Moonwalk Biosciences 宣布:放弃原有的表观遗传编辑计划,全面转型开发 siRNA药物。
1.圣因生物
公司宣布与基因泰克达成一项全球研发合作与许可协议,双方将基于圣因生物专有的RNAi药物研发平台共同推进一款RNAi疗法的开发。圣因生物将获得2亿美元的首付款,并有权收取开发和销售里程碑付款,共计15亿美元;以及分级特许权使用费。2.前沿生物
前沿生物(688221)宣布已于2月16日与葛兰素史克(GSK)签署独家授权许可协议,将旗下两款小核酸(siRNA)在研产品的全球权益授予GSK。公司将获得4000万美元首付款及1300万美元近期里程碑付款,此外还有累计9.5亿美元的开发、监管及商业化里程碑付款。3.Junevity
公司专注于通过 siRNA 抑制转录因子来逆转细胞衰老状态,是核酸药物在“抗衰/代谢”领域的新势力。完成新一轮融资,推进 RESET 代谢重编程平台。4.Atrium Therapeutics
从诺华收购 Avidity 的交易中剥离,专注心脏特异性 RNA 递送,拥有领先的心肌病管线。2026年2月27日正式分拆上市,获得 2.7 亿美元现金。
免责声明:以上内容仅供参考!不做任何投资建议,凡据此购入者,概不负责,盈亏自负!
siRNA核酸药物引进/卖出上市批准并购
2026-02-28
·九洲药业
近日,Arrowhead宣布已完成ARO-DIMER-PA的1/2a期临床试验的首批受试者给药。ARO-DIMER-PA旨在抑制PCSK9(前蛋白转化酶枯草杆菌蛋白酶/kexin9型)和APOC3(载脂蛋白C3)基因的表达,以治疗混合型高脂血症。ARO-DIMER-PA是Arrowhead公司基于TRiM平台研发的首个能同时靶向两个基因的临床候选药物。Arrowhead此前在2025年美国国家脂质协会(NLA)年度科学会议上公布了ARO-DIMER-PA的临床前数据,结果显示ARO-DIMER-PA能有效降低食蟹猴中的低密度脂蛋白胆固醇(LDL-C)以及甘油三酯(TG)的水平。
Jiuzhou News
关于ARO-DIMER-PA-1001 1/2a期研究
ARO-DIMER-PA-1001 (NCT07223658) 是一项1/2a期安慰剂对照剂量递增研究,旨在评估单剂量ARO-DIMER-PA(第1部分)和多剂量ARO-DIMER-PA(第2部分)在78名混合型高脂血症成年受试者中的安全性、耐受性、药代动力学、药效学以及对LDL-C、TG的影响。
关于混合型高脂血症
混合型高脂血症是一种高发疾病,其特征是LDL-C和TG水平同时升高,是动脉粥样硬化性心血管疾病(ASCVD)的主要危险因素。ASCVD相关疾病是全球首要致死因素,并伴随较大的发病率和医疗费用。尽管降低LDL-C水平的疗法能够有效降低ASCVD风险,但并不能完全满足混合型高脂血症患者的临床需求。
关于ARO-DIMER-PA
ARO-DIMER-PA是一种偶联GalNAc配体的双靶点siRNA药物。ARO-DIMER-PA能靶向并特异结合肝细胞PCSK9和APOC-3基因的 mRNA,激活核酸酶RNase H降解上述mRNA,以减少人体LDL-C和APOC-3的产生,进而治疗混合型高脂血症。LDL-C常被称为“坏胆固醇”,是提示ASCVD风险的关键指标,当LDL-C水平升高,将促进动脉粥样硬化斑块的形成,增加ASCVD风险;PCSK9的作用机制为破坏LDL受体,以提高LDL-C的水平。APOC-3是一种主要在肝脏中合成的载脂蛋白,负责调节血浆中的TG代谢,能有效升高TG水平;APOC-3的作用机制包括抑制富含TG的脂蛋白(TRLs)脂解作用、抑制脂蛋白脂酶LPL活性以及促进肝内极低密度脂蛋白VLDL的组装和分泌等。ARO-DIMER-PA旨在同时降低体内PCSK9和APOC-3基因的表达,进而降低LDL-C和TG的水平,以有效治疗混合型高脂血症。
参考文献
1.Arrowhead官网
免责声明
本公众号注明原创的内容权利均属九洲药业所有,未经授权,不得擅自使用或许可他人使用。如需获得授权,请和九洲药业提前联系。已获得授权的,应在授权范围内使用,并注明来源且不得再全部或部分转授权他人。
本公众号对转载、分享的内容、陈述、观点判断保持中立,不对所包含内容的合法性、准确性、可靠性或完善性提供任何明示或暗示的保证,该等内容版权归原作者所有,仅供学习参考之用,若对转载、分享的内容有任何权利疑问,烦请联系九洲药业。
临床结果siRNAASCO会议临床研究
100 项与 ARO-DIMER-PA 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 混合型高脂血症 | 临床2期 | 新西兰 | 2025-12-22 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用