预约演示
【浙江】药物临床试验机构监督检查指南发布
药物审批
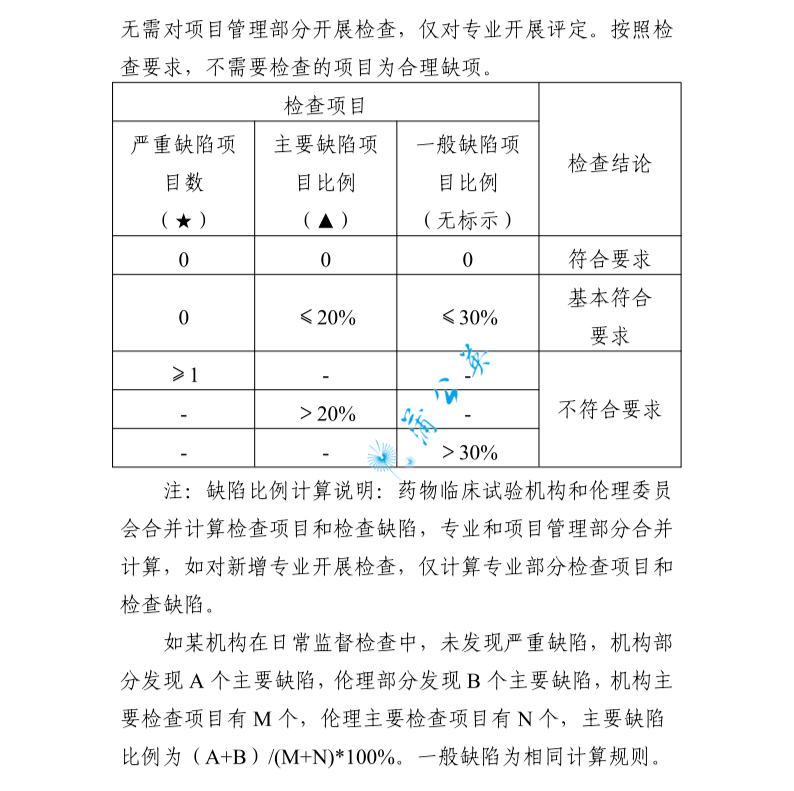
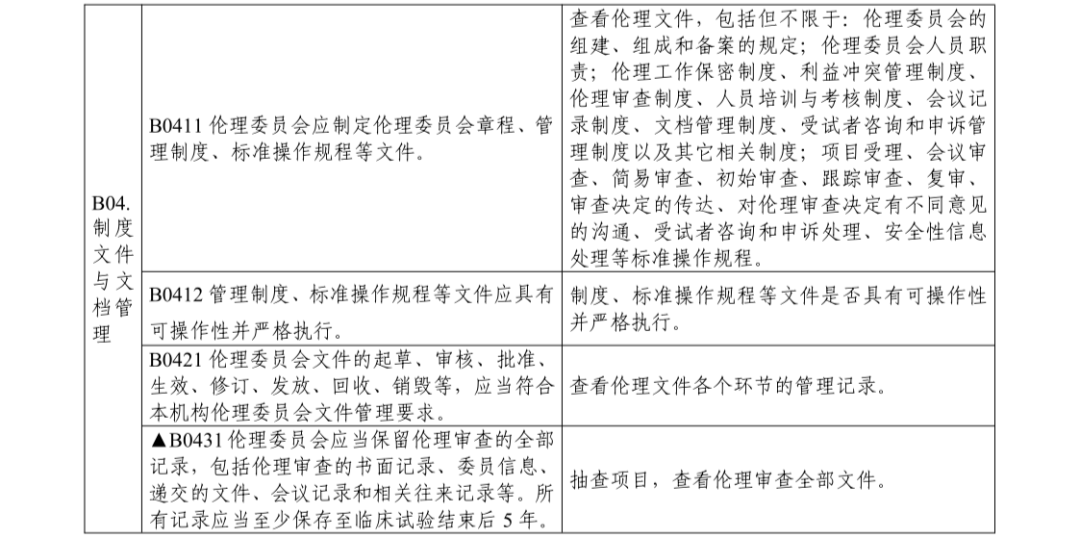
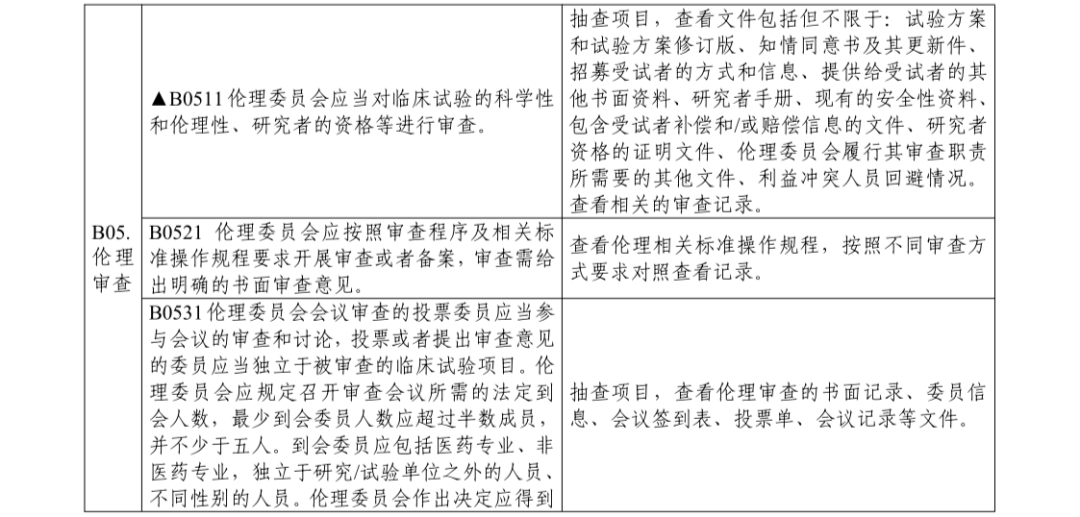
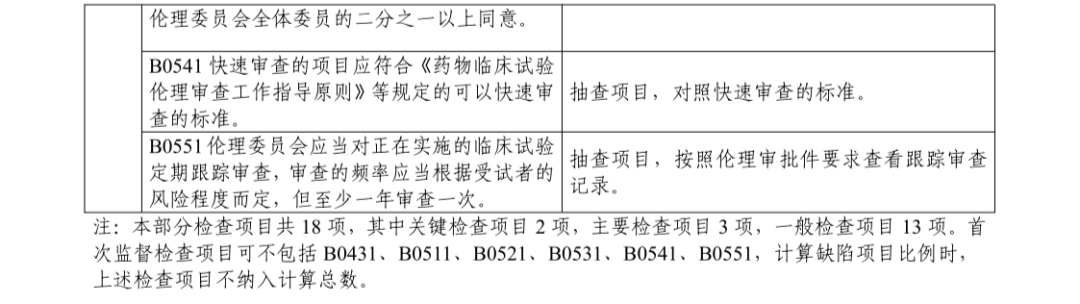
来源:浙江药监局 编辑:wangxinglai2004 2022年12月06日,浙江药监局发布了《浙江省药物临床试验机构监督检查指南》,检查内容分为药物临床试验组织管理机构、伦理委员会、专业和项目管理四个部分,包含对备案条件、机构运行管理、项目实施等方面的检查内容,共 103 个检查项目,自发布之日起施行。主要内容检查内容分为药物临床试验组织管理机构、伦理委员会、专业和项目管理四个部分,包含对备案条件、机构运行管理、项目实施等方面的检查内容,共 103 个检查项目;检查结束后,检查组应告知被检查机构于 10 个工作日内将整改报告报送组织检查单位;检查项目分为关键项目(标示为“★”)、主要项目(标示为“▲”)和一般项目(无标示),不符合相应检查项目的缺陷等级分别为“严重缺陷”、“主要缺陷”和“一般缺陷”;如果单一问题判定为主要缺陷,但经评估,有数个较为严重的,且为广泛的或系统性的主要缺陷,可综合数个主要缺陷后上升为严重缺陷;药物临床试验机构和伦理委员会合并计算检查项目和检查缺陷,专业和项目管理部分合并计算,如对新增专业开展检查,仅计算专业部分检查项目和检查缺陷。
通知原文根据《药物临床试验机构管理规定》《药物临床试验质量管理规范》,我局组织制定了《浙江省药物临床试验机构监督检查指南》,现予发布,自发布之日起施行。

Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao

Preview
来源: 蒲公英Ouryao

Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao

Preview
来源: 蒲公英Ouryao

Preview
来源: 蒲公英Ouryao

Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao
Preview
来源: 蒲公英Ouryao
机构
-适应症
-靶点
-药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


