预约演示
Mol Metabol:科学家识别出关键蛋白调节低密度脂蛋白胆固醇背后的特定分子机制
2023-02-09
基因疗法核酸药物
Preview
来源: 生物谷
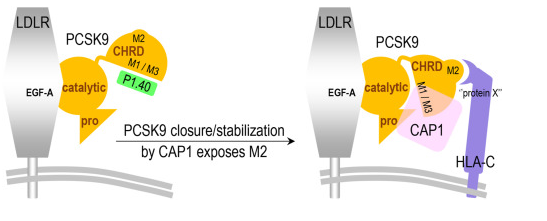
科学家识别出关键蛋白调节低密度脂蛋白胆固醇背后的特定分子机制。
图片来源:Molecular Metabolism (2022). DOI:10.1016/j.molmet.2022.101662
原始出处:
CaroleFruchart Gaillard,Ali Ben Djoudi Ouadda,Lidia Ciccone, et al. Molecular interactions of PCSK9 with an inhibitory nanobody, CAP1 and HLA-C: Functional regulation of LDLR levels, Molecular Metabolism (2022). DOI:10.1016/j.molmet.2022.101662
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
-药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


