更新于:2023-12-28

Nanjing Vazyme Biotech Co., Ltd.
更新于:2023-12-28
概览
关联
100 项与 Nanjing Vazyme Biotech Co., Ltd. 相关的临床结果
登录后查看更多信息
0 项与 Nanjing Vazyme Biotech Co., Ltd. 相关的专利(医药)
登录后查看更多信息
63
项与 Nanjing Vazyme Biotech Co., Ltd. 相关的新闻(医药)2023-12-14
抗体药物可以说是现代生物医药产业的主力军。据公开数据显示,2022年全球抗体药物市场规模达到2200亿美元,其中前50款抗体新药合计销售额2063亿美元,占到94%。另外,截至2023年10月底,FDA累计批准了131款抗体新药。图1:FDA历年获批上市抗体药情况作为一种由多个氨基酸组成的生物大分子,抗体的结构具有特殊性和复杂性,这也导致了其质量的不均一性。抗体药物中使用到的单克隆抗体(IgG)在生产工艺(细胞培养、分离纯化)与保存过程中易发生不均一性的变化,包括抗体蛋白的二聚体、多聚体、脱酰胺化、末端氨基酸突变以及糖链部分的结构差异。这些不均一性会显著影响药物的安全性和有效性。在抗体药物的研发、申报和生产流程中,质量表征始终贯穿于全过程。因此,如何全面表征分析抗体药物的关键质量属性(CQA),是抗体药物开发的关键点和难点。在药品制造过程中制定相应的控制策略,来得到目标的抗体质量属性很重要。抗体药物质量分析就是对影响抗体药物药效的关键质量属性进行鉴定。ICH Q8(R2)法规指南中对关键质量属性(CQA)的定义为应在适宜限度、范围和分布内以保证药品质量的物理、化学、生物或微生物属性或特性。CQA评估的目的是鉴定出哪些质量属性在后续的生产工艺设计中需要进行控制。那如何判断一个属性是否为CQA呢?这取决于当该属性超出可接受范围时由风险评估获得的该属性对药品的有效性和安全性的影响程度和不确定性。抗体药物质量分析主要包括结构表征、寡糖分布、异质性(分子大小/电荷异质性)、活性和杂质等。图2:质量属性分析内容(来源:抗体药物质量研究与评价/王兰/中检院)其中,活性分析是对药物的有效成分和含量以及药物效价的测定,是确保抗体类药物有效性的重要质控指标,因而需要建立完整的体系进行表征。无论是抗体药物Fab区需要考量的Antigen binding,还是Fc介导的CDC,ADCC,ADCP以及FcRn介导的抗体半衰期反应,都是抗体药物研发过程中的活性分析必不可少的部分。一般而言,活性测定包括生物学活性测定和结合活性测定。结合活性可以直接的反映抗体结合抗原的能力,以及与效应分子/受体的结合能力,如FcγRIII、C1q等。在此基础上,通过细胞学生物活性测定,如抗体依赖性细胞介导的细胞毒性(ADCC)、补体依赖的细胞毒性(CDC)、细胞增殖抑制实验及细胞因子测定等,组成了体外检测抗体活性的全面表征体系。可以说,这是抗体药物进入活体实验的基础和临床实验获得成功的保证。基于此,12月16日(周六) 13:30-17:00,诺唯赞联合生物制品圈将共同组织了一场以“抗体药关键质量属性分析及活性检测要点”为主题的线下沙龙活动,共同探讨抗体药关键质量研究基础和活性检测研究相关的内容。希望带给大家一些启发和帮助,共同助力抗体药行业的长久发展。1活动信息1、时间:2023年12月16日(周六)13:30-17:002、地点:上海(具体地点待定)3、参与人员:生物医药研发企业、科研院校和监管机构从业人员4、报名方式:扫描二维码加工作人员微信,备注“抗体沙龙”,活动仅限生物制药行业人员,规模在20人以内,本活动采用审核制,名额有限,最后以邮件确认为准。5、报名费用:50-100元(具体待定,含场地费用、茶歇等,报名缴费后若无法按时到场参与,报名费不予退还)2讨论话题一、抗体药关键质量研究基础1.关于抗体药质量研究,国内外有哪些重要的技术指南或规范?2.高产细胞株的筛选、细胞的检定有哪些关键考虑?3.抗体药质量分析技术主要有哪些?二、抗体药活性检测研究1、抗体药活性检测主要包含哪些?2、抗体药CMC阶段对高产细胞株的筛选要求都哪些?3、高产细胞株的筛选现常用的方法一般如何选择?测定方法的选择依据是怎样的?解决高通量的痛点,HTRF方法学是不是可以完全替换常规ELISA方法学?5、报告基因细胞株活性检测方法有何优点?有哪些应用场景?6、细胞株筛选和活性检测的方法学要求?eg特异性、稳定性、精密度、准确度;参考的标准是?7、抗体药的抗原结合活性测定一般在什么阶段?测定方法的选择依据是怎样的?HTRF方法的是否可以作为放行标准?8、关于ADCC活性分析,原代细胞方式和报告基因方式选择依据是什么?9、不同的药物类型eg:双抗、单抗、ADC、CAR-T对细胞因子检测的要求差异是怎样的?10、细胞因子不同测试阶段有哪些检测方法?常用方法CBA、MSD、ELISA、HTRF等选择的依据是什么?测试不同因子的选择依据是什么?是否会作为质控放行检项?3沙龙宗旨生物蜂:“蜂”有勤劳,传播,奉献之意。作为生物制品圈线下平台这一延伸,生物蜂旨在打造一个近距离的,高效的,中立的交流平台,为生物制品圈的技术达人创造交流空间!参考资料:[1]抗体药物质量研究的共性问题.抗体君.2023-03-21.[2]候选新药关键点!抗体质量全面表征之活性测定.药融圈.2022-07-21.[3]抗体药物质量研究与评价.王兰.中检院单抗室.[4]关键质量属性(CQA)的评估.星辰纯视界.2020-02-09.[5]2022年抗体药销售排行TOP50.医药笔记.2023-02-12.[6]2023 FDA 批准上市新药(1-10月).早研早聊.2023-10-31.识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
上市批准抗体药物偶联物临床研究医药出海
2023-12-03
mRNA可实现对工艺过程和配方进行最少的改变,就能在一个走通的技术平台上快速生产针对新靶标(新变体或新疾病)的疫苗,但这套工艺依赖于mRNA平台CQAs的牢固确立,以及支持CQAs的可靠测量方法和标准。所以在大规模制备工艺、产品过程控制、质量控制与质量体系等多方面依然存在较大挑战。上期直播由师从夏宁邵院士的徐灵杰分享了dsRNA及IVT工具酶杂质的检测标准和方法。除了杂质影响外,5’帽和poly A尾巴的长度和分布对于确保产生的蛋白质抗原的质量和mRNA的一致性也极其重要。mRNA的5’端帽子结构可维持体内稳定性,促进蛋白的翻译。加帽与未加帽的mRNA仅相差一个核苷酸(m7G),相较于完整的mRNA难以区分。目前USP草案基于RNase H、磁珠前处理,推荐反相液相色谱-质谱联用(RP-LC-MS/MS)/离子对反相高效液相色谱法(IP-RP-HPLC),用于mRNA加帽率的测定。在mRNA 3’端,Poly A尾长度的增加为“核心”序列提供了额外的稳定性,该序列可保证细胞核中mRNA的稳定和细胞质中mRNA的降解,调配mRNA与核糖核蛋白的结合以及随后的宿主免疫反应。目前有基于内切酶与 IP-RP-HPLC/LC-MS平台的poly A尾检测,或是基于二代或三代测序技术表征poly A。在之后的制剂环节,包封率是指包裹在脂质纳米颗粒内部的mRNA占全部mRNA的比例,它可以评估LNP有效成分的装载效率,也同样是一个重要指标,目前的分析思路主要基于荧光染料法检测包封率。诺唯赞与生物制品圈联合推出的mRNA疫苗/药物质量控制(QC)分析方案探讨系列直播第三期将就“mRNA原液/制剂质控—加帽加尾检测与包封率检测”展开探讨。本期直播将于12月4日(周一)19:30上线,扫描下方二维码,即可完成报名预约,期待与大家见面!关于诺唯赞南京诺唯赞生物科技股份有限公司(股票代码:688105.SH)作为国内酶、抗原、抗体等蛋白质创新与应用解决方案的原料供应商,拥有卓越的产品生产质量体系以及大规模供应链管理经验。诺唯赞将持续以原料药标准供应安全、高性能和质量可控的GMP级mRNA工具酶与化学原料,以及mRNA质控相关残留检测试剂盒,助力mRNA疫苗/药物的研发与生产,保障客户mRNA项目更快走向临床,造福更多患者。识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
信使RNA疫苗寡核苷酸
2023-11-30
mRNA可实现对工艺过程和配方进行最少的改变,就能在一个走通的技术平台上快速生产针对新靶标(新变体或新疾病)的疫苗,但这套工艺依赖于mRNA平台CQAs的牢固确立,以及支持CQAs的可靠测量方法和标准。所以在大规模制备工艺、产品过程控制、质量控制与质量体系等多方面依然存在较大挑战。上期直播由师从夏宁邵院士的徐灵杰分享了dsRNA及IVT工具酶杂质的检测标准和方法。除了杂质影响外,5’帽和poly A尾巴的长度和分布对于确保产生的蛋白质抗原的质量和mRNA的一致性也极其重要。mRNA的5’端帽子结构可维持体内稳定性,促进蛋白的翻译。加帽与未加帽的mRNA仅相差一个核苷酸(m7G),相较于完整的mRNA难以区分。目前USP草案基于RNase H、磁珠前处理,推荐反相液相色谱-质谱联用(RP-LC-MS/MS)/离子对反相高效液相色谱法(IP-RP-HPLC),用于mRNA加帽率的测定。在mRNA 3’端,Poly A尾长度的增加为“核心”序列提供了额外的稳定性,该序列可保证细胞核中mRNA的稳定和细胞质中mRNA的降解,调配mRNA与核糖核蛋白的结合以及随后的宿主免疫反应。目前有基于内切酶与 IP-RP-HPLC/LC-MS平台的poly A尾检测,或是基于二代或三代测序技术表征poly A。在之后的制剂环节,包封率是指包裹在脂质纳米颗粒内部的mRNA占全部mRNA的比例,它可以评估LNP有效成分的装载效率,也同样是一个重要指标,目前的分析思路主要基于荧光染料法检测包封率。诺唯赞与生物制品圈联合推出的mRNA疫苗/药物质量控制(QC)分析方案探讨系列直播第三期将就“mRNA原液/制剂质控—加帽加尾检测与包封率检测”展开探讨。本期直播将于12月4日(周一)19:30上线,扫描下方二维码,即可完成报名预约,期待与大家见面!关于诺唯赞南京诺唯赞生物科技股份有限公司(股票代码:688105.SH)作为国内酶、抗原、抗体等蛋白质创新与应用解决方案的原料供应商,拥有卓越的产品生产质量体系以及大规模供应链管理经验。诺唯赞将持续以原料药标准供应安全、高性能和质量可控的GMP级mRNA工具酶与化学原料,以及mRNA质控相关残留检测试剂盒,助力mRNA疫苗/药物的研发与生产,保障客户mRNA项目更快走向临床,造福更多患者。识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
信使RNA疫苗临床3期
100 项与 Nanjing Vazyme Biotech Co., Ltd. 相关的药物交易
登录后查看更多信息
100 项与 Nanjing Vazyme Biotech Co., Ltd. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2024年05月20日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
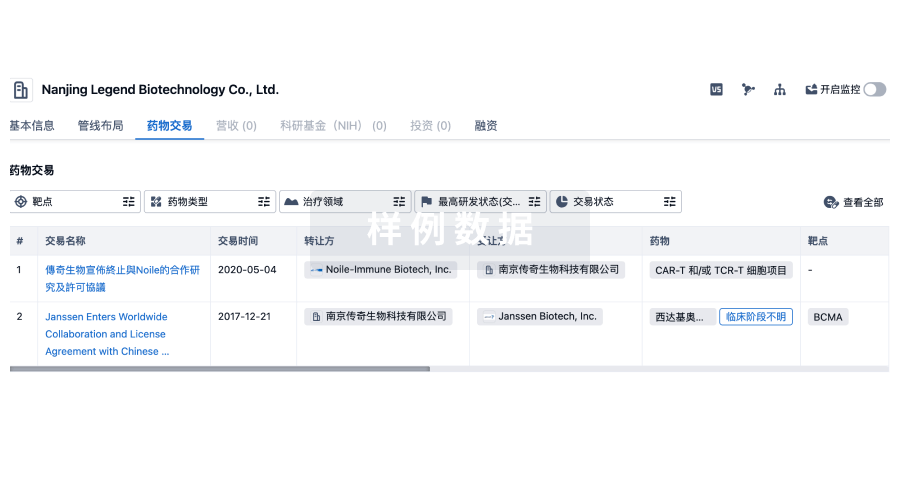
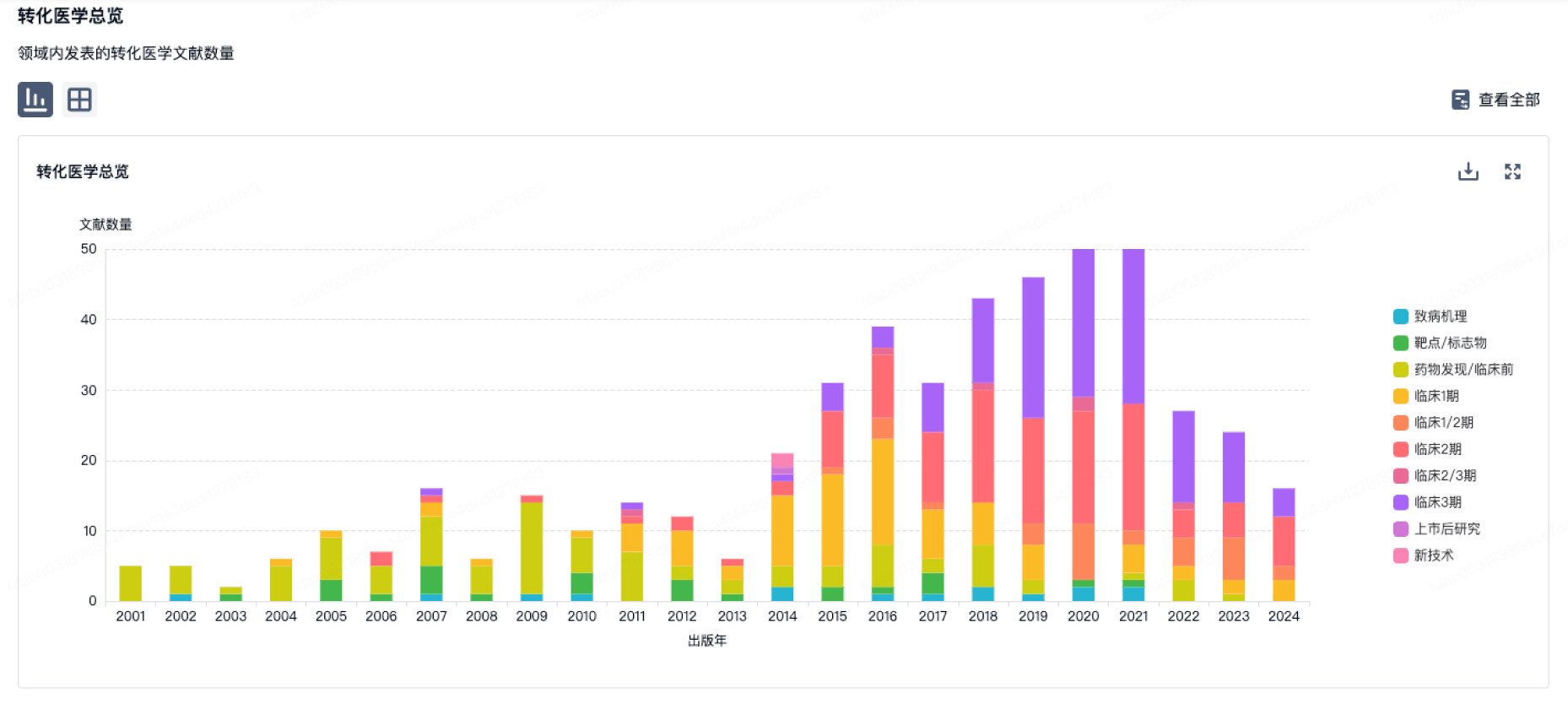
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
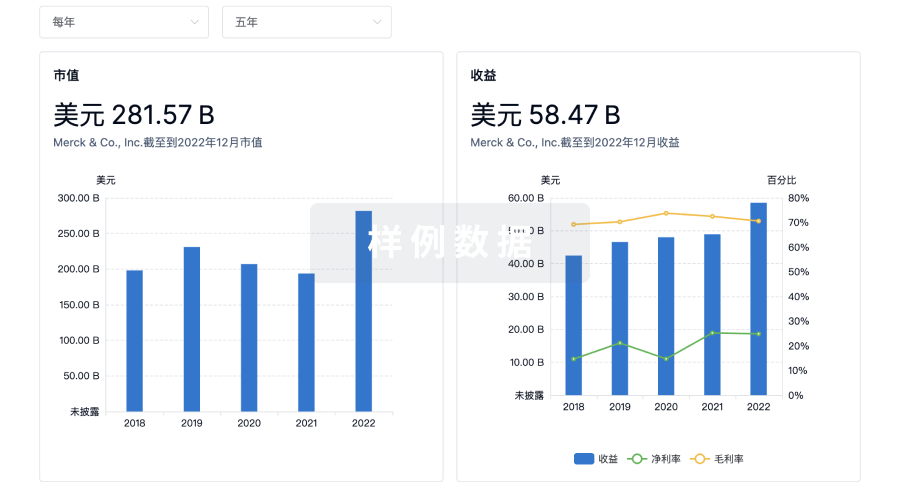
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
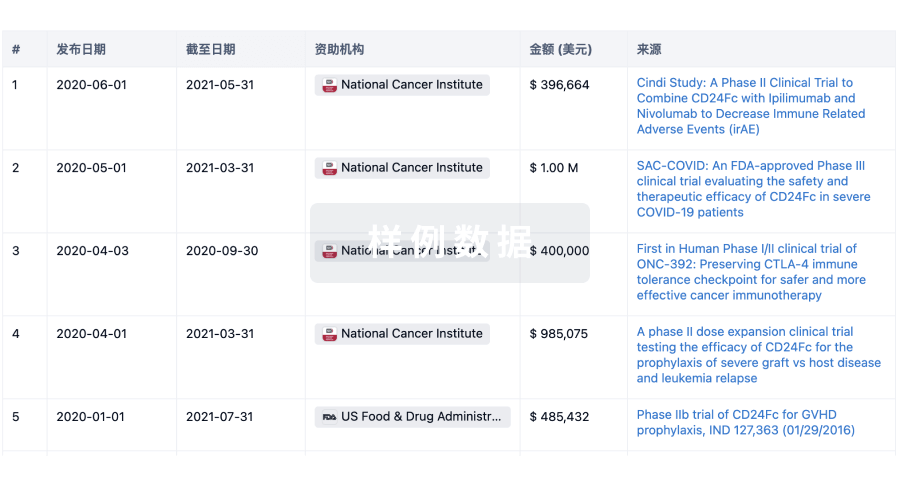
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用