更新于:2024-05-01

Avoro Capital Advisors
更新于:2024-05-01
概览
关联
100 项与 Avoro Capital Advisors 相关的临床结果
登录后查看更多信息
0 项与 Avoro Capital Advisors 相关的专利(医药)
登录后查看更多信息
18
项与 Avoro Capital Advisors 相关的新闻(医药)2024-02-28
·药明康德
▎药明康德内容团队编辑整理(来源:STAT)今日,行业媒体STAT公布了2024年STATUS榜单,上榜人士中有些是生物技术和公共卫生领域的杰出领导者和意见领袖,也有默默无闻的“无名英雄”。文章表示,他们由STAT编辑团队和外部专家组从数百位候选人中选出,在过去一年里在各自的领域做出了突出的贡献。STATUS榜单列举了50位杰出人士。今日,药明康德内容团队将与读者分享工业界和学术界的上榜人士,点击文末“阅读全文/Read more”,即可浏览榜单原文。Greg Adams,Kaiser Permanente公司董事长兼首席执行官作为Kaiser Permanente的董事长兼首席执行官,Greg Adams先生在去年监督了许多变革。去年春天,Kaiser宣布计划收购Geisinger,目标是创建一个全国性非营利医疗系统Risant Health。这一医疗系统计划在随后几年里收购5-6个医疗系统,进一步扩展其覆盖范围。Behzad Aghazadeh,Avoro Capital管理合伙人兼投资组合经理Behzad Aghazadeh博士是生物技术领域最著名的投资者之一。去年晚些时候,他在接受行业媒体STAT采访时谈到了2024年生物技术行业的前景,他指出,在行业最近的动荡之后,Avoro评估公司是否是值得投资的方法相应地发生了演变。“我们花了更多的时间来评估管理团队,”他说,“我们需要确保他们曾经同舟共济,团结在一起取得过成功。”Kristina Burow,ARCH Venture Partners常务董事ARCH Venture Partners是目前最大、表现最佳的生物技术风险投资公司之一,Kristina Burow女士的努力功不可没。她帮助创建了Neumora,这是2023年为数不多的上市生物技术公司之一,该公司计划开发包括阿尔茨海默病、精神分裂症和双相情感障碍在内的神经和精神疾病治疗方法。2023年,Burow女士共同创立的RNA初创公司Orbital宣布获得2.7亿美元A轮融资,以帮助其开发一系列基于RNA的药物。在接受STAT采访时,Burow女士表示精准免疫学领域存在巨大潜力。她还指出,目前很多归为一类的疾病将进一步细分,无论是阿尔茨海默病还是红斑狼疮。随着对基础生物学越来越多的理解,我们将发现疾病背后更多的细微差别。Susan Galbraith,阿斯利康肿瘤学研发执行副总裁阿斯利康已成为癌症药物开发的主导力量之一。Susan Galbraith博士的贡献不可忽视。自2010年加入该公司以来,她在选择推进哪些药物方面发挥了关键作用,并成为医药行业中最杰出的女性之一。阿斯利康近日在肿瘤治疗领域取得了新进展。其药物Tagrisso用于非小细胞肺癌(NSCLC)患者术后治疗,显示出亮眼的生存率提升。另外,阿斯利康与第一三共共同研发的抗体偶联药物datopotamab deruxtecan在3期临床试验中也表现出色,该试验针对的是HR阳性、HER2低表达或阴性的乳腺癌患者。Matt Gline,Roivant Sciences公司首席执行官去年,罗氏斥资超70亿美元,收购了Roivant Sciences治疗炎症性肠病的在研疗法RVT-3101。而就在不到一年前,该公司只用了5000万美元从辉瑞手中收购了这款药物,并为未来的后期临床试验进行了投资。该公司的研发管线中还有多款创新在研疗法已经进入后期临床开发阶段,其研发策略并不专注于单一治疗领域或治疗模式,候选疗法涉及免疫学、肿瘤学、血液学和皮肤科等多种领域。Reshma Kewalramani,Vertex Pharmaceuticals首席执行官兼总裁这是Reshma Kewalramani博士连续第二年入选STATUS名单,显示了Vertex的首席执行官在药物开发方面继续产生的巨大影响。近几个月,监管机构首次批准了基于CRISPR的基因编辑药物Casgevy。它由Vertex和CRISPR Therapeutics共同开发,用于治疗并有可能治愈镰刀型细胞贫血症以及β地中海贫血。Vertex还在VX-548上的研发上取得了进展,这是一种非成瘾性止痛药,希望能成为阿片类药物的安全有效替代品。该公司在今年1月宣布,VX-548在两项关键性3期临床试验中获得积极结果,计划在今年年中向美国FDA递交新药申请(NDA)。Lotte Knudsen,诺和诺德公司首席科学顾问GLP-1类药物在减重方面的革命性潜力得到广泛关注,而丹麦科学家Lotte Knudsen女士对这些药物的存在功不可没,她从1990年代开始的持续研究最终导致了诺和诺德公司的重磅药物Ozempic和Wegovy的问世。在接受STAT采访时,她表示GLP-1类药物在治疗像阿尔茨海默病这样的疾病方面可能还有更多潜力。相关阅读:重磅GLP-1药物诞生记——这名女性科学家如何带来减重疗法新时代Peter Lee,微软研究与孵化部企业副总裁Peter Lee博士是微软在医疗领域应用人工智能探索的驱动者之一,特别是他领导了与电子健康记录软件供应商Epic的合作,实现了利用AI自动编写临床医生笔记的功能。他认为,生成式AI技术将成为医疗保健和医学领域内最具革命性的工具。Ted Love,BIO主席Ted Love博士近日成为生物医药领域最大、最有影响力的行业组织之一BIO的主席。Love博士此前担任Global Blood Therapeutics的首席执行官。在BIO,他将在塑造行业形象、制定应对法规的有效策略,以及组织多元化方面发挥关键作用。Karen S. Lynch,CVS Health总裁兼首席执行官在2023年,CVS收购了Oak Street Health和Signify Health。Oak Street Health为老年人提供初级保健服务,而Signify Health则提供分析和技术支持,用于支持家庭内的健康评估。这些大胆的举措指向了一种更广泛的经营战略,包括保险公司寻求直接向患者提供初级保健。行业观察者将在未来一年密切关注CVS,以了解这些探索的成果如何。Joshua Miele,Amazon首席无障碍研究员(principal accessibility researcher)曾获得麦克阿瑟“天才奖”的Joshua Miele先生在儿童时期失明。他作为残疾人生活的个人经历赋予了他独特且富有创造性的方法来设计新的无障碍工具,这些工具包括使Amazon的语音助手Alexa适用于无法说话的人的触摸功能,以及通过盲文和凸起线条允许人们通过触觉地图进行导航。Miele先生表示,医疗保健行业应该考虑如何使服务更易于获得,提高对残疾人的可及性。Umer Raffat,Evercore ISI公司高级董事总经理Umer Raffat先生是华尔街最受尊敬的生物技术和医药行业分析师之一,他在Institutional Investor年度分析师排名中19次获得第一名。行业人士依赖他对如GLP-1减肥药前景等热门话题的丰富见解,以及他对新闻的敏锐洞察力。Daniel Skovronsky,礼来公司首席科学官Daniel Skovronsky博士正在监督开发礼来公司可能改变阿尔茨海默病、肥胖症和癌症治疗的潜在疗法。FDA批准了其重磅药物tirzepatide用于减肥,3期临床试验结果显示,服用该药物的参与者体重减轻了超过15%。而礼来公司针对淀粉样蛋白的阿尔茨海默病药物donanemab被证明能减缓认知衰退,增加了最终获得FDA批准的希望。Tim Van Hauwermeiren,argenx公司首席执行官argenx公司的皮下注射疗法Vyvgart Hytrulo去年获得美国FDA的批准上市,用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人全身性重症肌无力(gMG)患者。这是FDA批准治疗这一患者群体的首款皮下注射疗法。这一注射剂型可将患者原本需要1个小时的静脉输注缩短为用时30-90秒的皮下注射,为患者用药提供极大便利。此外,Vyvgart Hytrulo在治疗慢性炎症性脱髓鞘性多发性神经病(CIDP)的2期临床试验取得了积极的初步结果。美国FDA已经授予其补充生物制品许可申请(sBLA)优先审评资格。Chris Viehbacher,渤健总裁兼首席执行官Viehbacher先生担任渤健的首席执行官已经一年有余。过去一年里,该公司的多款创新疗法获得监管批准,包括与Ionis联合开发,治疗具有超氧化物歧化酶1突变的肌萎缩侧索硬化(SOD1-ALS)的反义寡核苷酸(ASO)疗法Qalsody。这是FDA批准治疗遗传性ALS的首款疗法。这也是首款基于生物标志物加速批准的ALS疗法。此外,该公司与Ionis联合开发的tau蛋白靶向ASO疗法BIIB080在治疗轻度阿尔茨海默病的1b期临床试验中也获得积极结果。Viehbacher先生表示,渤健在神经科学方面的根本兴趣不会改变,但他也看到了在免疫学和罕见病领域的未来潜力。Andrew Witty,UnitedHealth Group首席执行官Witty先生是美国最大的医疗保险公司的负责人,他还主导了UnitedHealth成为美国最大的门诊护理提供者之一,与近10%的医生有合作关系。这意味着Witty先生对医疗保健的未来具有巨大的影响力。David Baker,华盛顿大学生物化学教授、蛋白质设计研究所所长David Baker教授为人工智能(AI)驱动的蛋白质折叠和设计的先驱。2003年,Baker教授的团队设计出了第一个原本并不存在于自然界中的蛋白质。而其团队所开发的RoseTTAFold系统在解析蛋白质3D结构方面的表现与AlphaFold2的水平相当。2020年,他因“开发的技术让人们可以设计大自然中从未见到过的蛋白”获得了素有“科学界的奥斯卡”之称的科学突破奖——生命科学科学突破奖。2022年8月,Baker教授团队在《细胞》杂志上发表论文,他们已利用AI技术平台精准地从头设计出能够穿过细胞膜的大环多肽分子,开辟了设计全新口服药物的新途径。参考阅读:从头设计出自然界中不存在的蛋白质,他让人类离“上帝之手”越来越近Ruha Benjamin,普林斯顿大学非裔美国人研究教授Benjamin教授是Ida B. Wells JUST数据实验室的创始主任,其研究主要专注于将种族偏见参数编码到影响患者护理的算法当中,以改进在不同种族间接受医疗科技不平等的问题。Elisabeth Bik,Harbers Bik公司科学顾问Bik博士是科学图像分析领域的专家,其对科研论文中图像分析的研究推动整个科研界对于图像审查的关注,以及对图像数据的真实性有更为严格的要求。Emmanuelle Charpentier,马克斯·普朗克病原体科学研究所科学和常务董事、代理行政主管2020年,Charpentier博士由于其对基因编辑科技的贡献,与Jennifer Doudna博士共同获得当年的诺贝尔化学奖。她也联合创建了CRISPR Therapeutics公司,该公司后来与Vertex Pharmaceuticals共同合作开发出全球首款基因编辑疗法Casgevy,用以治疗镰刀型细胞贫血病(SCD)与输血依赖性β地中海贫血(TDT)患者。参考阅读:全球首款CRISPR基因编辑疗法获批,这种“基因剪刀“技术是如何诞生的?Rory Cooper,匹兹堡大学人类工程研究实验室创始主任Cooper博士的职业生涯致力于推进轮椅技术和其他改善残疾人行动能力的技术,他本身亦使用轮椅。他曾入选美国国家发明家名人堂,并获得国家技术与创新奖章。他拥有25项美国专利,涉及的产品范围包括从可连接到轮椅以帮助转移的机械臂,以及广泛采用的人体工程学推轮,该轮椅设计有助于降低使用者的腕管综合症的发病率。Diana Greene Foster,加州大学旧金山分校妇产科和生殖科学教授Foster博士专注于对避孕和流产护理中心患者的需求和偏好研究。例如,其团队证明,提供一年份的口服避孕药(而不是按月领取)可以减少意外怀孕,从长远来看单次提供一年份的避孕药更具有成本效益。Foster博士最为著名的是其所进行的Turnaway研究,该研究调查了堕胎对妇女的身体、精神和经济的影响。Turnaway研究至此已衍生出50多篇相关论文和一本书的诞生,并对家庭计划政策的制定带来显著的影响。她在2023年因着她卓越的研究,获得当年麦克阿瑟天才奖(MacArthur Fellows)。Judy Gichoya,埃默里大学医学院介入放射学和信息学副教授Gichoya博士是基于人工智能的医学影像分析领域的先驱。她的研究兴趣包括微创手术的临床差异、验证真实临床环境中的机器学习模型。她在埃默里大学共同领导的医疗保健创新和翻译信息学(HITI)实验室正在构建和整理多样化的成像数据集,其影响力正不断扩增中。今年,Gichoya还将国际人工智能研究人员聚集在一起,重点是识别和防止基于图像的人工智能算法中的偏见,并推动人工智能在医学领域的开发和使用。Barney S. Graham,莫尔豪斯医学院大卫·萨彻全球健康公平研究所所长身为免疫学家和病毒学家的Graham博士的主要研究成果之一为识别、研究呼吸道合胞病毒(RSV)用来进入人体细胞的病毒融合蛋白F(viral fusion protein F),该研究奠定了2023年全球首款RSV疫苗开发的基础。此外,他对新冠病毒刺突蛋白(spike protein)的研究也对相关疫苗的开发有着重要的贡献。Jacob Hanna,魏茨曼科学研究所干细胞生物学和合成胚胎学教授Hanna博士的研究开创迄今为止最晚期的人类胚胎模型之一,其团队利用干细胞培养模型,使其发育成相当于子宫内14天大的胚胎。Hanna博士于近期共同创立了一家初创公司Renewal Bio,该公司旨在利用他的研究来培育胚胎模型,从而将细胞转化为胚胎,以培养用于移植的组织和器官。Monica McLemore,华盛顿大学儿童、家庭和群体健康护理系教授McLemore教授担任《健康公平》( Health Equity)杂志的主编,她的研究领域位于生殖健康和健康公平领域的最前沿。她致力于提出一系列策略,旨在解决护理行业中普遍存在的种族主义问题。同时,她还参与创立了一个学程,该学程旨在教育华盛顿大学的临床医生和高级护理实践学生如何提供堕胎护理服务。Dariush Mozaffarian,塔夫茨大学“食品即医学”研究所所长作为一名心脏病学家兼营养学教授,Mozaffarian博士致力于推广健康食品作为提升公共健康的干预手段。根据最近对2012年至2022年发表研究的分析,他的学术论文是世界上被引用次数最多的论文之一,《纽约时报》等媒体经常引用他的观点,探讨可可和鲑鱼的健康益处,以及为什么奶酪不应该被负面看待。Ida Sim,加州大学旧金山分校教授兼首席研究信息官Sim教授致力于推进数字医学领域的发展,尝试解决患者健康数据相关的棘手技术问题。她共同创建了非营利组织Open mHealth,该组织开发开如CommonHealth等开放软件架构来扩大移动医疗的覆盖范围。她近期担任加州大学旧金山与伯克利分校计算精确健康联合项目的主任,预备在学术界培训下一代数字健康领导者。Feng Zhang(张锋),Howard Hughes医学研究所研究员、麻省理工学院和哈佛大学Broad研究所核心成员张锋教授是CRISPR技术开发的最初先驱者之一。他曾共同创建Editas Medicine与Aera Therapeutics公司。前者致力于基因编辑疗法的开发,后者则专注开发其专有蛋白质纳米粒子(PNP)递送平台,旨在将基因疗法、mRNA、RNAi、反义寡核苷酸(ASO)、基因编辑系统等不同载荷精准递送到广泛的人体组织和器官中。张锋教授于今年1月与基因测序专家Alex Aravanis博士等共同创立Moonwalk Biosciences,旨在开发表观遗传治疗药物。STATUS榜单还列举了医学界、非营利组织、政界和慈善界的杰出领导者,限于篇幅,本文不做一一介绍,点击文末“阅读全文/Read more”,即可浏览榜单原文。文中图片来源:上榜人士工作单位官网或个人主页大家都在看▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放参考资料:[1] STAT US LIST 2024. Retrieved February 27, 2024 from https://www.statnews.com/status-list/2024/#industry-academia免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。分享,点赞,在看,聚焦全球生物医药健康创新
并购临床3期
2023-08-19
·药通社
声明:因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及);本文不构成任何投资建议。8月7日,生物技术公司Krystal
Biotech公布2023上半年业绩:净亏损7850万美元,折合人民币5.7亿元(1美元
≈ 7.2569人民币),亏损同比扩大0.5%,其中研发费用2443万美元,同比增加20.9%,研发费用包括基于股票的补偿540万美元。在首款可重复外用的基因疗法获得FDA批准上市的利好刺激下,Krystal Biotech股价今年已经大涨60%,目前市值突破30亿美元(约218亿人民币)。5月19日,美国FDA批准了Krystal
Biotech公司开发的基因疗法VYJUVEK™(beremagene
geperpavec-svdt,B-VEC)凝胶用于治疗6月龄及以上营养不良型大疱性表皮松解症(DEB)患者。这是FDA批准的首款可重复用药的基因疗法和首款外用基因疗法药物,同时也是首个FDA批准同时用于显性和隐性营养不良性大疱性表皮松解症(DEB)治疗的基因疗法药物。 VYJUVEK™ 的花费为 24,250 美元/瓶,平均每位患者每年使用 26 瓶。这意味着每位患者每年的费用约为63万美元,经过政府强制折扣后为48.5万美元。VYJUVEK™采用1型单纯疱疹病毒(HSV-1)作为其重复递送的载体。其治疗原理是将COL7A1基因的正常拷贝输送至DEB患者的分裂和非分裂皮肤细胞,纠正遗传缺陷,使其皮肤细胞能够产生COL7蛋白,稳定患者脆弱的皮肤。5月22日,Krystal完成1.6亿美元的私募股权融资。该笔资金将用于VYJUVEK™的启动、商业化运营及其他管线药物开发,预计可支持至2026年底。此轮融资由Avoro
Capital Advisors和Redmile
Group领投,Braidwell
LP和Frazier
Life
Sciences参与其中。VYJUVEK™预计今年第三季度在美国上市。公司预计将于2023年下半年在欧洲启动正式的上市许可申请程序,并可能在2024年获得批准。VYJUVEK™获批同时,Krystal获得了罕见儿科疾病优先审查凭证(PRV),可用于为另一产品申请优先审查。这为Krystal加速其他管线获批创造了新的机会。关于Krystal
BiotechKrystal
Biotech(纳斯达克股票代码:KRYS)是一家商业阶段的生物技术公司,专注于基因药物的发现、开发和商业化,以治疗医疗需求未得到满足的疾病。VYJUVEK
TM是该公司的第一个商业产品,第一个可重复基因疗法,也是FDA批准的唯一用于治疗营养不良性大疱性表皮松解症的药物。该公司正在快速推进呼吸系统、肿瘤学、皮肤病学、眼科和美容领域的研究性基因药物的强大临床前和临床产品线。Krystal
Biotech研发管线(来源:Krystal
Biotech官网)参考资料:Krystal
Biotech官网
优先审批基因疗法上市批准财报
2023-07-10
·药融圈
▲8月03-04日 CMC-China大会 · 限时免费扫码报名中注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及),不代表平台立场。任何文章转载需得到授权。里程碑式基因疗法斩获多项“第一”药融圈旗下,药融云数据www.pharnexcloud.com显示:2023年5月19日,美国FDA批准了Krystal
Biotech公司开发的基因疗法VYJUVEK™(beremagene
geperpavec-svdt,B-VEC)凝胶用于治疗6月龄及以上营养不良型大疱性表皮松解症(DEB)患者。VYJUVEK™(B-VEC)是一款里程碑式疗法,斩获多项“第一”:是FDA批准的首款局部外用的涂抹型基因疗法、有史以来首个可重复使用的基因治疗药物,也是首个且目前唯一的针对DEB的基因治疗药物。该药物基于单纯疱疹病毒1型(HSV-1)开发,旨在通过递送人COL7A1基因的功能性拷贝,从根本上解决DEB的遗传病因,以促进伤口愈合和持续的功能性COL7蛋白表达。VYJUVEK™(B-VEC)预计将于2023年第三季度在美国上市。药融圈旗下,药融云数据www.pharnexcloud.com显示,欧洲药品管理局此前已授予B-VEC治疗DEB的孤儿药认定和优先药物资格,公司预计将于2023年下半年在欧洲启动正式的上市许可申请程序,并可能在2024年获得批准。该公司还与日本药品和医疗器械局合作研究B-VEC,并寻求在日本批准上市。2023年4月,日本厚生劳动省(MHLW)通知该公司,根据“卡塔赫纳法”(Cartagena
Act),B-VEC被确认为可安全进口。随着“卡塔赫纳法”批准B-VEC的进口,公司计划在日本启动B-VEC的规模开放标签扩展研究,预计将于2025年初在日本获得批准。▲截图自药融云数据拯救“蝴蝶宝贝”营养不良性大疱性表皮松解症(DEB)是一种极其罕见且严重的遗传性皮肤病,由COL7A1基因突变引起,它编码VII型胶原蛋白(COL7),影响皮肤和粘膜组织。由于缺乏功能性COL7蛋白,患者皮肤的真皮(皮肤内层)与表皮(皮肤外层)的粘附被破坏,极其脆弱,轻微的擦碰就会导致水疱和撕裂,甚至可影响到胃肠道、口腔、眼睛等器官,开放性伤口引起复发性皮肤感染和纤维化,导致手指和脚趾融合,最终增加侵袭性皮肤癌的风险,如侵袭性鳞状细胞癌。这些患者被称为“蝴蝶宝贝”,形容患者皮肤像蝴蝶般脆弱。(纪录片《支离破碎的男孩》就描述了一位大疱性表皮松解症患者的故事)据统计,全球范围内大约有9000例DEB患者。目前,该病的治疗方法主要以专业的皮肤护理和避免皮肤机械损伤为主,慢性伤口管理、绷带、疼痛和感染控制,以及手术干预,导致每年的护理费用估计为20万至40万美元,且当前只有美国可以提供支持性护理服务。VYJUVEK™(B-VEC)作为全球首款且目前唯一一款治疗DEB的矫正疗法,无疑为这些患者带来了希望。据悉,该药物每瓶价格为2.425万美元,平均每位患者每年使用26瓶,每位患者每年治疗费用约为63.1万美元,经政府强制折扣后为48.5万美元。为了满足患者、护理人员和家属的需求,公司开发了个性化的支持项目Krystal
Connect。该计划包括可以回答有关VYJUVEK的问题、验证健康益处、支持治疗计划和管理,以及为符合条件的患者提供有关经济援助的信息资源。此外,公司为了确保疾病的准确诊断,还推出了基因检测项目Decode
DEB。基因治疗递送载体的突破在基因治疗药物开发过程中,递送系统是主要的核心与挑战之一,也是药物实现临床应用的重要基础。(相关阅读:核酸药物“淘金热”,递送系统成角逐“高地”)VYJUVEK™(B-VEC)的成功获批不仅是基因治疗领域的里程碑,也是非AAV(腺相关病毒)递送载体的里程碑。COL7A1基因的转录产物大小达到了约9
kb,为工程化基因治疗载体的开发提出了一大挑战。这样的大小超出了腺病毒和腺相关病毒等大部分病毒载体的荷载能力,COL7A1只能经过大量定向修饰后,在慢病毒和逆转录病毒载体中功能化表达。相比之下,HSV-1病毒(单纯疱疹病毒1型)的转基因有效载荷能力超过30
kb,且由于HSV-1载体是非整合的,因此不构成任何插入突变的风险,这些特性使HSV-1载体特别适合在体(In
vivo)基因治疗。Krystal
Biotech公司基于此开发了专有的可重复基因治疗平台,即皮肤靶向给药平台(STAR-D,Skin
TARgeted Delivery
platform),该平台由经改造的非整合、复制缺陷的工程化HSV-1载体和皮肤优化基因转移技术组成,利用HSV-1的独特特性克服了其他常用载体的荷载能力、免疫原性和潜在的安全问题,并可以有效地穿透广泛的皮肤细胞,适用于将一个或多个与皮肤病相关的治疗性基因引入患者体内。该技术平台优势包括:1)可以局部给药;2)对于分裂和非分裂细胞均具有转导能力,提高治疗性基因转移效率;3)非复制性,可被细胞分裂稀释,导致瞬时转基因表达;4)高有效载荷能力可容纳大的基因或多个基因;5)允许重复给药;6)不会插入或以其他方式破坏人类基因组。这些优势使得STAR-D平台成为直接和重复向皮肤递送治疗性基因的合适选择。1/2期(GEM-1/2)临床试验显示,B-VEC疗法介导的COL7A1转基因靶向适当的细胞,并引导功能性全长COL7蛋白(包括NC1和NC2结构域)在真皮-表皮基底膜正确位置的表达。发表在《新英格兰医学杂志》上的关键3期(GEM-3)临床试验数据显示,该试验在六个月时达到了伤口完全愈合的主要终点,在三个月时达到了伤口完全愈合的关键次要终点。B-VEC组患者在治疗六个月时有67.4%的伤口完全愈合,安慰剂组为21.6%;在治疗三个月时,B-VEC组患者有70.6%的伤口完全愈合,安慰剂组为19.7%。(相关阅读:3期临床成功,涨150%,这家Biotech的基因疗法获突破)▲图源:NEJM基于上述研究的结果,VYJUVEK™(B-VEC)外用凝胶获得美国FDA批准,用于治疗六个月或以上的隐性或显性DEB患者,由医疗保健专业人员在医疗保健专业机构(例如诊所)或家庭环境中使用。获得批准后,FDA还向Krystal
Biotech公司颁发了罕见儿科疾病优先审查凭证(PRV)。成立18个月即IPO的基因治疗“新星”Krystal
Biotech公司专注于为罕见疾病患者开发和商业化基因治疗药物,目标是开发易于使用的药物,以极大地改善罕见疾病和慢性病患者的生活。除了拥有基于工程化HSV-1的基因治疗技术平台之外,Krystal公司内部还拥有商业规模的符合CGMP的制造能力,从而支持产品的制造需求以及未来增长。公司创始人是在生物技术领域拥有丰富经验的Krish
Krishnan和Suma
Krishnan夫妇,从自筹资金组建Krystal
Biotech到公司IPO,只花了18个月。药融圈旗下,药融云数据www.pharnexcloud.com显示,2016年4月,Krystal
Biotech开始正式运营,并于2017年9月登陆纳斯达克(NASDAQ:KRYS),IPO募得资金4554万美元。2023年5月,Krystal
Biotech在宣布VYJUVEK™(B-VEC)获批消息之后,随即完成1.6亿美元的私募股权融资,由Avoro
Capital Advisors和Redmile
Group领投,Braidwell
LP和Frazier
Life Sciences参与。截止目前,公司市值约31亿美元。该公司早前被Fierce
Biotech评为2023年生物技术领域十大并购目标之一。Krystal
Biotech公司当前的生物制药管线主要聚焦在皮肤科、呼吸科和眼科三个领域。除了VYJUVEK™(B-VEC)已获批之外,其他产品均处于在研阶段。▲Krystal
Biotech产品管线(更新至2023年6月)在皮肤科领域,公司主要还开发了另两款局部凝胶制剂,分别针对不用的罕见皮肤疾病。KB105(inetagugene
geperpavec)正在被开发用于治疗常染色体隐性遗传的先天性鱼鳞病(ARCI),该病是一种严重的罕见皮肤病,患者往往表现出终身明显的板状皮肤鳞屑,通常是深色,可覆盖整个身体。ARCI常由TGM1(转谷氨酰胺酶1)基因失活突变引起,该基因编码一种对皮肤屏障正常形成至关重要的蛋白质。KB105作为一种可重复的现成基因疗法,旨在局部应用于皮肤,递送两个TGM1基因的拷贝,从而在给药部位直接补充TGM1蛋白。药融云数据www.pharnexcloud.com显示,FDA和EMA已分别授予KB105孤儿药称号用于治疗TGM1缺陷型ARCI,FDA已授予KB105快速通道认定和罕见儿科疾病用药认定用于治疗TGM1-ARCI。目前,该药正在进行一项1/2期临床试验,预计将在2023年年中启动2期临床。KB104被开发用于治疗内瑟顿(Netherton)综合征,该病是一种罕见的常染色体隐性遗传性皮肤病,由SPINK5基因(由Kazal
5型丝氨酸蛋白酶抑制剂基因)突变引起,该基因编码一种表达于上皮和黏膜表面的丝氨酸蛋白酶抑制剂。患者因SPINK5基因突变,皮肤中的丝氨酸蛋白酶过度活化,引起不受控制的脱屑,导致皮肤屏障缺陷,特征是先天性鱼鳞病样红皮病、毛干缺陷、反复感染等。KB104旨在将SPINK5基因的两个拷贝递送到相关皮肤细胞,直接向皮肤补充功能性SPINK5,纠正脱屑并改善皮肤的屏障功能。公司预计将在2023下半年提交该药的IND申请,此前KB104已获得FDA授予的KB104罕见儿科疾病用药认定用于治疗内瑟顿综合征。在呼吸科领域,Krystal
Biotech主要开发了两款吸入(雾化)制剂,同样是针对罕见疾病。KB407被开发用于治疗囊性纤维化(CF),该病是一种进行性遗传疾病,由囊性纤维化跨膜传导调节因子(CFTR)基因突变引起,患者分泌性气道上皮中缺乏功能性CFTR蛋白,引起Cl-、碳酸氢盐和硫氰酸盐分泌缺陷,加上Na+吸收和粘液产生增多,导致气道表面液体脱水和酸化,特征是反复肺部感染、气道分泌物增加,最终导致呼吸衰竭。KB407作为一种可重复的现成的基因疗法,旨在通过吸入(雾化)给药将两个全长CFTR转基因拷贝直接递送到气道上皮,诱导肺部全长正常CFTR蛋白表达。体外研究显示,KB407纠正了患者来源的3D肠道类器官中的CFTR缺陷,且与CFTR突变类型无关。目前,KB407正在美国和澳大利亚开展两项1期临床研究。此前FDA和EMA已分别授予KB407孤儿药称号用于治疗囊性纤维化,FDA已授予KB407罕见儿科疾病用药认定用于治疗囊性纤维化。KB408被开发用于治疗α-1抗胰蛋白酶缺乏症(AATD),该病是一种常染色体共显性遗传病,由蛋白酶抑制剂基因位点处的SERPINA1基因内发生等位基因突变所致,患者血清α-1-抗胰蛋白酶(AAT)水平低,导致进行性肺损伤和严重的呼吸功能不全,表现为慢性阻塞性肺病(COPD)和全腺泡性肺气肿等。KB408旨在递送编码正常人α-1-抗胰蛋白酶蛋白的SERPINA1转基因的两个拷贝,从而治疗AATD,公司预计将在2023年底提交IND申请。在眼科领域,Krystal
Biotech开发了眼用的B-VEC,用于治疗DEB(营养不良性大疱性表皮松解症)的眼部并发症。在DEB患者中,很大一部分存在COL7缺乏相关的眼部并发症,表现为角膜擦伤、瘢痕和血管翳等,可导致进行性视力丧失甚至失明,在RDEB(隐性营养不良性大疱性表皮松解症)患者中,超过50%的患者存在眼部并发症。B-VEC眼部制剂旨在恢复DEB患者的局部COL7A1表达和眼部功能。在同情用药计划中,B-VEC眼部制剂显著改善了DEB患者眼部并发症,患者视力显著改善,公司计划与FDA召开会议以调整眼部制剂的进一步开发路径。这也表明了公司的基因治疗平台具有治疗多种眼部疾病的潜力。医美布局虽然目前Krystal
Biotech的重点是开发基因疗法以治疗严重罕见疾病,但同时公司也在评估技术平台应用于更常见疾病和/或非遗传性疾病的潜力。2019年4月,Krystal
Biotech在特拉华州注册成立全资子公司Jeune
Aesthetics,借助公司技术平台的能力,该子公司专注于医美领域的产品开发,向皮肤细胞递送目标蛋白质以对抗皮肤老化。Jeune
Aesthetics的领先产品KB301旨在通过皮内注射给药,递送编码3型胶原蛋白(COL3)的基因COL3A1以刺激皮肤的生物再生,从而对抗皮肤老化或受损迹象,目前正在积极开展1期临床试验。2022年3月,Jeune宣布了PEARL-1试验有效性队列中关于改善(上脸颊、下脸颊以及膝盖皮肤)细纹和皱纹的积极概念验证、安全性和有效性数据。2022年11月,Jeune公布了来自PEARL-1扩展队列的数据,显示在给予高剂量KB301后,效果的持久性长达9个月。2023年4月,Jeune完成了KB301的1期临床试验队列3研究中针对静止状态下的外眦纹(鱼尾纹,LCL)的首例患者给药,受试者将在KB301治疗后随访3个月,研究预计在2023年下半年完成。这项研究完成后,Jeune计划启动KB301针对LCL的2期临床研究。此外,如上图所示,Jeune还有其他几种处于临床前不同开发阶段的医美候选产品。财务状况截至2023年3月底,Krystal
Biotech拥有现金、现金等价物和短期投资共约3.504亿美元,足以支持公司未来至少12个月的运营开支。由于尚未有产品业绩产生,公司自正式运营以来一直处于亏损状态,截至2023年3月31日,累计赤字为3.261亿美元。2022年、2021年和2020年,公司净亏损分别为1.4亿美元、6960万美元和3220万美元。2023年第一季度净亏损4530万美元。不过随着已获批产品销售工作的推进,以及潜在的对外合作和许可,公司未来或将从产品销售、产品销售特许、里程碑或者其他预付款中获得收入。2022全年,公司研发费用为4246万美元,一般与管理费用为7774万美元,与上一年度相比均有增长。2023年第一季度,公司研发费用为1229万美元,一般与管理费用为2404万美元,与去年同期相比均有增长。其中的诉讼和解费用来源于早前Krystal
Biotech与基因治疗公司PeriphaGen的商业秘密纠纷(PeriphaGen使用HSV-1载体用于神经系统疾病等)。2020年5月,PeriphaGen起诉Krystal
Biotech违反合同和盗用商业秘密,主要涉及Krystal的基因递送载体骨架和STAR-D技术平台。2020年6月,Krystal否认指控,提起反诉,并指控PeriphaGen违约。2022年4月,两家公司签订最终和解协议,Krystal向PeriphaGen支付2500万美元的预付款,包括解除PeriphaGen公司商业秘密诉讼中的所有索赔;收购PeriphaGen的生物材料和皮肤科资产;PeriphaGen授予Krystal在皮肤科领域的应用许可。在美国FDA批准Krystal首款产品之后,公司向PeriphaGen支付额外的1250万美元;在累计销售总额分别达到1亿美元、2亿美元和3亿美元时,再向PeriphaGen支付3次额外的1250万美元里程碑付款。未来计划对于未来机会,Krystal
Biotech认为公司专有基因治疗递送载体的重复给药能力,以及较大的有效荷载能力,能够实现多个基因和其他效应物的递送,从而治疗非单基因皮肤病,如牛皮癣和特应性皮炎,以及不一定是遗传基因缺陷疾病的疗法开发,如慢性伤口。例如,作为概念验证,Krystal
Biotech已经生成了一个设计用于递送抗炎抗体的载体库。其中有一款载体已在特应性皮炎的动物模型中进行了评估,且证实了抗体的表达并观察到疗效。若能够成功开发出治疗这些非罕见疾病的候选药物,Krystal
Biotech计划寻求对外合作以实现候选产品的进一步开发和潜在的商业化。此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场参考:NMPA/CDE;药融云数据www.pharnexcloud.comFDA/EMA/PMDA;相关公司公开披露(正文图片均来自企业官方,除非另有说明);https://www.krystalbio.com/;https://ir.krystalbio.com/news-releases/news-release-details/krystal-biotech-receives-fda-approval-first-ever-redosable-gene;https://www.nature.com/articles/s41591-022-01737-y;https://www.nejm.org/doi/full/10.1056/NEJMoa2206663;https://www.fiercebiotech.com/special-reports/top-10-ma-targets-biotech-2023;https://www.smartbusinessdealmakers.com/articles/topic/krystal-biotech-krish-krishnan-startup-ipo/;等等。「 会议推荐」点分享点点赞点在看
孤儿药基因疗法上市批准
100 项与 Avoro Capital Advisors 相关的药物交易
登录后查看更多信息
100 项与 Avoro Capital Advisors 相关的转化医学
登录后查看更多信息
管线布局
2024年05月06日管线快照
无数据报导
登录后保持更新
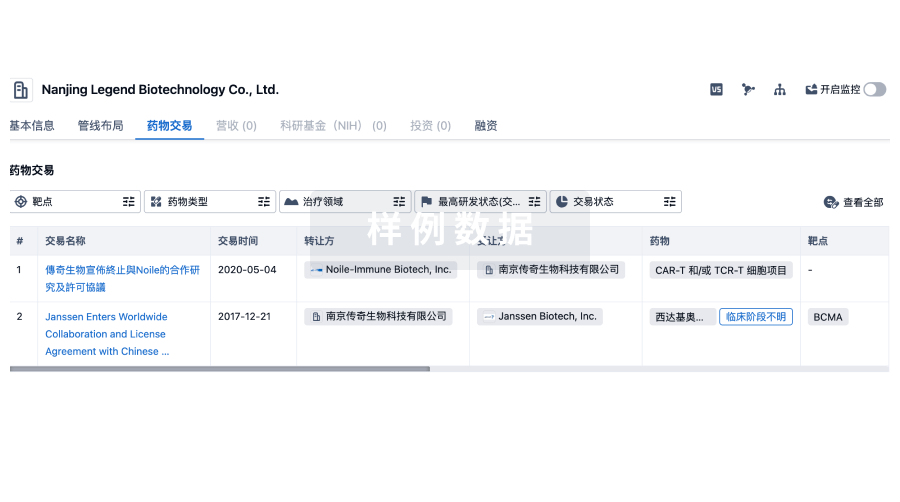
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
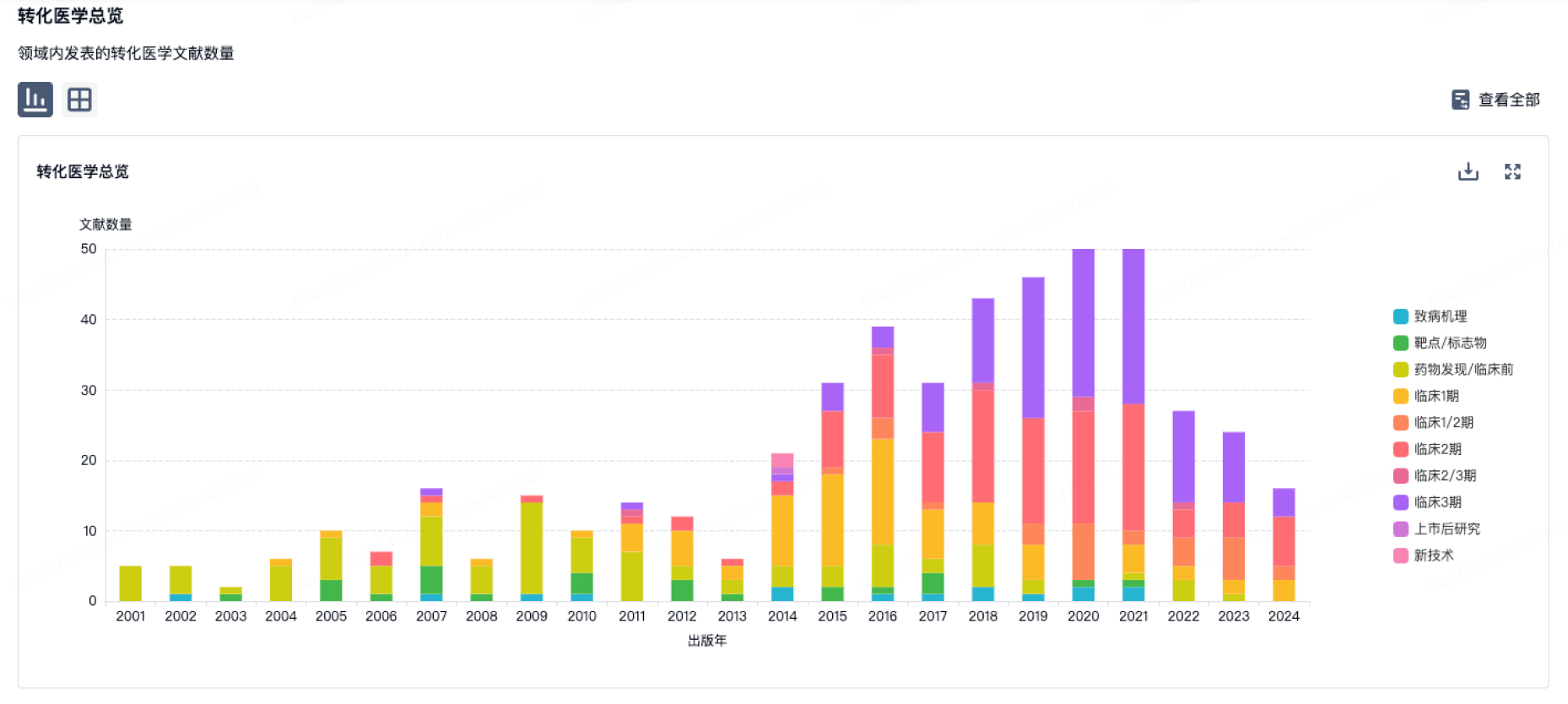
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
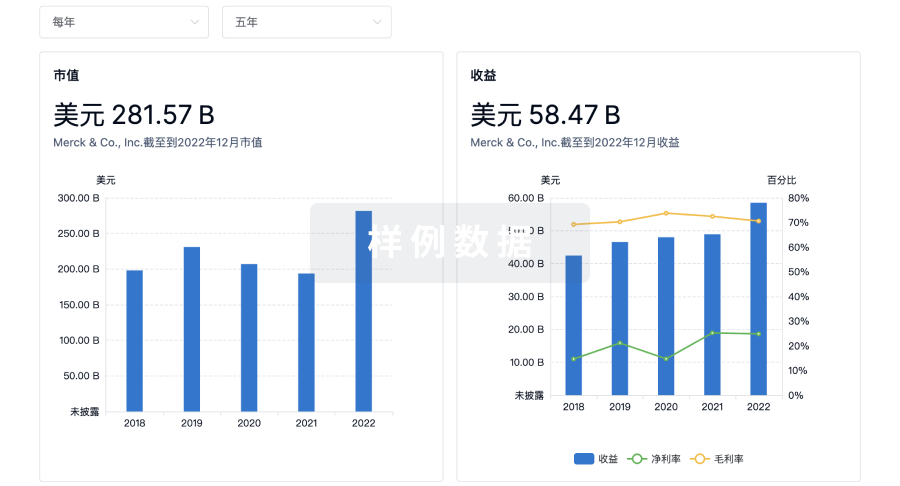
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
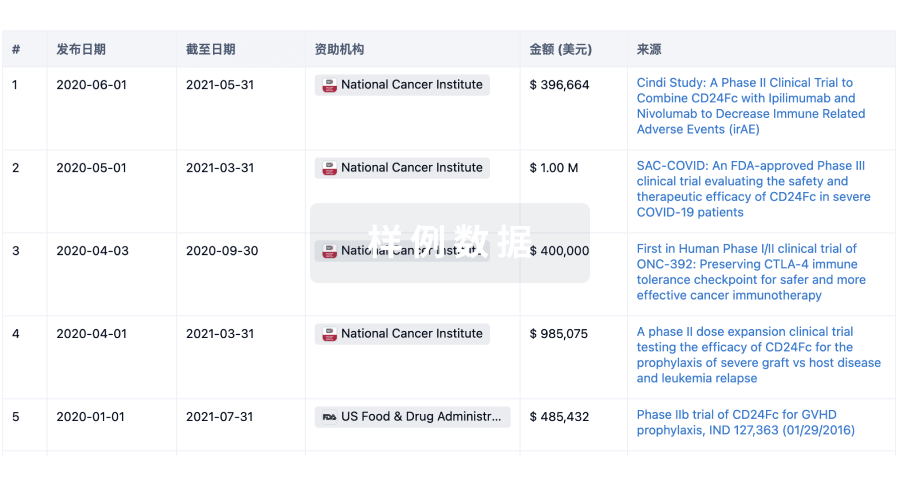
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用