更新于:2023-07-15

f2 Clinical Ltd.
更新于:2023-07-15
概览
关联
100 项与 f2 Clinical Ltd. 相关的临床结果
登录后查看更多信息
0 项与 f2 Clinical Ltd. 相关的专利(医药)
登录后查看更多信息
9
项与 f2 Clinical Ltd. 相关的新闻(医药)2023-05-28
·医药观澜
▎药明康德内容团队报道本周,全球细胞和基因疗法(CGT)领域迎来系列进展。例如:诺和诺德、诺华等就基因治疗产品达成新合作;斯微生物等新锐获得新一轮融资,其中多家融资金额超1亿美元;BCMA CAR-T疗法、siRNA、基因疗法等创新产品研发取得新进展等。本文将节选其中部分重要进展做简单介绍,仅供读者参阅。图片来源:123RF———✦授权合作✦———诺和诺德(Novo Nordisk)宣布与Life Edit Therapeutics建立多靶点合作,发现和开发治疗罕见病和心脏代谢疾病的基因编辑疗法。Life Edit公司将获得现金预付款,并有资格获得7个开发项目中每一个项目2.5~3.35亿美元的里程碑付款,及全球净销售额的分级特许权使用费。诺和诺德将利用Life Edit公司的基因编辑技术以精确编辑基因组,从而开发治疗罕见遗传疾病、心脏代谢疾病等的创新疗法。另外,诺和诺德将对Life Edit母公司ElevateBio进行股权投资,作为后者4.01亿美元D轮融资的一部分。AVROBIO公司宣布,以8750万美元向诺华(Novartis)出售其用于治疗膀胱炎的在研造血干细胞(HSC)基因治疗项目。AVROBIO公司将保留HSC基因疗法组合针对戈谢病1型和3型、亨特综合征和庞贝病的全部权利。AVROBIO公司的愿景是为全球患者带来个体化的基因治疗,通过将受影响基因的功能拷贝引入患者自身的造血干细胞来靶向遗传病的根本原因,从而在中枢神经系统等全身持久表达治疗蛋白。图片来源:123RF———✦新锐融资✦———斯微生物(StemiRNA)宣布完成数亿元的Pre-D轮融资,融资所得主要用于加快肿瘤治疗疫苗及传染病疫苗管线的开发,并持续布局人工智能算法及mRNA序列设计优化等技术。斯微生物成立于2016年,致力于研究开发基于mRNA技术的肿瘤治疗和传染病预防疫苗管线。目前,该公司个性化肿瘤疫苗管线已经在澳洲开展1期临床,并已同步在中国多家医院开展IIT研究;编码细胞因子IL-12的非复制mRNA瘤内注射剂SW0715已在中国递交新药临床试验(IND)申请。ReNAgade Therapeutics宣布完成由MPM BioImpact和F2 Ventures领投的3亿美元A轮融资。ReNAgade是一家专注开发RNA疗法的公司,旨在通过使RNA药物能够递送到以前无法接触的人体组织和细胞,从而解决RNA治疗的主要限制。根据行业媒体STAT报道,ReNAgade公司的管线已完成体外与小鼠实验,并有接近10项非人灵长类的临床前实验正在进行中。Krystal Biotech宣布完成由Avoro Capital Advisors和Redmile Group领投的1.6亿美元私募股权融资。Krystal Biotech是一家专注于为罕见疾病患者开发和商业化基因药物的生物技术公司。今年5月,该公司基因疗法Vyjuvek刚获得美国FDA批准上市,用于治疗营养不良性大疱性表皮松解症。这是一款可重复给药、现货型外用基因疗法,通过基因工程改造的HSV-1载体来进行基因递送。ElevateBio公司宣布完成4.01亿美元D轮融资,所得资金将用于进一步完善该公司的基因编辑、诱导多能干细胞(iPSCs)、RNA等技术平台建设,加速细胞和基因治疗的设计、制造和开发等。ElevateBio是一家致力于开发变革性细胞和基因疗法的生物技术公司。2021年11月,该公司收购了Life Edit Therapeutics公司,囊获其基因编辑技术平台,有潜力对任何基因组序列进行删减、添加和修改。图片来源:123RF———✦新药进展✦———传奇生物宣布,向欧洲药品管理局(EMA)递交了BCMA CAR-T疗法Carvykti(cilta-cel,西达基奥仑赛)的II类变更申请。此次扩大适应症申请基于一项随机的3期CARTITUDE-4研究的数据,该研究评估了既往接受过1-3线治疗后复发且来那度胺耐药的多发性骨髓瘤成人患者的疗效。试验中Carvykti将患者的疾病进展/死亡风险降低了74%,并且总体缓解率、完全缓解率(CR)或更好比率以及总体微小残留病灶(MRD)阴性率显著提高,总生存期呈积极趋势。REGENXBIO公司宣布,FDA授予了其基于腺相关病毒(AAV)的在研一次性基因疗法RGX-121再生医学先进疗法认定(RMAT)。该疗法旨在治疗II型黏多糖贮积症(MPS II)。RGX-121是一种一次性的基因疗法,旨在使用AAV9载体将编码I2S酶的人艾杜糖酸-2-硫酸酯酶(IDS)基因递送至中枢神经系统(CNS)。此前,RGX-121已获得FDA授予的孤儿药资格、罕见儿科疾病认定和快速通道资格。艾码生物(ExoRNA Bio)宣布,其开发的创新药ER2001获FDA授予孤儿药资格,用于治疗亨廷顿舞蹈症(HD)。动物实验证明,ER2001通过利用人体或动物体的自身器官组织作为生物反应器,在体内被“加工”成为活性形式的siRNA,并组装进入“生物反应器”同步产生的中枢神经系统靶向的内源外泌体中,经外泌体分泌“运输”到神经元细胞,降解其中突变亨廷顿蛋白(mHTT)的mRNA,从而产生药效。邦耀生物首席执行官(CEO)郑彪博士在第26届美国基因与细胞治疗学会年会(ASGCT)以口头报告形式公开基因疗法产品BRL-101更新的早期临床研究结果,针对输血依赖型β-地中海贫血。研究共入组6名年龄在5~15岁的患者,临床治疗结果显示,所有患者接受经基因编辑的造血干细胞移植治疗后,红细胞数量和总体胎儿血红蛋白(HbF)水平开始出现显著上升,2/3的患者在2个月内就脱离了输血依赖,HbF达到正常范围。瑞博生物宣布,其研发的用于治疗慢性乙型肝炎病毒(HBV)感染者的RBD1016注射液临床试验申请在欧盟获批,即将启动国际多中心2期临床试验。RBD1016是一款GalNAc-siRNA药物,靶向HBV的X基因,通过RNA干扰机制对HBV的4个转录本均有抑制作用。它可以抑制HBV DNA复制,降低共价闭合环状DNA(cccDNA),并且具有整合DNA来源的乙肝表面抗原(HBsAg)以及其他抗原的能力。除了上述动态,本周细胞和基因疗法领域还有一些其它进展,限于篇幅,本文不再一一介绍。希望该领域迎来更多的新进展和突破,惠及更多患者。本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
临床1期细胞疗法基因疗法引进/卖出免疫疗法
2023-05-26
·生物谷
1、斯微生物顺利完成数亿元Pre-D轮融资近日斯微生物正式完成数亿元的Pre-D轮融资。该笔融资主要用于加快肿瘤治疗疫苗及传染病疫苗管线的开发,并持续布局人工智能算法及mRNA序列设计优化等技术,进一步夯实斯微生物的技术领先优势。(斯微生物)2、4亿美元D轮融资!打造颠覆性基因编辑iPSC平台,累积融资12.46亿美金近日,ElevateBio完成4.01亿美元D轮融资,由AyurMayaCapitalManagement领投,诺和诺德等跟投,是截止至今2023年生物技术领域最大的私募融资。融资所得将进一步改进公司的基因编辑、RNA、蛋白质和诱导多能干细胞等前沿技术平台。除了继续推进优化其技术平台之外,ElevateBio 还将利用此轮融资来提高其制造生产能力,以满足其行业和学术合作伙伴的需求。(风起药界)3、突破RNA治疗限制!3亿美元A轮融资强化默沙东合作使用平台ReNAgade Therapeutics近日宣布完成由MPM BioImpact和F2 Ventures领投的3亿美元A轮融资。ReNAgade是一家专注开发RNA疗法的公司。根据行业媒体STAT报道,ReNAgade的管线已完成体外与小鼠实验,并有接近10项非人灵长类的临床前实验正在进行中。(腾讯新闻)4、大睿生物:自研首款siRNA管线产品成功提交澳洲I期临床实验申请大睿生物,一家领先开创的核酸创新药平台公司,今日宣布在澳洲成功提交了第一款自主研发的潜在最佳 (best-in-class) siRNA管线产品PCSK9抑制剂RN0191的I期临床实验申请,该产品针对高胆固醇血症人群和动脉粥样硬化人群。这项自主研发产品的新进展标志着大睿生物实现了从药物早研阶段进入临床阶段的里程碑式的跨越。大睿生物在公司成立不到2年,临床前候选化合物(PCC)确立后进入临床前研究不到10个月取得这一突破性进展彰显了公司差异化平台创新的能力和高效的执行力。后续临床试验的批准以及推进将助力大睿生物实现以创新核酸药物惠及全球患者的愿景。(细胞基因治疗前沿)5、马斯克脑机接口公司称已获人体试验批准据 arstechnica 报道,5 月 26 日,埃隆·马斯克(Elon Musk)的脑机接口公司 Neuralink 在推特上宣布,美国食品药品监督管理局(FDA)已批准其开展首例人体试验。目前,Neuralink 尚未发布有关招募试验对象和试验内容细节的信息。2022 年 11 月,马斯克曾在一次演讲中表示将在 2023 年春天获得 FDA 的人体试验批准,并将在 6 个月内开始人体临床试验。然而今年 3 月,FDA 一度因安全风险过大拒绝了 Neuralink 的申请,并概述了该公司在进行人体试验之前必须解决的数十个问题。(arstechnica)
siRNA疫苗信使RNA临床1期
2023-05-26
·生物谷
今年以来,多家专注于 RNA 治疗的公司获得大量资金支持,除 ReNAgade 外,Orbital Therapeutics 在今年 4 月的 A 轮融资中筹集了 2.7 亿美元,以帮助推进其 RN
当地时间 5 月 23 日,RNA 治疗领域公司 ReNAgade Therapeutics(以下简称 ReNAgade) 宣布获得由 MPM BioImpact 和 F2 Ventures 领投的 3 亿美元 A 轮融资,从而在 RNA 技术领域崭露头角。公司方面还表示,计划在未来 12 个月内推出其产品线。
ReNAgade 由 MPM BioImpact 创立于 2020 年,总部位于美国剑桥,目前拥有大约 100 名员工。公司的目标是,凭借其递送系统将 RNA 药物递送到体内以前无法进入的组织和细胞,来解决 RNA 疗法的主要局限性——RNA 药物目前受到组织靶向递送和缺乏综合治疗平台的限制。
ReNAgade 结合新型 RNA 递送平台与综合 RNA 平台,建立了一个全面的互补平台,将其专有的递送技术(包括新型脂质纳米颗粒(LNP))与广泛的编码、编辑和基因插入工具结合在一个全 RNA 系统中。可进行编码、编辑和基因插入,以生产新药物。
(来源:ReNAgade官网)
据了解,ReNAgade 有两位高管来自 Moderna。
首席科学官 Peter Smith 博士在 2017 年加入生物制药公司 Alnylam Pharmaceuticals 之前,曾在 Moderna 担任首席早期开发官和高级副总裁兼非临床研发主管;首席运营官 Ciaran Lawlor 博士在波士顿咨询公司工作之前是 Moderna 的首席科学家。
(来源:ReNAgade官网)
董事长兼首席执行官 Amit Munshi 拥有 30 多年领先生物技术公司经验,此前曾担任 Arena Pharmaceuticals 的首席执行官,后来 Arena 被辉瑞公司以 67 亿美元的价格收购。
Amit D. Munshi 透露,“为了开发具有治疗身体任何部位、任何疾病潜力的 RNA 药物,ReNAgade 组建了一支世界级的多学科团队,该团队共取得过 25 项 NDA(包括 4 项 RNA 药物)和 200 项 IND,并且一直是 RNA 药物领域的先驱。”
(来源:ReNAgade 官网)
在公司的拓展方面,ReNAgade 已经与 Orna Therapeutics 成立了一家合资企业,将 ReNAgade 的 RNA 递送技术与 Orna 的环状 RNA 技术相结合。
根据资料,Orna 在 2022 年 8 月完成了 2.21 亿美元的 B 轮融资,并与美国默克公司(NYSE: MRK)签署了一项协议,在多个治疗项目中进行合作,其中包括在 Orna/ReNAgade JV 下开发的技术。与默沙东的交易可能会让 Orna 获得总计 35 亿美元的里程碑付款。
今年以来,多家专注于 RNA 治疗的公司获得大量资金支持,除 ReNAgade 外,Orbital Therapeutics 在今年 4 月的 A 轮融资中筹集了 2.7 亿美元,以帮助推进其 RNA 疗法产品组合。此外,COVID-19 以外的潜在 RNA 疫苗也受到诸多关注,例如 BioNTech 的胰腺癌 mRNA 疫苗,其已获得积极的早期数据。

信使RNA并购核酸药物siRNA临床申请
100 项与 f2 Clinical Ltd. 相关的药物交易
登录后查看更多信息
100 项与 f2 Clinical Ltd. 相关的转化医学
登录后查看更多信息
管线布局
2024年05月06日管线快照
无数据报导
登录后保持更新
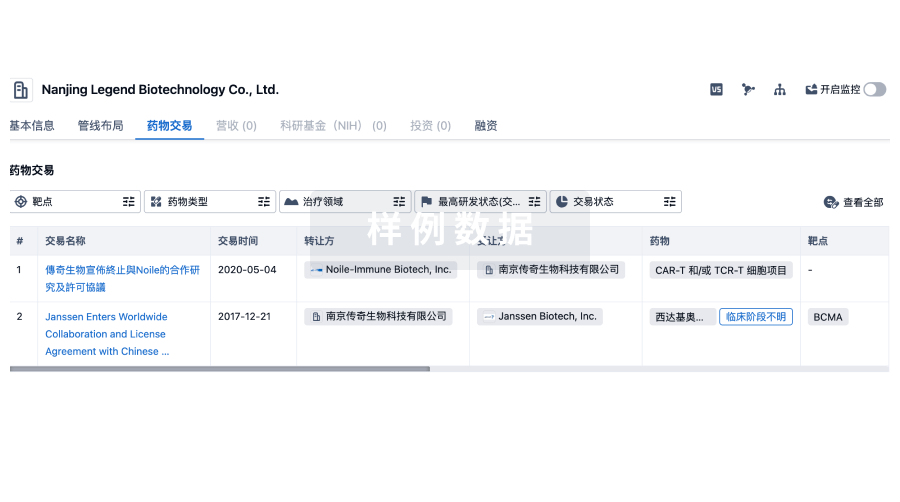
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
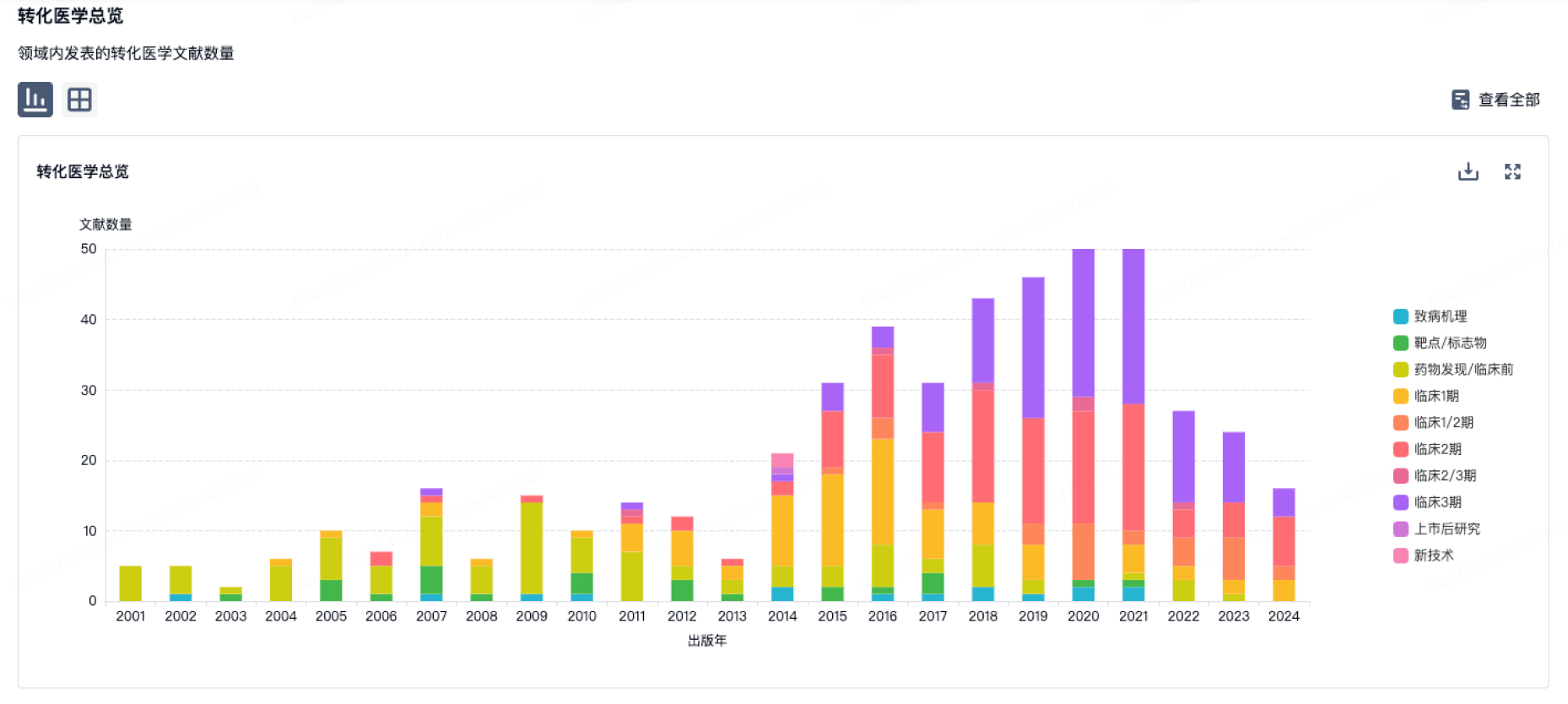
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
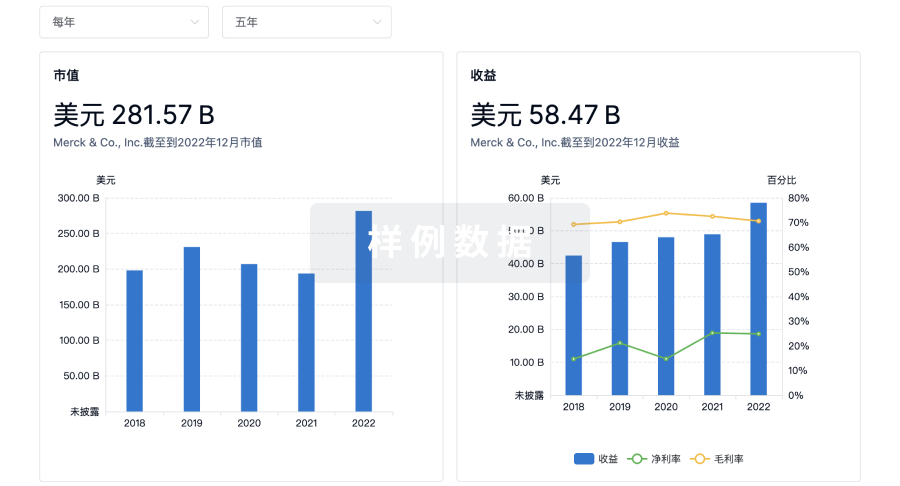
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
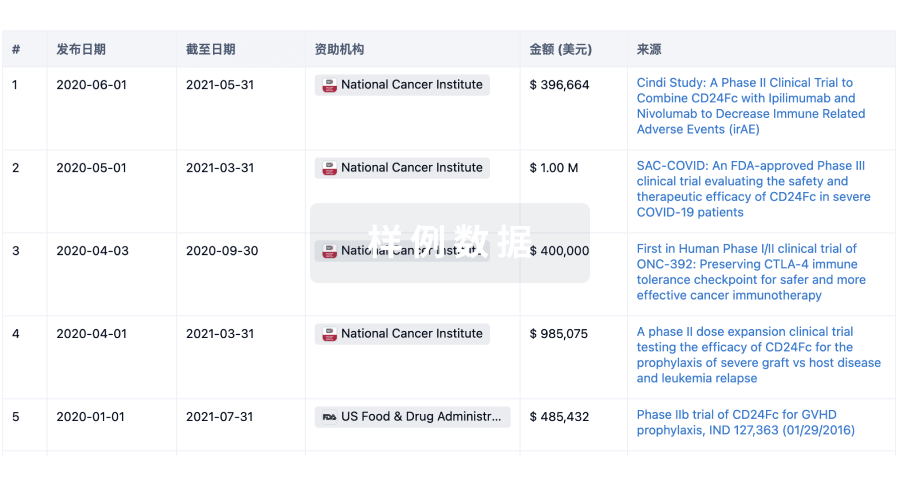
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
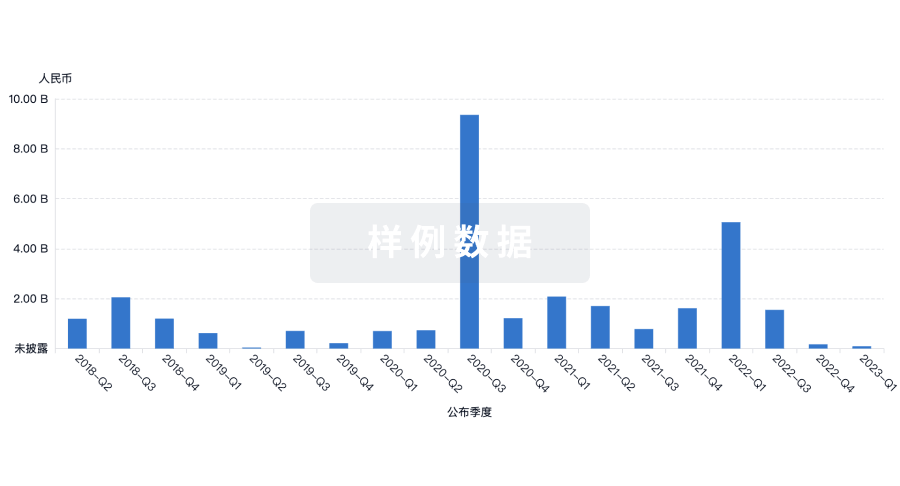
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
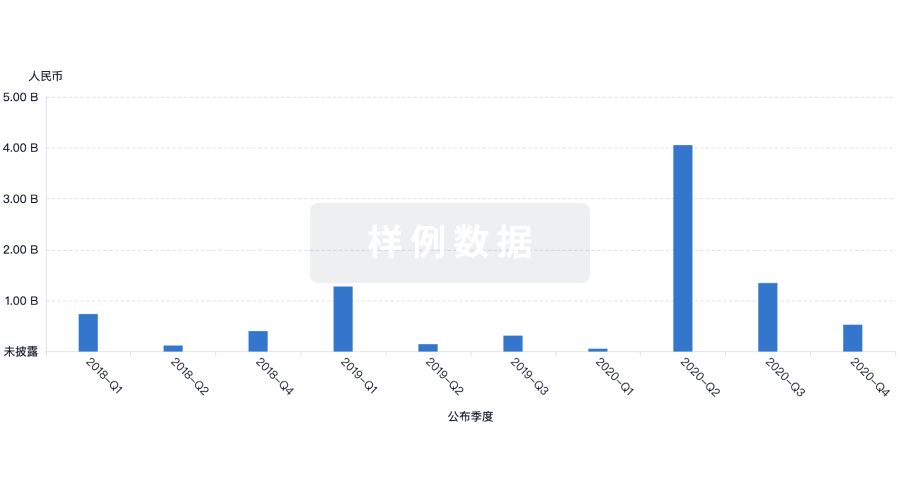
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用