预约演示
更新于:2026-03-26
AR-v7 x NONO
更新于:2026-03-26
关联
100 项与 AR-v7 x NONO 相关的临床结果
登录后查看更多信息
100 项与 AR-v7 x NONO 相关的转化医学
登录后查看更多信息
0 项与 AR-v7 x NONO 相关的专利(医药)
登录后查看更多信息
1
项与 AR-v7 x NONO 相关的新闻(医药)2023-04-03
mRNA转录后需要经过剪接、转运和修饰,才能翻译成蛋白质,而这些过程都受RNA结合蛋白(RNA-binding proteins, RBPs)的作用控制。RBPs构成了人类蛋白质组的很大一部分,与许多人类疾病有关,并监督编码关键致癌蛋白的mRNA的成熟和质量控制。尽管RBP在人类生理和疾病中发挥着重要作用,但在化学探针和药物发现方面,其研究尚不充分。RBPs小分子调节剂的发现面临的一些挑战,包括结合位点缺乏和功能检测方法有限。许多RBP在细胞中也作为大型动态复合物的一部分发挥作用,这在重组的生化系统中很难研究。识别RBP的化学探针可以抑制多种疾病相关蛋白的表达和活性,包括致癌转录因子,如雄激素受体(androgen receptor, AR)——前列腺癌的主要驱动因素。前列腺癌的一线治疗包括AR拮抗剂,如恩杂鲁胺,但对这些药物的耐药性经常出现,当前临床评价的AR小分子降解物(例如,蛋白水解靶向嵌合体),可能也无法治疗雄激素配体结合位点发生突变或产生截短的剪接变体的癌症,如AR- V7,亟需新的多种靶向AR和AR- V7的替代方法。 近来,美国Scripps研究所的研究人员通过半胱氨酸定向亲电小分子的聚焦筛选,发现α-氯乙酰胺化合物及其类似物可选择性地抑制全长AR (AR- FL)和AR- V7剪接变体的转录和蛋白表达。进一步,基于活性的蛋白质分析(activity-based
protein profiling, ABPP)识别了这些化合物的靶标为果蝇行为和人类剪接(Drosophilabehavior and human splicing, DBHS)家族RBP NONO,且与NONO中的半胱氨酸(C145)发生立体选择性和位点特异性反应;这些化合物以NONO 依赖性方式调节RNA稳态和信号转导富集的基因网络的表达和癌细胞的生长,为RBP NONO作为前列腺新靶标和干预分子发现提供了理论基础。首先,研究人员评估了内部收集的约500个含有半胱氨酸定向反应基团的亲电化合物(例如α-氯乙酰酰胺和丙烯酰胺)对22Rv1人类前列腺癌细胞系中编码AR-FL和AR-V7转录本的影响。在化合物处理后6小时,他们测量了AR- FL和AR- v7 mRNA的表达,并通过高内涵成像测量处理24小时后AR和AR- V7蛋白的总含量,最终发现了一个命中化合物B21可以抑制了22Rv1细胞中的AR-FL和AR-V7转录和蛋白表达,且没有引起实质性的细胞毒性。B21在治疗后4-6小时内最大限度地抑制AR- FL和AR- V7转录,而AR蛋白的降低速度则较慢,表明化合物作用的直接模式涉及降低AR mRNA的含量(其对AR- FL和AR- V7 的IC50 分别为 8.4µM和19µM)。此外,一些化合物(2-5)及其对映体对活性具有较大差异,说明了AR转录抑制的严格构效关系,其中(R)-10和(R)-11降低AR-FL和AR- V7转录的表达,IC50值为2.7-5.5µM,而(S)-10和(S)-11则无活性,通过结构性质关系分析,最终得到活性分子(R)-SKBG-1。研究人员通过化学蛋白质组学来识别活性化合物的蛋白质靶点:用活性(R)-SKBG-1及非活性对照(6-9,(S)-10和(S)-SKBG-1)化合物处理22Rv1细胞1小时,并通过半胱氨酸定向的ABPP分析其蛋白质组。结果表明,只有少量的半胱氨酸(~10个)参与所有活性化合物的作用,并且其中大多数也参与一种或多种非活性对照化合物。只有NONO的C145参与所有活性化合物的作用,但不参与非活性对照化。NONO(或p54nrb)是RNA和DNA结合蛋白的DBHS家族的成员,该家族还包括其同源蛋白PSPC1和SFPQ(或PSF)。DBHS蛋白作为异二聚体和同二聚体参与基因调控的不同步骤,包括DNA解旋、转录以及mRNA剪接、转运和质量控制。NONO与PSPC1和SFPQ有大约40-50%的序列相同,但C145是NONO所特有的,这表明活性化合物应该选择性地与DBHS蛋白中的NONO结合。NONO - PSPC1异二聚体的晶体结构进一步揭示了C145位于NONO的两个RNA识别基序(RNA recognition motifs, RRMs)之间的铰链区域,靠近对RNA结合重要的残基。为了确定NONO是否是介导活性分子抑制AR的主要功能靶标,研究人员使用 CRISPR-Cas9 技术生成了NONO阻断的22Rv1细胞。与 sgControl 细胞相比,含有靶向 NONO 的sgRNA(sgNONO)的细胞AR-FL 或 AR-V7 mRNA水平没有显著改变,而且对(R)-SKBG-1的抑制作用产生抗性。(R)-SKBG-1抑制AR表达的能力在表达NONO WT的 sgNONO细胞中得到恢复,但在表达NONO C145S突变体的细胞中没有恢复。因而,上述数据表明(R)-SKBG-1通过一种依赖于NONO的C145共价修饰机制促进AR抑制,并且这种效应被NONO基因破坏所阻断。接下来,他们检测了NONO在癌细胞中转录组学和蛋白质组学的效应。RNA测序(RNA-seq)显示,大部分由(R)-SKBG-1特异性引起的转录组改变需要NONO在22Rv1细胞中的存在。蛋白质组学结果明确了AR等几种蛋白质在(R)-SKBG-1处理的sgControl细胞中的表达下降。通路分析显示,激素信号、RNA合成和GTPase信号转导通路在(R)-SKBG-1处理的22Rv1细胞中富集,包括乳腺癌依赖蛋白TRPS1和Wnt -β-catenin通路成分AFF3等。这些结果强调了NONO再重构癌细胞中的调控潜力。为了更好地理解NONO的抑制方式,研究人员在表达内源性NONO WT的22Rv1细胞中异位表达重组NONO WT或NONO C145S。这些实验表明,重组NONO WT和NONO C145S可以双向调控(R)-SKBG-1的AR表达、全局转录组和生长效应,其中NONO WT的表达增强了(R)-SKBG-1效应,NONO C145S的表达抑制了化合物活性。NONO C145S对(R)-SKBG-1作用的部分阻断表明,虽然共价配体的活性需要NONO,但它们的药理作用并不完全占主导地位,至少可以通过共表达配体不敏感的NONO突变体来部分挽救。在sgNONO细胞中,PSPC1和SFPQ的mRNA和蛋白质水平增加。此外,与DMSO或(S)-SKBG-1处理的sgControl细胞相比,(R)-SKBG-1处理的sgControl细胞中PSPC1和SFPQ也表现出强烈的升高。这表明NONO的遗传或急性化学扰动会导致PSPC1和SFPQ表达增加。他们还发现NONO在相分离的亚核体paraspeckles中发挥作用,该结构由DBHS蛋白与长链非编码 RNA的结合而组织起来,并且通过特定mRNA的核保留来调节基因表达。免疫荧光研究显示,NONO可以被诱导形成大亚核灶,并持续强化至24小时。Meta基因分析表明,(R)-SKBG-1通过增强与RNA的第一个外显子和第一个内含子5 '端相互作用,影响了NONO在这些转录本中的位置偏好。深度RNA-seq和rMATs分析显示NONO配体也干扰mRNA剪接,如在(R)-SKBG-1处理的sgControl细胞中量化了更多的包含和排除外显子的事件。因此,由(R)-SKBG-1引起的一些剪接变化可能反映了RBP/剪接/转录网络的显著重构。综上,利用筛选机制新颖的抑制全长AR (AR- FL)和AR- V7剪接变体转录/蛋白表达的化学探针(R)-SKBG-1,可选择性地与RBP NONO发生位点特异性反应,并通过一种崭新机制来重塑癌细胞的转录组和蛋白质组,包括诱导NONO在核灶和未成熟转录本的5 '端积聚等。未来,(R)-SKGB-1还可进一步作为作为一种多功能的化学探针来研究NONO在不同生物环境中的功能。参考文献:Stefan G Kathman, Seong Joo Koo, Garrett L Lindsey, Hsuan-Lin Her, Steven M Blue, Haoxin Li , Steffen Jaensch, Jarrett R Remsberg, Kay Ahn, Gene W Yeo, Brahma Ghosh, Benjamin F Cravatt. Remodeling oncogenic transcriptomes by small molecules targeting NONO. Nat Chem Biol . 2023 Mar 2. doi: 10.1038/s41589-023-01270-0.识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场
信使RNA
分析
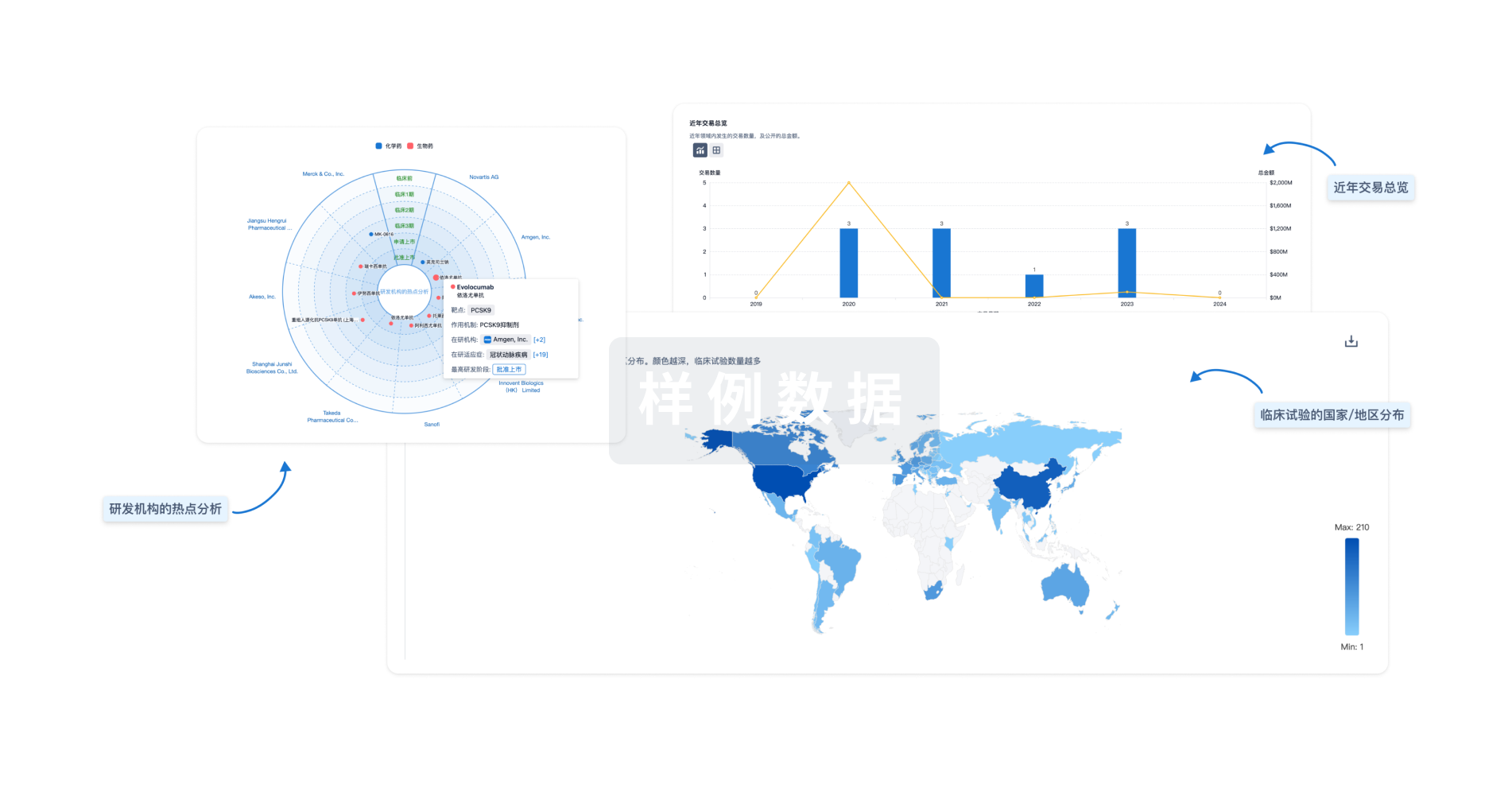
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用