预约演示
更新于:2026-02-06
ER-2001
更新于:2026-02-06
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)临床1/2期 |
特殊审评孤儿药 (美国) |
登录后查看时间轴
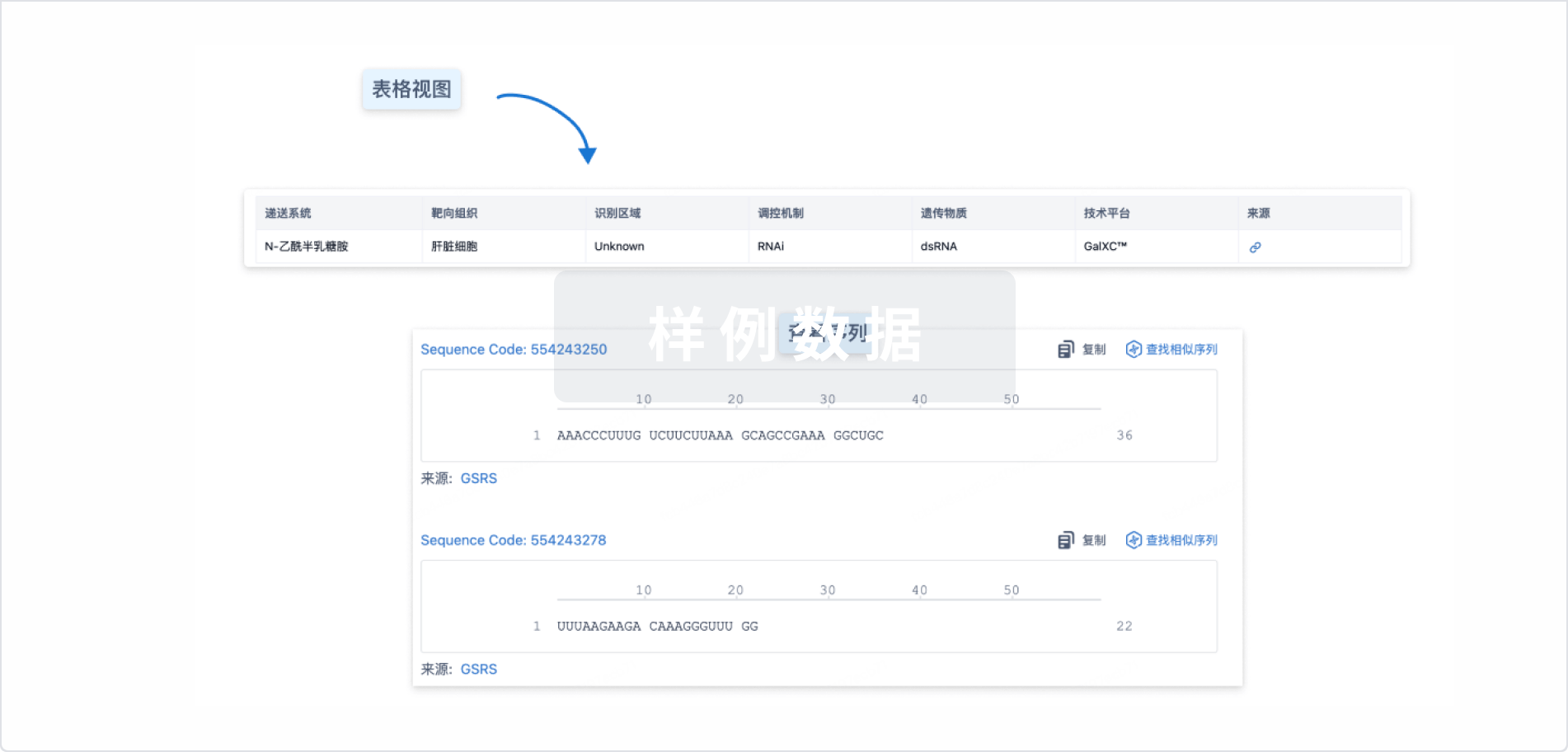
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
3
项与 ER-2001 相关的临床试验NCT07339514
A Randomized, Double-Blind, Placebo-Controlled Phase I Clinical Study of ER2001 Intravenous Injection in Adults With Early Manifest Huntington's Disease.
This is a dose escalation and expansion clinical study to evaluate the safety, tolerability, PK profile and preliminary efficacy of ER2001 Injection vs. placebo in subjects with definitive diagnosis of early manifest HD.
The study consists of a dose escalation phase (Part A, an open-label without placebo, which will be carried out firstly) and a dose expansion phase (Part B,randomized, blinded, placebo-controlled), both of which include a screening period (4 week prior to the first administration), a treatment period (for 6 consecutive weeks, once a week [QW] for 6 weeks), and a safety follow-up period (24 weeks).
The study consists of a dose escalation phase (Part A, an open-label without placebo, which will be carried out firstly) and a dose expansion phase (Part B,randomized, blinded, placebo-controlled), both of which include a screening period (4 week prior to the first administration), a treatment period (for 6 consecutive weeks, once a week [QW] for 6 weeks), and a safety follow-up period (24 weeks).
开始日期2025-02-11 |
申办/合作机构 |
NCT07344519
Open-Label, Dose Escalation Early Phase 1 Study of ER2001 Intravenous Injection Repetitive Treatment in Adults With Early Manifest Huntington's Disease.
This is an open label, dose escalation clinic trial to evaluate safety, tolerability and pharmacokinetics with ER2001 Intravenous Injection repetitive treatment in Huntington's Disease patients who Completed Study ER2001-001(NCT06024265). Furthermore, pharmacodynamics in particular target engagement, and clinical signs of efficacy will be assessed. This study will evaluate increasing doses of ER2001 in sequential cohorts. ER2001 was escalated over 3 dose levels . The planned duration of this additional treatment is 6 weeks for one course.
开始日期2024-06-25 |
申办/合作机构 |
NCT06024265
An Open-Label, Dose Escalation Early Phase 1 Study of ER2001 Intravenous Injection in Adults With Early Manifest Huntington's Disease
This is an open label, dose escalation clinic trial of ER2001 intravenous injection to evaluate safety, tolerability and pharmacokinetics of ascending single and multiple doses of intravenously administered ER2001 in patients with early manifest Huntington's Disease. Furthermore, pharmacodynamics in particular target engagement, and early clinical signs of efficacy will be assessed. This study will evaluate increasing doses of ER2001 in sequential cohorts. ER2001 was escalated over 4 dose levels . The planned duration of this treatment is 14 weeks.
开始日期2023-04-04 |
申办/合作机构 |
100 项与 ER-2001 相关的临床结果
登录后查看更多信息
100 项与 ER-2001 相关的转化医学
登录后查看更多信息
100 项与 ER-2001 相关的专利(医药)
登录后查看更多信息
28
项与 ER-2001 相关的新闻(医药)2026-02-04
上次讲到中国核酸药在世界范围内的竞争状态(中国核酸力量,在跟随中寻找差异化),今天盘一盘国内企业“内斗”情况。
继小分子和抗体药物之后,核酸药物(尤其是小核酸药物)正成为生物医药的第三大核心支柱。基于最新的全球及国内在研管线数据,中国企业在siRNA领域已形成规模化的研发集群。从PCSK9、AGT等“红海”靶点的激烈厮杀,到中枢神经、罕见病等“蓝海”赛道的差异化布局,国内Biotech正通过自主研发与国际合作双轮驱动,重塑全球竞争版图。国内新兴Biotech与传统大药企在核酸赛道上你争我夺,到底有哪些差异化的布局与创新?第一部分:国内头部管线全景速览
基于整理数据,国内第一梯队在研小核酸药物主要集中在心血管代谢、肝脏疾病及肾脏疾病等领域。以下为代表性企业管线一览表:
公司名称
核心靶点/药物
代表适应症
最高阶段
核心亮点瑞博生物
PCSK9 (SR043)
高脂血症
II期
管线最丰富,与齐鲁合作,覆盖心肾代谢多靶点圣因生物
PCSK9 (SGB-3403)
高脂血症
I期
进度神速,与信达合作,覆盖PCSK9/INHBE/C3等舶望制药
AGT (BW-00163)
高血压
II期
诺华重金合作,AGT/PKK/CFB多靶点并进维亚臻生物
ANGPTL3 (VSA003)
家族性高胆固醇血症
III期
国内该靶点进度领先,与Arrowhead合作石药集团
PCSK9 (SYH2053)
高脂血症
II期
传统药企转型,临床开发能力强劲信立泰
AGT (GW906)
高血压
II期
心血管领域优势明显,与国为合作必贝特 (BEBT)
PCSK9+AGT (BEBT-701)
高血压/高血脂
申报临床差异化双靶点
,兼顾罕见病(TMPRSS6)圣诺医药
TGF-β1/COX-2 (STP707)
肿瘤/医美
I期
独特的PNP递送平台,非肝靶向差异化中美瑞康
SOD1 (RAG-17)
肌萎缩侧索硬化症
II期
罕见神经病赛道领先,具备肝外递送潜力靖因药业
Factor XI (SRSD107)
抗凝
II期
与CRISPR Therapeutics合作第二部分:多维度竞争格局深度解析1. 靶点竞争:从“红海厮杀”到“蓝海突围”
红海战场:心血管代谢(极度内卷)在PCSK9(降脂)和AGT(降压)这两个赛道,国内玩家已超过10家,竞争烈度堪比PD-1。PCSK9赛道
:国际巨头Alnylam的英克司兰已上市,国内瑞博、圣因、石药、鼎新等企业均已推进至II期。未来胜负手在于给药频率的优化、联合疗法的潜力以及国产化成本优势。AGT赛道
:舶望制药与诺华合作的BW-00163、信立泰的GW906、恒瑞的HRS-9563等均已进入II期。由于该靶点市场空间巨大,即便竞争者众多,各家仍有通过细分人群(如难治性高血压)突围的机会。
蓝海高地:罕见病与中枢神经(高壁垒)相比心血管赛道,罕见遗传病领域玩家较少,但技术门槛极高,是建立护城河的关键。神经退行性疾病
:中美瑞康针对ALS的RAG-17已进入II期,是国内该领域的领跑者;艾码生物针对亨廷顿氏病的ER2001也进入了I/II期,暗示其具备跨越血脑屏障的递送技术。罕见血液病
:必贝特针对真性红细胞增多症的BEBT-507(靶点TMPRSS6)处于I期。国内该靶点布局极少,竞争格局良好,一旦成功将享有市场独占期。2. 适应症赛道:聚焦常见慢性病,探索医美新场景常见病为主流
:超过60%的国内管线集中在心血管、代谢(NASH)、乙肝和肾脏疾病。这是患者基数最大的市场,也是各大药企必争之地。医美等新场景
:圣诺医药与香雪制药合作的“科特拉尼”布局了瘢痕、脂肪填充等医美适应症。siRNA在局部给药(如瘢痕部位)的应用,避开了系统性给药的递送难题,开辟了商业化新路径。3. 技术平台:GalNAc主流与肝外递送的探索主流GalNAc肝靶向
:瑞博、圣因、石药等绝大多数企业均采用成熟的GalNAc偶联技术,实现了肝脏的长效靶向。这是目前siRNA药物实现商业化的“金标准”。肝外递送的突破PNP平台
(圣诺医药):多肽纳米颗粒,用于肿瘤局部给药,具备差异化优势。CNS递送
(中美瑞康、艾码生物):针对中枢神经系统疾病,这是siRNA领域的“圣杯”,技术壁垒极高。多肽偶联
必贝特:BEBT-730项目涉及“多肽偶联药物;siRNA疗法”,表明必贝特正在探索多肽偶联递送技术。4. 商业化与合作:License-out验证平台价值
国内企业通过与MNC或国内Big Pharma合作,验证了自身平台价值。国际MNC合作
:舶望(诺华)、瑞博(BI)、靖因(CRISPR Therapeutics)等案例显示,国内头部企业的技术已具备全球竞争力。国内Big Pharma合作
:瑞博(齐鲁)、信达(圣因)、信立泰(国为)等合作,则是为了借力国内强大的临床开发和销售网络,实现产品快速商业化落地。
第三部分:企业竞争梯队与潜力评估
综合管线宽度、临床进度、技术独特性及合作资源,国内企业可划分为以下梯队:
梯队
代表企业
核心特征
潜力评估第一梯队:领跑者
瑞博生物、圣因生物、舶望制药
管线广度大,II/III期项目多,国际/国内合作丰富
最有可能成为“中国Alnylam”第二梯队:强劲挑战者
维亚臻生物、石药集团、信立泰、恒瑞医药
特定靶点进度领先(如维亚臻ANGPTL3),或依托传统药企临床开发优势
在细分赛道有强竞争力第三梯队:特色/黑马必贝特、圣诺医药、中美瑞康、艾码生物技术或适应症极具差异化,虽管线数量不多,但具备独特的战略抓手高赔率选手,一旦双靶点或罕见病管线验证成功,将重塑格局第四部分:未来展望与风险提示1. 行业趋势预判减重siRNA爆发
INHBE靶点(圣因、大睿、舶望等多家布局)将成为继PCSK9/AGT之后的下一个必争之地。从罕见病走向大市场
虽然罕见病管线(如ALS、亨廷顿病)进度领先,但企业仍需努力将这些技术应用到更广阔的患者群体中。联合疗法常态化
单药治疗将面临天花板,与单抗、小分子药物的联合使用将成为提升疗效的关键。
[注:本文仅做信息交流目的,不构成投资建议]
临床2期核酸药物siRNA基因疗法临床3期
2026-01-15
礼新医药中国III期临床试验
2026年1月14日,礼新医药的cafelkibart(CCR8单克隆抗体)正式启动一项针对胃癌、食管腺癌及胃食管交界处癌的中国III期临床试验。该试验编号为CTR20260090。
试验标题为:评估LM-108联合特瑞普利单抗对比紫杉醇,作为二线治疗CCR8阳性的局部晚期或转移性胃癌/胃食管交界处腺癌的有效性和安全性的多中心、随机、开放、平行对照的III期临床研究。
本研究将在全国范围内多个中心同步开展,预计入组400例患者。
试验组治疗方案为特瑞普利单抗联合cafelkibart。
对照组则采用紫杉醇单药治疗。
该临床试验的主要终点是CCR8阳性人群的总生存期(OS),以全面评估新型联合治疗的疗效与安全性。
Merck KGaA启动了一项名为NCT07340827的III期临床试验
2026年1月14日,Merck KGaA启动了一项名为NCT07340827的III期临床试验。
该研究评估促卵泡素α、促黄体激素α、绒促性素α(LH/FSH, 重组;CG, 重组)以及西曲瑞克(GnRHR拮抗剂)在促卵泡生成激素低下、辅助生殖技术(ART)相关不孕不育患者中的应用。
临床试验标题为:A Parallel-group Treatment, 2-arm Study to Compare the Efficacy and Safety of Follitropin Alfa and Lutropin Alfa Fixed Dose Combination Versus hMG for Inducing Follicular Development in Japanese Participants With LH and FSH Deficiency Undergoing ART。
本研究计划纳入333名受试者。 本次临床试验的试验组用药包括:绒促性素α、促卵泡素α+促黄体激素α、西曲瑞克和黄体酮。
对照组用药为:尿促卵泡素+尿促黄体生成素、绒促性素α、西曲瑞克和黄体酮。
箕星药业启动国际多中心Ⅱ期临床试验
2026年1月14日,箕星药业启动了VCT220(GLP-1R激动剂)用于2型糖尿病的国际多中心Ⅱ期临床试验。
该试验的编号为NCT07340320,标题为“A Multicenter, Randomized, Double-Blind, Placebo-Controlled Dose-Finding Study of CX11 Tablets in Patients With Type 2 Diabetes Mellitus”(多中心、随机、双盲、安慰剂对照的CX11片剂治疗2型糖尿病患者的剂量探索研究)。该试验计划在国际多中心区域开展,目标入组人数为240人。
本次临床试验的研究药物为VCT220。
信诺维启动滤泡性淋巴瘤的中国II期临床试验
2026年1月14日,信诺维的依格美妥司他(EZH2抑制剂)正式启动一项针对滤泡性淋巴瘤的中国II期临床试验(试验编号:CTR20260012)。
本次试验旨在评估XNW5004片用于治疗复发或难治性滤泡性淋巴瘤(EZH2野生型)患者的疗效和安全性,计划在中国地区招募65名受试者。
临床试验的试验药品为依格美妥司他。
本研究的主要终点是由独立评审委员会(IRC)评定的客观缓解率(ORR),以全面评估药物的临床疗效。
艾码生物已在中国启动一项针对亨廷顿氏病的I/II期临床试验
2026年1月14日,艾码生物的ER2001(HTT,基因疗法/siRNA疗法)已在中国启动一项针对亨廷顿氏病的I/II期临床试验。
该试验编号为NCT07339514,标题为“A Randomized, Double-Blind, Placebo-Controlled Phase I Clinical Study of ER2001 Intravenous Injection in Adults With Early Manifest Huntington's Disease.”
本次试验的开展地区为中国,计划入组目标患者人数为27名。
试验组所使用的药物为ER2001。
玉森新药启动了一项中国境内的Ⅲ期临床试验
2026年1月14日,玉森新药的“九味止咳”(暂未公布详细成分,属其他类别)启动了一项中国境内的Ⅲ期临床试验,针对急性支气管炎、咳嗽及支气管炎进行研究。
本次临床试验编号为CTR20260094,试验标题为:风叶咳喘平口服液(儿童型)治疗小儿急性支气管炎(风热咳嗽)确证评价其有效性和安全性的随机、双盲、极低剂量对照、多中心Ⅲ期临床试验。
本研究计划在中国多个中心开展,目标入组人数为480例。试验组药品为“九味止咳”。
本次临床试验的主要终点为:咳嗽消失率,旨在科学评价药物在小儿急性支气管炎(风热咳嗽)治疗中的有效性与安全性。
恒瑞医药启动中国境内治疗乳腺癌的III期临床试验
2026年1月14日,恒瑞医药启动了HRS-8080(达尔西利,ER选择性雌激素受体降解剂及CDK4/CDK6抑制剂)在中国境内治疗乳腺癌的III期临床试验(试验编号:CTR20260083)。本研究是一项多中心、开放、随机对照的III期临床试验,旨在评估HRS-8080联合达尔西利与达尔西利联合氟维司群在对内分泌治疗耐药的局部晚期或转移性乳腺癌患者中的有效性及安全性。目标入组人数为912人。
本试验的研究药物设置如下:
试验组:达尔西利和HRS-8080联合应用
对照组:达尔西利与氟维司群联合使用
该研究的主要终点为研究者评估的无进展生存期(PFS)。
勤浩医药完成超3亿元人民币Crossover轮融资
全球新一代抗肿瘤小分子药物的研发企业勤浩医药(苏州)股份有限公司(简称:勤浩医药)宣布已完成超3亿元人民币Crossover轮融资。本轮融资由松禾资本领投,林拙投资、元生创投、广州产投、VIVATEC、薄荷基金、国聚投资等多家机构共同参与。
勤浩医药成立于2014年,位于江苏苏州,作为一家人工智能驱动的Biotech,聚焦于全球领先的靶向抗肿瘤小分子药物开发,公司紧密围绕流程化、模块化的创新药研发体系,全方位的依托AI赋能,基于首创提出的 “AI/Biology-Driven Smart Design” 的药物开发理念,打造了具有自主持续创新能力的组合技术平台:结构生物学平台、新药发现与设计平台、成药性评价平台、转化医学平台,深耕Ras-MAPK信号通路(1.0管线)和合成致死领域(2.0管线),形成了以靶向抗肿瘤品种为核心的产品管线。
兄弟创业AI制药公司,获英伟达两度投资,BMS合作达成里程碑
在AI药物研发公司Terray Therapeutics位于美国加利福尼亚州蒙罗维亚的自动化实验室里,机械臂低鸣运转,将微升量级的液体精准移至工作站,身着实验服、戴着无菌手套与护目镜的科学家们监控着每一台设备的运行。
但真正的“舞台”在纳米尺度:定制硅芯片上的数百万个微孔中,小分子化合物与靶蛋白在溶液中相遇、结合,每一次相互作用都被记录下来,每天生成约50TB原始数据(相当于12000多部电影的数据量)。
在AI驱动的药物发现领域,技术路径正明显分化。一些公司侧重通用计算模型(如蛋白质结构预测)、表型成像或物理建模,而Terray Therapeutics则选择了一条不同的道路:不是先优化算法,而是先构建前所未有的高质量、大规模化学数据集。
艾里奥斯完成逾亿元pre-B轮融资,以自主创新的膜材料技术
中国生物制药工艺用途过滤膜与过滤器领域的领军企业艾里奥斯生物科技(上海)有限公司(以下简称“艾里奥斯”)宣布完成逾亿元人民币的pre-B轮融资,本轮融资由国投创合领投,弘毅投资、倚锋资本及国舜投资跟投,启峰资本、羿水澜山担任财务顾问,这是继2025年 9 月完成龙磐投资、国海创新资本及上海徐汇科创投超亿元的 A++ 轮融资后,艾里奥斯在短时间内获得的又一轮重磅注资。
资金将主要用于公司自研过滤膜的持续研发与产业化、市场拓展等,充分彰显了市场对艾里奥斯在生物制药供应链安全问题上提供解决方案的技术实力、市场地位及发展前景的高度认可。
璧辰医药达成出海合作
2026年1月14日,璧辰医药(ABM Therapeutics)今日宣布,公司已与总部位于波士顿的生物技术公司 Mosaica Medicines就其自主研发的MEK1/2抑制剂ABM-168 达成全球授权与合作协议。
根据该协议条款,璧辰医药将获得首付款,并有资格获得后续研发、监管及销售里程碑付款。ABM-168是一种高效的变构型MEK1/2抑制剂,在多项临床前动物模型中,无论单药使用还是与其他药物联合使用,均展现出显著的抗肿瘤活性。
临床前研究还表明,ABM-168具有优异的血脑屏障穿透能力,能够有效作用于脑转移癌细胞及恶性原发性脑肿瘤细胞。
ABM-168于2022年10月获得美国食品药品监督管理局(FDA)授予的临床试验许可(IND),并已在美国多家肿瘤中心开展I期临床试验(NCT05831995)。
2023年8月,ABM-168也获得中国国家药品监督管理局(NMPA)批准,在晚期实体瘤患者中开展I期临床试验,重点关注脑转移患者及原发性脑肿瘤患者。
该研究旨在评估ABM-168 的安全性、耐受性、药代动力学特征以及初步抗肿瘤活性。
嘉因生物递表港股IPO,上轮投后5.77亿美元
2026年1月14日,嘉因生物港股IPO申请获得受理,招股书正式公开。
嘉因生物成立于2019年,建立起自主知识产权的AAV技术平台和SODA沉默寡核苷酸技术平台。研发管线包括治疗SMA 1型的EXG001-307、治疗wAMD等眼科适应症的EXG102-031和EXG202等。
嘉因生物成立以来历经多轮融资,2021年6月完成7000万美元B++轮融资,投后估值5.77亿美元。
荃信生物NewCo公司获1.125亿美元融资
2026年1月14日,Caldera Therapeutics宣布完成1.125亿美元融资,并已在其主导项目CLD-423的1期临床试验中完成首批受试者给药。 值得关注的是,该公司于2025年4月自荃信生物获得了CLD-423的独家全球开发和商业化权利,该笔NewCo交易总额达5.55亿美元。 CLD-423是一款首创靶向IL-23p19/TL1A的双特异性抗体,目前正开发用于治疗炎症性肠病(IBD)及其他免疫炎症性疾病。双特异性有可能重新定义IBD的疗效标准,CLD-423经过合理设计,可实现最佳的疾病状况,具有优化的疗效、安全性、药代动力学和可开发性。
亦诺微医药港股IPO申请获得受理,招股书正式公开
2026年1月14日,亦诺微医药港股IPO申请获得受理,招股书正式公开。
亦诺微医药成立于2015年,致力于开发新型溶瘤免疫疗法和工程化外泌体疗法。
亦诺微医药已经建立起丰富具差异化特色的研发管线,包括2款溶瘤病毒疗法和5款外泌体疗法。
亦诺微医药溶瘤病毒疗法主要用于治疗实体瘤,工程化外泌体疗法主要用于解决慢性难治性疾病和年龄相关问题。
亦诺微医药成立以来历经多轮融资,2024年1月完成1440万美元C+轮融资,投后估值为4.85亿美元。
约31亿!药明合联收购东曜药业
1月14日,药明生物发布公告,宣布一项收购要约,旗下子公司药明合联将收购东曜药业。
东曜药业凭借丰富的实践经验和成熟的技术平台及质量体系,东曜药业与国内外制药公司开展多元的战略合作,提供药物开发生产一站式CDMO解决方案,帮助客户加速生物药特别是抗体偶联药(ADC)的开发和生产,赋能产业高质量发展。
东曜药业拥有符合GMP规范的大规模生物药商业化生产基地,配备多条完整的上下游产线,总产能已突破20000L,公司已搭建ADC一体化平台,具备核心研发技术优势,可实现ADC抗体/抗体中间体、原液、制剂等关键生产环节集中一地完成,降低转移成本并减少监管风险;目前,公司已建立符合商业化生产的质量管理体系,并已支持多个上市产品的商业化生产。
未来如星辰大海般璀璨,不必踟躇于过去的半亩方塘!
2025-12-30
2025年10月25日,广东省健康管理学会干细胞与再生医学专委会第二届委员代表大会召开。大会由学会副会长兼秘书长冉炜教授主持,王深明会长、廖振尔常务副会长出席并致辞。干细胞与再生医学专业委员会第一届主任委员裴中教授作工作报告,系统回顾了五年来专委会在平台搭建、标准制定、临床转化与国际合作等方面取得的突破。
全体参会代表以举手表决方式产生第二届专委会领导班子,裴中教授连任主任委员。王深明会长为新一届主委、副主委及常务委员颁发证书,勉励团队继续以临床需求为导向,加速干细胞技术从“实验室”走向“病床旁”。换届大会圆满结束后,学术年会随即拉开帷幕。
上午的学术讲座内容覆盖基础创新、工艺放大、质控标准到临床评价全链条;从神经退行性疾病、运动障碍到衰老干预,多学科交叉,由叶升教授、苏焕兴教授、王宗任教授、王安训教授、刘希哲教授及郑一帆教授联合主持。
首先,项鹏教授(中山大学)以“干细胞创新药物研发进展与挑战”讲题开篇,抛出“双轨制”出口数据:国内已备案项目183项、IND默示许可140项,并提示“异质性、分布局限性、微环境适配”三大瓶颈正成为卡脖子环节;团队建立的MSC多组学效力评价体系,可将临床应答预测准确率提升至87%,为III期试验精准入组提供决策工具。
谷佳明博士(中国科学院香港再生医学与健康中心 潘光锦教授团队)带来“人多能干细胞分化与细胞治疗”的最新进展:利用双Wnt激活+中期CHIR方案,可将iPSC向中脑A9多巴胺前体细胞定向效率提升至83%,并首次鉴定表面标志SSTR2可纯化NP2亚群;小鼠移植6个月后,纹状体18F-DOPA摄取率恢复44%,无畸胎瘤形成,为即将启动的帕金森注册临床奠定细胞来源与质控标准。
Miguel Esteban 教授(华大细胞深圳3D实验室)详解了Translational roadmap for PSC-derived dopaminergic neuron therapies香港研究:其团队以scRNA-seq+scATAC-seq双组学追踪分化轨迹,发现F3/SSTR2可分别标记NP1/NP2两群中间前体,为“同源、同质、高纯度”A9神经元制备提供可放大工艺;预计2026 Q1在中美同步开启Ⅰ/Ⅱa多中心试验,目标入组<30例。
裴中教授(中山大学附属第一医院)在“脑健康与脑疾病的精准防治”报告中,首次发布“脑+免疫”双维度衰老评估模型:结合血浆NfL、端粒长度、NK细胞毒性及MRI脑龄算法,可将AD/PD临床前风险分层提前10-15年;团队主导的ER2001外泌体-siRNA亨廷顿病疗法,已完成中美Ⅰ期首例给药,脑脊液突变亨廷顿蛋白较基线下降28%,无DLT发生,标志着神经系统自组装小核酸药迈入“可治”时代。
冼文彪教授(中山大学附属第一医院)以“帕金森病细胞疗法新进展”为题,系统对比MSC、NK与神经干细胞三大路线:MSC通过“肺-脑轴”静脉回输可改善UPDRS-Ⅲ评分20.4%;自体NK细胞(SNK01)鼻内给药6次后,患者α-突触核蛋白寡聚体水平下降42%,运动与认知复合评分稳定提升;iPSC-多巴胺前体移植18个月数据显示Ki值提升44.7%,无移植诱导运动障碍,为“细胞-基因-免疫”三联干预提供循证依据。
李振韬博士(墨尔本大学)在“干细胞来源细胞外囊泡的质量控制与临床研究”讲座中汇报:其团队已建成800㎡ GMP级外泌体生产线,B级洁净区200㎡;自主研发的膜曲率+PS亲和层析技术,1 h即可收获>10^11 particles高纯度EVs;雾化吸入hUCMSC-EVs治疗间质性肺异常IIT(n=60)初步结果显示,7天疗程FVC提升18%,两名患者薄层CT纤维化病灶显著消退;阿尔茨海默症鼻滴EVs多中心IIT已获伦理批件,计划2026 Q2启动。
最后,裴中教授作总结结束了上午的干细胞讲座。下午为亨廷顿病学术主题,会议内容涵盖“降低亨廷顿蛋白新策略”“RNA靶向治疗”“数字化早筛与生物标志物”“HD干细胞治疗策略”等主题,系统呈现从病因干预到功能康复的最新进展。会议由裴中教授、黄珊珊教授、甘世锐教授、肖友生教授、陈定邦教授及邱伟教授联袂主持;四川大学华西医院商慧芳教授作为特邀嘉宾及中国亨廷顿病协作网发起人之一线上致欢迎词,寄语全国同道继续携手推进相关研究。
首先,瑞士伯尔尼大学Jean-Marc Burgunder教授介绍了最新的亨廷蛋白(Huntingtin)降低疗法研究进展。他指出,体细胞中 CAG 重复序列的扩展是由错配修复基因(如 PMS1)驱动的,并展示了多个新兴治疗管线,包括:Skyhawk 公司的剪接转换剂(SKY-0515),PTC518 小分子伪外显子插入剂,和uniQure 公司的miRNA 基因疗法(AMT-130)等。这些疗法均能在血液或脑脊液中实现 HTT mRNA 或蛋白剂量的下降。其中,PIVOT-HD 研究已达到 12 周的主要终点,并在 24 个月时与匹配的 ENROL-HD 对照组相比显示出改善结果。Sarepta 公司的鞘内注射 siRNA 也已准备好于 2025 年进入临床试验阶段。总体而言,降低亨廷蛋白水平的多个策略目前已具备相当的可行性,下一步的重点是验证其长期安全性及生物标志物的临床获益。
香港中文大学陈浩然教授报告了肽类药物 RP001v63 的最新研究进展。该药物为一种 31 个氨基酸的肽,优先结合突变型 CAG 重复 RNA,阻止 RNA 聚集及下游突变亨廷蛋白的聚集。经非侵入性鼻内给药后,药物可在 10 分钟内到达纹状体和皮层,半衰期为 57–67 分钟。在 R6/2 小鼠模型中,从第 4 周至第 11 周每日给药,可使可溶性突变亨廷蛋白降低 60%,聚集物和 RNA 聚集减少 40%,并显著改善运动障碍,且未发现明显不良反应。项目目前正在进行 IND 申报研究,有计划于 2026 年启动首次临床试验。
暨南大学闫森教授介绍了大型动物模型中亨廷顿病基因疗法的进展。研究团队使用 CRISPR/Cas9 和 RNA 靶向 CasRx 系统,通过 AAV 载体递送至 HD基因敲入猪模型。单次颅内或静脉注射后,突变亨廷蛋白在整个纹状体和皮层中显著减少,蛋白聚集减少,神经元基因表达谱恢复正常,运动症状在超过六个月的时间内显著改善。单细胞分析发现猪纹状体中出现类似人类的 CD8+ T 细胞浸润和 IFN 激活的小胶质细胞,为优化剂量、手术路径和免疫监测提供了具有转化价值的研究平台。
暨南大学王璐教授概述了亨廷顿病 PET 成像工具包的最新进展。新一代放射性配体可在体内定量三个关键病理节点:TSPO用于小胶质细胞激活;PDE10A用于纹状体神经元完整性;CYP46A1用于脑胆固醇代谢平衡。在 HD 小鼠模型和 17 例患者的初步纵向成像中,这些信号在症状出现前,最多可提前 20 年发生变化,为未来临床试验提供了可量化的生物标志物,并可用于患者分层、靶点评估及治疗性神经炎症、神经元丢失和胆固醇代谢恢复的监测。
广州医科大学附属第一医院吴腾腾博士报告了 ER2001 的首次临床试验结果。ER2001 是一种自组装的 HTT-siRNA,经简单静脉注射后可被循环外泌体包裹。在已完成的 1 期试点研究中(12 例早期 HD 患者,每周一次×6 次,后每 6 周一次),药物耐受性良好,无严重不良反应,脑脊液中突变亨廷蛋白中位下降 28%,并伴随轻微的运动评分改善。药代动力学显示,siRNA 在 1 小时内加载至血浆外泌体并进入中枢神经系统。目前正在进行安慰剂对照扩展试验,计划招募少于 30 名受试者,以脑脊液 mHTT 降低为主要药效学指标。
四川大学华西医院程扬帆博士介绍了其关于外周血体细胞 CAG 扩展(SER)的研究成果。在 349 例中国 HD 患者中,基线时更高的 SER 可预测未来 1–8 年内 cUHDRS、TMS 及尾状核/壳核体积的更快下降,且 SER 可解释约 50% 的遗传 CAG 长度对临床评分的影响。血清钙、尿酸和淋巴细胞计数是影响 SER 最强的因素。因此, PBMC DNA 的 SER 检测可用于评估疾病进展风险,并可能作为抑制体细胞扩展的临床试验中便捷的药效学标志物。
中山大学附属第一医院林丽山博士报告了一项基于 1 分钟普通话故事朗读的特征语音指数 研究。研究证明该指数在 210 名志愿者中逐步下降,从健康对照到前 HD、再到第 1 和第 2 阶段患者,与 TMS、TFC、SDMT 及纹状体体积高度相关,并可预测临床恶化及尾状核/壳核萎缩。该工具具有非侵入性、可基于手机采集、语言通用等特点,已准备扩展到多中心及纵向随访验证研究。
中山大学附属第一医院杨慧明博士在 AAV-mHTT 小鼠模型中测试了鼻内给予载有 BDNF 的小细胞外囊泡的治疗效果。每日鼻内给药 4 周后,纹状体 mHTT 聚集减少 40%,反应性胶质细胞减少,NeuN+ 神经元得以保存,运动功能恢复,且未观察到毒性。囊泡在 10 分钟内即可到达皮层和纹状体,为神经营养治疗提供了一种简单、非侵入的递送方式,可能成为降低 mHTT 的新策略。
华中科技大学谭亮平博士介绍了一款用于下肢无力患者的智能站立辅助机器人。该设备采用被动并联的连杆结构,可在几秒钟内将用户从床上抬升至完全站立状态,支持室内无辅助行走、下蹲训练和转移。该设备已用于相关神经运动疾病患者的行走辅助和康复训练中,团队正在收集步态和使用数据以进一步验证和优化训练效果。
中山大学附属第一医院裴中教授概述了亨廷顿病“全程管理”新策略:围绕基因预测、早期筛查、药物分层、晚期支持和家庭赋能五大节点,构建多学科-全周期照护体系,把“等待药物”转变为“主动管理”。他全面地介绍了不同阶段的治疗和护理方案,同时呼吁重视吞咽营养、辅助装置、物理治疗与患者教育,构建覆盖家庭-社区-医院的连续照护链,让患者和家庭在每个病程节点都有方案、有温度、有希望。
裴中教授在闭幕辞中表示:上午六场报告一气呵成,串起“细胞来源—工艺放大—质控标准—临床评价”完整闭环,为干细胞与外泌体产品规范化、产业化提供了可复制、可推广的“广东模板”;下午议题则集中展示亨廷顿病在“降低有毒亨廷蛋白、保护脑细胞、无创早筛”三大战线的突破性进展,标志着HD治疗正从“对症处理”阔步迈入“病因干预”的历史拐点。科学探索永无终点,期待国内外同道携手并肩,在干细胞与相关疾病治疗领域持续产出更多原创成果,为患者赢得更长窗口期与更高质量的生活。至此,大会在热烈的掌声中圆满落幕。
干细胞与再生医学专委会供稿
siRNA临床申请细胞疗法
100 项与 ER-2001 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 亨廷顿舞蹈病 | 临床2期 | 中国 | 2025-02-11 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用