预约演示
更新于:2026-06-06
SGB-7342
更新于:2026-06-06
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)临床1期 |
特殊审评- |
登录后查看时间轴
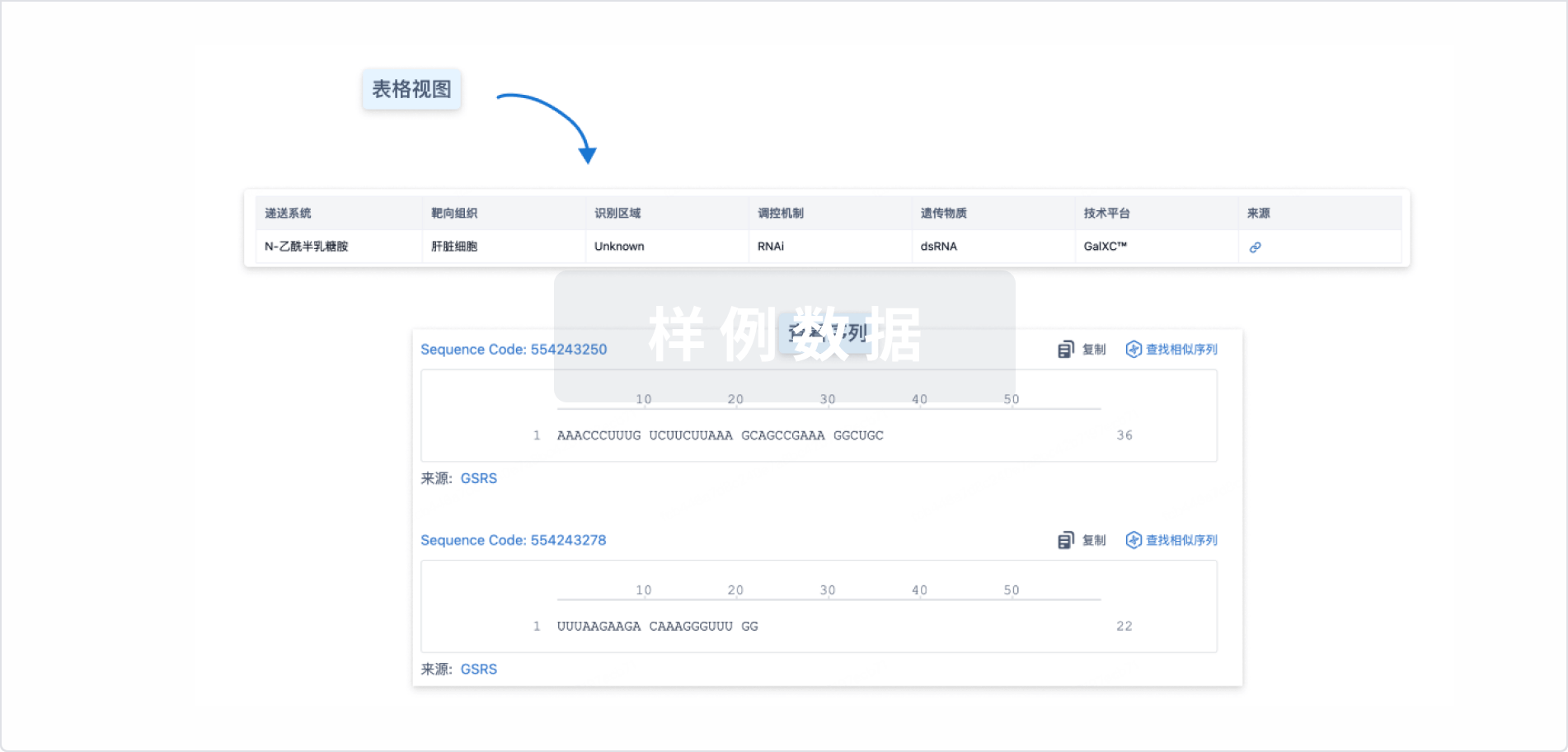
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
2
项与 SGB-7342 相关的临床试验NCT07324850
A Phase 1, Randomized, Double-blind, Placebo-controlled Single Ascending Dose Study to Evaluate the Safety, Tolerability, Pharmacokinetics, and Pharmacodynamics of Subcutaneously Administered SGB-7342 in Subjects With Obesity or Overweight
The purpose of this study is to evaluate the safety and tolerability of subcutaneously administered SGB-7342 in adult subjects with obesity and overweight.
开始日期2026-01-12 |
申办/合作机构 |
CTR20261539
在中国肥胖且伴有2型糖尿病患者中评价多次皮下给药SGB-7342注射液的安全性、耐受性、药代动力学以及药效学特征的I期临床试验
主要目的:在中国肥胖且伴有2型糖尿病患者中评价SGB-7342多次皮下给药的安全性和耐受性;次要目的:评价SGB-7342多次皮下给药的药代动力学(PK)特征;评价SGB-7342多次皮下给药的药效学作用;探索性研究目的:评价SGB-7342多次皮下给药的免疫原性
开始日期- |
申办/合作机构 |
100 项与 SGB-7342 相关的临床结果
登录后查看更多信息
100 项与 SGB-7342 相关的转化医学
登录后查看更多信息
100 项与 SGB-7342 相关的专利(医药)
登录后查看更多信息
75
项与 SGB-7342 相关的新闻(医药)2026-05-20
·青梅煮药
一、报告概述
国盛证券研究所发布的《小核酸药物行业专题:奇点已至:小核酸药物迈向平台多维布局新纪元》系统梳理了小核酸药物的技术原理、发展历程、市场规模、在研管线及海内外企业竞争格局。报告指出,小核酸药物凭借其直接调控基因表达的独特机制,正在重构现代制药版图。在GalNAc递送系统等关键技术的推动下,多款重磅药物相继上市,全球小核酸药物市场从2019年的27亿美元增长到2024年的57亿美元,预计2034年将达到549亿美元。截至2025年底,已有三款小核酸药物进入十亿美元销售行列。适应症方面,小核酸药物正从肝脏靶器官逐步向脑靶、脂肪靶向拓展,在降脂、减重、MASH、高血压、乙肝等领域的临床进展不断突破现有药物边界。
【核心观点】奇点已至:小核酸药物正迈向平台多维布局新纪元,国内企业凭借高效的临床开发效率和全面的管线布局,开始在全球小核酸药物竞争中占据主动权。二、小核酸药物:重构现代制药版图的创新力量1. 定义与分类
小核酸是化学合成的短核酸序列(通常为15-25个核苷酸),用于调节基因表达水平,通过mRNA转录水平调控达到治疗疾病目的。与传统药物直接作用于致病蛋白不同,小核酸药物从上游直接调控致病蛋白的生成,从源头上干预“致病”因素。
小核酸药物主要包括四大类:
反义寡核苷酸(ASO):单链,18-30 nt。通过阻断翻译、促进降解、调控剪接、上调翻译等多种机制发挥作用。
小干扰RNA(siRNA):双链,19-23 bp。通过RNA干扰机制,加载至RISC复合体,特异性降解靶mRNA,抑制蛋白表达。
微小RNA(miRNA):单链,约22 nt。通过抑制/裂解mRNA调控基因表达。
核酸适配体(Aptamer):单链,20-100 nt,折叠成特定三维结构。通过结合并阻断靶蛋白功能、激活目标受体或递送药物分子发挥作用。
表1:siRNA、ASO与适配体:三类小核酸药物的特性对比表
2. 差异化优势:突破不可成药限制
与小分子药物和抗体药物相比,小核酸药物具备显著差异化优势:特性siRNA小分子抗体分子量通常>7 kDa通常<500 Da约>150 kDa作用靶点主要为RNA主要为蛋白质特异性蛋白质作用机制基因表达调控蛋白质功能调控蛋白质调控特异性高中高影响持续时间长短中给药频率每月/季度/双季度每日每月/双月生产方法/成本化学合成/适中化学合成/低生物工艺/高临床开发成功率高中低3. 临床开发效率显著优于行业基准
Alnylam的RNAi治疗平台在药物研发各阶段的成功率(POS)均显著高于行业平均水平:
I期→II期:Alnylam 85.7% vs 行业 35.2%
II期→III期:Alnylam 88.9% vs 行业 27.4%
III期成功率:Alnylam 87.5% vs 行业 69.2%
累计成功率:Alnylam 66.7% vs 行业 5.7%
图1:各阶段临床试验成功率——Alnylam vs 行业基准
该图直观展示了Alnylam在小核酸药物领域的平台化优势,从I期到上市的累计成功率是行业平均的11.7倍,验证了小核酸技术平台的临床可预测性和研发效率。三、商业化与BD:方兴未艾的市场热潮1. 全球市场规模高速增长
全球小核酸药物市场呈现强劲且持续的增长态势:
2019年:27亿美元 → 2024年:57亿美元,CAGR 16.2%
预计2029年:206亿美元,CAGR 29.4%
预计2034年:549亿美元,CAGR 21.6%
图2:小核酸疗法市场规模(2019—2034E)
该图清晰展示了市场从加速增长到稳步扩张的完整曲线,反映了技术进步与临床验证共同驱动的市场扩容趋势。2. 已上市药物:三款进入十亿美元行列
截至2026年3月,全球已获批23款小核酸药物(含已退市3款),包括12款ASO、8款siRNA、2款适配体及1个寡核苷酸端粒酶抑制剂。2025年商业化表现尤为亮眼:
三款药物进入十亿美元俱乐部:
Amvuttra(vutrisiran,Alnylam):2025年销售额23.14亿美元,同比增长138%,靶向TTR,用于ATTR淀粉样变性
Spinraza(诺西那生,渤健):2025年销售额15.47亿美元,靶向SMN2,用于脊髓性肌萎缩症
Leqvio(英克司兰钠,诺华):2025年销售额11.98亿美元,同比增长59%,靶向PCSK9,用于高胆固醇血症
表2:全球已上市小核酸药物商业化表现(2020—2025年)
该表完整列出了Spinraza、Amvuttra、Leqvio、Givlaari、Oxlumo等核心产品的年度销售额及同比增长率,直观呈现了不同产品的放量节奏和市场格局。3. BD交易持续升温
全球小核酸领域交易金额及数量整体呈上升趋势。2025年小核酸领域交易金额达322.10亿美元,交易数量46起,创历史新高。
转让方TOP3:Ionis Pharmaceuticals(58项)、Alnylam Pharmaceuticals(20项)、Arrowhead Pharmaceuticals(11项)
受让方TOP3:诺华制药(15项)、渤健制药(13项)、阿斯利康制药(11项)
图3:历年全球小核酸领域BD金额及交易数量趋势图
该图展示了交易金额从早期数亿美元攀升至2025年322亿美元的跃升过程,印证了小核酸药物技术成熟度和商业价值获得全球药企高度认可。四、适应症破局:由点及面的多维延展
小核酸药物的适应症正从肝脏靶器官逐步向更广泛的疾病领域拓展,核心突破方向包括:1. 降脂领域:PCSK9、ANGPTL3、Lp(a)多点开花
全球高脂血症/高胆固醇血症小核酸管线密集布局。PCSK9靶向siRNA已有诺华Leqvio率先上市,国内齐鲁制药RBD7022、石药集团SYH2053、圣因生物SGB-3403等进入II期临床。ANGPTL3靶向有Arrowhead Zodasiran进入II期。Lp(a)靶向有靖因药业SRSD101、舶望制药BW-20829等推进中。2. 高血压领域:AGT靶向成为热门的慢病布局方向
全球高血压小核酸药物管线以AGT(血管紧张素原)为核心靶点。多款产品已进入III期临床:诺华BW-00163、Ionis Evazarsen/Tonlamarsen、圣因生物SGB-3908、石药集团SYH2062、成都先衍LDR2402、悦康药业YKYY029等。与每日口服降压药相比,小核酸药物有望实现每半年或一年给药一次,极大提升患者依从性。3. 减重领域:INHBE、ALK7、GPR75等新靶点涌现
肥胖/减重领域成为小核酸药物新兴布局方向。INHBE靶向:Arrowhead ARO-INHBE、WAVE WVE-007、圣因生物SGB-7342等进入临床。ALK7靶向:Alnylam ALN-2232、Arrowhead ARO-ALK7等在研。GPR75靶向:再生元与Alnylam合作开发。减重小核酸药物旨在通过调控脂肪组织代谢通路实现减重,有望与GLP-1类药物形成差异化竞争或协同。4. MASH领域:HSD17B13、PNPLA3等遗传靶点受关注
代谢功能障碍相关脂肪性肝炎(MASH)是小核酸药物的重要布局方向。核心靶点包括HSD17B13(葛兰素史克/Arrowhead ARO-HSD、再生元Rapisorisan、维亚维VSA006)、PNPLA3(阿斯利康AZD2693、再生元ALN-PNP)等。靶向这些遗传易感基因的小核酸药物有望从上游干预MASH疾病进程。5. 肝炎领域:HBV功能性治愈仍是核心方向
乙肝功能性治愈是小核酸药物的重要探索方向。罗氏、强生、Alnylam、Aligos等均有布局。国内悦康药业YKYY013、星曜坤泽HT-101等进入临床。小核酸药物联合核苷(酸)类似物或干扰素,有望实现乙肝表面抗原(HBsAg)清除。
五、全球竞速:海内外药企各显锋芒1. Alnylam:RNAi领域全球领导者
Alnylam是RNAi治疗领域的先驱和领导者,拥有Amvuttra、Onpattro、Givlaari、Oxlumo、Leqvio等多款上市产品。核心管线包括:治疗ATTR心肌病的nucresiran(III期)、治疗高血压的zilebesiran(III期)、以及多款早期管线。Alnylam凭借其脂质纳米颗粒(LNP)和GalNAc递送系统,构建了持续产出的RNAi平台。2. Ionis:ASO寡核苷酸疗法龙头
Ionis是ASO领域的领军企业,拥有Spinraza、Tegsedi、Waylivra、TRYNGOLZA等上市产品,并与渤健、阿斯利康等多家跨国药企深度合作。2025年获批的TRYNGOLZA(olezarsen)是美国首个且唯一获批用于家族性乳糜微粒血症综合征(FCS)的药物,销售快速增长。3. Arrowhead:多靶点多器官布局的RNAi平台
Arrowhead的核心技术为TRiM™(Targeted RNAi Molecule)平台,通过配体介导递送技术实现组织特异性靶向,覆盖肝脏、肺、肌肉、神经等组织。管线包括Zodasiran(ANGPTL3,II期)、ARO-ALK7/ARO-INHBE(减重,II期)等。4. 瑞博生物:厚积薄发的小核酸开拓者
瑞博生物依托自主研发的RiboGalSTART™肝靶向递送技术,推动多款产品进入临床。RiboOncoSTART™布局肿瘤靶向,RiboPepSTART™布局肾脏、中枢神经、脂肪等肝外组织靶向。公司实现小核酸药物全周期技术覆盖,是国内小核酸领域的代表性企业。5. 舶望制药:国内小核酸企业领军者
舶望制药拥有行业领先的RADS平台(更强活性、持久性和安全性的RNA分子),管线覆盖心血管、罕见病、CNS、乙肝、代谢疾病等。核心管线包括:BW-20507(乙肝,II期)、BW-20829(Lp(a),II期)、BW-00112(ANGPTL3,II期)、BW-4002(IgA肾病/阵发性睡眠性血红蛋白尿症,II期)等。6. 靖因药业:深耕心血管与代谢
靖因药业成立于2021年,由OrbiMed及Creacion Ventures联合创立,中美双总部运营。核心管线SRSD101(PCSK9)已进入临床,另有SRSD107(FXI,抗凝)等在研。7. 赫吉亚(中国生物制药收购):长效递送平台稀缺性突出
2026年1月,中国生物制药以12亿元全资收购赫吉亚。赫吉亚拥有三大核心技术平台:MVIP肝靶向平台(全球首个经临床验证可实现“一年一针”长效给药的siRNA递送技术)、DDP双靶点递送平台(实现“1+1>2”协同疗效)、NSDP神经靶向平台(CNS/PNS递送)。已有4款产品进入临床,超20个项目处于临床前,在研管线覆盖减重代谢、心脑血管、神经系统三大慢病领域。8. 前沿生物:双靶点率先突围,牵手GSK
2026年2月,前沿生物与GSK达成独家授权协议:GSK获得两款siRNA管线全球权益(一款IND阶段、一款临床前)。前沿生物将获得4000万美元首付款,最高9.63亿美元里程碑付款,及全球净销售额分级特许权使用费。六、未来趋势与投资建议1. 技术演进方向
递送系统突破:从肝脏靶向(GalNAc)向肝外靶向(CNS、脂肪、肌肉、肾脏)拓展,是下一阶段小核酸药物竞争的核心壁垒。
长效化给药:“一年一针”成为可能,慢病治疗范式或将被颠覆。
双靶点/多靶点协同:DDP等双靶点递送平台有望实现“1+1>2”的协同疗效。
平台化竞争:拥有自主知识产权的递送平台和化学修饰平台的头部企业将持续扩大领先优势。2. 商业化关键节点
降脂:Leqvio已验证PCSK9 siRNA的商业价值,国内PCSK9 siRNA有望在未来2-3年陆续上市。
高血压:多款AGT siRNA处于III期临床,预计2027-2028年有望迎来首个高血压siRNA药物上市。
减重:INHBE、ALK7等靶点处于早期临床,差异化机制有望在GLP-1类药物治疗后或联合用药场景中占据一席之地。
乙肝功能性治愈:小核酸联合治疗方案的临床数据读出将是未来2-3年的关键观察窗口。3. 建议关注
国内企业:前沿生物、瑞博生物、中国生物制药(收购赫吉亚)、舶望制药(未上市)、靖因药业(未上市)、圣因生物(未上市)、必贝特、阳光诺和、悦康药业、恒瑞医药、石药集团、腾盛博药、成都先导等
海外企业:Alnylam、Ionis、Arrowhead等七、风险提示
竞争风险:同靶点竞争激烈,临床推进速度不及预期可能影响产品竞争格局身位
研发风险:临床试验结果不及预期可能对行业产生负向影响
市场震荡风险:短期宏观环境变化可能影响相关企业估值稳定性八、结论
小核酸药物正处于从技术突破向平台多维布局迈进的“奇点时刻”。在递送系统、化学修饰、CMC工艺等核心技术的持续迭代下,小核酸药物的研发效率和临床成功率显著高于行业平均水平。全球小核酸药物市场正以29%的年复合增长率高速扩容,到2034年有望达到549亿美元。降脂、高血压、减重、MASH、乙肝等慢病领域的广泛布局,正在重塑这些传统“小分子+抗体”主导领域的治疗范式。国内企业凭借高效的临床开发能力、差异化的管线布局以及日益成熟的平台技术,开始在全球小核酸药物竞争中占据主动权。随着赫吉亚“一年一针”长效递送平台、前沿生物与GSK的授权合作等标志性事件的落地,中国小核酸药物产业正从“跟跑”迈向“并跑”新阶段。拥有自主知识产权递送平台、差异化靶点布局及强大临床推进能力的企业,有望在小核酸黄金十年中脱颖而出。
报告原文来源:国盛证券研究所《国盛医药小核酸药物行业专题:奇点已至:小核酸药物迈向平台多维布局新纪元》
siRNA临床2期核酸药物寡核苷酸信使RNA
2026-04-15
前言
过去三年,医药行业最不缺的就是 “风口”,但真正具备颠覆性、持续性、全球化的主线赛道寥寥无几。
小核酸(siRNA/ASO)不是一阵热度,而是继小分子、抗体之后,第三次制药底层逻辑的重构。
本文完整呈现:小核酸到底走到了哪一步、谁在真正领跑、哪些机会最值得医药人抓住。一、先破后立:小核酸的爆发,本质是 “递送成熟”
小核酸的历史,就是一部递送突破史。
前 20 年:被核酸酶降解、细胞膜穿透差、无法靶向,停留在实验室。
近 8 年:GalNAc 肝靶向成熟,让 siRNA/ASO 第一次实现 “皮下注射、长效稳定、肝脏富集”。
当下:肝外递送进入突破期(心脏、神经、肌肉、眼、肿瘤),打开下一个十倍空间。
三个关键结论(行业内行共识)递送 = 小核酸的命门
序列可以设计、修饰可以优化,但递送平台决定能不能成药、能治什么病。
GalNAc 奠定商业化底座
全球已上市小核酸药物,90% 以上依托肝靶向,适应症集中在代谢、血脂、乙肝、罕见病。
肝外递送 = 下一轮竞争核心
谁先突破血脑屏障、心肌靶向、肌肉递送,谁就能拿下神经、心衰、骨科等超大病种。一句话:递送成熟,小核酸才真正成为药。
二、全球格局:三足鼎立,中国从 “跟跑” 进入 “并跑”1. 美国:源头创新 + 商业化成熟(全球标杆)
代表企业:Alnylam、Ionis、Arrowhead、Sarepta
优势:靶点发现早、平台完善、获批药物最多、商业化验证充分
现状:从罕见病向慢病、减重、神经扩张,重磅药物年销售额突破 20 亿美元。
2. 欧洲:监管成熟 + 罕见病优势
代表企业:赛诺菲、诺华
优势:孤儿药政策友好、患者招募规范、临床数据认可度高
现状:以并购与合作快速补齐自研,抢占心血管与代谢大病种。
3. 中国:临床最快、慢病最猛、BD 最活跃
优势:临床速度全球领先、慢病市场空间巨大、企业执行力强
特点:不追小众罕见病,直接切入血脂、降压、减重、乙肝等十亿 / 百亿赛道
地位:全球第二大小核酸管线国家,从 “引进来” 全面转向 “走出去”。
三、国内企业真实梯队:谁有干货?谁在爬坡?谁纯布局?
(基于 2026 年 4 月最新临床、融资、BD、专利真实情况划分)第一梯队:有临床、有数据、有全球化(可重点关注)
瑞博生物
中国生物制药(赫吉亚生物)
圣因生物
舶望制药
石药集团
亿腾嘉和
前沿生物
第二梯队:有平台、有专利、推进至 IND/I 期
华润医药(华润双鹤 × 炫景生物)
大睿生物
广州必贝特
东阳光
悦康药业
成都先导
第三梯队:早期布局、专利为主、暂无线下临床
传统药企转型布局、高校成果转化、早期 Biotech
猎头视角提醒:
第一梯队人才溢价最高、岗位最稳、成长最快;
第二梯队适合赌成长性、拿期权;
第三梯队更适合研发底层人才,谨慎选择临床 / 商业化岗。
四、国内核心企业管线全景表(2026 最新・真实可查)
企业
核心品种
类型
靶点
适应症
临床阶段
核心价值
中国生物制药(赫吉亚)
Kylo-11
siRNA
Lp(a)
Lp(a)
II 期(2025年10月已启动中美国际多中心II期)
一年一针,领先长效
中国生物制药(赫吉亚)
Kylo-12
siRNA
APOC3
高甘油三酯
I 期
长效降脂,FCS 适用
瑞博生物
RBD4059
siRNA
FXI
血栓抗凝
II 期
瑞博生物
RBD5044
siRNA
APOC3
高甘油三酯
II 期
国内 APOC3 领先
瑞博生物
RBD1016
siRNA
HBV
慢性乙肝
Ib 期
功能性治愈方向
亿腾嘉和
EDP167
siRNA
ANGPTL3
HoFH / 混合型高脂
II 期(2026年2月完成首例给药)
不依赖 LDLR,他汀无效人群可用
石药集团
SYH2053
siRNA
PCSK9
高胆固醇
III 期
国内降脂 siRNA 第一梯队
石药集团
SYH2061
siRNA
C5
肾病 / 自免
I 期
长效,数月一针
华润医药
RG008
siRNA
代谢靶点
慢病
PCC
双鹤 × 炫景合作
华润医药
DC50292A
siRNA
肿瘤靶点
实体瘤
IND
中美双报
前沿生物
FB7013
siRNA
MASP-2
IgA 肾病
IND
全球首创,超长效
前沿生物
FB7011
siRNA
MASP-2/CFB
IgA 肾病
临床前
双靶点,全球首创
圣因生物
SGB-7342
siRNA
INHBE
肥胖
I 期
肝外递送,长效减重
必贝特
双靶 siRNA
siRNA
多靶点
血脂 / 高血压
专利 / 临床前
双序列 + GalNAc
东阳光
AGT siRNA
siRNA
AGT
高血压
专利布局
降压大靶点
悦康药业
YKYY015
siRNA
PCSK9
高胆固醇
临床
中美双报
成都先导
LDR2402
siRNA
AGT
高血压
II 期
超长效降压五、人才市场真相:谁最稀缺?谁能跨界?谁在涨薪?
小核酸不是 “玄学行业”,传统医药人完全能转,但岗位差异极大。
1. 最稀缺、溢价最高的三类人递送技术人才(LNP/GalNAc/ 偶联 / 肝外)缺口最大、薪资最高、期权最慷慨,跨界难度大。CMC / 工艺 / 分析人才
(寡核苷酸合成、纯化、质控)传统化药 / 多肽背景可转,溢价 30%–70%。
临床 / 医学 / PV 人才
(小核酸临床方案、长效安全、信号检测)传统创新药背景直接转,溢价 20%–50%,是最大人群红利。
2. 最容易跨界的岗位(零壁垒转型)
医学经理 / 医学总监
临床项目经理(CPM)
药物警戒(PV)
注册申报
质量与 QA
医学写作
只要做过创新药,就能转小核酸,不需要懂分子生物学。3. 真实薪资现状(2026 市场)
传统背景转小核酸:溢价 20%–40%
有小核酸项目经验:溢价 50%–80%
递送 / CMC 核心人才:年薪百万 + 期权常态化
六、冷静判断:小核酸的泡沫、风险与确定性
任何深度行业分析,必须讲风险,才可信。风险点(必须清醒)靶点同质化
PCSK9、APOC3、AGT、Lp (a) 扎堆,未来会卷。递送仍有瓶颈
肝外递送仍在早期,成功率低、研发投入大。商业化未全面验证
国内尚无重磅小核酸药物上市,销售体系仍在搭建。未来 3 年三大确定性(机会大于风险)国内产品密集上市
2026–2028 是 “中国小核酸上市元年”。肝外递送迎来突破
神经、心脏、肌肉适应症会出现 FIC 品种。人才争夺白热化
传统医药人转型窗口仅剩 2–3 年,越早越占优。七、结语:对医药人来说,小核酸意味着什么?
小核酸不是选择题,是未来十年创新药的主线。它不依赖运气、不依赖单一靶点、不依赖营销驱动,而是平台驱动、技术驱动、全球竞争。
小分子已经红海
抗体药内卷严重
小核酸,是为数不多仍处在增长早期→爆发期的黄金赛道
中国企业已经站在全球舞台,临床在推进、BD 在爆发、人才在崛起。
看懂小核酸,就是看懂下一个十年。
布局小核酸,就是布局自己的职业天花板。
推荐阅读:
一问读懂心源性猝死,为自己的健康保驾护航
Q1结束了,创新药对外授权成绩单如何?
一年减掉30斤!这款新药刷屏,但更值得关注的是:中国近亿人正面临这个危机
又一里程碑!英矽智能与礼来达成药物研发战略合作
百济神州×泽布替尼,中国创新药的全球突围之路
深度解读 2026政府工作报告 - 生物医药跻身新型支柱产业
2026-04-09
一、小核酸药物核心作用机制小核酸药物主要分为siRNA(小干扰RNA)和ASO(反义寡核苷酸)两大类,核心是在转录/转录后水平精准调控基因表达,攻克传统小分子/抗体药无法靶向的“不可成药”靶点:1. siRNA:双链RNA分子,通过RNA干扰(RNAi)通路发挥作用。进入靶细胞后被组装到RNA诱导沉默复合体(RISC)中,正义链降解,反义链精准互补结合靶mRNA,触发AGO2内切酶切割靶mRNA使其降解,从根源上阻断致病蛋白的合成,主流GalNAc修饰可实现肝脏精准靶向,给药频率低至3-12个月一针。
2. ASO:单链寡核苷酸,可进入细胞核,作用更灵活:① 降解型:结合靶mRNA后招募RNase H酶切割mRNA,沉默致病基因;② 剪接调控型:结合pre-mRNA,调控外显子剪接,修复/生成功能性蛋白(如SMA治疗药物);还可实现miRNA抑制等功能。二、全球已上市的核心小核酸药物(截至2026年4月)全球累计获批小核酸药物超20款(剔除退市品种),核心上市品种如下:1. siRNA类(7款已上市,均为肝脏靶向)靶点 药物名称 企业 获批时间 核心适应症 作用机制 1、药物名称:Patisiran(Onpattro),靶点为TTR。Alnylam在2018年上市,核心适应症为转甲状腺素蛋白淀粉样变性伴多发性神经病变,作用机制是(ATTR-PN) 沉默肝脏TTR mRNA,减少错误折叠的TTR蛋白生成,抑制组织淀粉样沉积 。
2、药物名称:Givosiran(Givlaari),靶点为ALAS1。Alnylam在2019年上市,适应症为急性肝卟啉症(AHP),作用机制是通过沉默肝脏δ-氨基乙酰丙酸合酶1(ALAS1)mRNA,减少血红素合成通路毒性中间产物积累。
3、药物名称:Lumasiran(Oxlumo),靶点为HAO1,Alnylam在2020年上市,适应症是原发性高草酸尿症1型(PH1),通过沉默肝脏羟基酸氧化酶1(HAO1)mRNA,阻断草酸的从头合成。
4、药物名称:Inclisiran(Leqvio/英克司兰) ,靶点为PCSK9 ,诺华/Alnylam分别在2020年(欧盟)、2023年(中国)上市, 适应症是高胆固醇血症、动脉粥样硬化性心血管疾病,通过沉默肝脏PCSK9 mRNA,减少PCSK9蛋白表达,增加LDL受体循环,强效降低LDL-C,半年一针
5、药物名称:Vutrisiran(Amvuttra),靶点是TTR,Alnylam在2022年上市,适应症是 ATTR-PN、ATTR淀粉样变性心肌病(ATTR-CM),通过GalNAc修饰长效siRNA,沉默TTR mRNA,每3个月一针,2025年销售额突破23亿美元
6、药物名称:Plozasiran(普乐司兰钠),靶点是APOC3,赛诺菲分别在2025年(FDA)、2026年(中国)上市,适应症是家族性乳糜微粒血症综合征(FCS)、严重高甘油三酯血症,通过沉默肝脏APOC3 mRNA,降低APOC3蛋白表达,解除对脂蛋白脂酶的抑制,甘油三酯降幅超75% 2. ASO类(核心上市品种)靶点 药物名称 企业 获批时间 核心适应症 作用机制 1、药物名称:Nusinersen(Spinraza),靶点是SMN2,Ionis/百健在2016年上市,适应症是脊髓性肌萎缩症(SMA),通过剪接调控型ASO,修饰SMN2 pre-mRNA的剪接过程,增加功能性全长SMN蛋白表达。
2、药物名称:Eteplirsen/Golodirsen/Casimersen,靶点是DMD(外显子51/53/45),Sarepta在2021年上市,适应症为杜氏肌营养不良(DMD),通过外显子跳跃ASO,修复DMD基因的阅读框,生成截短但有功能的抗肌萎缩蛋白
3、药物名称:Inotersen(Tegsedi),靶点是TTR。Ionis 在2018年上市,适应症为ATTR-PN,通过降解型ASO,沉默TTR mRNA,减少毒性TTR蛋白生成
4、药物名称:Mipomersen(Kynamro)靶点是ApoB。Ionis在2013年上市,适应症为纯合子家族性高胆固醇血症,通过沉默ApoB mRNA,减少低密度脂蛋白合成,降低LDL-C。三、在研热门靶点及成药潜力排序按成药确定性从高到低,分为三大梯队,核心靶点均有人类遗传学验证,成药逻辑清晰:
1. 成药确定性极高(III期临床,2026-2027年大概率获批)
(1)Lp(a)(脂蛋白a)
作用机制:沉默肝脏LPA基因的mRNA,降低循环中Lp(a)水平。遗传学已证实高Lp(a)是动脉粥样硬化性心血管疾病、主动脉瓣狭窄的独立危险因素,目前无针对性获批药物,临床需求极大。核心管线:诺华Pelacarsen(III期临床,2026年上半年读出终点数据)、安进Olpasiran(III期),均可使Lp(a)水平降幅超90%,显著降低心梗、卒中风险。
成药潜力:★★★★★,靶点验证充分,临床数据积极,是继PCSK9后下一代心血管小核酸核心品种,市场空间超百亿美元。(2)AGT(血管紧张素原)
作用机制:沉默肝脏AGT mRNA,减少血管紧张素原生成,从源头阻断肾素-血管紧张素-醛固酮系统(RAAS)激活,实现长效降压。核心管线:Alnylam的Zilebesiran,正在开展III期万人临床试验,单次给药降压效果持续6个月,可解决高血压患者长期服药的依从性问题,2026年有望提交上市申请。成药潜力:★★★★★,高血压患者基数庞大,长效给药优势显著,靶点通路成熟,成药风险极低。(3)ANGPTL3(血管生成素样蛋白3)作用机制:沉默肝脏ANGPTL3 mRNA,降低ANGPTL3蛋白表达,激活脂蛋白脂酶和内皮脂肪酶,同时强效降低LDL-C和甘油三酯。遗传学证实ANGPTL3功能缺失突变人群血脂水平显著更低,心血管疾病风险下降。核心管线:Arrowhead的Zodasiran(III期临床),针对纯合子家族性高胆固醇血症、严重高甘油三酯血症,对他汀类药物不耐受/无效患者优势显著。
成药潜力:★★★★☆,靶点验证充分,降脂谱广,填补难治性高血脂的治疗空白。(4)HBV(乙肝病毒相关靶点,HBsAg/HBx)作用机制:靶向HBV的RNA序列,沉默病毒基因表达,抑制乙肝表面抗原(HBsAg)等病毒蛋白生成,打破宿主免疫耐受,有望实现慢性乙肝的功能性治愈。
核心管线:GSK的Bepirovirsen(ASO,2026年2月日本已受理上市申请)、瑞博生物RBD1016(siRNA,靶向HBx,II期临床)、Alnylam的ALN-HBV,均可使HBsAg持续显著下降。
成药潜力:★★★★☆,乙肝全球患者基数庞大,现有疗法无法实现治愈,功能性治愈是行业终极目标,成药空间广阔。2. 高潜力临床后期靶点(II期临床,数据积极,成药逻辑清晰)(1)INHBE(减重/代谢)作用机制:沉默肝脏INHBE基因,减少其编码的Activin E蛋白表达,解除对脂肪分解的抑制,实现减脂增肌,无GLP-1类药物的胃肠道副作用,单次给药疗效持续超6个月。核心管线:大睿生物RN3161(全球进度第二,I期临床完成)、圣因生物SGB-7342(I期临床),猴模型中可使INHBE mRNA下调超90%,减重效果显著。成药潜力:★★★★,减重是全球最大慢病赛道,小核酸长效、无胃肠道副作用的优势显著,有望颠覆GLP-1治疗格局。(2)HTT(亨廷顿舞蹈症)作用机制:靶向沉默突变的亨廷顿基因(HTT)mRNA,减少毒性亨廷顿蛋白的生成,延缓神经退行性病变进展。核心管线:Ionis/罗氏的RO7234292(II期临床),可显著降低脑脊液中的突变HTT蛋白,改善患者临床症状,是目前CNS小核酸领域进度最快的管线之一。成药潜力:★★★☆,亨廷顿舞蹈症无有效治疗药物,靶点验证充分,核心瓶颈是血脑屏障递送,目前鞘内注射/新型递送技术已实现突破。(3)MAPT(Tau蛋白,阿尔茨海默病)作用机制:沉默MAPT基因mRNA,减少Tau蛋白表达,抑制神经原纤维缠结的形成,延缓阿尔茨海默病的认知衰退。核心管线:Arrowhead的ARO-MAPT(I/II期临床),通过新型递送技术实现皮下注射穿透血脑屏障,可显著降低脑内Tau蛋白水平,是AD领域极具潜力的疾病修正疗法。3. 前沿潜力靶点(早期临床,技术突破驱动)肿瘤靶点:KRAS、MYC、PD-L1、STAT3等,核心是解决肿瘤组织的递送难题,多采用LNP、抗体偶联等递送技术,目前多处于I期临床,成药潜力待验证,是下一代小核酸的核心突破方向。补体靶点:MASP-2、CFB,针对IgA肾病、阵发性睡眠性血红蛋白尿症等补体介导的疾病,通过沉默补体通路关键基因抑制过度免疫激活,前沿生物FB700等管线处于临床前/早期临床阶段。肌肉靶向靶点:针对DMD、肌萎缩等疾病的新型肌肉递送小核酸,突破肝脏靶向的局限,目前处于临床前/早期临床阶段,是肝外递送的核心方向。
关于中国药学年鉴
感谢您阅读《中国药学年鉴》微信平台文章,也欢迎各位读者分享、转载、引用。
《中国药学年鉴》是由中国药科大学主办,涵盖我国药学领域各个方面的药学综合性年刊,内容包括专论、药学研究、新药研发、药学教育、药品生产与流通、医院药学、药品监管、人物、书刊、学会与学术活动、大事记等。
更多精彩回顾,请戳这里!
中国药学会2021"最美科技工作者”评选揭晓
恒瑞VS复星:内部研发与外部合作
关于举办2021年中国药学大会的通知(第三轮)
中国药科大学孔令义团队在STTT发表肝纤维化治疗最新研究成果
来源:E药学苑
100 项与 SGB-7342 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 2型糖尿病 | 临床1期 | 中国 | 2026-04-24 | |
| 肥胖 | 临床1期 | 中国 | 2026-01-07 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
