预约演示
更新于:2026-05-09
RG002C0106
更新于:2026-05-09
概要
基本信息
原研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评- |
登录后查看时间轴
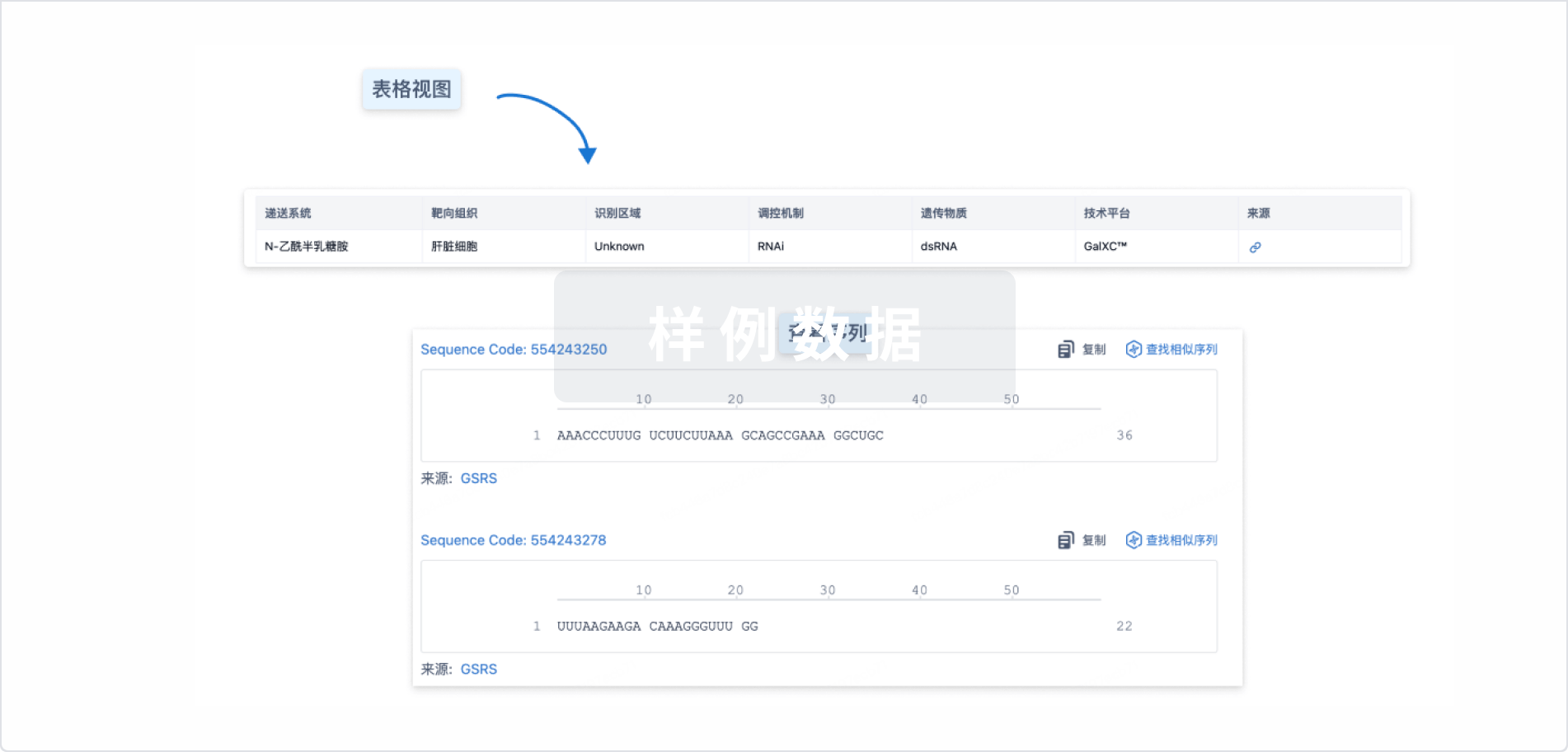
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
3
项与 RG002C0106 相关的临床试验NCT07445906
A Phase I Clinical Study to Evaluate the Safety, Tolerability, PK and PD of RG002C0106 Injection in Adult Participants With Normal Renal Function and Mild-to-Moderate Renal Impairment
This is a Phase I trial designed to evaluate the impact of renal impairment on the efficacy and safety of the drug by comparing pharmacokinetic (PK) parameters and pharmacodynamic (PD) markers after a single subcutaneous injection of RG002C0106 between trial participants with normal renal function and those with mild to moderate renal impairment.
开始日期2026-03-15 |
申办/合作机构 |
NCT07305974
A Multicenter, Randomized, Double-Blind, Placebo-Controlled Phase IIa Clinical Study to Evaluate the Safety, Preliminary Efficacy, and Pharmacokinetic/Pharmacodynamic Characteristics of RG002C0106 Injection in Subjects With Primary IgA Nephropathy
This study looks at how well and safely RG002C0106 works for patients with certain kidney disease: primary IgA nephropathy. It's a phase IIa trial done at several locations where both patients and doctors unknow what treatment is being given.
开始日期2025-09-08 |
申办/合作机构 |
NCT06494527
A Randomized, Double-blind, Placebo-controlled, Single/Multiple Ascending Dose, Phase 1 International Multi-center Clinical Study to Evaluate the Safety/Tolerability, Pharmacokinetics/Pharmacodynamics of RG002C0106 Injection in Healthy Adults
This is a randomized, double-blind, placebo-controlled study to evaluate the safety, tolerability and PK/PD profiles of RG002C0106 injection in healthy adult subjects. The study will be divided into the following parts:
Part A, conducted : SAD stage Part B, conducted: MAD stage
Part A, conducted : SAD stage Part B, conducted: MAD stage
开始日期2024-10-18 |
申办/合作机构 |
100 项与 RG002C0106 相关的临床结果
登录后查看更多信息
100 项与 RG002C0106 相关的转化医学
登录后查看更多信息
100 项与 RG002C0106 相关的专利(医药)
登录后查看更多信息
33
项与 RG002C0106 相关的文献(医药)2024-03-01·Journal of pharmaceutical and biomedical analysis
20(S)-Ginsenoside Rg2 amino acid derivatives for anti hemorrhagic shock: Synthesis, characterization and evaluation
Article
作者: Fang Lin ; Qinghai Dong ; Fei Shi ; Jihua Liu ; Jun Su ; Yang An ; Jiayin Liu ; Hongliu Xie
The purpose of this study is to screen a novel Rg2 derivative for anti hemorrhagic shock. Eight Rg2 amino acid ester derivatives were designed and synthesized, and their effects on hypoxia and shock were studied. Among them, the derivative 1 (D1) exhibited excellent anti hypoxia by promoting survival rate of H9c2 cells damaged by hypoxia. D1 improved physiological indicators of the rats in hemorrhagic shock, such as blood pressure, heart rate, lactate, acid-base balance, and alleviate oxidative stress and inflammatory damage. Its latent mechanisms were explored by a method of plasma metabolomics based on UPLC-QTOF-MS. As a result, a total of 16 biomarkers were identified involving 6 metabolic pathways. The results of this study contained that the derivative 1 could be considered as potent drug candidates for anti shock and deserved further research and development.
2023-01-01·Therapeutic advances in medical oncology
Patient outcomes following a response biomarker-guided approach to treatment using 177Lu-PSMA-I&T in men with metastatic castrate-resistant prostate cancer (Re-SPECT)
Article
作者: John, Nikeith ; Pranavan, Ganes ; Counter, William ; Nguyen, Andrew ; Guminski, Alex ; Hickey, Adam ; Sharma, Shikha ; Gedye, Craig ; Joshua, Anthony M. ; Ayers, Maria ; Eu, Peter ; Stockler, Martin R. ; Agrawal, Shikha ; Lee, Adrian ; Mallesara, Girish ; Poole, Aron ; Emmett, Louise ; Crumbaker, Megan ; Pathmanandavel, Sarennya ; Hovey, Elizabeth
Background::
177LuPSMA is an effective treatment in metastatic castrate-resistant prostate cancer with trials adopting a standardised dose interval. Adjusting treatment intervals utilising early response biomarkers may improve patient outcomes.
Objective::
This study evaluated progression-free survival (PFS) and overall survival (OS) based on treatment interval adjustment utilising 177LuPSMA 24-h SPECT/CT (177Lu-SPECT) and early prostate-specific antigen (PSA) response.
Design::
Retrospective analysis of a clinical 177Lu-PSMA-I&T treatment programme.
Methods::
In all, 125 men were treated with 6-weekly 177LuPSMA-I&T [median 3 cycles, interquartile range (IQR): 2–4], median dose 8.0 GBq [95% confidence interval (CI): 7.5–8.0]. Imaging screening involved 68GaPSMA-11 PET/diagnostic CT. 177Lu-SPECT/diagnostic CT was acquired following each therapy, and clinical assessments 3-weekly. Following dose 2 (week 6), a composite PSA and 177Lu-SPECT/CT imaging response [partial response (PR), stable disease (SD), and progressive disease (PD)] determined ongoing management. Response group (RG) 1 (marked reduction in PSA/imaging PR) break in treatment until subsequent PSA rise, then re-treatment. RG 2 (stable or reduced PSA and/or imaging SD) 6-weekly treatments until six doses, or no longer clinically benefitting. RG 3 (rise in PSA and/or imaging PD) recommended for an alternative treatment.
Results::
Overall PSA50% response rate (PSARR) was 60% (75/125), median PSA-PFS 6.1 months (95%CI: 5.5–6.7), and median OS 16.8 months (95%CI: 13.5–20.1). 35% (41/116) were classified as RG 1, 34% (39/116) RG 2, and 31% (36/116) RG 3. PSARRs by RG were 95% (38/41), 74% (29/39), and 8% (3/36); median PSA-PFS rates were 12.1 months (95%CI: 9.3–17.4), 6.1 months (95%CI: 5.8–9.0), and 2.6 months (95%CI: 1.6–3.1); and OS rates were 19.2 months (95%CI: 16.8–20.7), 13.2 months (95%CI: 12.0–18.8), and 11.2 months (95%CI: 8.7–15.6) for RG 1, 2, and 3, respectively. The median months of ‘treatment holiday’ for RG 1 was 6.1 months (IQR: 3.4–8.7). Nine men had received prior 177LuPSMA-617 and were retreated with 177LuPSMA-I&T, with a PSARR of 56% on re-treatment.
Conclusion::
Personalising dosing regimens using early response biomarkers with 177LuPSMA has the potential to achieve similar treatment responses to continuous dosing while allowing treatment breaks or intensification. Further evaluation of early response biomarker-guided treatment regimens in prospective trials is warranted.
Plain Language Summary:
Lutetium-PSMA therapy is a new therapy for metastatic prostate cancer that is well tolerated and effective. However, not all men respond equally, with some responding very well and others progressing early. Personalising treatments require tools that can accurately measure treatment responses, preferably early in the treatment course, so adjustments to treatment can be made. Lutetium-PSMA can measure tumour sites after each therapy by taking whole body 3D images at 24 h using a small radiation wave from the treatment itself. This is called a SPECT scan. Previous work has shown that both prostate-specific antigen (PSA) response and changes in tumour volume on a SPECT scan can predict how patients will respond to treatment as early as dose 2. This study demonstrates that stratifying how men are treated based on the results of the 6-week SPECT scan and PSA response potentially allows a third of men to have break in treatment and that these men have both longer time to disease progression and OS. Men with an increase in tumour volume and increase in PSA early in treatment (6 weeks) had shorter time to disease progression and OS. Men with early biomarker disease progression were offered alternative treatments early in an attempt to allow the opportunity to allow a more effective potential therapy, if one was available. The study is an analysis of a clinical programme, and was not a prospective trial. As such, there are potential biases that could influence results. Hence, while the study is encouraging for the use of early response biomarkers to guide better treatment decisions, this must be validated in a well-designed clinical trial.
2023-01-01·Journal of Cancer
Inhibition of STAT3 signaling as critical molecular event in HUC-MSCs suppressed Glioblastoma Cells
Article
作者: Wang, Mingming ; Liu, Yusi ; Xu, Xiangrong ; Zhang, Jing ; Jia, Yuna ; Shi, Haiyan ; He, Jing ; Zhang, Yunqing ; Zhang, Yufu ; Liu, Min
Objective: We investigated the effect of human umbilical cord mesenchymal stem cells (HUC-MSCs) supernatants on proliferation, migration, invasion, and apoptosis in glioblastoma (GBM) cell lines RG-2, U251, U87-MG, and LN-428, as well as their apoptosis and autophagy-mediated through IL-6/JAK2/STAT3 signaling pathway to explore the molecular mechanisms. Methods: In this study, RG-2, U251, U87-MG, and LN-428 cells were treated with 9 mg/ml HUC-MSCs supernatants. Their responses to HUC-MSCs supernatants treatment and the status of STAT3 signaling were analyzed by multiple experimental approaches to elucidate the importance of HUC-MSCs supernatants for GBM. Results: The results demonstrated that after treatment with HUC-MSCs supernatants, in vitro proliferation of RG-2, U251, U87-MG, and LN-428 cells were inhibited, and their sustained growth was also blocked. RG-2, U251, and U87-MG cells showed significant S phase accumulation, while LN-428 cells were blocked in G0/G1 phase. Their migratory invasive capacities were inhibited, and their apoptosis and autophagy ratios were increased. These effects were mediated through the IL-6/JAK2/STAT3 and its downstream signaling pathway. Conclusion: Our data showed that HUC-MSCs supernatants had anti-tumor effects on GBM cells. It inhibited the proliferation, migration, and invasion of GBM cells and promoted their apoptosis. Negative regulation of the IL-6/JAK2/STAT3 signaling pathway enhanced apoptosis and autophagy in tumor cells, thereby improving the therapeutic effect on GBM.
41
项与 RG002C0106 相关的新闻(医药)2026-05-06
引言:肾脏疾病治疗的迫切需求与补体系统新靶点
慢性肾脏疾病已成为全球范围内对人类健康构成重大威胁的临床问题,其高患病率、低知晓率以及患病后的高死亡率和致残率,让无数患者和家庭承受着沉重的负担。在中国,肾脏疾病患者群体庞大,而其中相当一部分患者伴随着不同程度的肾功能不全。对于这些患者而言,药物治疗面临着特殊的挑战——肾功能不全会显著影响药物的代谢和排泄,可能导致药物在体内蓄积,增加不良反应风险。
在这一背景下,补体系统作为人体天然免疫系统的重要组成部分,近年来成为肾脏疾病治疗研究的热点靶点。补体因子C3作为补体激活途径的核心因子,在多种肾脏疾病的发病机制中扮演着关键角色。然而,传统补体抑制剂往往存在给药频繁、作用时间短、特异性不足等问题,难以满足临床长期治疗的需求。
RG002C0106:全球首批进入临床阶段的C3靶向siRNA药物
RG002C0106注射液是由炫景生物自主研发的靶向补体因子C3的小干扰核酸(siRNA)I类创新药。这款药物基于炫景生物自主建立的RIHOST®、RICMO®、LICOD®等核心技术平台,利用其自主开发的第二代N'-乙酰半乳糖胺(GalNAc)缀合技术开发而成。
与现有疗法相比的预期优势
RG002C0106作为全球首批进入临床阶段的靶向补体C3的小干扰核酸(siRNA)药物,与现有IgA肾病疗法相比具有多方面的预期优势:1. 作用机制更精准,直击疾病核心
现有IgA肾病治疗主要依赖传统激素、免疫抑制剂(如环磷酰胺、霉酚酸酯)以及支持治疗(RAS抑制剂、SGLT2抑制剂等),这些疗法多为非特异性免疫抑制,副作用较大且疗效有限。
RG002C0106采用GalNAc偶联siRNA技术,能够特异性沉默肝脏中补体C3基因的表达,从源头抑制C3蛋白的生成。补体C3在IgA肾病的发病机制中发挥核心作用,几乎所有IgA肾病患者肾组织中均有明显的C3沉积。这种精准靶向机制有望实现更高效、更特异的治疗效果。2. 长效作用,大幅提高患者依从性
传统免疫抑制剂需要每日或频繁给药,而RG002C0106的I期临床研究显示,单次和重复给药均能实现持续的C3抑制以及补体通路的下调,结果支持后续开展季度或更长给药间隔的方案。这种长效特性将显著提高患者依从性,减少因漏服药物导致的疗效波动。3. 安全性优势显著
I期临床试验(NCT06494527)在50例中国健康受试者中评估了RG002C0106的安全性,剂量范围为25mg至600mg。结果显示:未观察到严重不良事件(SAEs);无因不良事件(AEs)导致的停药;药物耐受性良好。与传统免疫抑制剂常见的感染、骨髓抑制、肝肾功能损害等严重副作用相比,RG002C0106显示出更好的安全性特征。4. 临床前疗效数据令人鼓舞
在食蟹猴(NHP)疾病模型中,RG002C0106显示出显著的肾脏保护作用:尿蛋白/肌酐比(uPCR)较基线下降超过50%。这一数据为RG002C0106在IgA肾病患者中的潜在疗效提供了有力支持。5. 全球竞争优势明显
与同靶点竞品(如美国箭头公司开发的ARO-C3)相比,RG002C0106在临床前灵长类动物研究中表现出更优的药效,单次给药后药效可持续数月,并且是全球首次在IgA肾病食蟹猴模型中高效达成临床终点指标。这使其有望成为同类最优(best-in-class)药物。6. 满足巨大未满足临床需求
IgA肾病是全球最常见的原发性肾小球疾病,也是我国青壮年尿毒症的首要病因。全球患者超过8亿,仅中国患者就超过千万。目前全球尚无专门针对IgA肾病的靶向特效药,RG002C0106有望填补这一全球治疗空白。
2024年,RG002C0106注射液获得国家药品监督管理局药物临床试验批准通知书(通知书编号:2024LP01976),正式启动“评价RG002C0106注射液在肾功能正常和轻-中度肾功能不全的成年试验参与者中的安全性、耐受性、药代动力学和药效学特征的I期临床研究”(方案编号:RG002C0106-102)。
研究设计的科学性与创新性:
这项研究的设计体现了对特殊用药人群的高度关注。研究计划在全国招募22-24名试验参与者,其中包括:
肾功能正常试验参与者8例
轻度肾功能不全试验参与者8例
中度肾功能不全试验参与者6-8例
研究主要目的:
比较单次注射RG002C0106在肾功能正常、轻度肾功能不全和中度肾功能不全的试验参与者中的药代动力学特征
评估RG002C0106在肾功能不全患者中的安全性和耐受性肾功能不全患者的药代动力学挑战
肾功能不全患者的药代动力学特点与健康人群存在显著差异,这直接影响药物的安全性和有效性:
吸收方面:肾功能不全患者常伴有胃肠功能紊乱,如腹泻、呕吐,这些均可能减少药物的吸收。同时,维生素D羟化不足也会影响某些药物的吸收。
分布方面:大多数药物在肾功能不全患者体内表现为分布容积增加,而某些蛋白结合率低的药物分布容积可能无改变。特别值得注意的是,酸性药物的蛋白结合率会下降,导致游离血药浓度增高,作用增强,毒性增加。
代谢方面:尿毒症患者可能出现维生素D3的第二次羟化障碍等代谢改变。
排泄方面:这是肾功能不全影响最显著的环节。肾小球滤过减少会导致地高辛、普鲁卡因胺、氨基糖苷类抗生素等药物容易在体内蓄积。肾小管分泌减少是由于尿毒症患者体内蓄积的内源性有机酸可与弱酸性药物在转运上发生竞争。肾小管重吸收增加则是因为肾功能不全患者体内酸性产物增加,尿液pH值下降,弱酸性药物离子化减少,重吸收增加。
正是基于这些复杂的药代动力学变化,专门针对肾功能不全患者的临床研究显得尤为重要。RG002C0106-102研究正是为了系统评估这一创新药物在肾功能不全人群中的药代动力学特征,为后续临床用药提供科学依据。已有临床研究数据回顾:安全性与有效性的坚实基础
在开展肾功能不全人群研究之前,RG002C0106已经在健康受试者中完成了初步的I期临床研究,并取得了令人鼓舞的结果。
健康受试者I期研究(NCT06494527)关键发现:
研究规模:50例中国健康受试者参与
剂量范围:单次或多次皮下注射,剂量范围为25mg至600mg
安全性表现:未观察到严重不良事件(SAEs);无因不良事件(AEs)导致的停药;药物耐受性良好
药效学数据:RG002C0106在整个剂量范围内显著且持续地降低了血清C3水平,并同时抑制了经典和替代性补体通路的活化
临床前研究数据支持:
在转基因hC3小鼠和食蟹猴(NHP疾病模型)中,RG002C0106显示出对肝组织C3 mRNA及血清C3蛋白的显著抑制作用。特别是在NHP疾病模型中,其尿蛋白/肌酐比(uPCR)较基线下降超过50%,显示出显著的肾脏保护作用。
这些数据为RG002C0106在肾功能不全患者中的研究奠定了坚实的基础,也增强了研究者对药物安全性的信心。研究进展与患者招募现状
目前,RG002C0106-102研究正在全国范围内积极推进患者招募工作。河南科技大学第一附属医院作为参与中心之一,已经启动了试验参与者的招募工作。
患者招募标准:
年龄要求:成年试验参与者
分组情况:包括肾功能正常、轻度肾功能不全和中度肾功能不全三组
研究设计:采用严格的入组标准和排除标准,确保研究数据的科学性和可靠性
研究时间线:
根据公开信息,RG002C0106的整体研发进展迅速。2024年8月30日,该药物获得中国国家药品监督管理局药品审评中心(CDE)批准开展临床试验。同年8月22日,还获得了澳大利亚人类研究伦理委员会(HREC)批准开展临床I期试验研究。2024年10月23日,RG002C0106在北京友谊医院研究型病房顺利完成临床I期试验的首例受试者给药。
更令人振奋的是,RG002C0106的研发已经进入II期临床阶段。2025年8月23日,炫景生物主办的“RG002C0106-201临床试验全国研究者会”在北京顺利举办,启动了在原发性IgA肾病受试者中评价RG002C0106注射液的安全性、初步有效性及其药代/药效动力学特征的多中心、随机、双盲、安慰剂对照的IIa期临床研究(临床试验登记号:CTR20253001)。临床意义与患者价值
对肾功能不全患者的特殊价值:
个体化用药指导:通过系统研究RG002C0106在肾功能不全患者中的药代动力学特征,为临床医生提供精准的剂量调整依据
安全性保障:明确药物在肾功能不全人群中的安全性和耐受性,避免因药物蓄积导致的毒性反应
治疗机会平等:确保肾功能不全患者能够安全有效地使用这一创新疗法,不因肾功能状态而被排除在治疗之外
对肾脏疾病治疗领域的贡献:
填补临床空白:这是全球首个专门针对肾功能不全患者设计的补体C3靶向siRNA药物临床研究
推动精准医疗:为肾功能不全患者的个体化治疗提供科学依据
拓展适应症范围:为RG002C0106在更广泛患者群体中的应用奠定基础技术平台优势与创新突破
炫景生物在RG002C0106研发过程中展现的技术实力令人瞩目。公司开发了具有全球自主知识产权、行业领先的多个小核酸药物研发技术平台,包括药物设计筛选技术平台RIHOST®、化学修饰技术平台RICMO®和药物递送技术平台LICOD®。相关技术平台已申请超30件发明专利,其中5件已获专利授权。
GalNAc缀合技术的突破:
RG002C0106采用的第二代N'-乙酰半乳糖胺(GalNAc)缀合技术,能够实现药物在肝脏的特异性递送。GalNAc是一种特异性识别肝细胞表面去唾液酸糖蛋白受体(ASGPR)的配体,通过GalNAc修饰,siRNA药物能够高效、特异性地被肝细胞摄取,从而在肝脏中发挥靶向沉默C3基因的作用。
这一技术不仅提高了药物的靶向性和疗效,还显著降低了全身暴露带来的潜在副作用,为长期治疗提供了可能。未来展望与临床开发计划
根据炫景生物的研发规划,RG002C0106有望成为同类最优及全球首批上市的靶向C3的siRNA药物。公司预计该药物将于2028/2029年实现首发适应症获批上市,峰值年销售额将超20亿元。
后续临床开发策略:
扩大适应症范围:除了已经获批的肾小球疾病和补体介导的溶血性疾病,RG002C0106还有望拓展至其他补体介导的疾病领域
优化给药方案:基于I期研究的药代动力学数据,探索更优化的给药间隔和剂量方案
联合治疗探索:研究RG002C0106与其他肾脏疾病治疗药物的联合应用潜力
长期安全性评估:开展长期随访研究,评估药物的长期安全性和持久疗效
对肾脏疾病治疗格局的影响:
RG002C0106的成功开发有望彻底改变补体介导肾脏疾病的治疗格局。与传统补体抑制剂相比,siRNA药物具有作用持久、给药间隔长、特异性高等优势。单次和重复给药均能实现持续的C3抑制以及补体通路的下调,研究结果支持后续开展季度或更长给药间隔的方案。结语:开启肾功能不全患者精准治疗新时代
RG002C0106注射液在肾功能正常和轻-中度肾功能不全成年试验参与者中的I期临床研究,不仅是一项科学的临床试验,更是对肾功能不全患者用药安全的高度负责。这项研究将为我们提供宝贵的数据,指导临床医生如何在这一特殊人群中安全、有效地使用这一创新疗法。
随着我国人口老龄化进程加快,慢性肾脏疾病的患病率持续上升,肾功能不全患者的药物治疗需求日益迫切。RG002C0106的研究进展,为这些患者带来了新的希望。通过精准靶向补体C3,这一创新药物有望为肾功能不全患者提供更安全、更有效、更便捷的治疗选择。
我们期待RG002C0106-102研究能够顺利推进,早日为临床提供科学依据,让更多肾功能不全患者能够从这一创新疗法中获益。同时,这也将推动我国在创新药物研发和特殊人群用药研究方面达到新的高度,为全球肾脏疾病治疗贡献中国智慧和中国方案。
【报名资料】
1.肾病病历
2.血液检查
3.用药记录
【研究中心】河南科技大学第一附属医院
参考文本来源:
【声 明】图文版权归属原始权利人,本平台非商业用途。观点仅代表作者本人,不代表本平台立场。如果本文侵犯了您的权利,请及时联系我们,以便洽谈授权或及时删除!
咨询可联系客服
2026-04-08
·今日头条
> 2026年4月8日,前沿生物药业(南京)股份有限公司(688221.SH)在投资者互动平台宣布,其靶向MASP-2的siRNA疗法FB7013注射液的中国Ⅰ期临床试验已获国家药品监督管理局(NMPA)批准开展。
公司表示正积极推进临床试验启动相关工作,但项目整体入组完成时间受志愿者招募等多重因素影响,暂无法具体预估。这一进展不仅是前沿生物小核酸管线的重要里程碑,也意味着针对IgA肾病这一全球最常见原发性肾小球疾病的治疗探索,增添了一种基于全新机制的长效潜在选择。
## 临床试验获批:从申报到启动筹备
根据公司公告,FB7013注射液的临床试验申请(IND)此前已获得受理,并于近期正式获得NMPA的批准通知书。目前,公司的工作重点已转向临床试验的启动筹备。然而,新药临床试验的推进充满变量,**志愿者招募**的进度将成为影响整体时间表的关键因素之一。
> 前沿生物在互动平台回答投资者提问时表示,FB7013中国Ⅰ期临床试验已获NMPA批准开展,目前公司正积极推进临床试验启动相关工作。
## FB7013解析:瞄准MASP-2的长效潜力
FB7013是前沿生物小核酸药物研发平台的先导产品,是一款**靶向MASP-2(甘露聚糖结合凝集素丝氨酸蛋白酶2)的siRNA疗法**,拟用于治疗原发性IgA肾病。IgA肾病作为一种常见的慢性肾脏病,存在巨大的未满足临床需求。
从技术路径看,该药物采用了目前应用较为广泛的**GalNac缀合递送系统**,旨在实现药物的精准靶向。根据公司披露的临床前研究数据,FB7013已显示出**长效治疗的潜力**,这为未来可能减少患者给药频率、提升治疗依从性提供了想象空间。
## 技术底气:双递送平台与巨头背书
前沿生物在小核酸领域的布局不止于单一技术。公司既应用了成熟的GalNac系统,又自主研发了旨在突破肝外递送难题的**siRNA递送载体——ACORDE平台**,并已提交国际发明专利申请。
更为市场关注的是,公司技术平台的全球竞争力获得了顶级药企的验证。2026年2月,前沿生物与**葛兰素史克(GSK)就肾科领域小核酸管线达成了总额超10亿美元的授权合作协议**。
- 该交易包含**4000万美元首付款及近期里程碑付款**,为公司研发注入了现金流。
- GSK的背书被视为对前沿生物ACORDE平台及其管线资产全球竞争力的**权威验证**。
## 市场竞速:IgA肾病治疗格局生变
IgA肾病治疗领域正处于创新活跃期。除了前沿生物等企业探索的补体途径靶向药物,其他机制疗法也在同步推进。例如,在2026年世界肾脏病大会(WCN)上,**靶向CD38的单抗菲泽妥单抗**公布了II期研究数据,展示了在降低蛋白尿的同时保留患者体液免疫安全的潜力。

此外,国内其他生物技术公司也在开发用于IgA肾病的siRNA药物,如炫景生物的RG002C0106管线已进入临床Ⅱ期研究。这预示着针对这一疾病的治疗选择未来可能更加多元化,竞争也将加剧。
## 公司转型:从小核酸平台驱动增长
前沿生物以国内首个原创长效抗艾药**艾可宁(艾博韦泰)** 起家,该产品构成了公司当前稳健的收入基本盘。
为寻求突破,公司战略性地将研发重心转向小核酸药物领域,构建了“**抗HIV药物+小核酸创新药+高端仿制药**”三大业务板块,其中**小核酸平台被视为驱动未来增长的核心引擎**。
与GSK的合作标志着公司“**自主研发+全球授权**”的商业模式获得成功开局,不仅验证了技术价值,也提升了其在全球资本市场的认知度。
## 挑战在前:临床验证之路仍存不确定性
尽管Ⅰ期临床试验获批是积极的信号,但FB7013的最终成药性仍需历经严格的临床验证。公司也在相关报告中提示了包括**临床转化不及预期**在内的多项风险。
短期来看,市场的关注点将集中于FB7013的临床启动及早期数据;中期则取决于其I/II期临床数据能否证明平台技术的成药性与市场价值。对于数千万IgA肾病患者而言,每一种新机制的探索都代表着新的希望,但从实验室到药房,这条道路依然漫长且充满挑战。
siRNA临床1期引进/卖出临床申请临床2期
2026-04-02
April 2,
2026
Innovative siRNA biotech
startup Rigerna Therapeutics has announced the completion of an additional
US$30m
financing
round
, led by
Bayland Capital
(Pharmaron CVC) and
other reputable healthcare investors. Since its inception, Rigerna has raised a
total of US$60m to support its mission of developing transformative therapies
for kidney diseases.
Its lead pipeline candidate,
RG002 (C3-siRNA), has entered Phase 2 trial in IgA nephropathy (IgAN) in China
and remains on track to a proof-of-concept readout in Q4 2026. RG002 is being
developed to become the 1
st
twice-yearly siRNA therapy for IgAN, with
the potential to reshape the treatment landscapes. “We are confident with the
Phase 2 trial based on early readouts,” Dr. Yuanyu Huang, founder of Rigerna, “We
look forward to sharing the exciting findings at the 2026 ASN meeting in November.”
Meanwhile, Rigerna is also
advancing kidney-targeting technologies for proximal tubule, distal tubule and
collecting duct cells. Delivering siRNA to specific renal cell types could
enable breakthrough therapies for a range of genetic kidney diseases in the
future. “We have made remarkable progresses in tackling those challenging
problems, and we believe that we can address the global unmet needs for renal
patients in the future.” Dr. Huang added.
About Rigerna
Rigerna is an innovative
siRNA biotech company dedicated to discovering therapies for kidney diseases.
Leveraging its proprietary modification platforms, the company has advanced its
initial pipeline into Phase 2 clinical trials, with the goal of developing a
first-in-class siRNA therapy for IgA nephropathy. In addition, Rigerna has
discovered a novel kidney-targeting approach and is pursuing proof-of-mechanism
in preclinical studies. Based in Suzhou and Beijing, Rigerna has attracted
experts in oligonucleotide therapeutics and innovative drug development. The
company welcomes diverse collaboration opportunities with pharmaceutical and
biotech partners.
Please contact
mma@rignerna.com
for further information.
More about Rigerna on
临床2期寡核苷酸
100 项与 RG002C0106 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 免疫球蛋白a肾病 | 临床2期 | 中国 | 2025-08-28 | |
| 肾小球疾病 | 临床1期 | 中国 | 2024-10-18 | |
| 非典型溶血性尿毒症综合征 | 临床申请批准 | 中国 | 2025-11-29 | |
| 冷凝集素病 | 临床申请批准 | 中国 | 2025-11-29 | |
| 阵发性睡眠性血红蛋白尿症 | 临床申请批准 | 中国 | 2025-11-29 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
