预约演示
更新于:2026-04-30
EMP-012
更新于:2026-04-30
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
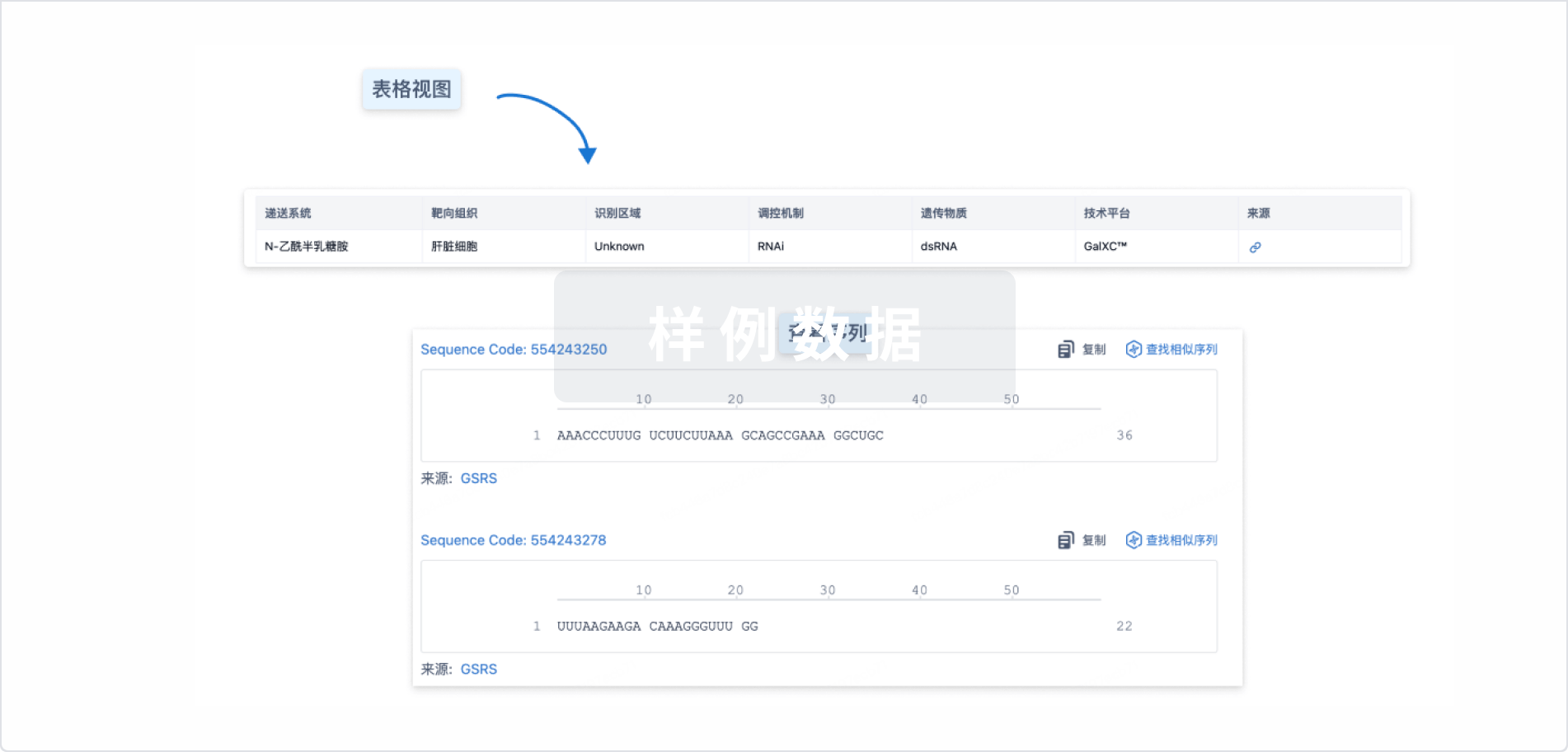
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
2
项与 EMP-012 相关的临床试验ISRCTN55493273
Phase 1 Trial: EMP-012-1
开始日期2025-02-24 |
申办/合作机构 |
ACTRN12624000650594
A 3-part study consisting of a randomised, double-blind, placebo-controlled, single ascending dose study in healthy participants, followed by an open-labelled single dose LPS-challenge study in healthy participants and an open-labelled multiple dose study in COPD patients to Assess the Safety, Tolerability, Pharmacokinetics, and Pharmacodynamics of EMP-012 for Injection Administered Subcutaneously. (PART A) *This registration is for Part A only (as Part B and Part C are registered separately from this on ISRCTN)
开始日期2024-07-31 |
申办/合作机构  Empirico, Inc. Empirico, Inc. [+1] |
100 项与 EMP-012 相关的临床结果
登录后查看更多信息
100 项与 EMP-012 相关的转化医学
登录后查看更多信息
100 项与 EMP-012 相关的专利(医药)
登录后查看更多信息
47
项与 EMP-012 相关的新闻(医药)2026-04-14
·禾开生物
1
COPD新疗法有哪些
慢性阻塞性肺疾病(COPD)作为全球高发的慢性呼吸系统疾病,长期受限于传统治疗手段,患者常面临症状反复、肺功能持续下降的困境。近年来,随着医学研究的不断突破,多款具有里程碑意义的新疗法相继问世,打破了20余年的治疗僵局。以下为大家梳理COPD五大新疗法,每一款都为患者带来了全新的呼吸希望。
表1.COPD新疗法TOP5
2
五大COPD新疗法
逐一介绍
1
PDE3/4双重抑制剂:
全球首个吸入式 PDE3/4 双抑制剂
Ensifentrine是一种首创的吸入性磷酸二酯酶3和4(PDE3和PDE4)双重抑制剂。其独特优势在于单药同时实现支气管扩张与抗炎双重效应:抑制PDE3可松弛气道平滑肌,抑制PDE4则能广泛抑制炎症细胞活性。此外,它还能激活囊性纤维化跨膜传导调节因子(CFTR),增强氯离子分泌和黏液纤毛清除功能,从多途径干预COPD病理过程。
Ensifentrine由Verona Pharma开发,于 2024 年 6 月获得FDA批准,用于成人COPD患者的维持治疗,是 20 多年来具有新作用机制的首个吸入式疗法。
关键III期临床试验ENHANCE-1和ENHANCE-2结果显示:与安慰剂相比,ensifentrine显著改善肺功能,FEV₁(第1秒用力呼气容积)分别增加87 mL和94 mL(p<0.001);在患者报告的结局指标和急性加重率方面也观察到显著获益。此外,Ensifentrine不依赖嗜酸性粒细胞计数,适用人群更为广泛。
图1. ENHANCE系列临床试验疗效数据
(来源:Verona Pharma官网)
2
IL-4Rα靶向生物制剂:
首个获批COPD适应症的靶向生物药
Dupilumab是一种全人源单克隆抗体,靶向IL-4受体α亚基(IL-4Rα),同时阻断IL-4和IL-13的信号传导——这两种细胞因子是2型炎症的核心驱动因素。约20%-40%的COPD患者存在嗜酸性粒细胞表型,其气道炎症由2型通路主导,对常规ICS反应欠佳。
Dupilumab由赛诺菲/再生元开发,于2024年7月在欧盟获得批准用于COPD,成为首个针对COPD患者的靶向治疗生物药。2025年GOLD报告已将其纳入特定嗜酸性粒细胞表型患者的升级治疗选项。
关键III期临床试验BOREAS和NOTUS结果显示:对于血嗜酸性粒细胞≥300细胞/μL的患者,与安慰剂相比,dupilumab可使中重度急性加重年发生率降低30%,同时FEV₁较基线改善160 mL,且在52周内持续维持。
图2. BOREAS 和 NOTUS 试验数据[1]
3
IL-5靶向生物制剂:
每月一次给药的便利选择
Mepolizumab是一种靶向IL-5的单克隆抗体。IL-5是嗜酸性粒细胞成熟、活化和存活的关键细胞因子。通过精准中和IL-5,mepolizumab可减少嗜酸性粒细胞介导的气道炎症,而不广泛抑制其他免疫功能。
该药于2025年5月在美国获批COPD新适应症,并于2025年12月在中国获批,成为中国首个且唯一每月给药一次、用于治疗血嗜酸性粒细胞计数(BEC)≥150细胞/μL的广泛COPD患者的生物制剂。
关键III期临床试验MATINEE(52-104周)结果显示:在标准三联吸入治疗基础上加用mepolizumab,可使中重度急性加重年发生率降低21%(率比0.79,p=0.01);更值得注意的是,导致住院或急诊就诊的急性加重风险降低35%(率比0.65),这对减轻患者和医疗系统负担具有重要意义。
Mepolizumab为中国近1亿COPD患者中约67%的嗜酸性粒细胞表型患者提供了新的治疗选择。其每月一次皮下注射的给药方式,有望提高长期治疗的依从性。
图3.COPDIII期临床试验试验数据[2]
4
siRNA核酸药物:
基因沉默技术进军非2型炎症
EMP-012由Empirico公司发现,2025年10月,GSK以8500万美元首付款、总计6.6亿美元里程碑付款获得其全球独家许可。该药是一款针对性极强的siRNA寡核苷酸,现在正处于针对慢性阻塞性肺病(COPD)的I期临床试验阶段。
作为寡核苷酸药物,EMP-012的作用机制是“从基因根源上沉默”致病表达,能精准阻断COPD炎症通路中关键蛋白的生成,实现对因治疗,而非停留在对症缓解的层面。
EMP-012瞄准的炎症通路有潜力成为“不依赖基线2型炎症、不考虑吸烟史、不考虑共病情况”的通用治疗方案。对那些不符合生物制剂治疗条件、反复加重住院的患者来说,siRNA技术可能是他们等了多年的新希望。
图4. EMP-012新闻稿
(来源:Verona Pharma官网)
5
干细胞与再生医学:
从缓解症状到修复组织
间充质干细胞(MSCs)具有多向分化潜能、免疫调节和组织修复能力。MSCs可通过分泌前列腺素E2(PGE2)、IL-10等因子,将促炎的M1巨噬细胞转化为抗炎的M2型;同时,其分泌的外泌体(exosomes)可携带miRNA(如miR-22-3p、miR-30b-3p)调控NF-κB等炎症通路,抑制炎症反应。更重要的是,MSCs还能促进线粒体转移,保护肺泡上皮细胞免受氧化应激损伤,并分泌肝细胞生长因子(HGF)、血管内皮生长因子(VEGF)等促进组织修复。
目前全球范围内尚无正式获批用于COPD的干细胞疗法,但多项临床前研究和早期临床试验正在推进。动物实验表明,MSCs可有效改善香烟烟雾或臭氧诱导的肺气肿和气道炎症。外泌体疗法因其较低的免疫原性和易于穿透肺生物屏障的特性,成为新的研究热点。
与现有药物仅能控制症状不同,干细胞疗法的终极目标是修复受损的肺实质和肺泡结构,真正延缓或逆转疾病进展。尽管仍面临致瘤性、标准化生产、长期安全性等挑战,但这一方向代表着COPD治疗的未来愿景。
图5.MSCs对呼吸系统疾病的治疗机制 [3]
文末小好奇:
参考文献:
1.Bhatt SP, Rabe KF, Hanania NA. Dupilumab for chronic obstructive pulmonary disease with type 2 inflammation: a pooled analysis of two phase 3, randomised, double-blind, placebo-controlled trials. Lancet Respir Med. 2025 Mar;13(3):234-243.
2.Sciurba F, et al. Mepolizumab to prevent exacerbations in COPD with an eosinophilic phenotype. N Engl J Med. Apr 2025;392:1710-1720. Available at nejm.org.
3.袁园园, 岳乐淇, 张华兴, 武艳, 李全海. 间充质干细胞在呼吸系统疾病模型中肺组织分布及治疗机制的研究进展[J/OL]. 中华细胞与干细胞杂志(电子版), 2024, 14(06): 374-381.
作者:方圆几里
审核:丁颖
编辑:景妍
禾开生物 ——“自身免疫模型专家”,是一家专注于自身免疫疾病领域体内药效服务的临床前研究 CRO 公司。禾开生物核心技术团队具备 20 年以上自身免疫疾病新药开发经验,公司已通过 ISO9001 质量体系认证,拥有位于苏州工业园区的分子、细胞、病理、小动物及检测试验基地,以及广西、苏州两地的非人灵长类试验基地。目前员工近 60 人,项目负责人均具有硕博士以上学历,团队累计完成过 300 多项新药 IND 申报经验,擅长处理自免新药研发和申报过程中的各种疑难问题。
• 50+非人灵长类动物自免疾病模型。
• 300+自身免疫性疾病动物模型。
• 500+项自身免疫性疾病IND申报经验。
免责声明:文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部责任。本公众号发布的各类文章重在分享,如有侵权请联系我们,我们将会删除。
2026-02-27
2 月 27 日晚间,前沿生物(688221.SH)披露 2025 年度业绩快报,去年公司实现营收 1.44 亿元,同比增长 10.96%;扣非后净利润亏损 2.96 亿元,较上年亏损收窄 3107.03 万元。业绩快报再次提到上市公司小核酸(以下又称 siRNA)管线产品达成重要国际合作一事。2 月 23 日(春节假期休市最后一天)晚间,上市公司已披露,其与葛兰素史克公司(下简称 GSK)签署独家授权许可协议,将两款小核酸管线产品的全球独家开发、生产及商业化权利授予对方。根据协议,前沿生物将获得 4000 万美元首付款、1300 万美元近期里程碑付款,公司还将额外在两个项目中累计获得最高 9.5 亿美元的基于成功开发、监管及商业化里程碑的付款。也就是说,交易总金额突破 10 亿美元。然而,这一重磅 BD(商务拓展)并未提振前沿生物股价。在春节假期后的首个交易日(2 月 24 日),前沿生物股价大涨 9.29%。但此后三个交易日中,公司股价上演"过山车"行情,累计下跌 14.17%,回吐了此前的所有涨幅。从大涨到下跌,这笔看似救急的交易,似乎还不足以驱散市场的疑虑。"" 前沿生物股价 5 日走势图 图片来源:百度截图前沿生物书面回复《每日经济新闻》称,本次交易对公司财务层面产生了积极且切实的影响。首付款直接增加公司现金流,为核心管线研发提供资金支撑;中长期的里程碑付款与销售提成,为公司提供可预期的收入来源,有望持续带来现金流。 GSK 为何看中了前沿生物?根据公告,GSK 将获得前沿生物旗下两款小核酸管线产品在全球范围内的独家开发、生产及商业化权利,其中一款候选药物已进入新药临床试验申请(IND)阶段。前沿生物方面并未在公告中详细披露上述两款小核酸产品的靶点、适应证等信息。根据公司官网披露的研发管线进展,前沿生物目前共有 7 款小核酸药物产品在研,治疗领域涵盖肝炎、高尿酸血症与痛风、肿瘤、高脂血症等。其中提交 IND 的仅有一款代号为 FB7013 的产品,适应证为 IgA 肾病。"" 图片来源:公司官网截图另据前沿生物企业公众号,GSK 呼吸、免疫与炎症研发高级副总裁兼全球负责人 Kaivan Khavandi 提及:"该协议进一步强化了我们的免疫学管线,新增了两款具有潜在全球首创价值的寡核苷酸(寡核苷酸包括小核酸)疗法,为改善多种肾病患者预后带来重要机遇。"本次前沿生物与 GSK 达成授权合作的两款产品均处于早期研发阶段,这与去年以来达成的多笔重磅 BD 呈现出相似特征。有分析师向记者表示,此类合作本质是跨国药企以相对较低的前期成本锁定潜在技术平台或创新靶点。同时,跨国药企对中国创新药资产的关注,正从"临床验证后的管线"转向"尚未成熟的创新分子"和底层研发平台能力。资料显示,相较于传统小分子和生物药,以 siRNA 药物为代表的核酸疗法可精准沉默致病蛋白,高效降解且作用时间长,目前已成为新药开发热门方向。据 Evaluate 和 BCG 预测,2026 年全球寡核苷酸类药物市场规模将超 150 亿美元,2020 年至 2025 年复合年增长率 35%。从 GSK 的角度看,其对小核酸药物的布局实则谋划已久,并已然形成较为系统的合作版图:早在 2021 年 11 月,GSK 便与 Arrowhead 公司达成合作,引进后者治疗非酒精性脂肪性肝炎(NASH)的 RNAi 疗法 ARO-HSD。2022 年 12 月,GSK 又与 Wave Life Sciences 公司签署总额约 33 亿美元的合作协议,共同推进寡核苷酸药物的研究。近两年,GSK 的合作重心进一步向具体适应证延伸。2025 年 10 月,GSK 宣布与 Empirico 公司合作开发针对慢阻肺的 siRNA 项目 EMP-012,总交易额约 7.45 亿美元。而此次与前沿生物的合作,则延伸至肾病方向。这恰恰也是国内小核酸药物的优势领域。据 Cytiva 发布的《中国小核酸药物行业发展报告》,截至 2024 年 1 月,我国开展的小核酸药物研发项目共 35 项,大多数处于临床早期阶段。与国外不同的是,我国药企基本直接跳过了小核酸药物罕见病适应症的研发,而是聚焦心血管系统疾病和肝病等常见慢性疾病上,两者占比合计 68.3% 左右。主要原因在于我国慢性疾病患病人数庞大且发病总体呈上升趋势,市场发展空间大,这也使得国内药企聚焦小核酸药物在慢性疾病方面的研发。 前沿生物 5 年累计亏损超 17 亿元进入 2026 年,创新药领域的 BD 热潮仍在持续。但与此前"一个 BD 公告拉出多个涨停板"的情形不同,近期多起重磅合作公布后,相关公司股价反应较平淡,甚至后续出现明显回调。对于这一现象,CIC 灼识咨询总监卢李康在 1 月末接受《每日经济新闻》记者采访时分析称,资本市场对近期大额 BD 交易反应平淡,是多种因素共同作用的结果。一方面,可能是市场预期已提前消化。在交易正式公布前,市场可能已有传闻或预期,利好消息在公告时已被部分消化;另一方面,资本市场对标的资产长期价值的审慎评估,使得市场越来越关注 BD 交易背后的产品临床数据优劣、靶点创新性、市场格局等实质价值,而非单纯交易金额。具体到前沿生物的这笔交易中,两款小核酸药物管线均处于早期阶段,后续研究、审批至商业化周期漫长,不确定性极高。一个有力的参照是,就在本月,GSK 刚刚"退货"了一款数据更为成熟的在研小核酸药物。2 月初,Wave Life Sciences 公司宣布从 GSK 手中收回其罕见病药物 WVE-006 的全部权利。值得注意的是,GSK 退回 WVE-006 并非因为产品失败,而是源于公司的战略调整。双方达成共识,认为该罕见病项目应该由更专注该领域的公司主导推进,而 GSK 则将资源集中于患者基数更大的核心治疗领域。回溯这笔交易,GSK 在 2022 年 12 月为获得 WVE-006 的全球独家许可,曾支付了高达 1.7 亿美元的预付款。连这样一款曾被寄予厚望、拥有积极临床数据且交易对价不菲的药物,都可能因跨国药企的战略转向而被放弃,这无疑为前沿生物的合作前景敲响了警钟。股价"过山车"的背后,还有前沿生物的基本面现状。曾被一些媒体称为"抗艾第一股"的前沿生物,自 2020 年 10 月登陆科创板以来,始终未能实现盈利。财务数据显示,2020 年至 2024 年,公司的扣非净利润持续亏损,累计亏损金额超过 16 亿元。"" 前沿生物主要财务数据 图片来源:东方财富网页截图另就现金流情况而言,截至 2025 年三季度末,前沿生物的期末现金及现金等价物仅为 0.97 亿元。"" 图片来源:公告截图前沿生物方面向记者表示,公司早在数年前便聚焦小核酸赛道,并看好该领域的临床应用与市场前景。未来 3 到 5 年,公司将聚焦三大板块:一是深耕 HIV(艾滋病)治疗主业,依托在该领域积累的研发团队、技术与人才优势,围绕差异化临床需求布局新产品,争取推进一款新的创新药早研产品进入 PCC(临床前候选化合物)阶段;二是推进高端仿制药上市,弥补公司现金流,为创新研发提供支撑;三是重点布局小核酸创新药领域,同时探索与公司技术能力、产能布局具备协同性的新品种。每日经济新闻
2026-02-25
With no buyer, BioMarin pulls gene therapy from shelvesGSK inks $1B kidney-focused siRNA pactFDA approves Immedica's ultra-rare metabolic disease therapyPatient death triggers partial hold of MacroGenics' mid-stage cancer studyWith no buyer, BioMarin pulls gene therapy from shelvesHaving failed to find a buyer for its haemophilia A gene therapy, BioMarin Pharmaceutical said Monday that it will withdraw Roctavian (valoctocogene roxaparvovec-rvox) from the market. The company announced plans to divest the programme in October, after the therapy posted third-quarter sales of just $3 million. According to BioMarin, it "undertook a comprehensive effort to identify a potential buyer."In connection with its decision to pull Roctavian from shelves, BioMarin said it will take a $240 million charge, including a $119-million inventory write-off. -Elizabeth EatonGSK inks $1B kidney-focused siRNA pact GSK has agreed to shell out $40 million upfront for global rights to two siRNA programmes from China's Frontier Biotechnologies in a deal that could net the Chinese drugmaker up to $963 million in milestones, plus tiered royalties (see – Vital Signs: Charting China's course westward into 2026).In return, the UK drugmaker obtains exclusive worldwide rights to the two assets; one candidate is at the IND stage, while the second remains preclinical. Frontier will advance one programme through a Phase I study in China and complete IND-enabling work on the other before GSK assumes responsibility for global clinical development, regulatory filings and commercialisation."This agreement further strengthens our immunology pipeline, adding two potential first-in-class oligonucleotide therapies with significant opportunity to improve patient outcomes across multiple kidney diseases," said Kaivan Khavandi, global head for respiratory, immunology and inflammation R&D at GSK.The Frontier pact follows GSK's licensing deal with Empirico last October for rights to a Phase I siRNA programme, EMP-012, in chronic obstructive pulmonary disease. Empirico received $85 million upfront and is eligible for up to $660 million in milestones.-Anna BratulicFDA approves Immedica's ultra-rare metabolic disease therapyThe FDA on Monday awarded Immedica Pharma's arginine specific enzyme therapy, Loargys (pegzilarginase-nbln), with an accelerated approval to treat hyperargininaemia in patients 2 years and older with arginase 1 deficiency (ARG1-D) in conjunction with dietary protein restriction. The treatment is expected to be available in the US starting in April. The clearance was based on findings from the Phase III PEACE trial, in which Loargys significantly reduced plasma arginine from baseline compared with placebo at 24 weeks. According to Immedica, the therapy is the first and only treatment to address persistently elevated levels of plasma arginine, the disease's main driver. ARG1-D is an ultra-rare progressive metabolic disease that affects an estimated 250 people living in the US.-Elizabeth EatonPatient death triggers partial hold of MacroGenics' mid-stage cancer studyMacroGenics said Monday that the FDA has placed a partial clinical hold on the Phase II LINNET study of its experimental cancer drug lorigerlimab following a patient death, pausing patient enrolment. The company reported safety events that occurred across four patients, including two cases of grade 4 thrombocytopenia, one report of grade 4 myocarditis, and one patient with grade 4 neutropenia and concurrent septic shock, which resulted in their death. MacroGenics has dosed 41 patients with platinum-resistant ovarian cancer or clear cell gynaecologic cancer with lorigerlimab, a bispecific DART molecule that targets PD-1 and CTLA-4. Though enrolment is paused, study participants can continue to receive lorigerlimab."MacroGenics is fully committed to working closely with the FDA to resolve the partial clinical hold and we intend to resume study enrollment as soon as possible," said CEO Eric Risser.-Elizabeth Eaton
临床3期临床2期引进/卖出上市批准临床结果
100 项与 EMP-012 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 慢性阻塞性肺疾病 | 临床1期 | 澳大利亚 | 2024-07-07 | |
| 炎症 | 临床1期 | - | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
