预约演示
更新于:2026-05-30
LDR2402
更新于:2026-05-30
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评- |
登录后查看时间轴
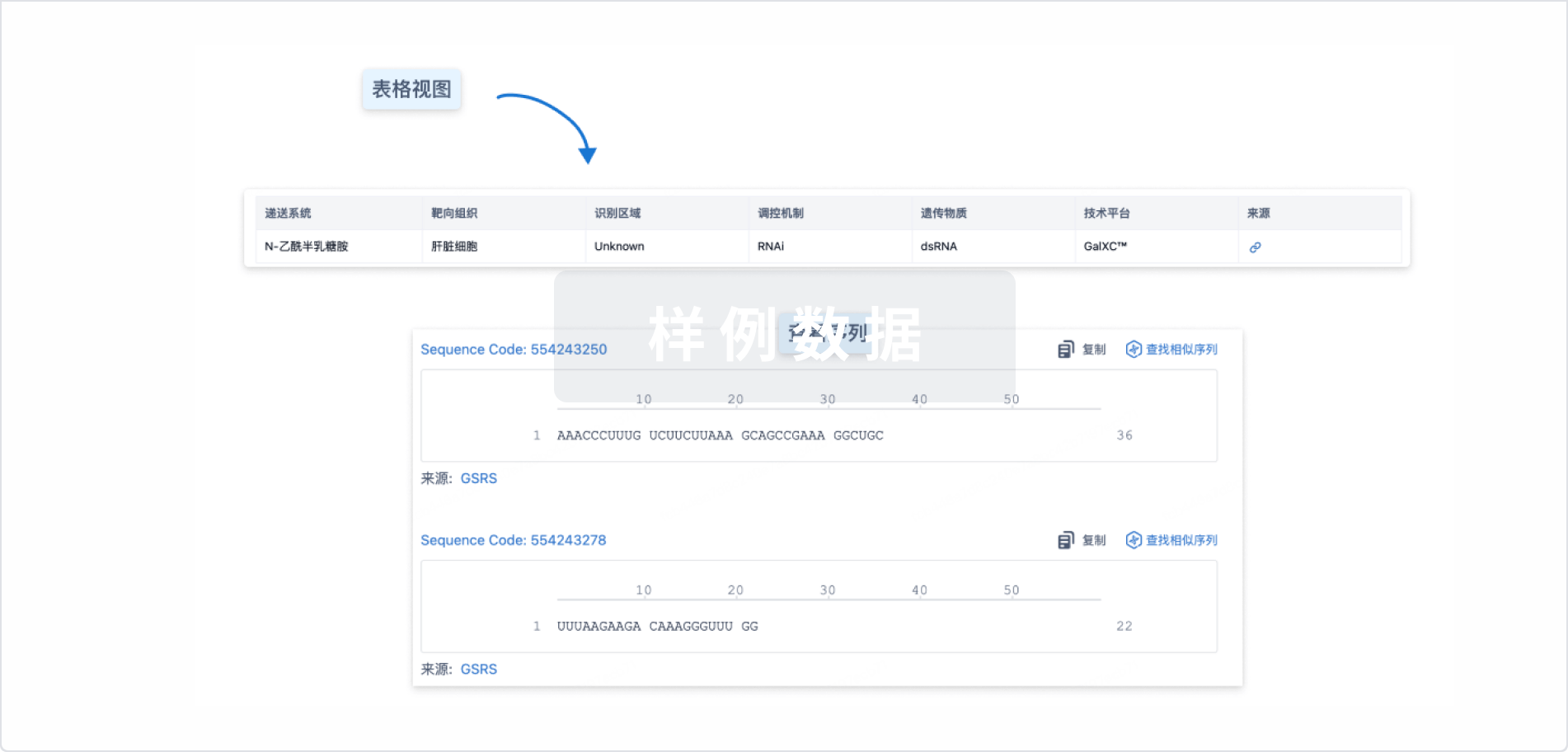
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
2
项与 LDR2402 相关的临床试验CTR20253348
一项评估 LDR2402 注射液在中国轻中度高血压受试者中的安全性及有效性的随机对照、双盲、多中心的 II 期临床研究
评估多次皮下注射 LDR2402 后的安全性与耐受性;
评估在多次皮下注射 LDR2402 后的药效学(PD)特征;
开始日期2025-09-22 |
申办/合作机构 |
CTR20244278
一项评估LDR2402注射液在中国健康受试者/轻度高血压受试者中的安全性、耐受性、药代动力学及药效学特征的随机、双盲、安慰剂对照的I期临床研究
1.评估单次皮下注射LDR2402后的安全性与耐受性。 2.评估单次皮下注射LDR2402后原型药的药代动力学(PK)特征。
开始日期2024-11-14 |
申办/合作机构 |
100 项与 LDR2402 相关的临床结果
登录后查看更多信息
100 项与 LDR2402 相关的转化医学
登录后查看更多信息
100 项与 LDR2402 相关的专利(医药)
登录后查看更多信息
127
项与 LDR2402 相关的新闻(医药)2026-05-29
·有驾
来源:新浪证券-红岸工作室
5月29日,成都先导跌0.60%,成交额7.50亿元,换手率6.34%,总市值118.72亿元。
异动分析
CRO概念+减肥药+重组蛋白+创新药+智能医疗
1、公司凭借DNA编码化合物技术的独特性,与国内其他药物发现CRO公司形成了较好的差异化竞争优势与技术壁垒,目前在国内药物发现CRO行业中属于具有技术特色的成长性企业。
2、根据2026年1月8日投资者关系活动记录表:先衍生物作为公司孵化和参股的子公司,已经建立起包括新颖的小核酸修饰技术、肝外递送技术和单分子双靶点调节技术在内的创新技术体系,并聚焦慢病治疗领域,布局针对高血压、高血脂、高体脂等疾病的小核酸新药管线。目前,其针对AGT靶点的超长效降压药物LDR2402已经进入Ⅱ期临床研究;用于治疗肥胖的小核酸新药LDR2515注射液(INHBE靶点)的临床试验申请(IND)已于近日获得中国国家药品监督管理局药品审评中心(CDE)受理。
3、公司能够提供一整套从靶基因到新药临床试验申请阶段的研发服务,覆盖范围包括重组蛋白表达纯化、结构生物学、计算化学与药物化学、生物化学和生物物理学、细胞生物学、体内药理学、药代动力学、药学研究等。
4、发行人的核心技术主要围绕DNA编码小分子化合物库技术,具体包括:DNA编码化合物库的设计、合成与表征纯化技术,生物靶点活性验证与 DNA编码化合物库筛选技术,以及基于 DEL 技术的自主创新药研发平台。
5、2025年半年报:公司基于 AI 模型主要聚焦两个方向的研究: 1) 利用成都先导已经积累的 DEL 筛选项目的大量数据集, 构建靶点-万亿化合物的亲和力预测模型, 赋能高质量苗头化合物发现环节; 2) 成都先导聚焦 AI 分子生成和评估、 高精度结合自由能计算以及 AI 成药性评估, 结合公司搭建的高效化学合成和高通量化合物检测平台, 建设 DEL+AI+自动化的“设计-合成-测试-分析”(DMTA) 分子优化的能力平台, 干湿结合加速化合物优化环节, 旨在通过建设迭代式的 DMTA 循环模式以加速临床前候选药物发现及优化过程。
(免责声明:分析内容来源于互联网,不构成投资建议,请投资者根据不同行情独立判断)
资金分析
今日主力净流入-2786.48万,占比0.04%,行业排名46/52,连续3日被主力资金减仓;所属行业主力净流入-4.07亿,连续3日被主力资金减仓。
主力持仓
主力没有控盘,筹码分布非常分散,主力成交额2.99亿,占总成交额的8.76%。
技术面:筹码平均交易成本为29.22元
该股筹码平均交易成本为29.22元,近期该股获筹码青睐,且集中度渐增;目前股价靠近支撑位28.55,注意支撑位处反弹,若跌破支撑位则可能会开启一波下跌行情。
公司简介
资料显示,成都先导药物开发股份有限公司位于四川省成都天府国际生物城(双流区生物城中路二段18号),成立日期2012年2月22日,上市日期2020年4月16日,公司主营业务涉及利用其核心技术-DEL技术提供药物早期发现阶段的研发服务以及新药研发项目转让。主营业务收入构成为:新药研发服务99.97%,其他(补充)0.03%。
成都先导所属申万行业为:医药生物-医疗服务-医疗研发外包。所属概念板块包括:科创企业同股同权、中盘成长、转融券标的、融资融券、沪股通等。
截至3月31日,成都先导股东户数2.58万,较上期增加25.56%;人均流通股15531股,较上期减少20.36%。2026年1月-3月,成都先导实现营业收入1.61亿元,同比增长50.40%;归母净利润4150.02万元,同比增长46.72%。
分红方面,成都先导A股上市后累计派现1.34亿元。近三年,累计派现4393.85万元。
机构持仓方面,截止2026年3月31日,成都先导十大流通股东中,香港中央结算有限公司位居第六大流通股东,持股615.80万股,相比上期减少526.54万股。
声明:市场有风险,投资需谨慎。本文基于第三方数据库自动发布,不代表新浪财经观点,任何在本文出现的信息均只作为参考,不构成个人投资建议。如有出入请以实际公告为准。如有疑问,请联系biz@staff.sina.com.cn。
2026-05-28
·百度百家
来源:新浪证券-红岸工作室
5月28日,成都先导跌5.81%,成交额7.57亿元,换手率6.28%,总市值119.44亿元。
异动分析
CRO概念+减肥药+重组蛋白+创新药+智能医疗
1、公司凭借DNA编码化合物技术的独特性,与国内其他药物发现CRO公司形成了较好的差异化竞争优势与技术壁垒,目前在国内药物发现CRO行业中属于具有技术特色的成长性企业。
2、根据2026年1月8日投资者关系活动记录表:先衍生物作为公司孵化和参股的子公司,已经建立起包括新颖的小核酸修饰技术、肝外递送技术和单分子双靶点调节技术在内的创新技术体系,并聚焦慢病治疗领域,布局针对高血压、高血脂、高体脂等疾病的小核酸新药管线。目前,其针对AGT靶点的超长效降压药物LDR2402已经进入Ⅱ期临床研究;用于治疗肥胖的小核酸新药LDR2515注射液(INHBE靶点)的临床试验申请(IND)已于近日获得中国国家药品监督管理局药品审评中心(CDE)受理。
3、公司能够提供一整套从靶基因到新药临床试验申请阶段的研发服务,覆盖范围包括重组蛋白表达纯化、结构生物学、计算化学与药物化学、生物化学和生物物理学、细胞生物学、体内药理学、药代动力学、药学研究等。
4、发行人的核心技术主要围绕DNA编码小分子化合物库技术,具体包括:DNA编码化合物库的设计、合成与表征纯化技术,生物靶点活性验证与 DNA编码化合物库筛选技术,以及基于 DEL 技术的自主创新药研发平台。
5、2025年半年报:公司基于 AI 模型主要聚焦两个方向的研究: 1) 利用成都先导已经积累的 DEL 筛选项目的大量数据集, 构建靶点-万亿化合物的亲和力预测模型, 赋能高质量苗头化合物发现环节; 2) 成都先导聚焦 AI 分子生成和评估、 高精度结合自由能计算以及 AI 成药性评估, 结合公司搭建的高效化学合成和高通量化合物检测平台, 建设 DEL+AI+自动化的“设计-合成-测试-分析”(DMTA) 分子优化的能力平台, 干湿结合加速化合物优化环节, 旨在通过建设迭代式的 DMTA 循环模式以加速临床前候选药物发现及优化过程。
(免责声明:分析内容来源于互联网,不构成投资建议,请投资者根据不同行情独立判断)
资金分析
今日主力净流入-1.01亿,占比0.13%,行业排名51/52,连续2日被主力资金减仓;所属行业主力净流入-4.43亿,连续3日被主力资金减仓。
主力持仓
主力没有控盘,筹码分布非常分散,主力成交额3.44亿,占总成交额的9.27%。
技术面:筹码平均交易成本为29.19元
该股筹码平均交易成本为29.19元,近期该股快速吸筹,短线操作建议关注;目前股价靠近支撑位28.55,注意支撑位处反弹,若跌破支撑位则可能会开启一波下跌行情。
公司简介
资料显示,成都先导药物开发股份有限公司位于四川省成都天府国际生物城(双流区生物城中路二段18号),成立日期2012年2月22日,上市日期2020年4月16日,公司主营业务涉及利用其核心技术-DEL技术提供药物早期发现阶段的研发服务以及新药研发项目转让。主营业务收入构成为:新药研发服务99.97%,其他(补充)0.03%。
成都先导所属申万行业为:医药生物-医疗服务-医疗研发外包。所属概念板块包括:科创企业同股同权、中盘成长、转融券标的、融资融券、沪股通等。
截至3月31日,成都先导股东户数2.58万,较上期增加25.56%;人均流通股15531股,较上期减少20.36%。2026年1月-3月,成都先导实现营业收入1.61亿元,同比增长50.40%;归母净利润4150.02万元,同比增长46.72%。
分红方面,成都先导A股上市后累计派现1.34亿元。近三年,累计派现4393.85万元。
机构持仓方面,截止2026年3月31日,成都先导十大流通股东中,香港中央结算有限公司位居第六大流通股东,持股615.80万股,相比上期减少526.54万股。
声明:市场有风险,投资需谨慎。本文基于第三方数据库自动发布,不代表新浪财经观点,任何在本文出现的信息均只作为参考,不构成个人投资建议。如有出入请以实际公告为准。如有疑问,请联系biz@staff.sina.com.cn。
2026-05-28
·有驾
来源:新浪证券-红岸工作室
5月28日,成都先导跌5.81%,成交额7.57亿元,换手率6.28%,总市值119.44亿元。
异动分析
CRO概念+减肥药+重组蛋白+创新药+智能医疗
1、公司凭借DNA编码化合物技术的独特性,与国内其他药物发现CRO公司形成了较好的差异化竞争优势与技术壁垒,目前在国内药物发现CRO行业中属于具有技术特色的成长性企业。
2、根据2026年1月8日投资者关系活动记录表:先衍生物作为公司孵化和参股的子公司,已经建立起包括新颖的小核酸修饰技术、肝外递送技术和单分子双靶点调节技术在内的创新技术体系,并聚焦慢病治疗领域,布局针对高血压、高血脂、高体脂等疾病的小核酸新药管线。目前,其针对AGT靶点的超长效降压药物LDR2402已经进入Ⅱ期临床研究;用于治疗肥胖的小核酸新药LDR2515注射液(INHBE靶点)的临床试验申请(IND)已于近日获得中国国家药品监督管理局药品审评中心(CDE)受理。
3、公司能够提供一整套从靶基因到新药临床试验申请阶段的研发服务,覆盖范围包括重组蛋白表达纯化、结构生物学、计算化学与药物化学、生物化学和生物物理学、细胞生物学、体内药理学、药代动力学、药学研究等。
4、发行人的核心技术主要围绕DNA编码小分子化合物库技术,具体包括:DNA编码化合物库的设计、合成与表征纯化技术,生物靶点活性验证与 DNA编码化合物库筛选技术,以及基于 DEL 技术的自主创新药研发平台。
5、2025年半年报:公司基于 AI 模型主要聚焦两个方向的研究: 1) 利用成都先导已经积累的 DEL 筛选项目的大量数据集, 构建靶点-万亿化合物的亲和力预测模型, 赋能高质量苗头化合物发现环节; 2) 成都先导聚焦 AI 分子生成和评估、 高精度结合自由能计算以及 AI 成药性评估, 结合公司搭建的高效化学合成和高通量化合物检测平台, 建设 DEL+AI+自动化的“设计-合成-测试-分析”(DMTA) 分子优化的能力平台, 干湿结合加速化合物优化环节, 旨在通过建设迭代式的 DMTA 循环模式以加速临床前候选药物发现及优化过程。
(免责声明:分析内容来源于互联网,不构成投资建议,请投资者根据不同行情独立判断)
资金分析
今日主力净流入-1.01亿,占比0.13%,行业排名51/52,连续2日被主力资金减仓;所属行业主力净流入-4.43亿,连续3日被主力资金减仓。
主力持仓
主力没有控盘,筹码分布非常分散,主力成交额3.44亿,占总成交额的9.27%。
技术面:筹码平均交易成本为29.19元
该股筹码平均交易成本为29.19元,近期该股快速吸筹,短线操作建议关注;目前股价靠近支撑位28.55,注意支撑位处反弹,若跌破支撑位则可能会开启一波下跌行情。
公司简介
资料显示,成都先导药物开发股份有限公司位于四川省成都天府国际生物城(双流区生物城中路二段18号),成立日期2012年2月22日,上市日期2020年4月16日,公司主营业务涉及利用其核心技术-DEL技术提供药物早期发现阶段的研发服务以及新药研发项目转让。主营业务收入构成为:新药研发服务99.97%,其他(补充)0.03%。
成都先导所属申万行业为:医药生物-医疗服务-医疗研发外包。所属概念板块包括:科创企业同股同权、中盘成长、转融券标的、融资融券、沪股通等。
截至3月31日,成都先导股东户数2.58万,较上期增加25.56%;人均流通股15531股,较上期减少20.36%。2026年1月-3月,成都先导实现营业收入1.61亿元,同比增长50.40%;归母净利润4150.02万元,同比增长46.72%。
分红方面,成都先导A股上市后累计派现1.34亿元。近三年,累计派现4393.85万元。
机构持仓方面,截止2026年3月31日,成都先导十大流通股东中,香港中央结算有限公司位居第六大流通股东,持股615.80万股,相比上期减少526.54万股。
声明:市场有风险,投资需谨慎。本文基于第三方数据库自动发布,不代表新浪财经观点,任何在本文出现的信息均只作为参考,不构成个人投资建议。如有出入请以实际公告为准。如有疑问,请联系biz@staff.sina.com.cn。
100 项与 LDR2402 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 原发性高血压 | 临床2期 | 中国 | 2025-09-22 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用