预约演示
更新于:2026-04-02
Zilganersen
更新于:2026-04-02
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段申请上市 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评优先审评 (美国)、突破性疗法 (美国)、孤儿药 (美国)、罕见儿科疾病 (美国)、孤儿药 (欧盟)、快速通道 (美国) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
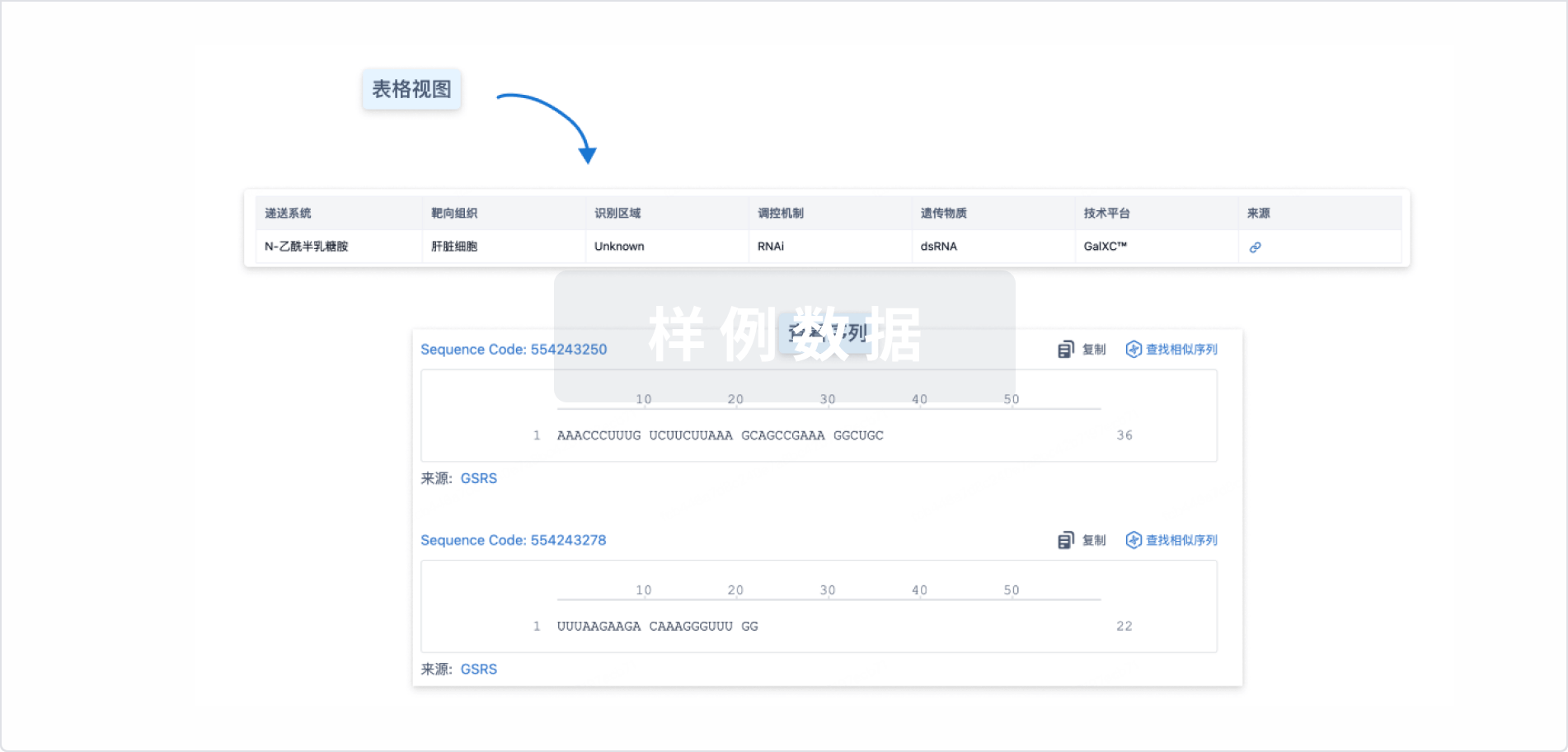
Sequence Code 544671472

来源: *****
关联
2
项与 Zilganersen 相关的临床试验NCT04849741
A Phase 1-3, Double-Blind, Randomized, Placebo-Controlled Study to Evaluate the Efficacy, Safety, Pharmacokinetics and Pharmacodynamics of Intrathecally Administered ION373 in Patients With Alexander Disease
The purpose of this study is to evaluate the safety and efficacy of zilganersen (ION373) in improving or stabilizing gross motor function across the full range of affected domains in patients with AxD.
开始日期2021-06-01 |
申办/合作机构 |
NCT07487389
Zilganersen Expanded Access Program for Individuals With Alexander Disease
The purpose of the expanded access program (EAP) is to provide access to zilganersen for eligible individuals with Alexander disease (AxD).
开始日期- |
申办/合作机构 |
100 项与 Zilganersen 相关的临床结果
登录后查看更多信息
100 项与 Zilganersen 相关的转化医学
登录后查看更多信息
100 项与 Zilganersen 相关的专利(医药)
登录后查看更多信息
69
项与 Zilganersen 相关的新闻(医药)2026-03-30
·财华恒医
核心观点
AACR大会将给创新药带来数据催化,中国企业继续闪耀
AACR年会将于2026年4月17-22日在美国圣地亚哥召开,今年共有超过100家中国药企亮相AACR,带来近400项研究成果,涵盖恒瑞、百济神州、荣昌生物、亚盛医药、先声药业、齐鲁制药、映恩生物、复宏汉霖、德琪医药等多家代表性企业。覆盖CDH17、Claudin18.2、HER2、Nectin-4等热门靶点,核药、DAC、细胞治疗、mRNA等前沿技术也将披露临床前数据。
大会有望带动创新药情绪回暖
从大会披露的信息来看,中国在多个主流赛道实现了稳定输出,包括ADC、双抗/双抗-ADC、蛋白降解剂以及放射性药物等方向。无论是项目数量密度、技术覆盖广度,还是学术讨论的参与深度,中国企业的存在感都显著提升。创新药具有极强的数据与事件催化属性,本次大会与五月的ASCO有望带动行业情绪回暖。
减重药市场进入口服时代
Orforglipron是一款口服GLP-1受体激动剂,礼来预计该药将在今年Q2获批。口服小分子相较于注射GLP-1与口服多肽有巨大优势,包括可显著扩大患者人群(减重维持与惧怕打针患者)、供应链稳定性、无需面临短缺风险、在联合用药、固定剂量复方制剂开发上更具灵活性,且无饮食饮水限制,每日一次给药即可,临床实践中更易被患者接受等。随着Orforglipron的获批上市,其产业链有望迎来巨大投资机会。
建议关注
投资建议:过往具有较好与礼来等MNC公司在小分子CDMO生产合作及具有放大生产能力的原料药、中间体及相关试剂公司,建议关注药明康德、诚达药业、海特生物、凯莱英、昊帆生物、康龙化成等。创新药关注具有解决未被满足临床需求、产生大单品的公司,建议关注恒瑞医药、万邦徳、复宏汉霖、荣昌生物、前沿生物、百济神州等公司。
风险提示
风险提示:行业反腐影响超出预期的风险;新药研发进展的不确定性风险;销售不达预期风险;集采降价超预期的风险等。
行业动态
诺和诺德:每周一次长效胰岛素在美国获批上市
3 月 27 日,诺和诺德宣布,美国 FDA 已批准 Awiqli®(icodec-abae 胰岛素)700 单位/毫升注射液,这是首款也是唯一一款每周一次给药的长效基础胰岛素,适用于成年 2 型糖尿病患者,作为饮食和运动的辅助手段,以改善血糖控制。
依柯胰岛素是一种新型长效胰岛素类似物,可与白蛋白可逆性结合,在循环系统形成储库并缓慢持续释放。在一周给药间隔内,依柯胰岛素降糖作用分布均匀,并且在临床相关剂量下降糖作用时间可覆盖一周。
海和药物:PI3Kα抑制剂在日本获批上市
3 月 23 日,海和药物宣布,其自主开发的 PI3Kα 选择性抑制剂甲磺酸瑞索利塞片(研发代号:CYH33;中文商品名:海泽欣®)获得日本厚生劳动省(MHLW)批准上市,用于治疗化疗后疾病进展且携带 PIK3CA 基因突变的卵巢透明细胞癌(OCCC)。
CYH33 是海和药物的一款强效、高选择性的小分子 PI3Kα抑制剂,具有全新的化学结构。本次获批主要基于 CYH33-G201 关键 II 期研究(NCT05043922;jRCT2031210216)的有效性与安全性数据。
Corcept:卵巢癌新药在美国获批上市
当地时间 3 月 25 日,Corcept Therapeutics 宣布,美国 FDA 已批准 Lifyorli™(relacorilant)上市,联合白蛋白结合型紫杉醇(nab-paclitaxel)用于治疗既往接受过 1 至 3 线全身治疗方案(其中至少一线包含贝伐珠单抗)的铂耐药性上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者。
Lifyorli 是首个获得 FDA 批准的选择性糖皮质激素受体拮抗剂(SGRA),可竞争性结合糖皮质激素受体(GR),通过抑制皮质醇对细胞凋亡的抑制作用来增强化疗敏感性。
Ionis:反义寡核苷酸疗法在美国申报上市
当地时间 3 月 23 日,Ionis 宣布,美国 FDA 已受理针对 zilganersen 的新药申请(NDA)并授予优先审评资格,FDA 已设定 PDUFA 目标行动日期为 2026 年 9 月 22 日。
Zilganersen 是一种反义寡核苷酸药物,用于治疗亚历山大病(AxD),这是一种罕见、渐进性且往往致命的神经系统疾病。如果获批,zilganersen将成为亚历山大病的首个也是唯一的治疗方法。
百利天恒:双抗 ADC 联用PD-1 临床数据首次公布
本周,2026 年欧洲肺癌大会(ELCC)在丹麦哥本哈根盛大召开。本次大会上,百利天恒以口头报告的形式,首次披露了 Iza-bren(EGFR×HER3 双抗 ADC)联合斯鲁利单抗,用于一线治疗广泛期小细胞肺癌(ES-SCLC)的临床研究成果。
本次大会公布该研究的 II 期结果,纳入人群均为初治的 ES-SCLC 患者。截至 2025 年 11 月 30 日,该 II 期研究共纳入 82 例患者:
队列 1:41 例患者接受 Iza-bren 2.5 mg/kg D1D8 Q3W 联合斯鲁利单抗一线治疗;
队列 2:41 例患者接受 Iza-bren 2.75 mg/kg D1D8 Q3W 联合斯鲁利单抗一线治疗。
主要研究终点为客观缓解率(ORR)和联合治疗的推荐 II 期剂量(RP2D)。
其中,队列 1 近半数患者基线伴肝转移,肿瘤负荷重,基线伴肝转移占比 48.8%,具体研究结果显示:
100% 患者靶病灶缩小且 85% 患者实现了深度缓解,中位缓解持续时间超过 7 个月:靶病灶缩瘤率 100%,中位缩瘤幅度达 64.4%;ORR 高达 85%,mDoR 7.3 个月;
最高 1 年 OS 率和 mPFS 突破 8 个月:1 年 OS 率最高,达 85.7%,mPFS 达 8.2 个月;
联合治疗方案安全可耐受:Iza-bren 联合斯鲁利单抗常见血液学毒性,患者无明显体感;同时,该联合方案肺部安全性良好,ILD 发生率低(2.4%),无≥3 级事件。Iza-bren 的停药率低,仅 2.4%,保障患者的长期用药获益。
吉利德收购康诺亚 NewCo
3 月 24 日,康诺亚宣布,其 NewCo 合作企业 Ouro Medicines 已与吉利德科学签署并购协议,吉利德将通过并购方式收购 Ouro Medicines,交易金额包括 16.75 亿美元首付款(可按惯例调整)和最高 5 亿美元里程碑付款,总交易金额可达 21.75 亿美元。
此次并购交易将加速推进 CM336/OM336 作为潜在 best-in-class TCE(T 细胞衔接器 T Cell Engager, TCE)在多种临床亟需的自身免疫疾病治疗领域的全球开发,进一步拓展 CM336/OM336 的全球价值;同时,该交易也充分体现了市场对康诺亚 TCE 自主研发平台 best-in-class 创新潜质的认可。
云顶新耀收购箕星药业一款产品
3 月 23 日,云顶新耀宣布与箕星药业达成资产收购协议 ,获得艾曲帕米(Etripamil)鼻喷雾剂(拟定中文商品名:星必妥®)在大中华区的开发、商业化及产品地产化权益,本次合作总金额不超过 5000 万美元(约合 3.4 亿元)。艾曲帕米已在美国获批用于治疗成人阵发性室上性心动过速(PSVT)急性症状性发作,并已在中国申报上市。
艾曲帕米鼻喷雾剂是一款新型、速效的钙离子通道阻滞剂,采用便携式鼻喷雾剂给药,起效迅速且耐受性良好,可居家自行使用,可及性高。2025 年 12 月,该药物获得美国FDA 批准上市,成为 30 多年来首款且唯一获批用于成人PSVT 急性症状性发作的疗法。
安进/阿斯利康:TSLP 单抗在华获批上市
3 月 27 日,NMPA 官网显示,阿斯利康和安进联合递交的 TSLP 单抗特泽利尤单抗注射液获批上市。本次该药获批 2 个适应症,分别是哮喘(受理号:JXSS2400102/3)和慢性鼻窦炎伴鼻息肉病(受理号:JXSS2500019/20)。
特泽利尤单抗由阿斯利康与安进合作开发,是一种同类首创的人类单克隆抗体,可抑制 TSLP 的作用。TSLP 是一种关键的上皮细胞因子,位于多个炎症级联的顶端,与严重哮喘和其他炎症疾病相关的过敏性、嗜酸性和其他类型内皮炎症息息相关。2021 年该药首次获 FDA 批准上市,2022 年该药先后在欧盟和日本获批。
GSK:半年一次超长效单抗新药在华获批上市
3 月 27 日,NMPA 官网显示,葛兰素史克「德莫奇单抗」获批上市,用于治疗嗜酸性粒细胞哮喘(受理号:JXSS2400113/4)。
德莫奇单抗(Depemokimab)是 GSK 开发的新一代抗白介素 5(IL-5)单抗,具有长半衰期、高结合亲和力和高效力,是全球首款半年一次超长效 IL-5 生物制剂。2025 年 12月,德莫奇单抗先后在美国、日本、欧盟等国家和地区获批上市。本次是该药首次登陆中国市场。
远大医药:眼科新药获批上市
3 月 22 日,远大医药宣布,其引进的用于治疗蠕形螨睑缘炎的全球创新眼科药物洛替拉纳滴眼液(TP-03)获得 NMPA 批准上市。
TP-03 由 Tarsus Pharmaceuticals 开发,2023 年 7 月获得美国 FDA 批准上市,成为全球首款也是唯一一款批准用于治疗蠕形螨睑缘炎的产品。
第一三共/阿斯利康:德曲妥珠单抗国内获批第 7 项适应症
3 月 27 日,第一三共宣布,与阿斯利康合作开发的重磅 ADC 药物「德曲妥珠单抗」(优赫得®/Enhertu)在国内获批第 7 项适应症,用于 HER2 阳性乳腺癌患者的新辅助治疗(受理号:JXSS2500110),这也是该适应症的全球首批。此前,该项申请曾被纳入优先审评。
荣昌生物:维迪西妥单抗获批第 4 项新适应症
3 月 23 日,荣昌生物发布公告,其 HER2 ADC「维迪西妥单抗」第 4 项新适应症国内获批上市,适用于治疗既往在转移性疾病阶段接受过至少一种系统治疗的,或在辅助化疗期间或完成辅助化疗之后 12 个月内复发的,不可切除或转移性 HER2 低表达(IHC 1+或 IHC 2+/ISH-)且存在肝转移的成人乳腺癌患者。
而除本次获批适应症之外,维迪西妥单抗的第 5 项适应症也已经于 2025 年 7 月申报上市,联合特瑞普利单抗一线治疗 HER2 表达(定义为 HER2 免疫组织化学检查结果为 1+、2+ 或 3+)的局部晚期或转移性尿路上皮癌患者,当前仍在审评中。
翰森制药:伊奈利珠单抗新适应症获批上市,治疗重症肌无力
3 月 27 日,NMPA 官网显示,伊奈利珠单抗注射液新适应症获批上市,用于治疗全身型重症肌无力(gMG)成人患者。
伊奈利珠单抗是靶向 CD19 B 细胞消耗性抗体。2019 年 5 月 24 日,翰森制药与 Viela Bio 订立许可协议,获得于中国内地、香港、澳门地区开发及商业化该产品的独家许可(Viela Bio 于 2021 年被Horizon Therapeutics 收购,后者于 2023 年被安进收购)。
优时比:比奇珠单抗国内再获批双适应症
3 月 27 日,优时比(UCB)宣布自研生物制剂比奇珠单抗(商品名:倍捷乐)双适应症同日获 NMPA 批准,用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病成人患者,以及治疗常规系统性治疗疗效不佳的中度至重度化脓性汗腺炎(反常性痤疮)成人患者。
这意味着全球首个且目前中国唯一获批的 IL-17A/F 双靶点一线生物制剂在中国正式从风湿免疫领域拓展至皮肤科领域。
GSK:全球首创乙肝新药国内申报上市
3 月 27 日,CDE 官网显示,GSK 的贝普若韦生注射液上市申请获受理,用于慢性乙型肝炎病毒感染者的有限疗程治疗,适用于以下人群:核苷(酸)类似物在治、HBsAg≤3000IU/mL、无肝硬化的成人慢性乙型肝炎病毒感染者。
此前,该产品已在国内获得突破性疗法资格和优先审评资格。
贝普若韦生是 Ionis 开发的一款 ASO 疗法,具有三重机制,能够识别并降解引发慢性感染的乙型肝炎病毒的遗传物质(即RNA),从而抑制体内病毒 DNA 的复制,降低血液中乙肝表面抗原(HBsAg)的水平,并刺激免疫系统提高持久性应答的机会。
强生:重磅 TCE 双抗三次获CDE 拟突破性疗法
3 月 24 日,CDE 官网显示,强生 Teclistamab(特立妥单抗)注射液拟纳入突破性治疗品种,用于既往至少接受过一线治疗的复发或难治性多发性骨髓瘤(R/R MM)成人患者。
特立妥单抗是一款全球首创、即用型、基于体重给药的皮下注射 BCMA × CD3 双特异性抗体,2022年 8 月和 10 月先后获 EMA 和 FDA 批准上市,单药适用于既往至少接受过三线治疗的 R/R MM 成人患者。2024 年6 月,该产品在中国获批同适应症。
-END-
注:文中报告摘自财通证券研究所已公开发布研究报告,具体报告内容及相关风险提示等详见完整版报告
证券研究报告:《医药生物行业投资策略周报:口服减重药产业机遇即将到来》
对外发布时间:2026年3月30日
报告发布机构:财通证券股份有限公司
报告署名分析师:
分析师|华挺
SAC证书编号:S0160523010002
邮箱地址:huating@ctsec.com
法律声明:
本文节选自财通证券股份有限公司(简称“财通证券”)已公开发布的研究报告,如需了解详细内容,请具体参见财通证券发布的完整版报告。本微信号推送的内容仅面向财通证券客户中的专业投资者,若您并非该类客户,请勿订阅、转载或使用本微信号的信息。本微信号建设受限于难以设置访问权限,财通证券不会因您订阅本微信号的行为或者收到本微信号推送消息而视为我们的当然客户。
本微信号旨在及时分享研究成果,并不是我们的研究报告发布平台。所载资料与我们正式发布的报告相较存在延时转发的情况,并可能因报告发布日之后的情势变化而不再准确或失效,且本微信号不承担更新推送信息或另行通知的义务,后续更新信息请以财通证券研究正式发布的研究报告为准。
在任何情况下本微信号所推送信息或所表述的意见并不构成对任何人的投资建议,投资者不应单纯依靠所接收我们推送的信息而取代自身的独立判断,必须充分了解各类投资风险,自主做出决策并自行承担投资风险。为避免投资者不当使用所载资料,提示应关注以下事项:(1)本微信号所载资料涉及的盈利预测、投资评级、目标价等,均是基于特定的假设条件、特定的评级标准、相对的市场基准指数而得出的中长期价值判断,不涉及对具体证券或金融工具在具体时点的判断。(2)本微信号所载资料涉及的数据或信息均来源皆被财通证券认为可靠,但财通证券不对前述数据或信息的准确性或完整性做出任何保证,报告内容亦仅供参考。(3)不同时期,财通证券可能会依据不同的假设和标准、采用不同的分析方法而口头或书面发表与本资料意见不一致的市场评论或投资观点。
为控制投资风险,投资者应仔细阅读本资料所附的各项声明、信息披露事项及风险提示。由于上述所列风险提醒事项并未囊括不当使用本资料所涉的全部风险,投资者必要时应寻求专业投资顾问指导。
本微信号版权仅为财通证券股份公司所有,并保留一切法律权利。未经事先书面许可,任何机构和个人不得以任何形式翻版、转载和发表。
抗体药物偶联物上市批准AACR会议申请上市
2026-03-29
据 Insight 数据库「全球新药」模块,本周(3 月 22 日—3 月 28 日)全球共有 95 款创新药(含改良新)研发进度推进到了新阶段,其中 6 款首次获批上市,1 款首次申报上市,6 款首次登记 III 期临床,23 款首次登记 I 期临床。
下文,Insight 将分别摘取本周国内外部分重点项目进展做介绍。
*数据说明:本期周报数据采集时间:2026-3-29 13:00。因 Insight 数据库持续高速更新,不同时段检索结果可能存在时效性差异,请以最新查询为准。
境外创新药进展
境外部分,本周共有 29 款药物在该地区范围发生研发阶段推进,包括 4 款首次在境外获批上市,1 款首次在境外申报上市,7 款首次在境外登记 I 期临床。
获批上市
据 Insight 数据库显示,本周共有 15 条新药/新适应症(不含类似药)在三大海外主要国家/地区(美国、EMA、日本)获批,其中 11 条来自日本。
本周获批新药/新适应症
截图来自:Insight 数据库网页版
1、诺和诺德:每周一次长效胰岛素在美国获批上市
3 月 27 日,诺和诺德宣布,美国 FDA 已批准 Awiqli®(icodec-abae 胰岛素)700 单位/毫升注射液,这是首款也是唯一一款每周一次给药的长效基础胰岛素,适用于成年 2 型糖尿病患者,作为饮食和运动的辅助手段,以改善血糖控制。
据 Insight 数据库显示,此前该药已在欧盟、中国、加拿大、日本、韩国等全球各地区获批上市。
截图来源:企业官网
依柯胰岛素是一种新型长效胰岛素类似物,可与白蛋白可逆性结合,在循环系统形成储库并缓慢持续释放。在一周给药间隔内,依柯胰岛素降糖作用分布均匀,并且在临床相关剂量下降糖作用时间可覆盖一周。
此次获批基于 ONWARDS 3a 期项目中针对每周一次给药的 Awiqli® 注射液在 2 型糖尿病患者中的研究结果。该项目包括四项随机、活性对照、达标治疗试验,涉及约 2680 名血糖控制不佳的成年 2 型糖尿病患者,Awiqli® 与餐时胰岛素联合使用,或与常见口服降糖药和/或 GLP-1 受体激动剂联合使用。
该临床项目将每周一次给药的 Awiqli® 与每日一次的基础胰岛素进行了对比,结果显示,在 ONWARDS 关键临床试验项目中,Awiqli® 在降低糖化血红蛋白(HbA1c)这一主要终点上显示出有效性。在 ONWARDS 各项试验中,Awiqli® 的安全性总体上与每日一次的基础胰岛素类别一致。
2、海和药物:PI3Kα 抑制剂在日本获批上市
3 月 23 日,海和药物宣布,其自主开发的 PI3Kα 选择性抑制剂甲磺酸瑞索利塞片(研发代号:CYH33;中文商品名:海泽欣® )获得日本厚生劳动省(MHLW)批准上市,用于治疗化疗后疾病进展且携带 PIK3CA 基因突变的卵巢透明细胞癌(OCCC)。
这是海和药物自主开发并在日本获批上市的第 2 款创新药。新闻稿也指出,瑞索利塞是全球首个用于化疗后疾病进展 OCCC 的单药靶向治疗药物,也是全球首个在日本获批的 PI3Kα 选择性抑制剂。
截图来源:海和药物官网
CYH33 是海和药物的一款强效、高选择性的小分子 PI3Kα抑制剂,具有全新的化学结构。本次获批主要基于 CYH33-G201 关键 II 期研究(NCT05043922;jRCT2031210216)的有效性与安全性数据。
CYH33-G201 为一项单臂、开放标签、国际多中心的关键 II 期临床试验,旨在评估瑞索利塞用于化疗后疾病进展且携带 PIK3CA 基因突变的卵巢透明细胞癌人群的疗效和安全性。该研究在中国和日本共 39 个中心开展,以盲态独立评审委员会(BIRC)评估的客观缓解率(ORR)为主要终点,采用 40 mg 每日一次的空腹口服给药方案。
数据显示,在 84 例(中国:45.2%,日本:54.8%)疗效可评估的患者中,瑞索利塞显示出具有临床意义的抗肿瘤活性。其总体安全性可控、耐受性良好,常见的不良反应为高血糖和皮疹,与已批准的其它 PI3Kα 抑制剂的安全性特征总体一致,经过对症处理或剂量调整可有效管理和逆转。
海和药物与艾德生物合作开发的用于检测 PIK3CA 基因突变的体外伴随诊断试剂(CDx):AmoyDx® PIK3CA 突变检测试剂盒已于本月 5 日获得日本厚生劳动省 (MHLW) 批准。
3、Corcept:卵巢癌新药在美国获批上市
当地时间 3 月 25 日,Corcept Therapeutics 宣布,美国 FDA 已批准 Lifyorli™(relacorilant)上市,联合白蛋白结合型紫杉醇(nab-paclitaxel)用于治疗既往接受过 1 至 3 线全身治疗方案(其中至少一线包含贝伐珠单抗)的铂耐药性上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者。
新闻稿指出,Lifyorli 是首个获得 FDA 批准的选择性糖皮质激素受体拮抗剂(SGRA),可竞争性结合糖皮质激素受体(GR),通过抑制皮质醇对细胞凋亡的抑制作用来增强化疗敏感性。
截图来源:Businesswire
此次获批是基于关键临床研究 ROSELLA 试验的积极结果。该试验纳入了 381 例既往接受过 1 至 3 线治疗(其中至少一线包含贝伐珠单抗)的铂耐药性卵巢癌患者,按 1:1 随机分组,分别接受 Lifyorli 联合白蛋白结合型紫杉醇治疗或白蛋白结合型紫杉醇单药治疗。
ROSELLA 研究达到了 PFS 和 OS 双主要终点。与仅接受白蛋白结合型紫杉醇治疗的患者相比,在白蛋白结合型紫杉醇基础上增加适用 Lifyorli 治疗的患者死亡风险降低了 35%(风险比:0.65;p 值:0.0004),中位 OS 为 16.0 个月 VS 11.9 个月;疾病进展风险也降低了 30%(风险比:0.70;p 值:0.008)。
安全性方面,联合疗法耐受性良好且易于管理。
该项研究数据已在 2025 ASCO 年会上首次公布,并同时发表在《柳叶刀》杂志上;完整结果将于 4 月在妇科肿瘤学会(SGO)会议上公布。
申报上市
1、Ionis:反义寡核苷酸疗法在美国申报上市
当地时间 3 月 23 日,Ionis 宣布,美国 FDA 已受理针对 zilganersen 的新药申请(NDA)并授予优先审评资格,FDA 已设定 PDUFA 目标行动日期为 2026 年 9 月 22 日。
Zilganersen 是一种反义寡核苷酸药物,用于治疗亚历山大病(AxD),这是一种罕见、渐进性且往往致命的神经系统疾病。如果获批,zilganersen 将成为亚历山大病的首个也是唯一的治疗方法。
来源:企业官网
Zilganersen 旨在抑制因胶质纤维酸性蛋白(GFAP)基因中的致病变异而积累的过量胶质纤维酸性蛋白的产生。此前,该药已获美国 FDA 授予的突破性疗法认定、孤儿药认定和罕见儿科疾病认定,也获得了欧盟 EMA 授予的孤儿药认定。
本次 NDA 是基于 zilganersen 在患有 AxD 的儿童和成人中开展的关键研究结果(NCT04849741)。该研究在 8 个国家招募了 54 名年龄在 1.5 岁至 53 岁之间的亚历山大病(AxD)患者,以 2:1 的比例随机分组,接受 zilganersen 或对照治疗,进行为期 60 周的双盲治疗期。
该研究设置了两个剂量组,分别为 25 毫克和 50 毫克,其中 50 毫克剂量组被作为关键剂量组进行分析,每 12 周给药一次。在 60 周时,所有符合条件的参与者进入开放标签治疗期,随后是为期 120 周的开放标签长期延长期治疗期,在此期间,25 毫克剂量组的参与者转为 50 毫克剂量组,最后是为期 28 周的治疗后随访期。
主要终点是在双盲治疗期结束时,通过 10 米步行测试(10MWT)评估的步态速度相对于基线的百分比变化,这是对功能活动能力的一种评估。关键次要终点包括患者自我认定的最困扰症状(MBS)评分、双盲治疗期结束时患者总体严重程度印象(PGIS)评分、患者总体变化印象(PGIC)评分和临床医生总体变化印象(CGIC)评分相对于基线的变化。
结果显示,与对照组相比,在第 61 周时,zilganersen 在主要终点上显示出具有统计学意义和临床意义的稳定改善(最小二乘均值差异为 33.3%,p=0.0412),且安全性和耐受性良好。在关键次要和探索性终点的结果也显示 zilganersen 更具优势。额外数据将在 2026 年于美国神经病学学会(AAN)年会上公布。
临床试验动态
1、百利天恒:双抗 ADC 联用 PD-1 临床数据首次公布
本周,2026 年欧洲肺癌大会(ELCC)在丹麦哥本哈根盛大召开。本次大会上,百利天恒以口头报告的形式,首次披露了 Iza-bren(EGFR×HER3 双抗 ADC)联合斯鲁利单抗,用于一线治疗广泛期小细胞肺癌(ES-SCLC)的临床研究成果。
值得注意的是,这也是全球首个公布 ADC 联合免疫检查点抑制剂一线治疗 ES-SCLC 结果的研究。
截图来源:ELCC 官网
本次大会公布该研究的 II 期结果,纳入人群均为初治的 ES-SCLC 患者。截至 2025 年 11 月 30 日,该 II 期研究共纳入 82 例患者:
队列 1:41 例患者接受 Iza-bren 2.5 mg/kg D1D8 Q3W 联合斯鲁利单抗一线治疗;
队列 2:41 例患者接受 Iza-bren 2.75 mg/kg D1D8 Q3W 联合斯鲁利单抗一线治疗。
主要研究终点为客观缓解率(ORR)和联合治疗的推荐 II 期剂量(RP2D)。
其中,队列 1 近半数患者基线伴肝转移,肿瘤负荷重,基线伴肝转移占比 48.8%,具体研究结果显示:
100% 患者靶病灶缩小且 85% 患者实现了深度缓解,中位缓解持续时间超过 7 个月:靶病灶缩瘤率 100%,中位缩瘤幅度达 64.4%;ORR 高达 85%,mDoR 7.3 个月;
最高 1 年 OS 率和 mPFS 突破 8 个月:1 年 OS 率最高,达 85.7%,mPFS 达 8.2 个月;
联合治疗方案安全可耐受:Iza-bren 联合斯鲁利单抗常见血液学毒性,患者无明显体感;同时,该联合方案肺部安全性良好,ILD 发生率低(2.4%),无≥3 级事件。Iza-bren 的停药率低,仅 2.4%,保障患者的长期用药获益。
研究者得出结论,Iza-bren 联合斯鲁利单抗的推荐剂量为 2.5 mg/kg D1D8 Q3W。该 II 期研究的积极结果将支持 Iza-bren 联合斯鲁利单抗一线治疗 ES-SCLC 关键注册 III 期研究的开展以及 Iza-bren 联合免疫检查点抑制剂在泛瘤种中的进一步拓展。
3、百济神州:CDK4 抑制剂启动首个 III 期临床
3 月 25 日,百济神州在 ClinicalTrials 官网登记了一项 BGB-43395 联合来曲唑治疗既往未接受过晚期或转移性疾病治疗的 HR+/HER2- 晚期或转移性乳腺癌的 III 期临床研究。根据公开信息,这是 BGB-43395 启动的首个 III 期。
截图来源:ClinicalTrials 官网
BGB-43395 是百济神州自主研发的一款不靶向 CDK6,而特异性靶向 CDK4 的高度选择性的强效抑制剂,具有降低剂量限制性毒性、提高耐受性,并获得可比或更好的有效性的潜力。
在 2025 年 SABCS 大会上,百济神州通过壁报展示了该药在 65例转移性 HR+/HER2- 乳腺癌或其他晚期实体瘤患者的早期安全性和耐受性数据。
这些患者接受了 BGB-43395 单药或联合氟维司群或来曲唑剂量递增研究。迄今为止,研究结果表明 BGB-43395 在不同剂量水平下总体耐受性良好,且展现出令人鼓舞的临床活性早期迹象,所获得的数据支持对该药物继续进行开发。
本次启动的是一项开放标签、随机、多中心 III 期研究,旨在评估 BGB-43395 联合来曲唑与 CDK4/6 抑制剂(阿贝西利、哌柏西利、瑞波西利)联合来曲唑治疗既往未接受过全身抗癌治疗的晚期或转移性 HR+/HER2- 乳腺癌患者的疗效和安全性。该试验拟入组 1056 人,研究的主要终点为由盲法独立中心审查(BICR)确定的 PFS。
值得一提的是,就在上周,辉瑞宣布其 CDK4 抑制剂 Atirmociclib 的 II 期临床试验 FOURLIGHT-1 研究取得积极顶线结果。
医药交易
据 Insight 数据库显示,本周(3 月 22 日 - 3 月 28 日)共发生 24 起交易事件。
1、超 21 亿美元!吉利德收购康诺亚 NewCo
3 月 24 日,康诺亚宣布,其 NewCo 合作企业 Ouro Medicines 已与吉利德科学签署并购协议,吉利德将通过并购方式收购 Ouro Medicines,交易金额包括 16.75 亿美元首付款(可按惯例调整)和最高 5 亿美元里程碑付款,总交易金额可达 21.75 亿美元。
根据并购协议,作为 Ouro Medicines 的股东,交易完成后康诺亚将获得约 2.5 亿美元首付款,以及最高约 7000 万美元的里程碑付款,总收入金额可达约 3.2 亿美元;同时,康诺亚对 CM336/OM336 的特许销售分层将由吉利德履行。交易完成后,康诺亚将不再持有 Ouro Medicines 股权。
此次并购交易将加速推进 CM336/OM336 作为潜在 best-in-class TCE(T 细胞衔接器 T Cell Engager, TCE)在多种临床亟需的自身免疫疾病治疗领域的全球开发,进一步拓展 CM336/OM336 的全球价值;同时,该交易也充分体现了市场对康诺亚 TCE 自主研发平台 best-in-class 创新潜质的认可。
康诺亚于 2024 年 11 月与 Ouro Medicines 订立独家许可协议,授权 Ouro Medicines 在全球范围(不包括中国内地、香港、澳门及台湾地区)研发、生产、注册及商业化 CM336/OM336 的独家权利。并购交易后,该授权协议将继续有效,康诺亚将继续保持授权协议中相关权益。
Ouro Medicines 的唯一产品 CM336/OM336 是由康诺亚自主研发的创新型 TCE 双特异性抗体药物,其活性成分为重组抗 B 细胞成熟抗原(BCMA)和 CD3 人源化双特异性抗体。CM336/OM336 治疗自身免疫性溶血性贫血(AIHA)和原发免疫性血小板减少症(ITP)获得美国 FDA 授予的快速通道资格(FTD)认定和孤儿药资格认定(ODD),预计将于 2027 年进入注册性研究;其治疗自身免疫性溶血性贫血研究结果发表于全球顶级医学期刊《新英格兰医学杂志》。
2、超 3.4 亿元!云顶新耀收购箕星药业一款产品
3 月 23 日,云顶新耀宣布与箕星药业达成资产收购协议 ,获得艾曲帕米(Etripamil)鼻喷雾剂(拟定中文商品名:星必妥®)在大中华区的开发、商业化及产品地产化权益,本次合作总金额不超过 5000 万美元(约合 3.4 亿元)。艾曲帕米已在美国获批用于治疗成人阵发性室上性心动过速(PSVT)急性症状性发作,并已在中国申报上市。
艾曲帕米鼻喷雾剂是一款新型、速效的钙离子通道阻滞剂,采用便携式鼻喷雾剂给药,起效迅速且耐受性良好,可居家自行使用,可及性高。2025 年 12 月,该药物获得美国 FDA 批准上市,成为 30 多年来首款且唯一获批用于成人 PSVT 急性症状性发作的疗法。
在中国,艾曲帕米鼻喷雾剂用于治疗 PSVT 的新药上市申请已于 2025 年 1 月 17 日获得 NMPA 正式受理,并预计于 2026 年 Q3 获批。
此外,艾曲帕米鼻喷雾剂还在被开发用于治疗伴有快速心室率反应的房颤(AFib-RVR)适应症,II 期临床研究已取得积极结果,并计划推进 III 期临床研究,未来有望进一步拓展至更广泛患者人群。
根据协议,云顶新耀将向箕星药业支付首付款 3000 万美元(相当于约人民币 2.07 亿元),以及最高不超过 2000 万美元(相当于约人民币 1.38 亿元)的开发里程碑付款。作为本协议的一部分,云顶新耀将获得箕星药业于 2021 年 5 月签订的许可协议及相关附属协议项下的权利、权益、主张、职责、义务及责任(不包括双方约定的部分除外责任)。
深度专题
2025 年全球药品销售额 TOP100 榜单尘埃落定,看似熟悉的名单背后,格局已悄然生变,有将近 10 个新面孔首次亮相。
整体来看,榜单总销售额为 5643 亿美元,上榜的门槛较过去两年显著抬升,已经来到 19 亿美元,销售额超过 50 亿美元的药物多达 34 款,超过 100 亿美元的超级重磅炸弹则有 10 款。
从增速来看,有 13 个药品同比增长在 40% 以上,其中 3 款增长率甚至超过了 100%,展现出现象级产品的爆发力。
详细清单及分析,欢迎点击跳转阅读 Insight 专题文章:2025 年全球药品销售额 TOP100
国内创新药进展
本周共有 75 款创新药(含改良新)在国内的研发进度推进到了新阶段,其中 4 款首次在国内获批上市,2 款首次在国内申报上市,4 款首次在国内登记 III 期临床,21 款首次在国内获批临床。
新药获批上市
1、安进/阿斯利康:TSLP 单抗在华获批上市
3 月 27 日,NMPA 官网显示,阿斯利康和安进联合递交的 TSLP 单抗特泽利尤单抗注射液获批上市。本次该药获批 2 个适应症,分别是哮喘(受理号:JXSS2400102/3)和慢性鼻窦炎伴鼻息肉病(受理号:JXSS2500019/20)。
截图来源:NMPA 官网
特泽利尤单抗由阿斯利康与安进合作开发,是一种同类首创的人类单克隆抗体,可抑制 TSLP 的作用。TSLP 是一种关键的上皮细胞因子,位于多个炎症级联的顶端,与严重哮喘和其他炎症疾病相关的过敏性、嗜酸性和其他类型内皮炎症息息相关。2021 年该药首次获 FDA 批准上市,2022 年该药先后在欧盟和日本获批。
在国内,该药已启动针对哮喘、嗜酸性粒细胞性食管炎、慢性鼻窦炎伴鼻息肉病、慢性阻塞性肺疾病的 III 期临床。
关于哮喘的 DESTINATION 临床试验是一项区域性、多中心、随机、双盲、安慰剂对照、平行组、III 期研究,旨在评价特泽利尤单抗在重度哮喘控制不佳的成年受试者中的有效性和安全性。在 2025 年美国过敏、哮喘和免疫学会年会(AAAAI)上公布的临床结果显示,与安慰剂相比,特泽利尤单抗在 52 周内显著降低患者哮喘急性发作率(AAER)达 74%。
在次要终点方面,与安慰剂相比,特泽利尤单抗在 52 周内显著改善患者肺功能,FEV1 改善达 250 ml,并显著改善患者哮喘症状控制及生活质量(根据 ACQ-6、AQLQ[S]+12 和 ASD 评估,治疗 52 周后,上述评分较基线均有显著改善)。
另一项 III 期 WAYPOINT 临床研究的阳性结果表明,与安慰剂相比,特泽利尤单抗显著减轻了慢性鼻窦炎伴鼻息肉患者的鼻息肉严重程度,减少患者后续鼻息肉手术的需求及系统性糖皮质激素使用的需求。相关数据发表于《新英格兰医学杂志》,并在 2025 年 AAAAI 大会上以最新突破性研究口头报告形式发布。
数据显示,使用特泽利尤单抗治疗显著降低了通过共同主要终点评估的鼻息肉严重程度:与使用安慰剂相比,治疗第 52 周时,鼻息肉评分(NPS)降低了 2.065 分,患者自我报告鼻塞症状评分(NCS)降低了 1.028 分 。NPS 的改善最早见于第 4 周,NCS 的改善最早见于第 2 周(分别为第一次治疗后评估),且疗效持续至第 52 周 。
在研究总体人群中,所有关键次要终点均显示出统计学意义及临床意义的改善。尤为重要的是,与安慰剂组相比,特泽利尤单抗显著减少了患者后续鼻息肉手术的需求(降幅达 98%)和系统性糖皮质激素使用的需求(降幅达 88%)。
Insight 数据库显示,特泽利尤单抗是目前全球唯一一款获批上市的 TSLP 单抗,2025 年大卖近 20 亿美元,首次上榜全球药品销售额 TOP100 榜单。除此之外,有 6 款已进入临床 III 期,分别来自博奥信/正大天晴(Bosakitug)、恒瑞/GSK(GSK5784283)、康诺亚/石药(CM326)、荃信生物(JKN24011)等,其中齐鲁制药 QL2302 是一款特泽利尤单抗生物类似药。
2、GSK:半年一次超长效单抗新药在华获批上市
3 月 27 日,NMPA 官网显示,葛兰素史克「德莫奇单抗」获批上市,用于治疗嗜酸性粒细胞哮喘(受理号:JXSS2400113/4)。
截图来源:NMPA 官网
德莫奇单抗(Depemokimab)是 GSK 开发的新一代抗白介素 5(IL-5)单抗,具有长半衰期、高结合亲和力和高效力,是全球首款半年一次超长效 IL-5 生物制剂。2025 年 12 月,德莫奇单抗先后在美国、日本、欧盟等国家和地区获批上市。本次是该药首次登陆中国市场。
III 期哮喘研究项目主要包括针对 2 型炎症性哮喘患者的 SWIFT-1 和 SWIFT-2 研究,以及一项开放标签扩展研究(AGILE)。2024 年 9 月 9 日,GSK 在欧洲呼吸学会国际会议上公布了 III 期临床试验 SWIFT-1 和 SWIFT-2 的完整结果,并同时发表在 NEJM。
SWIFT-1 和 SWIFT-2 是为期 52 周的随机、双盲、安慰剂对照、平行分组、多中心研究 III 期临床试验,具有相同主要和次要终点。两项试验评估了德莫奇单抗在伴有 2 型炎症(以血嗜酸性粒细胞计数升高为特征)的成人和青少年重度哮喘患者中的疗效和安全性。
在两项试验中,792 名患者进行了随机分组,762 名患者被纳入全面分析;其中 502 名患者被分配接受德莫奇单抗治疗,260 名患者接受安慰剂治疗。
两项试验均达到了主要终点。预先指定的汇总分析显示,与安慰剂相比,在 52 周内病情恶化率显著降低了 54%(95% CI 0.36 - 0.59,p < 0.001),具体而言:
在 SWIFT-1 试验中,德莫奇单抗组的年病情恶化率为 0.46(95% CI:0.36 - 0.58),安慰剂组为 1.11(95% CI:0.86 - 1.43)(95% CI:0.30 - 0.59;P < 0.001);
在 SWIFT-2 试验中,德莫奇单抗组的年病情恶化率为 0.56(95% CI:0.44 - 0.70),安慰剂组为 1.08(95% CI:0.83 - 1.41)(95% CI:0.36 至 0.73;P < 0.001)。
在 SWIFT-1 和 SWIFT-2 的汇总分析中,与安慰剂相比,需要住院治疗或急诊就诊的具有临床意义的病情恶化这一次要终点降低了 72%(95% CI 0.13 - 0.61,p = 0.002)。德莫奇单抗年化病情恶化率为 0.02,而安慰剂组为 0.09。
安全性方面,德莫奇单抗与安慰剂组发生任何不良事件(AE)的患者比例相似。
3、远大医药:眼科新药获批上市
3 月 22 日,远大医药宣布,其引进的用于治疗蠕形螨睑缘炎的全球创新眼科药物洛替拉纳滴眼液(TP-03)获得 NMPA 批准上市。
来源:企业官微
TP-03 由 Tarsus Pharmaceuticals 开发,2023 年 7 月获得美国 FDA 批准上市,成为全球首款也是唯一一款批准用于治疗蠕形螨睑缘炎的产品。
2021 年 3 月,联拓生物从 Tarsu 获得在大中华区对 TP-03 进行开发及商业化的独家授权,首付款为 1500 万美元,里程碑付款为 1.85 亿美元。
2024 年 3 月,远大医药与联拓生物和 Tarsu 达成合作协议,以 1500 万美元首付款和一定金额的注册里程碑费用为代价取得 TP-03 在大中华区(中国大陆、中国香港特别行政区、中国澳门特别行政区、台湾地区)的独家开发、生产及商业化权益。
TP-03 在美国已经完成了两项关键性临床研究,共入组 800 余名蠕形螨睑缘炎患者,根据临床结果显示,两项研究均达到了主要终点和所有次要终点,具有统计学意义,且未发生与治疗相关的严重不良事件。此外,TP-03 在美国开展的用于治疗蠕形螨导致的睑板腺功能障碍的 II 期临床研究也显示出了阳性的顶线结果。
中国注册方面,TP-03 已完成了 III 期临床研究,根据研究结果显示,与对照组相比,TP-03 治疗蠕形螨睑缘炎患者的蠕形螨感染根除率具有统计学显著性 (p<0.001),眼睑袖套状分泌物治愈率也呈现出阳性但无统计学意义的趋势 (p=0.15)。
此外,TP-03 耐受性良好,其安全性特征与其它大规模临床试验中观察到的结果相似,无治疗相关的停药情况。
4、誉颜制药/华东医药:除皱新药获批上市
3 月 27 日,NMPA 官网显示,誉颜制药自主研发的注射用重组 A 型肉毒毒素 YY001 获批上市,用于暂时性改善 65 岁及 65 岁以下成人因皱眉肌和/或降眉间肌活动引起的中度至重度眉间纹(受理号:CXSS2400144)。
截图来源:NMPA 官网
誉颜制药新闻稿曾指出,YY001 是全球肉毒毒素领域首款重组 A 型肉毒毒素。
作为一款重组 A 型肉毒毒素,YY001 在不改变蛋白活性的基础上,避免了传统技术路线使用肉毒杆菌生产肉毒毒素的生物安全风险。同时,通过全套创新设计的生产工艺,誉颜制药所生产的重组肉毒毒素具有纯度高、比活性高、免疫原性低的特征,被业内视为新一代肉毒毒素。
2023 年 11 月,华东医药已与誉颜制药达成合作,获得了 YY001 在中国大陆、香港、澳门地区用于改善成人中度至重度眉间纹适应症的独家商业化权益,并将负责该适应症在中国香港、澳门地区的独家临床开发和注册申报。
根据协议,华东医药将向誉颜制药支付 5000 万元首付款,以及最高不超过人民币 1 亿元注册里程碑付款。
2024 年 9 月,誉颜制药 YY001 治疗中、重度眉间纹适应症的 III 期临床研究(代号 YY001-001)取得全面成功。数据显示:YY001 在大规模人群的 III 期临床试验中表现出与已完成的 I/II 期临床结果的高度一致性;其有效性、安全性和免疫原性都达到了既定的临床试验终点,与对照药相比表现优异,树立了从天然肉毒毒素跨越到重组肉毒毒素的一个重要里程碑。
新适应症获批上市
1、第一三共/阿斯利康:德曲妥珠单抗国内获批第 7 项适应症
3 月 27 日,第一三共宣布,与阿斯利康合作开发的重磅 ADC 药物「德曲妥珠单抗」(优赫得®/Enhertu)在国内获批第 7 项适应症,用于 HER2 阳性乳腺癌患者的新辅助治疗(受理号:JXSS2500110),这也是该适应症的全球首批。此前,该项申请曾被纳入优先审评。
本次获批意味着德曲妥珠单抗乳腺癌版图的再度扩大。继 HER2 阳性乳腺癌(2L+)、HER2 低表达乳腺癌、HER2 超低表达乳腺癌之后,德曲妥珠单抗实现了从晚期到早期的布局跃迁。
截图来源:企业官微
本次新适应症的获批主要是基于 III 期临床试验 DESTINY-Breast11 的积极结果(登记号:NCT05113251/CTR20220458)。
DB-11 是一项全球多中心、随机、开放性 III 期研究,旨在评估 T-DXd (5.4 mg/kg)单药或 T-DXd 序贯紫杉醇、曲妥珠单抗和帕妥珠单抗(THP)作为新辅助治疗与标准治疗方案相比在高风险(淋巴结阳性 [N1-3] 或原发肿瘤分期 T3-4 期)、局部晚期或炎性 HER2 阳性早期乳腺癌患者中的疗效和安全性。
试验主要终点是病理完全缓解(pCR)率(乳腺及淋巴结无浸润性病灶)。次要终点包括无事件生存期、无浸润性疾病生存期、总生存期和安全性。
2025 ESMO 大会上发布的临床结果显示,
德曲妥珠单抗序贯 THP 组患者的 pCR 率为 67.3%,而 ddAC-THP 组为 56.3%,pCR 率提升 11.2%(95% CI:4.0–18.3;p=0.003),pCR 获益在激素受体阳性(HR+)和激素受体阴性(HR−)两个亚组中均有观察到;
在德曲妥珠单抗序贯 THP 组中,81.3% 的患者术后在切除的乳腺或淋巴结组织中未检出或仅检出极少量残余浸润性癌症病灶(残余癌症负荷 [RCB] 0+I),而对照组为 69.1%。
次要终点无事件生存期(EFS)的数据在本次分析时尚未成熟(数据截点成熟度为 4.5%);但早期分析显示,德曲妥珠单抗序贯 THP 较 ddAC-THP 呈获益趋势(HR=0.56;95% CI:0.26–1.17)。
安全性方面,在 DESTINY-Breast11 研究中,德曲妥珠单抗序贯 THP 的安全性特征与各单药治疗组分已知的安全性特征一致,期中分析未发现新的安全性问题,长期安全性仍需持续随访。
2、荣昌生物:维迪西妥单抗获批第 4 项新适应症
3 月 23 日,荣昌生物发布公告,其 HER2 ADC「维迪西妥单抗」第 4 项新适应症国内获批上市,适用于治疗既往在转移性疾病阶段接受过至少一种系统治疗的,或在辅助化疗期间或完成辅助化疗之后 12 个月内复发的,不可切除或转移性 HER2 低表达(IHC 1+或 IHC 2+/ISH-)且存在肝转移的成人乳腺癌患者。
据 Insight 数据库统计,这是维迪西妥单抗获批的第 4 项适应症。
截图来源:企业公告
维迪西妥单抗自 2021 年首次获批上市以来,此前已有 3 项适应症获批:
至少接受过 2 种系统化疗的 HER2 过表达局部晚期或转移性胃癌;
既往接受过系统化疗且 HER2 过表达局部晚期或转移性尿路上皮癌;
既往接受过曲妥珠单抗或其生物类似物和紫杉类药物治疗的 HER2 阳性且存在肝转移的晚期乳腺癌。
而除本次获批适应症之外,维迪西妥单抗的第 5 项适应症也已经于 2025 年 7 月申报上市,联合特瑞普利单抗一线治疗 HER2 表达(定义为 HER2 免疫组织化学检查结果为 1+、2+ 或 3+)的局部晚期或转移性尿路上皮癌患者,当前仍在审评中。
荣昌生物曾启动一项在国内 60 家机构开展的 III 期临床试验(登记号:NCT04400695/CTR20200646),旨在对比维迪西妥单抗与紫杉醇或多西他赛或长春瑞滨或卡培他滨用于治疗 HER2 低表达局部晚期或转移性乳腺癌的有效性,安全性,生活质量。
该试验最早登记于 2020 年 5 月,并已于 2024 年 3 月显示完成,实际入组了 377 名受试者,不过临床结果目前暂未公布。
早前曾在 2024 ESMO 公布的一项单臂 II 期 IIT 研究数据显示,在 31 例至少经历过中位 2 线前线化疗的 HER2 低表达转移性乳腺癌患者中,维迪西妥单抗治疗的 ORR 为 34.3%,mPFS 为 3.4 个月(95%CI,2.8-4.0)。
3、翰森制药:伊奈利珠单抗新适应症获批上市,治疗重症肌无力
3 月 27 日,NMPA 官网显示,伊奈利珠单抗注射液新适应症获批上市,用于治疗全身型重症肌无力(gMG)成人患者。
截图来源:NMPA 官网
伊奈利珠单抗是靶向 CD19 B 细胞消耗性抗体。2019 年 5 月 24 日,翰森制药与 Viela Bio 订立许可协议,获得于中国内地、香港、澳门地区开发及商业化该产品的独家许可(Viela Bio 于 2021 年被 Horizon Therapeutics 收购,后者于 2023 年被安进收购)。
2022 年 3 月,伊奈利珠单抗首次于中国获批上市,用于抗水通道蛋白4(AQP4)抗体阳性的视神经脊髓炎谱系疾病(NMOSD)成人患者的治疗;2025 年 9 月,伊奈利珠单抗获批新适应症,适用于免疫球蛋白G4相关性疾病(IgG4-RD)成人患者。本次是该药获批的第 3 项适应症。
此次新适应症获批上市是基于其全球关键性 III 期试验 MINT 的积极结果。MINT 是一项随机、双盲、多中心、安慰剂对照、III 期研究(含一个开放标签期),旨在成年重症肌无力患者中评价伊奈利珠单抗的疗效和安全性。主要终点指标是总研究人群第 26 周时重症肌无力日常生活量表(MG-ADL)评分相对于基线的变化。
第 26 周的结果显示,与安慰剂相比,伊奈利珠单抗治疗组患者的 MG-ADL 评分下降幅度更大(最小二乘均值分别为-4.2 和-2.2,差异-1.9,95% CI: -2.9 至-1.0,P<0.001);在定量重症肌无力量表(QMG)评分方面,伊奈利珠单抗组的下降幅度同样明显优于安慰剂组(最小二乘均值为-4.8 和-2.3,差异-2.5,95% CI: -3.8 至-1.2,P<0.001)。在 AChR+群体中,这一疗效的显著性表现得尤为突出。
试验还评估了 AChR+组患者第 52 周时 MG-ADL 评分较基线的变化,伊奈利珠单抗组相较安慰剂组持续显示更优疗效(校正后差异为-2.8,95% CI: -3.9 至-1.7)。伊奈利珠单抗组 AChR+患者中 72.3% 实现 MG-ADL 评分≥3 分改善,安慰剂组为 45.2%。
第 52 周时,伊奈利珠单抗组 QMG 评分较基线改善亦优于安慰剂组(校正后差异-4.3,95% CI: -5.9 至-2.8)。伊奈利珠单抗组 AChR+患者中 69.2% 实现 QMG 评分≥3 分改善,安慰剂组为 41.8%。
安全性方面,研究期间未发现新的安全性信号,不良事件(TEAE)特征与已知安全性特征一致,最常见不良事件包括输液相关反应、鼻咽炎及尿路感染。
Insight 数据库显示,在重症肌无力领域,国内已经批准多款产品上市,包括泰它西普(荣昌生物)、泽卢克布仑钠(优时比)、罗泽利昔珠单抗(优时比)、艾加莫德(Argenx/再鼎医药)、瑞利珠单抗(阿斯利康)等。
4、优时比:比奇珠单抗国内再获批双适应症
3 月 27 日,优时比(UCB)宣布自研生物制剂比奇珠单抗(商品名:倍捷乐)双适应症同日获 NMPA 批准,用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病成人患者,以及治疗常规系统性治疗疗效不佳的中度至重度化脓性汗腺炎(反常性痤疮)成人患者。
这意味着全球首个且目前中国唯一获批的 IL-17A/F 双靶点一线生物制剂在中国正式从风湿免疫领域拓展至皮肤科领域。
来源:优时比官微
银屑病全球多中心 III 期数据显示,近九成适合系统治疗或光疗的中度至重度斑块状银屑病成人患者在比奇珠单抗治疗 16 周实现显著的皮损清除或几乎清除;其中约 60% 的患者在第 16 周实现了皮损完全清除,且应答迅速并可持续长达一年。长期数据还显示,绝大多数患者在四年内维持了高水平的临床应答。
化脓性汗腺炎全球多中心 III 期临床研究数据显示,和安慰剂相比,接受比奇珠单抗治疗的患者中,有更高比例在第 16 周实现了 HS 体征和症状达到 50% 或更大幅度(HiSCR50)的改善,且疗效持续至第 48 周 。最新的三年随访数据进一步显示,比奇珠单抗可持续提升患者的临床改善应答率,并持续促进溢脓性窦道的愈合,为患者带来稳定且不断改善的临床获益。
比奇珠单抗是一款 IL-17A/F 双靶点抑制剂,已在中国获批用于常规治疗疗效不佳或不耐受的活动性强直性脊柱炎(AS)成人患者;及用于非甾体类抗炎药(NSAID)给药后疗效不佳或不耐受的活动性放射学阴性中轴型脊柱关节炎(nr-axSpA)伴客观炎症体征(根据C反应蛋白(CRP)升高和/或磁共振成像(MRI)检查提示)的成人患者;用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病成人患者,以及治疗常规系统性治疗疗效不佳的中度至重度化脓性汗腺炎(反常性痤疮)成人患者。
自 2021 年上市以来,比奇珠单抗销售额增长迅猛,2025 年已经达到了 25.19 亿美元,同比增长 285.03%,成功跻身全球畅销药 TOP100 榜单。
申报上市
1、GSK:全球首创乙肝新药国内申报上市
3 月 27 日,CDE 官网显示,GSK 的贝普若韦生注射液上市申请获受理,用于慢性乙型肝炎病毒感染者的有限疗程治疗,适用于以下人群:核苷(酸)类似物在治、HBsAg≤3000IU/mL、无肝硬化的成人慢性乙型肝炎病毒感染者。
此前,该产品已在国内获得突破性疗法资格和优先审评资格。
来源:CDE 官网
贝普若韦生是 Ionis 开发的一款 ASO 疗法,具有三重机制,能够识别并降解引发慢性感染的乙型肝炎病毒的遗传物质(即 RNA),从而抑制体内病毒 DNA 的复制,降低血液中乙肝表面抗原(HBsAg)的水平,并刺激免疫系统提高持久性应答的机会。
2019 年 8 月,GSK 从 Ionis 引进了该产品的开发和商业化权益,首付款和里程碑付款为 2.62 亿美元。
今年 1 月 7 日,GSK 宣布,贝普若韦生的两项关键性 III 期 B-Well 1 和 B-Well 2 研究均达到了主要终点。这两项研究共纳入了 1800 多名受试者,在 29 个国家开展。
结果显示,在 B-Well 研究中,贝普若韦生显示出了具有统计学意义和临床意义的功能性治愈率,且联合标准治疗的功能性治愈率显著高于单独使用标准治疗。
目前,贝普若韦生已经在中国、日本申报上市。如果获批,该产品有望成为首个慢性乙型肝炎的六个月有限疗程治疗选择,并成为未来序贯治疗的基石药物。
2、安睿特:国产「重组人白蛋白」申报上市
3 月 25 日,CDE 官网显示,安睿特递交的重组人白蛋白注射液上市申请获得受理。根据该药的临床研究进度,Insight 数据库推测本次申报的适应症为肝硬化腹水患者低白蛋白血症。此前,该产品已在俄罗斯获批上市,是全球首个上市销售的重组人白蛋白注射液产品。
截图来源:CDE 官网
腹水是失代偿期肝硬化患者常见且严重的并发症之一,也是肝硬化自然病程进展的重要标志。由于白蛋白具有维持胶体渗透压的作用,血清白蛋白降低成为水肿和腹水的主要原因之一,因此给肝硬化病人使用白蛋白可以提高血浆胶体渗透压,从而减轻或消除水肿和腹水。
人血白蛋白必须从血液提取,受到血源供应的限制,而且产品产量和质量控制难度较大。重组人白蛋白则是利用现代生物发酵技术生产的白蛋白产品,与血源白蛋白相比,重组人白蛋白不仅纯度更高,而且可以有效避免人血白蛋白携带病毒等风险,还可解决血源产品供应短缺等问题。
在国内,安睿特已完成重组人白蛋白注射液治疗肝硬化腹水患者低蛋白血症的关键性 Ⅲ 期临床研究。该研究采取多中心、随机、双盲、阳性药物对照设计,以治疗后血清白蛋白变化水平为主要疗效指标,比较重组人白蛋白(rHA)与人血白蛋白(HSA)注射液在肝硬化腹水患者中的疗效等效性。
根据 Insight 数据库,全球目前仅有两款重组人白蛋白产品获批上市,分别为:安睿特的重组人白蛋白,2024 年 4 月在俄罗斯获批;禾元生物的植物源重组人血清白蛋白(HY1001),2025 年 7 月在中国获批,是全球首个获批的植物源重组人血清白蛋白。
特殊通道认定
1、强生:重磅 TCE 双抗三次获 CDE 拟突破性疗法
3 月 24 日,CDE 官网显示,强生 Teclistamab(特立妥单抗)注射液拟纳入突破性治疗品种,用于既往至少接受过一线治疗的复发或难治性多发性骨髓瘤(R/R MM)成人患者。
来源:CDE 官网
根据 Inisght 数据库,这是特立妥单抗第 3 次获得 CDE 的突破性疗法资格,另外两项适应症分别为:用于治疗既往至少接受过 3 线治疗的 R/R MM 成人患者,其既往治疗包括一种蛋白酶体抑制剂(PI)、一种免疫调节剂(IMiD)和一种抗 CD38 单克隆抗体;与达雷妥尤单抗联合用药适用于既往至少接受过一线治疗的 R/R MM 成人患者。
特立妥单抗是一款全球首创、即用型、基于体重给药的皮下注射 BCMA × CD3 双特异性抗体,2022 年 8 月和 10 月先后获 EMA 和 FDA 批准上市,单药适用于既往至少接受过三线治疗的 R/R MM 成人患者。2024 年 6 月,该产品在中国获批同适应症。
自上市以来,特立妥单抗销售额持续高速增长,2025 年已经攀升至 6.7 亿美元,跻身十亿美元分子阵营指日可待。
临床试验动态
1、联邦制药/诺和诺德:国产长效三靶点激动剂 II 期临床再获成功
3 月 25 日,联邦制药与诺和诺德联合宣布,UBT251 注射液已完成在中国 2 型糖尿病患者中开展的 II 期临床研究,并取得积极结果。UBT251 是国产首个、全球第 2 个以化学合成多肽法制备的长效 GLP-1R/GIPR/GCGR 三靶点激动剂。
截图来源:联邦制药公告
UBT251 是一款长效 GLP-1(胰高血糖素样肽-1)/GIP(葡萄糖依赖性促胰岛素多肽)/GCG(胰高血糖素)三靶点受体激动剂。截至目前,该药已获准在中国及/或美国开展治疗成人 2 型糖尿病、超重/肥胖、慢性肾脏病、代谢相关脂肪性肝炎多个适应症的临床试验。
2025 年 3 月,诺和诺德以 20 亿美元获得 UBT251 在大中华区(中国大陆 、香港、澳门和台湾地区)外全球其它地区的开发、制造和商业化的权利。联邦制药则保留 UBT251 在大中华区的权利。
本次公布的是一项随机、双盲、安慰剂及司美格鲁肽对照 II 期研究,共纳入 211 名中国 2 型糖尿病患者(单纯生活方式干预或与二甲双胍联用)。患者基线平均糖化血红蛋白(HbA1c)为 8.12%, 基线体重为 80.1 kg,基线 BMI 为 29.1 kg/m2。患者被随机分配接受每周一次的皮下注射 UBT251,剂量分别为 2 mg、4 mg、6 mg 或安慰剂或司美格鲁肽 1 mg,连续给药 24 周。 本研究的主要终点是治疗 24 周后患者 HbA1c 较基线的变化。
II 期研究结果显示,治疗 24 周后,UBT251 治疗组平均 HbA1c 降幅最高达 2.16%,显著优于司美格鲁肽组(1.77%)和安慰剂组(0.66%);UBT251 治疗组平均体重降幅最高达 9.8%,司美格鲁肽组下降 4.8%,而安慰剂组仅为 1.4%。此外,与安慰剂组相比,UBT251 在包括腰围、血压和血脂的关键次要终点方面均显示出改善。
本研究中,UBT251 显示出良好的安全性和耐受性,与其它三激动剂临床试验中观察到的结果基本一致。 联邦制药在公告中表示,UBT251 注射液在 2 型糖尿病患者中的 II 期临床研究达到预期目标,将尽快启动 UBT251 在中国 2 型糖尿病患者的 III 期临床研究。
值得注意的是,2026 年 2 月,联邦制药宣布 UBT251 在中国超重/肥胖患者中的 II 期临床研究中取得积极结果。研究数据显示,UBT251 各剂量组减重效果显著。给药 24 周后,试验药组平均体重较基线变化最高达 -19.7%(-17.5 kg),安慰剂组为 -2.0%(-1.6 kg) 。
2、信达生物:长效眼科新药 III 期成功,拟报上市
3 月 24 日,信达生物宣布,其依莫芙普-α 注射液(IBI302)在中国新生血管性年龄相关性黄斑变性(nAMD)人群中开展的 III 期临床研究(STAR,登记号:NCT05972473)达成 52 周主要终点。
来源:信达生物官微
依莫芙普-α 是信达生物自主研发的一种全球首创双特异性重组全人源融合蛋白。在此研究中,依莫芙普-α 视力改善效果非劣效于阿柏西普,同时展现了 16 周超长间隔给药的临床优势以及降低 MA(黄斑萎缩)发生的潜力。这是国内首个自主研发的眼底新药抗 VEGF 融合蛋白药物在首个 III 期研究里实现 16 周给药间隔的能力。
STAR 是一项在中国 nAMD 受试者中评估 8mg IBI302 疗效和安全性的 III 期临床研究。600 例受试者以 1:1 随机分配至 8mg IBI302 组及 2mg 阿柏西普组。IBI302 组和 2mg 阿柏西普组均接受每 4 周一次,共三次负荷治疗。完成负荷治疗后,IBI302 组根据第 16 和 20 周疾病活动情况个性化调整给药间隔,按照 Q8W、Q12W 或 Q16W 间隔完成后续治疗,2mg 阿柏西普组按照 Q8W 间隔完成后续治疗。
该研究持续 100 周,主要终点为:第 44、48 和 52 周时,研究眼最佳矫正视力(BCVA)字母数均值较基线的改变。本研究随机分层因素为:研究眼光学相干断层扫描(OCT)上是否含有 II 型脉络膜新生血管(CNV),以及研究眼既往是否接受过抗 VEGF 治疗。
研究共入组 600 例受试者,基线平均 BCVA 为 58.1 个 ETDRS 字母,基线平均中央视网膜厚度(CST)为 420.75 μm。基线时,研究眼既往未接受过抗 VEGF 治疗的比例约 65%。
结果显示:8mg IBI302 组视力改善非劣效于 2mg 阿柏西普组,研究主要终点达成。第 44、48 和 52 周时,8mg IBI302 和 2mg 阿柏西普组平均 BCVA 较基线变化最小二乘估计均值(SE)分别为 10.37(0.547)和 10.11(0.545)个 ETDRS 字母。
给药间隔延长:8mg IBI302 组中,约 86% 受试者可实现≥Q12W 的给药间隔,72.8% 受试者可以达到 Q16W 给药。至第 52 周时,约 95% 接受 Q12/16W 给药的受试者可以维持此给药间隔而无需接受再治疗。此外,56.3% 的受试者在 W24 无疾病活动,具备延长至 Q20W 给药的潜力。
解剖学疗效指标改善:两组受试者第 16 周时黄斑中心凹无视网膜内积液且无视网膜下积液的比例相近,第 52 周时包括 CST 较基线变化等各解剖学指标较基线改善程度相近。
抗黄斑萎缩(MA)趋势:第 52 周时,8mg IBI302 组和 2mg 阿柏西普组新发 MA 的比例分别为 1.5% 和 2.9%,IBI302 治疗后新发 MA 比例相较阿柏西普组下降约 50%,趋势与 II 期研究结果一致,提示 IBI302 具有减少 MA 发生的潜力。
安全性良好:8mg IBI302 组总体不良事件发生率与阿柏西普 2mg 组相当。眼部不良事件以轻中度为主,观察或常规处理后预后良好。
基于以上研究结果,信达生物正积极准备递交新药上市申请。
3、甘李药业:启动长效 GLP-1 新 III 期临床
3 月 24 日,药物临床试验登记与信息公示平台官网显示,甘李药业登记了一项在不使用气道正压通气治疗的肥胖的中度至重度阻塞性睡眠呼吸暂停受试者中评价 GZR18(博凡格鲁肽)注射液疗效与安全性的多中心、随机、双盲、平行、安慰剂对照的 Ⅲ 期临床研究(登记号:CTR20261125)。
来源:药物临床试验登记与信息公示平台官网
该研究计划在国内入组 140 名受试者,主要终点是治疗 52 周后,呼吸暂停低通气指数(AHI)相对基线的变化。次要终点包括 AHI 相对基线变化的百分比、AHI 较基线下降 ≥ 50% 的受试者比例、体重相对基线变化的百分比等。
博凡格鲁肽是甘李药业自主研发的 GLP-1RA 双周制剂,目前已经开展了 6 项 III 期临床。
作为潜在全球首个 GLP-1RA 双周制剂,博凡格鲁肽已经达成了 2 项出海授权合作,分别将拉丁美洲地区、印度地区的开发和商业化权益授权给了 Laboratorios Carnot 和印度鲁宾。
4、强生:自免大药启动头对头新 III 期临床
3 月 25 日,药物临床试验登记与信息公示平台官网显示,强生登记了一项古塞奇尤单抗头对头利生奇珠单抗治疗中重度活动性克罗恩病的 III 期临床。
来源: 药物临床试验登记与信息公示平台官网
这是一项 IIIb 期、多中心、随机、开放性、阳性对照研究,旨在评估在中重度活动期克罗恩病(一种引起肠道严重炎症的长期疾病)患者中,古塞奇尤单抗和利生奇珠单抗的治疗效果对比。
该研究拟在国内入组 37 人,国际入组 530 人,研究的主要终点指标是第 52 周时获得深度缓解的受试者例数。
古塞奇尤单抗是首个获得批准的全人源、具有双重作用机制的白介素 23 抑制剂,不仅可以直接结合白介素 23,还能够定位到主要产生白介素 23 的 CD64+炎症细胞。2017 年 7 月,古塞奇尤单抗注射液获 FDA 批准,用于治疗成人中重度斑块状银屑病,此后又积极拓展其他适应症。自上市后,古塞奇尤单抗销售额一路上涨,2025 年全球销售额已达 51.55 亿美元,同比增长超 40%。
本次头对头试验的利生奇珠单抗同样是一种 IL-23 抑制剂,最初由勃林格殷格翰研发,2016 年艾伯维获得其开发和全球商业化权益,2019 年 3 月率先在日本获批上市。
截至目前,该药已在全球获批多项适应症:克罗恩病、斑块状银屑病、泛发性脓疱型银屑病、红皮病型银屑病和银屑病关节炎等;2024 年其全球销售额达 117.18 亿美元,跻身百亿美元俱乐部,2025 年继续保持稳健增长,全年斩获 175.62 亿美元。
获批临床
1、科伦博泰:又一双抗 ADC 获批临床
3 月 25 日,科伦药业发布公告称,科伦博泰自主研发的新型靶向肿瘤相关抗原及免疫肿瘤学抗原 (TAA-PD-L1) 的双抗 ADC SKB103 在国内获批临床,拟开发用于治疗晚期实体瘤。
SKB103 是科伦博泰基于专有的 OptiDC™平台研发的一款潜在同类最佳新型 TAA-PD-L1 双抗 ADC。作为单一分子,SKB103 在设计上有望同时实现肿瘤靶向递送细胞毒载荷及肿瘤免疫微环境调节。在临床前研究中,SKB103 展现出优异的抗肿瘤活性和安全性。
SKB103 是科伦博泰首个进入临床阶段的 TAA-PD-L1 双抗 ADC,也是继 SKB571 之后第二款进入临床阶段的用于肿瘤治疗的双抗 ADC。
2、信立泰:siRNA 新药获批临床
3 月 24 日,CDE 官网显示,信立泰的 1 类新药 SAL0145 注射液获批临床,拟开发用于治疗代谢相关脂肪性肝炎(MASH)成人患者。
MASH 是代谢功能障碍相关脂肪性肝病(MASLD)的进展形式之一,后者累及全球约 30% 成年人口。若不加以干预或治疗,MASH 会进一步发展为肝硬化甚至肝癌,对患者的生命健康造成威胁。
SAL0145 是一种小干扰核酸药物(siRNA)。siRNA 通常是由碱基对组成的短双链 RNA,通过 RNAi 机制实现转录后水平特异性沉默致病靶基因 mRNA,达到精准治疗疾病的目的。
siRNA 药物可以精准靶向致病基因,同时具备不易产生耐药性以及药效持久的优势,给药频率降低,大幅提高患者依从性,有望打破传统药物治疗方案,在慢性病治疗领域具有巨大应用潜力。
临床前研究显示,SAL0145 具有治疗 MASH 的潜力,若能研发成功并获批上市,将有望为患者提供新的用药选择。
3、百利天恒:又一 ARC 获批临床
3 月 23 日,百利天恒发布公告称,其自主研发的 1 类新药 BL-ARC002 注射液的临床试验获得 NMPA 批准,拟开发用于包括但不限于标准治疗失败或无法获得标准治疗的局部晚期或转移性实体瘤治疗。
BL-ARC002 是百利天恒开发的一款潜在全球首创(First-in-class)抗体放射性核素偶联物(ARC)药物。
基于在抗体和 ADC 领域的技术优势,百利天恒建立了用于 ARC 开发的 HIRE-ARC 平台,该平台可以整合抗体介导的精准靶向递送技术与放射性核素强大的肿瘤杀伤能力。相较于传统的放射性核素药物偶联物 (RDC) 药物,ARC 疗法靶点特异性强、肿瘤富集高,克服耐药性能力更优异。
BL-ARC002 之外,百利天恒还开发了 BL-ARC001,该药于 2025 年 9 月在国内获批临床,拟用于包括但不限于标准治疗失败或无法获得标准治疗的局部晚期或转移性实体瘤治疗,是百利天恒首款获批临床的 ARC 药物。
国内药企财报
本周,多家国内药企亮出 2025「成绩单」,业绩喜人。Insight 对财报进行了跟踪报道,可点击以下链接跳转阅读详情:
中国生物制药 2025 年财报:营业收入超 318 亿元,创新药收入暴增 26.2%!
恒瑞医药 2025 年财报:营业收入超 316 亿元,创新药收入占比 58%
石药集团财报: 2025 年收入 260 亿元,BD 合作总额超 282 亿美元
诺诚健华 2025 年财报:营收大涨 135%,首次扭亏为盈
药明康德 2025 年财报:营收超 454 亿元,同比增长 15.8%
康诺亚:司普奇拜单抗大卖超 3 亿元,暴涨 775%
内容来源:药企官方发布新闻/资料、Insight 数据库
封面来源:站酷海洛 Plus
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
PR 稿对接:微信 insightxb
投稿:微信 insightxb;邮箱 insight@dxy.cn
点击卡片进入 Insight 小程序
国内审评进度、全球新药开发…
随时随地查!
多样化功能、可溯源数据……
Insight 数据库网页版等你体验
点击阅读原文,立刻解锁!
上市批准临床3期生物类似药财报临床2期
2026-03-23
·药明康德
百时美施贵宝PD-1抑制剂再获FDA与EMA批准
百时美施贵宝(Bristol Myers Squibb)近日宣布,其PD-1抑制剂Opdivo(nivolumab)在美国和欧盟分别获得针对经典型霍奇金淋巴瘤(cHL)两项新适应症批准。FDA批准Opdivo联合多柔比星、长春碱及达卡巴嗪(AVD)方案,用于治疗既往未经治疗的III期或IV期成人及12岁及以上青少年cHL患者。欧洲药品管理局(EMA)则批准Opdivo联合CD30靶向抗体偶联药物Adcetris(brentuximab vedotin)用于既往接受过一线治疗后复发或难治的5岁及以上儿童、青少年及30岁以下的成人cHL患者。
这次FDA的批准主要基于3期SWOG 1826研究结果。数据显示,在中位随访13.7个月时,Opdivo联合AVD方案在主要终点无进展生存期(PFS)方面显著优于对照组,将疾病进展或死亡风险降低58%(HR=0.42;95% CI:0.27–0.67;P<0.0001)。在更长的36.7个月中位随访中,两组的总生存期(OS)均尚未达到,但Opdivo联合AVD组死亡事件数较低,该组的死亡事件为9例(1.8%),对照组为17例(3.4%)。目前基于SWOG 1826数据的监管申请也正在EMA审评中。
而这次EMA批准Opdivo组合则是基于CheckMate-744临床2期研究的结果。该研究评估了Opdivo联合brentuximab vedotin用于既往接受过一线治疗后复发或难治的cHL患者,纳入5岁及以上儿童、青少年及30岁以下成人患者。结果显示,该联合方案在上述患者群体中实现了较高的完全代谢缓解率。研究还表明,基于疗效应答结果的治疗策略使大多数患者能够顺利进入后续巩固治疗阶段,同时整体安全性可控。
每半年给药一次!创新抗体即将进入3期试验
Apogee Therapeutics今日宣布,其在研抗IL-13抗体zumilokibart(APG777)在2期APEX临床试验A部分中取得积极的52周维持期数据。该研究针对中重度特应性皮炎(AD)患者,结果显示,无论是每3个月还是每6个月给药一次的维持治疗方案,均可实现疗效的持久维持。同时,在全体患者中,各类皮损及瘙痒相关终点均观察到疗效进一步加深,提示zumilokibart在疗效及给药频率方面具有潜在差异化优势,尤其是在显著降低给药频次方面有望优于当前标准治疗方案。
具体来看,在52周时,每3个月和每6个月给药方案下,分别有75%和85%的患者维持EASI-75应答,86%和78%的患者维持经验证研究者总体评估(vIGA)评分为0(皮损清除)或1(皮损几乎清除)水平。此外,两种给药方案均显示出良好的耐受性,其安全性特征总体与同类药物一致。公司同时表示,APEX试验B部分的16周诱导期数据预计将于2026年第二季度公布,并有望支持在2026年下半年启动针对中重度特应性皮炎的3期临床试验,进一步推进zumilokibart的临床开发进程。
反义寡核苷酸疗法获优先审评资格
今日,Ionis Pharmaceuticals宣布,美国FDA已受理其在研反义寡核苷酸疗法zilganersen(ION373)的新药申请(NDA),并授予优先审评资格,用于治疗亚历山大病(AxD)。FDA已将该申请的PDUFA目标审评日期设定为2026年9月22日。
此次优先审评资格的授予主要基于一项关键性临床研究结果。研究显示,在儿童及成人AxD患者中,50 mg zilganersen在第61周时相较对照组,在主要终点10米步行测试(10MWT)评估的步行速度方面实现了具有统计学意义且临床意义明确的稳定效果(最小二乘均值差异33.3%,P=0.0412),同时展现出良好的安全性和耐受性。此外,在评估适应能力、沟通能力、胃肠道症状、睡眠及癫痫发作等关键次要及探索性终点中,zilganersen亦持续表现出优于对照的趋势。
AxD是一种罕见、进行性、最终致命的神经系统疾病。该病常在儿童期发病且进展迅速,患者可能丧失行走、说话与吞咽等基本功能。AxD的发生是神经胶质纤维酸性蛋白(GFAP)基因变异的结果,GFAP变异会破坏大脑中星形胶质细胞的结构和功能。Zilganersen旨在阻止由于GFAP基因中的致病变异导致的过量GFAP蛋白表达,从而减缓或稳定AxD患者的疾病进展。
参考资料:
[1] Bristol Myers Squibb Transforms the Classical Hodgkin Lymphoma Treatment Paradigm with Expanded U.S. and EMA Approvals for Opdivo® (nivolumab). Retrieved March 23, 2026 from https://news.bms.com/news/corporate-financial/2026/Bristol-Myers-Squibb-Transforms-the-Classical-Hodgkin-Lymphoma-Treatment-Paradigm-with-Expanded-U-S--and-EMA-Approvals-for-Opdivo-nivolumab/default.aspx
[2] Apogee Therapeutics Announces Positive Phase 2 Part A 52-Week Data of Zumilokibart (APG777), Demonstrating Maintenance and Deepening of Responses with Every 3- and 6-Month Dosing in Moderate-to-Severe Atopic Dermatitis. Retrieved March 23, 2026 from https://www.globenewswire.com/news-release/2026/03/23/3260201/0/en/Apogee-Therapeutics-Announces-Positive-Phase-2-Part-A-52-Week-Data-of-Zumilokibart-APG777-Demonstrating-Maintenance-and-Deepening-of-Responses-with-Every-3-and-6-Month-Dosing-in-Mo.html
[3] Ionis announces zilganersen New Drug Application for Alexander disease (AxD) accepted by FDA for Priority Review. Retrieved March 23, 2026 from https://www.businesswire.com/news/home/20260323790940/en/Ionis-announces-zilganersen-New-Drug-Application-for-Alexander-disease-AxD-accepted-by-FDA-for-Priority-Review
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医药健康创新
临床结果临床3期临床2期抗体药物偶联物上市批准
100 项与 Zilganersen 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 亚历山大病 | 申请上市 | 美国 | 2026-03-23 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床3期 | 54 | Zilganersen 50 mg | 壓鏇簾襯夢齋窪膚鹹遞(鏇顧鑰襯鹽窪遞衊構鏇): Difference (%) = 33.3, P-Value = 0.0412 达到 更多 | 积极 | 2025-09-22 | ||
placebo |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
