预约演示
更新于:2026-06-06
YKYY029
更新于:2026-06-06
概要
基本信息
原研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评- |
登录后查看时间轴
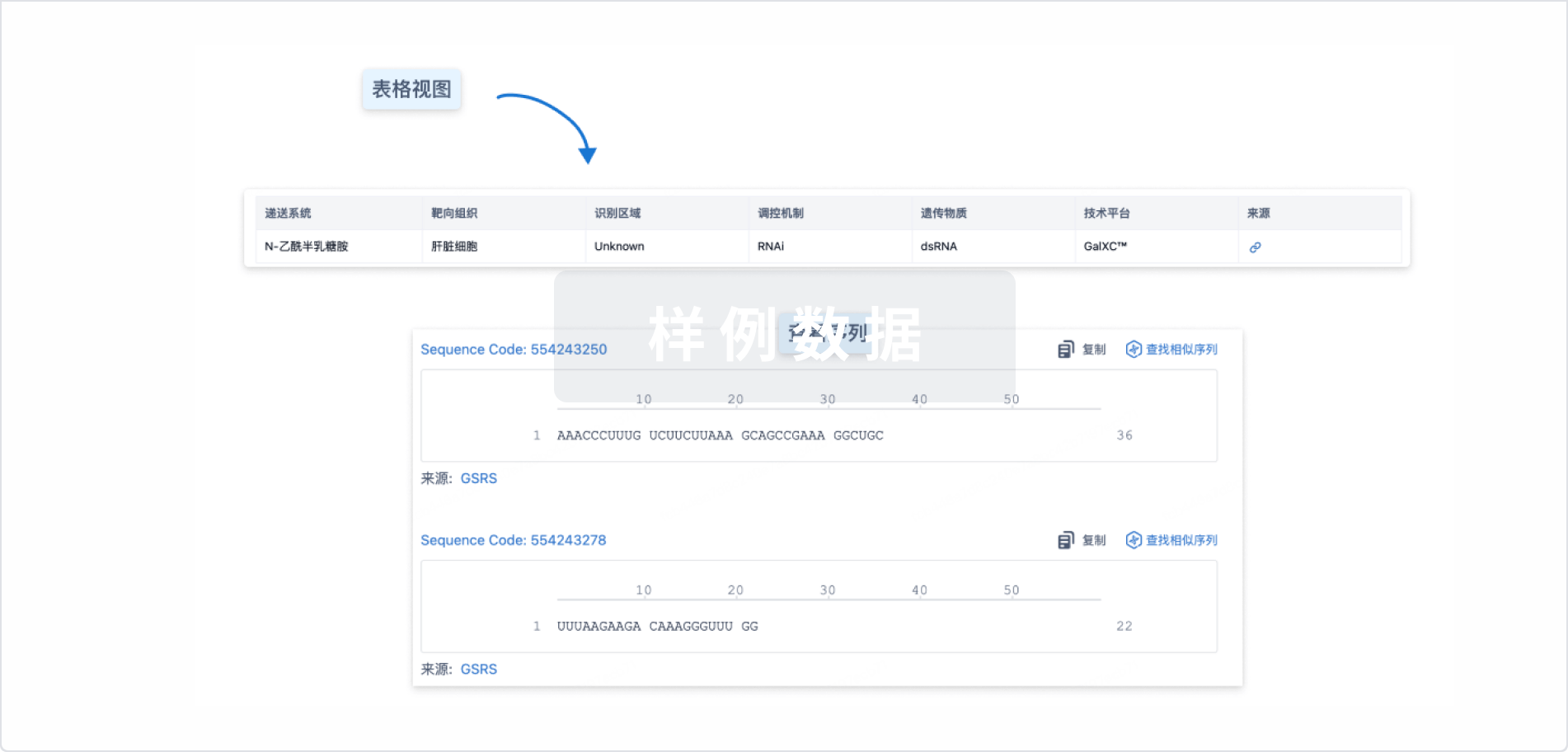
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
4
项与 YKYY029 相关的临床试验CTR20261322
在轻中度高血压患者中评价YKYY029注射液有效性和安全性的多中心、随机、双盲、安慰剂对照的Ⅱ期临床研究
主要目的
评价YKYY029注射液在轻中度高血压患者中,治疗第3个月时对收缩压(SBP)的影响;
次要目的
评价YKYY029注射液在轻中度高血压患者中,治疗第3个月时对舒张压(DBP)的影响。
评价YKYY029注射液在轻中度高血压患者中,治疗后第6个月、9个月、12个月对SBP和DBP的影响。
评价YKYY029注射液在轻中度高血压患者中,治疗后第3个月、6个月、9个月、12个月SBP、DBP的动态变化。
评价YKYY029注射液对血压昼夜节律的影响。
评价YKYY029注射液在轻中度高血压患者中多次给药治疗的安全性。
评价YKYY029注射液在参与者中的药代动力学(PK)特征。
评价YKYY029注射液在参与者中的药效动力学(PD)特征。
评价YKYY029注射液在参与者中的免疫原性。
开始日期2026-04-21 |
申办/合作机构  北京悦康科创医药科技股份有限公司 北京悦康科创医药科技股份有限公司 [+1] |
ChiCTR2600122200
A multicenter, randomized, double‑blind, placebo‑controlled, Phase II clinical study to evaluate the efficacy and safety of YKYY029 Injection in patients with mild to moderate hypertension
开始日期2026-03-01 |
申办/合作机构 |
CTR20252860
评估YKYY029注射液单次皮下注射在中国健康志愿者及原发性轻度高血压患者中的安全性、耐受性、药代动力学/药效学的I期临床研究
评价YKYY029注射液的安全性、耐受性、药代动力学/药效学
开始日期2025-07-24 |
申办/合作机构  北京悦康科创医药科技股份有限公司 北京悦康科创医药科技股份有限公司 [+1] |
100 项与 YKYY029 相关的临床结果
登录后查看更多信息
100 项与 YKYY029 相关的转化医学
登录后查看更多信息
100 项与 YKYY029 相关的专利(医药)
登录后查看更多信息
122
项与 YKYY029 相关的新闻(医药)2026-06-04
·中华网
本网消息 2026年5月30-31日,由中国商报社、中国工业报社主办,华夏商邦俱乐部、中国品牌发展网联合主办,中工智库、中国商业创新大会组委会承办的“2026华夏企业家论坛暨第九届品牌强国人物大会”在福州隆重举办。大会以“创新赋能·品牌向新”为主题,紧扣国家战略大势,汇聚政商学界精英,共话品牌建设、共探发展机遇、共绘品牌强国建设蓝图。2026品牌强国年度人物——悦康药业集团股份有限公司创始人、董事长于伟仕获奖理由:他,怀仁心之本,行致远之路,以赤诚深耕制药行业,以笃行守望万家安康。岁月淬炼初心,时光沉淀匠心,他深耕医药领域,深耕研发、精益求精,以严苛品质把控每一粒良药。他锚定民生医药赛道,温润济世、普惠于民,用心守护大众健康防线;秉持长远格局,开拓产业边界,雕琢享誉行业的民族医药品牌。风起潮涌,他坚守实业不改本色;步履不停,他深耕科研勇攀高峰。以情怀赋能产业,以责任承载使命,在生物医药的漫漫征途上,用坚守与热爱谱写一曲温润而磅礴的实业赞歌。2026品牌强国年度人物——悦康药业集团股份有限公司创始人、董事长 于伟仕2026品牌强国年度人物荣誉加冕现场第十一届全国人大常委会预算工作委员会原主任、原卫生部部长高强,原文化部副部长周和平,中国民族卫生协会会长吴英萍,福耀集团荣誉董事长、福耀科技大学理事长曹德旺,中国工业报社党委书记、社长徐金宝,中国商报社社长助理张家铭,华夏企业家论坛组委会秘书长、华夏商邦俱乐部秘书长曾跃,北京工业大学教授、博士生导师、品牌研究院院长祝合良,中国民族卫生协会副会长刘明慧、中国民族卫生协会副会长王湘雲,中国工业报社社长助理、中工智库执行秘书长孙崇铭,华夏企业家论坛组委会执行秘书长刘鹏,悦康药业集团股份有限公司创始人、董事长于伟仕,四川科伦药业股份有限公司董事长刘革新,第十一、十二届全国人大代表,中国商业联合会副会长、中国建筑材料流通协会执行委员会副会长、湖南万家丽实业集团董事长黄志明,全国政协委员、新大陆科技集团CEO王晶,修正药业集团总裁修远等领导、专家及企业家代表出席活动,并共同参与大会启动仪式。2026华夏企业家论坛暨第九届品牌强国人物大会启动仪式2026年作为“十五五”规划开局之年,中央经济工作会议明确提出强化企业创新主体地位、激发民间投资活力,为民营经济高质量发展指明方向,也为品牌强国建设注入强劲动能。企业家精神作为高质量发展的重要支撑,持续引领中国品牌转型升级、破浪前行。历经多年深耕沉淀,华夏企业家论坛已成为凝聚企业家共识、链接产业优质资源的重要平台,品牌强国人物大会更是国内发掘、表彰优秀品牌领军人物的权威专业平台。本次大会现场举办第九届品牌强国年度人物荣誉加冕仪式,悦康药业集团股份有限公司创始人、董事长于伟仕,四川科伦药业股份有限公司董事长刘革新,中国民族卫生协会会长、英平集团董事长吴英萍,第十一、十二届全国人大代表,中国商业联合会副会长、中国建筑材料流通协会执行委员会副会长、湖南万家丽实业集团董事长黄志明,全国政协委员、新大陆科技集团CEO王晶,修正药业集团总裁修远荣膺“2026品牌强国年度人物”荣誉称号。悦康药业集团股份有限公司创始人、董事长于伟仕出席大会悦康药业集团股份有限公司创始人、董事长于伟仕获评 2026 品牌强国年度人物(颁奖现场)悦康药业集团股份有限公司创始人、董事长于伟仕现场发表获奖感言2026品牌强国年度人物荣誉加冕现场中国商报社社长助理张家铭作为主办方代表致辞。他表示,将依托媒体聚力赋能优势,携手各界同仁凝聚奋进合力,共筑品牌强国事业。中国商报社社长助理张家铭致辞原文化部副部长周和平出席大会,并发表题为《深耕文化根脉 赋能品牌强国》的主题演讲,围绕品牌强国战略部署,深度分享文化赋能品牌建设、助力强国发展的思路与路径。原文化部副部长周和平发表主题演讲北京工业大学教授、博士生导师、品牌研究院院长祝合良出席大会,发表题为《数字时代的品牌营销策略》的主题演讲。他指出,数字经济时代下,企业需加快品牌建设数字化转型,主动拥抱数智营销新模式,助力品牌高质量发展、开启品牌发展新征程。北京工业大学教授、博导、品牌研究院院长祝合良发表主题演讲中国民族卫生协会会长吴英萍出席大会,发表题为《以民族健康品牌之力 筑品牌强国时代根基》的主题演讲。结合大健康产业发展趋势,她阐释了健康企业坚守品质初心、打造优质品牌、践行社会责任的发展路径。中国民族卫生协会会长吴英萍发表主题演讲华夏企业家论坛组委会秘书长、华夏商邦俱乐部秘书长曾跃发表题为《品牌追光者·筑梦中国芯》的主题演讲,并向到场领导、专家、企业家及媒体代表致以热烈欢迎。他表示,将以品牌深耕者的身份,携手各界实业同仁,共探中国品牌成长新路径、共担民族品牌振兴使命、共绘中国品牌走向世界的宏伟蓝图。华夏企业家论坛组委会秘书长、华夏商邦俱乐部秘书长曾跃发表致辞中国工业报社党委书记、社长徐金宝作为主办方领导致辞。他表示,希望以本次论坛为纽带,汇聚各方智慧力量,打通创新链、产业链、品牌链,助力企业提升核心竞争力,以品牌强企夯实品牌强国建设根基。中国工业报社党委书记、社长徐金宝发表致辞第十一届全国人大常委会预算工作委员会原主任、原卫生部部长高强为大会作主旨报告。他深入剖析当前中国经济发展的新特征、新机遇与新挑战,阐释政策支撑、创新驱动与品牌建设的内在关联,为企业把握发展大势、深耕实业根基、打造硬核品牌提供务实指引、提出殷切期望。第十一届全国人大常委会预算工作委员会原主任、原卫生部部长高强发表主旨报告福耀集团荣誉董事长、福耀科技大学理事长曹德旺亲临现场出席本次大会,与各界实业翘楚齐聚一堂,共探实业深耕与品牌发展路径。悦康药业集团股份有限公司创始人、董事长于伟仕,第十一、十二届全国人大代表、湖南万家丽实业集团董事长黄志明,修正药业集团有限公司总裁修远等优秀企业家代表先后发言,结合自身企业发展实践,分享经营管理智慧、行业发展研判与品牌建设经验。福耀集团荣誉董事长、福耀科技大学理事长曹德旺先生出席盛会悦康药业集团股份有限公司创始人、董事长于伟仕致辞第十一,十二届全国人大代表,中国商业联合会副会长,中国建筑材料流通协会执行委员会副会长,湖南万家丽实业集团董事长黄志明致辞修正药业集团有限公司总裁修远致辞华夏企业家论坛组委会执行秘书长刘鹏在大会庆典晚宴上发表祝酒辞。他表示,华夏企业家论坛将坚守赋能实业发展、培育优质品牌、链接产业资源、聚力合作共赢的初心,持续助力中国企业扎根实业、迭代升级、突破发展。华夏企业家论坛组委会执行秘书长刘鹏发表祝酒辞据悉,本届大会得到英平集团、悦康药业集团、修正药业集团、科伦药业、稻花香集团、万家丽实业集团、新大陆科技集团、睦白实业、新加坡FHK集团、易储数智能源集团、德化五洲陶瓷股份、华亚众盟企业管理咨询、明伦公益基金会等数等诸多优秀企业的大力支持。2026华夏企业家论坛暨第九届品牌强国人物大会现场(部分)个人简介:于伟仕出生于安徽省太和县,徽商全球理事会主席团终身主席,悦康药业集团股份有限公司创始人、董事长。常年负责在新药研发、药品生产、流通销售、国际贸易等领域。于伟仕先生在医药界辛勤耕耘40余年,现任中国医药保健品进出口商会副会长、徽商全球理事会主席团终身主席。多次荣膺“中国医药经济年度人物”称号,并先后获评“影响中国改革开放二十年20位企业家”、“中国经济贡献百名杰出人物”、“中国优秀创新企业家”、“中国大健康产业功勋人物”、“徽商‘奥斯卡’终身成就奖”等重大奖项。多年来,于伟仕始终致力于“做百姓用得起的好药”,带领悦康药业推出了以悦康通银杏叶提取物注射液、活心丸(浓缩丸)为代表的140余个品种、200余个品规的产品,覆盖心脑血管、呼吸系统、抗肿瘤、抗感染等核心治疗领域,并开发出中国第一款自主研发的ED治疗药物枸橼酸爱地那非,打破了我国在ED治疗领域无国产原研药物的历史。同时,每年投入数亿元进行创新研发,打造了十一大核心技术平台,涵盖核酸药物、多肽药物、细胞与基因治疗药物、中药创新药以及高端化药等领域,以前沿技术解决未被满足的临床需求,帮助人类治愈疾病、减轻病痛和提高生活质量。企业简介悦康药业集团成立于2001年,总部位于北京,是一家集新药研发、药品生产、流通销售及国际贸易于一体的医药集团企业。2020年12月24日,悦康药业在上海证券交易所科创板上市,股票代码688658。悦康药业以“产品、产能、产业链”为核心,在北京组建了集团药物研究院,并以安徽、河南医药原料基地为基础,在北京、广州、合肥建立了不同的制剂生产基地。集团现为中国医药工业百强企业、医药工业研发十强、国家技术创新示范企业、全国“质量标杆”企业、国家绿色制造体系建设示范企业“绿色工厂”、国家智能制造试点示范企业、国家认定企业技术中心。悦康药业通过技术创新、研发创新打造了全新的创新研发布局,目前已形成核酸药物靶点发现平台、多肽药物开发平台、细胞与基因治疗药物开发平台、缓控释制剂技术平台、全流程AI药物研发平台等十一大核心研发平台,涵盖核酸药物、多肽药物、细胞与基因治疗药物、中药创新药以及高端化药等领域,并相继组建了头孢药物晶型研究国家地方联合工程实验室、心脑血管北京市工程研究中心等,建立了悦康集团院士专家工作站、博士后科研工作站、博导工作站等完善的研发体系,并在2015、2016连续两年荣获国家科技进步二等奖。集团现有140余个品种、200余个品规的药品,涵盖心脑血管、消化系统、抗感染、内分泌、抗肿瘤等多个核心治疗领域。2021年,悦康药业联合解放军总医院第五医学中心正式开展核酸抗癌药CT102临床试验,全面切入核酸药物新赛道;截至目前,YKYY029(降压siRNA)、YKYY013(乙肝siRNA)等9个品种相继获得中美双IND批准,公司以核酸创新药为核心启动港股上市进程。三款一类中药创新药通络健脑片、紫花温肺止嗽颗粒、注射用羟基红花黄色素A,新药上市申请均已正式获得受理。在生产制造和质量管理方面,悦康集团不断推进技术革新,实施智能制造和绿色化生产,实现药品生产体系与国际接轨。自2011年起,悦康固体片剂和胶囊剂生产线已经多次通过欧盟GMP认证,广州药厂通过日本GMP认证。“营造全球喜悦,关爱人类健康”是悦康的企业宗旨,在“合和”文化的感召下,悦康人诚信勤奋,为实现“创行业名牌,建药业航母,打造百年老店”的目标努力奋斗。通讯员:向阳
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。责任编辑:kj005
文章投诉热线:157 3889 8464 投诉邮箱:7983347 16@qq.com
2026-05-31
(本报告:AI信息收集95% + 人类判断决策5%)
根据市场中,过去仿制药企业转型创新药,筛选出15家生物医药上市公司,同时由于这种公司对市场的强β刺激,所以部分公司在过去的一年半时间里表现异常的好!所以我们需要考虑公司的管线竞争力、所处的阶段,公司股价所处的位置以及市值大小等等,来筛选出最适合参与定增的上市公司。
从涨幅依次分为两个梯队:
中高涨幅:昂立康/广生堂/前沿生物/华人健康 /苑东生物/泰恩康
中低涨幅:汇宇制药/悦康药业/立方制药/润都股份/奥赛康/科兴制药/京新药业
我们由低到高开始分析,如果没有分析,那么大概率上市公司就是没有独立的创新药管线,要么就是不差钱,不需要定增!
①、科兴制药-评级:☆☆☆
总市值:42亿元、研发投入2.51亿元,占营收比例16.39%
科兴制药严格剔除生物类似药、改良型新药,共5个,全部为公司自主研发、拥有全球知识产权的1类新药,采 用中美双报策略!
5个1类新药同步推进(1个III期、1个II期、3个I期),2026-2028年将进⼊临床费用⾼峰期,公司账⾯货币资金约8亿元,仅能覆盖3年左右研发投⼊,叠加港股IPO募资仍可能存在缺⼝,定增需求持续存在!
重点分析最重要的三个创新药品种GB10、GB18和GB19
一、GB10(VEGF/Ang2双抗,nAMD)
眼科长效双抗第二梯队领跑者
1. 市场与临床痛点
全球nAMD患者超2000万,中国超400万,2024年全球眼底抗VEGF市场156亿美元,中国50 亿元
2、核心痛点:现有药物需每⽉/每2个⽉注射⼀次,患者依从性极差(仅30%患者坚持规范治疗)
3.科兴竞争优劣势
全球最⾼浓度眼科双抗制剂(140mg/mL),注射体积仅为罗氏Faricimab的1/3,患者舒适度⼤幅提升。临床前数据:VEGF阻断效力为对照药7.5倍,Ang2阻断效力为94倍,猴CNV模型药效与罗氏相当。兔眼玻璃体内半衰期59.4⼩时,⽀持每4个⽉给药⼀次,与全球⾦标准持平
劣势:进度落后于罗氏(已上市)和荣昌(III期),预计2030年后才能上市 ,眼科市场渠道壁垒⾼,需建⽴专业的眼科销售团队。
• 全球已形成"罗氏⼀家独⼤,国内多家追赶"的格局 科兴凭借超⾼浓度制剂的差异化优势,有望在上市后抢占10%-15%的国内市场份额,未来竞争焦点:给药间隔进⼀步延⻓(⾄每6个⽉)、多适应症拓展
⼆、GB18(GDF15纳⽶抗体,肿瘤恶病质):
1. 市场与临床痛点
全球肿瘤恶病质患者超2000万,中国超500万,恶性肿瘤患者发病率40%-70% ⽬前全球⽆任何获批的靶向治疗药物,仅能通过营养⽀持缓解,临床需求极度迫切
2.市场空间:预计⾸款药物上市后,全球市场规模将突破100亿美元
3. 科兴竞争优劣势
✅核心优势:
• 分⼦类型 国内唯⼀进⼊临床的GDF15靶点肿瘤恶病质药物,全球第三
•采用纳⽶抗体-Fc融合结构,稳定性显著优于全⼈源单抗,表达量达10g/L,⽣产成本更低
• 临床前数据:在三种肿瘤模型中完全逆转体重下降,肌⾁和脂肪恢复效果优于辉瑞同靶点药物 已完成中美双报,同步开展国际临床,具备全球商业化和BD潜力
❌劣势:
√、进度落后于辉瑞和CatalYm约2年,若辉瑞2028年获批,将抢占先发优势 靶点验证仍需临床数据⽀持,存在II/III期失败⻛险 4. 竞争格局总结:
全球仅4家企业进⼊临床,⽆获批药物,竞争格局极佳 科兴作为国内唯⼀、全球第三的玩家,若临床成功,将成为国内⾸款肿瘤恶病质靶向药物
未来竞争焦点:临床数据优劣、适应症拓展(心衰、代谢疾病)
三、GB19(BDCA2单抗,红斑狼疮):
1. 市场与临床痛点
全球SLE患者超500万,中国超100万,2025年全球SLE药物市场65亿美元,中国34亿美元 现有药物以激素和B细胞靶向药物为主,疗效有限且副作用⼤,约50%患者治疗效果不佳 BDCA2靶点通过抑制I型⼲扰素通路发挥作用,与现有药物机制互补,是SLE领域最具潜力的新靶 点之⼀!
2. 科兴竞争优劣势
✅核心优势:
√、国内唯⼀、全球第⼆进⼊临床的BDCA2单抗,全球同靶点仅4家在研,⽆获批药物
√、 单次给药靶点抑制时间超90天,给药频次(每4周1次)显著优于渤健(每2周1次),患者依 从性更⾼ ,
√、临床前数据:体外活性更⾼、免疫原性更低、安全性更好,具备同类最佳潜力。
√、 2026 年3⽉同时获NMPA和FDA临床批准,中美双报同步推进 ❌劣势:
进度落后于渤健约3年,渤健预计2029年获批 。
3. 竞争格局总结
• 全球竞争极度稀缺,仅渤健和科兴进⼊临床,是三个品种中竞争格局最好的
• 科兴凭借更⻓的给药间隔和更优的安全性,有望在上市后与渤健分庭抗礼 未来竞争焦点:III期临床数据、适应症拓展(硬⽪病、⼲燥综合征等)
②、京新药业—定增参与评级:☆
总市值:116亿元、研发投入4.52亿元,占营收比例11.1%
严格按照"已启动并正在正常推进临床、有实质性⼊组/数据产出"的标准筛选,京新药业⽬前确实只剩下JX2201(口服Lp(a)抑制剂)这⼀个真正在跑 的1.1类新药。
为什么只剩下Lp(a)⼀个: 京新药业2025年研发费用约4.5亿元,扣除地达西尼商业化和仿制药研发后,能投⼊到1类新药的资金不⾜2亿元 公司明确提出"聚焦核心管线"战略,砍掉了所有⾮核心、进度慢、竞争格局差的项⽬ JX2201 是⽬前唯⼀有明确BD价值、能带来⼤额现⾦流的品种,⾃然成为唯⼀重点!
公司最主要的核心产品“地达西尼”销售数据,2025年全年1.95亿元,2026年⼀季度0.55亿元,同⽐增长12%,环比增长8%,覆盖 3000 多家医院,其中三级医院900多家。
国内失眠药物市场规模约270亿元,地达西尼属于第三代GABA-A受体部分激动剂,与第四代⻝欲素受体拮抗剂形成差异化竞争:
✅核心优势:
• 唯⼀不依赖CYP450代谢的失眠创新药,药物相互作用⻛险为0,是⽼年患者、⾼⾎压/糖尿病合并失眠患者的⾸选
• 医保价格优势明显(19.8元/片),仅为进⼝⻝欲素受体拮抗剂的1/3
• 已完成全国渠道铺设,商业化团队超过500⼈
❌核心劣势:
• 对睡眠结构的改善不如⻝欲素受体拮抗剂,次⽇残留效应略明显 • 失眠药物属于医保严控品类,未来降价压力较⼤
增长天花板:预计峰值销售额8-10亿元,2028年前后达到,是公司稳定的现⾦⽜业务。
√、JX2201(口服Lp(a)抑制剂)
全球共7家企业的口服Lp(a)抑制剂进⼊临床阶段,其中中国有3家(恒瑞、京新、信⽴泰),恒瑞和京新并列国内第⼀梯队,均处于II期 临床。
✅优势:
• 公司全部创新药研发资源倾斜,疗效和安全性已得到验证
•公司战略⾼度聚焦,所有创新药资源全部倾斜给JX2201
• 地达西尼提供稳定现⾦流,研发资金有保障
❌劣势:
进度略落后于恒瑞约3-6个⽉ 商业化能力远弱于恒瑞 海外BD进展缓慢,尚未达成实质性交易
√、 全球地位:全球第三、国内并列第⼀的口服Lp(a)抑制剂,仅次于礼来和恒瑞!
√. 国内竞争格局:形成"恒瑞+京新双雄领跑,信⽴泰追赶"的格局,未来3-5年国内市场将主要由这 三家⽠分
√. 先发优势:⽐信⽴泰快⾄少18个⽉,⽐阿斯利康、诺华、辉瑞等MNC的中国进度快⾄少3年以上
√. 最⼤⻛险:恒瑞HRS-5346的II期数据优于京新,或者恒瑞率先获批上市,抢占先发优!(凡是有恒瑞的地方,就会寸草不生,尤其是在国内市场!)
③、奥赛康-评级:☆☆
总市值:135亿元、研发投入4.28亿元,占营收比例13.31%
截⾄2026年5⽉30⽇,奥赛康共有8款进⼊临床阶段的1类创新药(含1款已上市),其中3款处于III期/NDA阶段,管线梯度清晰,核心聚焦肺癌、胃癌、耐药菌感染三⼤临床未 满⾜需求,整体竞争格局呈现"核心赛道有梯队、差异化靶点有亮点、热⻔赛道压力⼤"的特点。
三代EGFR已经上市,并授权给信达生物推广,不做介绍分析!
一、处于III期/NDA阶段的1类创新药(3款)
√、 ASKB589注射液 (靶点:Claudin18.2单抗 )
2、适应症:胃及⻝管胃交界处腺癌⼀线治疗
3、最新进展:2026年5⽉完成III期临床⼊组,预计2026年底递交NDA 核心4、优势:亲和力⾼,ADCC效应强,对低表达Claudin18.2患者也有效
5、竞争格局:已上市:荣昌⽣物维迪西妥单抗(ADC)
III 期阶段:科伦SKB264(ADC)、乐普MRG003(ADC)、⽯药SYSA1801(ADC)
特点:Claudin18.2赛道极度拥挤,单抗类产品面临ADC的强力竞争。
√、ASKC202片 (⾼选择性c-Met抑制剂 )
2、适应症:与利厄替尼联合治疗EGFR-TKI耐药后MET异常的⾮小细胞肺癌
3、最新进展:III期临床⼊组中,预计2027年递交NDA
4、核心优势:选择性⾼,脱靶毒性低,与EGFR-TKI联合用药协同效应好
5、竞争格局: 已上市:恒瑞赛沃替尼、和⻩沃利替尼
III 期阶段:⻉达BPI-9016M、岸迈EMB-01(双抗)
6、特点:主要竞争在于联合用药方案,公司有⾃⼰的EGFR-TKI产品,协同优势明显
处于I/II期临床研究——最新核心管线平台“SmartKine细胞因子前药平台”
⼀、平台定位:专⻔解决“细胞因⼦毒性⼤、没法用”的痛点
传统细胞因⼦(IL-2、IL-15)抗癌强但全⾝毒性巨⼤:
√、半衰期短、要频繁⼤剂量,
√、全⾝激活免疫→细胞因⼦⻛暴、⾎管渗漏、低⾎压
√、治疗窗极窄,临床很难用
SmartKine 核心:把细胞因⼦做成“带锁的前药”,只在肿瘤⾥“开锁激活”,⾎液⾥⼏乎⽆活性。
总结:系统惰性、肿瘤局部激活、疗效保留、毒性⼤降、
二、平台核心优势(和传统IL-2/IL-15⽐)
1. 毒性断崖式下降:避免全⾝激活,治疗窗扩⼤5‒10倍,可更⾼剂量、更⻓周期。
2. 半衰期⼤幅延⻓:Fc融合+前药稳定,半衰期可达40‒60⼩时,数天打⼀次即可。
3. 肿瘤局部⾼浓度:激活只在肿瘤⾥,疗效⽐普通IL-15更强
4. 可模块化组装:IL-2/IL-15/IL-12+抗体(PD-1/CTLA-4/靶向)⾃由组合,快速出新品。
5. 全球专利壁垒:⼗⼏个专利家族,掩蔽+连接⼦+融合架构全覆盖。
三、平台管线:两个核心临床品种+后续梯队
1)ASKG315:IL-15前药-Fc融合(单药/联合PD-1)
√、全球首个进⼊临床的IL-15前药
√、结构:IL-15+可切割Mask+Fc(⻓效) —I期临床(中美),联合PD-1
√、特点:半衰期⻓、安全窗⼤、单药/联用均可
2)ASKG915:PD-1抗体/IL-15前药双功能融合(核心王牌)
√、全球首个PD-1+IL-15前药融合分⼦进⼊临床
√、结构:PD-1单抗⻣架+两个IL-15前药模块
√、机制:PD-1阻断+肿瘤靶向+局部IL-15激活三位⼀体
√、2026 ASCO数据(关键): 后线MSS结直肠癌:PR30%(传统PD-1单药⼏乎⽆效) 安全性好,剂量爬坡顺利,⽆严重细胞因⼦⻛暴
进展:中美I期,数据积极,有望First-in-class
3)后续储备:IL-2 前药、IL-12前药、双细胞因⼦组合、更多抗体-细胞因⼦融合分⼦ 全部基于同⼀平台,研发周期短、成本低、可快速迭。
SmartKine是奥赛康从仿制药企转型为创新Biotech的“硬核底盘”:用肿瘤微环境特异性前药激活,解决细胞因⼦,“强疗效+⾼毒性”的行业死⽳;ASKG915/315是全球进度领先的First/Best-in class资产,2026‒2027临床数据是奥赛康创新药估值的核心催化剂!
④、汇宇制药-定增参与评级:☆☆☆
总市值:75亿元、研发投入3.44亿元,占营收比例34.51%
截⾄2026年5⽉30⽇,汇宇制药共有5款进⼊临床阶段的1类创新药(全部聚焦肿瘤领域),其中4款处于I/II期,1款完成单药I期;管线以KRAS通路、多靶点 免疫治疗、ADC为核心方向,差异化布局全球新靶点!
√、 HYP-2090PTSA胶囊—KRASG12C/PI3K双靶点⼩分⼦抑制剂
1、适应症:KRASG12C突变的晚期实体瘤(⾮小细胞肺癌、结直肠癌为主)
2、 最新进展:I/II期临床进⾏中,已在全国6家中心开展多队列研究
3、核心优势:全球首个进⼊临床的KRASG12C/PI3K双靶点抑制剂,可同时阻断两条关键致癌通路, 克服单药耐药
4、竞争格局:
已上市:阿达格拉西布、索托拉西布(单靶点KRASG12C)
在研:国内多家企业布局单靶点KRASG12C,双靶点产品汇宇制药进度最快!
√、 HYP-6589片(HY-0006)——⾼选择性SOS1⼩分⼦抑制剂
1、适应症:晚期实体瘤;与奥希替尼联合治疗EGFR突变⾮小细胞肺癌
2、最新进展:单药I期临床完成;2026年1⽉获批与阿斯利康奥希替尼联合用药临床
3、核心优势:选择性⾼,脱靶毒性低;与阿斯利康达成全球临床合作,加速研发进程
4、竞争格局:
全球在研:MiratiMRTX-0902(II期)、⽯药SYH-2038(I期)
特点:SOS1是KRAS通路的关键上游靶点,联合用药潜力巨⼤。
√、注射用HY07121(HY-0007)—PD-1/TIGIT/IL-15 三特异性双抗融合蛋⽩
1、适应症:晚期实体瘤(肝癌、肺癌、胃癌等)
2、最新进展:I/II期临床进⾏中,2024年10⽉完成⾸例受试者⼊组
3、核心优势
全球首个进⼊临床的PD-1/TIGIT/IL-15三靶点融合蛋⽩,可同时阻断两个免疫检查点并 激活免疫细胞,克服免疫耐药
4、竞争格局
全球在研:同类三靶点产品均处于临床前或早期临床阶段,免疫治疗下⼀代热⻔方向,市场潜力巨大!
公司还有8款1类创新药处于临床前研究阶段,涵盖: KRAS通路其他靶点(如KRASG12D、KRASG12V);新⼀代ADC(不同靶点、不同毒素);双特异性抗体;蛋⽩降解剂(PROTAC)。公司计划未来3年每年有2-3个1类创新药进⼊临床阶段。
⑤、悦康药业-定增参与评级:☆☆
总市值:80亿元、研发投入4.57亿元,占营收比例18.67%
这家公司我们只关注其“小核酸管线”!
悦康药业是国内唯⼀同时拥有⾃主GalNAc和LNP递送系统、且5款⼩核酸全部实现中美 双报的传统转型药企。已临床的5款产品形成"1款II期、1款I/IIa期、3款I期"的梯度布局,全部 聚焦心脑⾎管、乙肝、肝癌三⼤千亿级市场,其中YKYY029(AGTsiRNA)全球进度第⼀、具备 First-in-class 潜力,YKYY015(PCSK9siRNA)是国内唯⼀获FDAIND的⾃主GalNAc产品!
⼩核酸药物的成败90%取决于递送系统,悦康的⾃主GalNAc平台是其最⼤差异化优势:
1、完全⾃主知识产权:已获中国发明专利授权(ZL202310705604.5)及PCT国际申请,突破 Alnylam 等国外企业的专利垄断
2、技术优势:采用独特的三价GalNAc结构和定点偶联技术,肝靶向效率⽐进⼝技术⾼20-30%,脱 靶效应降低50%以上,⽣产成本低30%以上!
3、平台化能力:已成功应用于YKYY015、YKYY029、YKYY013、YKYY032四款siRNA药物,实现"⼀ 个平台、多个产品"的快速迭代。
4、关键辅料⾃主:⾃主研发的阳离⼦脂质YK-009已完成美国FDADMF备案,是国内少数能规模化⽣ 产核酸药物关键辅料的企业。
公司的注射用CT102(ASO II期),国内首个自主研发的抗肝癌ASO,这个产品洪帮主瞧不上,直接跳过,进入最核心的管线:
√、YKYY015注射液(siRNA,I/IIa期)
国内唯⼀获FDA-IND的⾃主PCSK9 siRNA
1、作用机制:通过siRNA沉默肝脏PCSK9mRNA,增加肝细胞表⾯LDL受体数量,显著降低低密度 脂蛋⽩胆固醇(LDL-C)
2、最新进展:国内Ia期完成,Ib/IIa期进⾏中;2024年8⽉获美国FDA-IND批准,是国内唯⼀获 FDA批准临床的⾃主GalNAc PCSK9siRNA
3、核心临床数据:Ia期显⽰,单次给药后LDL-C最⼤降低超过65%,且持续时间超过6个⽉,安全性良好,⽆严重不良反应。
4、完全⾃主可控的GalNAc递送系统,⽣产成本⽐进⼝技术低30%以上;临床前数据显⽰降脂效果和持续时间优于同类产品;中美双报,具备出海潜力!
但进度落后于信达、恒瑞等头部企业,市场先发优势丧失;PCSK9赛道竞争激烈,价格战不可避免!
√、YKYY029注射液(siRNA,II期)
全球首个进⼊II期的AGT(血管紧张素)-siRNA
1、作用机制:通过siRNA沉默肝脏AGTmRNA,从源头阻断RAAS系统,实现⻓效平稳降压;
2、最新进展:2026年4⽉启动II期临床,由北京⼤学第三医院唐熠达教授牵头;2025年7⽉获中美双批IND,I期临床仅用数⽉即完成并推进⾄II期;
3、核心临床数据:I期显⽰,单次给药后⾎压最⼤降低超过20/10mmHg,且持续时间超过6个⽉, 安全性良好,⽆严重不良反应。;I期临床数据优于罗氏同类产品,有望彻底解决⾼⾎压患者依从性问题(传统药物需每⽇服药,约50%患者⾎压控制不佳)
√、YKYY013注射液(siRNA,I期)
覆盖全基因型的乙肝功能性治愈候选药
1、靶点:乙型肝炎病毒(HBV)基因组
2、作用机制:通过siRNA沉默HBVmRNA,抑制病毒复制和抗原表达,为宿主免疫重建创造条件, 有望实现乙肝功能性治愈;
3、 最新进展:2025年7⽉获中美双批IND,国内I期临床进⾏中;
4、核心优势:覆盖HBVA-J⼗种基因型,对所有流⾏株均有效;采用⾃主GalNAc递送系统,肝靶向 效率⾼,副作用小;
5、竞争格局 ◦
全球在研:GSK3228836(II期)、腾盛博药BRII-835(II期)、ArrowheadARO-HBV(II 期)
国内在研:腾盛博药、歌礼制药、广生堂等,均处于II期阶段;
√、YKYY032注射液(siRNA,I期):针对⽆药可治的⾼脂蛋⽩(a)⾎症
1、靶点:脂蛋⽩(a)(Lp(a))
2、作用机制:通过siRNA沉默肝脏LPAmRNA,显著降低⾎浆Lp(a)⽔平
3、最新进展:2025年7⽉获中美双批IND,国内I期临床进⾏中
4、 核心优势:Lp(a)是独⽴心⾎管⻛险因⼦,⽬前⽆有效治疗药物,市场需求巨⼤;采用⾃主 GalNAc递送系统,疗效和安全性好
5、竞争格局
全球在研:诺华/AlnylamPelacarsen(III期,2026年上半年读出数据)、默沙东MK-0616 (II 期);
国内在研:恒瑞医药、信达⽣物、君实⽣物等,均处于I期阶段;
⑥、苑东生物-定增参与评级:☆
总市值:93.7亿元、研发投入2.86亿元,占营收比例21.44%
截⾄2026年5⽉30⽇,苑东⽣物⽆已上市1.1类化学创新药,共有5款进⼊临床/IND 阶段的1类创新药,其中1款处于Ib/IIa期,4款处于I期/IND受理;核心聚焦麻醉镇痛、抗肿瘤、 ⾃⾝免疫性疾病三⼤领域,以靶向蛋⽩降解(TPD)、ADC、新型⼩分⼦为核心技术方向,整体处于创新转型中期、后期管线薄弱但早期管线差异化明显的阶段。
√、HP-001胶囊(核心重磅,CRBN分⼦胶)
1、靶点:CRBNE3泛素连接酶,选择性降解IKZF1/3转录因⼦
2、适应症:复发/难治性多发性⻣髓瘤(RRMM)、⾮霍奇⾦淋巴瘤等⾎液肿瘤 3、最新进展:已完成Ia期单药剂量爬坡,进⼊Ib期剂量拓展及IIa期联合地塞⽶松用药阶段,各剂量组均观察到有效性积极信号,安全性可控;
国内进度最快的IKZF1/3分⼦胶之⼀,临床前数据显⽰选择性优于来那度胺和泊⻢度胺,神经 毒性和⻣髓抑制显著降低。对来那度胺耐药的多发性⻣髓瘤细胞仍有强效杀伤作用,有望解决临床耐药问题,海思科的直接竞争对手!
√、EP-0210 单抗注射液(⾃⾝免疫领域核心)
1、靶点:肿瘤坏死因⼦样配体1A(TL1A)
2、适应症:炎症性肠病(克罗恩病、溃疡性结肠炎)
3、最新进展:2026年1⽉完成I期临床试验⾸例受试者给药
4、核心优势: 临床前数据显⽰靶点亲和力和体内药效优于国外同靶点竞品RVT-3101,TL1A是炎症性肠病领域的下⼀代热⻔靶点,现有TNF-α抑制剂存在应答率低、耐药性等问题
5、竞争格局
全球在研:辉瑞PF-06700841(II期)、罗氏RO7284129(II期)
国内在研:恒瑞医药、信达⽣物、君实⽣物等,均处于I期阶段;
√、EP-0226 片(麻醉镇痛领域核心)
1、靶点:新型钙离⼦通道Cav2.2α2δ亚基调节剂
2、适应症:神经病理性疼痛
3、最新进展:2026年1⽉完成I期临床试验⾸例受试者给药
4、核心优势: 作用机制新颖,与已上市的普瑞巴林、加巴喷丁相⽐,靶点选择性更⾼,中枢神经系统副作用 显著降低与公司麻醉镇痛主业形成协同,商业化渠道成熟;
5、竞争格局:
已上市:普瑞巴林、加巴喷丁(年销售额均超百亿元)
在研:国内仅少数企业布局同靶点创新药,竞争相对温和;
公司还有在研的TF-ADC产品和BTK(可透脑口服PROTAC降解剂)不过在洪帮主看来,都是竞争激烈,而且与公司主业偏离较远,临床进展也慢于同类公司!
公司还有10余款1类创新药处于临床前研究阶段,涵盖靶向蛋⽩降解(TPD):HP-003(VAV1分⼦胶)、HP-004(STAT3-PROTAC)等;ADC:YLSH004(靶向Claudin18.2)、YLSH005(靶向HER2)等,新型⼩分⼦:EP-0230(镇痛)、EP-0240(抗肿瘤)等。 公司计划未来3年每年有2-3个1类创新药进⼊临床阶段!
(未完待续)
文 | 洪帮主
微信号 | 洪帮主做价投
欢迎个人转发分享,网站、公众号等转载请联系授权
2026-05-20
·今日头条
司妥吉仑(Sitokiren,商品名:信妥安)是由上海医药研发的新一代口服非肽类小分子肾素抑制剂,于2025年12月9日获NMPA批准上市,用于治疗原发性高血压。这是全球第二款获批上市的肾素抑制剂,也是首款由中国本土药企自主研发上市的同类药物。
一、作用机制:RAAS系统源头的"精准调控者"
肾素-血管紧张素-醛固酮系统(RAAS)是人体调控血压的核心通路。现有主流降压药——ACEI(普利类)和ARB(沙坦类)——分别阻断该通路的中游和下游环节。然而,这两类药物存在一个共同的机制性缺陷:由于切断了负反馈环路,会导致上游血浆肾素活性(PRA)代偿性升高,产生所谓的"肾素逃逸"现象。逃逸后的肾素可能通过非ACE途径继续生成血管紧张素II,使得降压效果大打折扣。
司妥吉仑在机制上的创新之处在于:直接作用于RAAS系统的"最上游"和"关键限速步骤"——肾素本身,通过选择性抑制肾素活性,阻止血管紧张素原转化为血管紧张素Ⅰ,从源头阻断后续血管紧张素II的生成及醛固酮分泌、血管收缩等升压效应。通俗地说,ACEI/ARB是在下游"拦截",而司妥吉仑是在源头"关小水龙头",能够显著降低PRA,实现源头阻断RAAS激活,避免了传统药物的"逃逸现象"。
具体而言,司妥吉仑的作用机制可概括为:第一,源头阻断,在RAAS级联反应的起始步骤即进行阻断,理论上比中下游阻断更为彻底。第二,克服"肾素逃逸",ACEI/ARB阻断下游后,肾素活性会代偿性增高,甚至可达基线水平的数倍,司妥吉仑直接抑制肾素,使PRA显著下降,消除了这一隐患。第三,非肽类小分子结构,相比于第一代肾素抑制剂,司妥吉仑经过多轮结构优化,在口服生物利用度和药代动力学上展现出了更优异的表现。
此外,临床前研究还发现,司妥吉仑在抑制肠道炎症方面也有一定潜力。在实验性结肠炎小鼠模型中,司妥吉仑能够有效阻断结肠炎的发展,其机制至少部分是通过抑制黏膜TH1和TH17活化,同时促进IL-10产生,在结肠黏膜中形成抗炎环境。该药针对溃疡性结肠炎和糖尿病肾病的II期临床试验也正在进行中。
二、同靶点药物全景对比:全球仅两款获批
肾素抑制剂是RAAS靶向药物中获批品种最少的类别。目前全球仅有两款上市药物,司妥吉仑属于第二代。
第一代药物是诺华研发的阿利吉仑(商品名:锐思力),2007年在美国获批,2010年进入中国。阿利吉仑是全球首个获批的口服肾素抑制剂,上市后在国际市场取得了一定的商业成功,2010年全球销售额一度达到约20亿美元。然而,该药在中国市场遭遇了根本性困境——中国人的血浆肾素水平普遍偏低,而肾素抑制剂主要对高肾素活性患者有效,这使得阿利吉仑在中国的处方逻辑受到挑战:临床需要先检测血浆肾素水平才能判断是否适用,而该检测在基层医院的普及率很低。
司妥吉仑作为第二代药物,在分子特征上属于非肽类小分子,分子量为444.5,而阿利吉仑为非肽类小分子氨基甲酸衍生物。两药的半衰期均约为40小时。司妥吉仑的推荐剂量为100mg每日一次,阿利吉仑为150-300mg每日一次。在降压效果方面,司妥吉仑的III期研究显示其与缬沙坦非劣效,阿利吉仑的收缩压降幅约为12-16 mmHg。
在安全性方面,司妥吉仑临床研究显示不良反应发生率较低,未发生血管神经性水肿、咳嗽、皮疹、腹泻和肾功能损伤等同类药物已有报道的不良反应。阿利吉仑则存在腹泻、高钾血症、低血压等不良反应报告。
在中国人群适用性方面,司妥吉仑拥有充分的中国人群III期数据,共纳入828例患者。而阿利吉仑由于中国人群血浆肾素水平普遍偏低的生理特点,其响应受到明显限制。在商业化层面,阿利吉仑目前已转让给李氏大药厂,市场份额极小。司妥吉仑刚上市,目前非基药、非医保。
司妥吉仑针对阿利吉仑的不足进行了改进:它不仅是更高效、选择性更好的新一代非肽类小分子,还在临床设计上覆盖了更广泛的中国人群,III期研究数据充分验证了其在中国轻中度高血压患者中的疗效与安全性。
三、临床研发历程(2006-2025)
司妥吉仑的研发历程长达近20年。
2006年,上海医药参与一项国际合作项目,目标寻找非肽类、成药性更好的肾素抑制剂。经过约5年半多轮次结构优化,最终于2011年左右确定候选化合物SPH3127。2016年,首次进入临床研究阶段。2021年11月,II期临床试验(SPH3127-202研究)完成。约2023年6月,III期临床试验达到主要终点。2024年,II期临床结果发表于心血管领域权威期刊《Hypertension Research》。2025年12月9日,获NMPA批准上市。2026年2月10日,全国首张处方在上海浦东新区公利医院落地。2026年2月,在京东健康线上平台首发。
在关键临床数据方面,III期注册研究是一项全国多中心、随机、双盲、双模拟、阳性药物平行对照临床试验,由首都医科大学附属北京安贞医院马长生教授牵头,联合全国39家心血管领域顶尖临床中心共同开展。研究纳入828例原发性轻、中度高血压患者,随机分为缬沙坦组(415例,缬沙坦80mg每日一次)和司妥吉仑组(413例,司妥吉仑100mg每日一次),主要终点为治疗12周后平均坐位舒张压(msDBP)相对基线的变化。结果显示,司妥吉仑100mg每日一次治疗12周,在改善坐位舒张压方面与缬沙坦80mg相比达到非劣效研究终点。临床研究显示不良反应发生率较低,未发生血管神经性水肿、咳嗽、皮疹、腹泻和肾功能损伤等同类药已有报道的不良反应。
II期剂量探索研究是一项多中心、随机、双盲、安慰剂对照的剂量探索试验。司妥吉仑50mg、100mg、200mg和安慰剂组治疗8周,坐位舒张压分别下降5.7、8.6、3.8和3.1 mmHg,坐位收缩压分别下降11.8、13.8、11.1和7.7 mmHg。该研究确定了100mg每日一次为推荐临床剂量,并于2024年发表于《Hypertension Research》。
药效动力学研究显示,连续给药100mg以上,服药0.5小时后血浆肾素活性即可得到迅速且明显的抑制,90%以上肾素活性抑制持续24小时,连续7天用药在人体无明显蓄积。
四、销售额与市场现状
司妥吉仑于2025年12月刚获批上市,2026年2月首张处方才落地,上市销售时间极短,目前尚无公开的季度或年度销售数据。
从市场定位来看,司妥吉仑具有独特的差异化竞争优势。中国高血压患病人数已超过3亿,但控制率不足20%。然而,国内高血压药物市场受国家集采影响深远,氨氯地平、缬沙坦等常用药价格已低至几分钱至几毛钱。因此,司妥吉仑将主要面向难治性高血压、对现有药物不耐受、伴有微量蛋白尿或早期肾损害等未被满足的临床需求,走差异化创新路线。目前该药尚未纳入国家医保目录,也非基本药物。2026年2月,司妥吉仑已在京东健康线上平台首发。
五、靶点失败案例
阿利吉仑堪称该靶点最具戏剧性的失败案例。这款由诺华研发的first-in-class直接肾素抑制剂,经历了从"备受期待"到"致命挫败"的全过程。
阿利吉仑2007年获FDA批准上市后一度势头强劲,2010年全球销售额约达20亿美元。然而,转折发生在2011年底——大型III期ALTITUDE研究的数据与安全监察委员会发现,服用阿利吉仑的患者在治疗18-24个月后,出现非致命性卒中、肾脏并发症、高钾血症和低血压的风险增加,试验被提前终止。最终结果显示,阿利吉仑在复合终点事件上与安慰剂相比无获益,且呈现出令人担忧的风险趋势,尤其是在卒中方面。
ALTITUDE研究的失败对阿利吉仑造成了致命打击,它不仅在全球学术和商业地位一落千丈,更导致诺华在后续数年持续收缩对该品种的投入。2018年,诺华最终将阿利吉仑的中国大陆、港澳台独家代理权转让给了李氏大药厂。
此外,诺华还曾在2010年推进阿利吉仑用于心梗后心室重构的II期ASPIRE研究,结果同样未达到主要终点,未能减少心梗后患者的心室重构。虽还有其他企业在肾素抑制剂领域进行早期探索,如SC-56525等,但大多停留在早期阶段,未见临床突破性进展。可以说,阿利吉仑的失败教训几乎构成了整个肾素抑制剂领域的"前世记忆",而司妥吉仑的诞生,正是新一代科研人员在深刻吸取第一代DRI药物教训基础上实现的跨越。
六、国内肾素靶点其他药物研发情况
在司妥吉仑之外,国内围绕RAAS系统上游的研发并不限于肾素抑制剂这一个方向。当前国内呈现"三路并进"的格局。
第一路,新一代肾素抑制剂(DRI)。除司妥吉仑已获批外,上海医药作为该赛道的中国领导者,暂无其他本土企业的DRI进入临床中后期。
第二路,醛固酮合酶抑制剂(ASI)。这是比DRI更热门的RAAS上游靶点赛道。信立泰的SAL0140已于2025年12月获批开展针对原发性醛固酮增多症的临床试验,同时覆盖未控制高血压和CKD。该赛道其他企业的管线可参见此前关于巴昔多司他的讨论。
第三路,血管紧张素原(AGT)靶向siRNA。这是RAAS上游布局中技术路线差异化最大的方向,其作用靶点比肾素更靠上游,通过siRNA从基因层面沉默AGT mRNA,从源头阻断整个RAAS系统的激活。目前国内有三款AGT siRNA药物进入I期临床。悦康药业与杭州天龙合作的YKYY029,于2025年7月获NMPA及FDA临床试验批准,适应症为高血压。施能康与华东医药合作的SNK-2726,已获批临床并完成首例受试者给药,适应症为高血压。大睿生物的RN1871,于2025年4月获NMPA批准IND,适应症为高血压。上述AGT siRNA药物均处于I期临床阶段,距离上市仍有数年时间。作为对比,司妥吉仑在同靶点药物中具有明显的先发优势。
七、总结
司妥吉仑是中国创新药发展的一个重要里程碑。从2006年参与国际合作,到2025年获批上市,其近20年的研发历程经历了一个完整的新药创制周期。作为新一代非肽类小分子肾素抑制剂,它不仅在分子结构和药理特性上较第一代同类药物阿利吉仑有了显著改进,更在临床开发中建立了专门面向中国人群的充分证据。
随着2026年首张处方的落地,司妥吉仑的临床推广和市场教育才刚刚起步,其未被纳入国家医保的现状短期内可能对患者可及性构成一定挑战,但作为一款填补临床空白的差异化产品,其长期价值值得持续关注
100 项与 YKYY029 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 高血压 | 临床2期 | 中国 | - | 2026-03-01 |
| 原发性高血压 | 临床1期 | 中国 | - | 2025-07-23 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


