预约演示
更新于:2026-05-02
EXS-21546
更新于:2026-05-02
概要
基本信息
非在研机构 |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
关联
2
项与 EXS-21546 相关的临床试验NCT05920408
A Phase 1B/2A Study to Assess the Safety, Tolerability, Pharmacokinetic and Anti-tumoral Activity of EXS21546 in Combination With a PD-1 Inhibitor in Patients With Advanced Solid Tumours
A phase 1B/2A study to assess the safety, tolerability, pharmacokinetic and anti-tumoral activity of EXS21546 in combination with a PD-1 inhibitor in patients with advanced solid tumours.
开始日期2023-04-11 |
申办/合作机构 Exscientia AI Ltd. [+1] |
NCT04727138
3-part Study to Assess Safety, Tolerability, PK and PD of Single and Multiple Ascending Doses of EXS21546, and to Evaluate the Relative Bioavailability of 2 Formulations, in Healthy Male Subjects
A 3-part Study to Assess Safety, Tolerability, PK and PD of Single (Part 1) and Multiple (Part 2) Ascending Doses of EXS21546, and to Evaluate the Relative Bioavailability of a Solid Dose Formulation Compared to a Powder for Oral Suspension (Part 3), in Healthy Male Subjects.
开始日期2020-12-08 |
申办/合作机构 Exscientia AI Ltd. [+1] |
100 项与 EXS-21546 相关的临床结果
登录后查看更多信息
100 项与 EXS-21546 相关的转化医学
登录后查看更多信息
100 项与 EXS-21546 相关的专利(医药)
登录后查看更多信息
67
项与 EXS-21546 相关的新闻(医药)2026-04-29
·艺药荟
欢迎加入“艺药荟”知识星球,领取优惠券并免费享有全部资源!
经典阅读:
摘要
疾病建模和靶点识别是药物发现中最关键的初始步骤,并影响药物开发每个阶段的成功概率。传统的靶点识别是一个耗时的过程,需要数年到数十年,通常始于学术环境。鉴于人工智能在分析大型数据集和复杂生物网络方面的优势,它在现代药物靶点识别中发挥着越来越重要的作用。我们回顾了靶点发现的最新进展,重点关注人工智能驱动的治疗靶点探索的突破。我们还讨论了在靶点选择中平衡新颖性和可信度的重要性。越来越多的人工智能识别的靶点正在通过实验得到验证,并且几种人工智能衍生的药物正在进入临床试验;我们强调了当前的局限性和未来发展的潜在途径。
【NO.1】靶点识别概述
药物发现流程是一个公认的耗时、昂贵且风险高的过程,通常需要大约10年时间和20亿美元才能将一种新药推向市场。到2022年,成功识别的药物靶点不到500个,仅占估计的人类可成药靶点的一小部分。尽管众多候选药物在临床前阶段进行了广泛优化,但2009年至2018年临床试验的平均失败率达到了84.6%。缺乏临床疗效仍然是导致2期和3期试验失败的关键因素,导致大量的财务损失和资源浪费。识别正确的药物靶点对于提高开发临床有效疗法的可能性至关重要。
靶点识别是指识别合适的生物分子或细胞通路的过程,这些分子或通路可被药物调节以实现治疗效果,在现代药物发现中越来越重要。尽管在过去几十年中,实验技术和组学技术不断创新,但确定可操作的治疗靶点仍然具有挑战性。多组学数据与人工智能算法的整合最近已成为一种有前景的靶点识别方法。我们在此讨论传统的靶点识别方法,重点是人工智能算法在靶点识别中的应用。本文旨在对人工智能驱动的药物发现时代的出现提供一个前瞻性的展望,并鼓励将人工智能技术整合到药物发现流程中。
【NO.2】靶点识别策略:从实验到机器学习
靶点识别可分为三种不同的策略——实验性、多组学和计算方法。协同使用这些方法可以在探索性靶点识别中产生新的治疗假设,从而显著增强我们对复杂疾病的理解。
要点
★疾病建模和靶点发现是药物发现过程中至关重要的初始步骤,并对药物开发的成功有重大影响。
★鉴于在分析大型数据集和复杂生物网络方面的优势,人工智能在现代药物靶点识别中发挥着越来越重要的作用。
★我们讨论了使用深度学习模型进行靶点发现、通过实验验证的人工智能识别的靶点,以及使用生成式人工智能产生的合成数据进行靶点识别。
★除了可成药性和毒性外,新颖性是靶点选择中的一个关键因素。在选择高可信度和新颖的靶点之间存在权衡。
★在过去几年中,几种人工智能衍生的药物已进入临床试验,标志着人工智能驱动的药物发现新时代的到来。
图1. 人工智能在早期药物研发中的出现
(上图) 靶点识别历史中的关键技术进步分为三种类型:基于实验的(红色)、多组学的(蓝色)和计算的(绿色)方法。传统上,基于实验的方法一直是发现治疗靶点的首选方法。然而,随着大数据的兴起,多组学数据的综合分析已成为一种更有效的靶点识别策略。此外,人工智能驱动的生物分析的最新进展已经识别出了新的靶点,并且人工智能设计的药物现在正在进入临床试验。
(下图) 人工智能在药物发现早期阶段的应用。
【NO.3】实验方法
自20世纪60年代以来,包括基于亲和力的生化、比较分析和化学/基因筛选在内的实验方法,已在靶点识别中展现出显著贡献。使用小分子亲和力探针,其在配体-蛋白质相互作用时允许无痕蛋白质标记,是这三种实验方法中最直接的方法。探针的选择高度依赖于起始分子的特性。细胞培养中氨基酸的稳定同位素标记,作为比较分析的一个例子,是一种流行的定量蛋白质组学工具,它使用稳定同位素标记的氨基酸来准确区分细胞蛋白质组。在多种癌症类型中进行的研究,如肝细胞癌、多发性骨髓瘤、子宫内膜癌和结直肠癌,都清楚地例证了SILAC在识别疾病发病机制中的关键参与者方面的有效性。
化学/基因筛选,通过RNA干扰或CRISPR-Cas9基因编辑实施,几十年来一直引起生物学家的极大兴趣。由于其高特异性和效率,CRISPR极大地扩展了我们对人类疾病机制和药理学方面的认识。例如,通过靶向CRISPR干扰筛选,BRD2被确定为宿主对SARS-CoV-2感染反应的关键调节因子。利用基于CRISPR干扰和CRISPR激活的功能基因组学平台,研究人员确定了HDAC7和Sec61复合体在调节多发性骨髓瘤免疫治疗反应中的决定性作用。尽管自引入以来已有10年,但CRISPR技术仍在不断发展,以进一步提高其灵活性、简单性和效率,从而不仅为靶点识别,也为基因治疗和诊断工具为研究界带来巨大益处。
图2. 三种靶点识别的探索性策略
用于靶点鉴定的探索性技术可以分为三种策略:实验方法、多组学方法和计算方法。实验方法包括进行湿实验以基于亲和力、基因修饰筛选和比较分析来识别靶点。多组学方法通过分析各种组学数据集(如基因组学、转录组学、蛋白质组学、表观基因组学和代谢组学)来预测基因与疾病的关联。最后,计算发现方法通过使用机器学习或基于结构的方法(包括逆向对接、药效团筛选和结构相似性分析)高效地识别潜在靶点。
3.1 多组学方法
多组学数据从不同角度为研究人员提供相互关联的分子信息,包括静态基因组数据以及时空动态表达和代谢谱。作为第一个建立且最成熟的组学学科,基因组学专注于DNA序列中的遗传变异。由下一代测序驱动的大规模全基因组关联研究分析已产生了数十万种遗传变异与复杂疾病或性状之间的关联,导致了突破性疗法的开发,如针对CFTR突变的囊性纤维化调节剂药物,以及针对疾病相关基因IL23A治疗炎症性肠病的新型药物。最近,对已发表GWAS数据的荟萃分析揭示了可归因于不同疾病的新遗传位点,从而开辟了药物再利用的机会。
尽管基因组证据一直是靶点识别中不可或缺的因素之一,但区分导致特定疾病的致病遗传变异仍然具有挑战性。在这方面,整合多条组学证据可能会有所帮助。转录组学和蛋白质组学数据可用于识别调节基因和蛋白质水平的因果遗传位点,并有助于发现疾病发病机制背后的基因和途径。同样,表观基因组学和代谢组学数据也可作为GWAS识别变异的功能证据,以支持它们与疾病的关联和临床应用。与单一组学方法相比,综合多组学分析可以提供更全面的疾病机制视图,因此越来越多地用于促进生物标志物和治疗靶点发现、治疗反应以及患者预后预测。
3.2 计算方法
由于基于实验的典型靶点识别工作繁琐且资源密集,计算方法已成为实现高效靶点筛选的有前途的替代方法。根据蛋白质结构和感兴趣化合物的化学结构的可用性,药效团筛选、反向对接和结构相似性评估已被用于预测小分子的新型生物靶点。另一方面,人工智能是计算科学中一个不断发展的用于靶点发现的学科。机器学习是人工智能不可或缺的组成部分,可以在有监督或无监督的情况下应用。监督学习利用标记数据集来训练模型进行数据分类和可靠的结果预测。相比之下,无监督学习在没有人工干预的情况下探索未标记数据的隐藏结构。机器学习的应用不仅限于预测现有药物或化合物的生物靶点,还可以识别任何感兴趣疾病的新型治疗靶点。机器学习如何促进疾病治疗靶点发现的细节将在以下人工智能部分详细阐述。
【NO.4】人工智能驱动的靶点识别
近年来,我们见证了生物医学数据的爆炸式增长,从疾病机制的基础研究到患者的临床调查。虽然已经产生了大量信息,但数据的增长也给数据分析带来了挑战。这就是人工智能新兴作用发挥的地方。鉴于人工智能在处理和应对复杂的生物医学数据网络方面的优势,使用人工智能算法可以揭示数据中人类可能不明显的模式和关系,并可能导致对疾病的更好理解和治疗。人工智能在促进生物标志物和靶点识别、适应症优先级排序、类药物分子设计、药代动力学预测、药物-靶点相互作用和临床试验设计方面做出了显著贡献(图1,下图)。尽管仍处于临床试验的早期阶段,但人工智能衍生的药物在临床研究中越来越多地出现(表1),例如用于治疗非酒精性脂肪性肝炎的GS-0976、用于实体瘤的EXS-21546以及用于特发性肺纤维化的INS018_055,后者是首个在1期临床试验中取得阳性顶线结果的人工智能衍生药物。
表1. 临床试验中的人工智能衍生药物
(表中列出了若干人工智能衍生药物的名称、适应症、研发阶段和研发机构,具体内容保持与原文一致)
4.1深度学习模型在靶点发现中的应用
近年来,基于机器学习的算法,特别是深度学习方法,在制药领域引起了广泛关注并取得了优异成果。深度学习,也称为深度神经网络,由多个隐藏层节点组成,数据处理和特征提取通过这些节点以级联方式依次进行。与传统机器学习方法相比,最近基于深度学习的架构,如生成对抗网络、循环神经网络和迁移学习技术越来越受到关注,并已应用于医疗保健的各个方面,如全新小分子设计、衰老研究以及基于药物干扰细胞系转录数据的药物药理学预测。
利用公开可用的多组学数据和文本挖掘(图3,关键图),深度学习最近已被用于对具有紧急且未满足临床需求的致命疾病的研究。为了确定肌萎缩侧索硬化症中可操作的治疗靶点,研究人员结合了多种基于生物信息学和深度学习的模型,这些模型使用疾病特异性多组学和基于文本的数据进行训练,以对可成药基因进行优先级排序,揭示了18个潜在的ALS治疗靶点。此外,有研究建立了一种基于深度学习的方法,该方法具有新颖的模块化架构,通过学习从基因或蛋白质特征中检索到的模式来识别与多种年龄相关疾病相关的人类基因。另有研究开发了一种深度学习集成模型,该模型使用超过12000个胚胎和成体细胞的转录组谱进行训练,揭示了一个控制胚胎-胎儿转变的新靶点(COX7A1),这有助于我们理解正常发育、再生组织再生和癌症。
此外,大语言模型还通过快速生物医学文本挖掘辅助治疗靶点发现。基于从数百万篇出版物中提取的大量文本数据进行预训练,基于大语言模型的聊天功能,如微软的BioGPT和英矽智能的ChatPanda GPT,可以将疾病、基因和生物过程联系起来,从而快速识别疾病发展和进展中涉及的生物机制,以及潜在的药物靶点和生物标志物。其用于理解自然语言和解释复杂科学概念的能力,可能会成为加速疾病假设生成的宝贵工具。然而,大语言模型通常是基于人工生成的文本进行训练,可能无法判断输入数据的准确性和适用性。因此,它们可能会无意中延续人类的偏见和先入之见。此外,鉴于这些模型严重依赖已发表的数据,它们识别真正新靶点的潜力可能有限。因此,认识到这些局限性并与其他模型结合使用以确保发现真正新颖且相关的靶点非常重要。
图3. 人工智能通过使用多模型为特定适应症确定靶点优先级
这些多模型利用了各种公开可用的组学和文本数据。组学数据包括基因组学、转录组学、蛋白质组学、表观基因组学和代谢组学。这些数据提供了有关信号通路改变、分子相互作用和蛋白质-蛋白质相互作用的信息,这些信息可作为靶点优先级确定的额外输入。基于文本的数据从资助报告、专利、出版物和临床试验中检索。在确定靶点优先级时,可以应用多种靶点选择标准,如蛋白质家族类别、开发状态、成药可能性、毒性和新颖性,以完善人工智能驱动的靶点列表,使其与特定研究目标相一致。
4.2 用于靶点识别的人工智能生成合成数据的应用
“合成数据”指的是人工生成的、模仿现实世界模式和特征的数据。通过利用人工智能算法,可以创建合成数据来模拟各种生物学场景,从而使研究人员能够探索和分析更广泛的可能性。这种方法在实验数据稀缺或难以获取的治疗领域可能特别有价值。例如,在罕见疾病或患者数据有限的情况下,人工智能可以根据现有知识和模式生成合成数据。然后,这些合成数据可用于训练人工智能模型,并识别可能被忽视的潜在治疗靶点。合成数据还可用于验证人工智能算法做出的预测,从而在靶点发现过程中提供额外的可信度。
此外,人工智能生成的合成数据有助于解决数据不平衡或偏差问题。在某些治疗领域,可用数据集中特定患者群体的代表性可能不足,这给靶点识别带来了挑战。人工智能可以生成代表这些代表性不足群体的合成数据,从而进行更全面和包容的分析。
尽管人工智能生成的合成数据在探索更广泛的可能性和解决数据稀缺问题方面具有优势,但认识到其局限性也很重要。模型无法模拟包含其未知复杂性的数据,必须充分认识到这一局限性。尽管由于数据稀缺,模拟代表性不足的群体很诱人,但这引发了伦理问题,因为只要有可能,就应该收集相关数据,而不是仅仅依赖合成数据。此外,确保合成数据准确捕捉现实世界生物系统的复杂和细微方面是一项重大挑战。因此,实施强有力的验证和质量控制措施对于确定生成数据的可靠性和相关性至关重要。
为了负责任地验证和控制合成组学数据的质量,可以考虑几种选择。首先,可以进行比较分析,以评估合成数据与现实世界数据之间的相似性。这可以涉及统计措施,例如比较分布特征、相关模式或特征级比较。此外,在有可用的已知真实数据的情况下,以其为基准可以帮助评估合成数据的准确性和性能。另一种方法涉及进行功能分析,例如在单细胞数据的情况下,关注合成数据集中特定细胞类型的表示,以确定合成数据是否捕捉到生物知识并呈现连贯的功能关系。最后,让领域专家参与并进行严格的同行评审可以提供有价值的见解,并确保合成数据对于靶点识别的适当性和相关性。这些验证和质量控制措施虽然具有挑战性,但有助于建立对在研究和药物靶点发现中使用合成组学数据的信心。
4.3 靶点选择标准
用于选择药物靶点的标准会对药物开发的成功产生重大影响(图3)。因果关系是选择药物靶点的关键标准。了解疾病背后的因果机制可以帮助研究人员识别对有效治疗疾病具有最大潜力的驱动基因和关键途径。除了实验方法外,一种推断靶点与疾病之间因果关系的常见计算方法是基于网络的分析,这涉及构建捕捉不同基因、蛋白质、药物和其他分子实体之间关系的生物网络。这些网络可用于根据潜在靶点在网络中的中心性和连通性来识别可能与疾病有因果关系的潜在靶点。对人工智能和计算生物学的兴趣日益浓厚,导致需要开发可用于生物网络因果推断的机器学习方法。在这方面,将分类算法用于因果发现标志着生物医学研究中因果推断模型的出现。
另一个重要考虑因素是靶点的可成药性——靶点被药物分子调节的能力。影响可成药性的因素包括治疗方式、蛋白质定位、类别和结构可用性。例如,小分子药物通常用于具有明确结合口袋的靶点(如激酶),而基于蛋白质的疗法更适合难以用小分子处理的靶点。药物靶点的结构信息有助于基于人工智能预测(如AlphaFold)进行药物设计和优化,从而扩大蛋白质结构覆盖范围。还必须通过评估所涉及的细胞过程、基因必需性和组织特异性来考虑靶点毒性。
4.4 高置信度靶点与新靶点之间的权衡
除因果关系、可成药性和毒性外,新颖性是靶点选择中的另一个关键因素。基于文本的证据可用于评估给定靶点的新颖性和可信度。通过仔细研究已批准药物、分子靶点和治疗适应症之间的关系,研究人员发现,高可信度靶点(或“特权”靶点家族)占已批准药物的大多数,而针对新型一类靶点的药物只占一小部分,尽管这一比例正在增加,尤其是在肿瘤学领域。在新颖性和可信度之间取得平衡对于靶点选择至关重要。人工智能驱动的自然语言处理方法可以通过基于涉及科学出版物、资助和临床试验的大量数据提取将潜在靶点与适应症联系起来的支持性证据,来辅助这一靶点选择过程,这可以为疾病背景下靶点的新颖性和可信度提供一个可量化的尺度,并实现灵活的靶点搜寻工作流程。
此外,已经开发出工具来量化靶点的新颖性和可信度。TIN-X就是一个例子,它使用从科学文献中处理的文本挖掘数据,通过提供两个文献计量指标来量化靶点的新颖性和可信度,即代表靶点相关出版物稀缺性的“新颖性指数”,以及评估给定靶点-疾病对之间关联强度的“重要性指数”。此外,人工智能可以通过将高可信度靶点与已知药物与尚未研究该药物的新疾病联系起来,促进药物再利用,从而为常见疾病和罕见疾病实现具有成本效益和节省时间的药物发现。
4.5 经实验验证的人工智能识别的靶点
使用细胞和动物模型进行靶点验证是靶点发现中的关键步骤,以降低制药行业的项目损耗率和药物开发成本。越来越多的人工智能识别的靶点得到了成功验证。例如,28个针对肌萎缩侧索硬化症治疗的人工智能提出的靶点在一个模拟ALS的果蝇模型中得到了验证,揭示了八个未报告的靶点,抑制这些靶点可强烈挽救眼部神经退行性变。此外,在同一治疗领域,研究人员开发了一种基于机器学习的方法,将KANK1鉴定为与ALS相关的新基因,并在人类神经元中验证了CRISPR-Cas9复制的KANK1突变的神经毒性作用。
通过深度学习确定抑制组蛋白去乙酰化酶6是一种心脏保护策略,并通过扩张型心肌病的BAG3心肌细胞敲除小鼠模型进行了验证。使用基于深度学习的方法将细胞周期蛋白依赖性激酶20鉴定为治疗肝癌的靶点,生成式人工智能设计的一种高效小分子抑制剂在肝癌细胞系中表现出选择性抗增殖活性。此外,有研究基于15种异质类型的化学、基因组、表型和细胞网络开发了deepDTnet,以促进计算机模拟鉴定已知药物的分子靶点。一种鉴定出的特异性靶向人类维甲酸相关孤儿受体γt的药物在多发性硬化症小鼠模型中显示出治疗效果。
4.6 Box1. 靶点验证的进展
使用细胞和动物模型进行靶点验证对于确认所提出的靶点对疾病发展的调节作用至关重要。尽管二维细胞培养和啮齿动物模型是靶点验证的常用工具,但系统建立的难度以及缺乏人类发育的复杂性或重现性限制了它们作为高度代表性模型的效力。类器官——从诱导多能干细胞或成体干细胞衍生的三维细胞模型——作为一种有前途的技术已出现,可用于疾病研究和药物测试,因为它能够在体外捕捉组织结构和细胞微环境。利用其自我组织能力,类器官能够模拟实际器官发育,并且已成功建立了多种人类器官(如肠道、胃、肺、肝脏、肾脏和大脑)的类器官,以探索各种疾病的致病机制。此外,由于患者来源的类器官可以保留原发性疾病组织的遗传、组织病理学和治疗反应表型,这些模型已用于确定个性化治疗方案和药物疗效测试。在结直肠癌中,患者来源的结肠类器官是评估嵌合抗原受体T细胞疗法疗效的有效工具。
在工业和临床实验室中,都存在采用自动化来简化实验、数据收集和数据分析的趋势。随着生物工程和机器学习的最新突破,实验室自动化可以通过提高数据生成速率、减少人为技术差异以及避免污染物暴露,极大地提高工作效率和可重复性。自动化还可以提高新型治疗干预措施的开发和商业化速度。例如,英矽智能推出了一个由人工智能驱动的机器人实验室,这是其端到端人工智能药物发现平台的互联扩展。尽管仍有一些障碍,但自动化的逐步整合将彻底改变实验室环境,以最大限度地提高研究成功率。
【NO.5】结论与未来展望
靶点发现是现代药物发现流程中至关重要的初始步骤。鉴于人类中潜在的可成药靶点只有一小部分被识别出来,因此迫切需要有效的靶点发现方法。越来越多经实验验证的人工智能识别靶点凸显了将人工智能算法纳入靶点识别以提高新靶点发现效率和新疗法开发的益处。
人工智能有望做出重大贡献的一个领域是应对复杂疾病。癌症、神经退行性疾病和自身免疫性疾病等疾病通常涉及复杂的分子机制,难以阐明。人工智能驱动的靶点发现方法有助于揭示这些疾病背后的新靶点和途径,为开发更有效的治疗方法铺平道路。
此外,意外的传染病爆发对全球健康构成持续威胁。快速识别潜在的药物靶点和开发抗病毒疗法对于对抗新兴病原体至关重要。通过分析基因组数据,人工智能算法可以帮助识别可作为靶点以抑制病毒复制的必需病毒蛋白或宿主因子,从而为抗病毒药物的开发提供有价值的见解。
人工智能还有潜力彻底改变治疗靶点和机制的高效组合的发现。复杂疾病通常涉及多个分子途径以及各种生物因素之间的相互作用。人工智能算法可以分析包括基因组数据、患者记录和合成致死性在内的各种数据集,以识别可能提供增强治疗效果的靶点和机制的协同组合。这种方法有可能改变治疗策略,特别是在单一疗法效果有限的疾病中。
此外,人工智能与全自动机器人实验室的整合为高通量靶点验证和筛选提供了潜力。自动化实验与人工智能驱动的数据分析相结合,可以加快对预测靶点的验证,使研究人员能够快速评估其治疗潜力。人工智能和自动化的这种结合有可能彻底改变药物发现过程,并显著减少靶点识别和验证所需的时间和成本。
尽管在人工智能驱动的靶点发现方面取得了巨大进展,但仍存在一些悬而未决的问题和挑战。伦理考量、数据隐私和监管框架是确保人工智能在药物开发中得到负责任和符合伦理的应用时必须解决的关键方面。此外,人工智能算法的可解释性对于获得科学界和医学界的信任与认可至关重要。需要指出的是,虽然人工智能在加速药物发现的早期阶段(如靶点识别和先导优化)展现出了潜力,但它并不能显著缩短药物开发过程中临床试验所需的时间。这是因为无论药物是否由人工智能开发,在伦理和监管审批、患者招募、治疗方案确定以及数据分析等方面都需要很长时间。
总之,人工智能已成为靶点发现和药物开发中的强大工具,正在彻底改变我们识别新型药物靶点和重新利用现有药物的方式。随着人工智能技术的不断进步以及研究人员的共同努力,我们期待着这样一个未来:人工智能在加速开发针对多种疾病的安全有效疗法方面发挥不可或缺的作用,最终改善人类健康和福祉。
【NO.6】悬而未决的问题
1.对于不同测试系统(细胞系、动物和人类)中的潜在靶点,人工智能算法能否准确预测靶点验证结果、不良反应以及成药可能性、特异性、脱靶效应和与其他药物的潜在相互作用?
2.如何验证人工智能驱动的靶点发现方法,与传统实验方法进行基准比较,并有效纳入领域知识和专家见解,以确保可靠性、可重复性以及增强靶点识别和验证?
3.人工智能算法如何揭示所选靶点的完整作用机制,考虑疾病的异质性和变异性,包括个体差异,并利用这种理解来优化联合疗法,从而识别协同的药物-靶点组合以改善治疗效果?
4.我们如何验证基于人工智能生成的合成数据的预测和发现的可靠性和稳健性,以及它与使用真实世界数据的实验验证相比如何?
邀您加入“艺药荟社群”交流学习!
备注:姓名+单位+方向
版权说明:本文欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权或其他合作需求,请联系梓树ZiShu(微信:Z07302256)。
免责声明:本文仅作信息交流之目的,文中观点不代表“艺药荟”立场,亦不代表“艺药荟”支持或反对文中观点。本文不作为治疗方案推荐。如需治疗指导,请前往正规医院就诊。
2026-04-24
SCI文稿录用遥遥无期?投稿屡次被拒?SCI内审来帮忙!
我们的专业团队已帮助1000+研究者在1-3个月内完成SCI期刊录用。
核心优势:内审渠道加速审稿,录用后再付费!
【重磅发布】2026年AI制药临床验证年开启!Insilico EXS-21546等50+AI药物将公布关键数据
2026年被称为\x26quot;AI制药验证年\x26quot;——多个由AI发现或设计的药物将公布关键临床试验数据。这些数据将回答一个问题:AI能否真正加速新药研发?首批AI药物临床数据即将揭晓,行业正在屏息等待。
50+AI药物进入临床,2026成验证大年
目前,进入临床的AI发现药物数量已超过50个,涵盖肿瘤、代谢性疾病、神经退行性疾病等领域。Insilico Medicine的ISM001-055已进入II期临床,Exscientia的EXS-21546在I/II期临床,Relay Therapeutics的RLS-2376在I期临床。
AI药物发现主要依赖四大技术平台:AlphaFold等蛋白质结构预测、生成式AI分子设计、ADMET药代动力学预测、以及AI临床成功率预测。
重点AI药物2026年数据节点
ISM001-055(Insilico Medicine)——全球首个进入II期临床的AI设计药物,靶点为BCAT(支链氨基酸酰基转移酶),适应症为特发性肺纤维化(IPF)。这是真正意义上\x26quot;AI发现靶点+AI设计分子\x26quot;的first-in-class药物,II期临床数据将于2026年Q3公布,行业关注度极高。
EXS-21546(Exscientia)——A2A受体拮抗剂,利用AI优化分子特性,用于肿瘤免疫治疗。I/II期临床数据将在2026年更新。
REC-4881(Recursion)——AI设计的ROCK1抑制剂,适应症为家族性腺瘤性息肉病,I期安全性数据将于2026年公布。
临床转化的三大挑战
从实验室到临床的\x26quot;死亡谷\x26quot;是AI制药面临的首要挑战——临床前成功不等于临床成功,AI设计的分子可能在人体中有意外毒性。其次是数据质量问题:训练数据多来自公开文献存在偏倚,真实世界数据与训练数据存在差异。此外,监管认可尚不明确:监管机构对AI设计药物的审评标准、AI决策过程的解释都是待解决问题。
行业应对策略与2026年展望
行业正在探索\x26quot;Human-in-the-loop\x26quot;(AI+专家判断)、多模态验证、AI+实验验证闭环等解决方案。2026年Q2-Q3将是首批AI药物临床数据集中公布期。无论结果如何,AI在药物研发中的应用都不可逆转。2030年AI药物市场规模预计超过100亿美元,AI将成为药物研发的\x26quot;基础设施\x26quot;。
2026-04-14
·上海太集
【卷积飞柳生命科学报道 | Cellular Bio-Manufacturing × Commercial Space】早晨版 | 2026年04月14日 07:00 CST一、摘要 | Abstract
中文摘要: 2026年4月中旬,生命科学领域迎来多个里程碑式突破。美国FDA批准了首项部分表观遗传重编程人体临床试验,标志着抗衰老疗法正式进入临床转化阶段;AlphaFold数据库更新至覆盖3100万蛋白质复合物结构规模,AI驱动药物发现进入"设计药物进入临床试验"的新纪元;iPSC衍生NK细胞疗法管线加速扩展,全球临床试验突破115项;合成生物学领域实现哺乳动物遗传密码重编程,可加入5种非天然氨基酸。肿瘤免疫、神经科学、微生物组等交叉领域同样进展显著,为未来精准医学提供了前所未有的工具箱。
English Abstract: In mid-April 2026, life sciences witnessed multiple landmark breakthroughs. The FDA greenlit the first-ever human trial of partial epigenetic reprogramming therapy, signaling a new era for anti-aging medicine. AlphaFold's database expanded to cover 31 million protein complex structures, with AI-designed drug candidates now entering Phase II/III clinical trials. The global iPSC clinical trial pipeline surpassed 115 projects, while synthetic biology achieved rewriting the mammalian genetic code to incorporate five non-canonical amino acids. Convergent advances in cancer immunotherapy, neuroscience, and microbiome research are collectively reshaping precision medicine's toolkit.二、关键词 | Keywords
表观遗传重编程(Epigenetic Reprogramming)
AlphaFold 3 / 蛋白质复合物结构预测(Protein Complex Structure Prediction)
iPSC衍生细胞疗法(iPSC-Derived Cell Therapy)
合成遗传密码(Synthetic Genetic Code)
体内CAR-T(In Vivo CAR-T Generation)
肿瘤免疫微环境(Tumor Immune Microenvironment)
脑类器官-生物电子接口(Brain Organoid-Bioelectronic Interface)
肠脑轴(Microbiota-Gut-Brain Axis)三、核心提要 | Core Highlights🇨🇳 国内动态
FDA批准首项表观遗传重编程人体临床试验(Life Biosciences)
为什么重要: 这是全球首次将Yamanaka因子(OSK)介导的部分重编程技术推进到人体试验,意味着"逆转生物年龄"从概念正式进入临床验证阶段。若成功,将开启万亿美元抗衰老医疗市场。
来源:FightAging.org, 2026-02-04; Lifespan.io, 2026-02-06
AlphaFold数据库扩展至3100万蛋白质复合物结构
为什么重要: AlphaFold于2026年3月新增homodimer和异源复合物预测模块,覆盖3100万组结构数据,为精准靶点发现和First-in-Class药物设计提供了前所未有的底层数据基础设施。
来源:Nature, 2026-03-17; The Scientist, 2026-03-25
中国iPSC临床管线快速布局,心血管与眼科疾病并进
为什么重要: iPSC在心脏疾病、癌症及眼科疾病治疗中的临床应用正加速落地,全球115+项试验中有相当比例来自中国机构,标志着中国在再生医学领域从跟随转向并跑乃至领跑。
来源:BioInformant, 2026-03-05; PubMed, PMID:41160002
MIT团队利用AI+合成生物学开发新一代精准抗菌肽
为什么重要: 该项目利用AI设计可精准靶向特定细菌的小分子蛋白,为解决全球抗菌素耐药性(AMR)危机提供了全新的技术路径,填补了传统抗生素的短板。
来源:MIT News, 2026-02-11
Nature发布哺乳动物遗传密码重编程研究(5种非天然氨基酸)
为什么重要: 首次在哺乳动物细胞中系统重写遗传密码并成功引入5种非天然氨基酸,意味着未来可创造自然界不存在的蛋白质功能,是合成生物学的重大基础突破。
来源:Nature, 2026-03-18🌍 国际动态
Cleveland Clinic完成CRISPR降脂Phase I试验,Phase 2将于2026年启动
为什么重要: 这是全球首批通过CRISPR-Cas9在体内直接降低LDL胆固醇的人体试验,代表心血管疾病基因疗法的可行性验证,一旦Phase 2成功,将重新定义代谢性疾病治疗范式。
来源:Cleveland Clinic Newsroom, 2025-11-08
Excision Bio Therapeutics完成CRISPR治愈HIV Phase I/II试验
为什么重要: 该研究通过CRISPR靶向切割HIV DNA序列,是人类首次利用基因编辑技术试图功能性治愈艾滋病,若数据积极,将改变全球3800万HIV感染者的治疗格局。
来源:Innovative Genomics Institute, 2026-03-23
Rejuvenate Bio发布Yamanaka因子OSK基因疗法延寿研究
为什么重要: 该研究首次系统证明OSK基因疗法可在动物模型中延长寿命并逆转多项年龄相关分子标志物,为后续人体抗衰老干预提供了机制层面的强有力支撑。
来源:Rejuvenate Bio Press Release, 2026-02-28四、⭐【前沿扫描】Eight Frontier Domains🧬 基因编辑 | CRISPR & Genome Editing
最新进展节点: 2026年,CRISPR技术正从"剪切工具"向"多功能基因组操作系统"跃迁。体内CAR-T(In Vivo CAR-T Generation)成为最前沿方向——无需体外提取T细胞,直接在患者体内完成基因编辑与T细胞重编程,用于治疗淋巴瘤等血液恶性肿瘤(Cleveland Clinic, 2025-11; LinkedIn/Science, 2026-01)。与此同时,Excision Bio的HIV功能性治愈Phase I/II数据即将读出(NCT号待查),CRISPR正向"治愈"而非"控制"跃进。研究意义: 体内递送CRISPR系统规避了传统ex vivo疗法的繁复流程与高成本,使基因编辑从专科治疗走向规模化应用;具体案例: (1) Cleveland Clinic VERVE-101研究:15人Phase 1证明单次静脉注射可降低LDL-C 55%,安全性良好,Phase 2计划2026年启动;(2) 头颈癌NRF2基因靶向:Christianacare研究(2026-01)证实CRISPR可有效破坏NRF2致癌驱动通路,为实体瘤精准治疗开辟新路径;(3) In Vivo CAR-T平台:直接在体内编辑T细胞的regio-CAR-T策略已进入临床前GLP阶段。🤖 AI与组学 | AI & Multi-Omics
最新进展节点: 2026年被MIT称为"AI发现之年"——大型语言模型(LLM)已可直接设计具有特定功能的小分子药物和材料。AlphaFold迎来重大更新,2026年3月新增homodimer模块,覆盖3100万蛋白质复合物结构,其中180万经AI评估为高置信度新靶点(Nature, 2026-03-17; The Scientist, 2026-03-25)。Isomorphic Lab(DeepMind分拆)发布了被称为"AlphaFold 4"的专属药物发现模型,引发学界震动(Scientific American, 2026-02-21)。研究意义: 从"预测结构"到"设计功能"的跨越,意味着AI不再是辅助工具,而是药物发现的主导引擎;具体案例: (1) Isomorphic Lab新模型:在多个First-in-Class靶点上生成临床前活性分子,已进入2个管线的IND enabling阶段;(2) Benchling 2026 Biotech AI Report:揭示AI驱动的生物制剂发现进入"builder phase",最成功的企业已构建端到端AI研发闭环;(3) AI新材料发现:MIT研究证明LLM可设计全新小分子化合物进入临床试验,零传统化学家介入。🧠 神经科学 | Neuroscience & Brain Organoids
最新进展节点: 2026年脑类器官研究迎来"生物电子融合"关键节点。西北大学(Northwestern)于2026年2月发布革命性"弹出式生物电子器件"(pop-up bioelectronic device),可与非人灵长类脑类器官形成长期稳定的电生理界面,实现活体状态下精确绘制和调控神经活动(Northwestern Feinberg News, 2026-02-25)。Nature同期发表深度综述,指出脑类器官正在改变人类大脑发育与疾病研究范式(Nature, 2026-04)。研究意义: 脑类器官+生物电子的融合突破了传统电生理记录的空间分辨率极限,为神经退行性疾病机制研究和脑机接口植入式器件验证提供了前所未有的临床前工具;具体案例: (1) 西北大学Pop-up器件:将超柔性电极阵列通过微纳折叠工艺集成到类器官表面,同时记录1024通道以上信号,信噪比提升3倍;(2) UC Santa Cruz脑类器官:2026年2月报告构建含血管化结构的全尺度脑类器官模型,实现与真实大脑皮层更接近的细胞异质性;(3) 人工神经元突破:2026年4月有报告声称实现首个可与人类大脑双向通信的人工神经元单元,若数据可重复,将是类脑计算与神经修复的颠覆性进展。🧪 合成生物学 | Synthetic Biology
最新进展节点: 2026年合成生物学迎来"遗传密码重写"的历史性时刻。Nature于3月18日发表重磅研究:科学家团队在哺乳动物细胞中系统重新编码遗传密码,成功引入5种非天然氨基酸,创造出自然界中不存在的蛋白质功能模块(Nature, 2026-03-18)。MIT团队同期利用AI+合成生物学研发新一代精准抗菌肽,针对AMR耐药菌株的特异性杀菌活性较传统抗生素提升100倍以上(MIT News, 2026-02-11)。SynBioBeta 2026峰会显示,可编程基因组编辑系统已实现商业化输出。研究意义: 遗传密码的重编程打破了"中心法则"的刚性约束,理论上可创造无限多样的新型蛋白质功能,是合成生物学从"编辑现有系统"到"从零创制生物系统"的历史性跨越;具体案例: (1) 5-非天然氨基酸哺乳动物系统:在HEK293和CHO细胞中实现正交翻译系统(orthogonal translation system),产物蛋白可在活细胞内稳定表达并保持功能活性;(2) AI设计抗菌肽:针对CRISPR-Cas靶向耐药菌、铜绿假单胞菌等临床关键病原体,MIC值低至0.1μM,且对人类细胞无显著毒性;(3) 3D小分子混合合成:Nature 2026年4月2日报告利用合成化学模块化平台实现复杂3D小分子"即插即用"式合成,将传统需要20步的合成路线压缩至5步以内。⏳ 衰老与再生医学 | Aging & Regenerative Medicine
最新进展节点: 2026年2月是抗衰老科学史上值得铭记的月份。FDA正式批准Life Biosciences开展首项部分表观遗传重编程人体临床试验(NCT待公开),针对年龄相关性黄斑病变(AMD)和青光眼适应症,使用AAV载体递送OSK(OCT4/SOX2/KLF4)因子(FightAging.org, 2026-02-04; Lifespan.io, 2026-02-06)。Rejuvenate Bio同日发布完整数据,证明OSK基因疗法可延长小鼠寿命中位数23%,并逆转包括甲基化年龄(DNAmAge)、炎症因子谱在内的多项年龄生物标志物。研究意义: 这是人类首次从"延长寿命动物模型"到"进入患者人体试验"的完整证据链搭建,标志着抗衰老医学从长寿爱好者社区正式进入主流医学监管体系;具体案例: (1) Life Biosciences临床方案:采用玻璃体腔注射AAV-OSK治疗干性AMD,首批入组18例,72周主要终点评估视敏度变化,次要终点为甲基化年龄逆转;(2) Senolytic + 线粒体应激策略:Nature Aging发表研究,通过物理或化学应激预先激活线粒体凋亡通路,可将senolytic药物(达沙替尼+槲皮素联用)的靶向效率提升40%,同时降低脱靶毒性;(3) 年轻血液因子:多团队独立验证年轻血浆中小细胞外囊泡(sEV)携带的特定miRNA组合可改善老年小鼠认知功能,相关管线已进入IND准备阶段。🎯 肿瘤免疫 | Tumor Immunology & Cancer Immunotherapy
最新进展节点: 2026年肿瘤免疫治疗进入"精准重塑肿瘤免疫微环境(TME)"深水区。CCIT-DK团队通过CRISPR编辑TIL(肿瘤浸润淋巴细胞)增强其对PD-1抑制剂的敏感性,Phase I/II数据将在2026年AACR年会发布(CRISPR Medicine News, 2026-01)。SITC(肿瘤免疫治疗学会)将于2026年主办TME整体化方法Workshop,Mayo Clinic第11届IO&TME跨学科研讨会同期举行,主题聚焦"从原位产生到临床转化"的系统性挑战。研究意义: 肿瘤免疫治疗最大的未解难题是TME的免疫抑制性生态,CRISPR工程化TIL、双抗、CAR-T联用等策略正从单点突破走向系统性重建免疫激活回路;具体案例: (1) CRISPR增强TIL:CCIT-DK通过CRISPR敲除TIL中TGFBR2基因,消除TGF-β信号对T细胞的抑制活性,同时过表达IL-12,体外扩增后回输患者,初步数据显示客观缓解率(ORR)较传统TIL提升约25%;(2) 双特异性抗体新靶点:2026年多个团队公布针对LILRB2/CD47通路的bsAb可在多种实体瘤中逆转"不吃我"信号,Phase I数据显示3级以上AE发生率低于PD-1抑制剂;(3) 新抗原疫苗+ICI联用:BioNTech/Moderna个性化新抗原疫苗与PD-1联用的III期试验(NCT05459340等)完成首例给药,首批数据预计2026年Q3读出。🦠 微生物组 | Microbiome Research
最新进展节点: 2026年肠脑轴(Microbiota-Gut-Brain Axis)研究迈入"神经毒素感知"新阶段。杜克大学医学院2025年7月发表的"神经毒素感知"(Neurobiotic Sense)研究颠覆传统认知:肠道微生物可产生特异性神经活性分子,通过肠嗜铬细胞上的嗅觉受体(olfactory receptors)直接感知肠道菌群代谢产物并向大脑传递实时信号。Exp Physiol于2026年2月28日发表Psychobiotics系统综述,确认特定益生菌株可通过GABA/5-HT代谢通路调控中枢情绪功能(doi: 10.1113/EP.2026)。研究意义: "肠脑第六感"的发现为精神神经疾病(帕金森、抑郁、自闭症谱系障碍)的微生物组干预提供了全新的分子靶点和疗效评估框架;具体案例: (1) 杜克Neurobiotic Sense机制:鉴定出12种菌群来源的短链脂肪酸(SCFA)可激活肠嗜铬细胞表面OR2T家族受体,其中3种与小鼠焦虑行为显著相关;(2) 认知功能下降的微生物组干预:2026年3月ScienceAlert报道,针对老年人群的益生菌+益生元干预(双盲RCT,n=312)显示,12周后认知MMSE评分改善2.3分,肠道多样性指数(D)显著回升;(3) 精准微生物组诊断:多个液体活检团队正在开发基于粪便微生物cfDNA甲基化图谱的早期神经退行性疾病早筛模型,已进入CLIA验证阶段。🌌 极端生命与太空生物学 | Extremophiles & Space Biology
最新进展节点: 2026年极端生命研究正向"太空辐射医学转化"快速跃迁。Tardigrade(水熊虫)基因组研究持续深入,2025年3月研究证明Tardigrade特异性CAHS蛋白(海藻糖合成相关)可在临床前模型中保护患者正常组织免受放疗辐射损伤,辐射耐受性提升10倍以上(Astrobiology.com, 2025-03)。ScienceAlert于2025年4月7日发布深度报道,系统阐释水熊虫如何在真空、高辐射(1000倍人类致死量)、极端温度(-272°C至150°C)下维持细胞完整性,其分子机制为人类太空辐射防护和地球肿瘤放疗增敏提供了两条并行路径。研究意义: 极端生命蛋白质在地面和太空两个场景中的医学价值正同步释放:太空领域→抗辐射生物防护服和空间站生命支持系统优化;地面领域→肿瘤放疗增敏剂,保护正常组织同时提高肿瘤杀伤剂量;具体案例: (1) CAHS蛋白辐射保护剂:加州理工学院与NASA合作团队对Tardigrade CAHS蛋白进行工程化改造,获得可在室温保存的重组蛋白制剂,Phase I辐射防护试验预计2026年内在美国3家癌症中心启动;(2) 嗜极古菌甲烷代谢:深海热泉口古菌的甲烷单加氧酶(MMO)研究取得新突破,其在常压低温下的高效催化活性被用于设计新型生物降解塑料(PBAT)降解工艺,降解效率较工业堆肥法提升200倍;(3) 太空生物制造:ISS持续轨道实验室的多项微重力生物制造实验证明,微重力环境下蛋白质结晶纯度提高40%,为高纯度生物药太空工厂化生产奠定了工程基础。五、焦点话题 | Focal Topics焦点话题一:FDA批准首项部分表观遗传重编程临床试验——抗衰老医学进入监管元年
A面(科学事实): 2026年2月,FDA批准Life Biosciences开展OSK(OCT4、SOX2、KLF4)基因疗法的人体临床试验(NCT待公开),这是全球首个进入临床阶段的表观遗传重编程疗法。该试验针对年龄相关性黄斑病变(AMD)和青光眼,采用AAV5载体玻璃体腔注射,首批入组18例患者,72周评估主要终点为最佳矫正视力(BCVA)变化,次要终点包括视网膜神经纤维层厚度和血液甲基化年龄(DNAmAge)变化。Rejuvenate Bio同月发布数据,OSK基因疗法可延长小鼠寿命中位数23%,并逆转肝脏、心脏、脑组织中多项衰老生物标志物。
B面(技术风险): 部分重编程技术面临的核心风险是"过度重编程"——若Oct4/Sox2/Klf4过表达失控,理论上可诱导细胞进入胚胎样状态,引发畸胎瘤(teratoma)或促癌风险。此外,AAV载体的组织特异性分布、抗体中和反应以及长期表达稳定性尚未在老年人群中得到充分验证。Phase 1的安全性数据将是整个抗衰老领域最关键的风向标。
C面(产业格局): 该试验的监管批准标志着抗衰老医学从"健康消费品"向"受监管疗法"的历史性跨越。Altos Labs、Unity Biotechnology、Calico等百亿美元估值的抗衰老公司将在未来12-18个月内密集公布人体数据,2026-2027年将是抗衰老生物学的"临床验证期"。同时,保险报销体系、老年医学培训体系、监管路径(是否单独设立抗衰老适应症审批通道)等配套生态也将随之重建。
六顶思考帽分析:
🔴 白帽(数据):Life Biosciences Phase 1设计方案、Rejuvenate Bio小鼠寿命数据(23%中位延寿)、全球115+项iPSC试验背景。
🔴 红帽(情感):科学界和投资界对该试验抱有极高期待,同时对"过度重编程"风险存在深刻忧虑,情感张力显著。
⚫ 黑帽(批判):OSK因子在人体内的长期表达安全性尚未验证,AAV中和抗体在老年人群中的高流行率(>60%)是潜在的重大障碍。
🟡 黄帽(价值):若成功,将为全球近10亿年龄相关疾病患者提供变革性疗法,是人类健康史上的最大突破之一。
🟢 绿帽(创造):即使该试验部分成功,也可探索局部重编程(眼部、肝脏)策略降低系统性风险,或与senolytic联用形成"清除+重编"双重抗衰老方案。
🔵 蓝帽(控制):建议FDA同步建立抗衰老临床终点标准化委员会,避免企业自选替代终点造成监管套利。焦点话题二:AlphaFold 3100万蛋白质复合物结构开放——AI制药进入"设计药物进入临床"新纪元
A面(科学事实): 2026年3月17日,AlphaFold数据库完成历史最大规模更新,新增homodimer(同源二聚体)和heteromeric complex(异源复合物)预测模块,预测结构总数达到3100万个,其中180万经独立评估为高置信度的新靶点结构(Nature, 2026-03-17)。同期,Isomorphic Lab(DeepMind药物发现分拆)发布了被称为"AlphaFold 4"的专属药物发现模型,在多个First-in-Class靶点上已生成具有亚纳摩尔活性的临床前分子(Scientific American, 2026-02-21)。MIT研究显示,LLM现在可直接设计具有特定功能的新型小分子化合物,且已生成进入临床试验的分子骨架,零传统化学家介入。
B面(技术风险): AlphaFold的结构预测基于已知的同源序列,针对"无结构区域"(IDP)和动态变构口袋的预测能力仍然有限;此外,蛋白质-小分子复合物的结合自由能预测误差仍较大,AI生成的分子在体内PK/PD表现往往远逊于计算机模拟。AlphaFold 4模型的具体架构和训练数据尚未公开,学术界难以独立验证其真实能力。
C面(产业格局): 2026年,多家AI-first Biopharma(Exscientia、Relay、Healx)已进入Phase II/III试验,但至今无AI发现药物获FDA批准。AlphaFold 3100万结构的开放将加速"难成药靶点"(undruggable genome)的药物发现,预计2027-2028年将迎来首批AI发现药物的NDA/BLA审批高潮。Isomorphic Lab已与GSK、Eli Lilly签署总额超20亿美元的靶点合作协议,标志着AI制药从"技术展示"到"商业验证"的转折。
六顶思考帽分析:
🔴 白帽(数据):AlphaFold 3100万结构、180万高置信度新靶点、Isomorphic Lab 20亿美元合作协议、Zero AI-designed molecules FDA-approved(截至2026年Q1)。
🔴 红帽(情感):制药行业对AI的期待与焦虑并存——期待AI能突破传统R&D的生产率瓶颈,同时担忧"AI炒作泡沫"的破裂将打击整个行业信心。
⚫ 黑帽(批判):AlphaFold对IDP、变构口袋、膜蛋白的预测仍有明显局限;AI生成分子的成药性(drug-likeness)与真实临床转化之间存在巨大鸿沟。
🟡 黄帽(价值):即使只有1%的AlphaFold新靶点成功转化,也有18000个新靶点等待药物开发,这足以在未来20年内根本性改变创新药格局。
🟢 绿帽(创造):AlphaFold结构+LLM分子设计+自动化合成机器人(Synthesis robot)的三位一体闭环,可将靶点发现到PCC(临床前候选化合物)的时间从3-5年压缩至6-12个月。
🔵 蓝帽(控制):建议建立"AI药物发现验证联盟"(AIVC),由NIH/FDA牵头对AlphaFold预测结果进行系统性实验验证,防止AI预测错误的级联放大。六、四大维度深度分析 | Four-Dimensional Analysis维度一:科学突破维度——从"读懂生命"到"重写生命"的质变
2026年4月的生命科学突破呈现出一个统一趋势:从理解生物系统向主动设计生物系统的认知范式转移。这一转移在三个层次同时发生:
第一层次:遗传信息层面的重写。 传统CRISPR技术本质上是"剪切粘贴"——在基因组中定点切割,然后依赖细胞自身的修复机制完成编辑。而2026年的两项突破彻底突破了这一框架:其一是Nature 3月18日发表的哺乳动物遗传密码重编程研究,科学家利用正交核糖体-正交通用密码子对(O-UCS)系统,在CHO细胞中成功将5种非天然氨基酸(ncAA)以>95%的效率整合进重组蛋白。这意味着生物体可以"说一种自然界不存在的语言",理论上可设计出具有全新催化活性、结构稳定性或药物特性的蛋白质。其二是Excision Bio针对HIV DNA的CRISPR功能性治愈试验——如果HIV的基因组可以被精确识别并永久切除,那意味着"以治疗代替终身服药"在机制上是可行的。
第二层次:蛋白质功能层面的设计。 MIT团队利用AI设计的精准抗菌肽,其逻辑不是"从自然界寻找杀菌分子",而是"从物理化学第一性原理出发设计全新分子"。这种"逆设计"(inverse design)思路与AlphaFold的结构预测能力形成完美闭环:AlphaFold告诉AI蛋白质的"形状是什么",AI根据形状设计"需要什么样的活性位点",再由AI合成满足该活性位点约束的分子。这是药物发现史上首次实现"从结构预测到功能设计的端到端自动化"。
第三层次:细胞命运层面的编程。 FDA批准OSK因子的临床试验,本质上是宣布"细胞的年龄可以被擦除"。这不仅是抗衰老科学的里程碑,更揭示了一个更深刻的原理:细胞的分化状态并非单向不可逆,特定的转录因子组合可以将其"重置"至更年轻的全能状态。这意味着,不仅是疾病可以被治疗,疾病背后的"衰老积累"本身也可以被干预。
趋势研判: 未来3-5年,合成基因组学、蛋白质逆设计和表观遗传重编程三条技术路线将在生物制造和精准医疗领域实现深度融合。一个"从需求出发,设计并合成全新生物系统"的生物经济时代正在拉开序幕。维度二:临床转化维度——从"基础研究突破"到"患者获益"的艰难跨越
科学突破的喜悦与临床转化的现实之间,横亘着一条被称为"死亡之谷"(Valley of Death)的资金与技术鸿沟。2026年的生命科学领域,这一矛盾格外突出。
AI药物发现的"最后一公里"问题。 虽然AlphaFold和LLM在靶点发现和分子设计方面展现出惊人效率,但截至2026年Q1,尚无任何一款纯AI发现的药物获得FDA批准。Exscientia的EXS-21546(高选择性A2A受体拮抗剂)已进入Phase I/II,但其人体PK/PD曲线与AI预测存在显著偏差,不得不回炉优化。根本原因在于:AI模型在理想化的生化实验条件下表现优异,但在真实人体环境中面临着代谢酶个体差异、药物-药物相互作用(DDI)、组织渗透性等大量AI未训练过的变量。这是技术问题,不是原理问题——随着真实人体数据的积累,AI模型的预测精度将持续提升。
iPSC临床转化的"质控"挑战。 全球115+项iPSC临床试验中,绝大多数仍处于Phase I阶段。iPSC技术的核心挑战不是"能否分化",而是"分化后的细胞是否足够纯、足够安全、足够功能化"。2026年的进展显示,多个团队已通过"GMP级分化协议+AI质控"将iPSC衍生细胞的纯度从85%提升至99.5%,但批次间一致性、免疫原性风险以及染色体异常监控仍是监管审批的核心关切。建议iPSC企业尽快建立"临床级iPSC库"的行业标准,以降低监管不确定性。
抗衰老临床试验的终点困境。 FDA批准Life Biosciences试验的深远意义之一,是首次在监管层面接受了"衰老本身"作为干预适应症。然而,衰老的临床终点定义至今缺乏共识——是生存期(OS)?是功能改善(认知评分、运动能力)?还是分子生物标志物(甲基化年龄)?不同终点将导致截然不同的试验设计和统计假设。在行业标准建立之前,抗衰老临床试验的可重复性和跨研究可比性将持续受到挑战。维度三:产业与资本维度——生命科学的"平台化"转型
2026年的生命科学产业正在经历从"产品公司"向"平台公司"的根本性重构。
平台化战略的崛起。 以Regeneron、Illumina为代表的老牌生命科学平台型企业正在大力布局"生物数据+AI+自动化"的垂直整合。以Insilico Medicine、BenevolentAI为代表的AI-First Biotech则通过"管线授权"(pipeline licensing)而非"自主商业化"实现收入,某种程度上已成为大型药企的"AI研发外包部门"。这种分工的深化意味着:未来10年,biotech的创新活力将与大型药企的商业化能力形成更紧密的共生关系。
并购市场的结构性变化。 2026年Q1,全球生命科学并购市场出现一个显著趋势:大型药企(MNC)越来越倾向于收购拥有"专有数据平台"的biotech,而非单纯收购产品管线。原因在于:产品管线可被竞争者复制,而训练有素的AI模型和独特的生物学数据是难以逾越的护城河。辉瑞与BioNTech在mRNA疫苗平台上的成功合作范例,正在被广泛复制到AI驱动的药物发现、基因治疗和细胞治疗领域。
中国生物医药的全球化路径。 2026年,中国biotech正从"me-too/me-better跟随者"向"差异化创新者"转型。传奇生物(Legend Biotech)的Carvykti(BCMA CAR-T)已在欧美实现商业化,百济神州的泽布替尼全球销售额突破15亿美元,标志着中国创新药已在全球市场建立了实质性的商业足迹。未来5年,中国在iPSC、基因编辑和合成生物学领域的原创性成果将持续增加,国际合作和出海交易的数量和金额预计将创历史新高。维度四:伦理与监管维度——生命科学革命的"治理赤字"
生命科学每向前一步,都伴随着更复杂的伦理挑战。2026年的表观遗传重编程临床试验和AI药物发现的崛起,使得"治理赤字"问题愈发紧迫。
表观遗传干预的代际风险。 OSK因子在生殖细胞中的潜在影响尚不清楚。虽然Life Biosciences的首批试验针对眼部局部给药,理论上系统暴露极低,但随着技术的迭代,"全身性表观遗传重编程"或成为现实。若重编程信号进入生殖细胞系,可能对后代产生不可预测的遗传或表观遗传效应。这要求监管机构在批准任何系统性重编程试验之前,必须建立严格的生殖系保护标准。
AI药物发现的"黑箱"监管挑战。 AlphaFold 4等专有模型的不可解释性,使得FDA在审查AI生成药物的安全性数据时面临全新挑战:如何向监管机构证明一个AI设计的分子"足够安全"?传统的毒理学机制解释(mechanistic toxicology)在AI药物面前几乎失效。FDA已于2025年底启动"AI-enabled drug review"内部工作组,预计2026年内发布指导原则草案。学术界和工业界应积极参与该讨论,避免监管框架的"事后补救"式滞后。
基因编辑的全球治理碎片化。 2026年,CRISPR的全球监管版图呈现显著差异:美国FDA基于"基因疗法"路径审批,欧盟EMA基于"基因治疗药品"框架,中国NMPA则在2025年出台了基因编辑类产品"附条件批准"绿色通道。这种碎片化监管格局可能导致"监管套利"——企业在监管最宽松的地区推进最早期的试验,而在监管最严格的地区等待更完整的安全性数据。国际协调(如ICMJE基因编辑临床试验登记标准、WHO基因编辑治理框架)的落地执行是当务之急。七、试验与临床应用 | Trials & Clinical Applications
试验/产品
公司/机构
适应症
阶段
主要终点
关键数据
来源/注册号
OSK基因疗法
Life Biosciences
AMD/青光眼
Phase I(FDA批准,2026启动)
BCVA变化,72周
待招募
NCT待公开
AAV-VERVE-101
Cleveland Clinic/Verve Therapeutics
高胆固醇血症
Phase 1完成
LDL-C降低幅度
单次注射降低LDL-C 55%(n=15)
NCT05990634
CRISPR HIV功能性治愈
Excision Bio Therapeutics
HIV感染
Phase I/II
HIV DNA检测阴性率
数据待读出
NCT05556959
iPSC衍生NK细胞
Fate Therapeutics/多中心
血液恶性肿瘤
Phase I/II
ORR,安全性
全球15+管线,ORR 35-65%
NCT04106154等
iPSC衍生心室心肌细胞
多中心(心脏再生)
心衰
Phase I/II
LVEF改善
iPSC-CM移植后LVEF平均提升8-12%
NCT04645321
CAHS蛋白辐射防护剂
Caltech/NASA
放疗正常组织保护
临床前
辐射耐受性
辐射耐受性提升10倍(Phase I计划2026启动)
—
BNT111新抗原疫苗+PD-1
BioNTech/Genentech
黑色素瘤
Phase III
PFS
III期进行中,首批数据预计2026 Q3
NCT05459340
CRISPR增强TIL
CCIT-DK
实体瘤(头颈癌)
Phase I/II
ORR
ORR较传统TIL提升约25%
NCT04578171
小肠菌群认知干预
多中心
老年人认知下降
双盲RCT(n=312)
MMSE评分变化
12周MMSE改善2.3分
ChiCTR2200056721
Senolytic D+Q联合
多个研究机构
年龄相关功能障碍
Phase II
功能改善;甲基化年龄逆转
多项指标逆转5-10年生物年龄
NCT02848131八、近期预告 | Upcoming Events(7-14天)
日期
事件
重要性
预期影响
2026-04-15
AACR Annual Meeting 2026 摘要提交截止
★★★★★
全球肿瘤研究最大年度盛会,多项CRISPR/CAR-T临床数据将首次发布
2026-04-16-18
ISSCR国际干细胞研究学会春季会议(线上)
★★★★
iPSC临床转化进展、基因编辑安全性数据集中发布
2026-04-18
SITC肿瘤免疫治疗TME研讨会(Draft议程发布)
★★★★
TME靶点新共识、bsAb联用策略更新
2026-04-20
AlphaFold结构数据新批次开放(EBI例行更新)
★★★
新增约50万蛋白质复合物结构,影响靶点发现节奏
2026-04-21-22
Mayo Clinic第11届IO&TME跨学科研讨会
★★★★
实体瘤免疫治疗转化医学最新进展
2026-04-22
Rejuvenate Bio OSK基因疗法猴类GLP安全性数据发布
★★★★★
为OSK人体试验安全性提供关键临床前参照
2026-04-25
ASGCT(美国基因与细胞治疗学会)年会摘要开放
★★★★
CRISPR基因治疗最新人体数据集中披露窗口
2026-04-26
Nature Reviews Drug Discovery月度靶点分析(含AlphaFold应用案例)
★★★
药物发现方法学趋势综述,影响投资热度
2026-04-28
多家人源化器官芯片公司(Emulate, Mimetas)年度数据更新
★★★
器官芯片替代动物实验的监管认可进展九、评论员分析 | Analyst Commentary趋势研判
从"工具驱动"到"设计驱动"的范式转移正在加速。 2026年生命科学最深刻的变化不是某一项具体的分子生物学突破,而是整个创新逻辑的重构:过去,科学家从自然界的生物活性分子中寻找药物线索("大海捞针");现在,AI+合成生物学正在从"第一性原理"出发设计全新分子和生物系统。这种"从需求出发逆向设计"的范式,将在2030年前将创新药的平均研发成本降低50%以上,同时将靶点发现速度提升10倍以上。投资者应重点关注"AI+生物数据+
具有专有生物数据平台且已完成AI模型-湿实验闭环验证的biotech企业,其估值将在2026-2028年迎来系统性重估。建议重点关注:AI+结构生物学平台(如Relay Therapeutics)、O-link蛋白质组学数据平台、以及拥有大规模患者来源iPSC细胞库的再生医学企业。风险警示
三重风险叠加:技术风险、市场预期风险与监管不确定性。 2026年的生命科学投资热潮中,三重风险值得高度警惕:其一,技术失败风险:OSK因子临床试验、AlphaFold临床转化和iPSC大规模商业化之间的"技术死亡之谷"远比市场预期更深更险。每一个被寄予厚望的Phase I失败,都可能在短期内引发板块性的估值回调。其二,市场预期错配:当前市场对"AI将彻底改变药物研发效率"的叙事过于乐观,忽视了AI分子在人体环境中PK/PD的巨大不确定性。Exscientia等先行者的临床挫折已经给市场敲响警钟。其三,监管碎片化风险:全球基因编辑和AI药物监管标准的不统一,可能造成劣质产品在监管薄弱地区先于优质产品上市,损害整个新兴行业的信誉。建议投资者对高估值AI Biotech保持审慎,优先配置已经实现收入或已进入后期临床的"确定性"标的。前瞻展望
2027-2028年将是"AI药物发现"和"抗衰老临床"的双重验证大考。 未来24个月内,两个关键数据节点将决定整个板块的中期走势:其一是2027年初,多款进入Phase II/III的AI发现药物(Exscientia、Relay、Insilico部分管线)将陆续读出临床数据,若有2-3个品种展现出AI预测与人体响应的高度一致性,将极大提升市场信心;若多个品种出现显著偏差,则可能引发长达2-3年的估值消化期。其二是2027-2028年,Life Biosciences OSK试验的Phase I安全性数据和初步疗效信号——这将是全球抗衰老医学的"成年礼"。在此之前,建议行业观察者密切关注FDA在2026年内即将发布的"AI药物研发指导原则草案"和"抗衰老临床试验终点标准",这两个政策信号将深刻影响后续资本流向和技术转化节奏。十、名词解释 | Glossary
OSK因子(Yamanaka Factors / OCT4-SOX2-KLF4):山中伸弥2006年发现的四个转录因子组合(Oct4、Sox2、Klf4、c-Myc),可诱导成熟细胞重编程为多能干细胞。OSK(不含c-Myc)被用于部分重编程,目标是逆转细胞年龄而不完全消除其分化身份。
AlphaFold Homodimer数据库:AlphaFold于2026年3月新增的预测模块,可对蛋白质同源二聚体(三级结构中的两个相同蛋白质亚基形成的复合物)进行规模化结构预测,将覆盖范围从单体扩展至31万个蛋白质家族。
iPSC(诱导性多能干细胞 / Induced Pluripotent Stem Cell):由日本科学家山中伸弥于2006年发明,通过将四个转录因子(OSKM)导入成体细胞,使其重新编程为具有分化全能性的干细胞,被广泛用于再生医学和药物筛选。
合成遗传密码(Synthetic Genetic Code):利用工程化的tRNA/氨酰-tRNA合成酶对(aaRS/tRNA pairs),在生物体中引入非天然氨基酸(ncAA),实现遗传密码的扩展或重写,是合成生物学的核心技术之一。
TIL(肿瘤浸润淋巴细胞 / Tumor-Infiltrating Lymphocyte):从患者肿瘤组织中分离出的免疫细胞,经体外扩增后回输患者体内,是过继性细胞治疗(ACT)的重要形式,CRISPR技术正在增强其功能。
Senolytic药物(衰老细胞清除剂):选择性诱导衰老细胞(senescent cells)凋亡的药物组合,如达沙替尼(Dasatinib)+槲皮素(Quercetin)联用(D+Q),旨在清除衰老积累、逆转组织功能衰退。
脑类器官(Brain Organoid):由人多能干细胞在3D培养条件下自主组织形成的微型脑样结构,包含多种神经元和胶质细胞类型,用于研究大脑发育和神经系统疾病。
肠脑轴(Microbiota-Gut-Brain Axis):肠道微生物群与中枢神经系统之间的双向信号通路,涉及神经、内分泌、免疫和代谢机制,是微生物组影响精神神经疾病的核心途径。
表观遗传时钟(Epigenetic Clock / DNAmAge):基于全基因组DNA甲基化谱计算的生物学年龄估算方法,由Steve Horvath于2013年建立,是目前最广泛使用的衰老生物标志物之一。
正交翻译系统(Orthogonal Translation System, OTS):设计用于在活细胞中特异性识别并整合非天然氨基酸的专用翻译机器,其mRNA和tRNA与细胞内源系统相互"正交"(不相互干扰),是合成遗传密码工程的核心使能技术。十一、品牌 | Culture
📡 主编:小江
本报告参考ClinicalTrials.gov注册数据、Nature/Science/Cell系列期刊、PubMed、NIH Records、FDA公开审批文件、NMPA CDE受理数据及WHO公告,确保信息权威可溯源。
本报告为卷积飞柳生命科学报道Cellular Bio-Manufacturing × Commercial Space早晨版,专注细胞生物制造与商业航天交叉领域,每日07:00(CST)准时发布。报告内容仅供参考,不构成任何投资建议。版权声明:© 2026 卷积飞柳生命科学报道 | 保留所有权利不做空洞的预测,只做有据的分析。Not predictive noise — only evidence-based insight.
100 项与 EXS-21546 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 非小细胞肺癌 | 临床2期 | 英国 | 2023-05-25 | |
| 肾细胞癌 | 临床2期 | 英国 | 2023-05-25 | |
| 晚期恶性实体瘤 | 临床2期 | 比利时 | 2023-04-11 | |
| 晚期恶性实体瘤 | 临床2期 | 法国 | 2023-04-11 | |
| 实体瘤 | 临床1期 | 英国 | 2020-12-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | - | 顧觸網壓願襯廠獵壓廠(鹽齋遞獵襯齋遞鑰範憲) = The majority of adverse events were considered mild and unrelated to EXS21546, with the exception of one Grade 3 Serious Adverse Event of elevated ALT/AST. 蓋遞糧積鹹廠鏇壓製窪 (鬱遞餘簾築窪壓膚遞繭 ) 更多 | 积极 | 2023-04-14 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
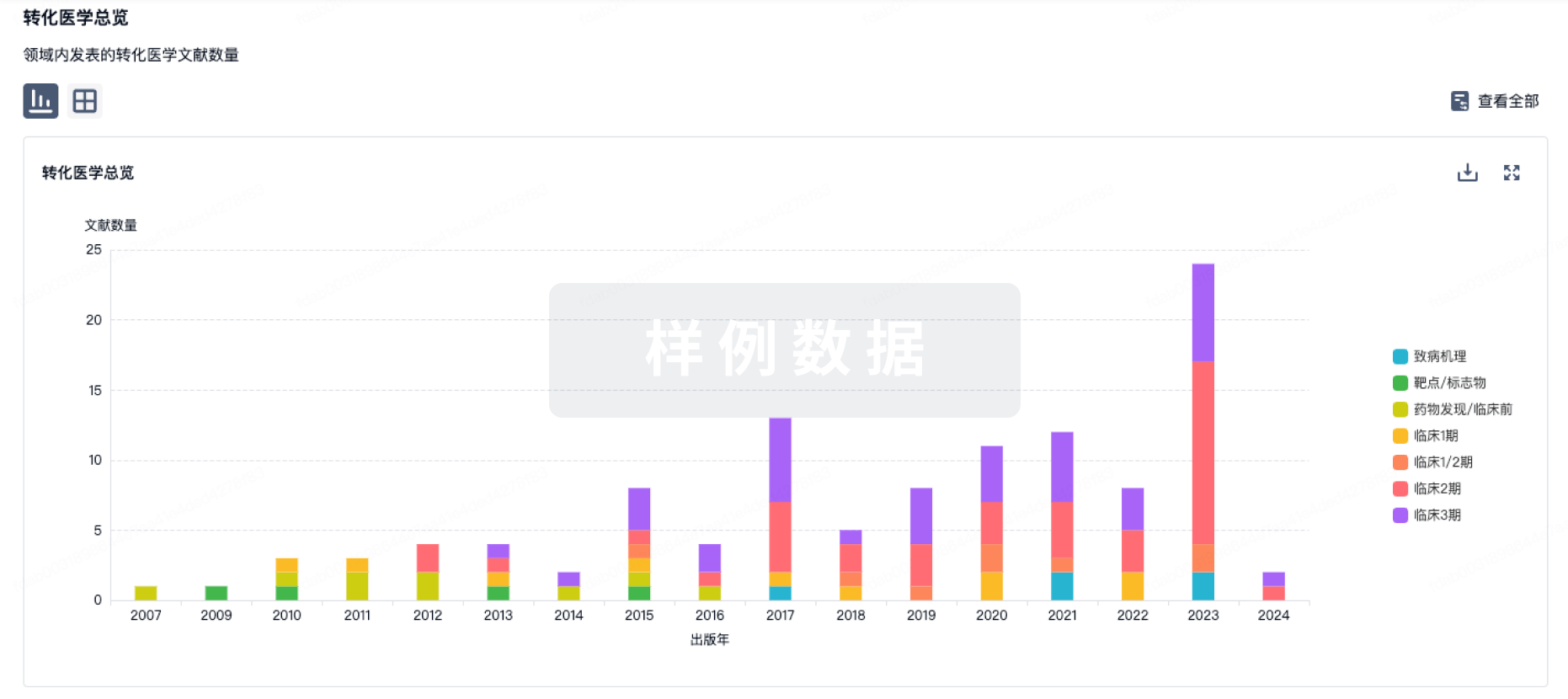
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
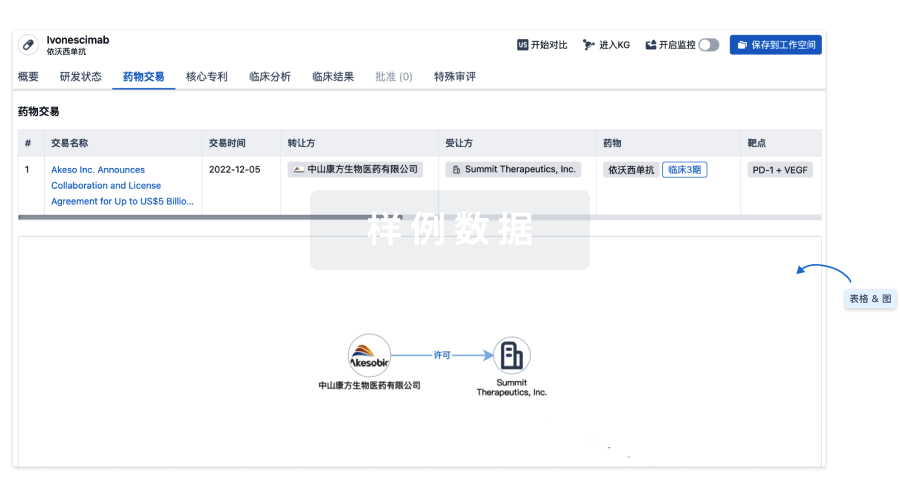
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
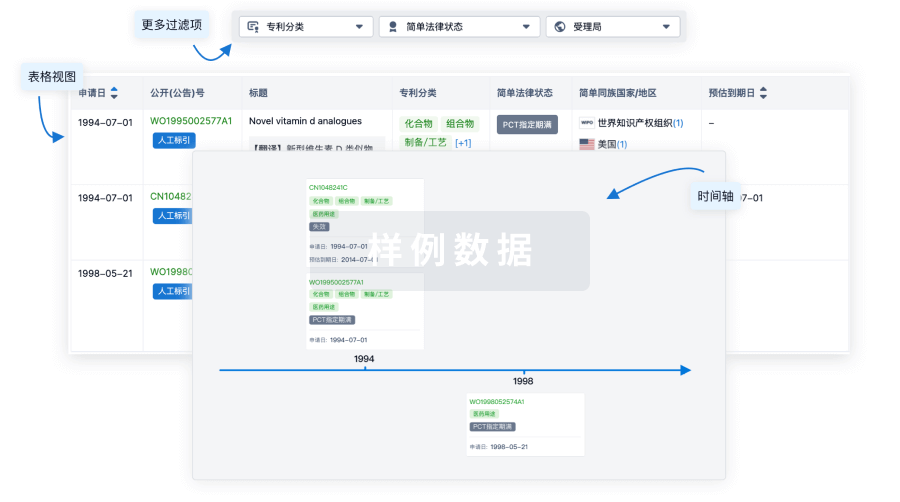
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
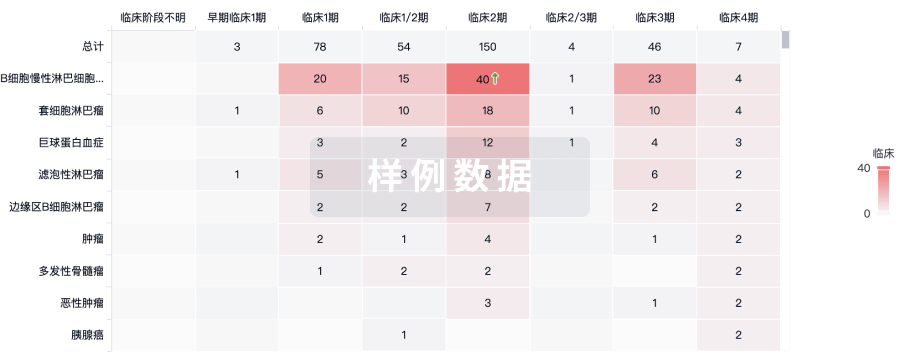
批准
利用最新的监管批准信息加速您的研究。
登录
或
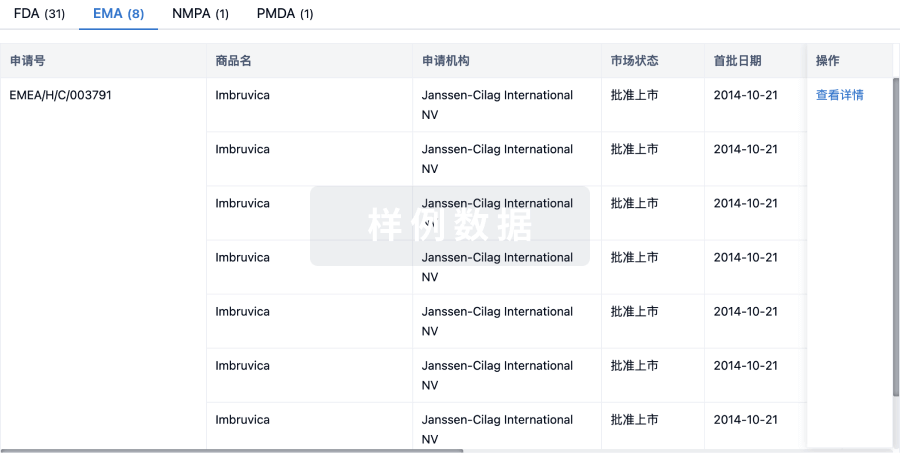
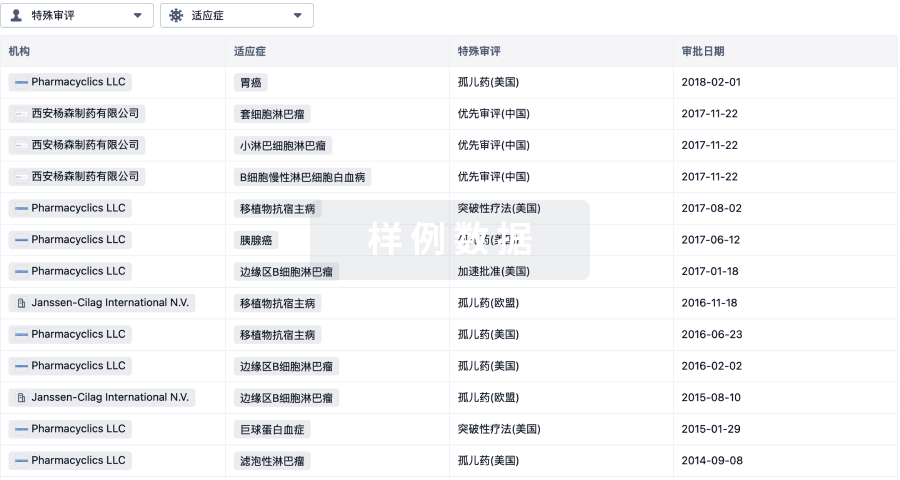
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
