预约演示
更新于:2026-03-14
RN3161
更新于:2026-03-14
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
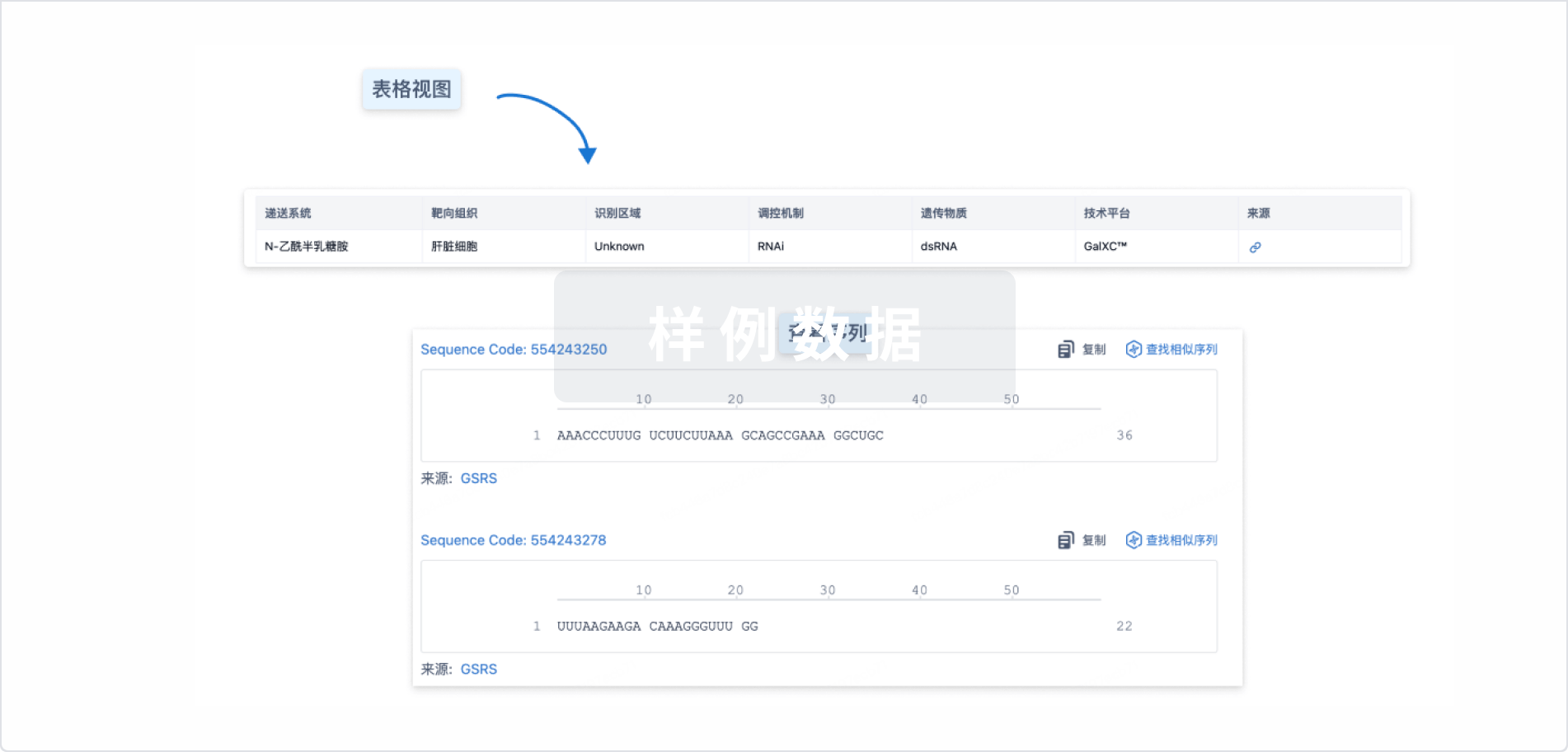
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
1
项与 RN3161 相关的临床试验NCT07245771
A Randomized, Double-Blind, Placebo-Controlled Phase 1/2a Study to Evaluate the Safety, Tolerability, Pharmacokinetics, Pharmacodynamics and Effect on Body Weight of RN3161 as Monotherapy and in Combination With Tirzepatide in Adults With Overweight and Obesity
Study to assess the safety, pharmacokinetics (the amount of study drug or any of its breakdown products in your body) and pharmacodynamics (how the study drug affects your body) of RN3161 alone (healthy volunteers) and RN3161 with tirzepatide (overweight and obese subjects)
开始日期2025-11-04 |
申办/合作机构 |
100 项与 RN3161 相关的临床结果
登录后查看更多信息
100 项与 RN3161 相关的转化医学
登录后查看更多信息
100 项与 RN3161 相关的专利(医药)
登录后查看更多信息
9
项与 RN3161 相关的新闻(医药)2026-03-10
·静思阅微
INHBE靶点小核酸药物研究进展
小核酸赛道新风口,靶向INHBE重塑减重治疗新格局,一文读懂核心进展、临床数据与未来前景
一、INHBE靶点:代谢疾病黄金靶点,遗传相关性显现
1.1 靶点核心特性
抑制素亚基βE(INHBE)属于TGF-β超家族核心成员,具备高度肝脏特异性表达的特点,其编码合成的激活素E(Activin E),是调控机体脂肪代谢、能量稳态的关键效应分子,也是近年代谢疾病领域炙手可热的新兴靶点。
依托扎实的人类遗传学证据,多项跨族群外显子测序研究证实:携带INHBE功能丧失型突变的人群,体脂分布更优质、内脏脂肪堆积量显著更低,对2型糖尿病、原发性肥胖、代谢综合征等疾病存在天然抗性,且无致命性生理缺陷,既印证了靶点的致病关联性,也为靶向药物研发筑牢了安全性根基。
1.2 核心致病通路
在肥胖、高糖高脂饮食、胰岛素抵抗等病理状态下,机体脂质代谢紊乱会直接触发肝脏INHBE基因异常过表达,促使激活素E大量合成释放入血,靶向结合脂肪细胞膜表面的ALK7受体,持续激活下游Smad2/3信号通路,形成双重病理损伤:
一方面抑制脂肪细胞脂解作用,阻断脂质分解供能,加剧脂肪异常囤积,尤其推动内脏脂肪过度蓄积,诱发腹型肥胖;另一方面干扰胰岛素信号传导,加重外周组织胰岛素抵抗,进一步恶化糖脂代谢,形成“肥胖-代谢异常-INHBE高表达”的恶性循环。
更具优势的是,该通路不依赖中枢神经系统,可从基因层面直接干预肝脏脂肪代谢,完美规避中枢性减重药常见的恶心呕吐、情绪异常、头晕等不良反应,兼具靶向性与安全性双重亮点。
二、INHBE小核酸药物:GalNAc-siRNA为主流,治疗优势突出
2.1 核心技术路线
目前全球INHBE靶点小核酸药物,均以GalNAc偶联siRNA为唯一主流技术,依托RNA干扰机制发挥疗效:通过特异性沉默肝脏INHBE基因的mRNA转录与翻译,阻断激活素E合成,从根源切断致病通路,实现减脂、改善胰岛素抵抗、调节糖脂代谢的治疗效果。
GalNAc修饰技术是核心突破点,可介导siRNA精准靶向肝脏实质细胞,大幅提升组织特异性与胞内递送效率,同时延长药物体内半衰期,解决传统小核酸递送难、代谢快、给药频繁的行业痛点,实现长效给药。
2.2 药物核心治疗优势
•减脂不减肌,高质量减重:仅靶向抑制脂肪合成与堆积,不干预肌肉代谢,临床前及早期临床数据证实,可在减少全身/内脏脂肪的同时增加瘦体重,避免减重伴随的肌肉流失,适配长期体重管理。
•长效低频次,依从性拉满:单次皮下注射药效可维持6个月以上,临床数据支持每年1-2次给药,对比每日/每周给药的传统减重药,大幅降低患者用药负担。
•靶向性强,安全性可控:靶点肝脏特异性表达+GalNAc精准递送,脱靶效应极低;INHBE功能丧失无致命缺陷,早期临床无严重治疗相关不良反应,耐受性优异。
•联用潜力大,适用人群广:可与GLP-1受体激动剂、双靶点激动剂联用,协同提升减重降糖幅度,改善单药停药反弹、疗效有限等短板,覆盖难治性肥胖、糖尿病合并肥胖等复杂病例。
三、核心临床数据对比|海内外研发布局一览
当前INHBE小核酸药物均处于早期临床阶段,海外品种率先披露临床数据,国内药企紧随其后,多款药物获批临床,赛道竞争白热化。以下为核心在研药物关键数据整合,直观呈现海内外研发差异:
药物名称
研发企业
研发进度
核心适应症
核心疗效数据
给药方案
WVE-007
Wave Life Sciences
Ⅰ期临床(中期)
单纯性肥胖
240mg给药3个月,全身脂肪降4.5%,内脏脂肪降9.4%,瘦体重升3.2%;无3级以上不良反应
每年1-2次皮下注射
ARO-INHBE
Arrowhead
Ⅰ期临床
肥胖+2型糖尿病
联用替尔泊肽16周,体重降幅9.4%,降糖减脂效果优于单药
长效皮下注射
RN3161
大睿生物
Ⅰ期临床(首例给药)
肥胖/代谢并发症
食蟹猴模型INHBE mRNA下调超90%,安全性耐受性良好
每年1-2次皮下注射
CMS-D008
康哲药业
获NMPA临床批准
超重/肥胖
临床前显著减重减脂,不影响瘦体重,拟联用自研双靶点激动剂
皮下注射(长效)
LDR2515
先衍生物
获NMPA临床批准
肥胖/代谢性疾病
长效抑制INHBE表达,不影响摄食量,联用GLP-1类增效明显
每半年-每年1次皮下注射
从临床数据可以看出:海外品种临床数据先行,减脂增肌效果明确;国内品种临床前数据亮眼,研发进度同步国际,长效给药优势高度一致,联合用药成为未来核心研发方向。
四、研发挑战与前景展望
4.1 现存核心挑战
•临床数据待完善:所有药物均处于Ⅰ期临床阶段,样本量小、随访周期短,长期疗效、安全性数据缺失,亟需推进大样本、多中心Ⅱ/Ⅲ期临床,验证不同人群中的治疗效果与耐受性。
•给药方案待优化:最优给药剂量、给药间隔尚未明确,与GLP-1类药物的联用配比、疗程设计、安全性适配性仍需大量临床探索,规避联用不良反应叠加风险。
•产业化待突破:小核酸药物修饰、递送、规模化合成成本偏高,量产工艺待优化,需降低生产成本与定价,提升药物可及性,助力商业化落地。
4.2 未来发展前景
INHBE作为兼具遗传学证据、明确致病通路与高安全性的代谢靶点,叠加GalNAc-siRNA技术的精准长效优势,有望打破传统减重药物的治疗局限,成为肥胖、2型糖尿病、代谢综合征等疾病的新一代核心治疗方案。
国内企业研发布局已跻身全球第一梯队,研发进度与技术水平同步接轨国际,随着临床研究推进、技术迭代升级,国产INHBE小核酸药物有望率先实现商业化,填补长效高质量减重药物的市场空白,既为全球代谢疾病患者提供全新选择,也助力我国小核酸产业在代谢领域实现弯道超车。
五、总结
INHBE是代谢领域极具价值的黄金靶点,GalNAc-siRNA小核酸药物凭借减脂不减肌、长效低频次、安全性高的核心优势,成为减重赛道的新晋风口。全球多款药物进入早期临床阶段,核心数据充分验证靶点有效性,国内研发紧追国际步伐,整体赛道潜力无限。
尽管现阶段仍面临临床数据不足、产业化成本偏高等挑战,但随着研发持续深入,INHBE小核酸药物有望成为代谢疾病治疗领域的突破性成果,引领减重与代谢治疗迈入“长效化、精准化、高质量”的全新阶段。
本文内容来源于网络公开资料,由作者整理归纳,仅限学习交流使用。文中观点不代表官方立场,因信息收集有限难免存在不足,欢迎各界朋友批评指正,共同探讨完善。
2026-02-10
·动脉网
2026年开年之初,小核酸赛道全面爆发。
技术突破和商业化落地共同推动小核酸领域进入了从1到10的商业化阶段。减重领域的小核酸药物临床数据接连公布,提振了市场的情绪。此外中国生物的十亿级重磅并购和小核酸企业瑞博生物的港股上市标志着资本的退出通道已经被打通。某创新药投资人告诉动脉网,小核酸赛道已经开始了商业化加速。
图1. 近期小核酸领域的重磅事件(资料来源:动脉网整理)
随着国内创新药龙头和MNC持续加大在小核酸领域的布局,小核酸已然进入创新药研发的核心赛道,未来这一领域的重磅事件有望接连出现。
01
重磅临床数据不断涌现
风头正劲的小核酸赛道,2026年迎来了全面爆发,重磅事件不断涌现。
1月6日,Arrowhead Pharmaceuticals披露了两款siRNA肥胖候选药物的临床数据,在合并2型糖尿病的肥胖患者中,ARO-INHBE、ARO-ALK7均实现了内脏脂肪、总脂肪等身体指标的改善。消息发布后,Arrowhead股价上涨了10.9%。但是由于临床结果中缺少了“体重下降”这一关键指标,市场情绪有所消退。但ARO-INHBE与替尔泊肽联用,在2型糖尿病肥胖患者中于第16周实现了-9.4%的体重下降,相较单用替尔泊肽(-4.8%)约提升2倍。这一数据仍然让投资者看到了小核酸药物的应用潜力。
就在一个月之前,即2025年12月8日,Wave Life Sciences公布了其siRNA药物WVE-007用于减重的Ⅰ期临床试验结果,单次给药后第12周减重幅度4.0%,肌肉增加0.9%。WVE-007在实现与司美格鲁肽相当的减脂效果的同时,避免了后者常见的肌肉流失风险。且WVE-007安全且耐受性良好,无受试者停药,未发生严重或重度治疗相关不良事件(TEAE)。当日,Wave股价暴涨147.3%。
小核酸减重赛道多款潜力产品接连发布的临床数据表明,小核酸药物有可能作为单药或与GLP-1类药物联合使用,在减脂的同时减少肌肉消耗。小核酸药物在减重领域的临床前景值得期待。
02
多起小核酸重磅交易爆发
此外,2025年小核酸领域BD交易火热,圣因生物、舶望制药、靖因药业这些小核酸研发企业都有大额BD授出,这一现象在2026年仍然持续。2026年新年伊始,安龙生物便与一家美国纳斯达克上市企业达成小核酸药物领域的国际战略合作协议,合作规模达上亿美元,这标志着安龙生物在国际BD合作方面取得重要突破。
安龙生物在小核酸领域持续布局,其肝外靶向递送技术平台得到了海外企业的认可,商业化能力凸显。除了BD交易,创新药企还通过并购的方式加码小核酸赛道。
2026年1月13日晚,中国生物制药发布公告称,将以12亿元人民币收购赫吉亚生物100%股权,进一步完善布局小核酸(siRNA)赛道。在长效给药和肝外递送方面,赫吉亚生物都有独特的优势。赫吉亚生物的MVIP肝内递送平台是全球首个且目前唯一经临床验证、可实现“一年一针”长效给药的siRNA递送系统。
肝外递送是小核酸药物的发展趋势,目前赫吉亚生物已攻克了多个组织的递送技术瓶颈,实现了肝脏、神经、脂肪等多组织的精准靶向。通过并购赫吉亚生物,中国生物制药在递送平台和产品管线方面都有收获。
并购赫吉亚生物是继投资圣因生物后,中国生物制药在小核酸赛道的又一重要布局,也是国内头部创新药企在小核酸领域的首次重磅并购。
新年伊始,接连出现的热门事件无疑在向我们表明,小核酸领域已经进入了爆发期。
03
减重领域有可能出现大的交易
小核酸药物当下的发展趋势在于向肝外适应症拓展。此前上市的小核酸药物多针对肝脏适应症,递送效率差异不大而且竞争比较激烈。随着小核酸药物在大适应症上获得突破,其应用领域得以拓展,产品的商业价值也被放大。
从当前的时点来看,动脉网认为减重是最有可能后续出现重磅交易的领域。这不仅是因为减重药物市场空间大,具备了诞生大额交易的可能,更重要的是随着减重领域的小核酸在研药物临床数据不断读出,其临床效果正在受到更多的认可。
以司美格鲁肽为代表的GLP-1受体激动剂虽然是降糖减重领域当前的热门药物,但这类产品往往存在副作用大、停药后体重反弹以及因食欲下降导致肌肉流失等问题。小核酸药物作为一种新兴治疗方式,有望实现更精准、持久的代谢调控。
Arrowhead和Wave Life此前公布的临床数据表明,小核酸药物有望与GLP-1类药物联合使用,实现协同增效、减少肌肉损耗;或者作为GLP-1药物停药后的维持疗法,抑制体重反弹;甚至有可能作为单药用于肥胖患者的减重增肌。
目前小核酸减重领域最火热的靶点是INHBE和ALK7。INHBE和ALK7都属于TGF-β超家族,它们在肥胖和代谢疾病的机制中扮演着关键角色:INHBE主要在肝脏细胞中表达,负责编码并分泌Activin E,后者与其他配体共同作用,通过结合ALK7来调控脂肪代谢;ALK7主要在脂肪组织中表达,当Activin E与ALK7结合后,可通过抑制脂肪分解过程来发挥作用。针对INHBE和ALK7这两个热门靶点,国内企业在都有布局。
1)大睿生物的INHBE靶点药物RN3161全球临床进度排名第二
针对研发进度领先的INHBE靶点,国内的在研管线颇为丰富,临床进展居前的是大睿生物的RN3161、倍思可的BC-006以及圣因生物的SGB-7342。
图2. 全球INHBE靶点小核酸在研管线(资料来源:摩熵医药)
RN3161基于大睿生物自研GAIA™平台开发,全球临床进度排名第二,其优化的GalNAc递送设计与化学修饰组合,降低了脱靶风险。早期数据表明,RN3161具有较好的治疗效果。在猴模型中,RN3161低剂量单次给药后就能实现INHBE mRNA表达下调超过90%,并在效力与持久性上实现了领先。此外RN3161能实现长时间有效。临床前研究显示,RN3161可实现超过半年的基因沉默效应,有望将给药频率降低至每年仅1–2次,显著提升患者依从性和长期管理价值。
基于GAIA™平台,大睿生物已经开发了四款进入临床阶段的产品:治疗高甘油三酯血症的RN0361,治疗高胆固醇血症的RN0191,用于治疗动脉粥样硬化的RN5681以及治疗肥胖的RN3161。
在2025年美国心脏协会年会上,大睿生物公布了RN0361的Ⅰ期临床数据。RN0361具备两大特点:1)作用时间持久。RN0361实现了显著且持久的ApoC3和甘油三酯降低作用,疗效持续至少六个月。2)临床效果明显。RN0361可用于预防严重高甘油三酯血症相关的胰腺炎,并降低由动脉粥样硬化性脂蛋白引起的心血管疾病风险,并展现出潜在的同类最佳(BIC)特征。
RN0361良好的临床数据进一步证明了大睿生物自研GAIA™平台的优异性。而作为基于该技术平台推出的第四个临床候选分子,RN3161在治疗肥胖方面的潜力也得到了进一步的佐证。
圣因生物的SGB-7342采用新一代GalNAc偶联技术,通过RNAi技术特异性沉默INHBE基因的表达,进而降低其编码蛋白Activin E的水平,能够有效抑制下游与脂质代谢和能量消耗相关的信号通路活性。临床前研究表明,RN3161能够强效且持久地沉默INHBE表达,显著减轻体重与脂肪量,同时维持肌肉量,并表现出良好的安全性与耐受性。
SGB-7342首例受试者于2026年1月13日在吉林大学第一医院完成给药,预计2026年公布初步数据。
2)圣因生物的SGB-ALK7展现出较好的早期临床数据
针对ALK7靶点,国内在研管线尚处于早期阶段,其中圣因生物的SGB-ALK7颇具看点。
SGB-ALK7是圣因生物基于其独有的LEAD平台开发的药物,这款产品表现出小核酸药物针对肥胖适应症的共同特点:1)长效作用:SGB-ALK7有望实现皮下注射每半年一次的超长效治疗。2)较好的治疗效果:在非人灵长类动物中证实,单次皮下给药后可实现mRNA抑制。在DIO小鼠模型中,SGB-ALK7体重减轻效果与司美格鲁肽相当,能够在保留瘦体重的同时减少脂肪量并促进减重。
目前这款产品还处于临床前研究阶段,随着更多的临床数据读出,SGB-ALK7的治疗效果将得到进一步的验证。
图3. 全球ALK7靶点小核酸在研管线(资料来源:摩熵医药)
在上述产品之外,还有更多的早期小核酸管线正在快速推进中。据动脉网了解,以CRO业务起家的上市公司阳光诺和正在向创新药方向转型,小核酸正是其创新药三大核心发展方向之一。目前有着近三十年小核酸研发经验的何军林教授已经加盟阳光诺和,且由其领衔的小核酸研发团队核心人员数量也从2024年的10人左右快速增加到2025年底的30-40人,在研管线数量也在持续增长。与多数小核酸Biotech企业不同的是,阳光诺和具备从分子发现、药物筛选、临床试验到审评审批的全流程经验,丰富的CRO项目积累可以加快小核酸项目的推进速度。据悉,阳光诺和正在大力推进减脂保肌领域小核酸产品的开发,预计今年年底前将会有早期临床数据公布。
从企业层面来看,动脉网比较看好圣因生物在减重领域的发展潜力。作为下一代RNAi技术领跑者,圣因生物专注于肥胖、心血管代谢及自身免疫性疾病领域的“Best-in-Class”RNAi药物开发。目前圣因生物在研管线共17条,其中治疗肥胖疾病的产品有7款。丰富的管线储备不仅为圣因生物的发展提供了保障,也为其BD交易提供了更多的可能性。
图4. 圣因生物肥胖适应症的在研管线情况(资料来源:圣因生物官网)
此外,圣因生物也有多项BD交易达成:2026年2月2日,圣因生物与罗氏旗下基因泰克达成战略合作,双方将共同推进一款RNAi疗法的开发,交易对价为2亿美元的首付款以及最高达15亿美元的总付款;2025年11月8日,圣因生物与礼来针对代谢性疾病RNAi药物达成12亿美元全球合作;在更早之前,圣因生物的siRNA药物IBI3016授权给了信达生物,用于高血压的治疗。
圣因生物持续的BD授权不仅证明了圣因生物的专有技术平台LEAD的开发潜力,也表明了圣因生物的商业化能力和龙头创新药企对公司的认可。基于这一技术平台开发的RNAi药物未来仍有看点。
04
潜在买家均为MNC
目前,各大药企在小核酸领域动作频频:赛诺菲与Arrowhead的子公司维亚臻在心血管领域达成合作;CRISPER Therapeutic 则与靖因药业合作开发心血管领域的siRNA产品;诺华更是四处出击,先后牵手Regulus、Arrowhead、舶望制药和Avidity,在拓展适应症和改进递送系统两个方向展开了一系列的布局。礼来与圣因生物的合作只是MNC在小核酸领域布局中的一例。
具体到减重领域,小核酸药物在与GLP-1类药物联合使用实现协同增效、减少肌肉损耗方面的效果已经得到了业内认可。因而动脉网认为,手握GLP-1重磅产品的创新药企有可能补充小核酸管线从而实现产品协同。
当前已经实现了GLP-1产品商业化的头部创新药企均布局了小核酸产品:诺和诺德已经与Replicate就自复制RNA(srRNA)平台达成合作协议,共同开发针对肥胖、2型糖尿病等代谢疾病的新型候选疗法;礼来则与圣因生物针对代谢性疾病达成12亿美元RNAi全球合作;信达生物通过与圣因生物合作+自研的方式在快速推进小核酸管线的布局。
在竞争日益激烈的GLP-1减重领域,MNC正在大力开发口服小分子药物:阿斯利康与诚益生物就小分子GLP-1药物ECC5004达成合作,不久前又与石药就GLP-1/GIP减重药物达成合作;罗氏则通过收购Carmot获得了口服小分子GLP-1药物CT-996;默沙东通过授权引进了翰森制药的口服小分子GLP-1药物HS-10535;辉瑞则在近期以总金额20.85亿美元引进了复星医药子公司药友制药的YP05002,在三度失利之后重回到口服小分子GLP-1药物的牌桌上。
在这些企业中,默沙东和辉瑞近两年在小核酸领域处于观望状态,未来有可能成为潜在买家;阿斯利康虽然在小核酸领域有布局,但仍有可能加码小核酸减重药物,从而与管线中的GLP-1产品形成组合,起到更好的效果。未来这几家MNC在这一领域的动向值得高度关注。
图5. 龙头GLP-1研发企业在小核酸领域的布局
(资料来源:动脉网不完全整理)
新年以来小核酸领域的持续火爆已经清晰地表明,小核酸领域的商业化开始加速了。有评论人士认为,2026年是小核酸商业化的元年。当前,小核酸最大的看点还是在减重领域。从恒瑞和信达这两大国内龙头创新药企围绕减重领域的布局逻辑我们可以看到,小核酸联用GLP-1药物实现更好的减脂增肌效果是这一领域当下的主流开发策略。
围绕这一思路,国内小核酸研发企业和MNC将会展开更多合作,后续的重磅交易值得期待。
*封面图片来源:pixabay
如果您认同文章中的观点、信息,或想进一步讨论,请与我们联系;也可加入动脉网行业社群,结交更多志同道合的好友。
近
期
推
荐
声明:动脉网所刊载内容之知识产权为动脉网及相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。文中如果涉及企业信息和数据,均由受访者向分析师提供并确认。
动脉网,未来医疗服务平台
2026-01-27
·小药研社
小核酸药物发展至今已经进入了蓄力期,竞争态势也愈发激烈。下场玩家有biotech,也有意在转型的大型药企。大量的需求也滋生了行业上下游的服务企业。
本次开个专题,盘点国内小核酸企业,这期先来盘点一下原生Biotech,后面两期分别盘点大型药企和上下游企业。大家有特别关注的企业可以留言告诉罗哥,可以开专题解析技术。瑞博生物(Ribo Bio)
公司成立于2007年,2026年1月正式通过港交所聆讯并启动招股,被认为是中国“小核酸第一股”。
其核心产品RBD4059是用于治疗血栓性疾病的siRNA,被认为是全球临床进展最快的抗凝siRNA药物。此外,其肝外递送平台RiboOncoSTAR™(肿瘤)和RiboPepSTAR™(多肽偶联)已开始在CNS和肌肉组织领域进行转化。
圣诺医药(Sirnaomics)
公司成立于2007年,总部位于美国,在苏州与广州设有子公司,2021年于港股上市。具有独特的PNP(多肽纳米颗粒)和GalNAc递送平台,覆盖局部和系统给药。其核心产品STP705是TGF-β1和COX-2双靶向抑制,用于治疗非黑色素瘤皮肤癌(isSCC/BCC),并在IIb/II期临床中展示了积极的治疗潜力。
赫吉亚生物 (Hygieia)
公司成立于2018年,专注于小核酸药物开发,凭借其核心的多组织递送平台(覆盖肝内外)及丰富的慢病管线(减重代谢、心脑血管、神经系统),于2026年1月被中国生物制药以12亿元人民币全资收购。该收购补全了中生的大慢病布局,旨在依托其平台技术打造FIC/BIC管线。
安龙生物 (Anlong Bio)
成立于2019年,罕见病以及眼科疾病的治疗。开发了ANOG小核酸技术平台Gal-Mola半乳糖小核酸药物递送载体。目前与凯因科技合作了HBV-siRNA的开发,与信立泰合作开发治疗高血压的小核酸药物。2026年1月公司宣布完成近亿元人民币B+轮融资并披露达成国际战略合作。
舶望制药(Argo Biopharma)
公司成立于2021年,在2024-2025年间与诺华(Novartis)达成了总金额高达93.65亿美元的全球战略合作,专注心血管及代谢疾病的siRNA药物研发。基于其在肝外递送技术(如骨骼肌、脂肪)的领先平台,该公司心代谢资产在跨国药企中备受瞩目,这一系列合作显著提升了其国际认可度。
大睿生物(Rona Therapeutics)
成立于2021年,平台主要搭建了核酸递送系统和多价结构设计,现已成功将多项创新siRNA资产推进至临床阶段。核心管线包括获NMPA批准的RN1871(AGT,高血压)、发布I期数据的RN0361(APOC3)以及进入I期的RN3161(INHBE,肥胖)。此外,公司已成功将“双靶点 bi-valent PCSK9-LPA siRNA”推进至临床开发。
靖因药业(Sirius Therapeutics)
成立于2021年,研发针对心血管和慢病的FIC/BIC。核心管线有FXI靶点的SRSD107是与CRISPR Therapeutics的抗血栓药物,在欧洲启动II期并完成首例给药;靶向Lp(a)的SRSD216在中国亦进入II期并首例给药。公司于2025年完成近5000万美元融资,全力加速心代谢疾病管线开发。
圣因生物(SanegeneBio)
公司成立于2021年,在中国和美国设有研发中心,依托自主知识产权的LEAD™技术平台,布局肝内及肝外靶向的创新药物管线。2025年公司发展迅速,与礼来(Eli Lilly)达成代谢性疾病RNAi研究合作,并与信达生物围绕AGTSGB-3908等项目布局心代谢慢病。同年11月公司宣布完成约1.1亿美元融资,用于推进管线临床与平台迭代。
炫景生物(Rigerna Therapetuics)
公司成立于2022年,对外宣布已经开发了多个肝外器官靶向递送技术,包括肾脏、骨骼肌、脂肪、心脏、CNS、肺、眼等。其核心产品RG002C0106是一种针对补体因子C3靶点的siRNA药物,旨在治疗由补体介导的原发性或继发性肾小球疾病,现处于I期研究阶段。与华润双鹤合作推进代谢疾病siRNA项目RG008(靶点未披露)。
先衍生物 (Leaderna Therapeutics)
公司成立于2022年,是成都先导体系内孵化/参股平台之一。核心管线LDR2402(高血压方向)已获NMPA批准临床并完成首例受试者入组,LDR2515(靶向INHBE)IND申请于2026年1月获CDE受理。2024年完成近亿元人民币融资。时安生物(Suzhou Siran Biotechnology)
公司成立于2022年,搭建了自主研发的eSAFE化学修饰、STORK肝内外递送平台及双靶 siRNA技术。公司聚焦慢乙肝、心血管代谢、自免等领域,推动FIC/BIC管线布局。SA1211单分子双靶siRNA用于慢乙肝治疗,于2025年10月获CDE临床默示许可,并在年底完成Pre-A轮融资。
结语
Biotech 用平台和速度加快临床前研发节奏,从肝内 GalNAc 到肝外多组织递送,从单靶点到双靶/多价结构,技术不断迭代。下一篇讲讲加速下场的大型药企通过自研转型或者并购,牢牢抓住慢病长期管理的下一代武器。
大家如果对某家公司的递送路线、化学修饰体系、双靶点设计或关键临床数据特别感兴趣,欢迎留言告诉罗哥——我会挑热度最高的,单独开一篇。
siRNA并购临床1期引进/卖出
100 项与 RN3161 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肥胖 | 临床2期 | 澳大利亚 | 2025-11-04 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
