预约演示
研究发现MAGI家族蛋白的PDZ-GK超结构域是一种新型磷酸化蛋白识别模块
2023-05-18
蛋白质的磷酸化/去磷酸化及其介导的蛋白复合物的组装/解离是细胞内信号转导的关键调控方式之一。磷酸化依赖的蛋白-蛋白相互作用通常是由磷酸化蛋白结合结构域介导。这些结构域包括14-3-3、FHA、MH2、
蛋白质的磷酸化/去磷酸化及其介导的蛋白复合物的组装/解离是细胞内信号转导的关键调控方式之一。磷酸化依赖的蛋白-蛋白相互作用通常是由磷酸化蛋白结合结构域介导。这些结构域包括14-3-3、FHA、MH2、WD40、BRCT、WW等,它们均能结合包含磷酸化丝氨酸/苏氨酸的特异性的多肽基序,介导高度特异的蛋白复合物的组装,在细胞动态行为中发挥重要作用。因此,发现新型磷酸化蛋白识别结构域并阐释其识别机制是细胞信号转导领域的基础科学问题。

Preview
来源: 生物谷
2023年5月11日,上海交通大学Bio-X研究院朱金伟课题组在Science Advances杂志在线发表题为Phosphorylation-dependent recognition of diverse protein targets by the cryptic GK domain of MAGI MAGUKs的研究论文,发现MAGI家族蛋白的PDZ-GK超结构域是一种新型磷酸化蛋白识别模块,并阐释了其识别磷酸化蛋白的分子机制。
Preview
来源: 生物谷
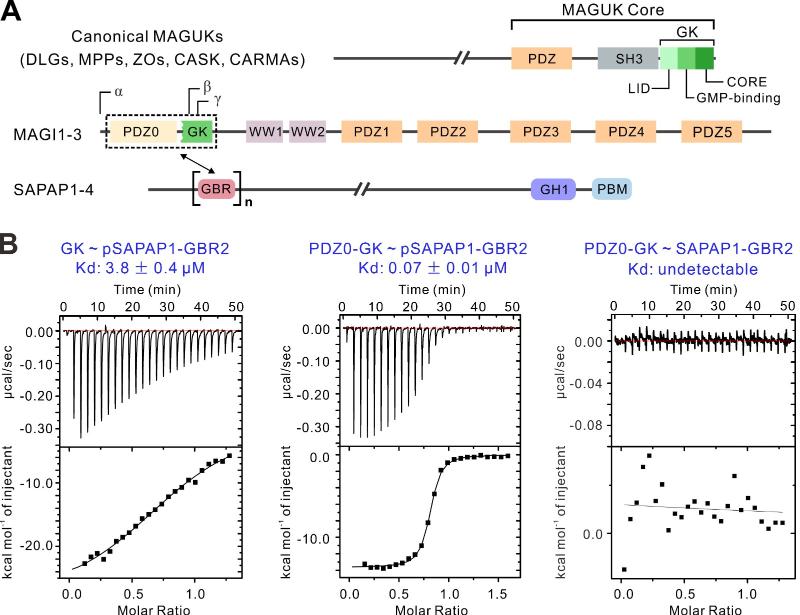
图1 MAGI2的PDZ0-GK超结构域识别磷酸化SAPAP多肽
Preview
来源: 生物谷
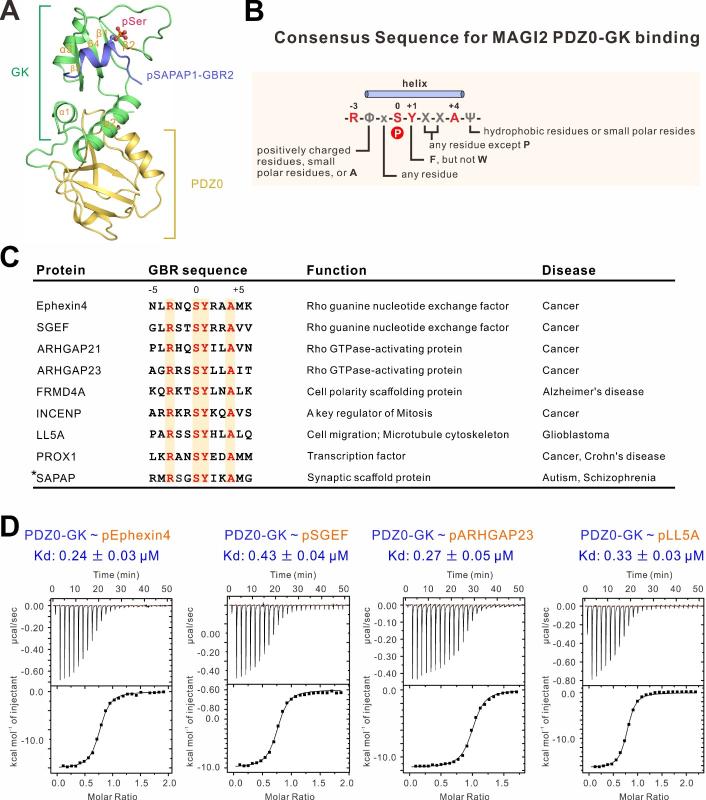
图2 基于PDZ0-GK识别磷酸化多肽的结构基础鉴定全新MAGI结合蛋白
本项工作发现,MAGI2的GK结构域与其相邻的PDZ0结构域存在相互作用,形成一个能够识别磷酸化蛋白的超结构域。与单独的GK结构域相比,PDZ0-GK超结构域结合磷酸化蛋白的结合解离强度(Kd)增强了50倍(图1)。课题组解析了PDZ0-GK与磷酸化SAPAP多肽的复合物三维结构,揭示了PDZ0-GK超结构域结合磷酸化蛋白的结构基础。基于生化和结构分析,课题组确定了PDZ0-GK识别磷酸化基序的一般规律:-R-Φ-x-S-Y-X-X-A-Ψ-(Φ: positively charged residues, small polar residues, or Ala; Ψ: hydrophobic residues or small polar residues; x: any residue; X: any residue except Pro)(图2)。进一步,课题组基于上述保守基序鉴定出全新的能够结合PDZ0-GK的蛋白质,包括Ephexin4、SGEF、ARHGAP21/23、LL5A等(图2)。
Preview
来源: 生物谷
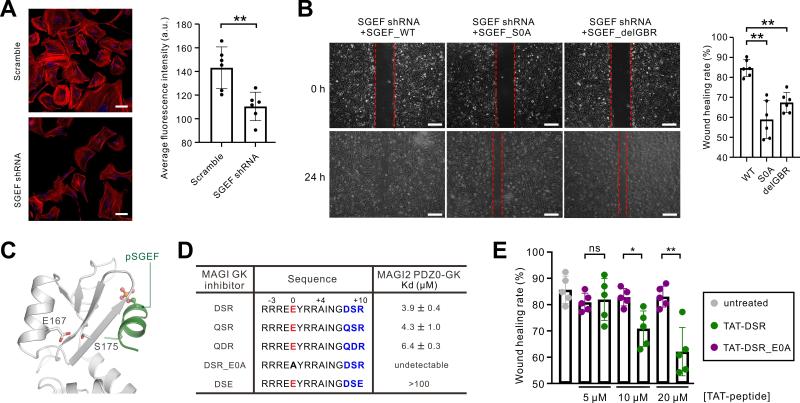
图3 磷酸化依赖的MAGI2-SGEF相互作用介导细胞迁移
该工作进一步解析了MAGI2-SGEF复合物和MAGI2-Ephexin4复合物的三维结构;揭示了PDZ0-GK识别磷酸化蛋白的普适性结构基础。课题组研究了MAGI2-SGEF复合物在细胞骨架动态调控和细胞运动中的全新功能。研究发现SGEF的下调明显减弱细胞骨架的组装,并导致细胞迁移速率下降;回补野生型SGEF能恢复细胞迁移能力,但回补SGEF突变体(S0A和delGBR突变体:两种突变体都破坏磷酸化依赖的MAGI2-SGEF相互作用)并不能显著恢复细胞迁移速率。上述结果提示,磷酸化依赖的MAGI2-SGEF相互作用在细胞骨架动态重组及细胞迁移过程中发挥作用。课题组进一步基于结构设计了抑制性多肽通过破坏内源性MAGI2-SGEF相互作用抑制细胞迁移(图3)。
上海交通大学Bio-X研究院博士后张猛、助理研究员林霖以及上海市第六人民医院肾内科曹爱丽副研究员为论文的共同第一作者。上海交通大学Bio-X研究院朱金伟研究员为论文的唯一通讯作者。本项工作受到南方科技大学生命科学学院讲席教授张明杰院士的大力支持。该工作得到国家重点研发计划、国家自然科学基金项目、科技部2030重大项目等基金资助。
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


