预约演示
百济神州PD-1抑制剂两项3期临床数据公布
ASCO会议临床3期临床结果
2023年欧洲肿瘤内科学会(ESMO)大会将于当地时间10月20日召开。根据百济神州近期发布的新闻稿,该公司多款在研产品的最新临床结果入选了本次会议。其中,PD-1抑制剂替雷利珠单抗分别治疗晚期胃或胃食管结合部(G/GEJ)腺癌和非小细胞肺癌(NSCLC)的两项3期研究入选年会最新突破摘要(Late Breaking Abstract,LBA)。下面,我们将结合ESMO已公布的摘要,分享这些临床研究的最新数据。

Preview
来源: 医药观澜
NSCLC新辅助治疗:MPR率提高至56.2%
RATIONALE 315试验是一项随机、双盲、安慰剂对照的3期临床研究,目的是评估可切除II-IIIA期NSCLC患者对新辅助替雷利珠单抗联合含铂双药化疗的病理学缓解。该试验主要研究终点为盲态独立中心(BICR)评估的无事件生存期(EFS)和独立中心病理实验室(BIPR)盲审主要病理缓解(MPR)。

Preview
来源: 医药观澜
2023年6月,百济神州已宣布RATIONALE 315试验达到其MPR的主要终点。替雷利珠单抗联合化疗作为新辅助治疗相较于化疗可显著提高其MPR。同时,试验达到其关键次要研究终点,观察到显著提高的病理完全缓解(pCR)。
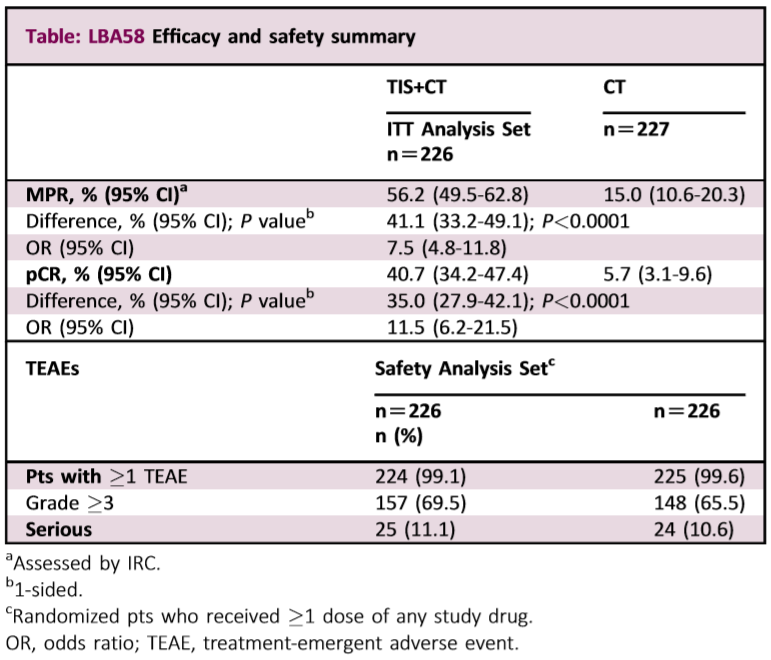
根据此次ESMO摘要公布的数据,截至2023年2月20日(中位随访:16.8个月),453名患者(试验组n=226;安慰剂组n=227)被随机分配到ITT人群中,并具有相似的基线特征。在接受新辅助治疗期治疗的452名(99.8%)患者中,421名(92.9%)完成了新辅助治疗;90例(19.9%)未接受手术。新辅助治疗期的疗效和安全性数据汇总见下表中。与化疗相比,替雷利珠单抗联合化疗作为新辅助治疗显著提高了MPR率(56.2% vs 15.0%)和pCR率(40.7% vs 5.7%)。替雷利珠单抗联合化疗不影响手术的可行性。
Preview
来源: 医药观澜
根据研究者得出的结论,与安慰剂联合化疗相比,替雷利珠单抗联合化疗在MPR和pCR率方面显示出具有临床意义和统计学意义的显著改善。替雷利珠单抗联合化疗的安全性与已知风险一致,并且在可切除的II-IIIA期NSCLC患者中是可控制的。
G/GEJ腺癌一线治疗:OS获显著改善
RATIONALE-305试验是一项随机、双盲、安慰剂对照、全球3期临床试验,目的是在晚期不可切除或转移性胃或胃食管结合部腺癌一线治疗中,探索替雷利珠单抗联合化疗(铂类和氟尿嘧啶类药物)对比安慰剂联合化疗的有效性和安全性。该试验主要终点是PD-L1阳性人群和意向治疗(ITT)人群的总生存期(OS)。

Preview
来源: 医药观澜
该试验的期中结果已在2023年美国临床肿瘤学会(ASCO)胃肠癌专题研讨会上口头报告。其中,试验组中位OS为17.2个月,与安慰剂组12.6个月相比,具有统计学显著性和临床意义的改善。联合疗法安全性特征可控,未发现新的安全性警示。
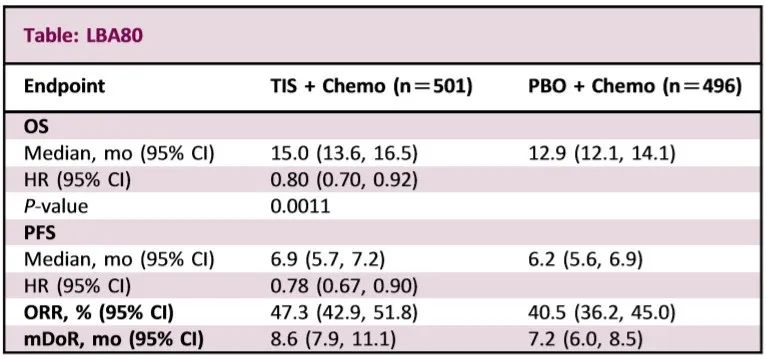
本次将在ESMO重磅公布的是RATIONALE-305试验的最终分析结果。数据截止时,997名患者被随机分配至试验组(n=501)或安慰剂组(n=496)。最小研究随访时间为24.6个月。与ITT人群中安慰剂组相比,试验组的OS显著改善,两组中位OS分别为15.0个月和12.9个月。其它主要疗效结果见下表。
Preview
来源: 医药观澜
安全性方面,试验组268例(53.8%)和安慰剂组246例(49.8%)发生3级治疗相关不良事件(TRAE),TRAE分别导致16.1%和8.1%的患者停药。
根据研究人员得出的结论,在ITT人群中,与安慰剂+化疗相比,替雷利珠单抗+化疗在OS方面表现出统计学意义和临床意义的改善,并且耐受性良好。这些数据支持替雷利珠单抗+化疗组合作为晚期G/GEJ患者的潜在一线治疗选择。
参考资料:[1]百济神州在2023年欧洲肿瘤内科学会上展示替雷利珠单抗作为单药和与管线资产联合用药的稳健的临床策略 . Retrieved Oct 16,2023, From https://mp.weixin.qq.com/s/uA0uT7yOo5bA6rZbvbVdaA
[2]ESMO摘要
内容来源于网络,如有侵权,请联系删除。
机构
-靶点
药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


