预约演示
重庆医科大学的研究者们揭示了一种很有前途的肝细胞癌治疗方法
2023-10-18
临床结果
自20世纪70年代以来,高果糖玉米糖浆(HFCS)的生产能力显著提高,并在食品和饮料中广泛使用,导致每日果糖消费量急剧增加。
自20世纪70年代以来,高果糖玉米糖浆(HFCS)的生产能力显著提高,并在食品和饮料中广泛使用,导致每日果糖消费量急剧增加。高果糖饮食与多种生活方式疾病的发病率不断上升有关,包括2型糖尿病、非酒精性脂肪肝(NAFLD)、,心血管疾病和癌症。
果糖代谢的关键酶,包括酮己糖激酶(KHK)和醛缩酶B(ALDOB),在HCC中显著下调,并与预后呈负相关,表明HCC中典型的果糖代谢降低。因此,果糖在HCC发展中作用的潜在机制尚不清楚,需要进一步探索。

Preview
来源: 生物谷
图片来源:https://doi.org/10.1016/j.cmet.2023.09.009
Preview
来源: 生物谷
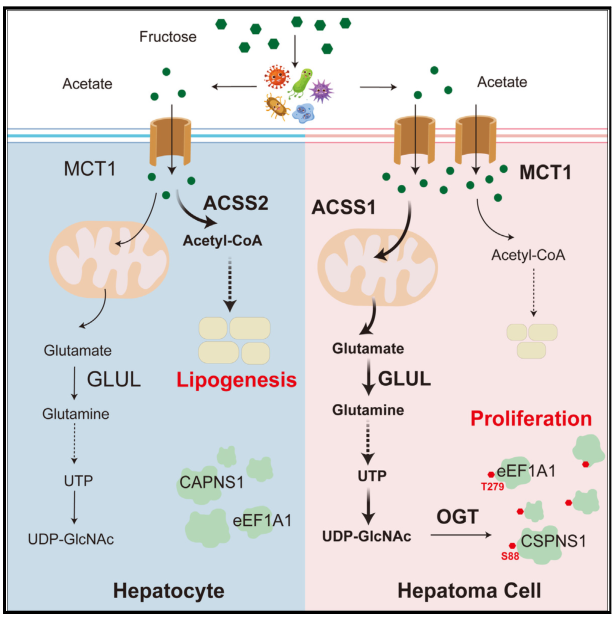
高膳食果糖通过微生物群衍生的乙酸盐增强O-GlcNA酰化作用促进肝细胞癌进展
图片来源:https://doi.org/10.1016/j.cmet.2023.09.009
参考文献
Peng Zhou et al. High dietary fructose promotes hepatocellular carcinoma progression by enhancing O-GlcNAcylation via microbiota-derived acetate Cell Metab. 2023 Sep 29:S1550-4131(23)00340-6. doi: 10.1016/j.cmet.2023.09.009.
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
药物
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。



