更新于:2024-05-01
Nimbus Lakshmi, Inc.
私营公司
私营公司
更新于:2024-05-01
概览
关联
100 项与 Nimbus Lakshmi, Inc. 相关的临床结果
登录后查看更多信息
0 项与 Nimbus Lakshmi, Inc. 相关的专利(医药)
登录后查看更多信息
2
项与 Nimbus Lakshmi, Inc. 相关的新闻(医药)2024-03-18
·医药观澜
▎药明康德内容团队编辑持续创新研发管线的拓展与深耕是生物医药公司永续发展的关键,也是整个行业不断进步、造福患者的源头。今日,行业媒体Endpoints News公布了2023年研发支出最高的全球前15名生物医药公司榜单。药明康德内容团队将为各位读者朋友们整理这些药企在2023年扩展研发管线所进行的布局,以进一步了解这些公司甚至是整个产业的潜在发展方向。点击文末“阅读原文/read more”,即可访问原始榜单页面。▲2023年研发投入最多TOP 15生物医药公司(图片来源:药明康德内容团队根据参考资料[1]制表)默沙东通过多项收购与授权交易,默沙东在2023年积极扩大其研发管线,研发支出占比大幅提升。例如,在去年10月,默沙东和第一三共(Daiichi Sankyo)就第一三共的三个抗体偶联药物(ADC)候选药物:patritumab deruxtecan(HER3-DXd)、ifinatamab deruxtecan(I-DXd)和raludotatug deruxtecan(R-DXd)达成了全球开发和商业化协议。今年1月,默沙东斥资近7亿元收购Harpoon Therapeutics,并获得一系列T细胞接合器在研疗法以扩展其肿瘤学研发管线。此外,默沙东在去年6月完成对Prometheus
Biosciences的收购,借此获得新的溃疡性结肠炎(UC)、克罗恩病(CD)和其他自身免疫性疾病候选药物来增强其免疫领域产品管线。2022年11月,默沙东通过收购Imago BioSciences扩大其血液学产品组合。罗氏罗氏在去年12月与与Carmot Therapeutics达成最终协议,将其多项GLP-1类研发管线纳入囊中,开发用以治疗肥胖与糖尿病患者。去年10月,罗氏也通过收购Telavant公司而获得其用以治疗炎症性肠病(IBD)的创新TL1A靶向抗体RVT-3101。罗氏公司的高层管理人员在今年2月份的投资者报告中提到,公司目前正进行着包含82种新分子实体(NME)在内的共146个临床项目,其中肿瘤学是其研发工作的核心领域,特别是在癌症免疫治疗方面。此外,该公司也着重于神经科学、眼科和免疫学领域管线的开发。参考阅读:罗氏2023年度财报公布,哪些创新疗法将在2024迎来里程碑?强生强生专注于肿瘤学、免疫学、心血管与视网膜相关疾病。今年1月,强生通过收购Ambrx Biopharma囊获多款临床期ADC。该公司在近期的报告中指出,该公司旗下的20款研发管线将在未来推动其5-7%的整体成长。强生旗下的几款疗法展现积极潜力,例如其与Protagonist Therapeutics共同开发的IL-23受体靶向口服多肽JNJ-2113,在日前公布的2b期试验中展现积极疗效。JNJ-2113在患有中度至重度斑块状银屑病(PsO)的成人患者中保持了52周的高皮肤病变清除率长达一年。诺华诺华在今年2月宣布将收购MorphoSys公司。这项收购将进一步扩展和补充诺华在肿瘤学领域的产品管线,同时也将加强诺华在血液学领域的全球布局。通过这项交易,诺华获得BET蛋白小分子抑制剂pelabresib(CPI-0610)与EZH1和EZH2蛋白双重抑制剂tulmimetostat(CPI-0209)两款处于临床阶段的在研疗法。此外,去年6月,诺华也与肾病精准药物开发公司Chinook
Therapeutics达成合并计划,通过此交易使得诺华获得该公司的主打项目atrasentan,这是一款处于3期临床阶段的内皮素受体拮抗剂,拟用于治疗IgA肾病和蛋白尿性肾小球疾病。阿斯利康阿斯利康积极开发多样化的研发管线。去年12月,该公司宣布收购Icosavax公司以获得其病毒样颗粒(VLP)平台技术,以及其主打项目IVX-A12。这是一种针对呼吸道合胞病毒(RSV)和人偏肺病毒(hMPV)的潜在"first-in-class"的VLP组合候选疫苗。阿斯利康也在GLP-1疗法领域进行布局。该公司在去年11月与诚益生物(Eccogene)达成独家协议,以潜在18.25亿美元的总额获得小分子GLP-1受体激动剂ECC5004(即AZD5004),用于包括肥胖症、2型糖尿病和其他合并症潜在治疗。在肿瘤领域方面,阿斯利康的PD-1和CTLA-4靶向双特异性抗体volrustomig也已进入3期试验阶段,用以治疗非小细胞肺癌(NSCLC)、宫颈癌、头颈部鳞状细胞癌(HNSCC)等患者。辉瑞辉瑞在去年3月斥资约430亿美元收购Seagen公司,获得其多款肿瘤学ADC药物,包含在去年12月获FDA完全批准用于一线治疗晚期或转移性尿路上皮癌患者的Nectin-4靶向ADC疗法Padcev(enfortumab
vedotin)。此外,辉瑞也投入于减重疗法的开发,其口服小分子GLP-1受体激动剂danuglipron的2b期临床试验结果显示,在2型糖尿病患者中,danuglipron显著降低患者的糖化血红蛋白(HbA1c)、空腹血糖水平和体重。接受最高剂量danuglipron治疗患者的HbA1c降低1.16个百分点,体重减少4.17公斤。参考阅读:8款以上潜在重磅疗法!辉瑞肿瘤学研发管线聚焦3大治疗模式(附PDF下载)礼来礼来重磅药物GIP/GLP-1受体双重激动剂tirzepatide的成功开发使其成为近年行业中令人瞩目的公司之一。去年11月,tirzepatide继获批用以改善成人2型糖尿病患者的血糖控制后(商品名:Mounjaro),再获美国FDA批准(商品名:Zepbound),用以使肥胖或超重成年患者减轻体重并保持体重稳定。而礼来的潜在重磅阿尔茨海默病疗法donanemab也正在接受FDA审评,有望于近日获得批准。此外,礼来也通过收购积极扩大其管线。例如,该公司在去年6月宣布与DICE Therapeutics达成收购协议,囊获其DELSCAPE小分子药物技术平台,并获得其用于治疗银屑病等免疫学慢性疾病的口服IL-17抑制剂DC-806与DC-853。百时美施贵宝百时美施贵宝积极拓展其现有管线范围。去年10月,该公司收购Mirati Therapeutics,囊获其KRAS
G12C抑制剂Krazati(adagrasib)以及数项肿瘤学临床管线。百时美施贵宝并在去年12月与Karuna
Therapeutics达成收购协议,获得其潜在“first-in-class”疗法KarXT(xanomeline-trospium),此药物用于治疗成人精神分裂症的新药申请已被美国FDA受理。此外,该公司也在同月与SystImmune公司达成研发合作协议,将共同开发潜在“first-in-class"的表皮生长因子受体和人表皮生长因子受体3(EGFR x HER3)靶向双特异性ADC疗法BL-B01D1,用于治疗肺癌、乳腺癌以及潜在其他癌症种类。GSKGSK的呼吸道合胞病毒(RSV)疫苗在美国、欧盟和日本均获得监管批准,成为首款获批上市的RSV疫苗。GSK持续在呼吸道疾病管线积极布局,该公司在去年4月通过收购BELLUS获得在研疗法camlipixant,这是一种具高度选择性的P2X3拮抗剂,为潜在“best-in-class”疗法,目前正处于临床3期试验,用于成人顽固性慢性咳嗽(RCC)患者的一线治疗。今年1月,GSK再次通过收购Aiolos Bio公司获得多项呼吸道疾病管线,包含一种即将进入2期临床阶段、用于治疗成人哮喘患者的长效抗胸腺基质淋巴细胞生成素(TSLP)单克隆抗体AIO-001。此外,GSK也在肿瘤领域中积极布局,去年12月,GSK通过与豪森药业(Hansoh Pharma)的合作,获得了B7-H3靶向ADC疗法HS-20093用以治疗卵巢/子宫内膜肿瘤在中国以外国家和地区的权益。艾伯维2023年5月,艾伯维和Genmab公司联合开发的双特异性抗体疗法Epkinly(epcoritamab)获美国FDA加速批准上市,用以治疗复发或难治性(R/R)弥漫性大B细胞淋巴瘤(DLBCL)。这是首款获FDA批准治疗DLBCL患者的双特异性抗体疗法。去年11月,艾伯维以总额达约101亿美元收购ImmunoGen公司,获得其叶酸受体α(FRα)靶向ADC疗法Elahere(mirvetuximab soravtansine)。艾伯维在隔月收购Cerevel Therapeutics以囊获其丰富的神经科学管线。Cerevel的管线由多项临床阶段和临床前候选药物组成,这些药物被开发用以治疗精神分裂症、帕金森病和情绪障碍等疾病。此次收购加强艾伯维在神经科学领域的布局。赛诺菲赛诺菲的研发重心之一是进一步扩展重磅药物Dupixent的适应症,Dupixent已经获批治疗9种不同的适应症。近日,Dupixent在治疗慢性阻塞性肺病(COPD)的两项3期临床试验中达到主要终点,有望为这款重磅药再添新的适应症。Dupixent之外,赛诺菲的研发管线中还有12款具有重磅药物潜力的新分子实体。今年1月,赛诺菲(Sanofi)和Inhibrx达成最终收购协议,获得其用以治疗α-1抗胰蛋白酶缺乏症(AATD)的潜在“best-in-class”在研疗法INBRX-101,进一步加强其在免疫介导呼吸疾病领域的研发部署。吉利德科学吉利德科学的战略转型正在逐渐成型,从2019年到2023年,临床管线数量增加了88%,有5个新药上市。肿瘤学在该公司的管线中也成了关键一环。靶向Trop-2的抗体偶联药物Trodelvy目前已获批用于3种不同癌症类型的治疗,还有超过30个活跃的临床试验,显示了治疗广泛癌症种类的潜力。吉利德科学预计在2024年将有至少5项3期临床试验的更新。肿瘤方向有Trodelvy的三个3期临床试验,HIV领域则有长效HIV药物lenacapavir的暴露后预防3期临床试验。武田武田与其合作伙伴和黄医药所共同开发的药物Fruzaqla(呋喹替尼/fruquintinib)在去年11月获得美国FDA的批准上市,治疗特定的结直肠癌患者。这个月初,美国FDA批准Eohilia(布地奈德口服混悬液)上市,治疗11岁以上嗜酸性粒细胞性食管炎(EoE)患者。新闻稿指出,这是FDA批准治疗EoE的首款口服疗法,有望解决患者的显著未竟需求。2022年12月,武田收购Nimbus的全资子公司Nimbus Lakshmi,并囊获及其酪氨酸激酶2(TYK2)抑制剂NDI-034858用以治疗包含银屑病在内的多种自身免疫性疾病。武田在去年初表示,该公司的10款后期开发项目有望在未来几年中递交新药上市申请或者扩展适应症。安进安进在2023年的关键成就包括通过并购Horizon以及ChemoCentryx建立罕见病方向的管线。此外,其潜在“first-in-class”在研减重疗法MariTide(AMG133)是一款抗体偶联多肽药物(antibody-peptide conjugate),在靶向胃抑制肽受体(GIPR)的单克隆抗体的特定位点上偶联了两个GLP-1类似物,在激活GLP-1受体的同时抑制GIPR。该疗法的1期临床试验结果显示,肥胖患者只需每月一针,接受高剂量MariTide治疗85天后,体重可降低14.5%(约26斤)。值得一提的是,这些患者在停药后150天,仍可维持体重降低11.2%。诺和诺德诺和诺德旗下重磅药物司美格鲁肽(semaglutide)分别在2017年与2021年获美国FDA批准上市,用于2型糖尿病患者的血糖控制(商品名:Ozempic)与治疗普通肥胖患者(商品名:Wegovy)。该药物的成功上市推动诺华诺德公司整体成长,该公司在近日召开的资本市场日(Capital Markets Day 2024)中也表示,未来将持续致力于糖尿病与减重领域的发展,除了开发下一代胰岛素与GLP-1类疗法外,也将着重改善这类患者的生活质量、降低其因相关共病死亡的风险。除了这两个领域,诺和诺德还将聚焦于以下不同领域疗法的开发,包含心血管疾病、罕见血液疾病、代谢功能障碍相关脂肪性肝炎(MASH)、罕见内分泌疾病、慢性肾病以及阿尔茨海默病与帕金森病。参考阅读:12周体重下降超13%!诺和诺德下一代减重疗法最新结果与公司开发战略公布参考资料:[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Mar 15, 2024, from https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d[2] Novo Nordisk to acquire Forma Therapeutics and expand presence in sickle cell disease and rare blood disorders. Retrieved September 1, 2022 from https://www.novonordisk.com/content/nncorp/global/en/news-and-media/news-and-ir-materials/news-details.html?id=132653[3]诺和诺德官网. From https://www.novonordisk.com/science-and-technology/r-d-pipeline.html本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转发授权请在「药明康德」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
并购抗体药物偶联物财报
2024-02-13
·医药观澜
银屑病(又称“牛皮癣”)是一种由T淋巴细胞介导的慢性炎症性疾病,影响着全球2-3%的人口。该病患者的皮肤细胞会过度生成,从而引起发炎、鳞屑性斑块,有时还伴有瘙痒或疼痛。这种疾病除了影响患者的身体健康以外,也成为了包括情绪健康、人际关系和日常生活的压力源。
好在近年来,针对银屑病的疗法有了一定的进展。其中,TH17/IL-17通路已被证明在银屑病的发病机制中扮演着重要的角色,而如IL-17、IL-23、肿瘤坏死因子(TNF)等炎症介质则成为了治疗该病的关键靶点。近期,《自然》杂志子刊Nature Reviews Drug Discovery发表了一篇文章,对银屑病治疗领域现有的治疗方法和新兴在研疗法进行了盘点。在今天的文章中,药明康德内容团队将与读者一道分享该领域的治疗、研发现状。
银屑病的治疗取决于疾病的类型、部位和程度。大多数局限性、斑块型银屑病可以使用局部治疗,而对于严重、广泛分布的银屑病,可以使用各种全身性的药物,具体可分为以下几类:
1. 局部治疗
在治疗轻度银屑病方面,局部糖皮质激素治疗是一种有效的治疗方法,但长期使用可能会导致疗效下降和皮肤萎缩。维生素D类似物钙泊三醇(calcipotriene)和维甲酸衍生物他扎罗汀(tazarotene)也是有效的局部疗法。
2. 全身性小分子疗法
免疫抑制剂甲氨蝶呤在银屑病患者,特别是伴有银屑病性关节炎的患者中疗效显著。其他免疫抑制剂如羟基脲、6-巯基鸟嘌呤、硫唑嘌呤和环孢霉素也时常被用于治疗银屑病。阿维A酸(acitretin)是一种口服维甲酸,也可用于治疗严重银屑病,但由于其致畸性作用,其使用受到限制。口服磷酸二酯酶4(PDE4)抑制剂阿普斯特(apremilast)也已获批用于治疗银屑病和银屑病性关节炎。
除上述疗法外,2022年9月,中重度银屑病口服疗法领域迎来了近10年来的首个创新——美国FDA批准了首款用于治疗中重度银屑病成人患者的TYK2抑制剂。
TYK2是JAK家族成员之一,是一种介导IL-23、IL-12和I型干扰素(IFN)信号转导的细胞内信号激酶。此前,靶向JAK家族成员的多种抑制剂已经获得批准,用于治疗炎症和免疫应答相关的多种疾病。但由于JAK家族成员可以介导多种细胞因子的信号通路,业界关注的一个问题是如何降低它们可能带来的副作用。
Deucravacitinib则很好地解决了这个难题。它是一款通过靶向结合假激酶(pseudokinase)蛋白域抑制激酶活性的别构抑制剂,能够与TYK2的调节性结构域相结合,将TYK2“锁定”在失活的状态,从而选择性抑制TYK2的活性,避免抑制JAK家族的其它蛋白JAK1-3。不仅如此,deucravacitinib在药物开发时还使用了氘代手段来增强化合物的稳定性。
在支持其上市的两项3期临床试验中,deucravacitinib使过半银屑病患者的皮肤症状几乎完全清除,而且这一比例随着治疗的持续进一步提高。此外,deucravacitinib的疗效持久,超过80%的患者在接受治疗52周后仍然能够维持症状缓解状态。目前,该疗法在欧盟和中国也已获批。
3. 靶向促炎细胞因子的生物制品
在过去的二十年中,靶向促炎细胞因子的生物制剂已成为中度至重度斑块型银屑病的重要治疗选择。从2004年开始,第一批用于治疗银屑病的生物制品是靶向TNF的单克隆抗体,包括依那西普(etanercept)、英夫利昔单抗(infliximab)和阿达木单抗(adalimumab)。随后,靶向T17/IL-17通路、IL-17家族或其受体,以及IL-23的单克隆抗体开始涌现并先后获批上市,包括ustekinumab、secukinumab、ixekizumab、brodalumab、risankizumab,、tildrakizumab、guselkumab等等。
2021年9月,一款与众不同的的IL-17靶向单克隆抗体bimekizumab在欧盟和英国获批上市了,随后于2023年10月在美国获批。这款单克隆抗体的特殊之处在于它能够同时抑制IL-17A和IL-17F这两种细胞因子,它也是全球首款获得批准用于治疗银屑病的IL-17A/IL-17F抑制剂。
IL-17A与IL-17F具有大于50%的结构同源性和重叠的生物学功能,它们在多种发炎的人体组织中均上调,并与其他促炎细胞因子,例如TNF协同作用,放大炎症反应。同时结合这两种细胞因子,阻止它们与细胞表面表达的IL-17受体相互作用,让bimekizumab能更好地发挥抗炎症的功能。
在支持其上市的三项3期临床试验中,接受bimekizumab治疗的患者在皮肤症状清除(PASI 90和IGA 0/1)方面的改善优于常见的获批银屑病疗法。不仅如此,bimekizumab的疗效也十分持久。在这些研究中,患者在接受治疗后第16周时获得的临床缓解可以维持长达一年。
目前,用于治疗银屑病的在研疗法依然围绕着PDE4、IL-17、IL-23、TYK2、JAK1等经过验证的靶点进行开发。这其中,进展较快的为靶向JAK家族成员的疗法。下面,我们将对其中一些已有较多临床结果的在研疗法进行介绍。
TAK-279是由Nimbus的全资子公司Nimbus Lakshmi开发的一种高选择性、口服别构TYK2抑制剂,正在被评估用于治疗多种自身免疫性疾病。2022年12月,武田以40亿美元的预付款和20亿美元的商业里程碑付款达成了对Nimbus Lakshmi公司及其TYK2抑制剂TAK-279(此前被称为NDI-034858)的收购。在临床前研究中,TAK-279表现出优异的功能选择性和广泛的治疗范围。在1期临床研究中,TAK-279显示出良好的耐受性、探索性临床活性的剂量依赖性趋势、以及支持每天一次固体口服用药的药代动力学特征。
2023年3月,武田公布了TAK-279在中重度斑块状银屑病患者中的2b期临床试验的积极结果。该研究达到其主要和次要终点,在12周时,与安慰剂组相比,5 mg、15 mg和30 mg TAK-279给药组中达到银屑病皮损面积和严重程度指数(PASI)降低75%、90%和100%的患者比例更高,并具有统计学意义。2023年9月,武田公布了TAK-279用于治疗活动性银屑病关节炎患者的2b期试验的积极结果。分析显示,该试验达到主要终点,与安慰剂相比,有较高比例接受每日一次TAK-279治疗的患者在第12周时其疾病体征和症状得到至少20%的改善。该疗法目前已进入3期临床阶段。
DC-806是礼来(Eli Lilly and Company)通过收购DICE Therapeutics公司获得的一款口服IL-17抑制剂。2022年10月,DICE Therapeutics公布了DC-806用于治疗银屑病的1期临床试验的积极结果。结果显示,治疗4周后,DC-806高剂量组的PASI比基线时减少的平均百分比为43.7%,而安慰剂组为13.3%。
基于这些积极结果,DC-806目前已推进到2期临床阶段,进一步检验其用于治疗银屑病和其它自身免疫性和炎症疾病的疗效。与DC-806相比,该公司的一款口服IL-17抑制剂DC-853具有更好的效力和代谢稳定性,目前正在1期临床试验中接受检验。
JNJ-2113是强生旗下杨森公司(Janssen Biotech)与Protagonist Therapeutics合作开发的针对IL-23受体的拮抗多肽,不仅能通过口服吸收,也能高亲和力地结合IL-23R。IL-23/IL-23R信号通路在免疫介导的炎症性疾病,包括银屑病的发病机制中起关键作用。JNJ-2113能选择性地有力阻止IL-23的信号通路和下游炎症细胞因子的产生。
2023年7月,两家公司共同宣布JNJ-2113在一项针对中度至重度斑块状银屑病成年患者的2b期临床试验中达到了所有主要和次要疗效终点。在第16周时,接受JNJ-2113治疗的患者中,达到PASI 75(主要终点)以及PASI 90和PASI 100的患者比例均超过安慰剂组。这些研究结果支持其进入3期临床开发。
Orismilast是由Union Therapeutics公司开发的下一代高效PDE4抑制剂。在一项2a期研究中,使用orismilast的即时释放制剂在第16周相较于安慰剂显著改善了患者的PASI评分。在健康受试者中,orismilast的改良释放制剂与即时释放制剂具有类似的药代动力学特性,但在胃肠道上的副作用更少。因此,该公司决定随后的开发将基于改良释放制剂。
2023年,Union Therapeutics公司报告了orismilast的2b期临床试验结果。在第16周时,40-49%接受orismilast治疗的患者达到了PASI 75,而接受安慰剂治疗的患者仅有17%达到了这一指标。该研究中未发现新的安全信号,证实了PDE4类药物具有良好的安全性。
ME3183是Meiji Seika Pharma公司发现的一种口服高活性、选择性PDE4抑制剂。在临床前研究中,该候选疗法对TNF-α信号的抑制效果比现有的口服型银屑病PDE4抑制剂高出约30倍,展现出更强的抗炎效果。同时,ME3183在大脑中的分布水平足够低。
2023年8月,该公司宣布,在美国和加拿大进行的针对中重度斑块状银屑病患者的2期临床试验中,ME3183达到了基于PASI-75的主要终点。与安慰剂组相比,ME3183治疗组的PASI-75改善比例明显更高。此外,接受ME3183治疗的患者在用药早期PASI即有所改善。研究还表明,ME3183的安全和耐受性良好。
在无数科学家和新药研发人员的共同持续努力下,我们在短短二十年多间就见证了银屑病治疗领域的重要进展。期待在不久的将来,目前的在研疗法能尽快取得更多积极结果,也希望看到更多创新机制疗法和有效治疗靶点的涌现,为此类患者提供更广阔的治疗选择空间。
参考资料:
[1] The pipeline and market for psoriasis drugs. Nature Reviews Drug Discovery. DOI: https://doi.org/10.1038/d41573-024-00018-2
[2] Bimekizumab Overview. Retrieved September 6, 2021, from https://www.creativebiolabs.net/bimekizumab-overview.htm
内容来源于网络,如有侵权,请联系删除。

免疫疗法临床研究
100 项与 Nimbus Lakshmi, Inc. 相关的药物交易
登录后查看更多信息
100 项与 Nimbus Lakshmi, Inc. 相关的转化医学
登录后查看更多信息
管线布局
2024年05月09日管线快照
无数据报导
登录后保持更新
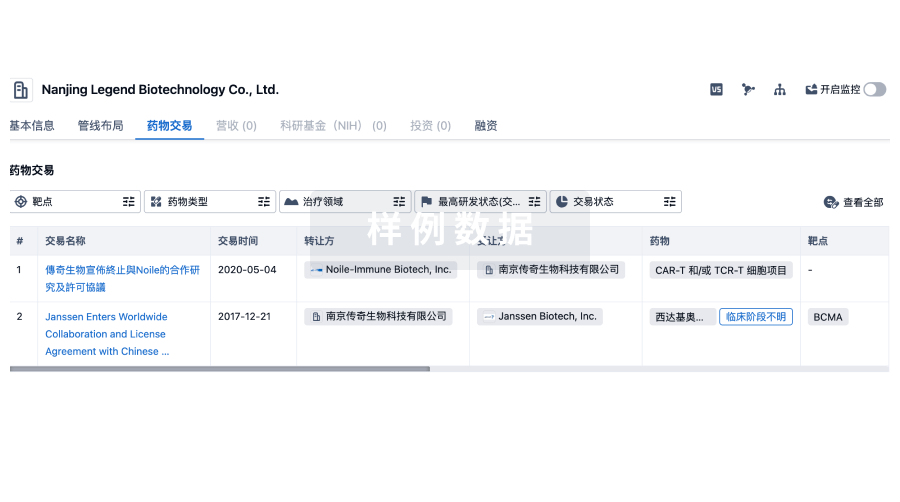
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
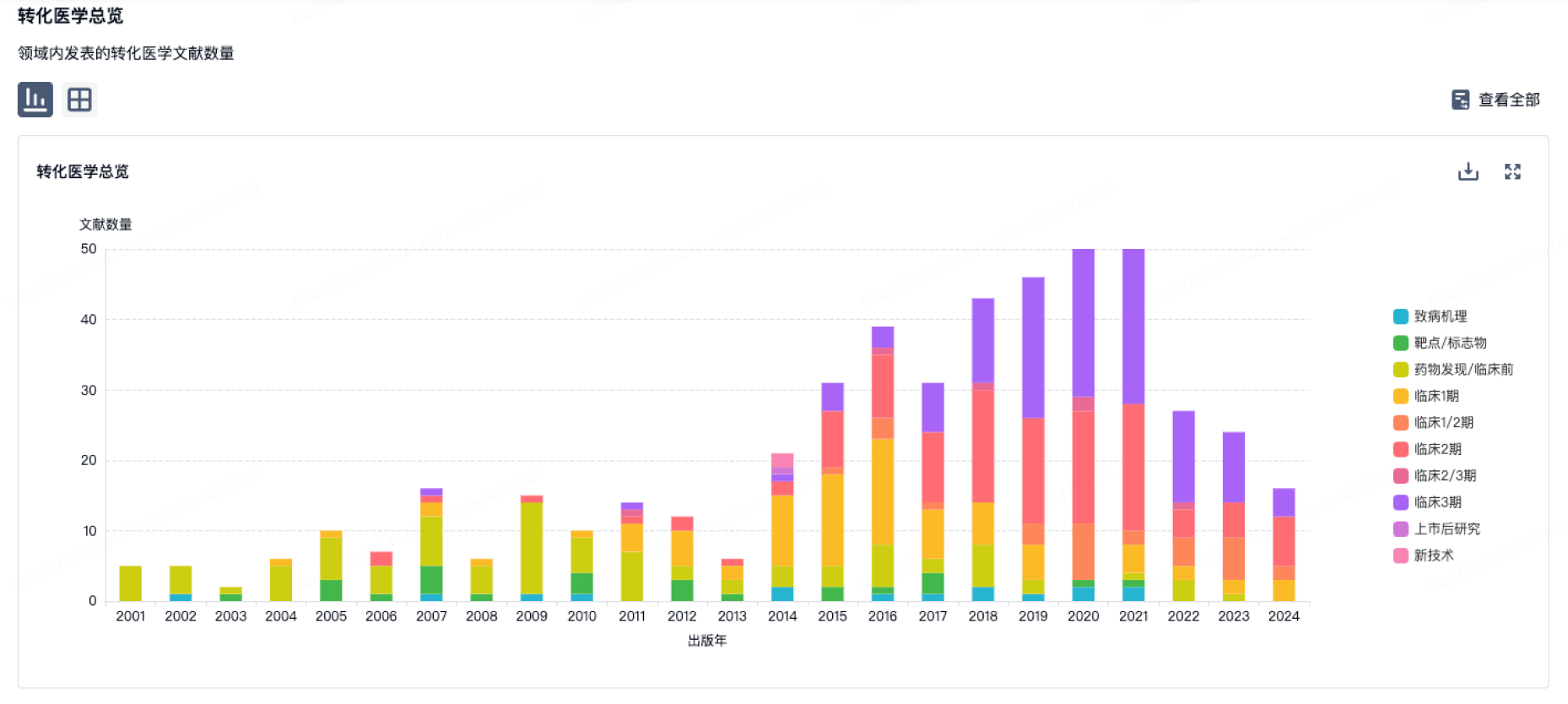
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
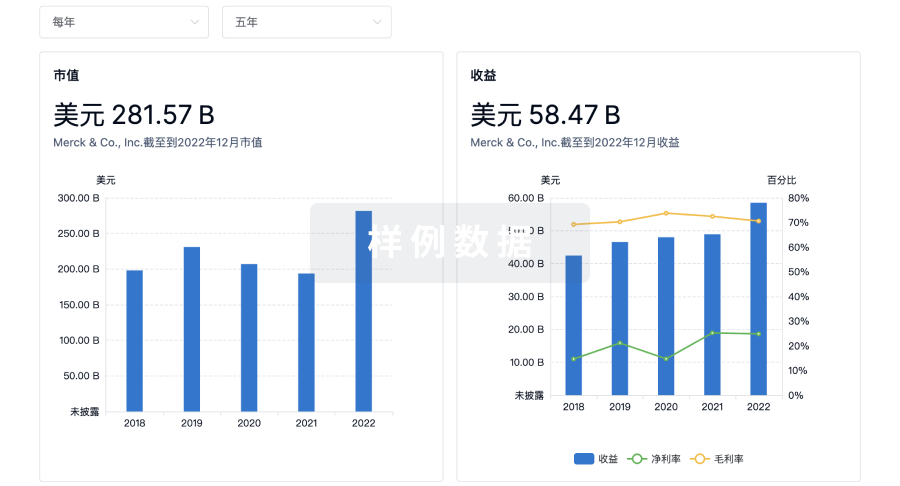
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
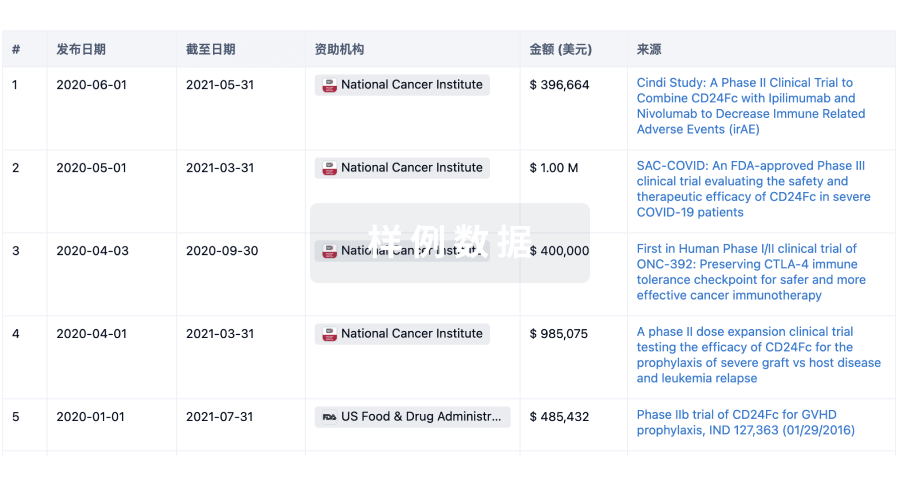
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
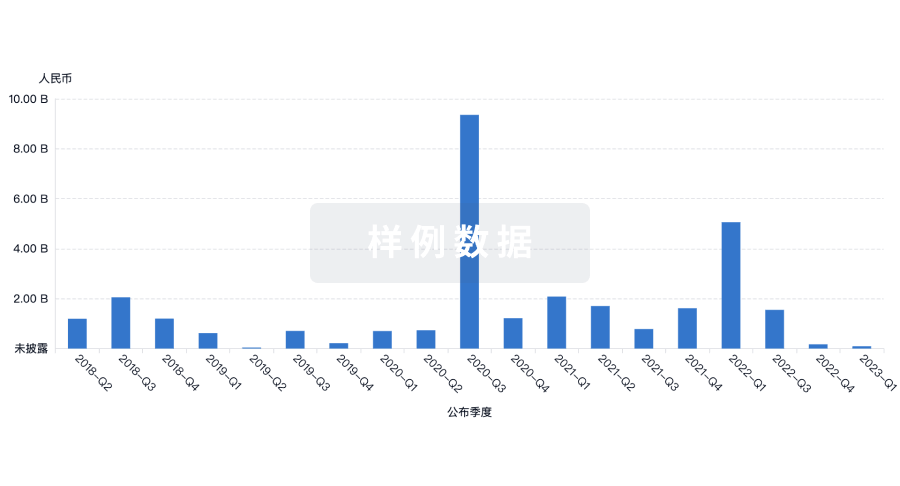
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
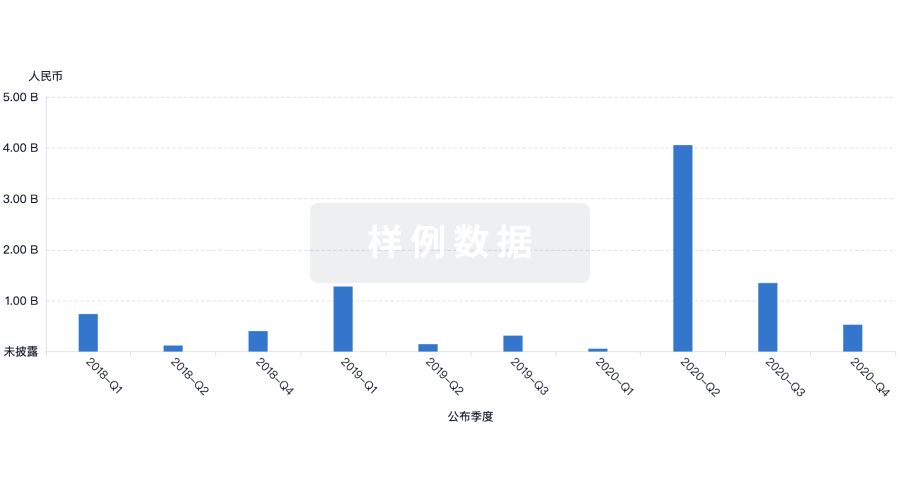
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用