更新于:2023-04-22

Foresite, Inc.
更新于:2023-04-22
概览
关联
100 项与 Foresite, Inc. 相关的临床结果
登录后查看更多信息
0 项与 Foresite, Inc. 相关的专利(医药)
登录后查看更多信息
103
项与 Foresite, Inc. 相关的新闻(医药)2023-01-05
·生物谷
根据医药魔方Pharma Invest数据库,2022年(截至12月22日)细胞疗法领域投融资事件数超88起(不含战略投资/并购/增发),融资总额超28亿美元
根据医药魔方Pharma Invest数据库,2022年(截至12月22日)细胞疗法领域投融资事件数超88起(不含战略投资/并购/增发),融资总额超28亿美元,与去年类似,主要集中在T细胞疗法(CAR-T、TCR-T、TIL)、干细胞疗法和NK细胞疗法方向。本文将按照融资金额,盘点今年细胞疗法领域的融资TOP10,以供参考。相较于去年,今年上榜的企业又是一波自带“独家秘诀”的新面孔。
融资轮次:B轮(9月6日)
投资机构:Softbank Vision Fund 2、BMS、Byers Capital等
公司官网:www.arsenalbio.com
Arsenal Biosciences成立于2019年,专注于整合基于CRISPR的基因编辑、规模化高通量靶点识别、合成生物学和机器学习等技术,以推进免疫细胞疗法的发现和开发新范式。该公司正在构建行业中最大型的治疗增强整合回路文库,利用逻辑门控改善肿瘤靶向,并且通过合成生物学让CAR-T疗法具有行使多种药物功能的潜力。
结合2019年10月完成的8500万美元A轮融资,Arsenal目前累计融资金额超3亿美元。此外,今年其与跨国制药巨头也发起了两项合作:1月,Arsenal宣布扩大与百时美施贵宝(BMS)的战略合作,以发现和推进用于治疗实体瘤的T细胞疗法;9月,Arsenal与罗氏旗下基因泰克达成7000万美元合作协议, 运用Arsenal专有科技进行高通量筛选与T细胞工程化,以识别T细胞类疗法成功的关键枢纽,开发未来实体瘤疗法。
公司联合创始人之一,加州大学旧金山分校的Kole Roybal教授,凭借其开发的全新T细胞免疫疗法成为2018年首届Sartorius & Science Prize for Regenerative Medicine & Cell Therapy大奖得主。2021年其在Science Translational Medicine发表的几篇论文指出,名为synNotch的调控系统能够提高CAR-T细胞靶向特异性,提高细胞疗法的持久性。
值得一提的是,Arsenal也上榜了由生物医药行业知名媒体网站BioSpace评选的2021年度新一代(NextGen)生物新锐公司。入选公司皆在近几年成立,BioSpace通过对公司资本助力、合作、研发管线、成长潜力以及创新方面进行综合评估。Arsenal的入选也体现其短短几年内对业界产生了重大影响。
融资金额:1.75亿美元
融资轮次:A轮(3月22日)
投资机构:Vida Ventures、Leaps by Bayer、Humboldt Fund、Fred Hutchinson Cancer Research Center等
公司官网:https://www.affinittx.com/
Affini-T Therapeutics是一家专注于T细胞免疫疗法的初创公司,成立于2021年,总部位于波士顿。公司致力于通过调节免疫系统来靶向致癌驱动突变,为难治性实体瘤患者开发可能改善生活的药物。3月22日,Affini-T 完成1.75亿美金的初始融资,用于发展其药物发现平台,以及支持多个药物进入临床试验,同时寻求其他技术以加强其细胞治疗平台等。
Affini-T的基础细胞疗法平台建立在创始团队开创性工作的基础上,旨在利用T细胞受体(TCR)发现引擎和一套合成生物学组件,开发靶向KRAS和p53等致癌驱动突变的潜在best-in-class疗法。
具体来说,Affini-T的团队利用先进的合成生物学和基因编辑技术,开创性地设计TCR-T细胞疗法以靶向致癌驱动突变。公司的TCR发现平台是一个强大的引擎,可用于识别罕见的高亲和力TCRs,在实体瘤中释放免疫应答。此外,Affini-T利用专有的合成生物学开关受体来重编程免疫细胞,以克服肿瘤微环境。
Affini-T的技术通过协调CD4/CD8的协同反应,引发更深入和显著的抗肿瘤效应。(来源:Affini-T)
Affini-T的创始团队及科学顾问委员会阵容豪华,包括Fred Hutchinson癌症研究中心免疫学负责人、癌症免疫治疗专家Phil Greenberg博士,癌症免疫疗法先驱、诺贝尔生理学或医学奖得主Jim Allison教授,知名癌症免疫疗法转化科学家Pam Sharma教授等。
融资金额:1.475亿美元
融资轮次:B轮(5月9日)
投资机构:谷歌、LYFE Capital、Revelation Partners、Alexandria Venture Investments和ARCH Venture Partners 等
公司官网:http://www.aspenneuroscience.com
5月9日,专注于开发自体细胞疗法的Aspen Neuroscience宣布完成1.475亿美元的B轮融资。该公司由Jeanne Loring博士在2018年创立,曾于2019完成650万美元的种子轮融资,并在2020年完成7000万美元的A轮融资。随着公司项目的推进,Aspen所获融资金额持续良性增长,截止目前,它的累计融资总额已达2.24亿美元。
体细胞重编程技术(来源:Aspen官网)
事实上,早在第一种人源多能干细胞,也即人胚胎干细胞系被建立的时候,研究人员就已经萌发出替代疗法的设想了。然而胚胎干细胞替代属于同种异体疗法,在治疗过程中需要持续免疫抑制,患者需要承担相应的副作用。与之相比,Aspen使用了自体细胞诱导iPSC并进行再分化的方法,不再产生免疫排斥效应,可以避免同种异体疗法的各种限制。在考虑了成本效益的情况下,这种方法能为患者带来更多的选择。
Aspen对外披露了两条管线,一个是针对散发性帕金森病的自体神经元替代疗法(ANPD001),另一条管线则针对了一种会增加帕金森病风险的遗传变异,是进行基因校正的自体神经元替代疗法(ANPD002)。4月,Aspen宣布开始ANPD001临床试验患者的筛选研究,标志着开启了IND申请的第一步。
融资轮次:IPO(2月8日)
公司官网:http://www.arcellx.com/
2月8日,临床阶段生物技术公司Arcellx宣布完成IPO,此次发行的总收益为1.423亿美元。所获资金将用于推动其主打CAR-T疗法(CART-ddBCMA)进入关键性临床试验,治疗复发/难治性多发性骨髓瘤(r/r MM),以及推动其“可控”CAR-T在研疗法进入临床开发阶段。CART-ddBCMA已获FDA授予的快速通道资格、先进再生医学疗法认定,和孤儿药资格。
总部位于美国马里兰州的Arcellx致力于开发更安全、更有效、更广泛的创新免疫疗法,以治疗癌症和其它无法治愈的疾病。该公司此前已完成8500万美元B轮融资(2019年)和1.15亿美元C轮融资(2021年)。
鉴于现有的细胞治疗方案大多使用基于生物的单链可变片段(scFv)结合域,往往只对有限的部分患者有益,还常常导致高毒性,并且在可治疗适应症中的适用性狭窄。Arcellx通过设计一类新的D-Domain驱动的自体和同种异体CAR-T细胞来克服这些限制,包括经典的单次输注CAR-T(称为ddCARs)和可剂量控制的通用型CAR-T(称为ARC-SparX)。
D-Domain是一种小型、稳定、全合成的接合剂,具有疏水核。当用于CARs时,其独特的结构可能实现更高的转导效率、更高细胞表面表达和更低的强直信号传导,其设计目的是提高靶标特异性,同时增强结合亲和力。D-Domain的独特性允许生成专有靶标结合域的多样库,并作为Arcellx专有的ddCAR和ARC-SparX平台的基础。(来源:Arcellx招股书和官网)
公司最新动态显示,12月9日,Arcellx公布了CART-ddBCMA在r/r MM中的I期临床试验数据,患者ORR达到100%,38例可评估患者中27例(71%)达到CR或sCR,34例(89%)达到非常好的部分缓解(VGPR)以上的缓解。同一日,吉利德科学旗下Kite宣布与Arcellx达成总计超3亿美元的研发合作协议,将共同开发和商业化Arcellx的临床后期在研疗法CART-ddBCMA,用于治疗r/r MM患者。
融资金额:1.3亿美元
融资轮次:B轮(4月14日)
投资机构:ARCH Venture Partners、BMS、Atlas Venture、RA Capital Management和武田风险投资等。
公司官网:https://www.be.bio/
4月14日,工程化B细胞药物(BeCM)发现和开发的先驱Be Biopharma 宣布完成1.3亿美元的B轮融资,加上2020年完成的A轮融资,目前该公司的融资总额已超1.8亿美元。这些收益将推动Be Bio专有的自体和同种异体工程化B细胞医学(BeCM)平台的发展及其肿瘤和罕见疾病候选产品的IND申请。
Be Bio总部位于美国马萨诸塞州,由Longwood Fund 和B细胞工程化先驱 David Rawlings、 Richard James 创立于2020年10月。旨在利用B细胞丰富的生物学和内在的药物样特性,通过精确的工程设计来打造一种新的细胞疗法。目前,公司的研究重心聚焦于罕见疾病和肿瘤学,未来可能扩展到传染病、神经疾病和自身免疫性疾病。
B细胞是天然制药厂,能通过产生蛋白质来对抗疾病和维持健康。Be Bio通过改造这类细胞,使其能够在体内持久地产生治疗性蛋白,具有剂量滴定的潜力,并在需要时重新给药,无需毒性预处理。
简单来说,该公司技术平台首先利用精准基因编辑改造B细胞,在其基因组中的特定位置精准插入表达目标蛋白的基因。然后将这些B细胞扩增并分化成为分泌治疗性蛋白的浆细胞,最后将这些浆细胞输注到患者体内。在患者体内,浆细胞会迁移到骨髓中并且持续生产治疗性蛋白。
来源:Be Bio官网
浆细胞,也即终末分化的B细胞,已经进化到能够更容易地逃避免疫检测,此外它们天然地向骨髓输送和移植。这些特性驱动了强大的现货型药物开发潜力,而不需要其他类别的细胞药物所需的毒性预处理。
融资金额:1.26亿美元
融资轮次:A轮(6月9日)
投资机构:Polaris Partners 、Temasek、EDBI、Heliconia Capital等。
公司官网:https://www.tessacell.com/
总部位于新加坡的Tessa成立于2012年,是一家临床阶段的细胞治疗公司,致力于开发下一代血液恶性肿瘤和实体肿瘤的癌症治疗方法。
今年6月Tessa完成了1.26亿美元的A轮融资,并计划利用这笔资金推进公司自体CD30-CAR-T疗法(TT11)和同种异体CD30.CAREBVST疗法(TT11X)项目的临床试验进度。TT11已被FDA授予再生医学先进疗法(RMAT)资格,并获得欧洲药品管理局授予的优先药物资格(PRIME)。TT11X最近在2022年亚太细胞和基因治疗卓越典礼(ACGTEA)中上被评为“最有前途的现货型疗法”。
这项融资是Tessa近期发展的一个重要里程碑,基于其CAR-T疗法II期临床试验结果数据的积极表现。在此之前,Tessa还于2017年底和2018年4月完成由Temasek领投的总计1.3亿美元融资,这些资金主要用于建设该公司的病毒特异性T细胞(VST)平台和推进其临床试验。
来源:Tessa官网
VST 平台是Tessa的核心技术平台。VST是在病毒感染期间产生的高度特异性的T细胞。这些细胞具有识别和杀死感染细胞的能力,同时激活免疫系统的其他部分以进行协调反应。无任何形式基因修饰的同种异体VST在早期试验中显示出良好的安全性和有效性。与当前同种异体细胞疗法相关的移植物抗宿主疾病、宿主抗移植物反应和其他严重反应的风险较低。VST的这些特性使其可以在同种异体环境中广泛应用。迄今为止,Tessa已在III期临床试验中成功制造并交付了150多种VST疗法。
融资金额:1.2亿美元
融资轮次:-(4月12日)
投资机构:Deerfield Management、Flying L Partners、Falcon Vision、Alcon等 。
公司官网:www.aurionbiotech.com
4月12日,临床阶段的生物技术公司Aurion Biotech宣布完成1.2亿美元的融资,这笔资金将用于推进其继发于内皮功能障碍的角膜水肿细胞疗法项目。
Aurion 总部位于西雅图、波士顿和东京,旨在通过改变生活的再生疗法为数百万患者恢复视力。该公司的第一个候选药物就是治疗继发于内皮功能障碍的角膜水肿,它也是第一个经临床验证的角膜护理细胞疗法,于2020 年从日本京都府立医科大学(KPUM)的眼外科医生和研究科学家Shigeru Kinoshita 实验室获得的授权。
在日本早期临床研究以及随后的剂量范围和验证性临床试验成功地证明了这一领先候选产品的安全性、有效性和耐受性。患者在角膜健康的关键指标:视力、角膜内皮细胞密度和中央角膜厚度方面经历了显著而持久的改善。
Aurion管线情况(来源:公司官网)
Aurion团队正在准备向日本PMDA提交NDA;在美国,他们正准备提交一份IND以启动临床试验;在欧盟,他们正在制定其他临床开发计划。
融资金额:超1.2亿美元
融资轮次:B轮 (8月1日)
投资机构:启明创投、泉创资本、上海科创基金、健壹资本(原国药资本)、苏州基金、博荃资本等 。
公司官网:https://www.oricell.com/
原启生物成立于2015年,在2019年底获得启明创投近亿元的Pre-A轮独家投资后,作为生物创新药研发资产从原能细胞集团剥离,开始以创新型细胞治疗技术平台为核心,聚焦于肿瘤免疫治疗领域的产品开发。
今年8月1日,原启生物宣布完成总金额超过1.2亿美元的B轮融资,资金将主要用于推进公司十余条经过充分概念验证(POC)的肿瘤细胞治疗产品管线的开发和商业化进程,继续完善公司自主创新技术平台的建设,以及未来商业化生产基地的规划与建设。
原启生物CAR-T产品管线(来源:原启生物官网)
在产品研发进展方面,公司首个自主开发靶向GPC3治疗晚期肝癌的CAR-T产品(Ori-C101)的临床试验申请(IND)获得了国家食品药品监督管理局药品审评中心(CDE)的受理。在过往的临床研究中,Ori-C101已经在GPC3阳性晚期肝癌患者中表现出良好安全性和有效性。
原启生物开发的中国首款GPRC5D CAR-T产品OriCAR-017 用于治疗r/r MM,其研究者发起的I期临床试验(POLARIS)充分证实了该产品极大的开发前景。原启生物以口头报告形式分别在2022 ASCO、2022 EHA年会上公布了截止至2022年4月30日的临床结果。数据显示,包括5例既往BCMA CAR-T治疗失败的受试者在内的所有受试者,均获得100%客观缓解率(ORR)和100%微小残留病灶(MRD)阴性率,持续无进展,无需任何额外抗肿瘤治疗以及良好的安全性。目前,原启生物正加快推进其中美两地的注册及临床开发速度。
融资金额:1.11亿美元
融资轮次:B轮(1月20日)
投资机构:VenBio Partners、Foresite Capital、Decheng Capital、Novartis Venture Fund等 。
公司官网:https://immpact-bio.com/
1月20日, ImmPACT Bio宣布完成了1.11亿美元的B轮融资。融资所得将用于推动该公司基于逻辑门的CAR-T细胞平台的开发。
ImmPACT是一家临床阶段生物技术公司,其基于逻辑门的CAR-T平台解决了癌症治疗中的关键生物学挑战,如抗原逃逸、脱靶毒性和免疫抑制肿瘤微环境。该公司的技术基于加州大学洛杉矶分校(UCLA)的先驱科学家Yvonne Chen博士和Antoni Ribas博士以及MIGAL-Galilee研究所Gideon Gross博士的工作。
包括B轮融资在内,ImmPACT迄今已筹集了约1.29亿美元(2020年8月完成由Johnson & Johnson Innovation、Takeda Ventures等支持的1800万美元A轮融资),其中大部分将用于资助正在进行的临床试验,并在洛杉矶West Hills建立一个制造工厂。
目前公司管线布局涉及血液系统恶性肿瘤以及肺癌和脑胶质瘤。
ImmPACT在研产品管线 (来源:ImmPACT官网)
ImmPACT公司拥有3大关键平台:
1)对于血液系统恶性肿瘤,ImmPACT的领先项目是CD19-CD20双特异性“OR门”CAR-T,旨在解决抗原逃逸问题。
2)ImmPACT第二个平台的激活性/抑制性“NOT门”CAR组合可特异性区分肿瘤细胞和正常细胞。激活性CAR(aCAR)杀死肿瘤细胞,同时抑制性CAR(iCAR)保护正常细胞。该平台通过配对不同的激活性/抑制性组合,有可能为实体瘤治疗提供多种产品,并为新兴和有希望的癌症治疗领域提供多种机会。
3)该公司的第三个平台为TGF-β CAR,它可以模块化地配备肿瘤靶向结合域以生成双特异性“OR门”CAR,重新连接T细胞对TGF-β的应答,从而将这种强效免疫抑制细胞因子转化为T细胞刺激物。单链双特异性CAR在直接靶向肿瘤表面抗原的同时可转换TGF-β信号,使T细胞能够在高度免疫抑制的微环境中也能强有力地清除肿瘤细胞。
融资金额:1.02亿美元
融资轮次:A轮 (9月14日)
投资机构:辉瑞风投、拜耳、礼来、诺华、百时美施贵宝 。
公司官网:https://www.capstantx.com/
9月14日,Capstan Therapeutics 宣布完成1.02亿美元A轮融资, 以推进其体内原位CAR-T疗法走向临床 。2021年11月,该公司完成了6300万美元种子轮融资。
Capstan的科学创始人团队和科学顾问委员会成员大咖云集,创始团队包括 Carl June (CAR-T之父) , Drew Weissman (mRNA技术奠基人) , Jonathan Epstein (体内原位CAR-T技术发明人)等。
今年1月6日,Science杂志以封面文章的形式发表了Drew Weissman等人的研究成果。通过注射包含mRNA的CD5靶向脂质纳米颗粒(LNP),能够在小鼠体内完整地产生治疗性CAR-T细胞。对心脏疾病小鼠模型的分析表明,瞬时表达CAR的治疗方法能够成功减少纤维化以及恢复心脏功能,有效避免了体外编辑CAR-T细胞后回输到体内后CAR-T细胞长时间存在的安全性问题。这项成果不仅代表了CAR-T适应证拓展方面的重要突破,更是体内CAR-T疗法领域的一项里程碑进展。
实际上,Capstan的技术平台正是建立在这项研究的基础上,该公司的原位 CAR 技术有3个相互关联的部分组成——非病毒递送系统、细胞特异性靶向分子和针对疾病设计的有效载荷。基于上述平台,Capstan开发了两种方式治疗疾病。一是通过工程化免疫细胞,这是将mRNA编码的CAR递送至特定亚型的免疫细胞,使其表达可破坏病原细胞的抗原;第二种是将mRNA编码的基因编辑器递送给病原细胞,通过修饰细胞的DNA达到治疗疾病的目的。
辉瑞、拜耳 、诺华、礼来和百时美施贵宝这五大制药巨头的风险投资部门齐聚一堂,共同投资的这家生物技术初创公司未来发展值得期待。

免疫疗法细胞疗法并购基因疗法
2022-12-16
·美通社
上海
2022年12月16日
/美通社/ --
近日,经久生物宣布
,公司新一代FGFR抑制剂KIN-3248临床试验申请获得国家药品监督管理局药审中心(CDE)默示许可,拟在中国大陆地区开展临床研究。该研究为一项国际多中心的I期临床研究
,
2022年1月获得美国FDA批准,旨在评估KIN-3248在携带FGFR2/3基因改变晚期实体瘤中的疗效和安全性。
KIN-3248作为新一代不可逆小分子泛FGFR抑制剂,具有高度选择性、不可逆、强效等特点。KIN-3248计划开发用于治疗原发 FGFR2/3基因改变以及对FGFR2/3靶向治疗耐药的实体瘤的治疗。
FGFR是目前"泛瘤种治疗"聚焦的热门靶点之一,其拥有4个亚型(FGFR1/2/3/4),在肝内胆管癌、胃癌、尿路上皮癌、子宫内膜癌、乳腺癌等多种恶性肿瘤中均发现包括FGFR基因突变、融合和扩增等异常。在中国,约32%
[1]
、14%
[2]
、11%
[3]
的尿路上皮癌、肝内胆管癌、胃癌患者发现FGFR2/3基因存在异常。对于目前已经获批上市的FGFR激酶抑制剂来说,继发性耐药极大地限制了这类药物的临床获益,仍存在巨大的未被满足的临床需求,亟需能够克服FGFR靶向治疗耐药的新一代FGFR激酶抑制剂来改变这一现状。在非临床研究中,KIN-3248不仅证明了对携带原发性FGFR2/3基因改变的肿瘤具有显著的抗肿瘤活性效果,而且对于携带FGFR2/3继发性耐药突变的肿瘤同样具有显著的抗肿瘤活性,有望在未来成为Best-In-Class药物,为患者带去新的治疗希望。
经久生物首席执行官及执行董事田丰先生表示:"KIN-3248有望为携带FGFR基因改变的实体瘤患者带来实质性的临床获益;经久生物也将继续致力于探索更多肿瘤精准治疗方案,为解决广大肿瘤患者未被满足的临床需求提供更多可能。"
Reference
[1] Zhang R, et al. J Urol. 2021 Oct;206(4):873-884.
[2] Dong L, et al. Cancer Cell. 2022 Jan 10;40(1):70-87.e15.
[3] Gu W, et al. Am J Cancer Res. 2021 Aug 15;11(8):3893-3906.
关于经久生物
Kinnjiu Biopharma Inc.(经久生物)由Kinnate Biopharma Inc. (纳斯达克:KNTE),奥博 (Orbimed) 亚洲基金,奥博资本以及Foresite Capital于2021年共同投资设立,A轮融资投资额达3500万美元。经久生物获得独家许可负责Kinnate Biopharma Inc.的多项肿瘤药物在大中华地区的研发及商业化,同时经久生物也将对其他项目及第三方的药物进行开发。
公司官网:www.kinnjiu.com
临床1期临床2期
2022-12-15
2022年12月13日,武田宣布收购Nimbus旗下的TYK2抑制剂NDI-034858。据协议条款,武田将向Nimbus预付40亿美元,年度净销售额达40亿美元和50亿美元后,分别支付10亿美元里程碑付款,总金额最高达60亿美元。该交易预计将在2023年上半年完成。武田以如此高的代价拿下的这款药物,有何特别之处?NDI-034858主要用于治疗中度至重度斑块状银屑病患者(俗称牛皮癣)。11月30日,其IIb期研究也取得了阳性结果,达到了主要疗效终点。银屑病目前尚未有方法可以治愈,且该病对患者外貌有重大影响,需要长期服药缓解。国内治疗方法以小分子治疗方案为主,治疗效果与生物药相差甚远。据数据显示,国内银屑病存量患者超过390万,对应治疗存在巨大未满足需求,药物市场规模接近700亿。在全球范围内,银屑病领域也诞生了大量的重磅炸弹,包括:古塞奇尤单抗、司库奇尤单抗、乌司奴单抗、阿达木单抗等。而值得注意的是,首款获批上市BMS的TYK2单抗更是在其临床三期击败了银屑病重磅药阿普斯特,引发了学术界对该靶点的热烈关注。肿瘤领域即便市场广阔,但不应忽视的是,自免领域亦是一座闪闪发光的金矿。1、国内创新药企自免分子交易逐渐增加据美国自身免疫相关疾病协会(AARDA)的统计,目前已经发现100多种自身免疫性疾病,常见的有类风湿性关节炎、强直性脊柱炎、银屑病、克罗恩氏病、溃疡性结肠炎 、系统性红斑狼疮、狼疮性肾炎、支气管哮喘等。大多数自身免疫性疾病难以治愈,一旦患病,大多数患者需要长期甚至终身服药,这也是阿达木单抗长期位居“药王”的秘诀之一。并且,部分疾病 (如狼疮性肾炎) 病情凶险,严重影响患者生活质量,威胁患者生命安全。自身免疫性疾病已经成为除心血管疾病和癌症外第三大慢性病。另一面在于:国内药企将自免早期分子License out给海外厂商也越来越多。2021年3月,海思科将一款临床前的TYK2抑制剂授予Foresite Capital,获得首付款6000万美元及最高1.2亿美元的里程碑款。2022年9月,先声药业将一款临床前IL-2融合蛋白海外权益授予欧洲药企Almirall,总里程碑款高达4.92亿美元2、中美自免药物市场规模差异2020年,全球销售额TOP100药品的合计销售规模约3558亿美元,自身免疫及炎症药物位列第二(约940亿美元,占比26.4%),过去更是诞生了阿达木单抗(TNF-α)、乌司奴单抗(IL12/23)、依那西普(TNF-α)这些年销售额超过50亿美元的重磅单品。2019年数据显示:美国自免药物市场为749亿美元,中国为24亿美元,中国市场规模仅为美国3%。自身免疫性疾病临床发病率高,临床表现复杂,易误诊漏诊。从患者人数上分析,美国的自免疾病患者大约占总人口20%(约5000万人);而有不完全统计显示,中国自身免疫性疾病患者约有5000-6000万人,但国内实际患者数量可能远不止这个数。据药融云数据显示:2022年上半年医院TOP5治疗大类分别为抗肿瘤药和免疫机能调节药、消化系统与代谢药、血液和造血系统用药、系统用抗感染药、心血管系统用药,自身免疫性疾病用药排在前五名甚至前十名开外。无论是相对狭窄的市场规模,还是“药王”阿达木单抗销售不利,中国一度被业界认为是“自免药物黑洞”市场。什么原因造成了如此窘境?至少有两个方面的原因:风湿免疫科资源匮乏、药物价格过高。据中泰证券研报指出,国内的风湿免疫科起步较晚,20世纪80年代才开始建科,科室规模不一、很多挂靠在其他科室、例如血液病风湿科、肾病风湿科等,还有相当部分的风湿病医生在其他科室挂职。风湿免疫医生不足,造成很大量风湿病人被漏诊、误诊。相反欧美国家自免患者诊疗更为规范,有明确临床路径和指南,漏诊、误诊比例更低。阿达木单抗2010年国内获批上市,却一直被三生国建的益赛普凭借价格优势压着打,直到2019年才纳入医保。据医药地理统计数据显示,2020年、2021年阿达木单抗在PDB样本医院市场销售数据出现爆发式的增长。究其背后原因,答案是阿达木单抗降价83%进入医保,并且3家生物类似药跑步入场,促使了销量的暴涨。从下图各个近年新批的自免药物年治疗费用审视,大部分均价格不菲,由于要长时间乃至终生用药,依旧给患者带来不小的负担。3、国内有潜力的重磅单品● 康方生物 AK-101:一款靶向IL-12/IL-23的单抗,主要在研适应症包括银屑病和溃疡性结肠炎,目前进度最快的适应症为中重度银屑病。AK-101是和强生的乌司奴单抗(Stelara)同靶点的药物,乌司奴单抗在2009年获批,2019年全球销售额64亿美元,是2019年全球治疗自身免疫性疾病的第三大畅销药。而从康方目前已有的实验数据看,AK101显示出比Stelara疗效更优的潜力。而AK-101也是目前唯一处于临床阶段的靶向IL-12/IL-23的单抗药物,潜力巨大。● 康诺亚 CM310:CM310是首个国产、全球第二款IL-4Rα单抗,目前已公布治疗AD及鼻窦炎伴鼻息肉两个适应症的II期临床数据,安全性良好,疗效具备优于度普利尤单抗潜力。赛诺菲的度普利尤单抗已经成功验证IL-4Rα靶点在2型过敏性疾病中的市场空间及放量曲线,2017-2020年的销售收入分别为2亿、9亿、23亿、40亿美元。其在中国于2020年6月获批,当年在中国销量便有1370万美元。2021年3月,康诺亚将CM310不包括港澳台在内的中国地区针对呼吸系统疾病进行开发和商业化的权益授予石药集团。● 荣昌生物 泰它西普:泰它西普是继贝利木单抗后为数不多获批系统性红斑狼疮适应症的创新药物,于国内2021年3月获批,当年销售额为4730万元。除系统性红斑狼疮(SLE)以外,荣昌生物正在开展其他6种未被充分满足临床需求的难治性自免疾病的临床试验,包括IgA肾炎、重症肌无力、类风湿性关节炎、干燥综合症等。目前,泰它西普正在海外进行SLE、IgA肾炎的三期临床,同时在近期重症肌无力适应症获得了FDA授予的孤儿药资格,一旦海外临床中期数据优良,那么可以预见一个巨大的License out交易。...结语:随着国内药企License out频频、商业化进展加速消息日益密集,头部创新药企的春天,似乎已经越来越近了。相关阅读:19位行业专家,4场知识盛宴,抗体药物大规模高效生产系列网络研讨会盛大开启!
引进/卖出临床3期并购临床2期
100 项与 Foresite, Inc. 相关的药物交易
登录后查看更多信息
100 项与 Foresite, Inc. 相关的转化医学
登录后查看更多信息
管线布局
2024年05月07日管线快照
无数据报导
登录后保持更新
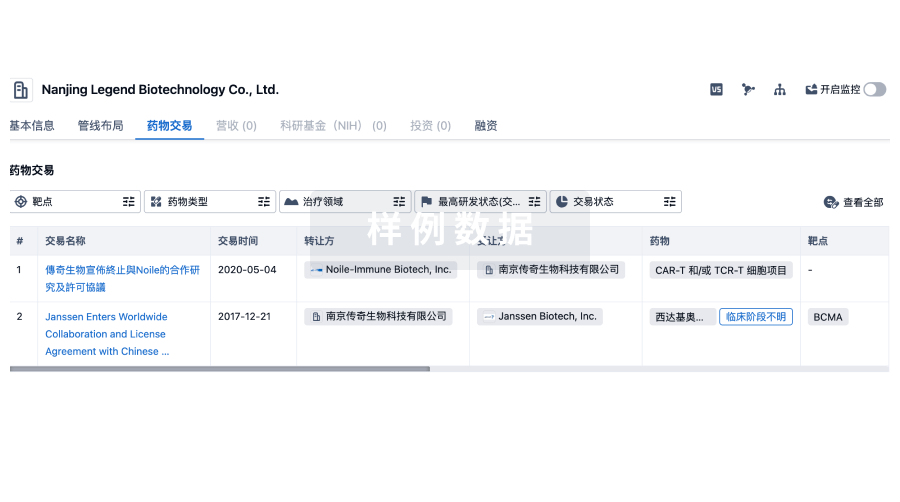
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
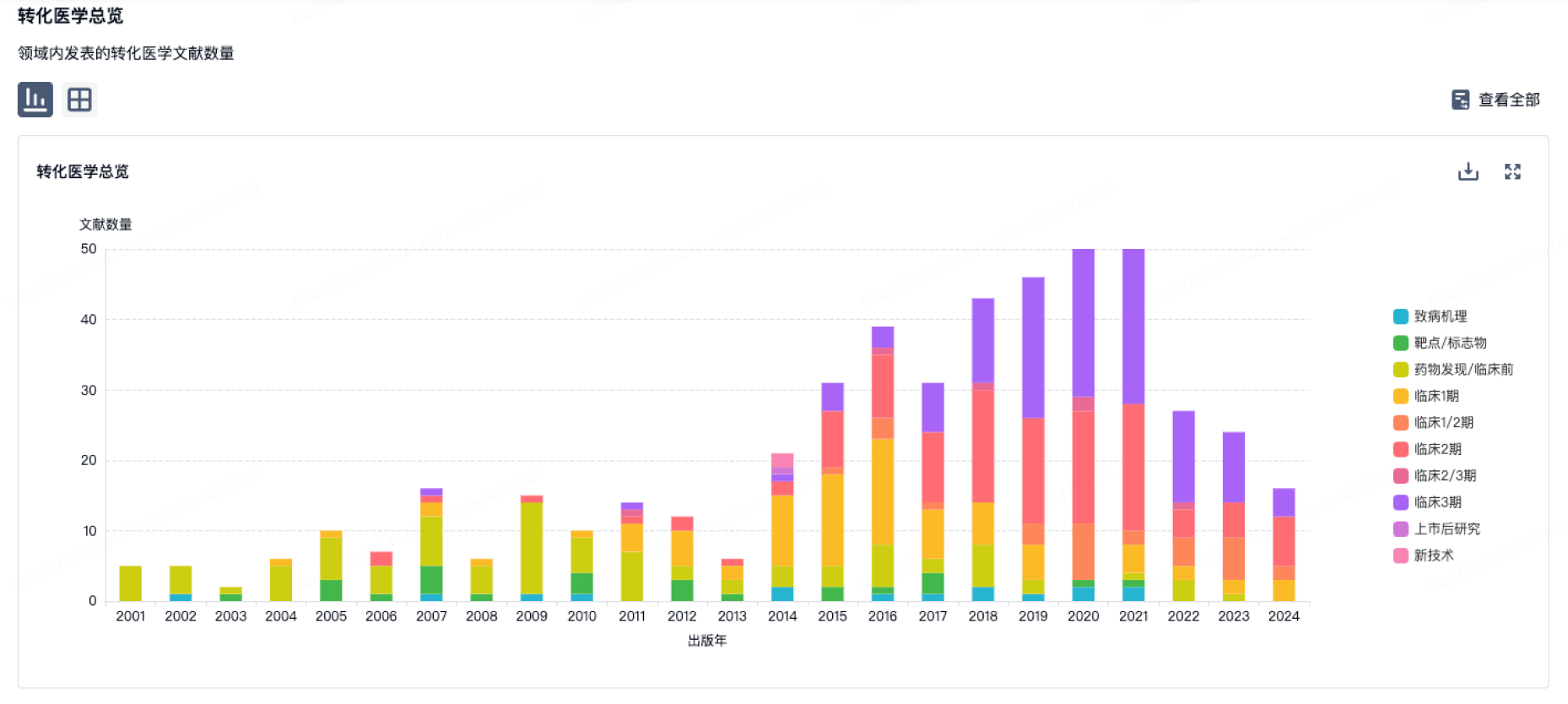
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
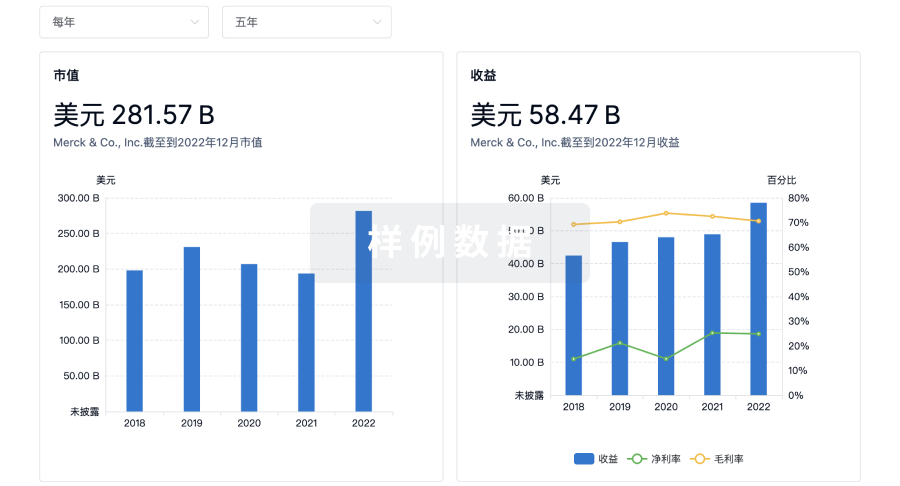
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
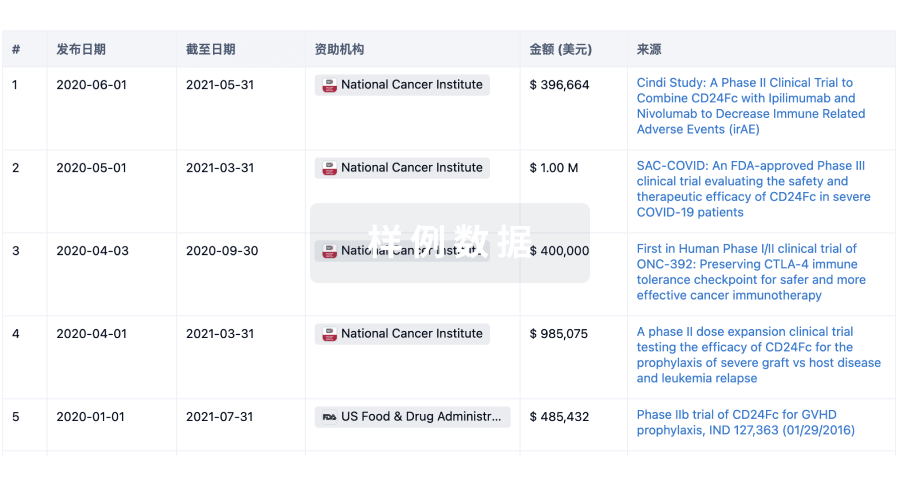
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
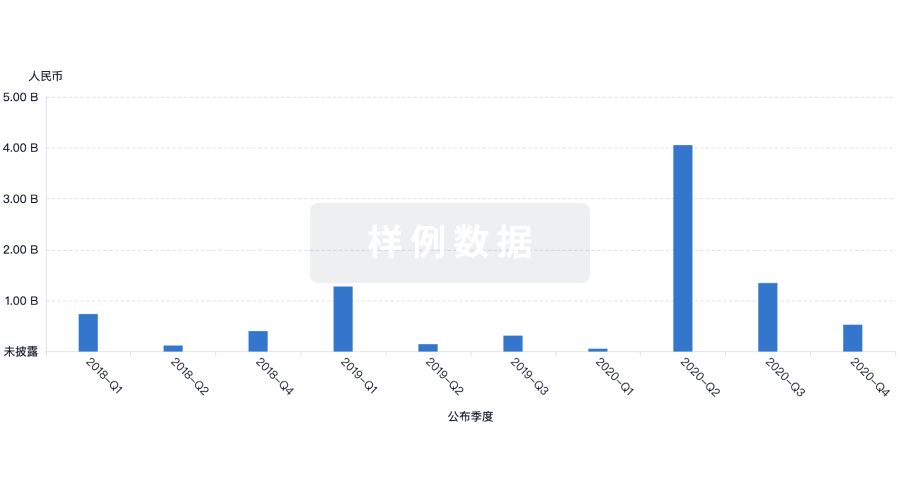
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
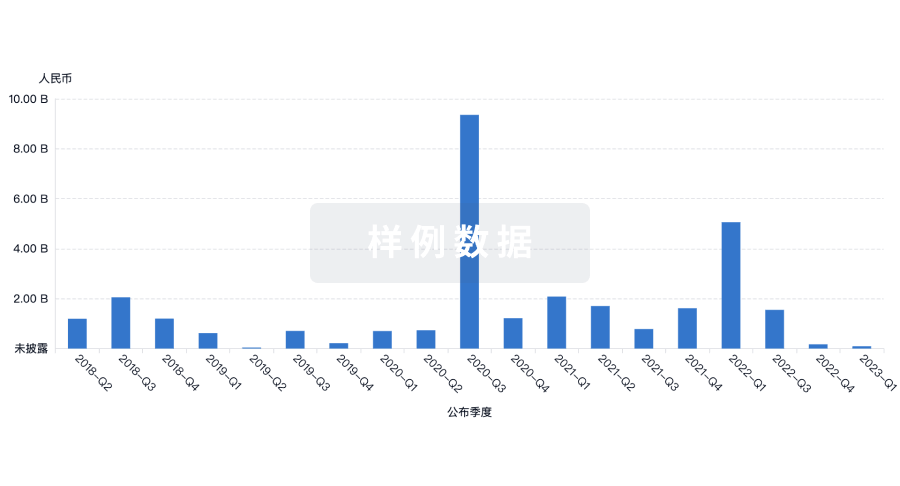
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用