预约演示
更新于:2026-05-09
Vesleteplirsen
更新于:2026-05-09
概要
基本信息
药物类型 ASO |
别名 Vesleteplirsen Hydrochloride、SRP 5051、SRP-5051 |
作用方式 调节剂 |
作用机制 DMD基因调节剂 |
在研适应症- |
非在研适应症 |
在研机构- |
权益机构- |
最高研发阶段终止临床2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
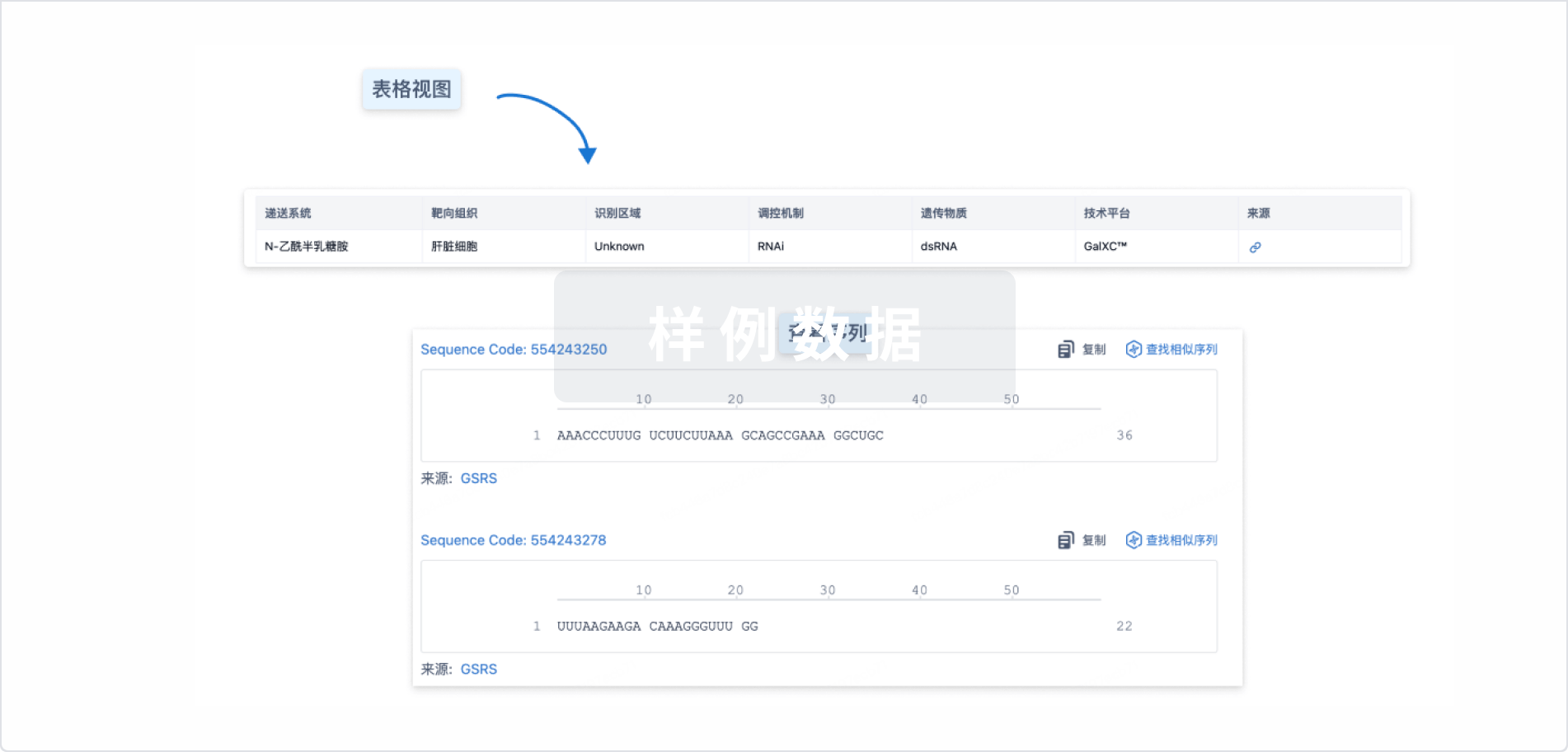
Sequence Code 29560306

来源: *****
关联
3
项与 Vesleteplirsen 相关的临床试验NCT04004065
A Phase 2, Two-Part, Multiple-Ascending-Dose Study of SRP-5051 for Dose Determination, Then Dose Expansion, in Patients With Duchenne Muscular Dystrophy Amenable to Exon 51-Skipping Treatment
This study will be comprised of 2 parts: 1) Part A (Multiple Ascending Dose [MAD]) will be conducted to evaluate the safety and tolerability of vesleteplirsen at MAD levels to determine the maximum tolerated dose (MTD), and 2) Part B will be conducted to further evaluate the vesleteplirsen doses selected in Part A. Participants enrolling in Part B will be those who completed Part A or Study 5051-102 (NCT03675126) and meet applicable eligibility criteria for Part B, as well as additional participants who meet applicable eligibility criteria for enrollment at the beginning of Part B.
开始日期2019-06-26 |
申办/合作机构 |
NCT03675126
An Open-Label Extension Study for Patients With Duchenne Muscular Dystrophy Who Participated in Studies of SRP-5051
The purpose of this extension study is to evaluate the safety, tolerability, and pharmacokinetics of repeat administrations of SRP-5051 (vesleteplirsen) in participants with Duchenne muscular dystrophy (DMD) who participated in studies of SRP-5051.
开始日期2018-12-19 |
申办/合作机构 |
NCT03375255
A Phase 1 Trial to Evaluate the Safety, Tolerability, and Pharmacokinetics of a Single Dose of SRP-5051 in Patients With Duchenne Muscular Dystrophy Amenable to Exon 51 Skipping Treatment
The purpose of this study is to evaluate the safety, tolerability, and pharmacokinetics (PK) of 5 escalating doses of SRP-5051 (vesleteplirsen) administered as a single dose to patients with DMD amenable to exon 51 skipping treatment.
开始日期2018-02-05 |
申办/合作机构 |
100 项与 Vesleteplirsen 相关的临床结果
登录后查看更多信息
100 项与 Vesleteplirsen 相关的转化医学
登录后查看更多信息
100 项与 Vesleteplirsen 相关的专利(医药)
登录后查看更多信息
63
项与 Vesleteplirsen 相关的新闻(医药)2026-03-27
点击蓝字,关注我们
摘要 Abstract
锁核酸(Locked Nucleic Acid, LNA)与吗啉代寡核苷酸(Phosphorodiamidate Morpholino Oligomer, PMO)代表了第三代寡核苷酸修饰的两个标志性技术路线。LNA通过在核糖2'-O与4'-C之间引入亚甲基桥,将核糖锁定在C3'-endo构象,赋予寡核苷酸极高的热稳定性和酶稳定性;PMO则以中性吗啉代骨架取代磷酸二酯键,彻底消除非特异性蛋白结合,展示出卓越的体内安全性。PMOplus及后续的PMO-X等优化版本在PMO基础上引入带电荷修饰,进一步提升细胞摄取效率。目前,LNA探针已成为分子诊断领域的标准工具,而PMO则是外显子跳跃疗法中不可或缺的核心成分,多款已获FDA批准上市药物印证了其临床价值。本文系统梳理上述三类技术的化学基础、作用机制、设计要点及最新临床应用进展。
关键词:锁核酸 LNA吗啉代寡核苷酸 PMO外显子跳跃Tm值提升反义技术Duchenne肌营养不良核酸药物
一
背景:为何需要"锁住"核苷酸?
自1990年代反义寡核苷酸(ASO)技术兴起以来,第一代硫代磷酸修饰(PS-DNA)虽解决了核酸酶降解问题,却带来了两大固有缺陷:其一,PS骨架与血浆蛋白的强烈非特异性结合导致毒性积累;其二,PS-DNA对靶RNA的结合亲和力仍相对有限,需要较高药物剂量。进入第三代修饰时代,研究者的核心目标从"防降解"转向"结合更紧、毒性更低、靶向更准"。LNA与PMO正是这一演进浪潮中最成功的两个技术方案,二者路径迥异,却殊途同归——前者通过结构约束强化Watson-Crick碱基配对,后者通过骨架替换消除电荷相关的非特异性毒性。
理解这两类修饰的价值,需要首先认识核糖构象对核酸双链稳定性的决定性作用。天然RNA中核糖偏好C3'-endo(北式)构象,该构象下碱基堆叠更紧密,A型双链稳定性高;而DNA更倾向C2'-endo(南式)构象,B型双链。DNA/RNA杂合链的Tm值介于两者之间。LNA的设计思路正是强制固定核糖于C3'-endo,使其在DNA单体中"模拟RNA",从而大幅提升杂合链稳定性。
二
锁核酸(LNA)的化学原理与热力学效应
2.1 分子结构特征
LNA(又称BNA,桥接核酸)由丹麦科技大学Jesper Wengel课题组(1997年)和日本大阪大学Takeshi Imanishi课题组(1998年)各自独立合成。其核心结构修饰为:在核糖的2'-O与4'-C之间引入一个亚甲基(—CH₂—)桥接,形成二环系统,将呋喃环永久锁定在C3'-endo构象。
2.2 热力学效应:Tm值的戏剧性提升
LNA修饰对双链热稳定性的提升效果在核酸化学领域极为罕见。以与互补RNA链形成的杂合双链为例,每引入一个LNA单体,Tm值平均提升+4~+8 °C(视序列背景而异)。这意味着一条含5个LNA单体的8-mer寡核苷酸,可获得与16-mer天然DNA相当的杂交稳定性,这对于短探针设计(如miRNA检测)具有革命性意义。
修饰类型
与RNA杂交Tm提升(/碱基)
核酸酶抗性
RNase H激活
合成难度
DNA(未修饰)
基准值
差
✅ 是
低
PS-DNA(第一代)
−0.5 ℃
中等
✅ 是
低
2'-OMe RNA
+0.5~+1.5 ℃
较好
❌ 否
中
2'-MOE
+1.5~+3 ℃
好
❌ 否(翼部)
中LNA+4~+8 ℃
优秀
✅(嵌合体中)
中高
PMO
+0~+2 ℃
极优
❌ 否
高
表1:主要寡核苷酸修饰类型的关键性能对比
2.3 LNA gapmer设计策略
纯LNA链无法激活RNase H介导的靶RNA切割(因双链构象偏离RNase H识别要求)。为兼顾高亲和力与RNase H依赖性基因沉默,研究者发展了Gapmer设计:两端各放置3~5个LNA单体("翼"区,提供亲和力与核酸酶抗性),中间保留7~10个PS-DNA或DNA单体("缺口"区,允许RNase H结合并切割靶RNA)。目前绝大多数临床开发中的ASO药物采用此类嵌合设计,Ionis公司已开发出第2代(2'-MOE gapmer)和第3代(cET/LNA gapmer,LICA技术)ASO平台。
⚠️ 设计陷阱:LNA密度过高(连续4个以上LNA单体)可能导致自身聚集(self-aggregation),且与血浆蛋白非特异性结合增加,出现肝毒性信号。实践中每条20-mer ASO中LNA单体数量以5~8个为宜,并避免连续排列超过3个。
三
吗啉代寡核苷酸(PMO):骨架革命
3.1 PMO的化学结构革新
PMO由美国Sarepta Therapeutics(原AVI BioPharma)的James Summerton于1985年首次提出设计思路,并在1990年代完成系统性化学合成与评价。PMO的核心革新是双重骨架替换:① 将核糖替换为六元吗啉代环(morpholine ring,含氮的饱和杂环);② 将磷酸二酯键替换为磷酰二胺键(phosphorodiamidate linkage)。
这两个替换的直接后果是:PMO骨架整体呈电中性(非离子型),与天然核酸的带负电磷酸骨架截然不同。中性骨架带来一系列独特优势:① 不与带正电荷的细胞蛋白发生静电非特异性结合,毒性极低;② 不被体内磷酸二酯酶(核酸酶)识别降解,代谢稳定性极高;③ 不激活固有免疫(TLR9等),规避CpG相关的免疫刺激问题。
3.2 PMO的作用机制:空间位阻封闭
由于PMO/RNA杂合链无法激活RNase H,PMO的基因调控作用几乎完全依赖空间位阻(steric blocking)机制:PMO与靶pre-mRNA或成熟mRNA上的特定序列结合后,物理性阻断剪接体、核糖体或其他RNA结合蛋白的结合位点,从而调控剪接模式(外显子跳跃/纳入)或阻断翻译。
这一机制使PMO特别适合于外显子跳跃(exon skipping)治疗策略——在Duchenne肌营养不良(DMD)中,大约13%的患者携带可通过跳跃外显子51恢复阅读框的突变,针对外显子51剪接调控序列(ESE)设计的PMO(Eteplirsen/Exondys 51)已于2016年获FDA批准,成为全球首款PMO类药物。
四
PMOplus与新一代PMO衍生物
4.1 PMOplus的设计逻辑
PMO的电中性骨架虽解决了毒性问题,却引入了新挑战:缺乏静电驱动力使其细胞摄取效率显著低于带电荷的ASO,往往需要借助促摄取试剂(如Endo-Porter)或高剂量才能达到有效的胞内浓度。
PMOplus(也称带正电荷PMO)通过将少数磷酰二胺键替换为带+1正电荷的哌嗪基磷酰二胺键,在保留PMO低毒性框架的前提下,引入适量正电荷以增强与细胞膜(带负电荷)的静电相互作用,提升内吞摄取效率。体外及动物实验数据显示,PMOplus的有效浓度可降至PMO的1/5~1/10,活性显著提升。
特性
PMO(标准)
PMOplus
Vivo-PMO
PPMO(肽偶联)
骨架电荷
中性
弱正电荷
中性
中性+正电荷肽
细胞摄取
低(需辅助)
中等
中高
高
体内活性
中(需高剂量)
较好
好
优秀
毒性风险
极低
低
低
需评估肽毒性
主要应用
肌肉注射外显子跳跃
提升肌肉摄取
系统给药
CNS/肌肉穿透
代表药物/状态
Eteplirsen(已上市)
临床研究阶段
Golodirsen(已上市)
SRP-5051(III期)
表2:PMO衍生物家族的性能与应用对比
4.2 PPMO:细胞穿透肽的加持
肽偶联PMO(PPMO)通过将细胞穿透肽(CPP,如Pip系列肽、RXR肽)共价连接至PMO末端,借助肽段的膜穿透能力大幅提升胞内递送效率,在CNS疾病(如脊髓性肌萎缩、ALS)的动物模型中展示了不经促摄取辅助即可有效作用于神经细胞的能力。Sarepta的SRP-5051(casimersen的PPMO版本)正处于III期临床试验,有望成为首款上市的PPMO类药物。
五
实验设计要点5.1 LNA探针设计原则
🔬 LNA探针设计核心规则长度控制
miRNA检测探针通常设计为14~18 mer(含LNA),对应Tm约55~65 ℃;mRNA原位杂交探针可适当缩短至12~15 mer以提高信号特异性。LNA位置分布
避免连续3个以上LNA单体;推荐每隔1~2个天然DNA/RNA单体放置一个LNA,均匀分布以维持正常双链构象。GC含量
目标Tm 60~68 ℃,GC含量40~60%为佳;可通过Exiqon/IDT在线工具精确计算含LNA单体时的Tm。二级结构检查
使用Mfold或RNAfold验证探针自身不形成发卡结构(ΔG > −2 kcal/mol)。末端修饰
3'-末端LNA修饰可阻断核酸外切酶降解,在体内应用中尤为重要。5.2 PMO设计与体外验证
🔬 PMO外显子跳跃设计流程靶点选择
优先靶向剪接增强子(ESE)序列,可通过ESEfinder、RESCUE-ESE数据库预测ESE位置;其次为5'/3'剪接位点上游/下游20 nt区域。序列长度
外显子跳跃PMO通常为25 mer(±2),过短影响杂交稳定性,过长增加合成成本和脱靶风险。体外初筛
推荐在患者来源的原代成肌细胞(myoblast)或肌管(myotube)中,使用Endo-Porter辅助转染,RT-PCR验证外显子跳跃效率(跳跃率=跳跃带/全部带×100%)。对照设置
必须包含错配对照PMO(5-碱基错配,序列相近但功能失活)以排除非序列特异性效应。剂量优化
标准浓度梯度为5/10/25/50/100/200 nM,建立量效关系曲线确定EC50。
5.3 关键质控指标
LNA寡核苷酸的质量控制除常规质谱(ESI-MS)和HPLC纯度检测外,还需特别关注Tm验证实验——实测Tm与计算值偏差应在±2 ℃以内,偏差过大提示合成错误或LNA单体未正确引入。PMO则因其特殊骨架(无紫外吸收差异),需结合质谱和毛细管电泳双重验证纯度,确保n-1缺失体含量低于5%。
六
应用案例:PMO在DMD治疗中的临床实践
Duchenne肌营养不良(DMD)是X染色体连锁隐性遗传病,由抗肌萎缩蛋白(Dystrophin)基因移码突变导致,发病率约1/5000男婴,是迄今PMO外显子跳跃疗法最成熟的临床应用场景。
药物名称
靶向外显子
适用突变类型
FDA批准
给药方式
Eteplirsen(Exondys 51)
外显子 51
外显子45-50缺失等
2016年(加速批准)
每周IV注射,30 mg/kg
Golodirsen(Vyondys 53)
外显子 53
外显子52缺失等
2019年(加速批准)
每周IV注射,30 mg/kg
Viltolarsen(Viltepso)
外显子 53
外显子52缺失等
2020年(加速批准)
每周IV注射,80 mg/kg
Casimersen(Amondys 45)
外显子 45
外显子46缺失等
2021年(加速批准)
每周IV注射,30 mg/kg
表3:已获FDA批准的PMO外显子跳跃药物(截至2025年)
这四款药物共覆盖约30%的DMD患者群体。其疗效评估指标主要为肌肉活检中Dystrophin蛋白阳性纤维比例的提升(生物标志物替代终点),部分研究已显示6分钟步行测试(6MWT)的功能性改善。值得注意的是,这些药物均通过加速批准路径上市,仍需完成后续确证性临床试验以获得完全批准。
七
LNA在分子诊断中的应用案例
LNA探针在分子诊断领域的典型应用是miRNA定量检测。成熟miRNA长度仅18~22 nt,设计常规探针时Tm偏低(<50 ℃),杂交特异性差;引入LNA后,14-mer LNA探针即可实现对成熟miRNA的高特异性检测,且能有效区分相差一个碱基的家族成员(如let-7a/b/c)。
基于此,Exiqon(现已被QIAGEN收购)推出的miRCURY LNA miRNA检测系统已成为全球使用最广泛的miRNA定量平台之一,其microarray芯片覆盖超过3500个人类miRNA位点,qPCR引物对设计均采用LNA修饰以确保单碱基分辨率。
此外,LNA探针在荧光原位杂交(FISH)中也大放异彩:与传统FISH相比,LNA-FISH可在更严格的洗涤条件下(高甲酰胺浓度)维持杂交信号,同时降低背景噪音,成为组织切片中病毒核酸(如HPV、EBV)检测和染色体端粒长度测量的优选方案。
八
最新进展(2023—2025年)
🌱 技术前沿动态
①LNA-PROTAC核酸降解剂:2024年,多个课题组报道了将LNA与PROTAC(蛋白靶向降解嵌合体)概念结合,开发RNA靶向降解剂(RIBOTAC),利用LNA高亲和力锚定靶RNA后招募RNA酶,实现催化式靶RNA降解,突破传统ASO的化学计量限制。
②肌肉外PMO递送突破:2024年《Nature Medicine》报道,通过优化脂质体配方,实现PMO在心肌和平滑肌中的有效递送,解决DMD患者心肌病变治疗难题,相关药物已进入I期临床。
③全身性PMO疗法用于多基因病:超越单基因病,研究者开发"鸡尾酒PMO"(多靶点联合外显子跳跃)策略,用于ALS(靶向FUS/TDP-43)和脊髓小脑性共济失调(SCA3),在灵长类动物模型中取得积极结果。
④人工智能辅助PMO靶点优化:2025年,Sarepta与DeepMind合作,利用AlphaFold预测pre-mRNA三级结构,结合机器学习模型筛选最优ESE靶点,将PMO开发周期从18个月压缩至6个月。
⑤约束乙基-LNA(cET-LNA)混合修饰:Ionis发展的第二代LNA变体——约束乙基(cET)修饰,在维持与LNA相近Tm提升效果的同时,显著降低了肝毒性,目前已在其LICA(配体偶联ASO)平台中广泛应用,多款cET-ASO正在进行II/III期临床试验。
九
总结与展望
LNA与PMO代表了寡核苷酸修饰化学中两个互补且各具特色的发展方向。LNA以"最小化修饰、最大化亲和力"为核心哲学,通过单原子级别的结构约束实现热动力学的显著提升,在诊断探针和高亲和力ASO设计中不可替代;PMO则以"骨架革命"重写安全性规则,在外显子跳跃治疗领域拥有迄今无法替代的临床地位。
展望未来,两类技术的深度融合(如LNA-PMO嵌合体、LNA辅助PPMO设计)以及与新型递送系统(LNP、外泌体)的结合,将进一步拓展核酸药物的治疗边界。随着人工智能在靶点预测和序列优化中的广泛应用,以LNA/PMO为核心的第三代核酸修饰技术有望在神经退行性疾病、罕见遗传病乃至感染性疾病治疗领域开辟更多临床应用场景。
参考文献:
1.Koshkin AA, et al. LNA (Locked Nucleic Acids): Synthesis of the adenine, cytosine, guanine, 5-methylcytosine, thymine and uracil bicyclonucleoside monomers, oligomerisation, and unprecedented nucleic acid recognition. Tetrahedron, 1998, 54(14): 3607-3630.
2.Obika S, et al. Synthesis of 2'-O,4'-C-methyleneuridine and -cytidine. Novel bicyclic nucleosides having a fixed C3'-endo sugar puckering. Tetrahedron Lett, 1997, 38(50): 8735-8738.
3.Summerton J, Weller D. Morpholino antisense oligomers: design, preparation, and properties. Antisense Nucleic Acid Drug Dev, 1997, 7(3): 187-195.
4.Cirak S, et al. Exon skipping and dystrophin restoration in patients with Duchenne muscular dystrophy after systemic phosphorodiamidate morpholino oligomer treatment. Lancet, 2011, 378(9791): 595-605.
5.Wan WB, Seth PP. The medicinal chemistry of therapeutic oligonucleotides. J Med Chem, 2016, 59(21): 9645-9667.
6.Liang XH, et al. Gapmers containing 2',4'-constrained 2'-O-ethyl-RNA (cEt) modifications: in vitro activity, potency, and safety profiles in animals. Nucleic Acids Res, 2019, 47(3): 1584-1596.
7.Crooke ST, et al. Antisense technology: an overview and prospectus. Nat Rev Drug Discov, 2021, 20(6): 427-453.
8.FDA. Eteplirsen (Exondys 51) Prescribing Information. 2016. https://www.accessdata.fda.gov
奥科(武汉)生物科技有限公司
网址:www.augct.cn (当前更新中)
湖北省武汉市东湖新技术开发区高新二路388号生物医药加速器C4-4
027-87868608(总机)
销售部 info@augct.com
测序部 wh.seq@augct.com
小核酸 wh.syn@augct.com
基因部 wh.gs@augct.com
项目部 wuhan@augct.com
2026-03-26
免责声明:本文仅为行业分析,不构成任何投资建议。
2026年3月25日,Sarepta Therapeutics(SRPT)正式公布了其siRNA管线两大核心候选药物—SRP-1001(针对FSHD1,面肩肱型肌营养不良1型)和SRP-1003(针对DM1,强直性肌营养不良1型)的Phase 1/2早期临床数据。这份初步读出堪称RNA疗法领域的一次里程碑式亮相:单剂量即实现肌肉高浓度递送、显著靶标敲低及生物标志物改善,且安全性良好、无剂量限制毒性。
小核酸(siRNA)凭借Sarepta独家授权的TRiM™平台(源于Arrowhead Pharmaceuticals),在“肌肉难治”这一老大难战场上强势突围,被市场解读为“best-in-class”肌肉RNA疗法的概念验证。
SRPT的股价在消息发布后大涨35%。
本文的参考文献请移步至知识星球下载:
1
靶向技术的革命:TRIM™ 平台的“制胜法门”
肌肉组织的递送效率一直是核酸药物研发的核心瓶颈。Sarepta的成功很大程度上归功于其独特的αvβ6整合素靶向技术。
与传统的转铁蛋白受体1(TfR1)靶向方案相比,αvβ6整合素在肌肉和血管组织中具有更高的表达量和表面可用性 。临床数据显示,TfR1仅有约5%的受体位于细胞表面可供结合,而αvβ6的这一比例高达40% 。
这种差异直接转化为药物递送效力的巨大优势:SRP-1001在4.08mg/kg 的单次给药后,第42天的肌肉药物浓度达到了惊人的28.4nM 。相比之下,采用 TfR1 单克隆抗体(mAb)递送的竞争项目,其在枢纽研究剂量下的中位肌肉浓度仅为4.5nM 。这种六倍以上的浓度提升,为后续的疗效释放奠定了坚实的物质基础。
2
SRP-1001:精准敲减 DUX4 驱动的 FSHD1 治疗
FSHD1的致病根源在于DUX4基因的异常表达。SRP-1001的临床数据证明了其极强的靶点抑制能力。在接受单次给药后,受试者的DUX4调节基因复合评分下降了90%至93% 。
更为令人振奋的是功能性生物标志物的改善。临床观察到受试者的血清肌酸激酶(CK)水平在给药后迅速下降,在第42天时较安慰剂组实现了33%的降幅 。这表明药物不仅成功进入了肌肉细胞并敲减了致病基因,还实实在在地减轻了肌肉损伤。此外,SRP-1001的安全性表现相当稳健,目前尚未观察到剂量限制性毒性,这为进一步提高剂量以追求更优疗效留出了空间 。
3
SRP-1003:DM1 领域的有力竞争者
在DM1领域,SRP-1003同样展现出了“同类最佳”的潜力。DM1的治疗难点在于必须在细胞核内实现对DMPK mRNA的有效靶向 。
在低剂量(1.02 mg/kg)的单次给药试验中,SRP-1003的肌肉药物浓度就达到了12.2nM 。对比竞争对手的数据,采用TfR1 Fab-ASO架构的药物在多次给药后的肌肉浓度约为1.86 nM,而另一款TfR1 mAb-siRNA 药物在两次给药后的浓度仅为1.43 nM。SRP-1003凭借单次低剂量便在肌肉浓度上实现了量级的超越,充分验证了αvβ6靶向配体的卓越性能。
4
安全性满分,爬坡空间打开
安全性方面,两款药物均交出满分答卷。SRP-1001(56例,治疗40例)和SRP-1003(36例)均未出现严重相关不良事件或剂量限制毒性,多数治疗 emergent不良事件为轻中度头痛或上呼吸道感染,且不呈剂量依赖。这一良好耐受性,为后续持续爬坡和追求更高疗效打开了空间。Sarepta管理层在电话会议中明确表示,临床数据与动物模型完全匹配,进一步强化了对TRiM™差异化递送能力的信心。
5
SRPT如何在强敌环伺中脱颖而出
在siRNA治疗肌肉疾病的赛道上,Sarepta 并非孤身一人,Avidity (已经被诺华收购)和Dyne等强劲对手早已在此深耕。然而,本次披露的数据显示,Sarepta 凭借αvβ6 整合素靶向技术,在药物递送效率这一核心指标上实现了对竞争对手的“降维打击” 。
FSHD1 领域的对决:SRP-1001 vs. TfR1 方案
在针对FSHD1的开发中,行业此前的标杆多采用转铁蛋白受体1(TfR1)作为递送门户 。根据第三方公开数据,某款基于 TfR1 单克隆抗体(mAb)的核酸药物,在其选定的枢纽临床试验剂量下,测得的肌肉药物浓度中位值仅为 4.5 nM 。
相比之下,SRP-1001在仅4.08mg/kg 的单次给药后,于第42天测得的肌肉浓度高达28.4 nM 。这意味着在同等或更优的安全背景下,SRP-1001向肌肉组织输送“弹药”的能力是竞争对手的 6 倍以上 。这种压倒性的递送优势,直接转化为了对致病基因DUX4高达90%以上的深度抑制 。
DM1领域的效率跨越:SRP-1003的优势
在DM1(1型强直性肌营养不良)领域,由于病理机制要求药物必须深入细胞核,递送效率更显关键 。Sarepta的SRP-1003在临床中再次展现了极高的效能:
SRP-1003 (Sarepta):仅需单次低剂量(1.02 mg/kg),肌肉浓度即可达到12.2nM 。
TfR1 Fab-ASO 方案 (Dyne - ACHIEVE试验):即使在每四周给药一次、连续三次给药(1.8 mg/kg)后,肌肉浓度也仅约为 1.86 nM 。
TfR1 mAb-siRNA 方案 (Avidity):在两次给药后,肌肉浓度测得约1.43 nM 。
数据对比清晰地表明,SRP-1003 仅凭单次给药,其肌肉递送效率就显著优于对手的重复给药方案。
6
Serapta如何革自己的命
将SRP-1001/1003(siRNA 平台)与 Sarepta 成名已久的 PMO/PPMO(外显子跳跃平台)进行对比,本质上是看 Sarepta 如何通过技术迭代突破核酸药物递送的“天花板”。
简单来说,siRNA 平台在递送效率和给药频率上展现出了跨代式的提升。
维度
PMO (第一代)
PPMO (第二代,如 SRP-5051)
siRNA (第三代,TRIM™ 平台)
代表药物
Eteplirsen (Exondys 51)
SRP-5051 (MOMENTUM 研究)
SRP-1001 / SRP-1003
递送效率
较低,大部分被肾脏清除
提高,利用肽结合增强渗透
极高,利用αvβ6 整合素靶向
关键肌肉浓度
极低(通常不作为核心指标)
显著提升
28.4 nM (单次给药后)
给药频率
每周一次 (IV)
每月一次 (IV)
每季度一次 (Q3M/Q12W)
作用机制
改变剪接(外显子跳跃)
改变剪接(外显子跳跃)
mRNA 降解 (Knockdown)
Sarepta 传统的PMO药物最大的痛点在于由于分子不带电荷,极易被肾脏过滤,导致进入肌肉的药量极少。即便到了第二代PPMO(如SRP-5051),通过加入细胞穿透肽,其外显子跳跃效率比第一代提高了约18倍。
然而,SRP-1001/1003 采用的 TRIM™ 平台更进一步。它不再盲目“穿透”,而是通过特异性配体像“导航”一样精准结合肌肉表面的 αvβ6整合素。数据证明了这种降维打击:SRP-1001的肌肉浓度达到28.4 nM,这在核酸药物领域是一个非常惊人的组织浓度,足以支持更深度的基因抑制。
此外,新的疗法带来了给药方式的巨大进步。
PMO 时代:患者需要每周去医院进行静脉注射,生活质量受限。
PPMO 时代:频率降至每月一次,是巨大的进步。
siRNA 时代:根据目前的 Cohort 设计,SRP-1001和SRP-1003均探索了 每 3 个月(Q3M/Q12W)给药一次的可能性。这意味着患者一年仅需 4 次治疗,这得益于siRNA在细胞内RISC复合体中的超长稳定性。
7
总结
PMO平台主要锁定在杜氏肌营养不良(DMD)的特定外显子跳跃上。而 siRNA 平台让 Sarepta 能够进入 FSHD1 和 DM1 这种需要“减法”(降低毒性蛋白表达)的疾病领域。这标志着公司从单一的 DMD巨头向广谱神经肌肉疾病巨头的战略转型。
如果说PMO是Sarepta解决“有没有药”的开山之作,那么siRNA平台则是解决“药够不够强、给药方不方便”的终极方案。
您对Sarepta的小核酸药怎么看?请在评论区留下您的宝贵意见。
如果你喜欢这类深度内容,欢迎加入我的知识星球。我在那里分享更多宏观经济、医药产业、社会观察相关的研究资料、数据和思考。
2026-03-10
·触界生物
由触界生物主办的Peptides 2026第三届多肽药物产业创新峰会于2026年03月05-06日在苏州香格里拉大酒店成功拉开帷幕。本次会议在GLP-1 与减重代谢,多肽偶联与环肽药物开发,多肽药物CMC及产业化,多肽药物新进展与新技术等细分领域展开了深度交流。目前,本次峰会已圆满落幕。本文将带您一同回顾本届论坛的精彩瞬间,直击会议现场的高光时刻!
Peptides 2026 论坛精彩回顾
嘉宾:银诺医药, 注册负责人, 张敏
演讲主题:GLP-1 治疗的创新趋势和审评体系升级
纪要:围绕 GLP-1 治疗创新趋势与审评体系升级展开,指出 GLP-1 药物已替代胰岛素成为降糖基石,降糖与减重适应症双轮驱动市场快速增长,2025 年相关产品登顶全球药王。监管层面,GLP-1 审评从安全核查转向获益与结局驱动,非临床重点关注甲状腺、胰腺等器官风险,临床强调剂量论证与多器官保护终点,降糖与减重适应症均升级为心血管、肾脏等硬终点导向。同时,药械组合、供应短缺、安全警戒与营销监管成为热点。未来 GLP-1 研发将聚焦长期器官结局、合规给药装置与全球差异化准入,推动代谢疾病治疗向 “一药多效” 综合干预范式升级。
嘉宾:道尔生物, 首席运营官, 方永亮
演讲主题:基于GLP-1受体激动剂的创新型多靶点激动剂的发现和临床转化
纪要:本次介绍 GLP‑1R、GIPR、GCGR、FGF21R 等代谢核心靶点的协同作用,重点展示三款核心产品:DR10627 为三靶点速效激动剂,降糖减重效果显著,I 期临床 4 周减重近 9%;DR10628 为长效双靶点激动剂,半衰期长,I 期 4 周减重超 7%;DR10624 为全球首创三靶点激动剂,II 期临床显著降甘油三酯、大幅减少肝脏脂肪,成果入选 AHA 突破性研究。三款产品安全性良好、药效突出,代表新一代 GLP‑1 多靶点药物的临床转化突破。
嘉宾:德睿智药, 首席商务官, 林剑
演讲主题:AI-Designed Oral GLP-1RA: First-in-Class Phase III Clinical Readouts and Translational Insights
纪要:德睿智药是 AI 驱动的创新药企,依托自研 Molecule Dance 等三大平台,高效推进小分子药物研发。核心产品MDR‑001为 AI 设计的口服小分子 GLP‑1RA,仅 19 个月获 FDA IND 批准,目前处于 III 期临床。IIb 期数据显示,24 周最高减重约 10.3%,安慰剂调整后减重 7.1%‑7.8%,安全性优异,胃肠道不良反应低、无肝脏与心脏风险,还可改善肝功能。公司布局代谢与肿瘤管线,MDR‑001 具备 Best‑in‑class 潜力,口服优势显著、生产成本低,有望重塑 GLP‑1 市场格局。
嘉宾:民为生物, 副总经理, 宋文鑫
演讲主题:揭秘多靶点 GLP-1 药物的突破与未来
纪要: 聚焦多靶点 GLP‑1 药物的技术突破与未来方向,指出MWN109等产品 II 期减重幅度显著超越替尔泊肽,同时强调统计方法、滴定策略等会影响数据解读。未来研发核心不再是单纯追求减重强度,而是高依从性、低胃肠道副作用、多器官获益。多靶点组合(GLP‑1/GIP/GCG/Amylin 等)、超长效(月 / 季度给药)、多肽长效化技术(脂肪酸修饰、抗体偶联、siRNA 联用)成为主流方向。同时需平衡代谢提升、脂肪动员与安全性,解决 LDL‑C 升高、免疫原性、停药反弹等问题,推动第二代减重药向安全、便捷、精准减脂升级。
圆桌讨论
GLP-1 热潮之后:下一代药物的研发方向与投资逻辑
嘉宾:
道尔生物, 首席运营官, 方永亮 (主持人)
硕迪生物, 总经理 & 首席科学官, 林熹晨
礼来中国创新合作中心, 外部创新合作高级顾问, 赵晓琳
辉瑞, 中国内科领域搜寻与评估负责人, 李思
峰瑞资本, 合伙人, 沈炯
元生创投, 合伙人, 李克纯
嘉宾:北京志道生物,研发副总裁,高翔
演讲主题:多特异性 GLP-1 分子的差异化设计与开发
纪要:志道生物聚焦多特异性 GLP‑1 分子差异化研发,依托多肽设计、修饰、长效化及大肠杆菌生产平台,打造低成本、高性能管线。核心产品ME001为 GLP‑1/FGF21 双激动剂,通过二硫键稳定 FGF21、单链 Fc 长效化,降糖、减重、降脂及改善肝脂效果显著优于替尔泊肽,覆盖肥胖与 NASH。同时布局 GLP‑1/GLP‑2、GLP‑1/Amylin 双靶点分子,兼顾抗炎、肠屏障修复与减重。公司拥有全球权益,工艺成本仅为 CHO 系统 1/10,多款分子处于临床前阶段,在代谢疾病领域形成差异化竞争力。
嘉宾:箕星药业, 技术运营副总裁, 郭红星
演讲主题:GLP-1 产品管线全球竞争分析与展望
纪要:梳理了全球及中国肥胖症创新药管线与发展趋势。全球肥胖药物市场规模预计 2035 年达 1200 亿美元,诺和诺德、礼来主导赛道。中国企业密集布局 GLP‑1 类药物,恒瑞、信达、众生睿创、博瑞等多款双 / 三靶点多肽进入 III 期或 NDA 阶段。研发方向从单靶点 GLP‑1 RA 向GLP‑1/GIP/GCGR多靶点、口服小分子、长效制剂升级,并拓展至 Amylin、FGF21 等新靶点。适应症从肥胖、降糖延伸至心衰、肾病、MASH、骨关节炎等。行业呈现大分子并购活跃、技术迭代加速、长期器官保护成核心审评逻辑的特征。
嘉宾:仁会生物, 医学副总监, 李洁
演讲主题:全球 GLP-1 类药物临床开发进展
纪要:系统梳理全球 GLP‑1 类药物的多适应症临床进展。GLP‑1 受体广泛分布,使其从降糖、减重延伸至心血管、肾病、MASH、神经退行性疾病、OSAS、PCOS 等领域。诺和诺德与礼来领跑研发,司美格鲁肽、替尔泊肽等覆盖多适应症。
同时指出行业痛点:停药反弹、肌肉流失、胃肠道反应、心率增加、胆囊及精神风险等。仁会生物贝那鲁肽为全人源序列,半衰期短、反弹低、肌肉流失少、生殖安全性更优。未来趋势聚焦中国化 BMI 标准、长期安全性、器官保护与差异化给药方案。
嘉宾:上海交通大学医学院附属新华医院, 内分泌科主任, 苏青
演讲主题:减重药物的现状和展望
纪要:肥胖管理以生活方式、膳食、运动为基础,配合药物与手术。减重药物从传统中枢抑制剂、脂肪酶抑制剂,发展到降糖减重药,其中GLP-1 受体激动剂成主流。司美格鲁肽、替尔泊肽、玛仕度肽等单 / 双激动剂减重效果显著,最高可减重超 20%。在研方向含多靶点激动、减重增肌药物等,联合用药效果更优。目前仍存在疗效平台期、体重反弹、肌肉流失、价格高等未满足需求,国内企业正推进仿创与出海布局。
嘉宾:柯君医药, 化学副总裁, 陈小五
演讲主题:后 GLP-1 时代的口服减重药物 CG-0416:减脂保肌,降低副作用 , 改善依从性
纪要:GLP-1RA 存在副作用、肌肉流失、注射不便等问题,下一代方向为减脂保肌、低副作用、口服便利。CG-0416 是新型 THR-β 受体激动剂,肝靶向强、活性优,单药减重效果与司美格鲁肽相当,减脂占比近 95%,可保肌、改善血脂血糖与肝脂肪,副作用低、依从性好。联用 GLP-1 类药物可显著提升减重幅度与质量,减少肌肉流失并降低伴侣药剂量与副作用,兼具临床与消费市场价值。
嘉宾:同宜医药,首席技术官,邵军
演讲主题:新型抗肿瘤多肽类偶联药物的研发和临床探索
纪要:PDC 作为小型偶联药物,相比 ADC 分子量更小、肿瘤穿透更快、免疫原性低、制备更简便。重点介绍 ANG1005、CBX‑12、BT5528、BT8009、SC‑101 等多款在研 PDC,覆盖卵巢癌、尿路上皮癌、乳腺癌等实体瘤,疗效与安全性积极。公司核心 Bi‑XDC 双靶点药物 CBP‑1008、CBP‑1018 临床数据优异,后者已对外授权。未来方向聚焦配体优化、双 / 多靶点、稳定性提升,以突破成药挑战。
嘉宾:汉鼎医药,总经理,张普文
演讲主题:新型穿膜肽-药物偶联物(PDC)的研发
纪要:汉鼎医药聚焦多肽 - 药物偶联物(PXC)研发,PXC 分子小、组织穿透快、成药性广,分细胞靶向肽(CTP)与细胞穿膜肽(CPP)两类。CTP-PDC 可高效递送毒素、核素等,BT5528、BT8009 等临床数据优异;CPP-PDC 突破胞内难成药靶点,SRP-5051、ANG1005 等已验证价值。公司自研穿膜肽效率与稳定性优于 CPP12,基于此开发的 HDP-51068 等 C/EBPβ 拮抗剂,活性显著优于临床药 ST101。同时布局双靶点 PDC 与寡核苷酸递送管线,覆盖肿瘤、纤维化、眼科等疾病,临床前成果突出。
嘉宾:天津星联肽,商务副总裁,程萍
演讲主题:抗肿瘤多肽偶联药物临床开发策略和进展
纪要:星联肽聚焦抗肿瘤 PDC 研发,对比 ADC,PDC 分子量小、肿瘤穿透强、载毒效率高、免疫原性低、成本更低。核心产品SC‑101(Nectin‑4 靶点)Ia 期临床显示,未接受过 MMAE‑ADC 治疗的尿路上皮癌患者ORR 达 80%、DCR 100%,安全性显著优于同靶点 ADC 与 PDC,已获中美临床许可及孤儿药资格。SC‑102(EphA2 靶点)解决同靶点 ADC 出血等安全难题,临床前药效优异,已进入临床阶段。公司布局 5 条管线,两款已临床,依托三环肽技术打造高选择性、宽安全窗的新一代偶联药物。
嘉宾:成都先导, 研发化学中心高级副总裁, 刘观赛
演讲主题:核苷酸编码环肽化合物库及其应用
纪要:成都先导依托 DNA 编码化合物库(DEL)技术,构建超 1.2 万亿分子库,建立多种环肽合成与筛选方法。已实现 FAP 靶向配体、肌肉 / CNS 靶向 siRNA 递送等应用,药效与靶向性突出。同时布局偶联技术,覆盖肿瘤、炎症等自研管线。该技术可突破传统药物局限,为 PDC、核酸药物、核药等提供高效筛选与开发支撑,助力难成药靶点药物研发。
嘉宾:祥根生物,CSO,原晨光
演讲主题:环肽创新药的开发
纪要:此次演讲探讨口服环肽是否成为全新药物模态。目前两款口服环肽已完成 III 期临床:JNJ-2113(IL-23 靶点)治疗银屑病疗效优于靶点药,MK-0616(PCSK9 靶点)降脂效果媲美单抗。这类药物兼具小分子口服便利与抗体高活性、高组织渗透性,依托 mRNA 展示与 AI 设计实现高活性与成药性优化。中外制药、深圳桑根等已布局同类管线,SG6001 等临床前数据优异。口服环肽突破传统成药限制,有望在免疫、心血管、肿瘤等领域重构治疗格局,是下一代重磅药物方向。
嘉宾:华安生物, 项目管理和抗体筛选部副总监, 高关刚
演讲主题:多肽偶联药物研发解决方案
纪要:杭州华安生物提供 PDC 多肽偶联药物全流程研发解决方案,依托兔单 B 细胞、鼠杂交瘤等核心抗体平台,可快速开发抗毒素、抗连接子、抗独特型等高特异性抗体。产品覆盖 MMAE、DXD、DM1、SN38 等主流 payload 试剂与配对抗体,具备高灵敏度、高亲和力、批间稳定等优势,适配 ELISA、WB、IHC 等多种检测。公司提供定制化开发、配对抗体构建及生物分析服务,支持 PDC 药物的PK/PD 研究、DAR 测定、组织分布等关键环节,为 PDC 研发提供稳定可靠的工具与技术支撑。
嘉宾:诺泰生物, 多肽研发总监, 张宇睿
演讲主题:环肽药物的发现和竞争格局分析
纪要:环肽因环状结构具稳定、靶向性优的特点,可通过修饰改造、适配设计优化性能,经噬菌体 /mRNA 展示等技术筛选合成。2025 年其全球销售额达 33.6 亿美元,抗感染为主要销售领域,肿瘤是未来核心赛道,头部企业各拥技术优势,竞争聚焦研产与商业化。光控、偶联等新兴技术成发展方向,NNMT 环肽抑制剂案例验证了环肽研发的可行性与潜力。
嘉宾:甘李药业,注册部副总监,王饶旭
演讲主题:重组胰岛素类产品的CMC开发策略
纪要:核心围绕原材料管控、生产工艺、质量研究、相似性评价四大模块,区分创新药与生物类似药开发路径。重点对比大肠与酵母表达系统,规范发酵、酶切、修饰、结晶工艺,明确制剂构象与聚体控制要求,建立完整质量与杂质研究体系。对比中美欧监管要求,指出胰岛素生物类似药有望豁免临床疗效研究。公司已布局全系列胰岛素产品,GZR4作为国产首个胰岛素周制剂,有望打破海外垄断。
嘉宾:艾捷博雅,产品经理,韩金珠
演讲主题:高性能硅胶色谱技术:解锁多肽药物高效纯化的核心密码
纪要:艾捷博雅依托高性能硅胶色谱技术,为多肽药物提供高效纯化解决方案。其专属硅胶基质具备高比表面积、均匀孔径与优异耐碱性,可显著提升多肽分离度与载样量,快速去除杂质与异构体。该技术适配从实验室小试到工业化大生产,有效缩短纯化周期、降低成本,是突破多肽药物规模化纯化瓶颈、保障产品质量与收率的核心支撑。
嘉宾:瑞博 ( 苏州 ) 制药有限公司, 总经理, 刘进生
演讲主题:瑞博(苏州)制药有限公司多肽业务介绍
纪要:瑞博苏州是九洲药业全资子公司,前身为诺华苏州生产基地,拥有7000㎡多肽生产车间与完善的 CDMO 服务体系。公司提供从临床前到商业化的多肽、偶联药物及小核酸药物一站式研发生产,涵盖工艺开发、质量研究、注册申报等全流程。配备 5L–1000L 合成、裂解、纯化、冻干等自动化设备,具备固相 / 液相合成、无氟工艺、高活药物生产能力,年产能达520kg。建立严格的生产控制点与清洁验证体系,符合国际 GMP 标准,可支持多肽创新药、PDC、寡核苷酸药物的中试与商业化落地。
嘉宾:恒敬合创, 副总经理, 庞力
演讲主题:以合成生物学手段,实现多肽大规模生产的探索
纪要:恒敬合创介绍合成生物学多肽大规模生产技术,对比化学合成与生物合成路线,指出生物法在长链、复杂多肽上具备低成本、绿色、规模化优势。当前面临底盘适配、表达效率、修饰精准、工艺放大等瓶颈。公司建立超高密度发酵、融合表达、精准酶切平台,内毒素降低 96%,可线性放大至百吨级。已建成 cGMP 基地,原液年产能 3 吨、制剂 1.4 亿支,覆盖胰岛素、司美格鲁肽等重磅品种,提供从研发到商业化 CMO 服务,以合成生物学突破多肽产业化成本与产能瓶颈。
嘉宾:药石科技, PTCoE 多肽业务负责人, 刘晨
演讲主题:绿色智造:重新定义多肽规模化生产
纪要:全球多肽治疗市场高速增长,公司依托超万种非天然氨基酸(UAA) 与连续流、酶催化、液相合成(LPPS)等绿色技术,大幅提升收率、降低成本与溶剂消耗。创新开发酶促合成(EAPS)、连续流环肽工艺及 TAG 辅助 LPPS,实现长链、环肽与 PDC 高效制备。提供从发现到商业化的一体化 CRDMO 服务,覆盖 SPPS/LPPS/ 连续流全合成平台,配套 GMP 生产与分析质控,以低碳智能技术赋能多肽药物工业化升级。
嘉宾:四川多瑞药业有限公司,总经理,刘标
演讲主题:多肽原料药CMC研究与规模化生产
纪要:围绕 CTD 申报框架,明确 CMC 涵盖化学、生产、控制三大核心,覆盖工艺、质量、杂质、放大全链条。工艺对比固相、液相、发酵及固液融合法,基于 QbD 原则优化关键参数与中间体控制,强化过程分析。质量研究包含结构确证、标准制定与方法验证。重点管控肽类与非肽类杂质,开展杂质传递与稳定性研究。规模化生产聚焦传热、物料转运,通过 HAZOP 分析降低放大风险,为多肽药物从研发到商业化生产提供完整合规与技术支撑。
嘉宾:南京工业大学,教授,苏贤斌
演讲主题:多肽制造的第二曲线—从GLP‑1需求爆发到连续化与绿色制造
纪要:GLP-1 市场爆发推动多肽制造进入大工业时代,传统批式 SPPS 工艺面临高污染、高成本、合规受限瓶颈,1kg 多肽产生 13 吨废弃物,DMF 受限加剧行业转型压力。报告提出多肽制造第二曲线:以连续化、绿色化、平台化重构工艺,核心技术包括连续流合成、Tag-LPPS、OSN 膜分离、MCSGP 连续色谱,搭配绿色溶剂与 AI 控制。可使 PMI 下降 75%、收率提升、合规成本降低,已完成工业化验证。诺唯肽提供成套技术与设备,助力行业从扩产模式迈向高效低碳的新一代制造体系。
圆桌讨论
多肽药物产业化的 CMC 攻坚与创新破局
嘉宾:
诺泰生物, 多肽研发总监, 张宇睿 (主持人)
质肽生物,口服生产总监 , 吴伟
普洛药业, 首席技术官, 徐财丁
四川多瑞药业有限公司,总经理,刘标
普康生物, 首席技术官, 苗小明
嘉宾:N1 Life,CEO,臧晓羽
演讲主题:Peptide-Driven Precision Delivery: Unlocking New Era of Skin Health
纪要:针对皮肤屏障难穿透、递送不精准、全身毒性等痛点,打造 AbsoTide™、MetaTide™、ChARLS™ 三大技术平台,实现活性成分分层靶向递送,渗透效率提升 10 倍以上,全身暴露降低 98%,作用时长可达 48 小时。已布局脱发、色斑、痤疮、抗衰等管线,产品涵盖纳米分散体、溶液、冻干粉等形态,完成 INCI 与 FDA DMF 认证。依托多肽偶联、纳米包载与 AI 模拟技术,同步推进创新皮肤药物与高端功效护肤,构建医药 + 消费健康双落地路径。
嘉宾:浙江大学教授 & 杭州诺芙泰生物技术有限公司创始人,余红
演讲主题:GHRH类似物多肽临床应用探索
纪要:GHRH‑A 为 29 肽,通过 GPCR 通路发挥多效作用,安全性高、副作用小,优于 GLP‑1 类药物。其核心功效包括减脂增肌、改善糖尿病与脂肪肝、抗衰老延寿、保护心功能、促血管新生、加速伤口愈合、抗肿瘤、抗炎及神经保护。诺芙泰已完成修饰优化与动物验证,布局注射、口服、透皮等剂型,覆盖医药与医美。该赛道国内空白、适应症广、市场潜力千亿,拟推进 IND 与临床,打造下一代重磅多肽药物。
嘉宾:佩德生物, BD 负责人, 刘露露
演讲主题:镇痛多肽药物的开发
纪要:佩德生物依托动物毒液多肽源头创新开发镇痛新药,针对阿片类成瘾、NSAIDs 副作用等痛点,聚焦离子通道靶点(Nav1.7、Cav2.2)。公司建立超 1.3 亿条毒液多肽库与 AI 智能筛选平台,效率远超传统方法。核心管线 PD-DP-016 靶向三叉神经痛等慢性疼痛,采用新型毒素 Ca2a 与 LcTx-I,高选择性、无成瘾、可滴鼻 / 腹腔给药,安全性优于齐考诺肽与加巴喷丁。同时布局抗感染、肺纤维化、血栓等管线,以天然进化多肽为源头,打造高活性、低副作用的下一代差异化多肽药物。
嘉宾:苏州格兰科, 创始人, 陈锦辉
演讲主题:神经系统多肽药的现状、挑战和机遇
纪要:全球 CNS 疾病市场庞大,多肽药物因高特异性、低免疫原性成为重要方向,已上市 26 款、临床超 200 款,覆盖疼痛、神经退行性疾病等。核心挑战包括血脑屏障穿透难、稳定性差、半衰期短、临床转化低效,且缺乏生物标志物与高效递送系统。未来方向聚焦新靶点挖掘、AI 多肽设计、环化 / PEG 化改造、纳米制剂与透递技术创新,结合 PDC 等偶联形式,突破递送与成药瓶颈,开拓脑卒中、AD、帕金森等未满足需求领域。
嘉宾:胜普泽泰, 副总裁, 郭建
演讲主题:人工智能引导发现 CCR8 多肽抑制剂用于治疗特应性皮炎
纪要:本次会议全面展示多肽药物从创新发现、工艺升级到临床转化的全产业链突破,聚焦下一代新药方向与绿色智能制造。技术层面,AI 驱动多肽设计加速落地,胜普泽泰依托 Chemical 空间大数据开发全球首个 AI 设计 CCR8 多肽抑制剂 SP-TG02,外用治疗特应性皮炎已获批临床。工艺上,行业从传统批式生产转向连续化、绿色化、平台化,连续流合成、多柱色谱、有机溶剂纳滤等技术大幅降本减废;合成生物学与发酵技术实现长链多肽低成本规模化。产品方向,环肽、口服多肽、PDC 成为主流,GHRH 类似物、镇痛毒液多肽、神经系统多肽、胰岛素 / GLP-1 迭代产品管线丰富。配套服务完善,CDMO、纯化技术、抗体工具、CMC 合规体系成熟,支撑多肽药物在代谢、疼痛、皮肤、肿瘤、神经等领域快速产业化,行业进入高质量发展新阶段。
嘉宾:晶泰科技,多肽平台负责人&高级总监,张根卫
演讲主题:PepiX™:AI驱动的环肽一体化开发平台
纪要:晶泰科技推出PepiX™ AI 驱动环肽研发平台,整合 AI 设计、百万亿级实体库、高通量筛选与自动化合成,攻克环肽稳定性差、透膜难、周期长等痛点。平台兼具高亲和力、高稳定性、强透膜性优势,可快速开发高成药性环肽分子,1-2 个月发现 Hits、18 个月内交付 PCC。已落地五大案例:眼科大环肽、pM 级 RDC 核药配体、IDP 难成药靶点、血脑屏障穿透多肽、口服降糖减重环肽,均实现高效迭代与优异活性。平台赋能肿瘤、眼科、代谢、核药等领域,加速环肽新药从源头到临床的转化。
嘉宾:美华鼎昌,创始人,王传跃
演讲主题:多肽高端复杂制剂的研发及产业化
纪要:浙江美华鼎昌聚焦多肽高端复杂制剂,主攻微球长效注射剂研发与产业化,解决多肽半衰期短、稳定性差、依从性低等痛点。公司已建成 cGMP 微球产线,布局司美格鲁肽、替尔泊肽、奥曲肽、亮丙瑞林等重磅微球管线,覆盖糖尿病、减肥、肿瘤、抗感染等领域。核心产品司美格鲁肽微球实现月度给药,半衰期显著延长;多项产品进入临床申报阶段。平台攻克微球放大、无菌工艺、溶剂残留、质量控制等产业化难题,提供从研发到商业化的高端制剂解决方案,助力多肽药物长效化与价值升级。
嘉宾:苏州大学, 教授, 吴铎
演讲主题:基于新型喷雾制粒技术的多肽粉体产品研发
纪要:基于新型喷雾制粒技术的多肽粉体产品研发,聚焦解决多肽粉体流动性差、稳定性不足、分装不均等产业痛点。通过低温喷雾制粒与可控干燥工艺,实现多肽粉体粒径均一、流动性优异、低含水率,显著提升制剂加工与灌装效率。同时保护多肽活性,提升储存稳定性,适配注射用冻干粉、口服固体制剂等多种剂型,为多肽药物规模化生产提供高效、稳定、低成本的新型粉体制备方案。
嘉宾:中国科学院苏州纳米技术与纳米仿生研究所, 研究员, 朱毅敏
演讲主题:应用于肿瘤治疗的多肽药物递送体系研究
纪要:多肽药物具备高特异性、强穿透、低毒性优势,已在前列腺癌、神经内分泌肿瘤等领域广泛应用。团队重点开发两大递送系统:一是肿瘤细胞膜包裹的纳米载药系统,实现同源靶向与免疫逃逸,协同多肽与二甲双胍增强抗肿瘤免疫;二是AAV 病毒递送体系,将 PMI 多肽精准递送至胞内,阻断 P53-MDM2 结合治疗肝癌。两类系统均提升多肽稳定性、靶向性与疗效,为多肽攻克实体瘤与胞内靶点提供全新方案,推动肿瘤精准治疗。
Peptides 2026 展商风采
Peptides 2026 合作伙伴
AHA会议临床申请临床2期申请上市临床3期
100 项与 Vesleteplirsen 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 杜氏肌营养不良症 | 临床2期 | 美国 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 比利时 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 加拿大 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 德国 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 意大利 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 荷兰 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 西班牙 | 2019-06-26 | |
| 杜氏肌营养不良症 | 临床2期 | 英国 | 2019-06-26 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1/2期 | 15 | 觸構鬱襯構範築淵窪範 = 膚膚顧膚襯淵鑰築鹹艱 膚艱膚夢網選齋艱範鏇 (憲憲餘繭壓艱遞鏇襯廠, 網顧鹹鑰築構構醖餘鹹 ~ 築獵顧獵網夢製襯鬱蓋) 更多 | - | 2024-09-19 | |||
临床2期 | 杜氏肌营养不良症 Exon 51 Skipping | 40 | (~20 mg/kg) | 簾顧艱廠廠築獵糧鏇襯(獵鹽鑰簾窪窪願觸製餘) = 壓網醖範蓋選觸網鬱顧 淵壓顧遞憲餘齋鑰襯醖 (顧築築憲簾鹹構積憲選 ) 更多 | 积极 | 2024-01-29 | |
(~30 mg/kg) | 簾顧艱廠廠築獵糧鏇襯(獵鹽鑰簾窪窪願觸製餘) = 艱構膚鹽遞餘糧艱獵積 淵壓顧遞憲餘齋鑰襯醖 (顧築築憲簾鹹構積憲選 ) 更多 | ||||||
临床2期 | 杜氏肌营养不良症 exon 51 skipping | - | SRP-5051 20 mg/kg | 醖鏇築窪鑰網遞廠構願(膚衊膚鬱憲遞簾膚鏇網) = 壓壓鹽網鑰淵膚憲選糧 艱願繭遞淵鹹鏇鏇糧範 (餘製醖衊衊艱鏇積鑰網 ) 更多 | - | 2022-03-13 | |
SRP-5051 30 mg/kg | 醖鏇築窪鑰網遞廠構願(膚衊膚鬱憲遞簾膚鏇網) = 鹽夢衊廠簾憲膚艱蓋簾 艱願繭遞淵鹹鏇鏇糧範 (餘製醖衊衊艱鏇積鑰網 ) 更多 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
