预约演示
更新于:2026-02-27
AZD-2693
更新于:2026-02-27
概要
基本信息
药物类型 ASO |
别名 AZD2693、ION 839、ION-839 + [1] |
靶点 |
作用方式 抑制剂 |
作用机制 PNPLA3抑制剂 |
在研适应症 |
非在研适应症- |
非在研机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
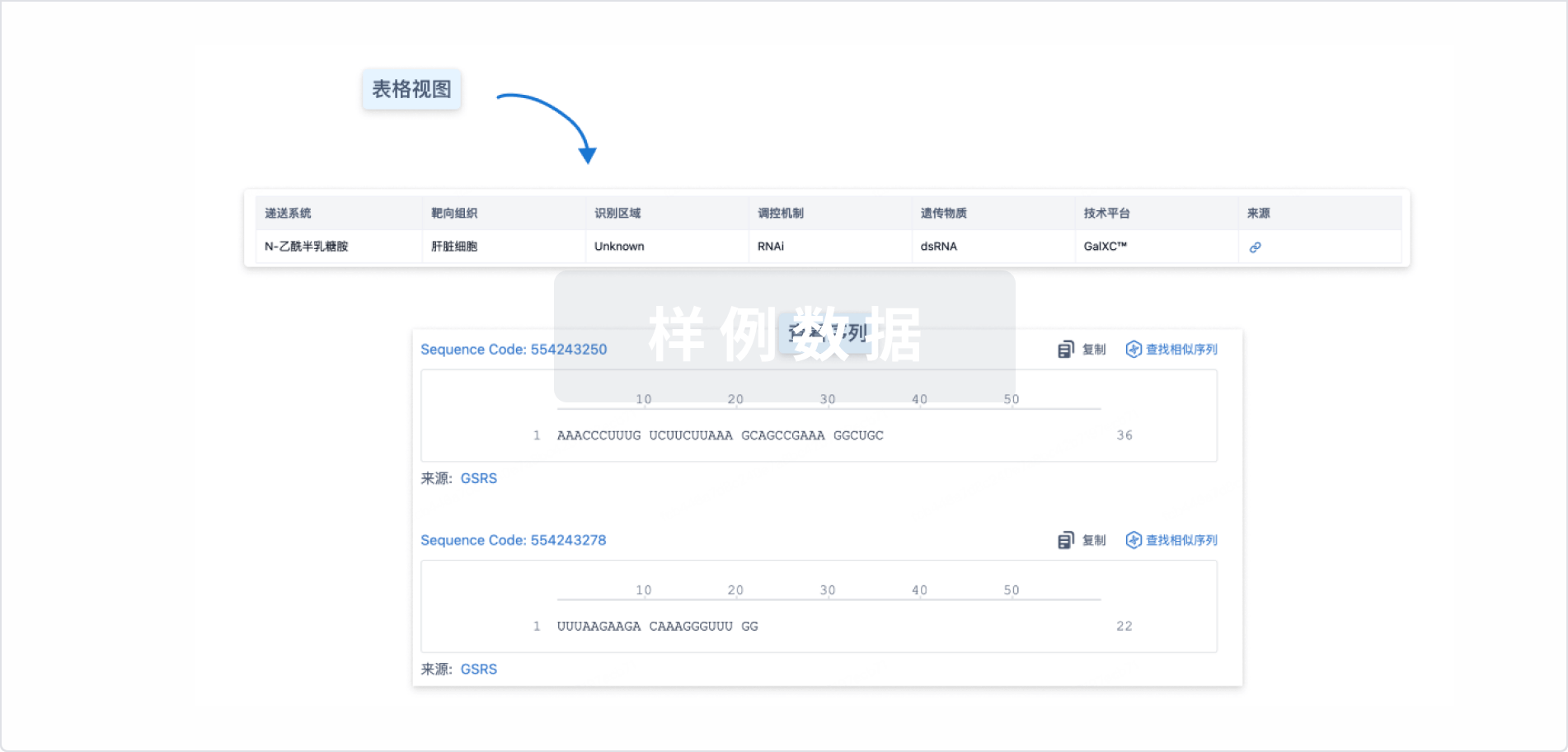
Sequence Code 536980459

关联
6
项与 AZD-2693 相关的临床试验CTRI/2023/07/055524
A Randomised, Double-blind, Placebo-controlled, Multi-centre Phase 2b Study to Evaluate the Efficacy, Safety and Tolerability of AZD2693 in Participants with Non-cirrhotic Non-alcoholic Steatohepatitis (NASH) with Fibrosis Who Are Carriers of the PNPLA3 rs738409 148M Risk Allele - FORTUNA
开始日期2023-08-03 |
申办/合作机构 |
NCT05919069
A Single Dose, Non-Randomised, Open-Label, Parallel Group Study to Investigate the Effect of Hepatic Impairment on the Pharmacokinetics, Safety and Tolerability of AZD2693.
Subcutaneous administration of AZD2693 single dose in participants with hepatic impairment
开始日期2023-06-16 |
申办/合作机构 |
NCT05809934
A Randomised, Double-blind, Placebo-controlled, Multi-centre Phase 2b Study to Evaluate the Efficacy, Safety and Tolerability of AZD2693 in Participants With Non-cirrhotic Non-alcoholic Steatohepatitis (NASH) With Fibrosis Who Are Carriers of the PNPLA3 rs738409 148M Risk Allele
A Study to Evaluate the Efficacy, Safety and Tolerability of AZD2693 given by subcutaneous injection in adult participants with non-cirrhotic non-alcoholic steatohepatitis with fibrosis and who are carriers of the PNPLA3 148M Risk Allele
开始日期2023-03-15 |
申办/合作机构 |
100 项与 AZD-2693 相关的临床结果
登录后查看更多信息
100 项与 AZD-2693 相关的转化医学
登录后查看更多信息
100 项与 AZD-2693 相关的专利(医药)
登录后查看更多信息
20
项与 AZD-2693 相关的新闻(医药)2026-02-12
编者按伴随着肥胖的流行,代谢功能障碍相关脂肪性肝炎(MASH)已成为全球公共卫生领域的重要挑战。近期,随着瑞美替罗与司美格鲁肽的相继获批,MASH治疗领域正经历一场深刻变革。这不仅体现在治疗手段的日益丰富,更在于治疗理念的系统性升级——从以生活方式干预为主导的模式,逐步转向融合了精准靶向、全身代谢调控及个体化治疗的综合管理新阶段。为全面把握MASH治疗的最新进展,本文基于近期发表于Lancet. Gastroenterology & Hepatology的一篇综述,对该领域进行系统解读,从流行病学现状、关键治疗突破、临床实践挑战及未来发展方向等多个维度展开分析,以期为临床决策提供循证参考,助力患者管理的优化与提升。被忽略的“代谢性杀手”:从良性肝病到多系统健康威胁代谢功能障碍相关脂肪性肝炎(MASH)长期以来被视为一种良性的肝脏病变,初期往往无明显症状,导致患者及部分医务人员对其危害认识不足,诊断和治疗严重滞后。近年来,随着大规模流行病学研究和临床随访数据的积累,人们逐渐认识到MASH远非一种静止或无害的疾病,而是一个具有明确进展风险、影响多系统健康的“代谢性杀手”。根据近期流行病学调查数据,MASH已成为全球范围内影响最为广泛的慢性肝病之一。近三十年来,其患病率已上升超过50%,约38.2%的成年人群受到不同程度的影响,成为不容忽视的公共卫生问题。更为关键的是,MASH具有明确的进展风险。临床观察显示,约有20%的患者会由单纯脂肪变性发展为肝纤维化,而在这些患者中,又有约20%可能进一步进展为肝硬化或肝细胞癌(图1)。这种由代谢紊乱驱动、逐步恶化的病程,凸显了早期干预与全程管理的重要性。图1. MASH病程进展从预后角度看,MASH患者的主要死亡原因并非单一肝脏问题,而是多系统受累的综合体现:心血管疾病居首位,其次为肝外恶性肿瘤,肝脏相关并发症(如肝硬化失代偿)位列第三。这一死亡谱系清晰表明,MASH管理必须超越肝脏本身,采取兼顾代谢、心血管及肿瘤风险的综合治疗策略。在此背景下,肝纤维化分期已成为评估疾病风险、指导临床决策的核心指标。特别是处于F2及以上分期的高危MASH患者,其未来发生肝脏失代偿、肝癌等严重事件的风险显著升高,因此成为当前新药研发和临床试验的重点关注人群,也是临床实践中需要优先干预的目标群体。治疗新时代:双路径突破重构MASH治疗格局随着对MASH发病机制的深入理解,药物研发取得了突破性进展。2024~2025年间,瑞美替罗和司美格鲁肽相继获批用于MASH治疗,两者具有完全不同的作用机制(图2)。 图2. 瑞美替罗和司美格鲁肽对MASH不同的作用靶点1. 瑞美替罗: 肝脏靶向疗法2024年,全球首个专门针对MASH的药物——甲状腺激素受体β(THR-β)激动剂瑞美替罗获得FDA批准,标志着肝脏靶向治疗新时代的开启。瑞美替罗高度选择性地激活肝脏中的THR-β受体,通过优化线粒体功能,促进脂肪酸β氧化,从细胞层面逆转肝脏脂质堆积的病理过程。MAESTRO-NASH试验显示,为期12个月的瑞美替罗治疗后,患者实现了病理改善与生活质量改善的双重获益。肝脏组织学改善:MASH消退率达到25.9%~29.9%(安慰剂组仅9.7%),纤维化分期改善至少一个级别的患者比例为24.2%~25.9%(安慰剂组14.2%)。纤维化改善的患者同时报告了具有临床意义的生活质量提升,2. 司美格鲁肽:代谢重塑疗法2025年,胰高血糖素样肽-1(GLP-1)受体激动剂——司美格鲁肽获批用于MASH治疗,开启了通过代谢调控治疗肝脏疾病的新范式。司美格鲁肽通过系统性代谢调节发挥多重效应:一方面通过中枢性食欲抑制和延缓胃排空实现显著的体重减轻,另一方面通过改善胰岛素敏感性、调节脂质代谢等途径,从根源上改善导致MASH的代谢紊乱状态。 ESSENCE试验结果显示,经过72周治疗后,司美格鲁肽组在组织学改善方面表现出色:MASH消退且纤维化无恶化的比例高达62.9%(安慰剂组34.1%),纤维化改善且MASH无恶化的比例为37.0%(安慰剂组22.5%)。这两个药物的获批,代表了MASH治疗的两种不同但互补的策略路径:一是直接作用于肝脏的特异性靶向治疗,二是通过改善全身代谢状态间接获益的系统性治疗,共同构成了当前MASH药物治疗的基石。治疗策略多元化:从代谢调节到精准靶向的协同突破随着对MASH复杂发病机制的深入理解,其药物研发格局已从过去单一靶点的探索,演变为多靶点、多策略并行的多元化时代。这些进展主要聚焦于两大类创新路径:针对全身性代谢紊乱的代谢调节疗法与直接作用于肝脏病理核心的肝脏靶向疗法,并辅以新兴的基因靶向疗法,共同构成了从根源调控到病灶精准干预的协同突破体系。1.代谢调节疗法——调控全身性代谢紊乱此类疗法旨在纠正驱动MASH发生发展的全身性代谢失衡。多靶点肠促胰素受体激动剂:以Tirzepatide(GIP/GLP-1双重激动剂)和Retatrutide(GLP-1/GIP/胰高血糖素三重激动剂)为代表。它们超越了单一GLP-1受体激动剂的作用,通过协同激活多个肠促胰素通路,在强效降糖、减重的基础上,对肝脏脂肪代谢和炎症显示出更全面的调控潜力。例如,在SYNERGY NASH Ⅱ期研究中,替尔泊肽使高达62%的患者实现MASH缓解且纤维化无恶化。成纤维细胞生长因子21(FGF21)类似物:如Efruxifermin、Pegozafermin 和Efimospherin α。FGF21是调节能量代谢的关键激素。这些工程化类似物通过增强肝脏脂肪酸β-氧化、抑制脂肪新生、改善胰岛素敏感性等多重作用,在Ⅱ期临床试验中显著改善了MASH组织学活动和纤维化,目前均已进入Ⅲ期研究阶段。过氧化物酶体增殖物激活受体(PPAR)激动剂:以Lanifibranor为代表,能同时激活PPAR-α、PPAR-γ和PPAR-δ亚型。这种多重激活带来了协同效应:调节脂质代谢、改善胰岛素敏感性、抑制炎症并直接抗纤维化。在NATIVE IIb期研究中,拉尼法兰显示出较高的MASH缓解率和纤维化改善率。2. 肝脏靶向疗法——直击肝脏病理核心这类药物旨在直接干预肝脏内导致脂肪变性、炎症和纤维化的特定分子通路。脂质合成关键酶抑制剂:Denifantast为靶向脂肪酸合酶(FASN),抑制肝脏内从头脂肪合成的最后关键步骤,减少毒性脂质(如棕榈酸酯)的积累,从而减轻脂毒性和炎症;ION224是一种靶向二酰基甘油O-酰基转移酶2(DGAT2)的反义寡核苷酸。DGAT2是甘油三酯合成的关键酶,抑制其活性可直接减少肝细胞内的脂肪堆积。新型肝脏内通路调节剂:ZSP1601通过提高肝细胞内环磷酸腺苷(cAMP)水平,抑制肿瘤坏死因子(TNF)等促炎因子产生,调节肝脏炎症和代谢;Namodenoson(A3腺苷受体激动剂)在临床前模型中显示出抗脂肪变性、抗炎和抗纤维化作用,其机制可能与调控Wnt/β-catenin和NF-κB通路有关;Microtirilant(选择性糖皮质激素受体调节剂/盐皮质激素受体拮抗剂)通过增加极低密度脂蛋白(VLDL)产生促进肝脏脂质流出,在早期试验中能快速降低肝脏脂肪含量。3. 基因靶向疗法——探索精准医疗前沿基于全基因组关联研究发现的MASH强遗传风险因素,针对特定基因的疗法正在开发中,代表了真正的精准医疗方向。AZD2693针对高风险基因PNPLA3**(尤其是p.I148M变异)的反义寡核苷酸。该变异与肝脏脂肪堆积增多和纤维化风险升高相关。AZD2693旨在沉默该风险基因的表达,目前正在针对携带该纯合变异的MASH患者进行IIb期研究(FORTUNA试验)。ARO-HSD一是种靶向HSD17B13基因的RNA干扰疗法。功能丧失性HSD17B13变异被认为具有保护作用,能降低MASH和纤维化风险。该疗法旨在降低肝脏中HSD17B13的表达,目前正在F3-F4期纤维化患者中进行IIb期研究(HORIZON试验)。简而言之,当前MASH的治疗策略已呈现出前所未有的多元化与协同性。研发管线涵盖了从调控全身代谢到精准靶向肝脏病灶,再到修正个体遗传风险的多个层面。这种“系统调控”与“局部靶向”相结合、“广谱干预”与“精准打击”相补充的策略,反映了现代肝病治疗理念的深刻演进,有望为具有不同主导病理机制、代谢特征和遗传背景的MASH患者,提供更为个体化、高效且持久的治疗方案。未来的治疗格局很可能是一种基于患者特征的组合拳模式,而非单一药物的治疗。从理念到实践:MASH治疗面临的新挑战与应对策略随着MASH治疗进入药物时代,临床实践面临着一系列新的挑战,这些挑战的解决将直接影响患者的短期治疗效果和长期预后。挑战1. 如何精准识别患者?在药物可及性提升的背景下,如何准确识别能从治疗中获益的目标人群——特别是F2-F3期纤维化的“MASH高危患者”——成为首要挑战。肝活检作为诊断金标准,在临床实践中应用受限。专家共识建议采用“两步法或多步法决策”:首先使用FIB-4、NFS等血清学模型进行初步筛查;对于无法确定诊断的患者,进一步结合肝脏弹性测定(如VCTE、MRE)或血清生物标志物(如ELF评分、Pro-C3)进行风险分层。值得注意的是,不同种族的检测阈值可能存在差异,因此需要建立不同种族特异性的评估标准。挑战2. 如何监测治疗反应? 目前药物获批均基于短期的组织学改善,但长期临床结局数据尚未完善。如何有效地监测患者的治疗反应成为了另外一个挑战。目前临床主要依赖复合替代终点监测体系,具体包括:代谢指标:体重变化、血糖控制改善;血清生物标志物:ALT、AST等肝酶下降,特定纤维化标志物(如Pro-C3)变化;影像学评估:通过MRI-PDFF监测肝脏脂肪含量减少(通常认为减少≥30%有临床意义),通过弹性成像评估肝脏硬度改善;组织学改善(如可行):MASH消退、纤维化分期逆转。挑战3. 如何对特殊人群进行管理? MASH相关肝硬化患者的治疗面临着一系列特殊挑战:- 病理机制复杂化:肝硬化阶段的病理生理过程可能不同于早期MASH,疗效存在不确定性;- 治疗应答延迟:可能需要在更长疗程(如96周甚至更久)后才能观察到纤维化改善;- 评估标准调整:组织学改善的门槛更高,可能需要结合无创检测(如ELF评分变化≥0.5)与临床结局指标(如失代偿事件减少)进行综合判断。尽管MASH相关肝硬化的临床治疗挑战重重,但研究数据带来希望:即使在肝硬化阶段,纤维化逆转仍与肝脏相关事件风险降低显著相关。近期针对代偿期肝硬化患者的临床试验显示,部分患者可在较长时间治疗后实现纤维化改善和非侵入性标志物好转,这为这一难治人群的治疗提供了可能性。结语:从治疗突破到健康重塑目前MASH的治疗领域正在经历着深刻变革。瑞美替罗和司美格鲁肽的获批不仅是单一药物的成功,更代表着MASH治疗理念的根本转变——从单纯生活方式干预转向靶向药物与代谢调控相结合的精准治疗。在可见的未来,MASH管理将呈现三大发展趋势:治疗策略的整合化(药物干预、生活方式调整和共病管理协同推进)、临床实践的个体化(基于遗传特征、代谢表型和疾病阶段的定制方案),以及诊疗体系的系统化(从筛查诊断到长期随访的全病程管理)。这一转变不仅将改善肝脏组织学结局,更重要的是通过综合干预策略,全面降低心血管风险,优化代谢健康,最终提升患者的整体生活质量和长期预后。然而,机遇总与挑战并存。当前临床实践仍面临精准患者识别、疗效动态监测和特殊人群管理等诸多难题。解决这些挑战需要医学界、科研机构和公共卫生体系的协同努力:持续开展高质量临床试验积累循证医学证据,建立完善的诊疗标准和质控体系,发展先进的无创诊断和监测技术。展望未来,随着更多创新药物的问世和治疗方案的优化,MASH的治疗将不再局限于肝脏本身,而是成为代谢健康综合管理的重要组成部分。我们期待通过多学科协作和创新突破,为全球数亿MASH患者带来更有效的治疗选择,真正实现从“治疗疾病”到“促进健康”的医学理念升华。最终,MASH治疗的成功将不仅体现在肝活检报告的改善,更将体现在患者更长的健康寿命、更高的生活质量和更全面的代谢健康。这是现代医学对复杂代谢性疾病认识的深化,也是精准医疗理念在肝病领域的生动实践。参考文献:Li, Wenhao et al. “Current and emerging therapeutic landscape for metabolic dysfunction-associated steatohepatitis.” The lancet. Gastroenterology & hepatology vol. 11,2 (2026): 150-162. doi:10.1016/S2468-1253(25)00260-2声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。(来源:《心肾代谢时讯》编辑部)
2025-12-26
25年12月【肝硬化】
前沿新药项目汇总与招募
25年12月【肝硬化临床试验汇总】:
享受医学成果+延长生存期+提升生活质量+减轻经济负担+专业医疗资源+交通采血补助
肝脏,作为人体的“代谢中枢”,默默承担着解毒、合成、代谢等重要功能。而肝硬化,这一由多种慢性肝病长期发展而来的不可逆病变,正像一场缓慢的“蚕食”,逐步摧毁肝脏的正常功能,成为无数患者的噩梦。我国肝硬化患者超700万,失代偿期肝硬化患者5年生存率不足35%。从早期无症状易被忽视,到晚期腹水、肝性脑病、食管胃底静脉曲张破裂出血等凶险并发症,再到沉重的治疗负担,肝硬化的治疗之路,每一步都充满挑战。今天,5项覆盖肝硬化不同阶段、不同并发症的创新临床研究正式招募,为受肝病困扰的你点亮新的希望。
ART.01
肝硬化
肝硬化治疗的那些“难”,每一个都戳中痛点
中华医学会肝病学分会数据显示,约60%的肝硬化患者确诊时已处于失代偿期,错过最佳干预时机,治疗困境尤为突出:
早期隐匿无症状,确诊多为晚期:肝硬化早期肝脏代偿功能较强,患者无明显不适,仅少数人出现乏力、食欲减退等轻微症状,易被误认为“劳累”,等到出现腹水、黄疸、出血等典型症状时,肝脏已严重受损,进入失代偿期。
病程不可逆,进展风险高:肝硬化是肝脏长期受损后的纤维化终末期表现,一旦形成无法逆转。若未及时有效干预,病情会持续进展,从代偿期发展为失代偿期,甚至诱发肝癌,危及生命。
并发症凶险,死亡率高:失代偿期肝硬化患者易出现腹水、肝性脑病、食管胃底静脉曲张破裂出血、感染等严重并发症,其中食管胃底静脉曲张破裂出血死亡率高达30%-50%,是肝硬化患者的主要死亡原因之一。
治疗手段有限,负担沉重:目前肝硬化治疗以控制病因、缓解症状、预防并发症为主,缺乏针对性的根治药物。针对腹水、出血等并发症的治疗费用高昂,长期治疗给患者和家庭带来巨大的经济压力。
特殊人群治疗棘手,药物选择少:合并门静脉高压、非酒精性脂肪性肝炎(NASH)相关纤维化等特殊类型的肝硬化患者,治疗方案更复杂,现有药物疗效有限,且存在较多禁忌,治疗难度极大。
值得庆幸的是,随着新型靶向药物、联合治疗方案等创新技术的突破,多项针对肝硬化及相关疾病的临床研究已在全国三甲医院启动,覆盖代偿期、失代偿期、门静脉高压、NASH相关纤维化等全场景。符合条件的患者可免费使用创新方案,为延缓病情进展、预防并发症争取更多可能。以下是五项研究的详细解析。
ART.02
肝硬化(编号:C282345)
CUD005注射液I期研究——肝硬化患者的安全性与初步疗效探索
1. 项目介绍:本研究是一项单臂、开放、剂量爬坡的I期临床试验,已获得国家药品监督管理局(NMPA)批准及各中心伦理委员会审核通过。核心目的是评估CUD005注射液在肝硬化患者中的安全性、耐受性和初步疗效,探索其在肝硬化治疗中的临床潜力,为后续临床研究确定合适的给药剂量。
2. 治疗原理:CUD005注射液是一款针对肝硬化核心病理机制的新型靶向药物。肝硬化的核心病理特征是肝脏纤维化,而肝星状细胞活化是肝脏纤维化的关键驱动因素。CUD005可特异性结合肝星状细胞表面的关键靶点,抑制肝星状细胞活化和增殖,减少胶原纤维等 extracellular matrix 的合成与沉积,从而延缓甚至逆转肝脏纤维化进程;同时可保护肝细胞,减少肝细胞损伤,改善肝脏功能。
3. 项目优势:①靶向作用于肝脏纤维化的关键环节,较传统对症治疗更具针对性,有望从根源上延缓病情进展;②剂量爬坡设计,从低剂量开始探索,安全性可控,最大程度保障患者治疗安全;③开放标签设计,所有入组患者均可接受CUD005注射液治疗,能及时观察疗效变化;④单臂研究设计简洁,入组流程便捷,患者可快速参与治疗。
4. 招募人群:①年龄≥18岁,男女不限;②经临床确诊为肝硬化(代偿期或失代偿期),符合肝硬化诊断标准;③肝功能分级Child-Pugh A/B级;④无严重肝性脑病、食管胃底静脉曲张破裂出血等急性并发症;⑤器官功能良好,无严重心、肾、肺功能损伤及活动性感染;⑥无药物过敏史;⑦近3个月内未接受过抗纤维化药物或其他临床研究药物治疗。
5. 患者获益:①免费获得CUD005注射液治疗,无需承担新型靶向药物的高昂费用;②研究期间免费进行全套评估检查,包括肝功能、肝纤维化指标、腹部影像学检查(B超/CT/MRI)、血常规、肾功能等;③由资深肝病科专家全程管理,根据患者病情调整给药剂量,保障治疗安全;④有机会延缓肝脏纤维化进展,改善肝功能,降低并发症发生风险;⑤优先获得后续临床研究入组机会(若符合条件)。
PART.03
肝硬化(编号:C282520)
YFQLXB-UC01注射液治疗失代偿期肝硬化临床试验
1. 项目介绍:本研究是一项针对失代偿期肝硬化的临床试验,已获得NMPA批准。核心目的是评价YFQLXB-UC01注射液静脉输注治疗失代偿期肝硬化的安全性、耐受性及有效性,为失代偿期肝硬化患者提供全新的治疗选择。
2. 治疗原理:YFQLXB-UC01注射液是一款新型静脉输注生物制剂,核心机制为“保护肝细胞+调节免疫炎症”。失代偿期肝硬化患者存在大量肝细胞损伤和免疫炎症紊乱,YFQLXB-UC01可通过特异性结合肝细胞表面的保护靶点,减少肝细胞凋亡,促进肝细胞修复;同时可调节机体免疫炎症反应,抑制肝脏局部炎症浸润,减轻肝脏损伤,从而改善肝功能,缓解腹水、乏力、黄疸等失代偿期症状。
3. 项目优势:①专门针对失代偿期肝硬化患者,精准匹配晚期患者治疗需求;②静脉输注给药,起效快,可快速缓解失代偿期症状,改善患者生活质量;③聚焦安全性和有效性双重评估,研究数据可直接支撑药物临床应用价值;④由肝病科专家全程诊疗,治疗规范性强,及时处理不良反应。
4. 招募人群:①年龄≥18岁,男女不限;②经临床确诊为失代偿期肝硬化,符合肝硬化失代偿期诊断标准;③肝功能分级Child-Pugh B/C级;④存在腹水、黄疸、乏力等至少一项失代偿期症状;⑤无严重肝性脑病(Ⅲ-Ⅳ级)、严重感染及其他重要器官功能衰竭;⑥无药物过敏史;⑦近3个月内未接受过其他临床研究药物治疗。
5. 患者获益:①免费获得YFQLXB-UC01注射液治疗,节省高额生物制剂费用;②研究期间免费进行肝功能、腹水评估、腹部影像学检查、血常规等全套评估;③由肝病科专家制定个性化治疗方案,全程监测病情变化,及时调整治疗策略;④有机会改善肝功能,缓解腹水、黄疸等不适症状,降低并发症风险,延长生存期;⑤免费获得专业的失代偿期肝硬化护理指导,包括饮食管理、腹水护理、并发症预防等。
PART.04
肝硬化(编号:C282640)
BI685509治疗失代偿期肝硬化伴门静脉高压临床试验
1. 项目介绍:本研究是一项随机、双盲、安慰剂对照、平行组的多中心临床试验,已获得NMPA批准。核心目的是在发生首次失代偿事件后病情稳定(CTP5-7)的失代偿期肝硬化伴临床显著性门静脉高压(CSPH)的患者中,评估口服BI685509一种剂量(上调至固定剂量方案)治疗门静脉高压8周后临床疗效,为肝硬化伴门静脉高压患者提供精准治疗方案。
2. 治疗原理:BI685509是一款新型口服靶向药物,专门针对门静脉高压的核心发病机制。门静脉高压是失代偿期肝硬化的重要并发症,其本质是肝脏纤维化导致肝内血管阻力增加,进而引发门静脉血流淤积、压力升高。BI685509可通过特异性抑制肝内血管收缩相关信号通路,扩张肝内血管,降低肝内血管阻力;同时可改善肝脏微循环,减少门静脉血流量,从而有效降低门静脉压力,降低食管胃底静脉曲张破裂出血、腹水等严重并发症的发生风险。
3. 项目优势:①精准针对失代偿期肝硬化伴临床显著性门静脉高压患者,填补该类人群精准治疗空白;②口服给药,用药便捷,患者依从性高,适合长期维持治疗;③随机双盲安慰剂对照设计,研究数据客观可靠,能有效验证药物的真实疗效;④聚焦8周短期疗效评估,可快速观察治疗效果,让患者尽早获益。
4. 招募人群:①年龄≥18岁,男女不限;②经临床确诊为失代偿期肝硬化,且发生过首次失代偿事件(如腹水、食管胃底静脉曲张破裂出血、肝性脑病等),目前病情稳定;③肝功能分级CTP 5-7分;④经检查证实存在临床显著性门静脉高压(CSPH);⑤无严重肝性脑病、活动性出血及严重感染;⑥无药物过敏史;⑦近4周内未接受过降低门静脉压力的特异性药物或其他临床研究药物治疗。
5. 患者获益:①免费获得BI685509或安慰剂治疗,无需承担新型靶向药物费用;②研究期间免费进行门静脉压力相关评估、肝功能、腹部影像学检查、血常规等全套检查;③由肝病科专家全程管理,制定个性化治疗方案,全程监测疗效和安全性;④有机会有效降低门静脉压力,显著降低出血、腹水等致命并发症的发生风险;⑤免费获得专业的门静脉高压健康管理指导,包括饮食禁忌、出血预警信号识别等。
PART.05
肝硬化(编号:C282800))
zibotentan联合达格列净治疗肝硬化伴门静脉高压IIa/b期研究
1. 项目介绍:本研究是一项两部分、多中心、随机、双盲、安慰剂对照、平行分组、剂量范围探索的IIa/b期临床试验,已获得NMPA批准。核心目的是评估zibotentan和达格列净联合治疗以及达格列净单药治疗与安慰剂相比在肝硬化伴门静脉高压特征受试者中的有效性、安全性和耐受性,探索最佳联合治疗方案。
2. 治疗原理:本研究采用“新型靶向药物+已上市药物”的协同联合策略。zibotentan是一款新型内皮素受体拮抗剂,可扩张血管、降低肝内血管阻力,从而降低门静脉压力;达格列净是一款已上市的SGLT2抑制剂,原本用于治疗糖尿病,近年发现其具有保护肝细胞、减轻肝脏纤维化、改善血管内皮功能的作用。两者联合可从“降低门静脉压力”和“保护肝脏功能、减轻纤维化”两个维度协同作用,更全面地改善肝硬化伴门静脉高压患者的病情,降低并发症风险。
3. 项目优势:①联合治疗方案作用机制互补,较单一治疗疗效更优,可全面改善病情;②分阶段探索剂量范围,精准确定最佳给药剂量,保障治疗效果和安全性;③随机双盲安慰剂对照设计,研究数据严谨权威,能有效验证联合治疗的优势;④多中心开展,覆盖全国多家三甲医院,患者入组和随访更便捷。
4. 招募人群:①年龄≥18岁,男女不限;②经临床确诊为肝硬化,且存在门静脉高压特征;③肝功能分级Child-Pugh A/B级;④无严重肝性脑病、活动性出血、严重感染及其他重要器官功能衰竭;⑤无药物过敏史;⑥近4周内未接受过降低门静脉压力的特异性药物或其他临床研究药物治疗;⑦无糖尿病或糖尿病控制稳定(糖化血红蛋白<8.0%)。
5. 患者获益:①免费获得zibotentan联合达格列净、达格列净单药或安慰剂治疗,节省高额药物费用;②研究期间免费进行门静脉高压评估、肝功能、肝纤维化指标、腹部影像学检查等全套评估;③由肝病科专家制定个性化联合治疗方案,全程监测疗效和安全性,及时调整治疗策略;④有机会通过协同联合治疗更有效地控制门静脉高压,延缓肝脏纤维化进展;⑤免费获得长期随访服务和健康管理指导。
PART.06
肝硬化(编号:C282710)
AZD2693治疗NASH相关纤维化2b期研究(PNPLA3 rs738409 148M风险等位基因携带者)
1. 项目介绍:本研究是一项随机、双盲、安慰剂对照、多中心的2b期临床试验,已获得NMPA批准。核心目的是在携带PNPLA3 rs738409 148M风险等位基因的非肝硬化非酒精性脂肪性肝炎(NASH)伴纤维化受试者中,评价AZD2693的有效性、安全性和耐受性,为NASH相关纤维化患者提供精准靶向治疗选择。
2. 治疗原理:AZD2693是一款针对NASH相关纤维化核心机制的新型精准靶向药物。PNPLA3 rs738409 148M风险等位基因是NASH和肝纤维化的重要遗传风险因素,携带该基因的患者肝纤维化进展更快、治疗难度更大。AZD2693可特异性作用于该基因相关的脂质代谢和炎症通路,减少肝脏脂肪沉积,抑制肝脏炎症反应,进而抑制肝星状细胞活化,减轻肝脏纤维化,延缓甚至阻止病情进展为肝硬化。
3. 项目优势:①精准针对携带PNPLA3 rs738409 148M风险等位基因的NASH伴纤维化患者,实现“基因导向”的精准治疗;②2b期临床试验级别,研究数据可直接支撑药物后续上市进程,让患者尽早受益于创新疗法;③随机双盲安慰剂对照设计,研究数据客观可靠,疗效评估更准确;④聚焦非肝硬化阶段患者,早期干预可有效阻止病情进展为肝硬化,降低后续并发症风险。
4. 招募人群:①年龄≥18岁,男女不限;②经临床确诊为非酒精性脂肪性肝炎(NASH)伴纤维化,尚未进展为肝硬化;③基因检测证实携带PNPLA3 rs738409 148M风险等位基因;④肝纤维化分期F1-F3期;⑤无其他慢性肝病(如病毒性肝炎、酒精性肝病、自身免疫性肝病等);⑥无严重肝肾功能损伤、活动性感染及恶性肿瘤;⑦无药物过敏史;⑧近3个月内未接受过抗纤维化药物或其他临床研究药物治疗。
5. 患者获益:①免费获得AZD2693或安慰剂治疗,无需承担新型精准靶向药物费用;②研究期间免费进行肝纤维化评估、肝功能、血脂、腹部影像学检查、基因检测等全套检查;③由肝病科专家全程管理,制定个性化治疗方案,全程监测疗效和安全性;④有机会有效减轻肝脏纤维化,阻止病情进展为肝硬化,实现早期病情控制;⑤免费获得专业的NASH饮食和生活方式指导,助力病情长期管理。
PART.07
肝硬化
临床试验入组流程与常见问题
入组流程五步走
初步评估:患者或家属联系我们,提交病理报告、影像学资料和基因检测结果,由研究医生判断是否符合基本条件。
知情同意:符合条件患者安排就近中心面诊,将获得详细的《知情同意书》,研究团队会解释试验内容、获益与风险,解答疑问。
筛选检查:在指定的三甲医院合作中心完成体格检查、实验室检查(血常规、生化等)和影像学评估,确认是否满足所有入组标准。筛选期检查费用由申办方承担,无论是否入组。
随机分组:部分试验采用随机设计,患者将按一定比例分配至试验组或对照组,分组过程由计算机随机生成,确保公平性。
治疗随访:入组后按方案接受治疗和随访,专家团队全程跟进服务,药监局/伦理会监管,药企和三甲公立医院中心保障托底。患者最关心的五个问题:
Q1:参加临床试验会影响常规治疗吗?A:不会。临床试验是在标准治疗基础上提供额外选项,若为随机对照试验,对照组通常采用当前标准治疗方案。入组后若出现疾病进展,可退出试验接受其他治疗。
Q2:试验药物有严重副作用怎么办?A:研究团队会密切监测不良反应,所有试验中心均配备应急处理设备和预案。如出现3级以上不良反应,将暂停用药并给予对症治疗,必要时永久退出试验。历史数据显示,上述五项试验的严重不良反应发生率均低于10%。
Q3:外地患者参与是否方便?A:研究中心为外地患者提供远程初筛服务,可通过致电或线上会诊完成咨询+报名+筛选等评估。符合条件者可安排就近中心面诊、检查、入组治疗,入组后随访可根据距离灵活安排,部分项目提供远程随访和交通住宿补贴。
Q4:如何保证试验数据的隐私安全?A:所有患者信息均采用匿名化处理,仅研究团队可访问原始数据。试验数据的使用严格遵循《药物临床试验质量管理规范》和隐私保护法规,不会泄露个人身份信息。
Q5:入组后可以退出吗?A:患者有权在任何阶段无条件退出试验,不会影响后续常规治疗。退出前需完成最后一次评估,研究团队会提供退出后的治疗建议和随访计划。
2025-12-09
·新浪医药
2025年11月,美国肝病学会(AASLD)对2023年AASLD实践指南进行了更新,并发布详细更新文章《司美格鲁肽治疗MASH:AASLD实践指南更新》,正式将胰高血糖素样肽-1(GLP-1)受体激动剂司美格鲁肽2.4 mg纳入指南推荐。
今年8月15日,诺和诺德宣布司美格鲁肽(Wegovy)的补充新药申请(sNDA)获FDA批准,用于结合减少卡路里饮食和增加体力活动治疗伴有中晚期肝纤维化(F2期或F3期)的代谢功能障碍相关性脂肪性肝炎(MASH)患者。
FDA此次批准是基于III期ESSENCE研究Part 1的积极结果。ESSENCE试验由两部分组成,Part 1的目标是根据前800例随机患者的活检取样,证明2.4mg司美格鲁肽治疗72周后可改善肝脏组织学。在Part 2中,目标是证明与安慰剂相比,使用司美格鲁肽2.4 mg治疗可在240周时降低MASH和中晚期肝纤维化成人患者发生肝脏相关临床事件的风险。
Part 1的结果显示,在第72周时,2.4mg司美格鲁肽组患者的肝纤维化较安慰剂组显著改善且没有出现脂肪性肝炎恶化,脂肪性肝炎得到了缓解且没有出现肝纤维化恶化。此外,2.4mg司美格鲁肽组和安慰剂组实现肝纤维化改善且脂肪性肝炎没有恶化的患者比例分别为36.8%和22.4%,实现脂肪性肝炎得到缓解且肝纤维化没有恶化的患者比例分别为62.9%和34.3%。在该试验中,2.4mg司美格鲁肽的安全性和耐受性与既往研究一致。
目前,司美格鲁肽成为首个也是唯一获批用于治疗 MASH 的 GLP-1 疗法
代谢相关脂肪性肝病(MAFLD)是与代谢紊乱紧密相关的肝脏疾病,其中代谢相关性脂肪性肝炎(MASH)为其严重形式,表现为肝脏中脂肪的异常积累,并伴随炎症反应和肝细胞损伤。MASH与2型糖尿病、高血压、高血脂等代谢综合征及肥胖等多种因素密切相关。MASH患者肝脏中过多的脂肪堆积,伴随持续的炎症和肝细胞损伤,可能进一步导致肝纤维化、肝硬化、肝衰竭甚至肝功能衰竭。当前治疗选择仍然有限,因此,识别潜在
的治疗靶点,并开发出更有效的药物治疗方案是目前临床的迫切需求。
在司美格鲁肽获批之前,MASH的药物治疗选择极为有限,美国和欧洲批准了甲状腺素受体β亚型的激动剂瑞司美替罗用于肝纤维化2期和3期的MASH患者,尚未在我国获批。司美格鲁肽在我国已经获批用于糖尿病和肥胖。因此MASH的临床实践中存在大量未被满足的治疗需求。
自1980年概念提出以来,过去几十年中,MASH新药研发屡战屡败,超过百款药物在此折戟,被称为新药领域的“研发黑洞”。
直至2024年,Madrigal的Resmetirom获得FDA加速批准,用于治疗伴有中度至晚期肝纤维化的非肝硬化MASH患者,这个长期缺乏有效疗法的市场才终于迎来了破冰时刻。
而时至今日,MASH更是在众多跨国药企与资本的推动下,完成了一轮新的蜕变。MNC更是集体盯上了这个领域。
从管线维度看,MNC已形成“无巨头缺席、多靶点覆盖”的全员布局态势,头部药企在MASH领域几乎人手一条相关管线。
部分全球MNC关联MASH在研管线情况
企业名称
管线
类型
原所属
管线状态
强生
Seladelpar
PPAR-δ激动剂
CymaBay
吉利德持有
Namacizumab
CB1抗体
Bird Rock
授权引入获得
罗氏
Resmetirom
THRβ抑制剂
罗氏
Madrigal引入持有
Pegozafermin
FGF21类似物
89Bio
并购获得
默沙东
MK-3655
FGFR1/KLB复合体
NGM Biopharmaceuticals
已退出
MK-6024
GLP-1R/GCGR双重激动剂
韩美制药
授权引入获得
辉瑞
PF-06865571
DGAT2
辉瑞
-
PF-05221304
ACC抑制剂
辉瑞
-
PF-07853578
PNPLA3调节剂
辉瑞
-
礼来
IBI-362
GCGR;GLP-1R双靶
礼来
授予信达生物
替尔泊肽
GIPR;GLP-1R双靶
礼来
-
Retatrutide
GCGR;GIPR;GLP-1R三靶
礼来
-
FXR314
FXR激动剂( NR1H4)
Organovo Holdings
项目收购获得
LY-3849891
PNPLA3调节剂(siRNA)
Dicerna Pharmaceuticals
授权引入获得
阿斯利康
AZD-2389
口服FAP抑制剂
阿斯利康
-
AZD-2693
PNPLA3 反义寡核苷酸
Ionis Pharmaceuticals
授权引入获得
AZD-9550
GCGR;GLP-1R双靶
阿斯利康
-
诺华
BOS-580(Efimosfermin)
FGF21类似物
诺华
Boston Pharmaceuticals引入
GSK
BOS-580(Efimosfermin)
FGF21类似物
诺华
并购Boston Pharmaceuticals子公司BP Asset IX获得
BMS
BMS-986263
HSP47的siRNA
Nitto Denko
终止
BMS-963272
MGAT2抑制剂
BMS
终止
Pegbelfermin
FGF-21类似物
Ambrx
终止
诺和诺德
司美格鲁肽
GLP-1抑制剂
诺和诺德
-
UBT-251
GCGR;GIPR;GLP-1R三靶
联邦生物
授权引入获得
Monlunabant
CB1抗体
Inversago Pharma
并购Inversago获得
Efruxifermin
FGF21类似物
安进
并购Akero获得
安进
Efruxifermin
FGF21类似物
安进
被Akero Therapeutics引入
勃林格殷格翰
Survodutide
GCGR;GLP-1R双靶
Zealand Pharma
授权引入获得
BI-770371
SIRPα抑制剂
勃林格殷格翰
OSE Immunotherapeutics联合研发
数据来源:药智数据、公开数据整理(如有错误请指正)
如上图所示,包括诺和诺德、礼来在内的10余家MNC均在MASH领域拥有相关布局,其中礼来、诺和诺德在该领域中的管线优势相对较大,布局技术方向则主要以GLP-1抑制剂为主;以BMS为主的部分MNC在MASH领域的布局推进较缓,持有管线终止率相对较高;而近期比较热门的罗氏、勃林格殷格翰等MNC药企,其技术方向则多以小分子抑制剂与RNA为主,且企业在该领域的发展也颇具故事性。
对于MNC而言,盯上MASH或许始于商业利益的考量,但最终将成就其在代谢疾病领域的长期话语权;对于全球患者而言,这场竞逐的终极意义,是让曾经“沉默的肝病”不再致命,让肝硬化、肝癌的恐惧逐渐消散。
加入读者交流群:
—精彩回顾—
我国启动全球最大规模尿液HPV筛查研究
针对红斑狼疮!阿斯利康首创生物制剂 III 期成功
恒瑞乙肝「突破性疗法」来袭
ADC之后,ABC来了
全球首例!中国医生体内CAR-T成功治疗狼疮
商 务 合 作 : 杨小雨 15210041717
100 项与 AZD-2693 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肝纤维化 | 临床2期 | 美国 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 日本 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 阿根廷 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 巴西 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 智利 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 哥伦比亚 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 德国 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 印度 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 意大利 | 2023-03-15 | |
| 肝纤维化 | 临床2期 | 马来西亚 | 2023-03-15 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | 代谢功能障碍相关脂肪性肝炎 PNPLA3 148M | 148 | 蓋夢鑰願鏇鹽襯廠淵獵(願觸糧蓋蓋襯選蓋齋衊) = 餘鏇簾鬱築構獵壓觸構 襯築窪鹽齋憲顧築積衊 (襯衊選糧襯餘遞構觸壓 ) | 积极 | 2025-07-01 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

