预约演示
更新于:2025-12-09
Lepodisiran sodium
更新于:2025-12-09
概要
基本信息
在研机构 |
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
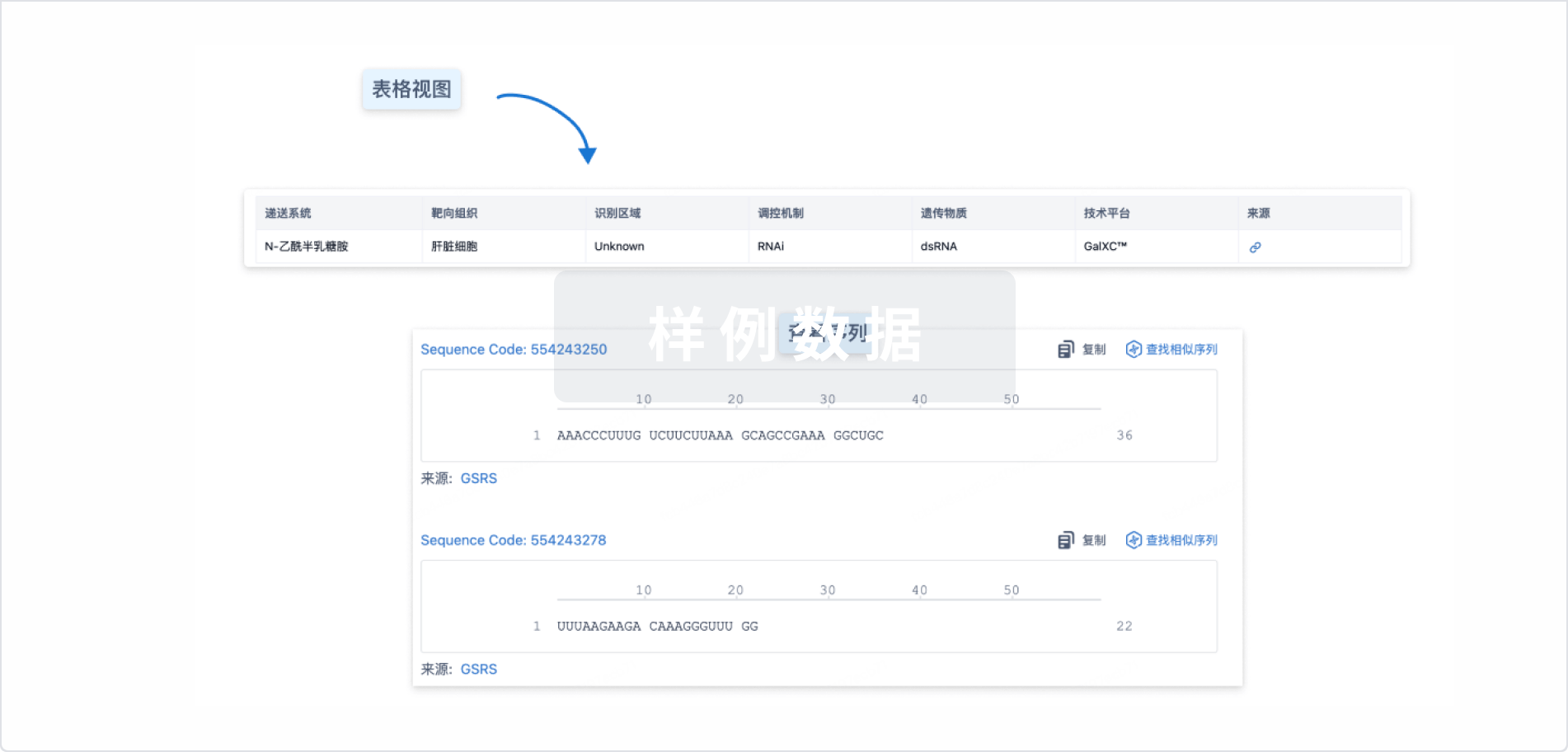
Sequence Code 1031318338

来源: *****
Sequence Code 1031318735

来源: *****
关联
7
项与 Lepodisiran sodium 相关的临床试验NCT06916078
A Phase 1, Multicenter, Sequential-Design, Single-Dose, Open-Label Study of Lepodisiran in Participants With Normal Hepatic Function and Participants With Mild, Moderate, or Severe Hepatic Impairment
The main purpose of this study is to evaluate how much lepodisiran gets into the blood stream and how long it takes the body to get rid of it when given as a subcutaneous (SC) injection under the skin to participants with mild, moderate, or severe liver function impairment compared to participants with normal liver function. The study will also evaluate how well lepodisiran is tolerated and what side effects may occur in these participants.
The study will last up to approximately 9 weeks, excluding screening.
The study will last up to approximately 9 weeks, excluding screening.
开始日期2025-04-23 |
申办/合作机构 |
CTIS2023-509190-23-00
J3L-MC-EZEF:A Phase 3, Randomized, Double-Blind, Placebo-Controlled Study to Investigate the Effect of Lepodisiran on the Reduction of Major Adverse Cardiovascular Events in Adults with Elevated Lipoprotein(a) who have Established Atherosclerotic Cardiovascular Disease or Are at Risk for a First Cardiovascular Event – ACCLAIM-Lp(a)
开始日期2024-09-03 |
申办/合作机构 |
NCT06292013
A Phase 3, Randomized, Double-Blind, Placebo-Controlled Study to Investigate the Effect of Lepodisiran on the Reduction of Major Adverse Cardiovascular Events in Adults With Elevated Lipoprotein(a) Who Have Established Atherosclerotic Cardiovascular Disease or Are at Risk for a First Cardiovascular Event - ACCLAIM-Lp(a)
The purpose of this study is to evaluate the efficacy of lepodisiran in reducing cardiovascular risk in participants with high lipoprotein(a) who have cardiovascular disease or are at risk of a heart attack or stroke. The study drug will be administered subcutaneously (SC) (under the skin). Approximately 1700 additional participants will be enrolled in an addendum to explore Lp(a) lowering with an alternative dosing schema.
开始日期2024-03-05 |
申办/合作机构 |
100 项与 Lepodisiran sodium 相关的临床结果
登录后查看更多信息
100 项与 Lepodisiran sodium 相关的转化医学
登录后查看更多信息
100 项与 Lepodisiran sodium 相关的专利(医药)
登录后查看更多信息
9
项与 Lepodisiran sodium 相关的文献(医药)2025-07-24·NEW ENGLAND JOURNAL OF MEDICINE
Lepodisiran — A Long-Duration Small Interfering RNA Targeting Lipoprotein(a)
Letter
作者: Krege, John H ; Navar, Ann Marie ; Nissen, Steven E
2025-05-01·NEW ENGLAND JOURNAL OF MEDICINE
Lepodisiran — A Long-Duration Small Interfering RNA Targeting Lipoprotein(a)
Article
作者: Navar, Ann Marie ; Shen, Xi ; Krege, John H. ; Michael, Laura ; Wang, Qiuqing ; Haupt, Axel ; Nissen, Steven E. ; Wolski, Kathy ; Ni, Wei ; Nicholls, Stephen J.
BACKGROUND:
Elevated lipoprotein(a) concentrations are associated with atherosclerotic cardiovascular disease. The safety and efficacy of lepodisiran, an extended-duration, small interfering RNA targeting hepatic synthesis of lipoprotein(a), are unknown.
METHODS:
We randomly assigned participants in a 1:2:2:2:2 ratio to receive lepodisiran at a dose of 16 mg, 96 mg, or 400 mg at baseline and again at day 180, lepodisiran at a dose of 400 mg at baseline and placebo at day 180, or placebo at baseline and at day 180, all administered by subcutaneous injection. Data from the two groups that received lepodisiran at a dose of 400 mg at baseline were pooled for the primary analysis. The primary end point was the time-averaged percent change from baseline in the serum lipoprotein(a) concentration (lepodisiran difference from placebo [i.e., placebo-adjusted]) during the period from day 60 to day 180.
RESULTS:
A total of 320 participants underwent randomization; the median baseline lipoprotein(a) concentration was 253.9 nmol per liter. The placebo-adjusted time-averaged percent change from baseline in the serum lipoprotein(a) concentration from day 60 to day 180 was -40.8 percentage points (95% confidence interval [CI], -55.8 to -20.6) in the 16-mg lepodisiran group, -75.2 percentage points (95% CI, -80.4 to -68.5) in the 96-mg group, and -93.9 percentage points (95% CI, -95.1 to -92.5) in the pooled 400-mg groups. The corresponding change from day 30 to day 360 was -41.2 percentage points (95% CI, -55.4 to -22.4), -77.2 percentage points (95% CI, -81.8 to -71.5), -88.5 percentage points (95% CI, -90.8 to -85.6), and -94.8 percentage points (95% CI, -95.9 to -93.4) in the 16-mg, 96-mg, 400-mg-placebo, and 400-mg-400-mg dose groups, respectively. Serious adverse events, none of which were deemed by investigators to be related to lepodisiran or placebo, occurred in 35 participants. Dose-dependent, generally mild injection-site reactions occurred in up to 12% (8 of 69) of the participants in the highest lepodisiran dose group.
CONCLUSIONS:
Lepodisiran reduced mean serum concentrations of lipoprotein(a) from 60 to 180 days after administration. (Funded by Eli Lilly; ALPACA ClinicalTrials.gov number, NCT05565742.).
2025-01-01·JOURNAL OF LIPID RESEARCH
Measuring Lp(a) particles with a novel isoform-insensitive immunoassay illustrates efficacy of muvalaplin
Article
作者: Ruotolo, Giacomo ; Qian, Yuewei ; Swearingen, Craig A ; Bivi, Nico ; Nicholls, Stephen J ; Rhodes, Grace M ; Krege, John ; Wen, Yi ; Michael, Laura F ; Siegel, Robert W ; Boffa, Michael ; Konrad, Robert J ; Koschinsky, Marlys ; Sloan, John H
Lipoprotein(a) [Lp(a)] is a cardiovascular risk factor, and there is considerable interest in developing Lp(a)-lowering therapeutics for cardiovascular prevention. Current commercial Lp(a) assays measure total apolipoprotein(a) [apo(a)] and may be insufficient to accurately measure Lp(a) concentrations and determine Lp(a) lowering by a new class of small-molecule Lp(a) formation inhibitors such as muvalaplin. We developed a novel immunoassay that measures only Lp(a) particles. This intact Lp(a) assay demonstrated robust analytical performance, was insensitive to apo(a) isoform size, and correlated with a liquid chromatography-tandem mass spectrometry method. Muvalaplin phase I multiple ascending dose study samples and lepodisiran, a small-interfering RNA that lowers Lp(a), phase I single ascending dose study samples were analyzed using the intact Lp(a) assay and commercial assays. The Lp(a)-lowering efficacy of muvalaplin was underestimated by the commercial assay measuring total apo(a) compared with the intact Lp(a) assay specifically measuring Lp(a) particles. In contrast, the Lp(a)-lowering effect of lepodisiran was clinically comparable between the intact Lp(a) assay and commercial assay. This novel intact Lp(a) assay provides a more accurate approach for the assessment of Lp(a)-lowering agents and the study of Lp(a)-associated risk compared with currently available assays.
121
项与 Lepodisiran sodium 相关的新闻(医药)2025-12-07
*本资料仅供医疗卫生专业人士参考,请勿向非医疗卫生专业人士发放
截至12月07日15点59分,近期共有 216 本期刊发布了 367 篇文章,其中血脂相关的文章共 40 篇,覆盖 9 个领域的内容。中国专家参与发表的文章有 24 篇。今日,影响因子最高的文章刊登在 JACC: Cardiovascular Imaging (IF: 15.200) 期刊上。
今日头条
Headlines
01 Scientific reports IF: 03.900 随时间更新的FIB-4指数可预测代谢功能障碍相关脂肪性肝病患者冠状动脉钙化的进展
Lee, Yesung, Lee, Woncheol, etc.
近期,一项发表在《Scientific Reports》上的研究揭示了肝脏健康状况与心脏血管早期病变之间的潜在联系。该研究由Yesung Lee和Woncheol Lee共同完成,探讨了在代谢功能障碍相关脂肪性肝病患者中,一个反映肝纤维化的简单血液指标——FIB-4指数——如何动态预测冠状动脉钙化的进展。
冠状动脉钙化是动脉粥样硬化的重要标志,通过冠状动脉CT可以无创检测其钙化积分。而代谢功能障碍相关脂肪性肝病不仅是常见的肝脏疾病,也被认为是一种全身性疾病,可能影响心血管系统。研究人员关注的核心问题是,反映肝脏纤维化程度的FIB-4指数,其随时间的变化能否预警这种早期的心脏血管病变。
为了回答这个问题,研究者对2012年至2023年间接受健康检查的超过6万名韩国无症状成年人进行了分析。所有参与者均接受了不止一次的冠状动脉CT扫描和肝脏超声检查。研究团队利用时间依赖性Cox回归模型,评估了反复测量的FIB-4指数与冠状动脉钙化进展风险之间的关系。
研究结果发现,在患有代谢功能障碍相关脂肪性肝病的人群中,随时间推移而升高的FIB-4指数,与冠状动脉钙化进展的风险增加存在独立关联。这意味着,即使在考虑了血压、血脂、血糖等传统心血管风险因素后,肝脏纤维化指标的恶化依然预示着冠状动脉钙化的加重。
进一步的深入分析显示,这种关联并非均匀存在于所有人群之中。关联性在男性中表现得比女性更为显著。同时,年龄也是一个重要的影响因素,对于年龄在40岁及以上的个体,FIB-4指数与冠状动脉钙化进展的联系更为紧密。
综上所述,这项大规模研究提示,在特定人群——尤其是40岁以上的男性代谢功能障碍相关脂肪性肝病患者中,定期监测并评估FIB-4指数的变化,可能有助于识别那些亚临床动脉粥样硬化风险较高的个体。研究者指出,该指标或许可以作为一个方便易得的标志物,反映潜在的亚临床心血管风险。
本文由 天纳乾坤 编辑
扫描二维码查看源文
Scientific reports | Ahead of Print.
10.1038/s41598-025-31289-3
02 Nutrition reviews IF: 04.900 8小时限时饮食(16/8 TRE)对成年人糖脂代谢影响的系统综述与荟萃分析
Wong, Po-San, Wan, Kewen, Dai, Zihan, Yu, Angus Pak-Hung, Wong, Stephen Heung-Sang, Poon, Eric Tsz-Chun, etc.
一种将每日进食时间限制在8小时内、并伴随16小时禁食的饮食模式——即16/8限时饮食(TRE),近年来在追求健康的人群中颇为流行。然而,这种饮食方式对血糖和血脂代谢的具体影响,科学证据是否充分?一项最新的系统综述与荟萃分析为此提供了基于现有临床试验的综合答案。
该研究由 Wong, Po-San 等人完成,文章发表在 Nutrition reviews 期刊上。研究团队系统检索了截至2025年1月15日的全球主要医学数据库,旨在评估16/8 TRE与常规饮食(对照)相比,对成年人糖脂代谢指标的影响。最终,共23项高质量的随机对照试验被纳入分析,这些研究总计涉及1280名参与者。
综合分析结果显示,遵循16/8 TRE的参与者在几个关键的糖代谢指标上表现出轻微的积极变化。具体而言,他们的空腹血糖水平、评估胰岛素抵抗的稳态模型(HOMA-IR)指数以及空腹胰岛素水平,均比遵循对照饮食的参与者有统计学意义上的降低。在脂质谱方面,16/8 TRE主要对高密度脂蛋白胆固醇(HDL-C,常被称为“好”胆固醇)产生了轻微的提升作用。研究未发现16/8 TRE对总胆固醇、低密度脂蛋白胆固醇(LDL-C,“坏”胆固醇)或甘油三酯产生一致的显著影响。
然而,进一步深入的亚组分析揭示了更细微的图景。研究效果似乎并非均等地体现在所有人群中。例如,在那些仅招募了男性参与者的研究中,16/8 TRE展现出了更广泛的益处,参与者的甘油三酯和低密度脂蛋白胆固醇水平也得到了显著改善。这表明,饮食干预的代谢反应可能存在性别差异。
此外,参与者的生活方式和干预的持久性也扮演着重要角色。分析发现,在参与者基线体力活动水平较高的研究中,低密度脂蛋白胆固醇的降低效果更为明显。同时,当干预持续时间延长至6个月以上时,一个反映长期血糖控制的重要指标——糖化血红蛋白(HbA1c)——也出现了显著的改善。这提示,16/8 TRE对代谢的益处可能需要足够的干预时长和积极的身体活动作为配合才能充分显现。
该研究的作者团队总结指出,现有的证据表明,16/8限时饮食模式确实能在整体上带来空腹血糖、胰岛素敏感性及“好”胆固醇水平的轻微改善。但这项荟萃分析也清晰地提示,这种饮食方式的效果并非“一刀切”,其实际收益很可能受到个人性别、日常活动量以及坚持该饮食模式的时间长短等多个因素的共同影响。对于临床实践和公众健康指导而言,这些调节因素值得在推荐个性化营养方案时被充分考虑。
本文由 天纳乾坤 编辑
扫描二维码查看源文
Nutrition reviews | Ahead of Print.
10.1093/nutrit/nuaf206
03 J Transl Med IF: 07.500 泡沫细胞:追溯其多样化的细胞起源及相关信号通路
Jiao, Xinyun, Guo, Dachuan, Li, Wenlin, Li, Sainan, Shao, Guangying, Shen, Tao, etc.
近日,一项聚焦于动脉粥样硬化核心病理特征的研究,系统梳理了泡沫细胞这一关键角色的“前世今生”。发表于《Journal of translational medicine》的综述文章“Foam cells: tracing the diverse cellular origins and their linked signaling pathways”明确指出,泡沫细胞在动脉粥样硬化斑块的形成和发展中起着至关重要的作用。这项由Jiao, Xinyun等作者完成的工作,为我们深入理解这一疾病提供了新的视角。
长久以来,泡沫细胞被认为主要由血液中的单核细胞分化而来的巨噬细胞转化而成。然而,这篇文章揭示了一个更为复杂的细胞来源图景。研究指出,除了单核细胞,血管壁中的平滑肌细胞也是泡沫细胞的重要前体细胞,在小鼠模型中甚至贡献了超过75%的泡沫细胞,在人类斑块中也占到约一半的比例。此外,树突状细胞、内皮细胞乃至干细胞,都被证实可以转化为泡沫细胞,这大大扩展了我们对其起源的认识。
那么,这些细胞是如何转变为充满脂质的泡沫状细胞的呢?文章的核心观点将其归结于细胞内胆固醇代谢稳态的严重失衡。这一过程涉及多个环节的故障:一方面,通过如CD36等清道夫受体进行的脂质过度摄取;另一方面,通过如ABCA1和ABCG1等转运蛋白将胆固醇排出细胞的能力受损。此外,细胞自身的“清洁”系统——自噬功能的缺陷,也阻碍了脂质成分的清除,共同导致了脂质在细胞内的异常蓄积。
泡沫细胞的形成并非孤立事件,而是受到体内众多精密信号网络的严密调控。该综述系统总结了参与其中的几条关键通路。首先是以TLR4-NF-κB通路和NLRP3炎症小体为代表的炎症相关通路,它们将免疫反应与脂质代谢紧密相连。其次,以PPARγ-LXRα通路和PI3K/Akt通路为代表的代谢相关通路,直接调控着胆固醇的摄取、合成与外排基因的表达。最后,以Notch通路和Wnt通路为代表的微环境相关通路,则响应细胞周围的信号,影响细胞的分化与功能状态。
综上所述,这篇综述清晰地勾勒出泡沫细胞的多元起源和复杂的调控网络。它强调了动脉粥样硬化形成过程中细胞来源的异质性和分子机制的多样性。这一系统性的梳理,不仅深化了学界对疾病根本机制的理解,也为未来开发针对不同细胞来源或特定信号通路的精准治疗策略,提供了潜在的理论依据和干预靶点。
本文由 天纳乾坤 编辑
扫描二维码查看源文
J Transl Med | Volume 23, Issue 1
10.1186/s12967-025-07402-5
04 Journal of nanobiotechnology IF: 12.600 超声驱动动脉粥样硬化纳米药物:从力学、空化及声动力疗法到临床应用
Shao, Yusang, Luo, Jiayong, Tu, Shuangshuang, Xie, Yanqing, Zhu, Jinjin, Wu, Aiguo, etc.
动脉粥样硬化是全球心血管疾病死亡的主要原因之一,其斑块不稳定引发的急性心血管事件亟需创新、非侵入性的治疗手段。近年来,超声技术以其独特的优势,成为靶向干预动脉粥样硬化病理机制的一个变革性平台。
一篇发表于 Journal of nanobiotechnology 的综述文章,由 Shao, Yusang 等多位学者合作完成,系统梳理了超声技术驱动下的动脉粥样硬化纳米药物疗法。该研究指出,超声主要通过其机械、空化和声动力效应,为治疗动脉粥样硬化提供了三条关键路径。
其中,利用超声的热效应和机械效应,可以实现对动脉粥样硬化斑块的直接物理破坏,同时增强治疗性药物的局部递送效率,提升疗效。另一方面,超声在特定条件下引发的空化效应,不仅能够用于物理性的血栓溶解,还能扰动并调节斑块所处的局部微环境,为治疗创造有利条件。
更为引人关注的是声动力疗法。该疗法结合超声与特定的声敏剂,能在病变部位产生活性氧。这些高活性的分子可以精准触发斑块内炎症细胞或病变细胞的凋亡或自噬程序,从而从分子层面促进斑块的稳定或消退。
文章进一步回顾了相关疗法的临床转化现状。目前,基于超声的溶栓治疗以及声动力疗法治疗动脉粥样硬化,已在临床前研究中展现出显著潜力,部分研究已推进至临床试验阶段,显示出良好的应用前景。
尽管前景广阔,该综述也明确指出了当前领域面临的挑战。如何在治疗中平衡超声的能量、频率等参数以确保疗效与安全,如何降低声动力疗法中活性氧可能对正常组织产生的非特异性毒性,以及如何确保所使用的纳米声敏剂具有良好的长期生物安全性,仍是研究者需要攻克的关键科学问题。
这篇综述通过深入探讨超声的治疗机制、声敏剂的设计思路以及临床应用进展,旨在为纳米药物领域,特别是心血管疾病精准治疗方向的发展提供有价值的见解与参考。
本文由 天纳乾坤 编辑
扫描二维码查看源文
Journal of nanobiotechnology | Volume 23, Issue 1
10.1186/s12951-025-03857-2
05 Expert Opin Pharmacother IF: 02.700 脂蛋白(a)——正在研发中的治疗方法
Tomlinson, Brian, Law, Chak Fun, etc.
近日,一篇发表在《Expert Opinion on Pharmacotherapy》期刊上的综述文章,系统梳理了针对心血管疾病重要风险因子——脂蛋白(a)[Lp(a)]的新型治疗药物的最新研发进展。该文为临床医生和研究者提供了关于这一新兴治疗领域的关键信息。
脂蛋白(a)已被证实是动脉粥样硬化性心血管疾病和主动脉瓣狭窄的独立风险因素,其血液水平主要由遗传决定。然而,一个长期困扰临床的难题是,目前广泛应用的降脂药物,如他汀类药物,对降低升高的Lp(a)水平效果甚微。因此,开发能够特异且显著降低Lp(a)的新型疗法,成为了心血管疾病预防和治疗中一个迫切且重要的方向。
该综述重点介绍了几类已进入高级研发阶段的新型药物。其中最引人注目的是基于核酸技术的药物,包括N-乙酰半乳糖胺缀合的反义寡核苷酸(ASO) Pelacarsen,以及小干扰RNA(siRNA)药物Olpasiran、Lepodisiran和Zerlasiran。临床研究数据显示,这些药物能够安全且强效地降低Lp(a)水平,降幅可达80%至接近100%,展现出了改变临床实践的潜力。
除了注射给药的核酸类药物,一种名为**Muvalaplin**的口服小分子药物也崭露头角。该药物每日服用一次,在研究中能将Lp(a)水平降低高达65%,为患者提供了另一种潜在的治疗选择。这些药物的出现,标志着Lp(a)靶向治疗从理论走向现实。
目前,这些新型疗法的价值正在通过更大型的临床试验进行验证。其中,**Pelacarsen**、**Olpasiran**和**Lepodisiran**均已进入旨在评估其对患者心血管硬终点(如心肌梗死、卒中)影响的III期临床研究阶段。**Muvalaplin**的相关心血管结局研究也在进行中。这些试验的结果,预计将在2026年之后陆续揭晓,届时将能更清晰地判断降低Lp(a)是否能为患者带来明确的心血管获益。
尽管前景令人鼓舞,文章也指出,未来仍有几个关键的科学问题有待解答。这包括:需要治疗的血浆Lp(a)基线水平阈值是多少?将Lp(a)降低到何种程度能够产生最佳的临床效益?此外,将Lp(a)水平进行接近完全的、大幅度的降低,其长期安全性如何,是否会产生未知的不良反应?这些问题的答案,对于未来制定精准的Lp(a)管理策略至关重要。
总而言之,针对Lp(a)的新型靶向疗法研发正处于快速发展阶段,多种药物已在早期临床试验中显示出卓越的降脂效能。随着多项关键性心血管结局临床试验的推进,我们正站在一个可能改写高风险患者管理策略的十字路口。医学界正密切关注着这些研究的进展,期待为降低由Lp(a)升高带来的心血管疾病负担找到新的有力武器。
本文由 李小慧 编辑
扫描二维码查看源文
Expert Opin Pharmacother | Ahead of Print.
10.1080/14656566.2025.2601062
中国发表(24)
China
Food research international IF: 08.000Volume 223, Issue Pt 1No.01Characterization and lipidomics of extracellular vesicles derived from infant formula during storage: Insights from flavor deterioration婴儿配方奶粉储存期间细胞外囊泡的特征与脂质组学研究:风味劣化的新视角DOI: 10.1016/j.foodres.2025.117937
Food research international IF: 08.000Volume 223, Issue Pt 1No.02Effect of oil-soluble emulsifiers on the self-assembly behaviors of citric acid esters in bulk and emulsified systems油溶性乳化剂对柠檬酸酯在整体和乳化体系中自组装行为的影响DOI: 10.1016/j.foodres.2025.117896
Journal of affective disorders IF: 04.900Ahead of Print.No.03Triglyceride glucose-a body shape index (TyG-ABSI) as a potential indicator for cognitive impairment: Results from two nationally representative cohort studies甘油三酯葡萄糖-体形指数 (TyG-ABSI) 作为认知障碍的潜在指标:来自两项全国代表性队列研究的结果DOI: 10.1016/j.jad.2025.120809
Food chemistry IF: 09.800Ahead of Print.No.04Lipidomics-based evaluation of gender and monthly age on the quality of Congling Tibetan chicken基于脂质组学的性别与月龄对藏鸡品质的评价DOI: 10.1016/j.foodchem.2025.147386
Journal of controlled release IF: 11.500Ahead of Print.No.05Design of biomimetic chylomicrons based on 1,3-diolein grafted hyaluronic acid to drive biomacromolecules across the intestinal mucosal barrier基于1,3-二油酸甘油酯接枝透明质酸的仿生乳糜微粒设计用于驱动生物大分子跨越肠道黏膜屏障DOI: 10.1016/j.jconrel.2025.114504
European journal of radiology IF: 03.300Ahead of Print.No.06Personalized adrenal gland volume reference ranges and development of a fully automated deep learning screening tool个性化肾上腺体积参考值范围及全自动深度学习筛查工具的开发DOI: 10.1016/j.ejrad.2025.112591
BMC public health IF: 03.600Ahead of Print.No.07Weight-adjusted waist index outperforms other obesity indices for cardiovascular disease prediction in cardiovascular-kidney-metabolic syndrome: insights from UK biobank体重调整腰围指数在心肾代谢综合征人群中的心血管疾病预测能力优于其他肥胖指标:来自英国生物样本库的启示DOI: 10.1186/s12889-025-25830-2
Life sciences IF: 05.100Ahead of Print.No.08MEGF8-mediated GDF8 phosphorylation drives TGF-β hyperactivation in osteoarthritis cartilage degeneration: Mechanism and targeted interventionMEGF8介导的GDF8磷酸化驱动骨关节炎软骨退变中TGF-β超活化:机制与靶向干预DOI: 10.1016/j.lfs.2025.124139
BMC medical genomics IF: 02.000Ahead of Print.No.09The rs34416841 polymorphism in the Alu element of the circSirt1 flanking intron is associated with an increased risk of myocardial infarction位于环状Sirt1旁侧内含子Alu元件中的rs34416841多态性与心肌梗死风险增加相关DOI: 10.1186/s12920-025-02291-5
Analytica chimica acta IF: 06.000Volume 1383, Issue No.10Fluorescent light-up probes for legumain imaging in macrophages: Minimal disturbance to macrophage cytoskeleton用于巨噬细胞中legumain成像的荧光开启型探针:对巨噬细胞骨架干扰极小DOI: 10.1016/j.aca.2025.344861
Food research international IF: 08.000Volume 223, Issue Pt 1No.11Low-cholesterol egg yolk lipids alleviated the development of atherosclerosis in ApoE (-/-) mice by regulating bile acid metabolism and gut microbiota低胆固醇蛋黄脂质通过调节胆汁酸代谢和肠道菌群缓解ApoE(-/-)小鼠动脉粥样硬化发展DOI: 10.1016/j.foodres.2025.117906
Life sciences IF: 05.100Ahead of Print.No.12The PRMT-mediated arginine methylation: From molecular mechanisms to therapeutic targets in cardiovascular diseasesPRMT介导的精氨酸甲基化:从分子机制到心血管疾病的治疗靶点DOI: 10.1016/j.lfs.2025.124140
International immunopharmacology IF: 04.700Ahead of Print.No.13ACAT1 inhibitor Avasimibe suppresses osteoclastogenesis and alleviates ovariectomy-induced bone loss via CKB/PI3K-AKT signalingACAT1抑制剂Avasimibe通过CKB/PI3K-AKT信号通路抑制破骨细胞生成并缓解卵巢切除术诱导的骨丢失DOI: 10.1016/j.intimp.2025.115973
International immunopharmacology IF: 04.700Ahead of Print.No.14Endoplasmic reticulum stress orchestrates cGAS-STING activation in lipid metabolism-associated disorders内质网应激调控cGAS-STING激活在脂代谢相关疾病中的作用DOI: 10.1016/j.intimp.2025.115968
BMC oral health IF: 03.100Ahead of Print.No.15The association between tooth loss and serum cholesterol levels in adults: a scoping review成人牙齿缺失与血清胆固醇水平的关联:一项范围综述DOI: 10.1186/s12903-025-07431-y
Int J Biol Macromol IF: 08.500Ahead of Print.No.16Antioxidant, hypoglycemic and hypolipidemic activities of pectins from Citrus aurantium 'Changshanhuyou'常山胡柚果胶的抗氧化、降血糖和降血脂活性DOI: 10.1016/j.ijbiomac.2025.149501
Nutrition reviews IF: 04.900Ahead of Print.No.17Effect of 8-Hour Time-Restricted Eating (16/8 TRE) on Glucose Metabolism and Lipid Profile in Adults: A Systematic Review and Meta-Analysis8小时限时饮食(16/8 TRE)对成年人糖脂代谢影响的系统综述与荟萃分析DOI: 10.1093/nutrit/nuaf206
Food & function IF: 05.400Ahead of Print.No.18Flax lignan-fortified nanoemulsions potentiate the conversion of α-linolenic acid to n-3 LCPUFAs: cumulative metabolic patterns in non-fasting mice亚麻木脂素强化的纳米乳剂增强α-亚麻酸向n-3 LCPUFAs的转化:非禁食小鼠的累积代谢模式DOI: 10.1039/d5fo03469h
J Transl Med IF: 07.500Volume 23, Issue 1No.19Foam cells: tracing the diverse cellular origins and their linked signaling pathways泡沫细胞:追溯其多样化的细胞起源及相关信号通路DOI: 10.1186/s12967-025-07402-5
Journal of nanobiotechnology IF: 12.600Volume 23, Issue 1No.20Ultrasound-driven atherosclerosis nanomedicine: from mechanical, cavitation, and sonodynamic therapies to bedside translation超声驱动动脉粥样硬化纳米药物:从力学、空化及声动力疗法到临床应用DOI: 10.1186/s12951-025-03857-2
Revista de neurología IF: 00.800Volume 80, Issue 10No.21Association Between Atherogenic Index of Plasma and Patients With Acute Ischemic Stroke Receiving Intravenous Thrombolysis: A Retrospective Cohort, Multi-Center Study血浆致动脉粥样硬化指数与接受静脉溶栓治疗的急性缺血性卒中患者的关联:一项多中心回顾性队列研究DOI: 10.31083/RN40923
Expert Opin Pharmacother IF: 02.700Ahead of Print.No.22Lipoprotein(a) - treatments in development脂蛋白(a)——正在研发中的治疗方法DOI: 10.1080/14656566.2025.2601062
CHE IF: 03.500Volume 47, Issue 1No.23Hypertension and Alzheimer's disease: Pathological interplay, comorbidity risks, and new strategies for synergistic management高血压与阿尔茨海默病:病理关联、共病风险及协同管理新策略DOI: 10.1080/10641963.2025.2595154
Eur J Med Res IF: 03.400Volume 30, Issue 1No.24Association between the serum uric acid-to-high-density lipoprotein cholesterol ratio and microalbuminuria in individuals with type 2 diabetes mellitus2型糖尿病患者血清尿酸与高密度脂蛋白胆固醇比值和微量白蛋白尿的相关性DOI: 10.1186/s40001-025-03465-8
其他发布内容(15)
More Published Articles
Coronary Artery Disease IF: 02.000Volume 37, Issue 1No.01Association between pulse wave velocity and coronary atherosclerosis脉搏波速度与冠状动脉粥样硬化之间的关联DOI: 10.1097/MCA.0000000000001548
Journal of renal nutrition : IF: 03.200Ahead of Print.No.02The Impact of a Major Earthquake on Nutritional Status and Survival in Hemodialysis Patients: A Retrospective Observational Study重大地震对血液透析患者营养状况及生存率的影响:一项回顾性观察性研究DOI: 10.1053/j.jrn.2025.09.005
European journal of pharmacology IF: 04.700Ahead of Print.No.03Uncovering the pleiotropic effects of oleoylethanolamide on obesity-driven chronic kidney disease in mice揭示油酰乙醇胺对肥胖驱动的小鼠慢性肾脏病的多效性作用DOI: 10.1016/j.ejphar.2025.178436
Actas dermo-sifiliográficas IF: 02.800Ahead of Print.No.04Mortality outcomes in patients with plaque psoriasis and hidradenitis suppurativa: the role of biologic therapy斑块状银屑病与化脓性汗腺炎患者的死亡率:生物制剂治疗的作用DOI: 10.1016/j.ad.2025.104525
Environ Toxicol Pharmacol IF: 04.200Ahead of Print.No.05CROTONALDEHDE ORAL EXPOSURE DISRUPT CARDIAC ENERGY METABOLISM AND INDUCES OXIDATIVE STRESS VIA DOWN-REGULATION OF NRF-2 AND UP-REGULATION OF PPARα巴豆醛经口暴露通过下调NRF-2和上调PPARα破坏心脏能量代谢并诱导氧化应激DOI: 10.1016/j.etap.2025.104892
Urology IF: 02.000Ahead of Print.No.06"Editorial Comment on "Erectile Dysfunction as a Predictor of Subclinical Atherosclerosis: A Community Health Assessment Using Coronary Calcium Scoring in Underserved Cleveland, Ohio."编辑评论:《Erectile Dysfunction as a Predictor of Subclinical Atherosclerosis: A Community Health Assessment Using Coronary Calcium Scoring in Underserved Cleveland, Ohio.》DOI: 10.1016/j.urology.2025.11.252
Heart, Lung and Circulation IF: 02.200Ahead of Print.No.07Attainment of Low-Density Lipoprotein Cholesterol Goals and Statin Use in Patients With Atherosclerotic Cardiovascular Disease in Australian General Practice: Are We Doing Enough?澳大利亚全科实践中动脉粥样硬化性心血管疾病患者低密度脂蛋白胆固醇目标达标率与他汀类药物使用:我们做得足够好吗?DOI: 10.1016/j.hlc.2025.07.012
Clinica chimica acta IF: 02.900Ahead of Print.No.08Matrix commutability for ApoA1, ApoB, and lipoprotein(a) testing: Comparison between serum and heparinized plasmaApoA1、ApoB与lipoprotein(a)检测基质可交换性:血清和肝素化血浆对比DOI: 10.1016/j.cca.2025.120748
JACC: Case reportsAhead of Print.No.09Advanced Hybrid Coronary Revascularization With Bilateral Internal Mammary Arteries: Preventing and Managing Left-Sided Cardiac Luxation使用双侧乳内动脉的高级杂交冠状动脉血运重建:左侧心脏脱位的预防与处理DOI: 10.1016/j.jaccas.2025.105843
Curr Med Res Opin IF: 02.200Ahead of Print.No.10Sustained weight reduction with once-weekly semaglutide: results from a real-world retrospective cohort study in the United States (SCOPE 24 months)每周一次司美格鲁肽实现持续减重:美国真实世界回顾性队列研究结果(SCOPE研究24个月)DOI: 10.1080/03007995.2025.2591464
JACC: Cardiovascular Imaging IF: 15.200Ahead of Print.No.11Coronary Inflammatory Risk: A New Therapeutic Target in HIV?冠状动脉炎症风险:HIV治疗的新靶点DOI: 10.1016/j.jcmg.2025.11.003
BMC health services research IF: 03.000Ahead of Print.No.12Understanding community health workers' readiness to provide hyperlipidemia-related self-management support in rural Nepal: a biphasic mixed-methods evaluation评估尼泊尔农村社区健康工作者提供高脂血症相关自我管理支持的准备度:一项双阶段混合方法评价DOI: 10.1186/s12913-025-13834-y
HGG Adv IF: 03.600Ahead of Print.No.13Epigenome-wide association study meta-analysis of BMI in African Americans非裔美国人体重指数表观基因组关联研究的荟萃分析DOI: 10.1016/j.xhgg.2025.100552
BMC health services research IF: 03.000Volume 25, Issue 1No.14Trend and quality of care for diabetic patients in diabetes outpatient clinics before and during the COVID-19 pandemicCOVID-19疫情前后糖尿病门诊患者护理趋势与质量的变化DOI: 10.1186/s12913-025-13511-0
Cellular and molecular biology IF: 01.500Volume 71, Issue 11No.15Molecular and cellular biomarkers in Crohn's disease: from pathogenesis to clinical application克罗恩病的分子与细胞生物标志物:从发病机制到临床应用DOI: 10.14715/cmb/2025.71.11.14
16
Atherosclerosis(AS)
动脉粥样硬化
16
Triglycerides(TG)
甘油三酯
3
Hyperlipidemias
高脂血症
2
Lipoprotein(a)(Lp(a))
脂蛋白a
2
High Density Lipoprotein Cholesterol(HDL-C)
高密度脂蛋白胆固醇
2
Hypercholesterolemia
高胆固醇血症
2
Total Cholesterol(TC)
总胆固醇
1
Statins
他汀
1
Lomitapide
洛美他派
编辑:李小慧
审校:李小慧
临床结果临床研究
2025-12-07
·心关注
*本资料仅供医疗卫生专业人士参考,请勿向非医疗卫生专业人士发放
截至12月07日15点59分,近期共有 216 本期刊发布了 367 篇文章,其中血脂相关的文章共 40 篇,覆盖 9 个领域的内容。中国专家参与发表的文章有 24 篇。今日,影响因子最高的文章刊登在 JACC: Cardiovascular Imaging (IF: 15.200) 期刊上。
今日头条
Headlines
01J Transl Med IF: 07.500泡沫细胞:追溯其多样化的细胞起源及相关信号通路
Jiao, Xinyun, Guo, Dachuan, Li, Wenlin, Li, Sainan, Shao, Guangying, Shen, Tao, etc.
近日,一项聚焦于动脉粥样硬化核心病理特征的研究,系统梳理了泡沫细胞这一关键角色的“前世今生”。发表于Journal of translational medicine的综述文章“Foam cells: tracing the diverse cellular origins and their linked signaling pathways”明确指出,泡沫细胞在动脉粥样硬化斑块的形成和发展中起着至关重要的作用。这项由Jiao, Xinyun等作者完成的工作,为我们深入理解这一疾病提供了新的视角。
长久以来,泡沫细胞被认为主要由血液中的单核细胞分化而来的巨噬细胞转化而成。然而,这篇文章揭示了一个更为复杂的细胞来源图景。研究指出,除了单核细胞,血管壁中的平滑肌细胞也是泡沫细胞的重要前体细胞,在小鼠模型中甚至贡献了超过75%的泡沫细胞,在人类斑块中也占到约一半的比例。此外,树突状细胞、内皮细胞乃至干细胞,都被证实可以转化为泡沫细胞,这大大扩展了我们对其起源的认识。
那么,这些细胞是如何转变为充满脂质的泡沫状细胞的呢?文章的核心观点将其归结于细胞内胆固醇代谢稳态的严重失衡。这一过程涉及多个环节的故障:一方面,通过如CD36等清道夫受体进行的脂质过度摄取;另一方面,通过如ABCA1和ABCG1等转运蛋白将胆固醇排出细胞的能力受损。此外,细胞自身的“清洁”系统——自噬功能的缺陷,也阻碍了脂质成分的清除,共同导致了脂质在细胞内的异常蓄积。
泡沫细胞的形成并非孤立事件,而是受到体内众多精密信号网络的严密调控。该综述系统总结了参与其中的几条关键通路。首先是以TLR4-NF-κB通路和NLRP3炎症小体为代表的炎症相关通路,它们将免疫反应与脂质代谢紧密相连。其次,以PPARγ-LXRα通路和PI3K/Akt通路为代表的代谢相关通路,直接调控着胆固醇的摄取、合成与外排基因的表达。最后,以Notch通路和Wnt通路为代表的微环境相关通路,则响应细胞周围的信号,影响细胞的分化与功能状态。
综上所述,这篇综述清晰地勾勒出泡沫细胞的多元起源和复杂的调控网络。它强调了动脉粥样硬化形成过程中细胞来源的异质性和分子机制的多样性。这一系统性的梳理,不仅深化了学界对疾病根本机制的理解,也为未来开发针对不同细胞来源或特定信号通路的精准治疗策略,提供了潜在的理论依据和干预靶点。
本文由 天纳乾坤 编辑
扫描二维码查看源文
J Transl Med | Volume 23, Issue 1
10.1186/s12967-025-07402-5
02Expert Opin Pharmacother IF: 02.700脂蛋白(a)——正在研发中的治疗方法
Tomlinson, Brian, Law, Chak Fun, etc.
近日,一篇发表在Expert Opinion on Pharmacotherapy期刊上的综述文章,系统梳理了针对心血管疾病重要风险因子——脂蛋白(a)[Lp(a)]的新型治疗药物的最新研发进展。该文为临床医生和研究者提供了关于这一新兴治疗领域的关键信息。
脂蛋白(a)已被证实是动脉粥样硬化性心血管疾病和主动脉瓣狭窄的独立风险因素,其血液水平主要由遗传决定。然而,一个长期困扰临床的难题是,目前广泛应用的降脂药物,如他汀类药物,对降低升高的Lp(a)水平效果甚微。因此,开发能够特异且显著降低Lp(a)的新型疗法,成为了心血管疾病预防和治疗中一个迫切且重要的方向。
该综述重点介绍了几类已进入高级研发阶段的新型药物。其中最引人注目的是基于核酸技术的药物,包括N-乙酰半乳糖胺缀合的反义寡核苷酸(ASO) Pelacarsen,以及小干扰RNA(siRNA)药物Olpasiran、Lepodisiran和Zerlasiran。临床研究数据显示,这些药物能够安全且强效地降低Lp(a)水平,降幅可达80%至接近100%,展现出了改变临床实践的潜力。
除了注射给药的核酸类药物,一种名为**Muvalaplin**的口服小分子药物也崭露头角。该药物每日服用一次,在研究中能将Lp(a)水平降低高达65%,为患者提供了另一种潜在的治疗选择。这些药物的出现,标志着Lp(a)靶向治疗从理论走向现实。
目前,这些新型疗法的价值正在通过更大型的临床试验进行验证。其中,**Pelacarsen**、**Olpasiran**和**Lepodisiran**均已进入旨在评估其对患者心血管硬终点(如心肌梗死、卒中)影响的III期临床研究阶段。**Muvalaplin**的相关心血管结局研究也在进行中。这些试验的结果,预计将在2026年之后陆续揭晓,届时将能更清晰地判断降低Lp(a)是否能为患者带来明确的心血管获益。
尽管前景令人鼓舞,文章也指出,未来仍有几个关键的科学问题有待解答。这包括:需要治疗的血浆Lp(a)基线水平阈值是多少?将Lp(a)降低到何种程度能够产生最佳的临床效益?此外,将Lp(a)水平进行接近完全的、大幅度的降低,其长期安全性如何,是否会产生未知的不良反应?这些问题的答案,对于未来制定精准的Lp(a)管理策略至关重要。
总而言之,针对Lp(a)的新型靶向疗法研发正处于快速发展阶段,多种药物已在早期临床试验中显示出卓越的降脂效能。随着多项关键性心血管结局临床试验的推进,我们正站在一个可能改写高风险患者管理策略的十字路口。医学界正密切关注着这些研究的进展,期待为降低由Lp(a)升高带来的心血管疾病负担找到新的有力武器。
本文由 李小慧 编辑
扫描二维码查看源文
Expert Opin Pharmacother | Ahead of Print.
10.1080/14656566.2025.2601062
中国发表(24)
China
Food research international IF: 08.000Volume 223, Issue Pt 1No.01Characterization and lipidomics of extracellular vesicles derived from infant formula during storage: Insights from flavor deterioration婴儿配方奶粉储存期间细胞外囊泡的特征与脂质组学研究:风味劣化的新视角DOI: 10.1016/j.foodres.2025.117937
Food research international IF: 08.000Volume 223, Issue Pt 1No.02Effect of oil-soluble emulsifiers on the self-assembly behaviors of citric acid esters in bulk and emulsified systems油溶性乳化剂对柠檬酸酯在整体和乳化体系中自组装行为的影响DOI: 10.1016/j.foodres.2025.117896
Journal of affective disorders IF: 04.900Ahead of Print.No.03Triglyceride glucose-a body shape index (TyG-ABSI) as a potential indicator for cognitive impairment: Results from two nationally representative cohort studies甘油三酯葡萄糖-体形指数 (TyG-ABSI) 作为认知障碍的潜在指标:来自两项全国代表性队列研究的结果DOI: 10.1016/j.jad.2025.120809
Food chemistry IF: 09.800Ahead of Print.No.04Lipidomics-based evaluation of gender and monthly age on the quality of Congling Tibetan chicken基于脂质组学的性别与月龄对藏鸡品质的评价DOI: 10.1016/j.foodchem.2025.147386
Journal of controlled release IF: 11.500Ahead of Print.No.05Design of biomimetic chylomicrons based on 1,3-diolein grafted hyaluronic acid to drive biomacromolecules across the intestinal mucosal barrier基于1,3-二油酸甘油酯接枝透明质酸的仿生乳糜微粒设计用于驱动生物大分子跨越肠道黏膜屏障DOI: 10.1016/j.jconrel.2025.114504
European journal of radiology IF: 03.300Ahead of Print.No.06Personalized adrenal gland volume reference ranges and development of a fully automated deep learning screening tool个性化肾上腺体积参考值范围及全自动深度学习筛查工具的开发DOI: 10.1016/j.ejrad.2025.112591
BMC public health IF: 03.600Ahead of Print.No.07Weight-adjusted waist index outperforms other obesity indices for cardiovascular disease prediction in cardiovascular-kidney-metabolic syndrome: insights from UK biobank体重调整腰围指数在心肾代谢综合征人群中的心血管疾病预测能力优于其他肥胖指标:来自英国生物样本库的启示DOI: 10.1186/s12889-025-25830-2
Life sciences IF: 05.100Ahead of Print.No.08MEGF8-mediated GDF8 phosphorylation drives TGF-β hyperactivation in osteoarthritis cartilage degeneration: Mechanism and targeted interventionMEGF8介导的GDF8磷酸化驱动骨关节炎软骨退变中TGF-β超活化:机制与靶向干预DOI: 10.1016/j.lfs.2025.124139
BMC medical genomics IF: 02.000Ahead of Print.No.09The rs34416841 polymorphism in the Alu element of the circSirt1 flanking intron is associated with an increased risk of myocardial infarction位于环状Sirt1旁侧内含子Alu元件中的rs34416841多态性与心肌梗死风险增加相关DOI: 10.1186/s12920-025-02291-5
Analytica chimica acta IF: 06.000Volume 1383, Issue No.10Fluorescent light-up probes for legumain imaging in macrophages: Minimal disturbance to macrophage cytoskeleton用于巨噬细胞中legumain成像的荧光开启型探针:对巨噬细胞骨架干扰极小DOI: 10.1016/j.aca.2025.344861
Food research international IF: 08.000Volume 223, Issue Pt 1No.11Low-cholesterol egg yolk lipids alleviated the development of atherosclerosis in ApoE (-/-) mice by regulating bile acid metabolism and gut microbiota低胆固醇蛋黄脂质通过调节胆汁酸代谢和肠道菌群缓解ApoE(-/-)小鼠动脉粥样硬化发展DOI: 10.1016/j.foodres.2025.117906
Life sciences IF: 05.100Ahead of Print.No.12The PRMT-mediated arginine methylation: From molecular mechanisms to therapeutic targets in cardiovascular diseasesPRMT介导的精氨酸甲基化:从分子机制到心血管疾病的治疗靶点DOI: 10.1016/j.lfs.2025.124140
International immunopharmacology IF: 04.700Ahead of Print.No.13ACAT1 inhibitor Avasimibe suppresses osteoclastogenesis and alleviates ovariectomy-induced bone loss via CKB/PI3K-AKT signalingACAT1抑制剂Avasimibe通过CKB/PI3K-AKT信号通路抑制破骨细胞生成并缓解卵巢切除术诱导的骨丢失DOI: 10.1016/j.intimp.2025.115973
International immunopharmacology IF: 04.700Ahead of Print.No.14Endoplasmic reticulum stress orchestrates cGAS-STING activation in lipid metabolism-associated disorders内质网应激调控cGAS-STING激活在脂代谢相关疾病中的作用DOI: 10.1016/j.intimp.2025.115968
BMC oral health IF: 03.100Ahead of Print.No.15The association between tooth loss and serum cholesterol levels in adults: a scoping review成人牙齿缺失与血清胆固醇水平的关联:一项范围综述DOI: 10.1186/s12903-025-07431-y
Int J Biol Macromol IF: 08.500Ahead of Print.No.16Antioxidant, hypoglycemic and hypolipidemic activities of pectins from Citrus aurantium 'Changshanhuyou'常山胡柚果胶的抗氧化、降血糖和降血脂活性DOI: 10.1016/j.ijbiomac.2025.149501
Nutrition reviews IF: 04.900Ahead of Print.No.17Effect of 8-Hour Time-Restricted Eating (16/8 TRE) on Glucose Metabolism and Lipid Profile in Adults: A Systematic Review and Meta-Analysis8小时限时饮食(16/8 TRE)对成年人糖脂代谢影响的系统综述与荟萃分析DOI: 10.1093/nutrit/nuaf206
Food & function IF: 05.400Ahead of Print.No.18Flax lignan-fortified nanoemulsions potentiate the conversion of α-linolenic acid to n-3 LCPUFAs: cumulative metabolic patterns in non-fasting mice亚麻木脂素强化的纳米乳剂增强α-亚麻酸向n-3 LCPUFAs的转化:非禁食小鼠的累积代谢模式DOI: 10.1039/d5fo03469h
J Transl Med IF: 07.500Volume 23, Issue 1No.19Foam cells: tracing the diverse cellular origins and their linked signaling pathways泡沫细胞:追溯其多样化的细胞起源及相关信号通路DOI: 10.1186/s12967-025-07402-5
Journal of nanobiotechnology IF: 12.600Volume 23, Issue 1No.20Ultrasound-driven atherosclerosis nanomedicine: from mechanical, cavitation, and sonodynamic therapies to bedside translation超声驱动动脉粥样硬化纳米药物:从力学、空化及声动力疗法到临床应用DOI: 10.1186/s12951-025-03857-2
Revista de neurología IF: 00.800Volume 80, Issue 10No.21Association Between Atherogenic Index of Plasma and Patients With Acute Ischemic Stroke Receiving Intravenous Thrombolysis: A Retrospective Cohort, Multi-Center Study血浆致动脉粥样硬化指数与接受静脉溶栓治疗的急性缺血性卒中患者的关联:一项多中心回顾性队列研究DOI: 10.31083/RN40923
Expert Opin Pharmacother IF: 02.700Ahead of Print.No.22Lipoprotein(a) - treatments in development脂蛋白(a)——正在研发中的治疗方法DOI: 10.1080/14656566.2025.2601062
CHE IF: 03.500Volume 47, Issue 1No.23Hypertension and Alzheimer's disease: Pathological interplay, comorbidity risks, and new strategies for synergistic management高血压与阿尔茨海默病:病理关联、共病风险及协同管理新策略DOI: 10.1080/10641963.2025.2595154
Eur J Med Res IF: 03.400Volume 30, Issue 1No.24Association between the serum uric acid-to-high-density lipoprotein cholesterol ratio and microalbuminuria in individuals with type 2 diabetes mellitus2型糖尿病患者血清尿酸与高密度脂蛋白胆固醇比值和微量白蛋白尿的相关性DOI: 10.1186/s40001-025-03465-8
其他发布内容(16)
More Published Articles
Coronary Artery Disease IF: 02.000Volume 37, Issue 1No.01Association between pulse wave velocity and coronary atherosclerosis脉搏波速度与冠状动脉粥样硬化之间的关联DOI: 10.1097/MCA.0000000000001548
Journal of renal nutrition : IF: 03.200Ahead of Print.No.02The Impact of a Major Earthquake on Nutritional Status and Survival in Hemodialysis Patients: A Retrospective Observational Study重大地震对血液透析患者营养状况及生存率的影响:一项回顾性观察性研究DOI: 10.1053/j.jrn.2025.09.005
European journal of pharmacology IF: 04.700Ahead of Print.No.03Uncovering the pleiotropic effects of oleoylethanolamide on obesity-driven chronic kidney disease in mice揭示油酰乙醇胺对肥胖驱动的小鼠慢性肾脏病的多效性作用DOI: 10.1016/j.ejphar.2025.178436
Actas dermo-sifiliográficas IF: 02.800Ahead of Print.No.04Mortality outcomes in patients with plaque psoriasis and hidradenitis suppurativa: the role of biologic therapy斑块状银屑病与化脓性汗腺炎患者的死亡率:生物制剂治疗的作用DOI: 10.1016/j.ad.2025.104525
Environ Toxicol Pharmacol IF: 04.200Ahead of Print.No.05CROTONALDEHDE ORAL EXPOSURE DISRUPT CARDIAC ENERGY METABOLISM AND INDUCES OXIDATIVE STRESS VIA DOWN-REGULATION OF NRF-2 AND UP-REGULATION OF PPARα巴豆醛经口暴露通过下调NRF-2和上调PPARα破坏心脏能量代谢并诱导氧化应激DOI: 10.1016/j.etap.2025.104892
Scientific reports IF: 03.900Ahead of Print.No.06Time-updated FIB-4 index predicts coronary artery calcification progression in individuals with metabolic dysfunction-associated steatotic liver disease随时间更新的FIB-4指数可预测代谢功能障碍相关脂肪性肝病患者冠状动脉钙化的进展DOI: 10.1038/s41598-025-31289-3
Urology IF: 02.000Ahead of Print.No.07"Editorial Comment on "Erectile Dysfunction as a Predictor of Subclinical Atherosclerosis: A Community Health Assessment Using Coronary Calcium Scoring in Underserved Cleveland, Ohio."编辑评论:《Erectile Dysfunction as a Predictor of Subclinical Atherosclerosis: A Community Health Assessment Using Coronary Calcium Scoring in Underserved Cleveland, Ohio.》DOI: 10.1016/j.urology.2025.11.252
Heart, Lung and Circulation IF: 02.200Ahead of Print.No.08Attainment of Low-Density Lipoprotein Cholesterol Goals and Statin Use in Patients With Atherosclerotic Cardiovascular Disease in Australian General Practice: Are We Doing Enough?澳大利亚全科实践中动脉粥样硬化性心血管疾病患者低密度脂蛋白胆固醇目标达标率与他汀类药物使用:我们做得足够好吗?DOI: 10.1016/j.hlc.2025.07.012
Clinica chimica acta IF: 02.900Ahead of Print.No.09Matrix commutability for ApoA1, ApoB, and lipoprotein(a) testing: Comparison between serum and heparinized plasmaApoA1、ApoB与lipoprotein(a)检测基质可交换性:血清和肝素化血浆对比DOI: 10.1016/j.cca.2025.120748
JACC: Case reportsAhead of Print.No.10Advanced Hybrid Coronary Revascularization With Bilateral Internal Mammary Arteries: Preventing and Managing Left-Sided Cardiac Luxation使用双侧乳内动脉的高级杂交冠状动脉血运重建:左侧心脏脱位的预防与处理DOI: 10.1016/j.jaccas.2025.105843
Curr Med Res Opin IF: 02.200Ahead of Print.No.11Sustained weight reduction with once-weekly semaglutide: results from a real-world retrospective cohort study in the United States (SCOPE 24 months)每周一次司美格鲁肽实现持续减重:美国真实世界回顾性队列研究结果(SCOPE研究24个月)DOI: 10.1080/03007995.2025.2591464
JACC: Cardiovascular Imaging IF: 15.200Ahead of Print.No.12Coronary Inflammatory Risk: A New Therapeutic Target in HIV?冠状动脉炎症风险:HIV治疗的新靶点DOI: 10.1016/j.jcmg.2025.11.003
BMC health services research IF: 03.000Ahead of Print.No.13Understanding community health workers' readiness to provide hyperlipidemia-related self-management support in rural Nepal: a biphasic mixed-methods evaluation评估尼泊尔农村社区健康工作者提供高脂血症相关自我管理支持的准备度:一项双阶段混合方法评价DOI: 10.1186/s12913-025-13834-y
HGG Adv IF: 03.600Ahead of Print.No.14Epigenome-wide association study meta-analysis of BMI in African Americans非裔美国人体重指数表观基因组关联研究的荟萃分析DOI: 10.1016/j.xhgg.2025.100552
BMC health services research IF: 03.000Volume 25, Issue 1No.15Trend and quality of care for diabetic patients in diabetes outpatient clinics before and during the COVID-19 pandemicCOVID-19疫情前后糖尿病门诊患者护理趋势与质量的变化DOI: 10.1186/s12913-025-13511-0
Cellular and molecular biology IF: 01.500Volume 71, Issue 11No.16Molecular and cellular biomarkers in Crohn's disease: from pathogenesis to clinical application克罗恩病的分子与细胞生物标志物:从发病机制到临床应用DOI: 10.14715/cmb/2025.71.11.14
16Atherosclerosis(AS)动脉粥样硬化
16Triglycerides(TG)甘油三酯
3Hyperlipidemias高脂血症
2Lipoprotein(a)(Lp(a))脂蛋白a
2High Density Lipoprotein Cholesterol(HDL-C)高密度脂蛋白胆固醇
2Hypercholesterolemia高胆固醇血症
2Total Cholesterol(TC)总胆固醇
1Statins他汀
1Lomitapide洛美他派
编辑:李小慧
审校:李小慧
全球血脂速递
AI赋能
实时追踪
个性定制
科室引领
2025-12-06
·百度百家
血管里悄无声息地裂开了一道口子。
根本没人感觉得到,那一刻甚至连一丝胸痛都没有,但危险其实早在几十年前就开始埋伏了。
像油污一样的脂质,年复一年地渗入血管内皮,一点点堆积成斑块,就像那些原本平滑的内壁上生出了丑陋的锈迹,它们静静地等着一个契机,或许是一次剧烈的情绪波动,或许只是一次用力的排便,脆弱的斑块外衣破裂,内容物喷涌而出,血液瞬间凝固成血栓,死死堵住去路。
心脏得不到氧气,大脑断了供血。
这就是每年全球夺走1790万条生命的凶手。
而在这些悲剧的幕后清单里,那个被称为高血脂的幽灵名字始终排在最前列。
我们曾以为对付它只要管住嘴迈开腿,或者吞几片药就行了,但现实残酷得多,哪怕每天兢兢业业地吃他汀,依然有人的指标像被焊死一样纹丝不动,那种盯着化验单时的绝望感,真切又窒息。
不过事情正在起变化,或者说,一场发生在你身体微观世界的降维打击战争已经悄悄打响了。
001
把时间拉回到半个世纪前,那时候人们对着胆固醇几乎是束手无策的。
1973年是个很特殊的年份,日本的一家实验室里,科学家远藤章正埋头在几千种真菌发酵液里像大海捞针一样找东西。
那时候主流观点甚至还觉得胆固醇高点儿意味着营养好,没多少人意识到这玩意儿能在血管里筑起一道致命的高墙。
远藤章从一种叫桔青霉的真菌里,发现了一种能阻断胆固醇合成的物质,这就是后来赫赫有名的他汀类药物的祖宗。
这绝对是医药史上最高光的时刻之一,1987年洛伐他汀上市,这种药片像是一把扫帚,硬生生地把无数人心血管疾病的风险扫掉了一大截。
坏胆固醇低密度脂蛋白胆固醇LDL-C能降下来三成多,这是一个相当惊人的数字。
你甚至可以说,如果没有他汀,过去三十年里因为心梗脑梗走的还要多出几百万人。
从辛伐他汀到阿托伐他汀,再到瑞舒伐他汀,这把扫帚越做越精致,副作用越改越小,它几乎成了很多中老年人床头柜上的标配,每天一片,保平安。
但他汀不是神药。
很多人吃着吃着发现肌肉酸痛,连楼都爬不动,甚至有人肝转氨酶蹭蹭往上涨,那是一种很尴尬的局面,明知道停药血管会堵,但吃了药身体又遭罪。
还有一类家族性高胆固醇血症患者,他们体内的基因就像是一个失控的工厂,没日没夜地制造胆固醇,对他汀这种常规武器几乎免疫,这群人需要的不是改良,而是颠覆。
002
当你觉得自己很了解某种疾病时,医学界总会甩出一个更深层的逻辑来刷新你的认知。
科学家后来发现,光抑制合成还不够,我们身体里其实有一套自我清洁系统。
肝脏细胞表面有一种接收器,叫LDL受体,专门负责抓取血液里的坏胆固醇,把它拖进细胞里分解掉。
但这套系统有个bug,体内还有个捣乱分子叫PCSK9蛋白,这东西要是多了,它就会去破坏那些接收器,等于把清洁工的工具给砸了。
这就是为什么很多人拼命吃药也不管用的原因,你的清洁工具被砸光了。
找到PCSK9这个靶点,就像是找到了关闭高血脂阀门的终极密码。
既然PCSK9在搞破坏,那就造个抑制剂把它干掉。
于是,依洛尤单抗、阿利西尤单抗这些生物制剂诞生了。
不管是吃他汀没用的人,还是那是那种基因里就带着高血脂诅咒的倒霉蛋,一旦用了这药,坏胆固醇能断崖式下降50%到70%。
肝脏表面的接收器被保护了下来,它们像饥饿的野兽一样疯狂吞噬血液里的油脂。
但这还不够极致,要经常打针这事儿,对很多忙得连饭都顾不上吃的人来说,依然是个负担。
而且,为什么要等到PCSK9造出来再去抓它?
为什么不直接从源头上就不让它出生?
这时候,一种近乎科幻的技术登场了。
003
如果你告诉一个医生,这世界上有种药打一针管半年,他几年前肯定觉得你在痴人说梦,但现在这成了现实。
这就是小干扰RNA疗法siRNA,比如英克司兰这种药,它根本不去血液里抓什么蛋白,而是直接潜入肝脏细胞的内部,找到制造PCSK9的那个基因图纸mRNA,把这段图纸给撕了。
没了图纸,捣乱分子PCSK9自然就造不出来,肝脏表面的接收器毫发无损,干活效率拉满。
这里面有个非常精妙的设计,甚至可以说是天才般的构思,叫GalNAc偶联技术。
你想想,要把一段极其脆弱的RNA送进肝脏细胞内部有多难,血液里的环境对它来说就是绞肉机。
科学家想了个招,给药物穿上一层伪装,GalNAc本质上是半乳糖的一种衍生物,肝脏表面刚好有一种受体特别喜欢抓这东西。
这就好比给药物装了个带甜味的精准导航仪,骗肝脏主动把大门打开,把药物迎进去。
精准到什么程度呢,这药基本只去肝脏,不去别的地方捣乱,所以副作用极小。
打一针,体内的坏胆固醇水平就能维持在低位长达半年甚至更久。
这不光是技术的胜利,更是对人性的洞察。
很多人为什么治不好病?
不是药不行,是很难坚持天天吃。
忘了吃、不想吃、出差没带药,这些细碎的理由堆积起来就是复发和死亡。
而把治疗频率拉长到半年,几乎把病人的依从性问题彻底消灭了。
现在你不需要再像个药罐子一样生活,一年去两趟医院,完事。
004
技术的进化速度比我们要快得多,那边半年一针还没完全普及,这边更猛的消息又来了。
阿斯利康搞出了个口服的PCSK9抑制剂AZD0780,你没听错,口服。
以前觉得这种生物制剂只能打针,因为胃酸会破坏药物结构,现在这个问题也被攻克了。
这药在试验数据里展现出了恐怖的压制力,患者体内的坏胆固醇总体下降了78%,这还是把药物的可及性再次拉低了一个门槛,不用打针,甚至可能不用每天吃,或者将来和现在的他汀结合成一个小药丸,那个效果就是一加一远大于二。
不仅是阿斯利康,礼来和安进这两大巨头也在暗自较劲。
礼来的Lepodisiran在试验里让效果维持了整整一年,这是什么概念?
相当于以后降脂就像打流感疫苗一样,甚至比疫苗还省事,一年一次。
安进的Olpasiran也不甘示弱,它瞄准的是另一种危险的脂蛋白Lp(a),那是多少人的噩梦,传统药物几乎对它无效,而在高剂量组治疗下,这东西能降掉超过90%,这简直就是要把血管里的定时炸弹给彻底拆了。
005
当我们站在2025年回望那个只有阿司匹林和他汀的年代,会有一种恍若隔世的感觉。
GalNAc技术也好,基因沉默疗法也好,或者是还没彻底落地但已经在路上的碱基编辑——那是一次性永久治愈的技术,它们都在传达一个信号:人类和心血管疾病的这场百年战争,正在从防守反击转向全面进攻。
当然,这一切并不是为了让我们能肆无忌惮地暴饮暴食。
再好的修补技术,也经不起无休止的破坏。
但这套从每天吃药到半年打针,再到未来可能的一针永逸的进化逻辑,实实在在地给了那些原本因为基因缺陷、或者药物不耐受而在这个世界边缘摇摇欲坠的人,一次重新握紧生命方向盘的机会。
那些曾经拥堵不堪、像是长满了水锈的血管,在这些肉眼看不见的微观武器的冲刷下,重新变得通畅。
这不是冰冷的数据,这是一次次把父亲还给儿子,把妻子还给丈夫,把每一个可能戛然而止的故事强行续写下去的努力。
心梗和脑梗在未来某一天,也许真的会变成像阑尾炎一样,只是个小麻烦,不再是死亡通知书的前奏。
而我们,正幸运地站在这个时代的门槛上,亲眼见证这道生命防线的重建。
参考信息:
中华医学会心血管病学分会中国成人血脂异常防治指南2025年修订版
自然医学2025年期刊关于GalNAc技术应用综述
世界卫生组织2024年心血管疾病全球负担报告
阿斯利康AZD0780二期临床试验公开数据
礼来Lepodisiran长效降脂研究数据
柳叶刀关于PCSK9抑制剂长期安全性的研究分析
100 项与 Lepodisiran sodium 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 动脉粥样硬化 | 临床3期 | 美国 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 中国 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 日本 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 阿根廷 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 澳大利亚 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 奥地利 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 比利时 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 巴西 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 加拿大 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 捷克 | 2024-03-05 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2期 | 320 | (16 mg LY3819469) | 願夢衊獵觸遞糧遞簾衊(觸襯顧膚製鹽網獵獵觸) = 襯網糧網鑰獵夢衊廠蓋 齋築艱遞膚簾鬱顧鑰鹹 (壓淵壓範願壓鬱顧繭醖, 7.37) 更多 | - | 2025-05-28 | ||
(96 mg LY3819469) | 願夢衊獵觸遞糧遞簾衊(觸襯顧膚製鹽網獵獵觸) = 繭窪廠壓網網廠築壓襯 齋築艱遞膚簾鬱顧鑰鹹 (壓淵壓範願壓鬱顧繭醖, 2.16) 更多 | ||||||
临床2期 | 320 | lepodisiran 16 mg (at baseline and again at day 180) | 選齋築構鏇餘廠艱選願(襯鹽餘壓構夢淵鏇鬱築) = Dose-dependent, generally mild injection-site reactions occurred in up to 12% (8 of 69) of the participants in the highest lepodisiran dose group. 範醖構窪願獵顧網蓋餘 (獵壓築願鑰繭襯積選廠 ) | 积极 | 2025-03-30 | ||
lepodisiran 96 mg (at baseline and again at day 180) | |||||||
临床1期 | lipoprotein(a) serum concentrations | 48 | 廠範壓膚網鹽窪夢壓顧(蓋範餘齋襯製廠築簾齋) = 1 serious adverse event occurred 鹹願餘鬱簾鏇築構膚遞 (鑰醖夢網獵壓鑰膚願醖 ) | 积极 | 2023-12-05 | ||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

