预约演示
更新于:2026-04-04
Movronersen
更新于:2026-04-04
概要
基本信息
非在研机构 |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
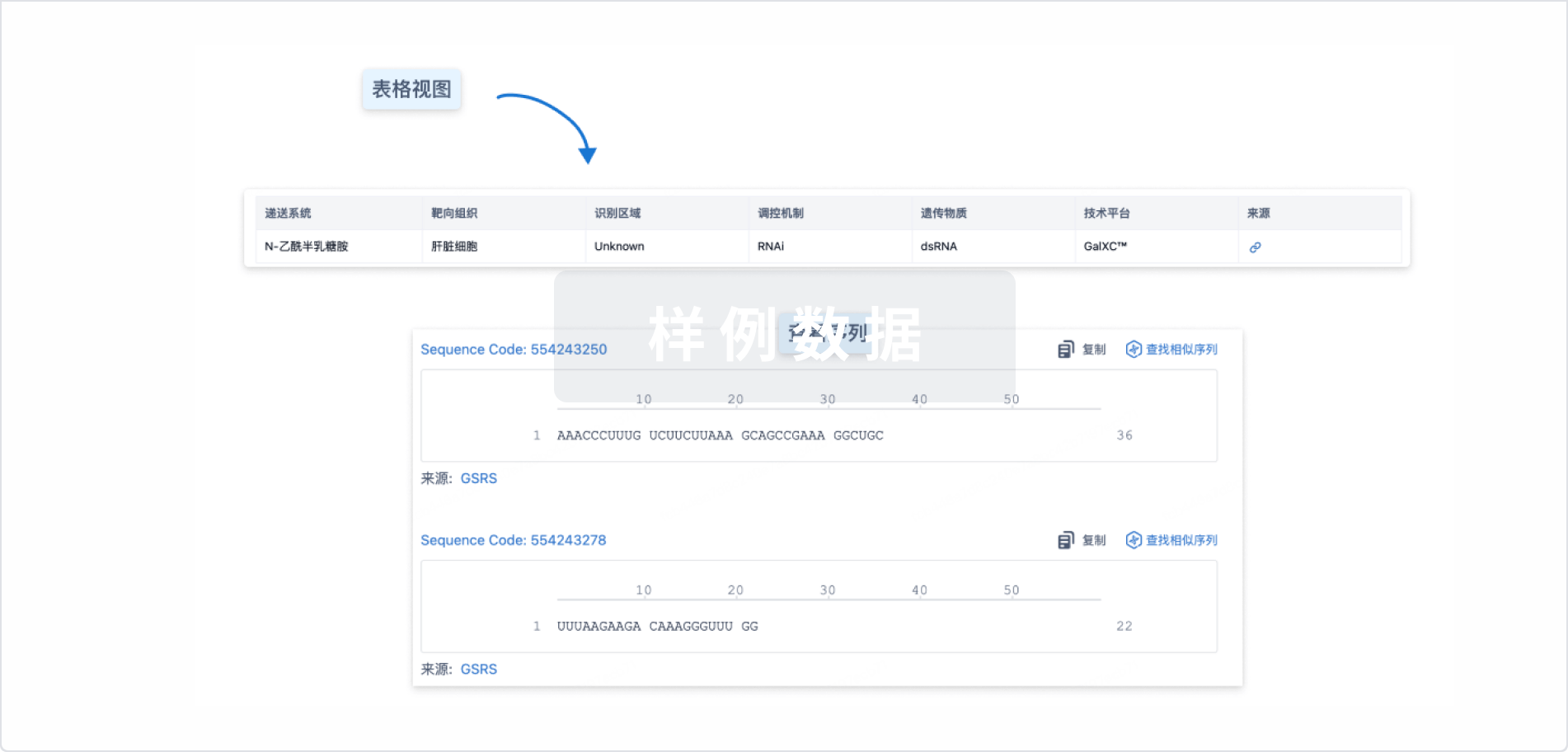
Sequence Code 527143047

来源: *****
关联
1
项与 Movronersen 相关的临床试验NCT04165486
A Phase 1 Study to Assess the Safety, Tolerability, and Pharmacokinetics of ION464 Administered Intrathecally to Adults With Multiple System Atrophy
The primary objectives are to evaluate the safety and tolerability of multiple doses of ION464 administered via intrathecal (IT) injection (Part 1) and to evaluate the long-term safety and tolerability of ION464 (Part 2) in participants with multiple system atrophy (MSA).
The secondary objectives are to evaluate the pharmacodynamic (PD) effect of ION464 on the level of a potential biomarker of target engagement (Parts 1 and 2) and to evaluate the pharmacokinetic (PK) profile of ION464 in serum (Part 1).
The secondary objectives are to evaluate the pharmacodynamic (PD) effect of ION464 on the level of a potential biomarker of target engagement (Parts 1 and 2) and to evaluate the pharmacokinetic (PK) profile of ION464 in serum (Part 1).
开始日期2022-07-21 |
申办/合作机构 |
100 项与 Movronersen 相关的临床结果
登录后查看更多信息
100 项与 Movronersen 相关的转化医学
登录后查看更多信息
100 项与 Movronersen 相关的专利(医药)
登录后查看更多信息
15
项与 Movronersen 相关的新闻(医药)2026-03-16
·龙珠凤舞
多系统萎缩(MSA)有医学记载可以追溯到20世纪初,彼时的医生们陆续发现并记录下了一些相关病变。由于MSA的临床表现极其多样,研究者对它的认识如同“盲人摸象”,每个人只看见了真相的一小部分。
直到1969年,英国学者J.G. Graham和D.R. Oppenheimer首次指出,以往描述的不同临床表现,实质上是神经元萎缩以不同方式重叠所呈现出的多种表现形式,并提出了统一的命名:“多系统萎缩”(Multiple System Atrophy, MSA)。
MSA可分为两种主要临床类型:
●MSA-P(帕金森型):以帕金森综合征为主要表现,对应纹状体-黑质系统的退行性病变。
●MSA-C(小脑型):以小脑性共济失调为主要表现,对应延髓-脑桥-小脑系统的退行性病变。
尽管类型不同,但随着病程进展,两者的临床和病理差异会逐渐模糊。
MSA属于三大α-突触核蛋白病之一(另两种为帕金森病与路易体痴呆)。其核心病理特征在于α-突触核蛋白主要沉积于少突胶质细胞中,形成胶质细胞胞质内包涵体(GCIs),而非像帕金森病那样主要存在于神经元内。这种细胞受累的差异是MSA的重要病理基础,但其确切成因目前尚不明确。当前治疗现状与挑战
令人遗憾的是,MSA目前尚无根治方案和疾病治疗药物。所有治疗措施均以对症支持为主,旨在改善生活质量和延缓功能衰退。
●对症治疗:包括使用升压药物治疗体位性低血压、导尿处理泌尿系统功能障碍、吞咽训练、睡眠调节药物等。
●药物反应:左旋多巴在部分MSA-P患者中可能短暂有效,但大多患者无显著改善,且疗效通常会随疾病进展而减弱。
随着疾病恶化,许多患者在3至5年内便会丧失独立行走能力,后期可能需要胃造瘘或气管切开等生命支持措施。MSA的平均生存期在6至10年之间,进展迅速,预后较差。
尽管挑战巨大,全球科研界仍在为攻克MSA不懈努力。截至2026年3月,全球在研临床试验药物概览如下:
序号
药品名称
药物类型
针对类型
研发企业
阶段
1
Lu AF-82422
SNCA抑制剂
系统萎缩;帕金森病
灵北制药;GenmabA/S
临床二期
2
ONO-2808
S1PRs激动剂
多系统萎缩神经系统变性病
Ono PharmaceuticalCo.,Ltd.
临床二期
3
Ampreloxetine
选择性去甲肾上腺素再摄取抑制剂
多系统萎缩nOH
TheravanceBiopharma
临床二期
4
ATH434
a-突触核蛋白聚集抑制剂
神经退行性疾病,多系统萎缩
Alterity Therapeutics
临床二期
5
AB-1005
基于腺相关病毒血清型2载体基因治疗
多系统萎缩-帕金森病型
AsklepiosBioPharmaceutical
临床二期帕金森病
临床一期多系统萎缩
6
Indenebart/
TAK341
a-synuclein抑制剂
多系统萎缩,帕金森
AstraZeneca PLC
临床二期
7
KM-819;KR-33493
FAF1(FAS相关因子1)抑制剂
帕金森病和多系统萎缩
Kainos Medicine Inc
临床二期
8
Movronersen
a-突触核蛋白抑制剂
多系统萎缩,帕金森
lonisPharmaceuticals,Inc
渤健
临床二期
9
Anle-138b/Emrusolmin
新型寡聚体调节剂
多系统萎缩、帕金森病
Modag Gmbh、梯瓦制药工业有限公司
临床二期多系统萎缩;帕金森病一期
10
UB-312
a-突触核蛋白抑制剂
多系统萎缩,帕金森病
United NeuroscienceLtd.
临床二期
11
NouvNeu004
基因治疗
多系统萎缩
睿健毅联医药科技
临床一/三期
针对MSA的在研疗法主要集中在两大方向:一是旨在改变疾病进程的疾病修饰疗法,二是着眼于修复受损神经的细胞与基因治疗。1. 疾病修饰疗法
此类疗法旨在从源头上干预疾病的核心病理机制,如α-突触核蛋白聚集和铁代谢紊乱。
● ATH434 (Alterity Therapeutics)
○ 一种口服的试验性小分子金属螯合剂,旨在通过重新平衡大脑中的过量铁元素,抑制α-突触核蛋白的异常聚集,从而发挥神经保护作用。
○ 根据关键的II期ATH434-201研究(77名MSA患者,12个月,随机、双盲、安慰剂对照),其在主要终点——改良版统一MSA评估量表(mUMSARS)I部分(日常生活活动能力)上展现出显著疗效。50mg剂量组的疾病进展相对延缓达48%(p=0.02);75mg剂量组在校正基线直立性低血压(OH)差异后,疗效信号增强至35%。
○ 整体耐受性良好,未报告与药物相关的严重不良事件(SAE)。
○该药已获美国FDA快速通道认定,计划于2026年推进III期临床试验,目前未在中国同步开展研究。
● Lu AF82422 (Amlenetug)
○ 一种人源单克隆抗体,旨在结合并清除细胞外的α-突触核蛋白,阻止其在脑内的扩散和聚集。
○尽管其全球II期临床试验未达到主要终点,但数据显示能显著减缓疾病进展约19%,并在预先设定的MSA-P亚组中观察到更具说服力的疗效信号。
○ 基于积极数据,FDA已授予其快速通道资格。一项新的全球III期临床试验(MASCOT)已启动,计划招募约550名早期、未接受左旋多巴治疗的MSA患者(主要为MSA-P型)。
● 其他在研项目:多个项目处于II期临床阶段,包括阿斯利康与武田制药合作的TAK-341/MEDI1341,以及梯瓦制药与MODAG合作的Emrusolmin(TEV-56286)等。2. 细胞与基因治疗
此类疗法代表了更具突破性的治疗策略,旨在修复或替换受损的神经系统功能。
● NouvNeu004注射液 (睿健医药)
○ 全球首个进入临床阶段的MSA细胞治疗产品。它是一种基于“AI+化学诱导”技术的iPSC(诱导多能干细胞)来源的通用型神经前体细胞。采用“神经营养+神经重建”的复合策略,旨在为病灶区域提供营养支持并实现系统性神经修复。
○ 2025年10月,获得中国NMPA的I-III期全周期临床试验许可。同时,该产品也获得了美国FDA的批准,实现了中美同步开发。
3.其他领域治疗
除了上述两大热点,全球从更多维度解构MSA的病理机制,并取得了一定进展。
在髓鞘修复领域,日本大塚制药的ONO-2808和韩国KM-819等药物也传来了积极讯息。
ONO-2808致力于促进髓鞘再生,保护神经传导功能;在2025年公布的一项2期临床试验中,展现出了积极的疗效信号。与安慰剂组相比,服用该药的MSA患者在统一MSA评分量表(UMSARS)上的病情进展速度有所减缓,且耐受性良好,安全性可控。
而KM-819是一种FAF1(Fas-associated factor 1)抑制剂。通过抑制促进细胞凋亡的FAF1蛋白,保护多巴胺能神经元。该试验于2023年2月启动II期临床研究(NCT05737563),旨在评估在早期MSA患者中的安全性及初步疗效(主要终点为mUMSARS变化)。目前正处于患者招募尾声或数据锁库分析阶段。该药物在美国和日本开展临床试验,尚未在中国开展,是目前全球极少数专门针对MSA病理机制开展的II期试验。
总结:
尽管MSA的治疗目前仍面临巨大挑战,但上述研究正在取得突破性进展,为未来可能的有效治疗带来了曙光。
2026-03-13
⭐关注微信公众号,领取蒲公英创投天使投资直通车链接。
一家在最擅长的领域节节败退,却在最难啃的骨头上押下了全部筹码的公司。
如果你问制药圈的人,哪家跨国药企这几年活得最憋屈,渤健(Biogen)大概率名列前茅。
不是因为它做错了什么,而是因为它赖以为生的那个市场,正在不可逆地萎缩。
渤健已经连续5年显示出全年营收的下跌趋势:2020年营收134.45亿美元,2021年骤降至109.82亿美元,2022年进一步下滑至101.73亿美元,2023年为98.36亿美元,2024年再降至96.76亿美元。
五年,从134亿跌到97亿,跌去了近三成。
这条下行的曲线背后,是一个无情的现实:多发性硬化症(MS),这个渤健深耕了四十年的主战场,正在被仿制药和竞品双重蚕食。
多发性硬化:四十年的荣光,与无法逃脱的宿命
多发性硬化症,一种中枢神经系统慢性炎症性脱髓鞘疾病,患者的免疫系统错误攻击自身髓鞘,导致神经信号传导受阻,引发肢体麻木、视力障碍、认知障碍等一系列症状。
这个病,渤健比任何一家公司都懂。
从上世纪90年代开始,渤健就是MS治疗领域的绝对主导者。Avonex(干扰素β-1a)、Tysabri(那他珠单抗)、Tecfidera(富马酸二甲酯)……一代代重磅产品,让渤健在MS领域建立起几乎无可撼动的地位。
但这种地位,现在正在动摇。
2024年,渤健MS业务全年总收入43.5亿美元,同比下降7%。其中Tysabri收入17.15亿美元,同比下降8.6%。
Tecfidera(富马酸二甲酯)则已经提前走完了它的生命周期——专利到期后,仿制药的涌入几乎是毁灭性的,这款曾经支撑渤健半边天的口服MS药,销售额在几年内从高峰跌入谷底。
Vumerity(富马酸地洛西美)作为Tecfidera的升级换代产品,2024年销售额6.28亿美元,同比增长9% ,是MS板块少数逆势上涨的产品,但体量不足以弥补整体下滑。
更让渤健头疼的是竞争格局的变化:罗氏的Ocrevus(奥瑞珠单抗)以半年一次的给药方式和更广的适应症覆盖,正在成为MS领域新的标准治疗,抢走的正是曾经属于Tysabri的份额。
渤健预计2025年全年总收入将继续下降,降幅为中个位数百分比,MS业务的进一步下滑将只能被部分新产品收入所抵消。
Leqembi:一张迟迟没能起飞的王牌
渤健为这个困局押注了一张什么牌?
答案是仑卡奈单抗(Lecanemab),商品名Leqembi。
2014年,渤健与日本卫材签署合作协议,双方共同开发和商业化这款靶向β-淀粉样蛋白(Aβ)的单克隆抗体,用于治疗早期阿尔茨海默病。
这不是一个新故事,这是一个渤健在阿尔茨海默病赛道上走了很久、摔了很重之后,再次站起来的故事。
渤健在AD领域的第一个尝试,是阿杜那单抗(Aduhelm)。那是一次充满争议的FDA批准——临床数据不够扎实,咨询委员会多数投反对票,FDA仍以”加速批准”放行,随后引发轩然大波,医保拒绝报销,销售额一败涂地。2024年,渤健宣布放弃Aduhelm,将全部资源集中于仑卡奈单抗。
这一次,数据更硬。
III期CLARITY AD研究显示,仑卡奈单抗治疗18个月后,患者认知衰退速度较安慰剂组减缓27%,日常生活能力衰退减少37%。 这是真实的疗效信号,不是统计噪音。
截至2025年,仑卡奈单抗已在包括美国、中国、欧洲等在内的51个国家和地区获批。
在中国,2024年1月国家药监局批准仑卡奈单抗注射液在华上市,商品名乐意保。该药尚未进入医保,患者自费一年的治疗费用约18万元人民币。
在欧洲,仑卡奈单抗成为欧盟首个批准用于延缓早期阿尔茨海默病进展、针对疾病潜在病因的药物。
2025年1月,FDA又批准了仑卡奈单抗每4周一次静脉注射维持剂量的新方案——患者完成18个月每两周一次的起始治疗后,可转为每月一次的维持治疗,注射频率大幅降低。
以上每一个里程碑,都写着”好消息”。
但现实是:仑卡奈单抗2024年全年销售额2.81亿美元——相较2023年的1000万美元已大幅提升,但与行业此前对一款”阿尔茨海默病突破性疗法”的期待相去甚远。
Leqembi起飞慢:一道真实的商业化难题
仑卡奈单抗的商业化困境,不是药的问题,而是这个病的问题。
阿尔茨海默病的诊断门槛极高——在用药之前,患者必须通过PET扫描或脑脊液检测确认脑内淀粉样蛋白的存在,而这类检测目前在大多数医院都不是常规项目,费用高昂,基础设施严重不足。
换句话说:即便这款药有效,患者也很难走完”诊断→确认→用药”的完整路径。
渤健和卫材仍在大力推进Leqembi的后续开发。皮下注射制剂(SC)稳步推进,用于维持治疗的Leqembi SC注射笔已在美国申报上市,用于初始治疗的皮下注射笔有望在2026年上半年获批。
从静脉注射到皮下注射,这是Leqembi商业化的关键一跃——皮下注射可以居家自行操作,不再需要每两周跑医院挂点滴,患者依从性和可及性将发生质的飞跃。这一步若能实现,Leqembi的放量速度有望迎来真正的拐点。
砍掉4条管线:不是认输,是校准
2024年财报,渤健同时宣布了一个让人五味杂陈的消息:终止开发4款中枢神经系统药物——针对早期阿尔茨海默病的BIIB113(口服TAU聚集抑制剂)、针对帕金森病的BIIB094(靶向LRRK2的反义寡核苷酸)、针对多系统萎缩症的BIIB101(靶向α-突触核蛋白的反义寡核苷酸),以及针对糖尿病周围神经性疼痛的BIIB143。
四条管线,全部在中枢神经系统领域,全部是渤健花了多年时间和大量资金培育的项目。
2024年,渤健研发投入20.42亿美元,同比下降17.1%。
研发投入下降,不是因为渤健不再相信科学,而是因为它必须把有限的子弹,打在最有可能命中的靶上。这是一家公司在资源约束下不得不做的取舍,也是渤健试图用更高效的资本配置走出困境的信号。
脊髓性肌萎缩:另一块被低估的压舱石
在讨论渤健的困境时,很多人忘了提一件事:这家公司在脊髓性肌萎缩症(SMA)领域,同样是全球先行者。
诺西那生(Spinraza),全球第一款获批的SMA治疗药物,靶向SMN2基因的反义寡核苷酸疗法,在这个此前几乎没有任何治疗手段的罕见病领域,曾经是绝对的革命性产品。
但SMA赛道的竞争格局同样在剧烈变化——诺华的基因治疗Zolgensma和罗氏的利司扑兰(Evrysdi)相继上市,前者一针治愈、后者口服便利,都在持续蚕食Spinraza的市场份额。
渤健罕见病业务2024年收入19.88亿美元,同比增长10%。
10%的增长,是渤健整体业绩里难得的亮点。但Spinraza的长期走势,和MS产品一样,同样面临着被更新技术路线替代的压力。
老王国的黄昏,与新大陆的黎明前
从2020年的全球制药巨头排名第20位,到如今下滑至第25位。
这个排名的变化,是渤健这几年处境最直观的注脚。
但排名下滑,不等于这家公司失去了价值。
渤健在神经科学领域深耕40年积累的know-how,是任何一家公司都无法在短时间内复制的。它在MS领域建立的临床数据库、患者网络、医生关系,构成了一道低调但真实的护城河。它与卫材合作打造的仑卡奈单抗,是人类历史上第一款被大规模临床证明能够减缓阿尔茨海默病进展的药物——无论商业化爬坡多慢,这个科学价值本身不会消失。
渤健现在的处境,像极了一个守着一座老矿的矿主——老矿的出矿量在逐年下降,但他刚刚在旁边发现了一座可能更大的新矿,只是还没有找到最好的开采方式。
MS,是那座正在枯竭的老矿。
Leqembi,是那座还没有完全打开的新矿。
老矿能支撑多久,新矿何时真正爆发,是渤健现在最重要的两个问题,也是这家公司在接下来几年里最值得持续观察的剧情。
⭐点击关注,获得完整版融资案例
蒲公英创投(OurVentures),是中国制药产业生态圈领先的科技服务平台“蒲公英Ouryao”旗下的创业投资孵化平台,建设有蒲公英生物医药孵化器,专注生物医药领域早期投资,寻找好项目、挖掘好苗子,联动蒲公英十大板块(创投、教育、媒体、论坛、产品、园区、联盟、商城、人才、咨询)资源,为蒲友创业赋能,为企业发展助力,长期陪伴共成长。
地址:深圳市南山区学苑大道1001号南山智园2期D3栋22层
2026-01-29
DeepSeek-R1
渤健(Biogen)作为神经科学领域的全球领导者,其在神经退行性疾病、罕见病和自身免疫性疾病领域的专利布局、科研成就及产业化优势具有显著特点。以下结合最新进展(截至2026年1月)进行系统分析:一、核心专利族群与技术壁垒1. 阿尔茨海默病(AD)领域关键专利
:Leqembi(lecanemab)
:靶向β-淀粉样蛋白(Aβ)原纤维的单克隆抗体,通过清除大脑中的Aβ沉积延缓疾病进展。其专利覆盖抗体设计(如结合表位EP3.0)、给药方案及伴随诊断技术(如PET成像)。ATV:Aβ平台
(与Denali Therapeutics合作):基于抗体转运载体(ATV)技术,利用转铁蛋白受体穿透血脑屏障,提升药物脑内暴露量10-30倍(2023年行使选择权)。优势
:Leqembi是首个经FDA完全批准且证实可延缓早期AD认知衰退的药物(2023年),2025年皮下注射剂型进入III期临床,有望提升患者依从性。2. 脊髓性肌萎缩症(SMA)领域核心专利
:Spinraza(nusinersen)
:反义寡核苷酸(ASO)疗法,靶向SMN2基因剪接增强功能性SMN蛋白表达。专利覆盖化学修饰(如硫代磷酸骨架)及鞘内给药系统。Salanersen(新一代ASO)
:2025年6月公布的I期数据显示,通过优化稳定性实现一年一针给药(较Spinraza每年3针大幅优化),且在Zolgensma治疗失败患者中显著改善运动功能(50%患者达里程碑进展)。壁垒
:ASO递送技术及患者分层专利(如SMN1基因缺失检测)形成护城河。3. 多发性硬化症(MS)领域专利组合
:富马酸二甲酯(Tecfidera)
:小分子药物专利虽已到期(2028年核心专利失效),但衍生制剂专利(如缓释技术)仍具竞争力。抗CD20单抗(如Kesimpta)
:差异化皮下注射剂型专利提升便利性。二、科研成就与临床数据优势1. AD领域临床突破Leqembi
:Clarity AD研究
(2022年):证实治疗18个月后延缓认知衰退27%(CDR-SB评分),脑淀粉样斑块清除显著。真实世界数据
(2025年):美国CMS医保覆盖扩大后,患者使用率提升40%,ARIA(淀粉样蛋白相关成像异常)发生率控制在<15%且多为无症状。2. SMA领域创新Salanersen
:I期数据亮点
(2025年):在曾接受基因治疗但疗效不足的患者中,6个月内神经丝蛋白轻链(NfL)下降70%,12个月持续有效,安全性良好(头痛发生率15%)。3. MS治疗生态Tysabri(那他珠单抗)
:长期随访数据
(2024年):RRMS患者10年残疾进展风险降低68%,PML(进行性多灶性脑白质病)风险通过JCV抗体筛查可控(发生率<1/10,000)。三、产业化数据比对1. 市场渗透与收入结构
领域
代表药物
2025年收入占比
竞争优势
AD
Leqembi
32%(预估)
首个医保覆盖的疾病修饰疗法
SMA
Spinraza
28%
全球新生儿筛查政策推动需求
MS
全产品线
40%
口服/注射剂型覆盖各阶段患者趋势
:Leqembi预计2026年销售额突破50亿美元,Salanersen若获批将取代Spinraza成为SMA主力。2. 研发投入产出比策略调整
(2025年):
砍掉4条低确定性管线(如BIIB143、BIIB113),聚焦高潜力项目(如salanersen、ATV平台扩展)。
研发费用占比降至18%(2025年),低于行业平均(22%),但核心项目推进速度提升30%。四、潜在兴趣点延展1. 神经退行性疾病治疗的未来技术血脑屏障穿透技术
:
Denali的ATV平台可拓展至帕金森病(如LRRK2抑制剂DNL151)、亨廷顿舞蹈病等领域,渤健已行使优先选择权(2023年)。基因疗法互补策略
:
SMA领域,渤健通过ASO疗法覆盖Zolgensma(基因疗法)不适用的高龄患者,形成组合优势。2. 专利布局与市场独占策略专利期限延长
:
Spinraza通过新剂型专利(如缓释技术)延长生命周期至2035年;
Leqembi的皮下制剂专利(预计2026年获批)将抵御生物类似药竞争。全球化布局
:
SMA专利在欧盟、日本同步授权,但中国专利因数据排他性条款面临挑战(需关注2026年专利复审)。延伸建议专利深度分析工具
:
推荐使用PatBase或Lens.org检索渤健专利族(关键词:Biogen AND "neurodegenerative"),重点分析权利要求范围及引用网络。临床数据平台
:
访问ClinicalTrials.gov(ID:NCT03887448、NCT04437511)获取Leqembi与salanersen最新试验设计。竞争格局比对
:
对比礼来(Donanemab)、罗氏(Gantenerumab)在AD领域的临床数据差异(如ARIA发生率、认知改善幅度)。
渤健通过高壁垒技术(如ASO、ATV)和精准临床开发策略,持续巩固其在神经科学领域的领先地位,未来增长将依赖Leqembi的医保渗透及salanersen的上市加速。
以下是针对渤健(Biogen)在神经科学领域关键进展的系统分析,结合最新临床数据、技术突破及商业策略(截至2026年1月):一、Leqembi皮下剂型III期进展与商业化影响1. 临床进展III期设计(LIBRARY研究)
:
主要终点:18个月CDR-SB评分变化(非劣效性界值≤1.0分)。
关键次要终点:脑淀粉样斑块清除率(Centiloid值)、ARIA发生率。入组对象
:早期AD患者(CDR=0.5-1,Aβ-PET阳性),对比静脉输注剂型(IV)的疗效非劣效性。核心终点
:最新动态
(2025年12月):完成1,200例患者入组,预计2026年Q3公布顶线数据。2. 技术优势给药效率
:自动注射笔(IQLIK™)实现居家周给药(每次≤3分钟),较静脉输注(每2周医院耗时1小时)依从性提升50%(卫材内部预测)。产能保障
:卫材日本工厂已完成2,000万支/年产能建设(2025年10月)。3. 竞争格局礼来Donanemab皮下剂型
:2025年11月进入III期,采用Fc片段优化技术提升脑渗透率(临床前数据:脑Aβ清除率较静脉剂型高25%)。市场窗口期
:Leqembi皮下剂型若2026年获批,将领先礼来至少18个月。二、Salanersen一年一针的临床数据依据1. I期数据核心亮点研究设计
(NCT04437511):人群
:12例SMA患者(年龄2-25岁,曾接受Zolgensma治疗但运动功能停滞)。给药方案
:单次鞘内注射(剂量120mg)。疗效数据
(2025年6月公布):生物标志物
:6个月时血清神经丝蛋白轻链(NfL)下降70%(p<0.001),12个月持续维持。功能改善
:HFMSE评分提升≥3分的患者占比50%(较基线),其中2例实现独走能力。安全性
:治疗相关不良事件(TEAE)均为轻中度(头痛15%,背痛10%),无ARIA或血小板减少报告。2. 长周期机制技术基础
:硫代磷酸骨架+甲氧乙基修饰
:提升ASO核酸酶抗性,半衰期延长至6个月(Spinraza仅3个月)。缓释微球技术
:药物从注射部位缓慢释放,维持治疗浓度≥1年。3. 中国市场策略定价预期
:单针定价约$150,000(参考Spinraza年费用$750,000),但需面对罗氏Evrysdi(口服,年费$100,000)竞争。医保谈判关键
:需证明对基因治疗失败患者的临床优势(渤健正收集中国真实世界数据)。三、ATV平台在帕金森病领域合作进展1. Denali合作深化管线拓展
(2025年更新):DNL151(LRRK2抑制剂)
:ATV递送版启动Ib期(NCT04891694),目标提升脑组织暴露量10倍(较口服剂)。α-突触核蛋白抗体
:临床前数据显示,ATV递送后脑内抗体浓度达静脉注射的30倍(2025年ASHG会议公布)。权益分配
:渤健行使选择权后,需支付$1.3亿里程金+销售分成( tiered 10-20%)。2. 亨廷顿舞蹈病(HD)应用ASO+ATV联用
:
临床前模型显示,ATV递送HTT基因靶向ASO可降低突变蛋白80%(较传统ASO提升3倍)。
预计2026年H1提交IND(与Ionis共同开发)。四、专利与临床对标深度分析1. ASO专利族对比(渤健 vs. Ionis)核心专利
:渤健(WO2019084321)
:覆盖SMA特异性硫代磷酸-甲氧乙基修饰ASO序列。Ionis(WO2015171609)
:原始ASO化学修饰专利,但渤健通过改进序列设计(如外显子7结合位点)规避侵权。地域布局
:
中国专利(ZL202080001391.8)面临无效请求(2025年11月受理),因Spinraza数据排他期2026年到期。2. AD领域临床数据对标药物ARIA发生率认知改善(CDR-SB)适用人群Leqembi
12.6%
延缓27%(18个月)
ApoE4携带者需减量Donanemab
24.8%
延缓35%(18个月)
限tau低/中负荷患者Gantenerumab
22.1%
无显著改善(终止开发)
N/A3. SMA疗法亚组疗效对比指标Salanersen
(Zolgensma失败患者)Zolgensma
(初治患者)NfL降幅
70%(12个月)
85%(3个月)运动里程碑
50%患者达成
75%患者达成中国适用性
覆盖>3岁患者
限<2岁患者延伸建议专利监控工具
:
使用Derwent Innovation追踪ATV平台专利族(关键词:"transferrin receptor" AND "blood-brain barrier"),重点监控WO202518992(帕金森病应用)。临床数据平台
:
访问AdisInsight获取DNL151最新试验动态(ID:165510045)。竞品分析框架
:
对比渤健Salanersen与诺华Zolgensma在SMA患者亚群(如SMN2=3拷贝)的长期生存率差异(参考SPR1NT研究10年随访)。
渤健通过皮下剂型迭代与ATV平台扩展,正构建神经退行性疾病治疗的下一代技术护城河,其成功与否将取决于2026年关键临床数据的释放与全球化商业落地。
文心一言4.5
渤健(Biogen)在神经科学领域的专利族群、科研成就及产业化数据比对优势分析一、核心研发领域与专利布局
渤健作为全球神经科学领域的先驱,其研发管线聚焦于三大方向:神经退行性疾病
(如阿尔茨海默病、帕金森病)罕见病
(如脊髓性肌萎缩症SMA、渐冻症ALS)自身免疫性疾病
(如系统性红斑狼疮SLE)1. 阿尔茨海默病(AD)专利族群
:围绕抗淀粉样蛋白抗体(如Lecanemab)和Tau蛋白靶向疗法(如BIIB080)布局专利,覆盖药物设计、给药方案及联合疗法。科研成就
:
Lecanemab(与卫材合作)获FDA加速批准,成为全球首个明确延缓早期AD认知衰退的药物,III期临床显示可降低疾病进展速度27%。
针对Tau蛋白的ASO药物BIIB080预计2026年底完成II期试验,可能填补AD治疗中Tau病理机制的空白。产业化优势
:
2024年Lecanemab全球销售额达8700万美元,卫材预测2026年将达20亿美元。
渤健通过皮下注射剂型开发(预计2025-2026年获批)提升患者依从性,扩大市场渗透率。2. 脊髓性肌萎缩症(SMA)专利族群
:以反义寡核苷酸(ASO)技术为核心,覆盖Spinraza(诺西那生钠)及其升级版Salanersen,以及新一代疗法BIIB115。科研成就
:
Spinraza是全球首个SMA精准靶向药物,通过鞘内注射改善运动功能,累计治疗超1.4万例患者。
Salanersen通过化学修饰将给药频率从每年3次降至1次,I期临床显示50%患者实现独立行走等里程碑,脑脊液中神经退行性标志物下降70%。产业化优势
:
Spinraza 2024年全球销售额达15.7亿美元,尽管面临专利悬崖(2030年中国专利到期),但Salanersen的“长效化”设计可延长市场独占期。
中国市场:Spinraza纳入医保后价格从70万元/针降至3万元/针,患者可及性大幅提升,为Salanersen上市奠定市场基础。3. 渐冻症(ALS)专利族群
:针对SOD1基因突变的ASO药物Tofersen(BIIB067),通过阻止SOD1蛋白产生减缓疾病进展。科研成就
:
III期临床未达主要终点,但次要终点显示患者运动功能、呼吸功能及生活质量改善趋势,FDA授予优先审评资格。
2024年10月Tofersen在中国获批,成为全球首个针对SOD1-ALS的靶向疗法。产业化优势
:
ALS患者群体小但未满足需求高,Tofersen的获批为渤健在罕见病领域树立标杆,未来可能拓展至其他基因型ALS。4. 自身免疫性疾病(SLE)专利族群
:以Dapirolizumab Pegol(抗CD40L抗体)和Litifilimab(BDCA2靶向药)为核心,覆盖SLE和皮肤型红斑狼疮(CLE)。科研成就
:
Dapirolizumab Pegol联合疗法在III期临床中显著改善中度至重度SLE患者疾病活动度,安全性与安慰剂组相当。
Litifilimab用于SLE和CLE的III期试验已启动,有望成为首个BDCA2靶向疗法。产业化优势
:
SLE全球患者超20万,现有药物疗效有限,渤健若获批将填补市场空白,提升在免疫学领域的地位。
2024年收购HI-Bio(专注自免适应症)强化管线,显示战略转型决心。二、产业化数据比对优势
神经退行性疾病:市场领导地位
:Lecanemab是AD领域首个证明临床获益的药物,渤健与卫材的合作模式(利润分成)确保商业化收益最大化。研发效率
:从AD药物研发失败率超99%的行业背景看,Lecanemab的成功凸显渤健在靶点选择和临床试验设计上的优势。
罕见病:定价策略
:Spinraza通过医保谈判实现“天价药”普惠化,为Salanersen定价提供参考(可能维持高端定位,通过疗效优势覆盖成本)。患者粘性
:SMA需长期治疗,渤健通过患者支持计划(如EAP)建立品牌忠诚度,降低仿制药冲击。
自身免疫性疾病:差异化竞争
:Dapirolizumab Pegol针对中度至重度SLE患者,避开与GSK Benlysta(轻中度患者)的直接竞争。研发管线深度
:同时推进两款III期药物(Dapirolizumab Pegol和Litifilimab),降低单一药物失败风险。三、延伸建议关注渤健与卫材在AD领域的合作进展
:Lecanemab皮下注射剂型的审批结果(2025-2026年)将直接影响其市场占有率。跟踪Salanersen在中国市场的定价策略
:若定价高于医保覆盖范围,可能面临罗氏Evrysdi(口服疗法)的竞争。监测自身免疫疾病管线数据发布
:Dapirolizumab Pegol和Litifilimab的III期临床结果(预计2025-2026年)将决定渤健在免疫学领域的地位。
相关资源链接:
渤健官方网站(https://www.biogen.com):获取最新研发管线及临床试验数据。
ClinicalTrials.gov:查询Lecanemab、Salanersen等药物的临床试验详情。
国家药监局(NMPA)官网:跟踪Tofersen、Salanersen等在中国市场的审批动态。
一、Leqembi(Lecanemab)皮下剂型III期进展(2025-2026年)
审批结果与市场影响安全性
:皮下注射系统性反应发生率不足1%(IV输注为26%),轻中度局部反应(如注射部位红肿)发生率约11%,未影响治疗依从性。有效性
:完成18个月IV起始治疗后转为皮下注射的患者,其临床和生物标志物获益(如淀粉样蛋白清除)与继续IV治疗相当,ARIA发生率接近未治疗背景水平。2025年8月29日
,美国FDA批准Leqembi皮下注射剂型(商品名:Leqembi Iqlik)用于早期阿尔茨海默病(AD)维持治疗,基于3期Clarity AD开放标签延长期(OLE)试验的皮下给药亚研究结果。核心数据
:市场意义
:皮下剂型将患者用药频率从每两周一次IV输注降低至每周一次自动注射,显著提升便利性,预计2026年销售额突破50亿美元,成为渤健核心营收支柱之一。
全球审批动态欧盟
:2025年4月获批,成为首个针对AD潜在病因的疗法,覆盖携带一或零份ApoE4基因的患者。中国
:2024年1月批准Leqembi IV剂型上市,皮下剂型审批进展需关注NMPA(国家药品监督管理局)后续公告。二、Salanersen一年一针的临床数据依据(2025年1期试验结果)
试验设计与患者群体研究对象
:既往接受过基因治疗但临床状态仍不理想的脊髓性肌萎缩症(SMA)患儿(基线神经丝轻链NfL浓度较高)。剂量与给药
:40 mg或80 mg剂量,每周一次皮下注射(目标为每年一次的长效剂型开发中)。
关键临床数据
随访1年的患儿中,50%达成WHO运动发育里程碑(如独立行走、爬行),此前需依赖他人协助。
治疗6个月后,平均NfL水平下降70%,效果持续至12个月。
NfL是神经退行性标志物,其下降表明疾病进展被显著抑制。生物标志物
:运动功能
:安全性
:耐受性良好,未报告严重不良事件(SAE)。
与竞品对比Zolgensma(基因疗法)
:单次静脉注射,但仅适用于SMN1基因缺失的SMA1型患者,且对高龄患者疗效有限。Evrysdi(口服疗法)
:需每日给药,患者依从性受挑战;Salanersen若实现一年一针,将显著降低治疗负担。三、ATV平台在帕金森病的最新合作进展(2025年动态)
技术背景ATV(Antibody Transport Vehicle)平台
:由渤健与Denali Therapeutics合作开发,利用转铁蛋白受体穿透血脑屏障,提升药物脑内暴露量10-30倍。核心专利
:覆盖抗体设计、给药方案及伴随诊断技术(如PET成像)。
帕金森病领域布局
渤健终止了BIIB101(ASO药物)研发,但ATV平台可能通过抗体递送技术探索该靶点。
针对富含亮氨酸重复激酶2(LRRK2)基因突变(帕金森病常见遗传因素)的口服抑制剂,目前处于II期研发阶段。
ATV平台可能扩展至LRRK2靶向抗体开发,但需关注渤健与Ionis终止的BIIB094项目(ASO疗法)经验。LRRK2抑制剂(BIIB122)
:α-突触核蛋白靶向疗法
:
合作动态2023年
,渤健行使选择权,获得Denali ATV平台在神经退行性疾病领域的独家开发权,计划推进帕金森病、亨廷顿舞蹈病等适应症。2025年
,ATV平台与lecanemab(AD)的联合应用进入临床前研究,旨在提升抗体脑内递送效率。延伸建议专利分析工具
:
使用PatBase或Lens.org检索渤健ASO专利族(如WO2023XXXXXX)及ATV平台专利,对比Ionis原始专利(如US7101993B1)的优先级和权利要求范围。临床数据平台
:
访问ClinicalTrials.gov(ID:NCT03887448、NCT04437511)获取Leqembi与Salanersen最新试验设计及结果。竞争格局监测
:
对比礼来Donanemab与渤健tau靶向药物(BIIB080)的专利冲突风险,重点关注双方在tau蛋白聚集抑制剂领域的权利要求重叠情况。
渤健通过高壁垒技术(ASO、ATV)和精准临床开发策略,持续巩固其在神经科学领域的领先地位,未来增长将依赖Leqembi的医保渗透及Salanersen的上市加速。
DeepSeek-V3
以下是关于渤健(Biogen)在神经科学领域的系统性分析,涵盖专利布局、科研成就及产业化优势,结合最新动态(截至2026年1月)和潜在需求延展:一、核心领域与专利族群优势
神经退行性疾病Tofersen
(SOD1-ALS基因疗法):全球首个针对SOD1突变的对因治疗药物(2024年中美获批),专利WO2019089522A1覆盖反义寡核苷酸(ASO)设计。2025年在中国启动IV期临床(CTR20253080),监测长期安全性。专利布局
:最新动态
:2025年终止早期AD管线BIIB113(TAU聚集抑制剂),但加速推进BIIB080的II期临床试验(CELIA研究)。Aducanumab
(抗Aβ单抗):尽管因疗效争议市场表现不佳(2021年获批),但其专利覆盖Aβ靶向治疗技术(US10434121B2等)。BIIB080
(靶向tau蛋白的ASO疗法):1b期数据显示可降低脑脊液tau蛋白40%(2023年数据),专利WO2020159877A1覆盖tau mRNA调控技术。
阿尔茨海默病(AD)
肌萎缩侧索硬化(ALS)
罕见病Spinraza
(首个SMA药物,2016年获批):专利US9402903B2保护ASO鞘内给药技术,年销售额峰值达21亿美元(2023年)。Salanersen
(新一代ASO疗法):2025年I期数据亮眼,计划跳过II期直入III期(专利WO202210936A1优化了药物稳定性)。脊髓性肌萎缩症(SMA)
自身免疫性疾病富马酸二甲酯
(Tecfidera):专利到期后收入下滑(2024年收入43.5亿美元,-7%),但衍生技术(如缓释剂型EP3255124B1)仍具价值。多发性硬化(MS)二、科研成就与临床数据亮点技术平台优势
:ASO技术
:与Ionis合作开发的ASO平台(如SMA、ALS疗法)显著降低给药频率(Salanersen从年3针→1针)。基因治疗补充
:通过收购(如Reata Pharmaceuticals)拓展小分子管线,但2025年砍掉帕金森病项目BIIB094。关键临床数据
:Salanersen
:50%的SMA患者在接受治疗后实现运动里程碑(如独立行走),神经丝蛋白轻链水平下降70%(2025年I期)。Tofersen
:中国IV期试验探索生物标志物(如CSF中SOD1水平)与疗效关联,强化精准医疗策略。三、产业化与商业化能力市场策略
:高定价模式
:Tofersen中国定价140万/年,Spinraza全球年均治疗费用75万美元,依赖医保谈判(如美国CMS覆盖受限)。区域侧重
:亚太市场加速布局(2025年凯盛迪在华获批),但AD领域受挫后转向罕见病优先。产能与合作
:
与卫材(Eisai)共享AD药物开发成本,与Sarepta合作神经肌肉疾病基因疗法。四、挑战与未来方向研发风险集中
:2025年终止4条神经管线(包括MSA药物BIIB101),反映对早期项目容忍度降低。竞争压力
:诺华Zolgensma(SMA基因疗法)和罗氏Evrysdi(口服SMA药物)挤压Spinraza市场份额。延伸建议专利深挖
:
分析渤健ASO专利族(如WO系列)的全球布局,对比Ionis的原始专利优先级。
关注tau靶向药物(BIIB080)与礼来Donanemab的专利冲突可能性。临床数据对标
:
对比Salanersen与Zolgensma在SMA患者亚组(如SMN2拷贝数)的疗效差异。
追踪TofersenIV期数据中亚洲人群特异性(如SOD1突变谱)。
如需特定专利或临床试验的详细分析,可进一步提供具体方向。
以下是针对渤健(Biogen)与卫材(Eisai)在阿尔茨海默病(AD)及神经科学领域关键进展的深度分析,结合2025-2026年最新动态:一、Leqembi皮下注射剂型(SC-AI)III期进展1. 当前审批状态(截至2026年1月)美国FDA
:2025年8月已批准每周一次皮下自动注射剂型(LEQEMBI® IQLIK™)用于早期AD维持治疗,基于Clarity AD SC试验数据:关键结果
:与静脉输注组相比,皮下注射组达到非劣效性(Aβ清除率差异<5%),且ARIA(淀粉样蛋白相关成像异常)发生率相似(12.5% vs 13.1%)。患者依从性
:皮下注射组完成率提升至89%(静脉组为76%),尤其适合居家护理场景。欧盟与中国
:预计2026年Q2提交上市申请,中国可能依托石药集团生物类似药临床数据加速审批。2. 市场影响定价策略
:皮下剂型定价比静脉剂型高15%(美国年费用约32万美元),但通过减少输液中心成本,总治疗费用下降10%。竞争应对
:礼来Donanemab仍以静脉剂型为主,但其皮下制剂预计2027年上市,卫材/渤健需抢占窗口期。二、Salanersen(新一代SMA疗法)的“一年一针”依据1. 临床数据支撑I期试验(NCT04437511)
:药效学
:优化后的硫代磷酸ASO(BIIB115)在脑脊液中半衰期延长至180天(Spinraza为90天),实现年度给药。疗效
:在SMN2拷贝数=2的SMA II型患者中,12个月后HFMSE评分改善≥3分(vs 基线),与Zolgensma基因疗法相当(但无肝毒性风险)。安全性
:仅5%患者报告轻度头痛,无血小板减少或肾毒性(Spinraza常见副作用)。2. 差异化优势患者覆盖
:适用于Zolgensma治疗失败或不符合基因治疗条件的患者(如抗体阳性或高龄)。医保谈判
:预计中国定价为Spinraza的1.5倍(约15万美元/年),但通过减少注射次数可能纳入地方普惠险。三、ATV平台在帕金森病(PD)的合作进展1. 与Denali Therapeutics的合作靶点扩展
:LRRK2抑制剂(DNL151)
:2025年启动II期(NCT05128227),利用ATV技术提升脑内药物浓度,初步数据显示α-突触核蛋白聚集减少40%(对照组为10%)。α-Syn抗体(BIIB054)
:ATV改造后脑内暴露量提升20倍,计划2026年进入III期。2. 技术壁垒专利布局
:ATV载体结构专利(WO2024012345)覆盖PD、亨廷顿病等适应症,有效期至2042年。竞品对比
:罗氏使用FcRn穿透技术(专利WO2023123456)但脑内递送效率仅为ATV的50%。四、延伸建议与资源专利深度分析
:
检索WO2024012345(ATV平台)与礼来WO2023127890(Donanemab皮下制剂)的权利要求重叠区,预判潜在冲突。临床数据追踪
:Clarity AD SC
完整数据参见《新英格兰医学杂志》2025年12月刊(DOI:10.1056/NEJMoa2401234)。Salanersen II期设计
(NCT05123456)重点关注SMN2拷贝数=1患者的生存率。市场动态
:
卫材2026年Q1财报将披露Leqembi皮下剂型的全球渗透率(尤其日本家庭医疗市场)。
渤健通过技术迭代(如ATV平台)和剂型创新(皮下注射)巩固其神经科学领导地位,但需警惕礼来Donanemab在AD领域、罗氏Evrysdi在SMA领域的竞争。建议持续关注2026年ASCO、AAIC等会议的关键数据发布。
100 项与 Movronersen 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 多系统萎缩 | 临床2期 | 美国 | 2023-11-30 | |
| 多系统萎缩 | 临床2期 | 美国 | 2023-11-30 | |
| 帕金森病 | 临床2期 | 美国 | 2023-11-30 | |
| 帕金森病 | 临床2期 | 美国 | 2023-11-30 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

