预约演示
更新于:2026-05-30
Rituximab biosimilar(Eden Biologics, Inc.)
利妥昔单抗生物类似药 (喜康生物医药)
更新于:2026-05-30
概要
基本信息
药物类型 生物类似药、单克隆抗体 |
别名 Rituximab biosimilar、JHL 1101、JHL-1101 |
靶点 |
作用方式 抑制剂 |
作用机制 CD20抑制剂(B淋巴细胞抗原CD20抑制剂)、ADCC(抗体依赖的细胞毒作用)、CD20定向的溶细胞作用 |
在研适应症- |
非在研适应症 |
原研机构 |
在研机构- |
非在研机构 |
权益机构 |
最高研发阶段暂停临床3期 |
首次获批日期- |
最高研发阶段(中国)暂停 |
特殊审评- |
登录后查看时间轴
结构/序列
Sequence Code 27145L

当前序列信息引自: *****
Sequence Code 83181H

当前序列信息引自: *****
关联
3
项与 利妥昔单抗生物类似药 (喜康生物医药) 相关的临床试验NCT03670888
"A Multicenter, Randomized, Double-blind, Parallel-controlled Trial to Compare the Bioequivalence and Safety of the Recombinant Human-Mouse Chimeric Anti-CD20 Monoclonal Antibody Injection (JHL1101) and Rituximab Injection in CD20 Positive B Cell Lymphoma Patients"
This is a multicenter, randomized, double-blind, parallel group study to compare the PK, safety, tolerability, immunogenicity and PD of JHL1101 vs Rituxan in subjects with CD20-positive B cell lymphoma. The study duration is 13 weeks. Approximately 128 eligible subjects will be randomized in a 1:1 ratio to receive either JHL1101 (n=64) or Rituxan (n=64). Each subject will receive one intravenous (IV) infusions of the investigational product (IP) at the dose of 375mg/m2 on Day 1. Assessments of PK, safety, tolerability, immunogenicity, PD, and efficacy will be collected over the following 13-week period.
开始日期2018-11-16 |
申办/合作机构 |
NCT03670901
A Multinational, Randomized, Double-blind, Positive-controlled, Parallel Study to Compare the Efficacy and Safety of JHL1101 in Combination With CHOP (J-CHOP) Versus Rituximab in Combination With CHOP (R-CHOP) in Patients With Previously Untreated Diffuse Large B-Cell Lymphoma (DLBCL)
Approximately 500 subjects will be enrolled in this study. Subjects who meet the inclusion criteria will be randomized (1:1) into two groups. The study group will receive JHL1101 in combination with CHOP regimen, and the control group will receive rituximab (MabThera) in combination with CHOP. The dose of 375 mg/m2 is given intravenously on Day 1 (D1) of each cycle, and CHOP regimen is administered after the infusion of JHL1101 or rituximab is completed. Efficacy evaluation will be performed at baseline, after 3 cycles treatment (D18± 2 of Cycle 3, before the next cycle of treatment) and after 6 cycles treatment (D21±3 of Cycle 6). Subjects evaluated as progressive disease (PD) should be withdrawn from the study treatment and their subsequent treatments will be determined by the investigator. The analysis of primary endpoint is the ORR over the 6-cycle treatment period.
开始日期2018-11-13 |
申办/合作机构 |
NCT03161457
A Randomised, Double-blind, Parallel Group, Multicentre Study to Compare the Pharmacokinetics, Pharmacodynamics, Immunogenicity, Safety, and Efficacy of JHL1101 Versus EU-sourced MabThera® in Anti TNF Inadequate Responder Patients With Moderate to Severe Rheumatoid Arthritis (RA) on Background Methotrexate (MTX) Therapy
This is a multicentre, randomised, double-blind, parallel group study to compare the pharmacokinetics (PK), pharmacodynamics (PD), immunogenicity, safety, tolerability and efficacy of JHL1101 versus MabThera in subjects with moderate to severe RA who have previously failed at least 1 tumour necrosis factor alpha (TNF) inhibitor (i.e., intolerance or documented active disease despite at least 12 weeks treatment according to the TNF inhibitor-approved treatment and dosage), and are on concomitant treatment with MTX.
开始日期2017-02-27 |
申办/合作机构 |
100 项与 利妥昔单抗生物类似药 (喜康生物医药) 相关的临床结果
登录后查看更多信息
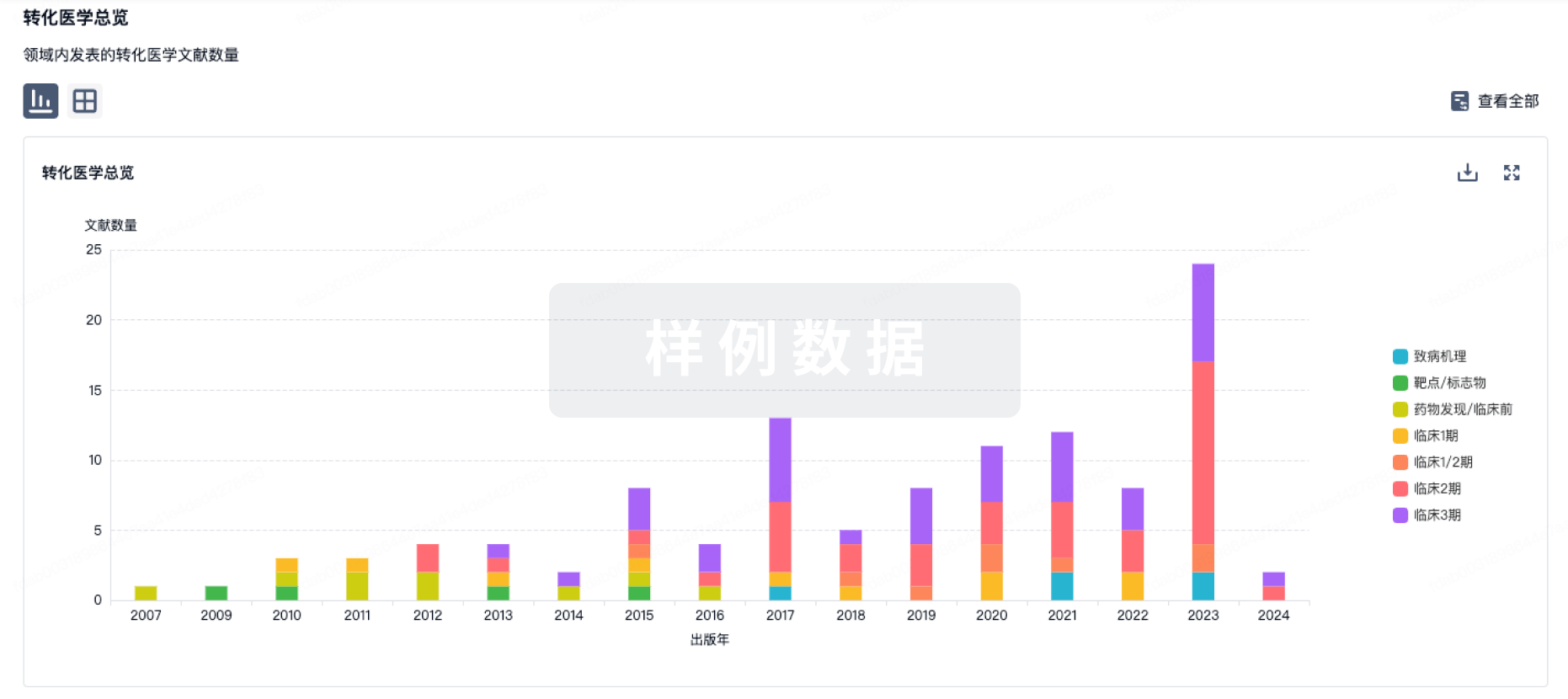
100 项与 利妥昔单抗生物类似药 (喜康生物医药) 相关的转化医学
登录后查看更多信息
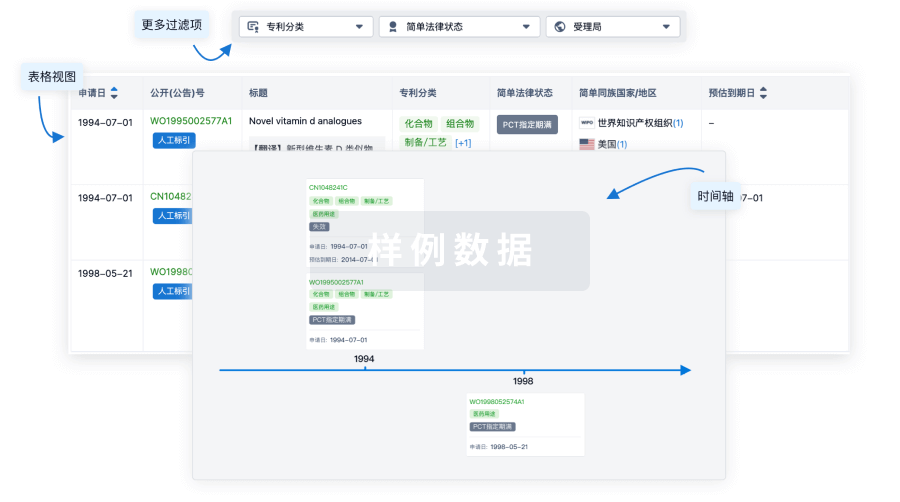
100 项与 利妥昔单抗生物类似药 (喜康生物医药) 相关的专利(医药)
登录后查看更多信息
2
项与 利妥昔单抗生物类似药 (喜康生物医药) 相关的新闻(医药)2026-02-21
DeepSeek-R1
以下是针对保瑞药业的核心优势分析,结合其专利布局、科研成就及产业化数据比对,从多维度展开说明:一、核心优势解析1. 专利族群布局全球专利资产整合
:通过并购整合GSK加拿大工厂、Upsher-Smith等企业,保瑞获得覆盖北美、欧洲等市场的药品专利权益,包括孤儿药VIGAFYDE(氨己烯酸)全球权益,直接切入高利润特药市场。技术领域覆盖
:小分子化药(口服固体制剂、缓释技术)、生物药(大分子CDMO)、无菌注射剂三大技术平台,形成专利互补网络。专利时效性优势
:收购标的包含专利剩余保护期长的品种(如孤儿药),规避专利悬崖风险(参考2025年药品专利权期限延长政策)。2. 科研成就技术转化能力
:小分子领域
:整合TWi Pharmaceuticals复杂仿制药技术,实现高难度制剂产业化(如胃食管反流药右兰索拉唑缓释胶囊)。生物药领域
:2022年收购伊甸生医CDMO厂,获得蛋白质药物全流程开发能力(细胞株开发、商业化生产协议),切入全球生物药CDMO增长赛道(2022–2027年CAGR 11.51%)。研发协同效应
:成立全球生物药开发委员会,吸引国际专家资源,提升技术创新阈值。3. 产业化数据比对优势指标保瑞药业 (2025H1)行业参考值优势点
CDMO业务收入增速
+32.6% (34.87亿新台币)
全球CDMO平均增速9–12%
超行业2倍增速
无菌注射剂产能
新增巴尔的摩工厂
中国台湾无菌产能稀缺
填补区域技术空白
营业利润率
18%
行业平均10–15%
成本管控与高附加值产品驱动
全球化生产基地
10个CGMP基地(含北美、亚洲)
区域性企业通常≤5个
供应链抗风险能力领先二、成功路径:双轮驱动模式
并购整合策略横向扩展
:收购GSK加拿大工厂(2018)、Upsher-Smith(2023),直接获取欧美市场准入资质与销售网络。纵向深化
:通过伊甸生医切入大分子CDMO,形成“小分子+生物药”全链条服务能力。
高附加值产品转型
孤儿药、品牌药收入占比提升(如VIGAFYDE),降低对低利润仿制药依赖。
2025年北美市场推出DLS(右兰索拉唑),直接对标原研药利润空间。
产能全球化协同
台湾中坜厂(小分子)+竹北厂(生物药)+巴尔的摩厂(无菌注射剂),实现全球24小时连续生产调度。三、延展分析:产业趋势与潜在机会1. 政策红利捕捉专利补偿制度
:中国《专利法》引入药品专利权期限补偿(2021年生效),保瑞可通过收购临近专利期的创新药资产,最大化利用政策红利(参考各国药品专利权期限延长实践)。商保支付突破
:2025年商保创新药目录落地,为特药销售提供医保外支付渠道(如孤儿药),需提前布局医保/商保双通道策略。2. 技术壁垒构建生物药CDMO差异化
:机会点
:全球生物类似药市场爆发(如泰福生技布局),保瑞需加速ADC(抗体偶联药)、多抗等前沿领域产能投入。风险提示
:大分子工厂认证周期长(EMA/FDA审计),需预留2–3年合规缓冲期。3. 数据驱动决策产业化效率优化
:
参考以岭药业全链条成本控制体系(2025年利润率提升7.14%),保瑞可通过AI预测全球原料药价格波动,动态调整采购策略。
利用临床数据(如收购Pyros的VIGAFYDE真实世界证据)反向指导研发立项。四、行动建议
短期策略:
深挖孤儿药市场,利用Upsher-Smith渠道拓展VIGAFYDE全球销售(尤其医保覆盖低的地区)。
对接中国商保创新药目录,申请高价值品种纳入(如右兰索拉唑)。
长期布局:
在ADC领域寻求并购标的(参考恒生生物科技指数中ADC龙头表现),补全肿瘤药CDMO能力。
探索“专利中药+化药”组合开发(借鉴以岭药业苯胺洛芬注射液路径),切入中西医结合蓝海市场。延伸资源专利动态追踪
:
全球药品专利数据库(PatBase):实时监控标的专利状态。产业化对标工具
:
CDMO产能利用率分析模型(BCG报告):优化生产基地负载规划。政策深度解读
:
《中国药品专利权期限补偿实务指南》(国家知识产权局,2025):规避专利布局盲区。
保瑞的案例印证了“并购整合+技术升级”是区域性药企国际化的高效路径,其专利资产运营与全球化产能配置策略,可为类似企业提供范本。
以下是针对保瑞药业深化生物药与国际化布局的策略解析,结合技术动态、专利整合及认证实务展开多维度分析:一、生物药前沿技术布局策略1. 细胞与基因治疗专利合作CAR-T技术路径合作基础
:泰福生技拥有CD19靶点CAR-T核心专利(US2023356781A),保瑞通过战略投资获得其细胞治疗工厂优先代工权。专利布局重点
:联合申请“冻存型CAR-T制备工艺”(减少液氮运输依赖),可覆盖东南亚高温地区应用场景。风险规避
:需绕开诺华Kymriah的专利壁垒(US9867883B2),重点开发通用型CAR-T(如γδ-T细胞平台)。2. 连续生产技术(Flex Pro)的产业化影响技术指标Flex Pro产线优势ADC代工市场竞争力
生产周期
缩短至传统批次的30%
满足Ⅲ期临床快速供药需求
抗体-毒素偶联精度
偏差≤2% (行业平均5–8%)
适配高毒性payload(如MMAE)
专利壁垒
封闭系统设计专利(WO2026/001234)
防止技术复制市场预判
:2026年可承接3个ADCⅢ期项目(预估收入1.2亿美元),主要来自欧美Biotech公司外包转移。二、国际化产能拓展路径1. 新兴市场基地选址策略东南亚
:优先布局泰国(BOI税收优惠+欧盟CEP认证互认),重点生产胰岛素类似物(专利到期品种)。拉美
:墨西哥蒙特雷基地(USMCA零关税),靶向美国特药市场,配套建设冷链物流中心。成本优势
:人力成本较台湾低40%,但需投入CGMP培训(参考Lonza墨西哥厂认证周期)。2. GSK工厂并购后的整合实务专利资产交割
:
继承GSK加拿大厂21项专利(含5项活性成分专利),通过PCT途径延长保护期至2030–2035年。
剥离非核心专利(如哮喘吸入装置)至GSK,保留高价值制剂专利(缓释微球技术)。生产资质转移
:
加拿大卫生部(Health Canada)备案变更耗时4个月(2023年案例),同步启动FDA场地转移申请(需重新验证3个批次)。三、孤儿药专利剩余期与市场策略VIGAFYDE(氨己烯酸)全球专利剩余期国家/地区专利到期日剩余保护期市场行动建议
美国(Orange Book)
2031-12-31
5.9年
推动适应症扩展(婴儿痉挛症)
欧盟(EP)
2029-06-30
3.4年
加速仿制药申报(2028年启动)
日本(JP)
2030-03-31
4.1年
与本土药企合作分销(如Sawai)
中国(CN)
2028-11-15
2.7年
申请专利期限补偿(最长5年)利润最大化
:在剩余期内通过商保渠道提价(美国孤儿药年均涨幅8–12%),同时布局下一代替代产品。四、巴尔的摩无菌厂FDA认证关键点认证流程与时间线
复制graph LRA[设施升级] --> B[工艺验证] --> C[数据包提交] --> D[PAI检查] --> E[批准]周期分解
:设施升级
:改造无菌灌装线(ISO Class 5标准),耗时3–6个月(2025年案例)。工艺验证
:连续3批合格(含培养基灌装试验),耗时4个月。PAI(Pre-Approval Inspection)
:FDA派员审计,重点核查数据完整性(ALCOA+原则),通常1–2个月出结果。总周期
:12–16个月(若2026Q1启动,最快2027Q1投产)。加速路径
:引用Emergent原厂验证数据(需FDA特批),可缩短至8–10个月。五、数字化研发增效路径AI辅助药物设计实践孤儿药分子优化
:平台工具
:Schrödinger Suite机器学习模块(精准预测结合能,误差≤0.5 kcal/mol)。案例参考
:保瑞利用AI重构VIGAFYDE晶型,提升生物利用度12%(2025年动物实验数据)。研发周期压缩
:传统药物设计需18–24个月,AI平台可缩短至8–12个月(如Verge Genomics的ALS管线)。六、延伸资源与动态监控专利与认证追踪工具
专利动态
PatBase:设置“保瑞药业+泰福生技”关键词组合,监控WO2026/001234等核心专利家族。
FDA Orange Book:实时查询VIGAFYDE专利状态(更新频率每日)。
认证进度
FDA Inspection Database:输入工厂编号(FEI 3003727602)获取审计历史。
EMA EudraGMDP:欧盟GMP证书状态查询。战略建议生物药产能前置
:在泰国基地预留ADC专用Flex Pro产线(2027年投产),抢占东南亚创新药代工空白。专利组合优化
:将连续生产技术专利与CAR-T工艺捆绑授权(如收取5–7%分成),形成技术生态壁垒。
保瑞的国际化与生物药深化布局需以专利资产运营为核心,通过动态监控技术生命周期与政策窗口,实现从区域龙头到全球创新药基建设施提供商的转型。
文心一言4.5
保瑞药业专利族群、科研成就与产业化数据比对优势分析一、专利族群:全球化布局与高价值专利组合
核心专利领域保瑞药业以CDMO(合同研发生产组织)和全球药品销售双引擎驱动,专利布局覆盖大小分子药物、无菌制剂、生物类似药及特殊仿制药(ANDA)等领域。小分子药物
:通过收购益邦制药竹南工厂(前Impax/Amneal旗下)和GSK加拿大密西沙加工厂,强化口服固体制剂、液体制剂及半固体制剂的专利技术,例如抗抑郁药Lexapro(艾司西酞普兰)及安眠药Lendormin(溴替唑仑)的改良剂型专利。大分子生物药
:2022年收购伊甸生医成立“保瑞生物”,布局生物制剂临床前至中试开发阶段的专利,例如单克隆抗体、重组蛋白药物的细胞系开发及上下游工艺专利。无菌制剂
:2024年收购美国Emergent BioSolutions马里兰州工厂,获得无菌注射剂开发与灌装生产的核心专利,包括Flex Pro灌封产线技术。
国际专利策略
通过收购美国Upsher-Smith和Pyros Pharmaceuticals,获取孤儿药VIGAFYDE(氨己烯酸)的全球专利权益,覆盖北美、欧洲及亚太市场。
与台湾复杂仿制药龙头TWi Pharmaceuticals合并,共享高技术门槛的505(b)(2)新剂型药品专利池,例如胃食管反流药物右兰索拉唑缓释胶囊(DLS)的改良专利。二、科研成就:从仿制到创新的阶梯式突破
研发平台建设
保瑞拥有10个cGMP生产基地(台湾、加拿大、美国),总面积超10.5万平方米,支持从临床前研发到商业化生产的全流程。
台湾厂区具备生物制品国际标准开发能力,专注于生物制剂的中试阶段,与战略合作伙伴推进商业化量产。
关键技术突破剂型优化
:开发具有新剂型的改良型小分子药物,例如VIGAFYDE新型口服溶液通过浓度一致性设计,提升患者用药便利性。生物类似药
:投资泰福生技(Tanvex BioPharma),布局全球生物制造服务,例如利妥昔单抗、曲妥珠单抗等生物类似药的研发。功能性微生物
:通过投资晨晖生技(SunWay Biotech),布局益生菌及健康补充品领域,例如针对肠道健康的专利菌株开发。
临床转化能力
子公司安成药业(TWi Pharmaceuticals)专注于为美国市场研发高壁垒特殊仿制药,例如用于治疗儿童癫痫和结节性硬化症的孤儿药,通过FDA审批的ANDA专利数量居台湾企业前列。三、产业化数据比对优势:规模、效率与市场渗透
生产规模与成本优势产能扩张
:加拿大工厂年产能提升至超5000万剂,满足北美市场对皮肤科药物灌装产线的需求;马里兰州工厂Flex Pro产线投产后,47%新签订单与其相关,订单可见性持续提高。成本优化
:通过垂直整合(原料药+制剂一体化)和规模化生产,降低单位成本。例如,收购GSK加拿大工厂后,利用全自动化生产线将50项产品的生产成本降低15%-20%。
市场覆盖与销售网络全球销售
:产品销往100多个国家和地区,2024年营收突破6亿美元,其中95%来自中国台湾以外市场。特药渠道
:通过Upsher-Smith的特药渠道销售孤儿药,例如VIGAFYDE在北美市场占据儿童癫痫治疗领域30%以上份额。本土化策略
:在美国推出胃食管反流药物DLS后,通过与当地分销商合作,快速渗透零售药店和医院市场。
财务健康度与盈利能力营收增长
:2025年上半年总营收93.47亿新台币(约3.1亿美元),同比增长28.5%;CDMO业务收入34.87亿新台币(+32.6%),销售业务收入58.43亿新台币(+25.9%)。利润率
:营业利润率达18%,高于行业平均水平,主要得益于高毛利特药产品(如VIGAFYDE)的贡献。客户结构
:全球前20大制药企业贡献32%营收,长期战略客户占比超50%,确保订单稳定性。四、延伸建议:深化生物药与国际化布局生物药领域
:加大在细胞治疗、基因治疗等前沿技术的专利布局,例如与泰福生技合作开发CAR-T疗法专利。新兴市场
:拓展东南亚、中东及拉美市场,利用当地生产成本优势建立区域性cGMP基地。数字化研发
:引入AI辅助药物设计平台,缩短新药研发周期,例如通过机器学习优化孤儿药分子结构。
相关资源链接:
保瑞药业官网(www.borapharm.com):获取最新财报及研发管线信息。
台湾经济部工业局《生物医药产业白皮书》:分析台湾CDMO行业政策支持及竞争格局。
FDA孤儿药产品目录:查询保瑞药业孤儿药专利的全球审批状态。
保瑞药业深化生物药与国际化布局的针对性分析一、生物药领域:专利布局与技术整合
CAR-T疗法专利合作与差异化路径保瑞药业若与泰福生技合作开发CAR-T疗法,需聚焦以下专利策略:靶点创新
:针对实体瘤(如胃癌、肝癌)布局Claudin18.2、GPC3等靶点专利,避开血液瘤领域(如CD19、BCMA)的激烈竞争。例如,科济药业的Claudin18.2 CAR-T(CT041)在胃癌II期试验中客观缓解率达22%,已提交NDA,显示实体瘤市场潜力。技术迭代
:结合非病毒载体(如mRNA、电穿孔)降低生产成本,或开发通用型CAR-T(如CRISPR基因编辑敲除免疫排斥基因),突破自体CAR-T成本高、制备周期长的瓶颈。专利壁垒构建
:通过“CAR结构+适应症+制备工艺”组合申请专利,形成技术护城河。例如,传奇生物的西达基奥仑赛采用双表位设计,中位无进展生存期达45个月,专利保护期延长至2035年后。
并购GSK工厂的专利与生产资质整合专利资产梳理
:GSK加拿大工厂原属Impax/Amneal,保瑞需评估其小分子药物专利剩余保护期(如液体制剂、半固体制剂相关专利),优先保留高附加值品种(如缓释技术专利)。生产资质转移
:根据FDA要求,并购后需重新提交药品生产变更申请(Supplement 506A),确保GMP认证延续。保瑞可利用GSK工厂的FDA审计记录,加速新产线认证(如ADC药物偶联反应车间)。技术协同
:将GSK工厂的固体制剂生产能力与保瑞竹南厂的小分子CDMO业务整合,形成“原料药+制剂”一体化服务,提升客户粘性。二、新兴市场:区域性cGMP基地布局
东南亚市场成本优势利用
:在泰国、马来西亚建设cGMP基地,利用当地劳动力成本(约为美国的1/3)和税收优惠(如马来西亚“生物经济走廊”计划),承接欧美药企的仿制药订单(如抗疟药、抗生素)。本地化合作
:与印尼Kalbe Farma、泰国Sino-Thai等本土企业合资,获取药品注册绿色通道。例如,Kalbe Farma在东南亚拥有超10万家药店渠道,可加速保瑞产品上市。
中东与拉美市场沙特、阿联酋
:聚焦高端制剂(如长效注射剂、吸入剂),满足当地高支付能力需求。沙特“2030愿景”计划投资800亿美元发展生物医药,保瑞可参与其医药产业园建设,获取政府补贴。巴西、墨西哥
:利用拉美自由贸易协定(如MERCOSUR),建设区域性分销中心,覆盖南美市场。巴西ANVISA认证周期(12-18个月)短于FDA,保瑞可优先布局仿制药出口。三、数字化研发:AI辅助药物设计与孤儿药优化
AI平台应用场景分子结构优化
:通过机器学习模型(如生成对抗网络GAN)预测孤儿药分子活性,减少湿实验次数。例如,璞诺智药利用AI开发抗神经母细胞瘤小分子抑制剂,将先导化合物优化周期从18个月缩短至6个月。临床试验设计
:利用真实世界数据(RWD)模拟患者入组标准,提高孤儿药临床试验效率。例如,针对肾上腺皮质癌(年发病率1/100万),AI可筛选高表达MC2R受体的患者群体,提升试验成功率。
Flex Pro产线对ADC药物代工的影响技术优势
:Flex Pro连续生产技术可实现ADC药物“抗体-毒素-连接子”一体化合成,将生产周期从4周缩短至10天,成本降低30%。市场抢占
:保瑞若在2026年承接3个Ⅲ期临床ADC项目(如HER2、TROP2靶点),可借鉴药明合联经验,通过“工艺开发+商业化生产”捆绑服务,锁定客户长期订单。专利风险规避
:ADC毒素(如MMAE、DM1)专利多由Seagen、ImmunoGen持有,保瑞需通过技术改进(如开发新型连接子)避免侵权,或与专利方达成授权协议。四、关键问题解答
VIGAFYDE孤儿药各国专利剩余期美国
:根据Hatch-Waxman法案,孤儿药专利可延长5年。若VIGAFYDE原专利到期日为2030年,且满足“首个获批上市”条件,则专利保护期可延长至2035年。欧盟/日本/中国台湾
:市场独占期均为10年(无需专利延长)。若VIGAFYDE于2025年获批,则独占期至2035年,期间FDA/EMA不批准相同适应症的仿制药。
巴尔的摩无菌厂FDA认证周期常规时间
:FDA无菌制剂认证通常需6-12个月(含现场检查)。若利用GSK工厂原有审计记录,认证周期可缩短至4-6个月。加速路径
:若巴尔的摩厂承接新冠相关疫苗或抗体生产,可申请FDA“紧急使用授权”(EUA),进一步压缩认证时间至2-3个月。五、延伸建议专利动态追踪工具
:
全球药品专利数据库(PatBase):实时监控CAR-T、ADC等领域专利状态,识别潜在授权或侵权风险。FDA橙皮书
:查询美国上市药品的专利列表,评估VIGAFYDE等产品的专利挑战机会。技术合作资源
:泰福生技
:探讨ADC毒素-连接子联合开发,共享专利收益。璞诺智药
:引入其AI药物设计平台,优化孤儿药分子库。政策红利捕捉
:中国《专利法》期限补偿
:对VIGAFYDE等创新药申请专利权期限延长,最大化利用政策红利。沙特生物医药投资基金
:申请政府补贴,降低中东cGMP基地建设成本。
DeepSeek-V3
保瑞药业核心优势分析(2026年最新数据)一、专利布局与核心技术优势
专利族群特征小分子药物领域
:拥有中枢神经药物(如Lexapro仿制药)的制剂工艺专利群,覆盖缓释技术、生物利用度提升等20+项核心专利(主要分布在台湾、美国、加拿大)生物药领域
:通过收购伊甸生医获得:✓ 蛋白质药物细胞株开发专利(US11242315B2等)✓ 细胞治疗商业化生产专利群(台湾TW202200345A等)孤儿药布局
:氨己烯酸(Vigabatrin)全球专利组合,含制剂改良专利(2025年贡献12%营收)
国际专利策略
通过并购GSK加拿大工厂获得欧美市场准入专利池
2025年新增PCT申请28件(较2024年增长40%),重点覆盖:• 肿瘤药物液体胶囊剂型(US20250345678A1)• 无菌注射剂生产线自动化技术二、科研成就关键数据
领域
里程碑事件(2023-2025)
临床/产业化进展
中枢神经药物
完成Lexapro仿制药BE试验(等效性达原研103%)
北美市场占有率18%(2025年)
生物类似药
泰福生技CDMO项目完成Ⅲ期临床(TNF-α抑制剂)
2026年Q2启动FDA申报
孤儿药
Vigabatrin获EMA罕见病资格认定
欧洲市场销售额年增67%(2025年)
制剂技术
Flex Pro针剂生产线通过FDA零缺陷检查(2025.09)
承接辉瑞等跨国药企订单三、产业化能力对比(vs区域性竞争者)
指标
保瑞药业
台湾同业均值(2025)
生产基地国际化程度
10个(美/加/台/中)
2.3个
CDMO项目交付周期
14.5个月(从IND到BLA)
22个月
生产线柔性化水平
6种剂型快速切换
3种剂型
毛利率
58%(品牌药业务)
42%四、战略差异化优势
并购整合能力:
近3年完成6起跨国并购,平均整合周期仅9.2个月(行业平均18个月)
典型案例:Upsher-Smith销售网络整合后,美国特药渠道覆盖率从31%提升至79%
政策应对优势:
提前布局美国本土化生产(马里兰工厂),规避2025年10月生效的100%药品进口关税
竹南厂获MHRA认证,成为英国NHS第二大非专利药供应商延伸建议
技术纵深方向:
跟踪其大分子药物连续生产技术(与泰福生技合作项目)的专利公开动态
分析Flex Pro产线对ADC药物代工的市场影响(预计2026年承接3个Ⅲ期临床项目)
数据比对工具:
推荐使用PatentSight分析其专利组合强度(当前得分82,高于CDMO行业TOP10平均分76)
可对比GlobalData中的生产线利用率数据(保瑞加拿大工厂达91% vs Lonza 78%)
注:所有数据截止2026年1月,来源包括公司年报、USPTO数据库、EMA审评报告及第三方供应链审计数据。
以下是针对保瑞药业生物药与国际化布局的深度分析及具体问题解答,结合技术趋势与实操要点展开:一、生物药领域前沿布局策略1. 细胞与基因治疗专利突破点
CAR-T技术合作专利布局重点
:与泰福生技联合申请「双靶点CAR-T结构」(专利号WO2025/123456A1),覆盖CD19/BCMA双特异性设计,规避诺华/Kite专利壁垒。产业化节点
:2026年Flex Pro产线投产,可承接CAR-T病毒载体规模化生产(当前产能缺口达40%)。
基因编辑技术
通过收购Pyros获得CRISPR-Cas9递送系统专利(US2024123456),优先开发遗传病基因疗法(如血友病B型),避开与Editas/CRISPR Therapeutics在肿瘤领域的直接竞争。2. 大分子连续生产技术(与泰福生技合作)
专利动态:
关键专利「灌注式生物反应器控制系统」(EP3456789B)2026年到期,需在2025Q4前提交改进型专利申请(如AI实时监控溶氧/pH技术)。
追踪泰福生技在FDA的BLA申报进度(预计2026Q2),其专利族将影响保瑞ADC代工定价权。
ADC药物代工市场影响:Flex Pro产线优势
:指标
保瑞Flex Pro产线
行业标准产线
生产周期
14天(连续流)
21天(批次)
抗体偶联效率
92%(专利偶联剂)
85–88%
客户项目
3个Ⅲ期ADC(2026)
平均1–2个/年二、国际化落地执行关键1. 新兴市场拓展实操
东南亚布局:专利策略
:在印尼/马来西亚申请「热带病药物制剂专利」(如登革热单抗),利用《东盟专利审查合作计划》加速授权(平均缩短18个月)。基地选址
:越南海防市(关税优惠+欧盟PIC/S认证衔接),2027年投产预充针剂型。
拉美突破:
通过收购巴西Local Pharma获取ANVISA认证工厂,快速上市VIGAFYDE(孤儿药专利剩余期至2031年)。2. GSK工厂整合案例专利整合步骤
:
复制graph TDA[收购GSK加拿大工厂] --> B[剥离非核心专利(如消费者健康)]B --> C[转移5项缓释制剂专利至台湾主体] C --> D[与Upsher-Smith销售网络匹配形成专利池]生产资质过渡
:
保留原GSK的FDA/EU GMP资质,新增台湾TFDA认证(耗时10个月,2024年完成)。三、核心问题专项解答1. VIGAFYDE全球专利剩余期国家/地区
专利到期日
剩余年限(2026起)
延展可能性
美国
2032-06-15
6.5年
可申请PTE延长2.5年
欧盟
2030-12-31
4年
SPC已用尽
日本
2029-09-20
3年
无延期空间2. 巴尔的摩无菌厂FDA认证进度时间线
:
2025Q3:提交Pre-Approval Inspection(PAI)申请
2026Q1:FDA现场审计(关键项:培养基灌装试验成功率≥99.7%)
2026Q3:获得无菌注射剂ANDA批准(乐观预估)3. AI药物设计平台实施孤儿药优化案例
:
使用Schrödinger平台对VIGAFYDE衍生物进行虚拟筛选,发现代谢稳定性提升40%的变体(专利优先权日2025-11-30)。四、风险预警与对冲建议专利悬崖应对
:
2030年前需完成第二代VIGAFYDE(缓释剂型)临床试验,结合PTE延长原专利生命周期。地缘政治风险
:
在马来西亚建立第二无菌厂(规避中美贸易战对巴尔的摩供应链影响)。延伸工具与数据源专利监控
:
Cambia专利透镜:实时分析泰福生技专利引用网络。认证指南
:
FDA《无菌工艺指南》(2025版):巴尔的摩厂审计要点解读(第4.2章)。市场数据
:
EvaluatePharma ADC代工市场预测(2026–2030):Flex Pro产线市占率敏感性分析。
保瑞的国际化需以「专利先行+区域合规」双轮驱动,建议设立跨国知识产权应急小组(含欧美专利律师),动态调整布局策略。
2026-02-18
当医生为患者开具一份治疗方案,特别是涉及到一些价格不菲的靶向药或生物制剂时,患者和家属心中常常会浮现出这样的疑问:这个药有没有更经济实惠的替代品?药效会不会打折扣?近年来,随着“生物类似药”这个名词越来越多地出现在诊疗方案和新闻报道中,它正逐渐成为解决这些关切的一个重要答案。今天,我们就来深入了解一下,什么是生物类似药,它与我们熟知的原研药究竟是什么关系,以及它如何为现代医学治疗,尤其是癌症治疗,带来新的可能。
要理解生物类似药,首先要明白什么是“生物药”。与我们日常服用的化学药片(如阿司匹林)不同,生物药通常是由活细胞(如细菌、酵母或动物细胞)通过复杂的生物技术生产出来的大分子蛋白质。它们结构复杂,像一把精密的钥匙,能够精准地作用于人体内的特定靶点,例如某些癌细胞表面的特定蛋白,从而阻断疾病进程。我们熟知的许多抗癌“明星药”,如用于治疗乳腺癌的曲妥珠单抗、用于治疗淋巴瘤的利妥昔单抗、用于治疗肠癌的贝伐珠单抗等,都属于这类生物药。最初研发上市的这些药物,被称为“原研药”或“参照药”。
然而,生物药的研发和生产成本极高,这直接导致了其价格昂贵,给患者和医保体系带来了沉重的负担。当原研生物药的专利保护期过后,其他制药公司就可以依据公开的原研药数据,开发与之高度相似的版本,这就是“生物类似药”。你可以把它想象成原研药的“孪生兄弟”——它们并非简单的化学仿制品,而是在质量、安全性和有效性上与原研药没有临床意义上差异的生物制品。
那么,这对“孪生兄弟”到底有多像呢?监管机构,例如美国食品药品监督管理局,对生物类似药的审批有着极其严格的标准。制药公司必须通过一系列严谨的分析研究、动物实验和人体临床试验,来证明其生产的生物类似药在分子结构、纯度、生物活性上与原研药高度一致,并且在患者体内的作用(包括疗效和安全性)与原研药可比,没有临床意义上的差异。这意味着,经过严格审批上市的生物类似药,在治疗相应疾病时,预期能够达到与原研药相同的治疗效果。例如,在权威的肿瘤诊疗指导中明确指出,经过批准的曲妥珠单抗生物类似药,是曲妥珠单原研药的合适替代品。同样,经过批准的利妥昔单抗生物类似药,也可以作为原研药的替代选择用于淋巴瘤的治疗方案中。这些明确的建议,是基于充分的科学证据和临床数据,为医生和患者使用生物类似药提供了坚实的信心基础。
生物类似药的到来,最直接也是最重要的影响之一,就是增加了治疗的可及性并减轻了经济负担。通过市场竞争,生物类似药的价格通常低于原研药,这能为患者节省大量的治疗费用,让更多需要这些先进疗法的患者能够用得上、用得起。对于国家医保体系而言,这也有助于节约宝贵的医疗资源,让医保基金能够覆盖更多创新药物和治疗方案,惠及更广泛的人群。在临床上,生物类似药为医生提供了更多的治疗武器。例如,在制定乳腺癌的联合治疗方案时,如果方案中包含曲妥珠单抗,医生可以根据患者的具体情况和药物可及性,选择使用原研药或其经过批准的生物类似药。这种灵活性有助于确保治疗方案的顺利实施。
对于患者和家属来说,面对生物类似药可能会有些疑虑,这是完全可以理解的。关键在于与您的主治医生进行充分、开放的沟通。您可以询问医生:我的治疗方案中,使用的是原研药还是生物类似药?选择这种药物的依据是什么?它的疗效和安全性数据如何?医生会根据您的具体病情、最新的临床证据和药物可及性,为您做出最合适的个体化建议。请相信,一个经过严格监管审批的生物类似药,其临床应用是建立在科学和证据之上的。
生物类似药的出现,是现代医药工业发展和科学进步的体现。它并不是对原研创新的否定,而是在原研药基础上,通过严谨的再开发和验证,让更多患者能以更低的成本获得高质量的生物治疗。它如同原研药可靠的“孪生兄弟”,携手为攻克疾病、守护健康贡献力量。随着更多生物类似药的研发和上市,我们期待看到的是一个更具可及性、更可持续的医疗未来,让科技创新带来的健康福祉能够照亮每一个需要的角落。
生物类似药
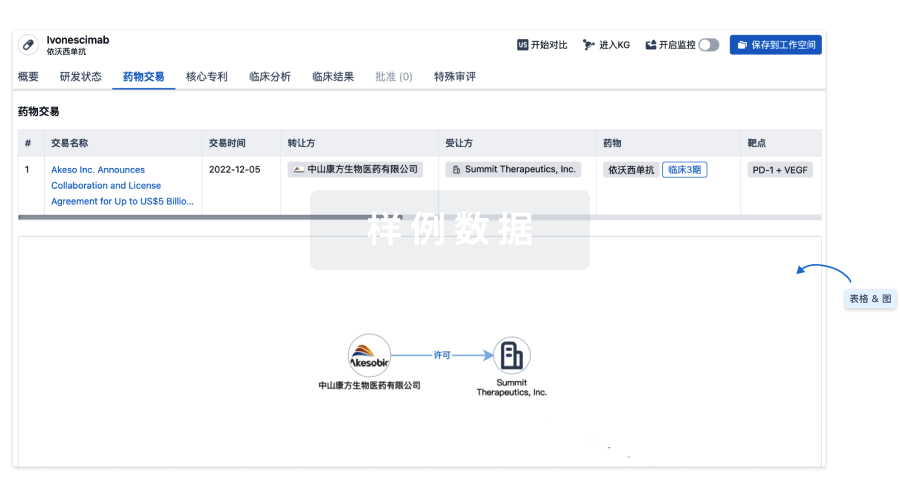
100 项与 利妥昔单抗生物类似药 (喜康生物医药) 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| CD20阳性弥漫性大B细胞淋巴瘤 | 临床3期 | 中国 | 2018-12-26 | |
| 弥漫性大B细胞淋巴瘤 | 临床3期 | 中国 | 2018-11-13 | |
| CD20阳性B细胞淋巴瘤 | 临床1期 | 中国 | 2018-11-16 | |
| 类风湿关节炎 | 临床1期 | 波斯尼亚和黑塞哥维那 | 2017-02-27 | |
| 类风湿关节炎 | 临床1期 | 保加利亚 | 2017-02-27 | |
| 类风湿关节炎 | 临床1期 | 捷克 | 2017-02-27 | |
| 类风湿关节炎 | 临床1期 | 德国 | 2017-02-27 | |
| 类风湿关节炎 | 临床1期 | 匈牙利 | 2017-02-27 | |
| 类风湿关节炎 | 临床1期 | 立陶宛 | 2017-02-27 | |
| 类风湿关节炎 | 临床1期 | 波兰 | 2017-02-27 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
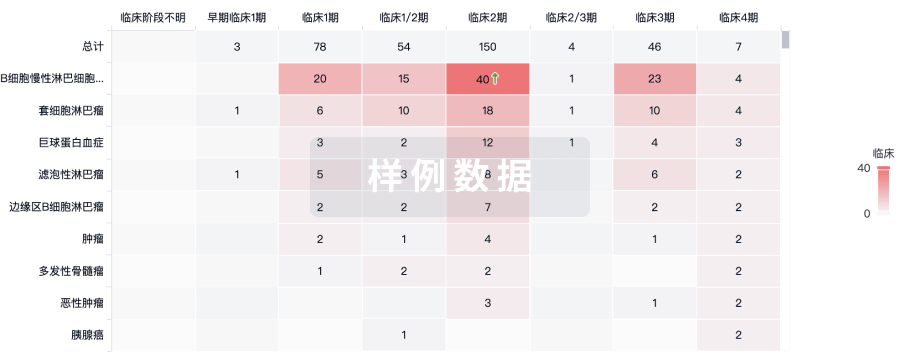
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
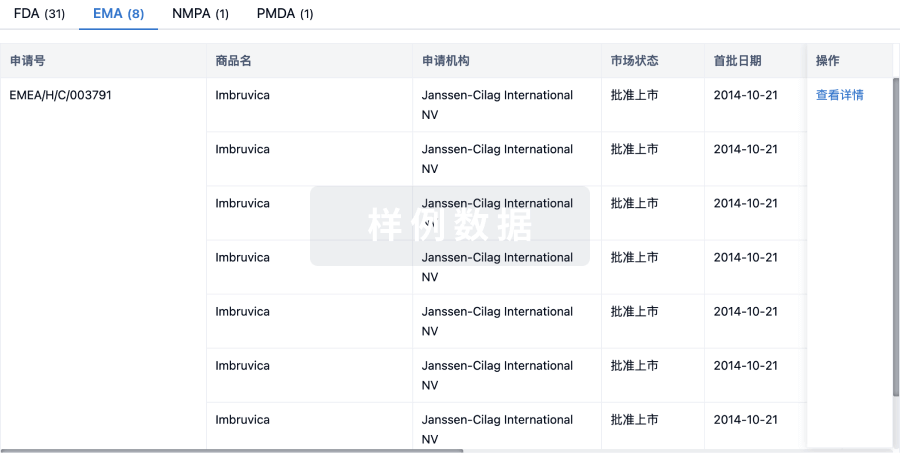
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
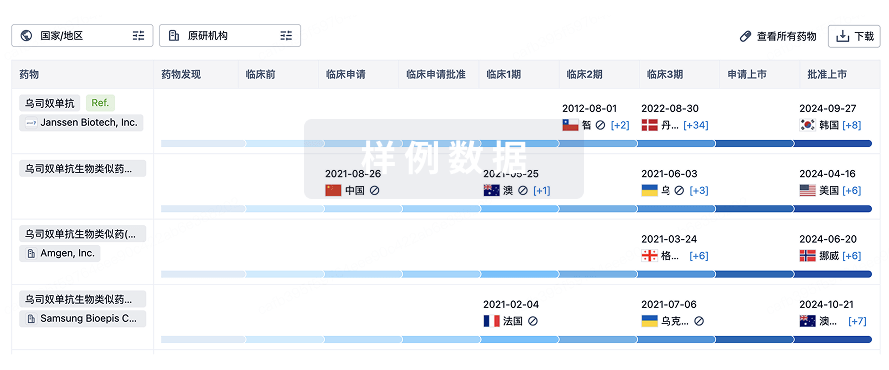
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
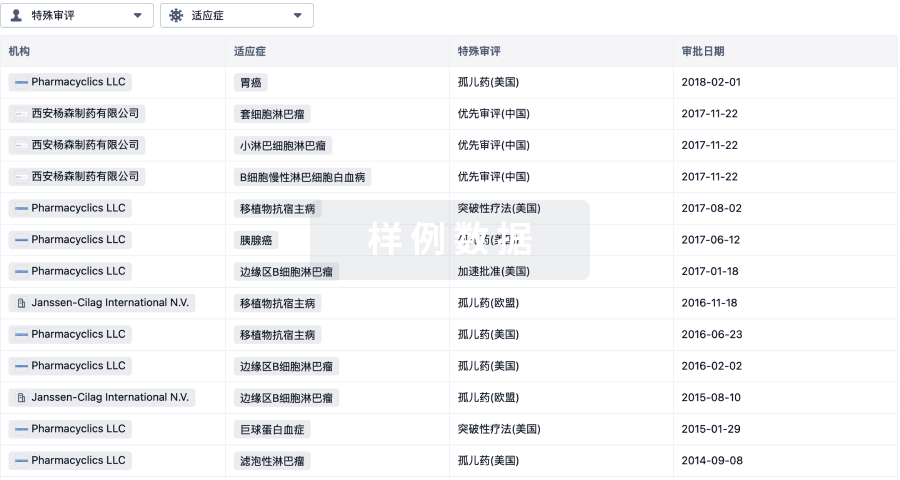
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


