|
|
|
|
|
|
最高研发阶段批准上市 |
|
首次获批日期2022-07-19 |
|
|
|
|
|
非在研适应症- |
最高研发阶段申请上市 |
首次获批国家/地区- |
首次获批日期- |
|
|
|
|
|
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
抗PD-1单克隆抗体HX008联合经肝动脉化疗栓塞术(TACE)一线治疗IV期M1c黑色素瘤肝转移的随机、开放、多中心III期临床研究
比较HX008联合TACE与替莫唑胺联合TACE一线治疗IV期M1c黑色素瘤肝转移的无进展生存期(PFS)、客观缓解率(ORR)、疾病控制率(DCR)、持续缓解时间(DOR)、总生存期(OS),安全性、PK和免疫原性
重组人源化抗PD-1单克隆抗体HX008注射液治疗BCG无应答的高危非肌层浸润膀胱癌的II期临床研究
评价HX008注射液治疗BCG无应答的高危非肌层浸润膀胱癌(HR-NMIBC)的有效性、安全性和耐受性、持续缓解时间 DOR、无进展生存期 PFS、无复发生存期 RFS、总生存期 OS、免疫原性等。
HX008联合伊立替康对比安慰剂联合伊立替康二线治疗晚期胃或胃食管交界处癌的Ⅲ期临床研究
比较HX008联合伊立替康与安慰剂联合伊立替康二线治疗晚期胃或胃食管交界处癌PD-L1阳性(CPS≥1)亚组和总人群的总生存期。
100 项与 鼎康(武汉)生物医药有限公司 相关的临床结果
0 项与 鼎康(武汉)生物医药有限公司 相关的专利(医药)
鼎立潮头,康伴同行!
我们以专业打磨每一份委托,用严谨浇筑品质高地。
奔赴丙午马年,
我们以敏捷响应每一次需求,用实力护航药物创新之路。
新岁启封,鼎康生物继续做生物医药人的“坚实战友”,共破壁垒;
新春大吉,愿每一位追光者心有山海,马到功成,步履不停!
鼎康生物是一家全球领先的CDMO公司,率先引进了全球首个模块化生物制药工厂KUBio™,赋能生物药从细胞株开发到商业化生产的全过程。我们位于瑞士巴塞尔的欧洲创新中心致力于提供快捷的各类抗体蛋白瞬时表达生产服务,位于上海的中国创新中心聚焦高效的细胞株开发和先进的工艺开发,与拥有多国临床试验申请和新药上市成功经验的武汉制造工厂相结合,鼎康生物正在为全球生物医药客户提供一站式的CMC解决方案。在鼎康生物,我们有一个共同的愿景: 致力于通过持续创新,提升前沿生物药物的全球可及性,为人类健康创造长期价值。
前言
为搭建沪港青年职业发展桥梁,助力香港科技大学学子深耕内地职场赛道,由香港科技大学主办,沪港青年会承办,推出了“上海职业探索项目”。该项目为期四天,聚焦制造、科技、金融、投资等领域,通过走进行业标杆企业(蚂蚁集团,美团,腾讯,字节跳动,鼎康生物,冯氏集团,东亚银行,复星蜂巢以及沪港联合控股有限公司)参与交流。
其中被投企业鼎康生物于2026年1月20日接待沪港青年会及港科大代表到访上海创新中心。
2026年1月20日,沪港青年会总干事蔡素霞、助理项目主任林怡伶,以及香港科技大学就业中心助理经理马恒熙一行到访鼎康生物上海创新中心。
鼎康生物上海创新中心总经理、项目管理部和法规事务高级副总裁彭彼得(Peter Pang)博士热情欢迎了远道而来的老师与同学们。他向今天来访嘉宾展示了鼎康生物的创新生态蓝图、产业布局及技术能力。他表示,鼎康生物的CDMO业务为全球包括香港地区在内的新药研发机构提供抗体药物生产支持,省去其自建生产线的投入,同时依托生产技术革新与多元专业团队,全程保障药物合规可控,助力新药顺利落地。
鼎康生物上海创新中心人力资源副总监沈文颖围绕企业深耕生物医药领域的核心优势、市场布局、行业地位进行了简要说明。同时,重点阐释了鼎康生物作为一家创新型生物药CDMO公司对人才梯队建设的重视和专业人才能力发展路径的规划,再就港校合作及港生实习与就业通道与嘉宾展开热烈讨论。
鼎康生物市场总监吕由以“全球药物市场、产业与鼎康生物”为主题,从宏观经济与全球医药消费市场切入,通过中美对比,解析了中国在研发效率上的显著优势,已使其成为全球创新药领域的重要增长极。接下来介绍了抗体药物发展历程以及当下衍生出的众多分子类型和作用机制,并从CMC视角详细介绍了抗体药物从临床前研究到商业化生产的全流程。最后概述了鼎康生物作为国际领先的生物药CDMO在技术能力与全球项目经验方面的独特优势。
嘉宾在鼎康生物相关负责人的陪同下参观上海创新中心实验室,通过直观领略鼎康生物在细胞株开发实验室的高标准实验管理与硬件投入,体会鼎康生物高质量服务的身体力行。
通过本次座谈与实地参观,嘉宾对鼎康生物的技术能力及国际化运营能力有了进一步认识。以此次访问为契机,双方将持续推动沪港两地在校企联合培养、科研成果转化及高端生物制药人才输送等领域的深度协同。
关于鼎康生物
鼎康生物是一家全球领先的CDMO公司,率先引进了全球首个模块化生物制药工厂KUBio™️,赋能生物药从细胞株开发到商业化生产的全过程。我们位于瑞士巴塞尔的欧洲创新中心致力于提供快捷的各类抗体蛋白瞬时表达生产服务,位于上海的中国创新中心聚焦高效的细胞株开发和先进的工艺开发,与拥有多国临床试验申请和新药上市成功经验的武汉制造工厂相结合,鼎康生物正在为全球生物医药客户提供一站式的CMC解决方案。在鼎康生物,我们有一个共同的愿景:致力于通过持续创新,提升前沿生物药物的全球可及性,为人类健康创造长期价值。如需了解更多信息,请访问:www.chimebiologics.com。
关于鼎珮集团
鼎珮成立于 2006 年,专门为大中华区和全球的投资人提供一系列另类投资产品和服务,主要围绕三大另类投资策略,包括私募股权、房地产及结构性融资。我们专注于医疗健康、科技及消费领域,针对家族办公室和机构投资客户的需求,提供覆盖全球私募股权、创投及对冲等领域的投资产品和策略,助力他们实现投资目标。鼎珮在另类投资领域累积了超过 20 年的专业经验,是区内领先的另类投资专家之一。有关鼎珮集团的更多信息,请访问 www.vmsam.com。
拓展阅读
1
鼎珮生态 | 鼎康生物成立欧洲创新中心及鼎康创新联盟
2
鼎珮生态 | 鼎康生物与韩国上市公司MedPacto建立战略合作伙伴关系,加速生物药全球开发与生产
3
鼎珮生态 | 鼎康生物与麦济生物达成PPQ里程碑 加速上市商业化生产进程
4
鼎珮活动 | 聚焦香港生物科技盛会 共话行业新机遇
(本文转载自鼎康生物公众号)
作为工信部首批重点培育中试平台之一,鼎康生物致力于重组蛋白药物技术研发与产业化,近日,中国银行武汉自贸区分行为这家科技型企业授信5000万元流动资金贷款,为其创新发展注入了强劲动力。
鼎康生物是武汉一家生物医药企业,为世界范围内的生物医药客户提供工艺开发以及制备、工艺优化、临床试验用药至商业化阶段药品生产等定制研发生产服务,该企业拥有超过400名员工,其中硕士和博士超过30%。
中国银行武汉自贸区分行采用为科技型企业量身定制的“科技金融授信模型”,为重组蛋白药物中试平台鼎康生物批复了5000万元流动资金贷款授信额度并完成首次提款,这一模式打破了以盈利能力为核心的传统风控逻辑,转而以科研价值、技术成熟度、产业生态培育潜力为评估依据,构建多维度风险分担机制。
随着中试金融服务的深入推进,中国银行武汉自贸区分行正从单一贷款支持向全方位、全周期综合金融服务转变。通过“创新金融产品+全球化服务+全生命周期支持”的组合策略,陪伴科技企业一路成长。
本文转载自长江日报大武汉客户端,如有任何问题请联系原作者
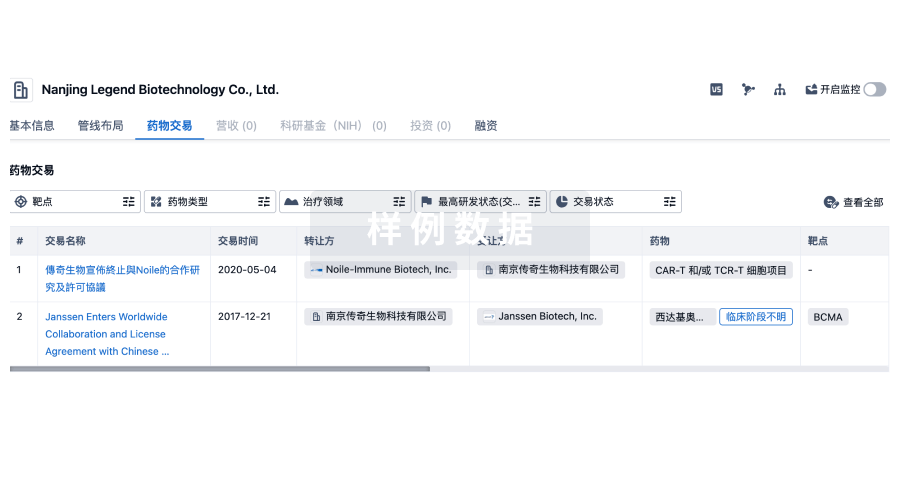
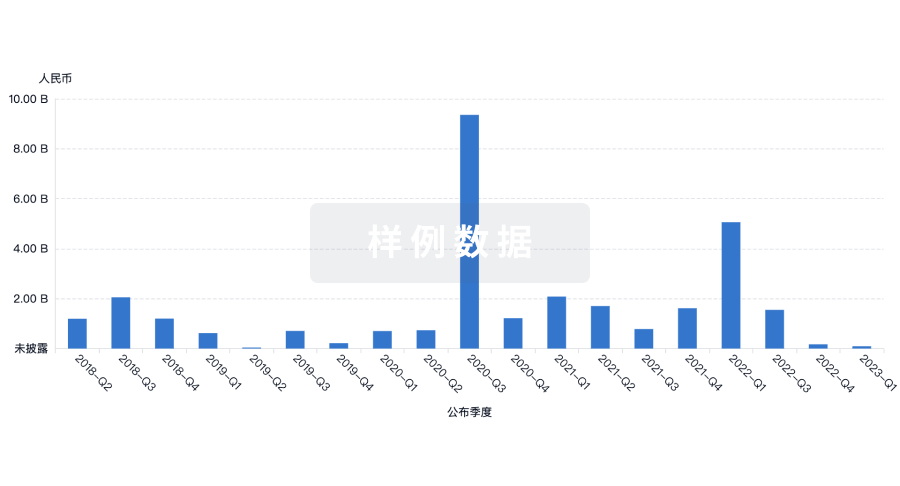
100 项与 鼎康(武汉)生物医药有限公司 相关的药物交易
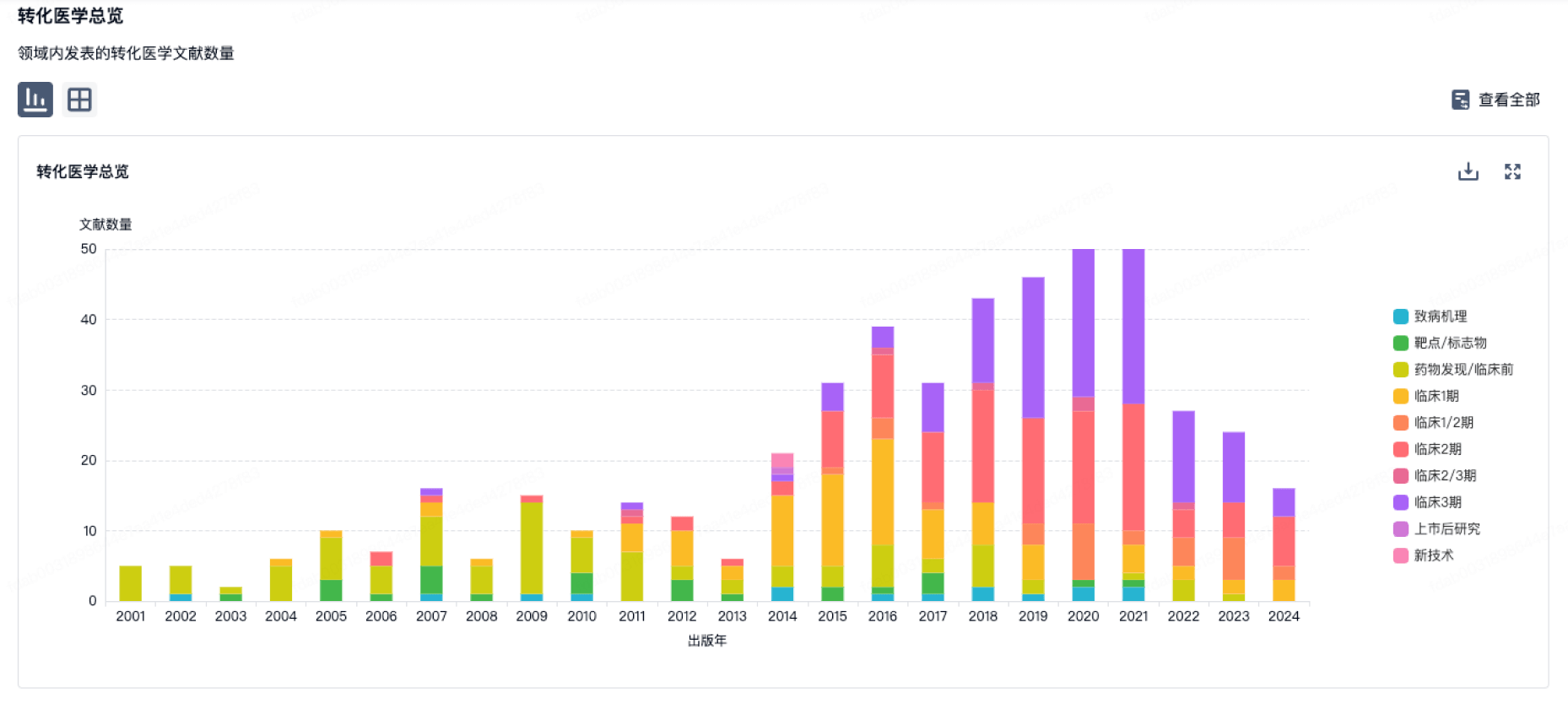
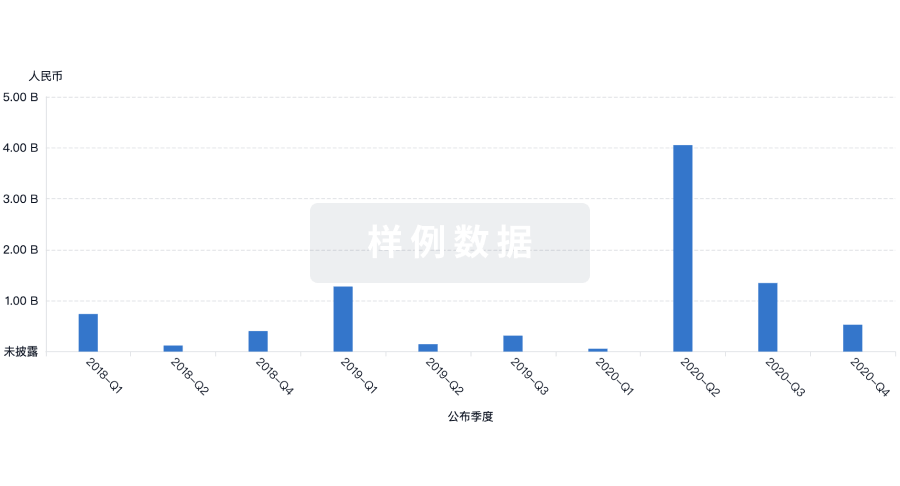
100 项与 鼎康(武汉)生物医药有限公司 相关的转化医学