预约演示
治疗MASH/NASH和2型糖尿病,创新药物达2期试验主要终点
突破性疗法基因疗法临床结果ASH会议
近日,Inventiva公司宣布,小分子泛PPAR激动剂lanifibranor联用SGLT2抑制剂恩格列净(empagliflozin)治疗代谢功能障碍相关性脂肪性肝炎(MASH)/非酒精性脂肪性肝炎(NASH)和控制不佳的2型糖尿病(T2D)患者的2期概念验证试验LEGEND取得了良好的中期分析结果,达到了主要疗效终点。

Preview
来源: 药明康德
此次公布结果的LEGEND试验是一项多中心、随机、安慰剂对照的2期概念验证试验,治疗周期为24周。非肝硬化MASH/NASH的诊断基于既往组织学评估或非侵入性方法(包括影像学检查)的组合。按照方案的计划,63名随机患者中有一半完成24周的治疗期或过早停止治疗后进行中期分析。
中期分析结果显示,与安慰剂组相比,lanifibranor治疗组和lanifibranor联用恩格列净治疗组的糖化血红蛋白水平(HbA1c)水平显著下降,达到了主要疗效终点。
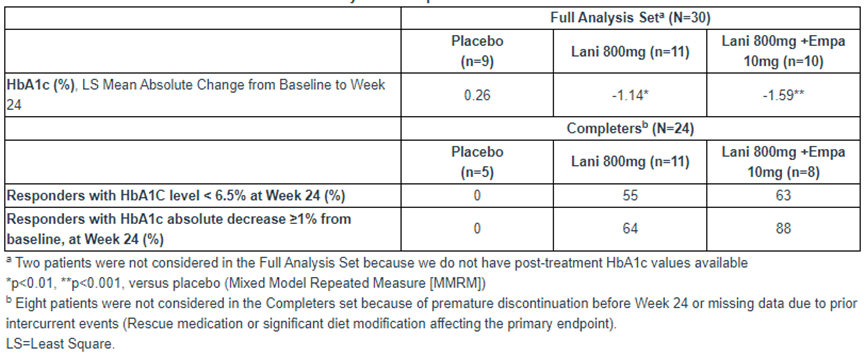
Preview
来源: 药明康德
此外,几种肝损伤指标、葡萄糖和脂质代谢指标以及肝脂肪变性指标也具有统计学意义的改善。
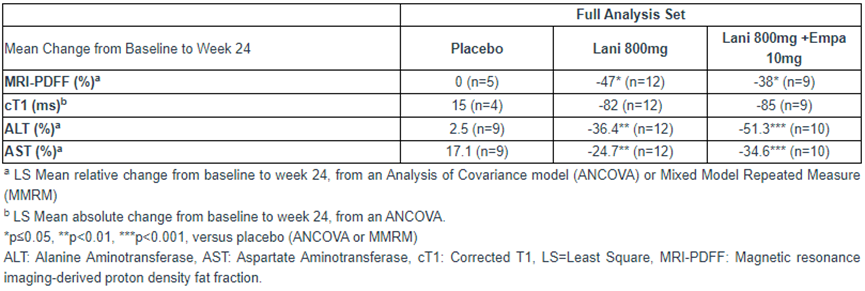
Preview
来源: 药明康德
在为期24周的研究中,接受lanifibranor联合恩格列净治疗的患者体重保持稳定,可能解决了在一些接受lanifibranor治疗的患者中观察到的体重增加和代谢方面的问题。此外,lanifibranor单药和lanifibranor联用恩格列净可显著降低患者腹部内脏脂肪(VAT)与皮下脂肪(SAT)的比率,这反映了促炎症内脏脂肪向代谢健康脂肪组织的转变。
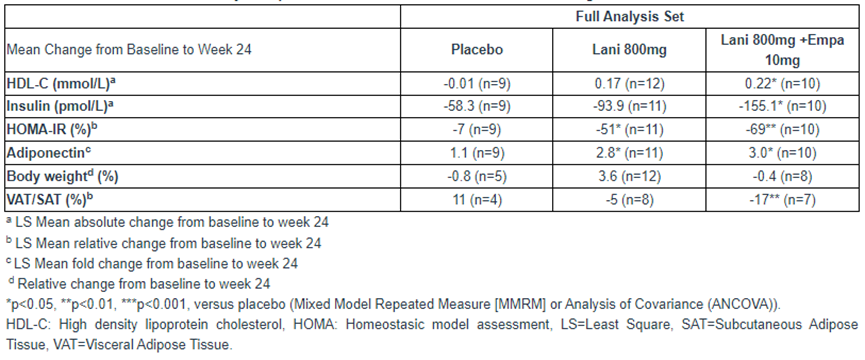
Preview
来源: 药明康德
安全性方面,患者接受lanifibranor 800 mg每天一次单药或联用恩格列净治疗24周的耐受性良好,无安全问题报告。
参考资料:[1] Inventiva announces positive results from the Phase II, LEGEND, Proof-of-Concept study combining lanifibranor with empagliflozin in patients with MASH/NASH and T2D. Retrieved March 19, 2024, from https://www.globenewswire.com/news-release/2024/03/18/2848135/0/en/Inventiva-announces-positive-results-from-the-Phase-II-LEGEND-Proof-of-Concept-study-combining-lanifibranor-with-empagliflozin-in-patients-with-MASH-NASH-and-T2D.html
内容来源于网络,如有侵权,请联系删除。
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。



