预约演示
超三千万患者获益!非奈利酮斩获在华新适应症
临床3期上市批准申请上市
慢性肾病是糖尿病患者最常见的并发症,也是心血管疾病的独立危险因素。大约40%的2型糖尿病患者会发展成为慢性肾病。即使按照指导意见进行治疗,与2型糖尿病相关的慢性肾脏病患者也处于慢性肾病进展和发生心血管事件的高风险中。据英国著名医学期刊柳叶刀统计,慢性肾病大约影响全球超过1.9亿2型糖尿病患者。中国慢性肾病患者近1.2亿,由2型糖尿病所致的慢性肾病患者约3108万。而与2型糖尿病相关的慢性肾脏病是我国终末期肾脏病的重要原因之一,患者需要透析或者肾移植才能存活。与2型糖尿病相关的慢性肾脏病患者的心血管相关死亡风险是单独患有2型糖尿病患者的3倍。
非奈利酮是一种非甾体选择性盐皮质激素受体拮抗剂,用于与2型糖尿病相关的慢性肾脏病成人患者(伴白蛋白尿),以降低肾小球滤过率估计值(eGFR)持续下降、终末期肾病、心血管死亡和因心衰住院的风险。
CPM新药研发检测数据库显示,基于FIDELIO-DKD III期研究的正向结果,非奈利酮于2021年7月获得美国FDA的上市批准,2022年2月在欧盟获批,2022年6月获得中国国家药品监督管理局(NMPA)的批准。2022年9月,拜耳公司宣布美国FDA批准非奈利酮更新说明书,纳入FIGARO-DKD III期研究中的心血管获益结果。
2023年2月,根据FIGARO-DKD III期研究结果,非奈利酮获得欧盟委员会批准扩展适应症,纳入与2型糖尿病相关的慢性肾脏病早期阶段患者群体。基于FIDELIO-DKD和FIGARO-DKD这两项关键性III期研究的正向结果,非奈利酮于2022年6月获得了日本的上市批准。其他多个国家和地区的卫生主管部门已经批准或正在审评该药的上市申请。
图1:美国上市批准非奈利酮的相关信息

Preview
来源: 医药地理
图2:欧盟上市批准非奈利酮的相关信息
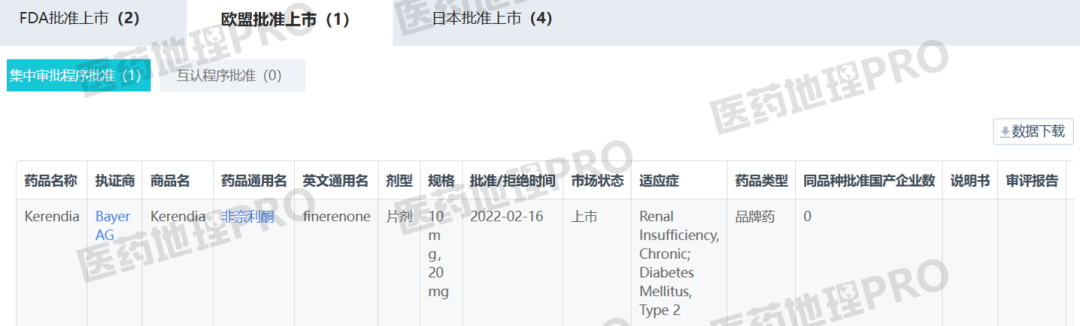
Preview
来源: 医药地理
图3:中国上市批准非奈利酮的相关信息
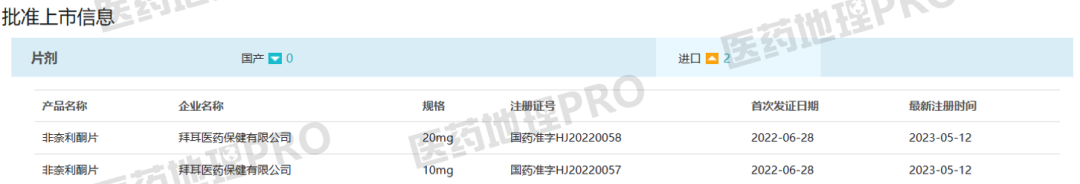
Preview
来源: 医药地理
图4:日本上市批准非奈利酮的相关信息
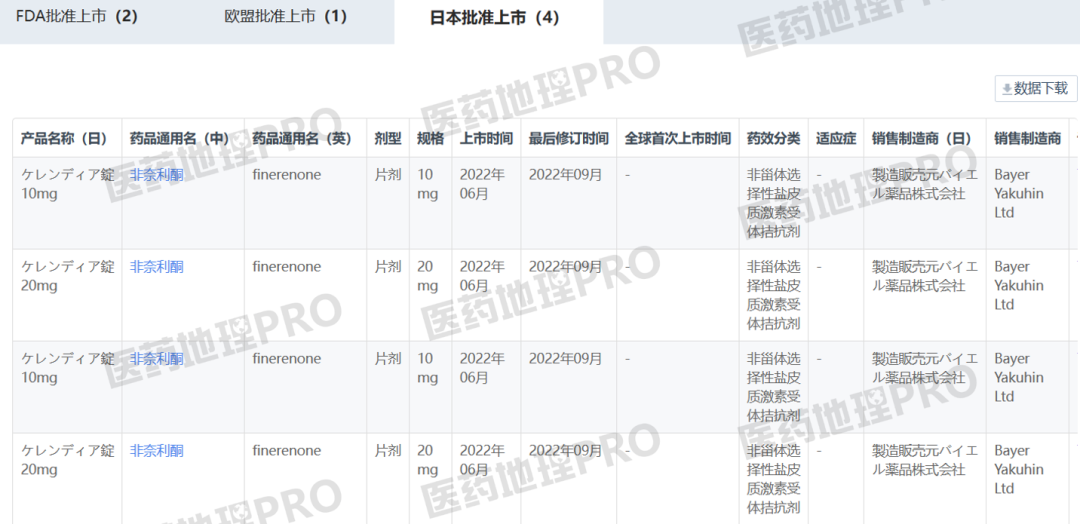
Preview
来源: 医药地理
非奈利酮的 III 期研究计划FINEOVATE目前包括5个具体项目,分别是FIDELIO-DKD、FIGARO-DKD、FINEARTS-HF、FIND-CKD和FIONA,还包括CONFIDENCE II期研究。非奈利酮用于治疗与2型糖尿病相关的慢性肾脏病患者的III期临床项目纳入了全球13,000多名患者,该项目包括两个研究FIDELIO-DKD和FIGARO-DKD,旨在评价在接受标准治疗基础上,非奈利酮与安慰剂相比在肾脏和心血管方面的获益。
非奈利酮适用人群扩展到早期阶段是基于丰富而坚实的临床研究结果。由于该药延缓2型糖尿病相关的慢性肾脏病炎症和纤维化的进展,而这是该疾病进展的关键因素,进而提供了一条独特途径降低肾脏和心血管疾病发生风险。非奈利酮或将提高患者的生活质量。
内容来源于网络,如有侵权,请联系删除。
机构
靶点
-药物
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。



