预约演示
更新于:2026-05-23

Zhejiang Pukang Biotechnology Co. Ltd.
更新于:2026-05-23
概览
标签
感染
消化系统疾病
肿瘤
预防性疫苗
灭活疫苗
重组载体疫苗
关联
5
项与 浙江普康生物技术股份有限公司 相关的药物靶点- |
作用机制 免疫刺激剂 |
在研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段批准上市 |
首次获批国家/地区 菲律宾 |
首次获批日期2018-04-30 |
靶点- |
作用机制 免疫刺激剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2000-01-01 |
靶点- |
作用机制- |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
4
项与 浙江普康生物技术股份有限公司 相关的临床试验CTR20252733
评价甲型肝炎灭活疫苗(人二倍体细胞)接种于健康人群后的安全性和免疫原性的随机、盲法、阳性疫苗对照的Ⅰ期临床试验
主要目的:评价甲型肝炎灭活疫苗(人二倍体细胞)的安全性和耐受性。
次要目的:初步评价甲型肝炎灭活疫苗(人二倍体细胞)的免疫原性。
开始日期2025-07-19 |
申办/合作机构 |
CTR20242601
评价冻干人用狂犬病疫苗(人二倍体细胞)以不同免疫程序接种于健康人群后的免疫原性和安全性的随机、盲法、阳性疫苗对照的Ⅲ期临床试验
主要目的:
评价试验疫苗(冻干人用狂犬病疫苗(人二倍体细胞))接种于10周岁及以上健康人群后的免疫原性非劣效于阳性对照疫苗。
次要目的:
1) 评价冻干人用狂犬病疫苗(人二倍体细胞)在10周岁及以上健康人群中的安全性。
2) 评价冻干人用狂犬病疫苗(人二倍体细胞)在10周岁及以上健康人群中的免疫持久性。
开始日期2024-07-26 |
申办/合作机构 |
CTR20240310
评价冻干人用狂犬病疫苗(人二倍体细胞)以不同免疫程序接种于健康人群后的安全性和免疫原性的随机、盲法、阳性疫苗对照的Ⅰ期临床试验
主要目的:评价冻干人用狂犬病疫苗(人二倍体细胞)的安全性和耐受性;次要目的:初步评价冻干人用狂犬病疫苗(人二倍体细胞)的免疫原性。
开始日期2024-02-25 |
申办/合作机构 |
100 项与 浙江普康生物技术股份有限公司 相关的临床结果
登录后查看更多信息
0 项与 浙江普康生物技术股份有限公司 相关的专利(医药)
登录后查看更多信息
1
项与 浙江普康生物技术股份有限公司 相关的文献(医药)2020-09-01·Virus research3区 · 医学
Muscle destruction caused by coxsackievirus A10 in gerbils: Construction of a novel animal model for antiviral evaluation
3区 · 医学
Article
作者: Yao, Pingping ; Chen, Chen ; Yang, Zhangnv ; Sun, Yisheng ; Xu, Fang ; Zhu, Shuirong ; Zhu, HanPing ; Lu, Hangjing ; Mao, Zian ; Miao, Ziping ; Gao, Meng ; Xia, Yong ; Ge, Qiong
The morbidity and mortality of coxsackievirus A10 (CVA10)-associated hand, foot, and mouth disease (HFMD) have been increasing in recent years, while few studies on the vaccine and animal model of CVA10 have been reported. Here, we first established a CVA10-infected gerbil model and employed it to evaluate the immunoprotective effect of an inactivated CVA10 vaccine. The results showed that gerbils up to the age of 14 days were fully susceptible to CVA10, and all died within five days post-infection by intraperitoneal inoculation. Lethargy, wasting, hind-limb paralysis, and even death could be observed in the CVA10-infected gerbils. Pathological examination suggested that CVA10 has a strong tropism toward muscle tissue, and muscle bundle fracture and muscular fibers necrosis were observed in the limb muscles. Additionally, active immunization results showed that gerbils immunized with the inactivated CVA10 vaccine were 100 % protected from lethal CVA10 challenge. The antisera from vaccinated gerbils also showed high neutralizing titers against CVA10. Based on these results, the CVA10-infected gerbil model was a suitable tool for analyzing the pathogenesis of CVA10 and assessing the protective efficacy of CVA10 candidate vaccines.
36
项与 浙江普康生物技术股份有限公司 相关的新闻(医药)2026-05-19
·药事纵横
2026年5月22日,“synbio深波”携手“可克达拉经济技术开发区”,组织“新疆生物发酵考察团”并同期举办【汇聚产业力量,共创生物未来】——可克达拉首届生物产业高质量发展交流会。特邀生物制造企业抢先入驻新疆投资展业、占领先机,深化政企合作,享受新疆生物制造产业第一手政策福利,共享可克达拉蓬勃发展新机遇。
可克达拉经济技术开发区立足新疆兵团第四师独特资源禀赋,以玉米精深加工 — 氨基酸 — 生物基材料全产业链为核心,依托兵团最大粮油生产基地优势、完善产业集群、稳定能源供给与高效政策服务,构建 “资源有支撑、产业有基础、创新有动能、服务有保障” 的生物制造产业生态,成为全国生物制造企业布局优选地。
报名通道(审核制,仅限决策层)
活动主题:汇聚产业力量,共创生物未来
会议名称:可克达拉首届生物产业高质量发展交流会
会议时间:2026年5月22日,09:30-20:30
会议地点:新疆·可克达拉宾馆
联合主办:可克达拉经济技术开发区、synbio深波
上午
AM
◇ 城西生物医药产业园参观
◇ 安琪酵母工厂参观
◇ 金海生物工厂参观
◇ 天熙生物工厂参观
◇ 沂利泓工厂参观
下午
PM
◇ 签约仪式
◇ 报告分享:以绿色能源和资源发展微生物蛋白产业
李德茂 中国科学院天津工业生物技术研究所研究员
◇ 报告分享:面向高细胞密度培养的生物反应器创新开发与应用实践
郑志永 江南大学教授
◇ 企业供需对接交流会
◇ 圆桌访谈:
主持人:药融圈创始人 王波
专家方阵:中科院研究员 顾阳、石规院副处长 闫泽、江南大学教授 张显
企业方阵:金海生物、普康生物、天熙生物、沂利泓
◇ 领导发言
晚上
PM
◇ 交流晚宴
新疆生物发酵考察成团名单(部分)
黑龙江新和成生物科技有限公司
弈柯莱生物科技(集团)股份有限公司
鲁南制药集团股份有限公司
成都倍特药业股份有限公司
元一(天津)生物科技有限公司
湖南利尔生物科技有限公司
湖南伊润生物科技股份有限公司
云南沃森生物技术股份有限公司
东莞市宇诺生物科技有限公司
福建砺善和光工程技术研究有限公司
山东奔月生物科技股份有限公司
合生汇(乌苏)生物技术有限公司
常德云港生物科技股份有限公司
天津辛巴达科技发展有限公司
海南质合生物科技有限公司
徐州恒世营养科技有限公司
上海燕鸿科技有限公司
深圳市美凯特科技有限公司
苏州上海大学创新中心
宿迁润川生物科技有限公司
巢湖学院
甘肃省科学院生物研究所
大昌生物医药(深圳)有限公司
长春拓华医药有限公司
湖南诺克素生物技术有限公司
江太生物科技(北京)有限公司
益昌纳米新材料科技(广东)有限公司
新乡市创新生物科技有限公司
苏州蒂法生物有限公司
沈阳合盛生物科技有限公司
平顶山学院
山西实美功能食品有限公司
新疆当地可链接企业名单(部分)
伊犁川宁生物技术股份有限公司
可克达拉安琪酵母有限公司
新疆伊力特实业股份有限公司
可克达拉金海生物科技有限公司
新疆天熙生物有限责任公司
新疆回盛生物科技有限公司
新疆沂利泓生物新材料科技有限公司
新疆苏源生物工程有限公司
新疆瑞诺生物科技有限公司
新疆可克达拉新壹天环保设备有限公司
新疆域膳坊食品有限公司
新疆军农乳业有限公司
新疆可克达拉河谷精酿啤酒生产有限责任公司
新疆婉桐葡萄酒业有限公司
生命粮(可克达拉)全谷物产业发展有限责任公司
常备佳(新疆)应急产业有限公司
新疆福泰宏远装配科技股份有限公司
河南鑫洋集团股份有限公司
新疆普康生物科技有限公司
中溶新能源(可克达拉)有限公司
伊犁新地新材料有限公司
可克达拉银皓化工有限责任公司
(新疆本地企业出席情况,以现场实际到场为准)
报名通道(审核制,仅限决策层)
参会联系人
可克达拉经开区立足自身禀赋,构建起独具优势的生物制造产业生态,形成了“资源有支撑、产业有基础、创新有动能、服务有保障”的发展格局,成为企业布局生物制造产业的优选之地。
优势一:资源禀赋得天独厚,筑牢产业发展根基
01
生物制造产业的发展,离不开优质原材料的支撑。可克达拉经开区所在的第四师可克达拉市,是兵团最大的粮油生产基地,连年获评“国家产粮大县”和“国家级玉米制种大县”,玉米种植规模、产量均占兵团较大比重,为生物制造产业提供了充足且优质的原料保障。
依托这份独特的资源优势,经开区重点打造“玉米精深加工-氨基酸-生物基材料”完整产业链,实现从玉米到淀粉、淀粉糖,再到发酵类产品、生物基材料的全产业链深度开发,让“一粒玉米”发挥最大价值。
优势二:产业集群初具规模,构建产业发展完整生态
02
经过多年培育,可克达拉经开区已形成较为完善的生物制造产业集群,目前拥有多家生物制造规上企业,涵盖氨基酸生产、生物基材料研发、玉米深加工等多个领域,产业集聚效应凸显。
在龙头企业引领下,经开区实现了“引进一个龙头、带动一串配套、形成一片产业”的链式发展。园区多家生物制造企业带动上下游产业协同发展,进一步完善产业链条,让行业内看到了合作共赢的广阔空间。
优势三:能源加持硬核配套,夯实产业发展动力基石
03
可克达拉经开区依托新疆丰富的煤炭、电力资源,深度整合兵团第四师完善的能源保障体系,构建起低成本、高效率、高稳定的能源供给网络,为辖区生物产业企业高质量发展筑牢能源根基。依托师市煤炭总产能490万吨/年的坚实基础,搭配中源电力集团布局的新型电力系统及共享储能项目,园区实现电力稳定供给,同时创新推出“跨区域绿电+产业一体化发展”新模式,高耗能产业绿电使用配比保持在20%以上,既保障能源稳定,又契合绿色发展趋势。
优势四:政策服务优质高效,厚植产业发展沃土
04
良好的营商环境,是企业落地生根、发展壮大的关键。可克达拉经开区围绕生物制造产业发展,出台一系列针对性扶持政策,涵盖招商引资、项目建设、技术创新、人才引育等多个方面,为企业提供全周期、全方位的优质服务。
经开区实施产业发展“链长制”“链主制”,绘制生物制造产业图谱,精准开展招优引强;针对重点项目,提供“贴心式”服务,全程跟踪对接,确保项目早建成、早投产、早见效;同时,依托新疆自贸试验区建设机遇,搭建对外开放平台,降低企业运营成本,为企业发展提供有力保障。
2026-05-07
📝 研报客AI助手-AI报告总结
杭州市生物药品制造行业中小企业数字化转型总结一、行业概况与发展趋势核心内容
杭州市生物药品制造行业以生物技术为核心,涵盖抗体药物、疫苗、基因治疗药物等产品,产业链复杂且协同要求高。中小企业在该行业中扮演重要角色,但面临资源瓶颈、成本压力及合规风险等挑战。主要观点
行业机遇:人口老龄化、慢性病增长及技术创新推动市场需求扩张。
政策支持:政府通过税收优惠、研发补贴、审批提速等措施优化中小企业发展环境。
行业趋势:中小企业正向专业化、创新化与智能化方向转型,聚焦细分领域,推动技术突破和流程优化。
关键信息
杭州作为试点城市,具备良好的创新生态与政策优势。
产业集群式发展,推动区域协同发展与资源整合。
二、中小企业数字化转型价值核心内容
数字化转型为生物药品制造行业中小企业提供技术赋能,助力其突破资源瓶颈,实现从成本驱动向创新价值驱动的转型。主要观点
研发效率提升:通过数据整合与AI辅助,缩短研发周期,提高成功率。
生产质量控制:实现全流程数字化管控,提升批次一致性与合规性。
供应链优化:通过系统集成与智能预测,提升库存管理与采购效率。
安全管理升级:构建智能预警与闭环管理体系,降低事故率与合规风险。
三、数字化转型应用场景与案例1. 产品生命周期数字化痛点需求
研发数据分散、格式不统一、合规成本高。
研发流程自动化低、跨部门协作效率差。
应用场景
1. 一级:使用化学设计工具辅助结构设计。
2. 二级:通过ELN系统实现研发流程规范化。
3. 三级:构建实验室信息管理一体化平台,实现跨部门协同。
4. 四级:引入AI技术,实现智能化研发管理。典型案例:浙江霍德生物
背景:研发数据分散,流程割裂。
举措:构建研发一体化平台,整合项目、实验、工艺等系统。
成效:研发数据检索效率提升80%,跨部门协作耗时减少60%,先导化合物确定周期缩短。
2. 生产执行数字化1. 计划排程痛点需求
人工排产效率低、紧急订单响应慢、数据联动不足、合规与灵活性矛盾。
应用场景
1. 一级:使用电子表格进行基础排程。
2. 二级:基于ERP系统实现生产计划管理。
3. 三级:应用APS系统进行精准化排产。
4. 四级:集成AI与预测性分析,实现智能排程与动态优化。典型案例:浙江亚林生物
背景:传统排程依赖Excel,响应慢、效率低。
举措:部署生产计划管理模块,集成ERP与MES数据。
成效:排产效率提升70%,物料损耗率降至5%,紧急订单响应时间缩短。
2. 生产管控痛点需求
生产数据管理低效、质量追溯困难、过程控制粗放、时间成本高。
应用场景
1. 一级:使用电子表格记录生产信息。
2. 二级:部署MES系统实现生产过程数字化管理。
3. 三级:建立生产数字化管控平台,实现多参数联动优化。
4. 四级:运用AI与数字孪生技术实现智能化生产管控。典型案例:浙江普康生物
背景:生产过程数字化水平低,质量追溯困难。
举措:引入MES与SCADA系统,实现全流程数据采集与信息化监控。
成效:生产数据准确率提升至99%,批次统计与放行时间节约70%,偏差处理等待时间减少。
3. 质量管理痛点需求
人工记录效率低、合规风险高、质量响应滞后、数据孤岛、分析能力弱。
应用场景
1. 一级:使用电子表格管理质量数据。
2. 二级:部署QMS系统实现质量流程电子化。
3. 三级:建立闭环质量保证体系,实现在线监测与智能预警。
4. 四级:融合AI技术,实现质量智能管控与风险预测。典型案例:杭州诺泰诺和
背景:面临FDA审计合规压力。
举措:引入eQMS平台,实现质量流程标准化与自动化。
成效:质量数据完整性达100%,QA人效提升20%,跨部门协作效率提升30%。
4. 安全生产痛点需求
高危操作环境复杂、设备维护滞后、合规压力大、数据孤岛问题突出。
应用场景
1. 一级:使用电子表格进行基础安全管理。
2. 二级:部署在线监测系统,实现安全数据电子化。
3. 三级:构建安全生产管理平台,实现联动监控与应急响应。
4. 四级:引入AI与数字孪生技术,实现智能预警与闭环管理。典型案例:某生物药企
背景:人工操作易引发事故,合规数据缺失。
举措:部署安全生产物联网平台,集成传感器与监控系统。
成效:设备故障率下降65%,灭菌柜稳定性提升至99.8%,GMP审计通过率提升至100%。
3. 供应链数字化1. 仓储物流痛点需求
仓储效率低、库存数据分散、合规风险高。
应用场景
1. 一级:使用电子表格进行基础仓储管理。
2. 二级:部署WMS系统实现仓储规范化。
3. 三级:构建集成化平台,实现库存与生产、采购联动。
4. 四级:引入AI算法进行库存预测与智能调度。典型案例:信达生物制药(杭州)
背景:仓储管理依赖人工与纸质单据,效率低。
举措:深度集成MES系统,实现线上流转与实时数据同步。
成效:仓储空间利用率提升20%,出入库效率提升30%,人工错误率归零。
四、总结核心内容
杭州市生物药品制造行业中小企业正通过数字化转型应对发展中的痛点,提升研发、生产、质量与供应链管理效率,实现从传统模式向智能化、协同化、合规化的转变。主要观点
数字化转型是中小企业突破资源瓶颈、实现高质量发展的关键路径。
技术赋能贯穿研发、生产、质量、安全与供应链各环节,形成闭环管理。
AI、MES、WMS、QMS等系统在转型中发挥重要作用,提升效率与合规性。
关键信息
通过系统集成与数据共享,实现跨部门、跨流程的协同管理。
数字化转型显著提升企业运营效率、质量控制与合规水平。
实践案例表明,数字化手段可有效降低运营成本、缩短研发周期、减少安全事故。
免费获取报告源文件,请点下方图片
📚 文章推荐
📌 哈尔滨市植物油加工行业中小企业数字化转型实践样本_28页_1mb.pdf
📌 _特斯拉人形机器人技术突破解读_报告_16页_836kb.pdf
📌 中国创投市场发展指数报告_22页_918kb.pdf
📌 科技人才创业法律风险方案指引_78页_4mb.pdf
📌 _亿欧智库_2025中国AIEV产业年度回顾及发展总结报告_40页_19mb.pdf
📌 成都市智能建造人工智能_AI_应用指南_2025_版_71页_1mb.pdf
📌 20260505-东证期货-国债期货热点报告_期债市场对外开放_背景_影响及机构策略_6页_2mb....
📌 从规模扩张到生态升级_中国ETF市场的趋势变革_28页_669kb.pdf
📌 20260505-华鑫证券-电力设备行业周报_算电协同加速落地_多因素共振持续强化国产算力产业趋势_...
📌 中国内地及香港IPO市场2025年回顾与2026年前景展望_62页_9mb.pdf
📌 20260505-国信证券-26FYQ3财报点评_AI年化营收370亿美元_计划2年内整体算力翻倍_...
📌 20260505-国信证券-26Q1财报点评_广告持续高速增长_上调Capex_AI_ROI引发市场...
📌 20260505-国信证券-中微公司-688012.SH-高端刻蚀设备全面导入_先进膜薄运付量快速增...
📌 20260505-国信证券-亚太科技-002540.SZ-铝价波动影响利润_持续拓展零部件及热管理业...
📌 20260505-国信证券-公用环保202604第4期_关于更高水平更高质量做好节能降碳工作的意见_...
📌 20260505-国信证券-学大教育-000526.SZ-2026Q1释放业绩弹性_全年业务拓展展望...
📌 2025年前三季度出版行业运行分析_8页_789kb.pdf
📌 武汉市汽车动力电池行业中小企业数字化转型实践样本_21页_1mb.pdf
📌 厦门市电子器件制造行业中小企业数字化转型实践样本_38页_2mb.pdf
📌 从传统模式到精准医疗_中美六大癌症治疗标准十年演进图谱_196页_12mb.pdf
研报客 - 全球行业报告 图表数据聚合AI平台
5000多家机构,五百万+报告 覆盖全行业深度研究
一站式行业研究报告平台,汇聚全球百强智库,百万中英文报告
✨ 核心功能
📊 海量报告:覆盖全行业,AI搜索+全文检索
🤖 AI翻译:多语言互译,保留原排版
💬 AI对话:智能研报助手,深度解读文档
🔔 实时推送:订阅关键词,更新主动通知
📱 全平台:网页、APP、小程序数据同步
🤖 AI能力
🔍 智能检索:快速理解问题意图,提供精准信息
🌐 多源整合:综合多个可靠来源,给出全面答案
💡 语境理解:不只是字面翻译,更能理解上下文和文化差异
🎯 专业领域:适应技术、文学、商务等不同领域的翻译需求
🧠 自然交流:理解复杂对话上下文,保持连贯性
📚 研报专家:深度理解文档,进行专业回复
⚡ 实时性:能够获取最新信息,主动推送更新
🎯 适用场景
💼 投资分析:券商研报、市场分析、投资策略
📈 市场调研:行业分析、市场趋势、竞争格局
🏭 行业研究:深度行业报告、产业链分析
🚀 趋势预测:未来趋势、技术发展、政策解读
🌐 访问方式
💻 网页版:pc.yanbaoke.cn
📱 APP下载:各大手机商店搜索「研报客」
🖥️ 软件版:pc.yanbaoke.cn/pc2.html
📲 小程序:微信搜索「研报客」
💡 PDF/DOC/PPT互转 | 文字版一键复制 | 支持下载分享
网页、APP、小程序多端同步,随时随地阅读研报
内容由ai生成,仅供参考
2026-03-19
·葯融圈
生物医药产业进入创新迭代的黄金周期,抗体药物与抗体药物偶联物(ADC)作为生物制药领域的核心增长极,正凭借独特优势重塑全球治疗格局、引领产业创新方向。当下,抗体与ADC药物行业正迎来爆发式增长与高质量转型的双重机遇。而ADC药物早期开发与上下游工艺的迭代升级,更成为推动产业从研发向产业化落地的核心支撑。机遇背后,行业发展仍面临多重共性瓶颈与挑战,亟待全产业链协同破解。为此药融圈联合多业界专家将于3月19-20日在成都举办“抗体药物与ADC药物创新开发”与“ADC药物早期开发与上下游工艺开发”两个论坛,凝聚行业共识、整合优质资源、破解发展难题。
会议日程以现场为准,更多嘉宾行程正在确认中……
13:30-13:55
多肽偶联药物新进展
徐寒梅 安吉生物,创始人
13:55-14:20
一类靶向多肽放射性核药的筛选开发与早期临床研究
高剑 禾泰健宇,董事长兼总经理
14:20-14:45
口服环肽创新药
原晨光 深圳市祥根生物,联合创始人/首席科学家
14:45-15:10
有毒动物镇痛药物开发
容明强 佩德生物,董事长
15:10-15:35
CMC研究与规模化生产
刘标 四川多瑞药业,总经理
13:30-14:00
免疫ADC药物的设计与开发
刘煜 上海医药集团中央研究院 ADC研发副总监
14:00-14:30
双抗和复杂重组蛋白CMC开发难点和解决策略
韦庆焜 汉腾生物,VP
14:30-15:00
ADC创新药研发进展(拟)
杨金亮 四川大学华西医院生物治疗全国重点实验室教授
15:00-15:30
多药聚乙二醇化(MD-PEG)单分子纳米靶向药物
李高全 阿普格雷生物,创始人、董事长
15:30-16:00
眼科疾病下一代治疗方案的差异化开发策略
杨玉婷 成都景泽研究院,项目规划总监
展商名录
点击企业名称获取详细介绍
A01展位:海纳医药
A02展位:兰安医疗
A03展位:健腾生物
A03A:恒敬生物
A09:微谱
A13展位:爱思唯尔
A13A展位:汇宇制药
A20展位:安谱实验
A21展位:药检院
A22展位:中科普瑞昇
A23展位:格林泰科
A23A展位:Ideals
A25展位:立沃生物
A26展位:美迪西
A27展位:华西海圻
A28展位:澳斯康生物
A29展位:普康生物
A30展位:微纯科技
A31展位:联合德艺
A32展位:北京全式金
A37展位:诺和晟泰
A38展位:NanoTemper
A39展位:问度色谱
A40展位:创志科技
商务合作
抢占 2026 年度会议黄金商机!我们已全面开放多元化合作通路,覆盖项目对接、人脉拓展、商务洽谈、媒体宣推、线下展位等核心板块,为您打造一站式品牌推广与资源对接的高端交流平台!
商务合作联系:
王经理 13588474548
刘经理 15558005219
高经理 15048470855
任经理 16657107242
杨经理 18047123661
李经理 17280794917
抗体药物偶联物申请上市
100 项与 浙江普康生物技术股份有限公司 相关的药物交易
登录后查看更多信息
100 项与 浙江普康生物技术股份有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月09日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床申请批准
1
2
临床1期
临床3期
1
2
批准上市
其他
1
登录后查看更多信息
当前项目
登录后查看更多信息
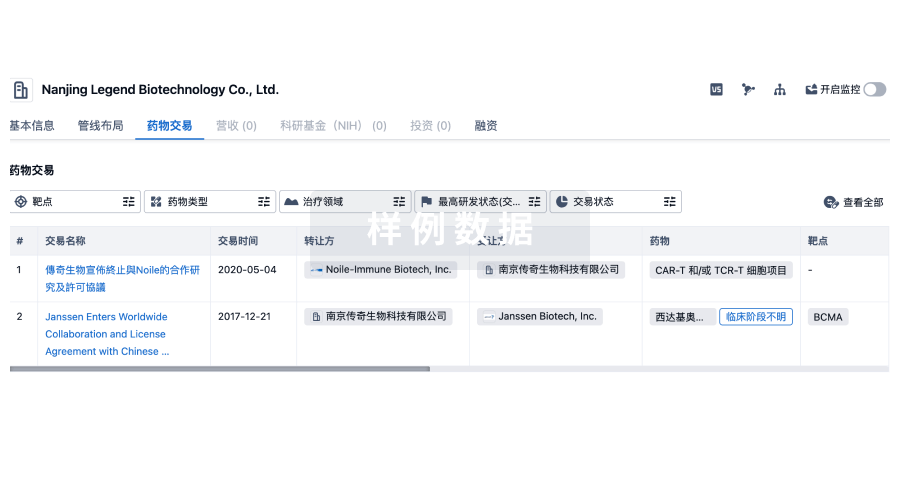
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
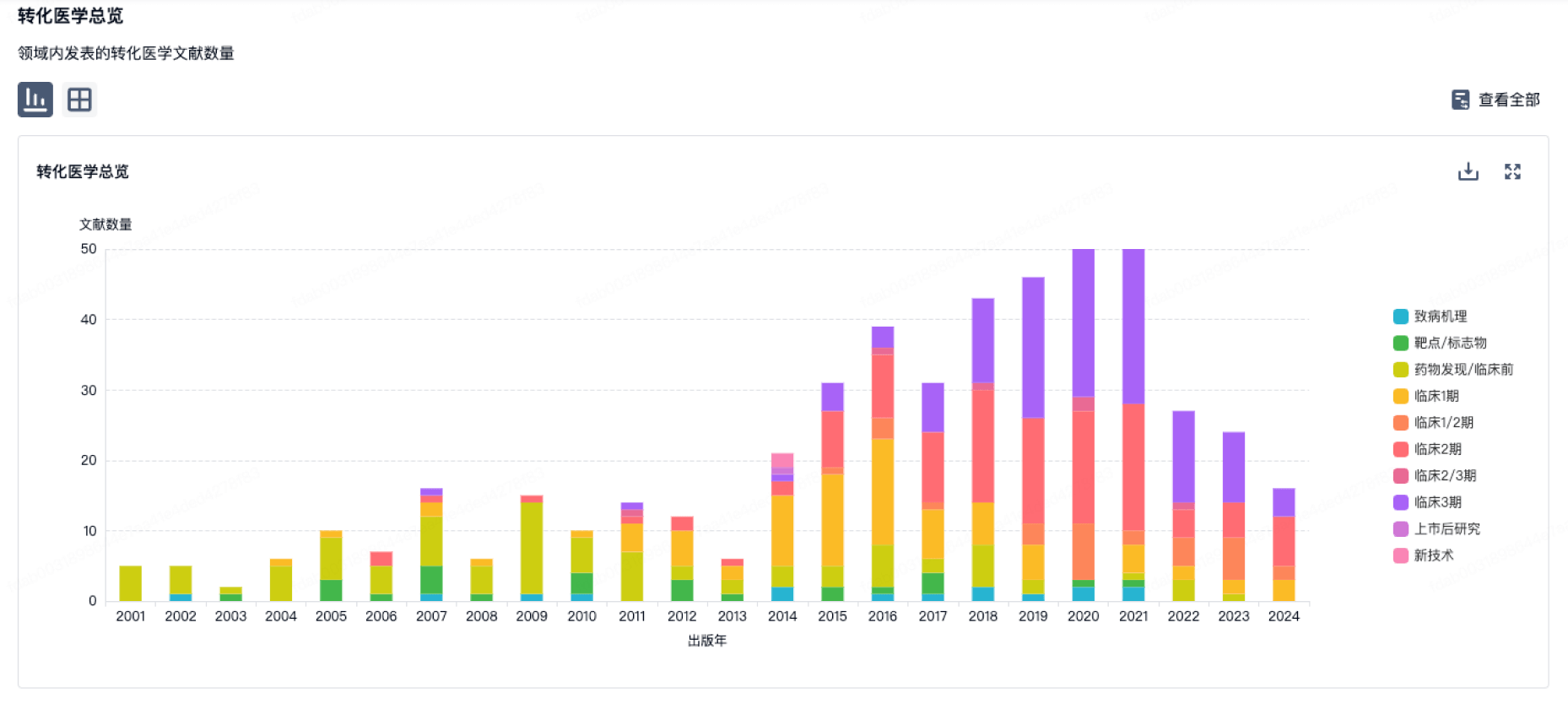
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
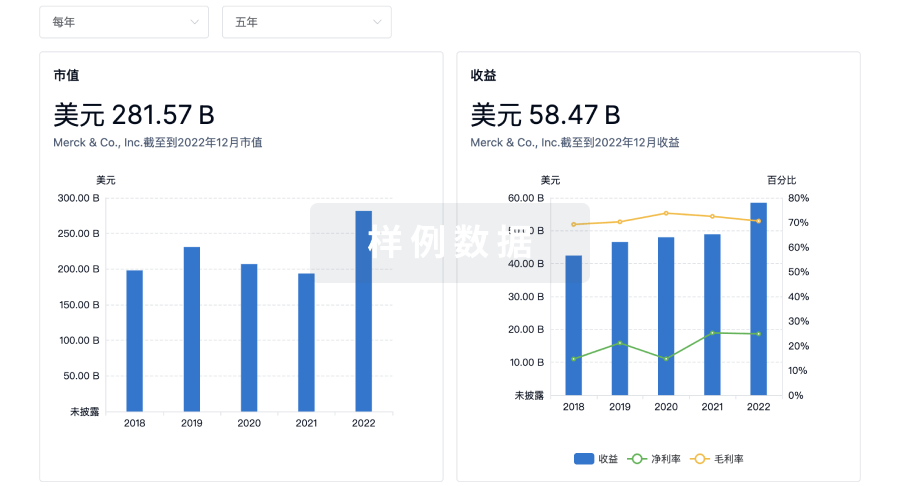
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
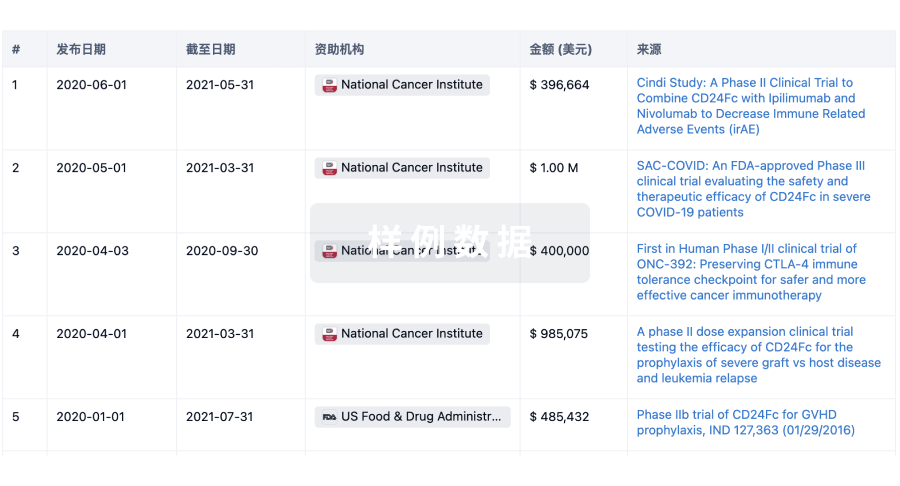
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
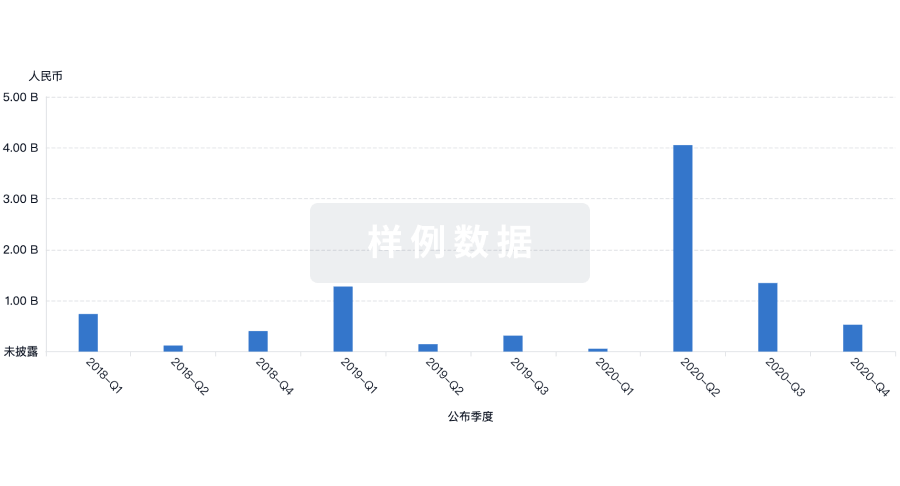
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
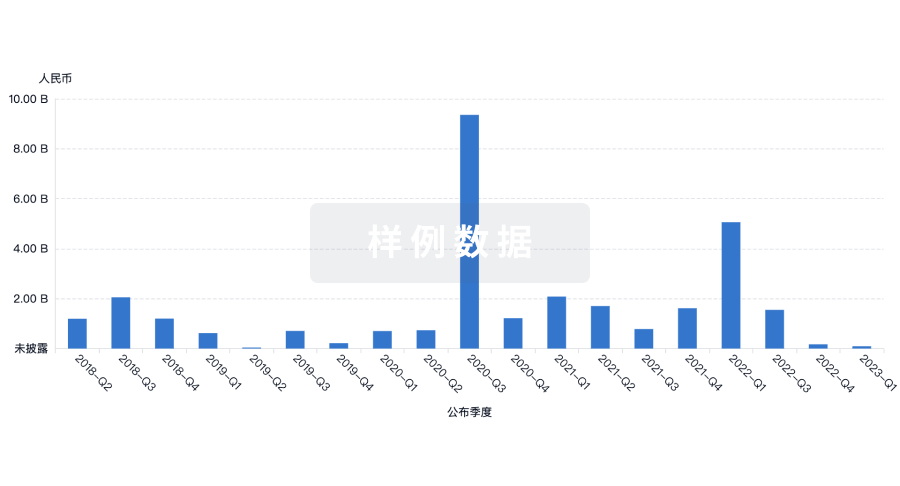
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用