预约演示
更新于:2026-06-05

Suzhou Lanma Medical Technology Co. Ltd.
更新于:2026-06-05
概览
标签
肿瘤
皮肤和肌肉骨骼疾病
泌尿生殖系统疾病
肿瘤浸润淋巴细胞
关联
5
项与 苏州蓝马医疗技术有限公司 相关的药物靶点- |
作用机制 免疫细胞毒性 [+1] |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床2期 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制- |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段早期临床1期 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制- |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
9
项与 苏州蓝马医疗技术有限公司 相关的临床试验NCT07444437
A Multicenter, Randomized, Controlled, Open-label, Phase IIa Trial on Autologous Tumor Infiltrating Lymphocyte Injection (LM103 TILs) for the Adjuvant Treatment of Non-small Cell Lung Cancer With Negative Driver Gene Mutations
After receiving neoadjuvant treatment with PD-1 antibody and undergoing radical resection, a total 36 to 45 NSCLC patients who met the inclusion criteria, will be randomly assigned in a 1:1:1 ratio to the experimental group 1, experimental group 2 and the control group in this Phase IIa clinical trial. The study will be followed up until 24 to 36 months after treatment.
开始日期2026-02-26 |
申办/合作机构 |
NCT07310784
A Multicenter, Randomized, Controlled, Open-label, Phase II Trial on Autologous Tumor Infiltrating Lymphocyte Injection (LM103 TILs) for the Treatment of Advanced Melanoma
A total of 92 subjects with advanced melanoma who met the inclusion criteria will be randomly assigned in a 1:1 ratio to the experimental group and the control group in this phase II trial. The study will be followed up until 24 months after treatment.
开始日期2025-12-16 |
申办/合作机构 |
NCT06695689
An Investigator-initiated Clinical Study of LM303 Injection for the Treatment of Advanced Solid Tumours
This is a single-arm, open-label, exploratory study to evaluate safety and efficacy of LM303 Injection in patients with advanced solid tumors. The purpose of this study is to evaluate the safety and tolerability, antitumor activity and immunoreactivity.
开始日期2024-10-17 |
申办/合作机构 |
100 项与 苏州蓝马医疗技术有限公司 相关的临床结果
登录后查看更多信息
0 项与 苏州蓝马医疗技术有限公司 相关的专利(医药)
登录后查看更多信息
29
项与 苏州蓝马医疗技术有限公司 相关的新闻(医药)2026-04-23
·药筛
过继性细胞免疫治疗(英文:Adoptive Cell Transfer,简称 ACT),又称过继性免疫,是一种高度个体化的肿瘤免疫疗法。
该疗法通过分离患者自身(自体)或供者(异体)的免疫细胞,在体外进行激活、基因修饰及大规模扩增后,再回输至患者体内,使其获得识别并杀伤肿瘤细胞的能力。
代表性技术包括 CAR-T、TCR-T 及 TIL等。
其中,TIL 疗法(Tumor-Infiltrating Lymphocytes Therapy)核心是,从患者手术切除的肿瘤组织中,分离出天然浸润的淋巴细胞,在体外通过高浓度 IL-2 进行大规模扩增和激活后,再回输至患者体内。
今天先来看看TIL疗法已上市以及在研管线情况。
1.已上市阶段
全球首款且唯一一款:Iovance的lifileucel(商品名Amtagvi)于2024.02.16在美国上市,并在上市当年就达到了1.036亿美元的销售额。
但根据公开信息,lifileucel在美国的标价为单次治疗51.5万美元,约合370万人民币,还是相当昂贵的。
2、申请上市阶段
暂无最高研发阶段是申请上市的TIL疗法。
3、I-III期
摩熵医药数据库显示,已有61个临床试验项目进入I-III期。
其中只有荷兰癌症研究所的 M14TIL进入III期,目前已完成招募,试验登记号NCT02278887。
这是一项比较非清髓性淋巴细胞清除化疗方案,联合肿瘤浸润淋巴细胞输注及白细胞介素-2,与标准伊匹木单抗治疗转移性黑色素瘤的疗效的,随机化III期研究。
根据2022年ESMO大会上Haanen报告的III期M14TIL试验结果,TIL疗法相较于标准伊匹木单抗治疗,显著延长了晚期黑色素瘤患者的无进展生存期,疾病进展或死亡风险降低50%。
进入I-II期的约1/3是国内企业,如广东昭泰细胞、沙砾生物、上海君赛、西比曼等等。
其中杭州华赛伯曼的HSIT-101、沙砾生物的GT-101、北京安韦森生物的ReT01 ACT、上海君赛的GC-101、苏州蓝马的LM-103、北京卡替的ScTIL-210已进入II期。
适应症方面:已从恶性黑色素瘤向宫颈癌、非小细胞肺癌、头颈癌、结直肠癌、卵巢癌、乳腺癌等多种癌种扩展。
TIL疗法已完成了从“概念”到“首个上市产品”的跨越,III期临床数据证明了其对实体瘤的有效性,国内企业也已进入II期冲刺阶段,适应症版图正在快速扩张。
但高昂成本、复杂工艺和有限的可及性仍是其广泛应用的现实障碍。未来,如何在保持疗效的同时简化流程、降低费用、拓展适应症,将是TIL疗法走向主流的核心命题。
(文中插图数据来源:摩熵医药数据库)
2026-03-31
·无癌家园
关注无癌家园
我们战癌到底
前段时间,120万一针的CAR-T疗法的余热未退去,另外一种针对实体瘤的新型细胞免疫疗法——肿瘤浸润淋巴细胞(TIL)疗法又掀起新的抗癌热潮。
TIL被喻为肿瘤细胞的“天然克星”。基于患者自体肿瘤浸润淋巴细胞开发的TIL疗法,具有肿瘤特异性靶点丰富、肿瘤趋向性好、浸润能力强和安全窗口高等优点。
靶病灶完全缓解!KRAS突变肺癌患者经TILs疗法GC101输注后持续获益!
近日,医学界传来了关于TILs疗法获得令人鼓舞疗效的好消息!一例KRAS突变阳性肺癌受试者经GC101 TIL治疗18周后,疗效评估靶病灶达到完全缓解(CR),非靶病灶正逐渐消退,为KRAS突变阳性肺癌患者带来希望。
这是一例KRAS G12D突变的肺腺癌ⅣB期患者,自2022年4月出现左胸疼痛,确诊后先后接受免疫与化疗的联合治疗,以及免疫、抗血管生成抑制剂与化疗的联合治疗,都因疾病进展或不耐受停药。在现有治疗手段无效时,患者参加了GC101 TIL细胞注射液注册临床试验。
TIL治疗过程,受试者除预处理过程短暂血液学毒性外无其他不良反应。回输第6周肿瘤缩小45%,肿瘤标志物恢复正常,癌痛减轻、颈部淋巴结消失;第12周靶病灶完全缓解(CR),18周时CR仍维持。
患者接受TIL治疗前和治疗后6周、18周增强CT扫描结果(左侧颈部淋巴结)
(图源上海九院官网,侵删)
GC101 TIL展现出卓越疗效,仅需单次给药,便可持续发挥对肿瘤的杀伤作用。在日常生活中,受试者完全能够自理,顺利回归正常家庭生活,这充分彰显了GC101 TIL在改善患者生活质量、助力患者回归正常生活方面的显著优势 。
在此之前,GC101 TIL注射液首个关键性II期注册临床试验已获得国家药品监督管理局药品审评中心(CDE)批准,用于经PD-1抗体治疗进展或不耐受的晚期黑色素瘤患者(NCT06703398)。
GC101是全球首款无需清淋、无需IL-2注射的天然TIL细胞疗法,其首个适应症获准进入关键II期临床,是实体瘤细胞治疗领域的一大重要突破。
GC101针对恶性黑色素瘤、宫颈癌、肺癌等多种类型晚期实体肿瘤的客观缓解率超35%,已有4例患者肿瘤完全缓解(CR),其中无瘤生存最久时间已近3年,未发生与治疗相关的严重不良反应,大幅提高TIL疗法的安全性、适用性与可及性。
如何寻求TIL细胞治疗>>
目前无癌家园有TILs免疫细胞临床试验正在招募中,急招黑色素瘤、非小细胞肺癌患者,除此之外,也招募宫颈癌、子宫内膜癌、乳腺癌,卵巢癌等实体瘤。
有意向的患者若想参加可整理出完整的病理报告、治疗经历、出院小结等再致电无癌家园医学部(400-626-9916),详细评估病情。
小试牛刀!21.4%非小细胞肺癌患者对TIL疗法有反应!
近期,美国纪念斯隆凯特琳癌症中心展示的一项2期临床试验中,所有入组的28例受试者均为转移性或全身扩散的非小细胞肺癌患者,且对其他大量肺癌疗法耐药,包括免疫检查点抑制剂(如PD-1)。
试验结果显示,在24例可评估的患者中,有6例使用TIL疗法后出现了抗癌反应,这意味着有21.4%(6/28)的非小细胞肺癌患者对TIL疗法有反应,一些患者治疗后,连续2年多未复发。
本次MSK斯隆的研究,头一次证明了肺癌肿瘤中生产出来的TIL细胞,可用于治疗肺癌。
图源MSKCC官网
一名41岁IV期粘液性肺腺癌男性患者接受TIL治疗前及治疗后6周的CT扫描。肿瘤携带KRAS G12D突变,TMB为3.3 mut/Mb,PD-L1表达为0%。患者在接受卡铂、紫杉醇和帕博利珠单抗等三线治疗后,初始缓解后出现疾病进展。CT扫描显示,TIL输注后12周,根据RECIST v1.1标准,部分缓解(PR)率为81%。
专家提醒:手术后将TILs细胞储存起来
几乎所有患者的肿瘤组织在手术后仅取一小部分做成病理蜡块,其余部分就直接作为医疗垃圾处理掉,浪费了我们自身宝贵的抗癌资源!
建议大家在手术前争得主治医生的同意,将新鲜手术组织保存,交由专业机构将TIL细胞提取,可以在术后回输预防复发,或者是先冻存起来,以备未来不时之需。因为手术后未经其他治疗时新鲜组织中的TIL细胞对肿瘤的杀伤能力才是最强的,一旦接受化疗和放疗,免疫细胞的杀伤能力会被削弱。具体的方法和冻存流程大家可以致电无癌家园医学部(400-626-9916)进行详情咨询。
国内研发产品层出不穷,横扫多种实体瘤!
Lovance的全球首款获批上市的肿瘤浸润淋巴细胞(TIL)疗法Amtagvi定价为51.5万美元(约合人民币370万)。这在所有上市的免疫疗法中是最昂贵的,如此昂贵的天价让众多病友望而却步。
然而,国内方面,多家公司公布了TILs管线临床获批的好消息。整体而言,能够感受到TILs赛道的热度在持续上升并日趋白热化,国内研究者们也在不断突破创新。
1.百吉生物:BST02
2023年10月26日,百吉生物在实体瘤领域又一重磅产品BST02的I/II期临床试验申请获得美国FDA批准,用于治疗所有类型的肝癌,是全球首款进入临床阶段针对肝癌的TIL细胞治疗药品。
2.君赛生物:GC101
2022年4月24日,君赛生物自主开发的“自体天然肿瘤浸润淋巴细胞注射液(GC101 TIL)”(受理号:CXSL2200070)正式获得NMPA的临床试验默示许可。该产品是全球首个既不需要淋巴细胞清除也不需要IL-2输注的天然TIL细胞治疗产品。
GC101是君赛生物的首款TIL细胞新药品种,在前期研究者发起的临床研究(IIT)中,展现良好的安全性与有效性。2例受试者达到完全缓解(CR)疗效,3例受试者达到部分缓解(PR)疗效,CR持续时间已分别超过8个月与6个月,初步展示了GC101良好的安全性与有效性。
3.沙砾生物:GT101
2022年4月22日,中国国家药监局药品审评中心(CDE)官网显示,沙砾生物自主研发的GT101注射液(受理号:CXSL2200061)正式获得国家药品监督管理局(NMPA)的临床试验默示许可。值得一提的是,GT101是国内首个获批临床的肿瘤浸润淋巴细胞药物(TIL),具有里程碑式的意义!
4.智瓴生物:ZLT-001
2023年1月28日,智瓴生物的ZLT-001注射液(受理号:CXSL2200552)正式获得国家药品监督管理局(NMPA)的临床试验默示许可,适应症为晚期复发或转移性宫颈癌,这是华南区首个获批临床的TIL药物,也是第三家在国内获批临床的TIL企业。
5.天科雅生物:HV-101
2023年1月29日,据CDE官网公示,天科雅生物医药科技有限公司提交的"HV-101注射液"获得临床试验默示许可,适应症为晚期复发或者转移性实体瘤(受理号:CXSL2200574)。
6.君赛生物:GC203
2024年2月6日,上海君赛生物自主研发的“GC203 TIL细胞注射液” 的新药临床试验(IND)申请获得国家药品监督管理局(NMPA)受理。
据无癌家园小编获悉,官方披露到,GC203为基因修饰TIL细胞药物,拟用于治疗晚期实体瘤。GC203是君赛生物第二款申请注册临床的TIL细胞新药,也是全球首个基于非病毒载体开发的TIL新药品种!第一款是之前无癌家园小编报道过的 GC101,同样也是用于治疗实体瘤的细胞新药。
与GC101一样,GC203无需清淋、无需IL-2注射联用,在普通病房便可完成整个治疗,预计单例患者便可节省15万+左右的配套临床费用,将大幅提升基因修饰TIL疗法的可及性。
据官方透露,在针对卵巢癌、宫颈癌、子宫内膜癌等妇科肿瘤的临床研究中,19例接受该候选产品治疗并可评估的晚期肿瘤患者中,肿瘤明显缩小,且长期缓解,疾病控制率(DCR)达84.2%,客观缓解率(ORR)为42.1%。让我们共同期待日后GC203将会给大家带来更多的惊喜!
7.沙砾生物:GT201
2023年7月11日,沙砾生物的第二款产品GT201,正式获得国家药品监督管理局的临床试验默示许可,成为国内首款进入注册临床试验的基因编辑型TIL药物。
GT201在体内外均表现出较传统TIL更强的增殖能力、肿瘤杀伤、细胞因子释放和更好的存续性,并可以降低对于IL-2的依赖性,从而克服传统TIL产品所面临的挑战,优化并提升传统TIL产品的功能和存续,并潜在降低临床应用中IL-2的使用剂量。此外,首个人体试验显示,GT201在多个晚期实体瘤患者体内均表现出良好的安全性,并展示出稳定的扩增和初步临床疗效。
8.沙砾生物:GT316
TILs的适应性细胞治疗在多种类型的实体瘤中表现出良好的治疗效果,并显著延长了晚期患者的生存期。然而,在制造过程中快速扩增后的最终TIL产品的 "易衰竭 "表型,以及肿瘤微环境(TME)中各种免疫抑制机制的存在,损害了TIL输注后的持久性和抗肿瘤功效。
而沙砾生物在2023年美国癌症研究协会(AACR)年会上,介绍了其下一代TIL疗法GT316,据报告称,该疗法能够解决TIL细胞在增殖过程中的衰竭,并保持疗效。
9.西比曼生物:C-TIL051
2022年10月,西比曼生物宣布FDA批准了公司新型TIL疗法C-TIL051的IND申请,适应证为PD-1抗体难治或复发的晚期非小细胞肺癌。
C-TIL051使用了西比曼生物专有的工艺,比传统制造方法生产的TIL更快、更有效地在人体内达到临床剂量。
从适应症布局看,多条管线对应多种适应症,覆盖黑色素瘤、非小细胞癌、宫颈癌、肺癌、头颈部鳞状细胞癌等广泛实体瘤癌种。
10.华赛伯曼:HS-IT101
2023年11月29日,华赛伯曼宣布,公司自主研发的首款TIL细胞1类新药——HS-IT101注射液(受理编号:CXSL2300599)用于治疗晚期实体瘤的IND申请获得NMPA临床试验默示许可。
HS-IT101是华赛伯曼自主研发的自体天然加强TIL产品,该产品是华赛伯曼首款获批进入临床的产品,预计在今年1月启动Ⅰ期临床试验。
11.蓝马医疗:LM103
2023年7月13日,国家药监局药品审评中心(CDE)官网显示,Medpark园内企业苏州蓝马医疗技术有限公司(以下简称:蓝马医疗)LM103注射液(TILs)正式获得国家药品监督管理局(NMPA)的临床试验默示许可。据无癌家园悉,这是国内TIL领域首个使用滋养细胞(Feeder)工艺的临床许可。
12.劲风生物:TILs疗法
2022年2月10日,劲风生物宣布其TILs疗法产品获得美国FDA批准进入临床一期。劲风生物成为国内首家TILs疗法产品获批进入临床的TILs疗法研发企业。
13.翊寿科技:自体肿瘤浸润淋巴细胞注射液
根据CDE官网,武汉翊寿科技和海南翊寿科技联合申报的1类新药“自体肿瘤浸润淋巴细胞注射液”已于2023年获批临床,拟开发用于肝癌等实体瘤的治疗。
14.卡替医疗:超强型TIL
2023年5月29日,卡替医疗的广谱抗癌细胞药物ScTIL——外周血来源的超强型类TIL细胞技术亮相2023年中关村论坛。
ScTIL技术是针对实体瘤的免疫细胞疗法,在外周血循环类TIL(cTIL)细胞的基础上负载靶向PD-L1的增强受体及CD19 CAR扩增因子,具有不限癌种、不限分期、不限肿瘤突变负荷的潜力和绝大多数肿瘤患者都适用的优势,且安全性和疗效较好。
15.毕诺济:BEN101
BEN101 注射液是专注于实体瘤领域的毕诺济(上海)生物技术有限公司自主研发的自体肿瘤浸润淋巴细胞(TILs)注射液,属于过继细胞疗法 (ACT),主要研究人群为晚期复发或转移性实体瘤(卵巢癌、宫颈癌、肾细胞癌和尿路上皮癌)。
小编有话说
目前,全球已经开展了TILs疗法针对转移性黑色素瘤、鼻咽癌、头颈部鳞状细胞癌、胆管癌、复发性或难治性卵巢癌、骨肉瘤、宫颈癌、卵巢癌、非小细胞肺癌、脑胶质瘤、胸膜间皮瘤等多种实体瘤的临床试验,TILs疗法在治疗包括转移性黑色素瘤、头颈部鳞状细胞癌、宫颈癌、非小细胞肺癌等多种实体瘤方面都展现出了临床价值。
此外,对于PD-1耐药的患者,接受TILs疗法也有显著疗效,无癌家园小编曾报道过关于TILs疗法联合PD-1让晚期转移性肺癌患者完全缓解的案例。
综上所述,TIL疗法在治疗实体瘤方面具有一些独特的优势,但仍面临一系列挑战。肿瘤免疫抑制微环境仍然是TIL治疗的主要障碍。此外,在有效肿瘤反应性 T 细胞的分离和扩增方面仍有相当大的改进空间,仍然需要探索替代联合疗法。
拓展阅读
除了上述提到的肿瘤浸润淋巴细胞疗法外,还有:
1. CAR-T疗法:CAR-T疗法(嵌合抗原受体T细胞免疫疗法)是一种治疗肿瘤的新型精准靶向治疗,只不过机制比PD-1更复杂。通过基因工程技术将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将T细胞这个普通“战士”改造成“超级战士”,即CAR-T细胞,专门识别体内肿瘤细胞,并高效杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。
2. 树突状细胞疫苗:一群异质性的免疫细胞,抗原提呈功能最强, 是唯一能够激活初始型T细胞的专职抗原递呈细胞,因此也称为免疫系统的“哨兵”。
3. TCR-T疗法:相较于CAR-T疗法,TCR-T疗法在实体瘤治疗领域具备独特优势;
4.CAR-NK疗法:2020年,CAR-NK免疫细胞治疗曾被权威学术期刊《自然-医学》纳入度生物医学领域的十代瞩目进展之一。在实体瘤方面优势较为突出!
5. CTL疗法:利用癌细胞特有的、正常细胞上没有或者含量很低的蛋白质做诱饵,把外周血中那“万里挑一”的真正能抗癌的淋巴细胞,挑选出来,然后在体外进一步改良和扩增,然后回输给患者。
若想了解更多关于细胞免疫疗法的相关临床试验及临床技术请持续关注无癌家园(400-626-9916)。
本文为无癌家园原创,转载需授权!
参考文献
1.https://www.fda.gov/news-events/press-announcements/fda-approves-first-cellular-therapy-treat-patients-unresectable-or-metastatic-melanoma
2.https://pubmed.ncbi.nlm.nih.gov/3264384/
3.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3131487/
4.https://www.iovance.com/
5.https://pubmed.ncbi.nlm.nih.gov/35727633/
如果您对于目前的治疗方案有疑问,或者想要咨询更合适的治疗方案,请联系无癌家园医学部(400-626-9916)申请国际会诊。
免疫治疗国际专家推荐
无癌家园提醒癌友们
国内细胞免疫治疗技术,包括CAR-T细胞(除上市的CAR-T外)、树突细胞疫苗、NK细胞、TILs细胞(除上市的TILs外)、TCR-T细胞(除上市的TCR-T外)、癌症疫苗等技术均处于临床试验阶段,未获准在医院正式使用。国内患者可以参加正规临床试验,在医生的监管下使用,无癌家园网不推荐患者冒然尝试任何医疗机构和研发机构的收费治疗。
热门推荐
细胞疗法相关文章
Review past ▶▶▶
1.8周肿瘤病灶完全消失!我国首例TILs疗法癌症治愈出现!国研多款疗法厚积薄发!
2.肿瘤病灶接近完全缓解!NK细胞疗法联合化疗、靶向治疗晚期胰腺癌疗效惊艳!
3.横扫33种癌症!最长生存期延长35个月!肿瘤免疫新贵γδT细胞主攻肺癌、肝癌等癌!
4.肿瘤完全缓解!TILs细胞疗法竟能调动全身免疫军团对抗“红颜杀手”宫颈癌!
分享、收藏、点赞、在看安排一下?
免疫疗法细胞疗法临床2期临床申请
2026-01-14
·医麦客
免费早鸟票,200 张限量领取
2026 年 1 月 15 日
医麦客新闻 eMedClub News
2025年,中国免疫细胞领域迎来政策与研发双重突破。
一方面,首版商保创新药目录落地及以《生物医学新技术临床研究和转化应用管理条例》为核心的多项政策从临床转化、审批加速、支付优化多维度提升患者可及性。
另一方面,2 款血液瘤 CAR-T 产品获批上市,全球首款实体瘤 CAR-T 疗法申报上市获受理,商业化进程显著提速。与此同时,产业创新成果集中涌现。
全年免疫细胞领域共获批近 60 项 IND(据 CDE 官网统计,如有错漏,欢迎补充),覆盖 CAR-T、TCR-T、TIL、CAR-NK、Treg、iNKT 等多赛道,在提升安全性和可及性上不断创新,并展现出从血液瘤向实体瘤、从肿瘤向自免与感染性疾病加速拓展的多元化创新格局。
向上滑动阅览
▲ 2025 年获批临床的免疫细胞疗法
(仅统计 1 类创新药)
在此背景下,各技术路径的发展态势与突破方向如下:
CAR-T
2025 年,CAR-T 疗法继续引领中国免疫细胞治疗创新,在实体瘤与血液瘤两大领域均取得里程碑式进展,并通过持续技术迭代,应对疗效、安全性与可及性等核心挑战。
实体瘤 CAR-T 实现突破性进展
科济药业 CLDN18.2 自体 CAR-T 细胞疗法(针对晚期胃/食管胃结合部腺癌)上市申请获药监局受理,且被纳入优先审评,系全球首款申报上市的实体瘤 CAR-T。
易慕峰同靶点产品 IMC002 的 Ⅲ 期临床顺利推进,该疗法采用高特异性 VHH 纳米抗体设计,有望提升耐受性、拓展临床剂量范围,并扩展至前线及联合治疗等场景,助力突破实体瘤治疗难题。
此外,以 EGFRvIII、GUCY2C、MSLN、DLL3 等靶点 CAR-T 密集获批临床,适应症涵盖复发或进展高级别脑胶质瘤、胃癌、卵巢癌、小细胞肺癌等难治性癌种。
其中,先博生物 DLL3 CAR-T 采用创新设计的拥有自主知识产权的装甲结构,临床前研究中展示出了比同类 CAR 设计更优效的活性。
血液瘤 CAR-T 商业化与迭代并进
2025 年,恒润达生雷尼基奥仑赛注射液、精准生物普基奥仑赛注射液相继获批上市,使国内已上市 CAR-T 产品增至 8 款。合源生物纳基奥仑赛注射液新适应症获批上市,成为国内唯一覆盖白血病和淋巴瘤两大血液肿瘤适应症的 CAR-T 疗法。
西比曼双靶点 CAR-T(C-CAR039,靶向CD19/CD20)已进入关键确证性临床,针对 CD20 或 CD19 阳性的复发性或难治性大B细胞淋巴瘤。该双靶设计旨在提高治疗效果并降低抗原逃逸。此外,亘喜生物、上海医药、松鹤免疫、三生制药 CAR-T 亦采用双靶点设计,且均已在国内获批临床。
博生吉 PA3-17 注射液作为全球首款获批 IND 的靶向 CD7 自体 CAR-T,已进入关键临床 Ⅱ 期,并展现高缓解率(Ⅰ期临床 ORR 达 85%),预计 2026/2027 年冲刺上市,有望为 T 细胞恶性肿瘤患者提供新选择。
行业还将 CAR-T 治疗拓展至自身免疫性疾病领域,如邦耀生物、合源生物、森朗生物等,且多以临床验证过的 BCMA、CD19 经典靶点为主。机制上,通过耗竭 B 细胞以「重置」免疫系统,探索潜在的治愈性疗法,这与肿瘤治疗中清除癌细胞的逻辑有本质区别。
前沿拓展:可及性提升
为破解传统自体 CAR-T 成本高、制备流程复杂、周期长的技术瓶颈,行业内正通过多条技术路径推进创新,以提升疗法可及性。
一、开发现货型异体型 CAR-T,从源头解决可及性问题。邦耀生物、启函生物、优赛诺生物、科济药业、茂行生物等企业。
二、优化自体 CAR-T 体外制备平台,缩短患者等待周期。如合源生物 HY001N 基于快速制备 NexT 技术平台,使患者等待时间缩短 50%,可达 10 天,亘喜生物 GC012F 依托 FasTCAR 次日生产平台。
三、挖掘新型细胞来源,布局通用型疗法。γδT 细胞、DNT 细胞凭借其不依赖 MHC 识别且无 GVHD 风险的特点,成为理想来源。博生吉、清辉联诺、瑞顺生物等公司已在此领域展开布局,最快已至 Ⅱ 期临床。
此外,in vivo CAR-T 因无需清淋、绕过体外制备环节直接在患者体内改造 T 细胞而具有低成本、高可及性潜力吸引国内企业竞相布局。其中,虹信生物、微滔生物、星锐医药等已将该疗法推进至早期临床阶段。
CAR-NK/NK
与 CAR-T 疗法相比,NK 细胞疗法安全性优势显著:其细胞因子释放综合征、神经毒性风险更低,且无 GVHD 风险。目前国内该领域处于早期临床阶段,适应症向血液瘤、自免疾病拓展及联合治疗成为核心趋势。
2025 年多类型 NK 细胞获批临床。奇迈永华、达博生物布局非基因改造自体 NK,依托天然杀伤活性,安全性优且成本可控;恩瑞恺诺 KN5501 融合 CAR 特异性与 NK 安全性,实现通用型现货供应;英百瑞 IBR854 采用非病毒载体、非基因编辑的抗体偶联技术,将靶向 5T4 的抗体与异体 NK 共价偶联,精准狙击实体瘤同时规避基因修饰突变风险。
此外,英百瑞 IBR854 联合培唑帕尼用于晚期肾细胞癌已启动 Ⅱ 期临床试验,达博生物自体自然杀伤细胞注射液已获批 Ⅱ 期临床。
TCR-T
与 CAR-T 疗法相比,TCR-T 的核心优势在于它能够识别细胞内抗原,这使得它在实体瘤治疗中具有独特潜力。
行业头部企业香雪生命科学进展领先:其首发管线 TAEST16001(靶向 NY-ESO-1)已启动针对软组织肉瘤的确证性临床且并被纳入突破性治疗,有望成为国内首款上市的 TCR-T;后续管线 XLS-103 则靶向新生抗原 KRAS G12V 。
同时,TCR-T技术正向慢性感染等新领域延伸。星汉德生物的 SCG101(靶向HBsAg)已获批临床用于慢性乙型肝炎治疗。2025年欧洲肝脏研究学会公布的数据显示,单次治疗后患者血清 HBsAg 可实现快速、深度且持续的降低,并在长达一年随访期内维持在低于 100 IU/mL 水平且无反弹。
此外,针对这一适应症,来恩生物的 mRNA 编码 TCR-T 细胞疗法产品 LioCyx-M004 也已在 2025 年获得 FDA 的 IND 批准,是首个获得 FDA 快速通道资格的乙肝病毒特异性 TCR-T 疗法。
TIL
TIL 疗法通过天然多克隆识别能力靶向多个肿瘤新抗原,在对抗肿瘤异质性、避免抗原逃逸及归巢性方面具备优势,与基因工程改造的 CAR-T/TCR-T 形成差异化路径。
截至 2025 年底,国内已有三款 TIL 治疗黑色素瘤进入关键临床试验阶段,分别来自君赛生物(GC101)、华赛伯曼(HS-IT101)和蓝马医疗(LM103)。
君赛生物凭借全球首款「免清淋、免 IL-2 注射」TIL 疗法 GC101 等构建竞争优势,预计 2026 年提交上市申请,冲刺国内首个获批上市 TIL 创新药。
华赛伯曼 FAST-TIL 自体天然 TIL 候选产品 HS-IT1011 在注册 Ⅰ 期临床试验中初步显示出有潜力的疗效信号(ORR 50%、CRR 20%、DCR 100%,n=10)。
蓝马 LM103 注射液成为国内首个同时拥有两个 Ⅱ 期临床的 TILs,在 2025 年底先后获批了恶性黑色素瘤适应症关键临床 Ⅱ 期和非小细胞肺癌术后辅助治疗 Ⅱ 期临床。
适应症探索已超越黑色素瘤。据官网披露,沙砾生物是首个进入关键 Ⅱ 期临床的中国 TIL 企业,其针对宫颈癌的GT101在 Ⅰ 期临床中取得 45.5% 的 ORR。百吉生物则启动了全球首个针对肝癌的 TIL BST02 注册临床研究。
与此同时,下一代 TIL 技术旨在攻克传统疗法的瓶颈。极客基因申 GK01 通过从患者肿瘤组织中分离浸润的 T 细胞,利用自主研发的细胞命运重编程技术进行体外功能优化,显著增强其肿瘤识别和杀伤能力。沙砾生物 GT307 利用 CRISPR 基因编辑技术敲除两个关键基因,以改善 T 细胞在肿瘤微环境中的持久性与抗耗竭能力,并于 2025 年底获 FDA 批准临床。
Treg/iNKT/CIK 细胞等其他免疫细胞疗法
2025年,永泰生物针对肝癌的 CIK(细胞因子诱导杀伤细胞)疗法上市许可申请获得受理,且被纳入优先审评,有望成为国内首个获批上市的 CIK。该疗法以 CD3+CD8+ 杀伤性 T 细胞为主,辅以 NK 细胞等多亚群,通过广谱杀伤作用对抗实体瘤,无需基因改造,长期安全性良好。
Treg 细胞疗法已在神经系统疾病领域取得实质性进展。赛尔欣生物的自体多克隆 Treg 已在国内获批临床,用于治疗多系统萎缩与肌萎缩侧索硬化症,通过免疫调节与组织修复功能为非肿瘤疾病提供新选择。
基因启明是全球 iNKT 细胞疗法领域的领跑者。iNKT 细胞兼具 T 细胞与 NK 细胞功能,可直接杀伤肿瘤并激活免疫系统。2025 年 11 月,公司获首个非肿瘤适应症 IND 批件,其异体即用型 iNKT 细胞疗法正式进入注册临床,填补国内该领域空白。
此外,康爱生物、希灵生物/景达生物、瑞宏迪医药等企业也在推进实体瘤细胞疗法,进一步丰富治疗选择。
小结与展望
2025 年,中国免疫细胞疗法产业在见证全球首批实体瘤 CAR-T 申报上市、血液瘤商业化持续扩容的同时,已形成 CAR-T、TCR-T、TIL、NK 及 Treg/iNKT 等多技术路径并进共荣的生态格局。
未来,产业发展将沿着「攻坚」与「普惠」双主线深化推进:一方面持续突破实体瘤治疗瓶颈,并将适应症拓展至自身免疫性疾病、慢性感染等更广阔领域;另一方面,通过工艺优化、通用型技术开发与支付体系创新以提升治疗可及性与可负担性。
责任编辑丨菊
校对丨菊
参考资料:
1.各企业公布资料
精彩活动
长按识别二维码立即参与↓
推荐 1
1 月 20 日 19:00-20:30
精准抗癌新引擎:ICE 疗法与双抗/多抗技术的协同发展
推荐 2
1 月 29 日 19:00-20:30
TFF 膜包清洁重复验证与新版 PDA TR26 技术报告解读
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。
版权说明:欢迎个人转发文章至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。如需转载请在文章下方留言获取授权。
封面来源网络,如有侵犯版权,请联系删除
点点“分享”、“点赞”和“在看”
给我充点儿电吧~
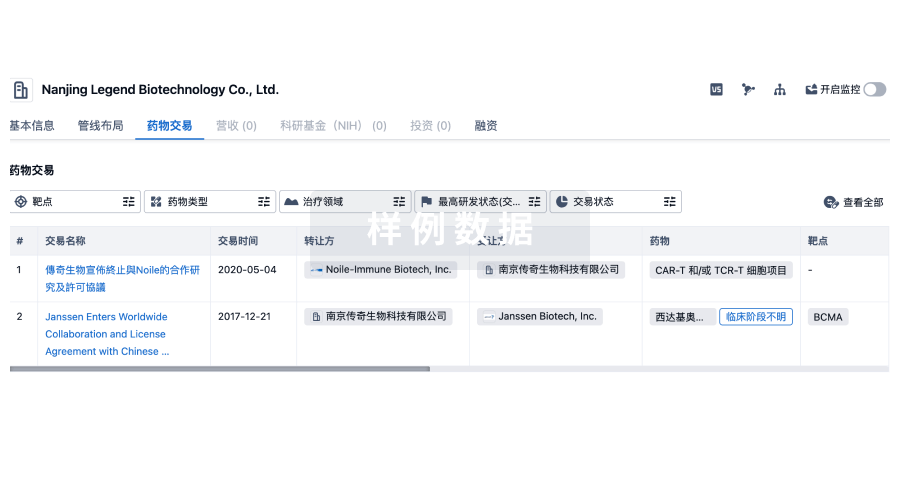
100 项与 苏州蓝马医疗技术有限公司 相关的药物交易
登录后查看更多信息
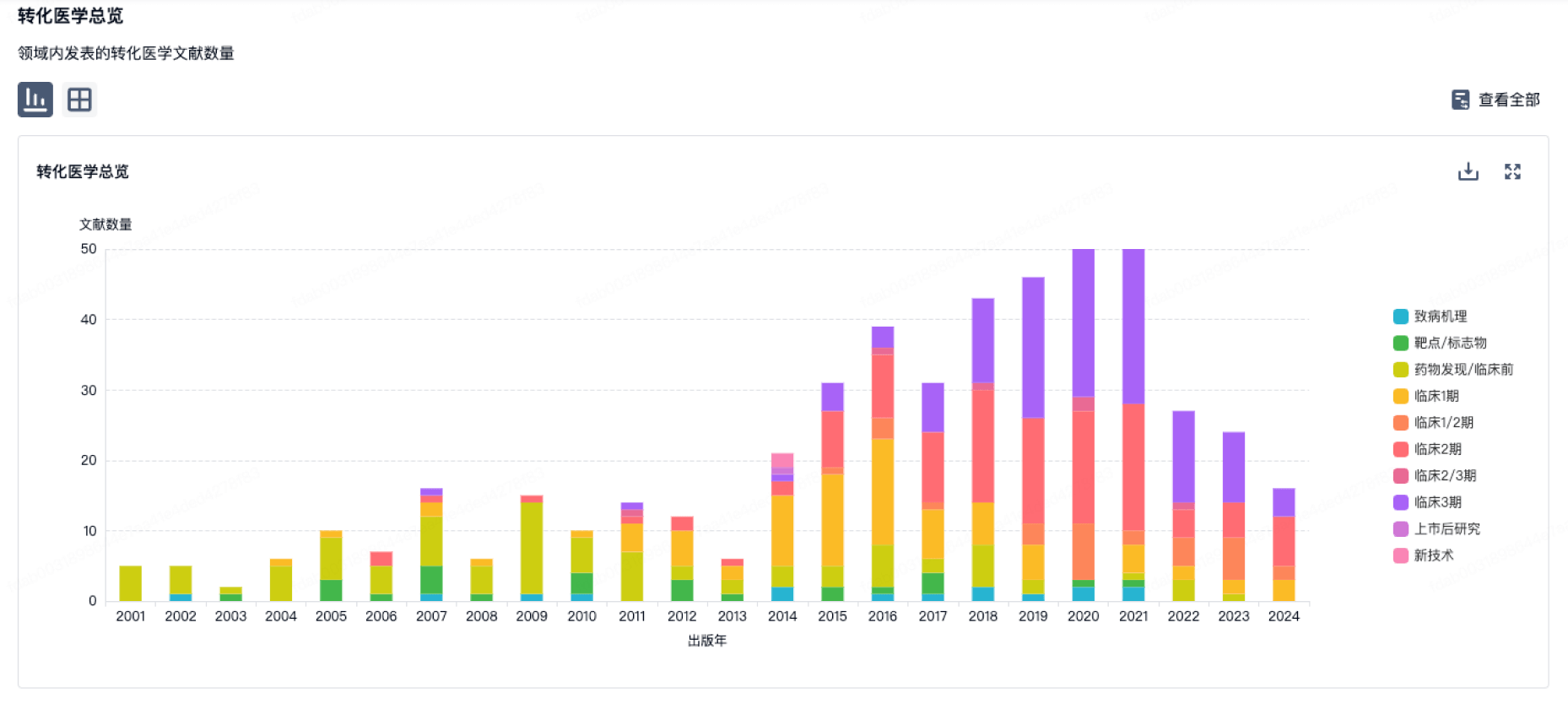
100 项与 苏州蓝马医疗技术有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月09日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床前
3
1
早期临床1期
临床2期
1
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
LM-103 | 局部晚期黑色素瘤 更多 | 早期临床1期 |
LM-303 | 晚期恶性实体瘤 更多 | 早期临床1期 |
TMER-TIL | 实体瘤 更多 | 临床前 |
LM103-Next | 实体瘤 更多 | 临床前 |
Power-TIL other | 实体瘤 更多 | 临床前 |
登录后查看更多信息
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
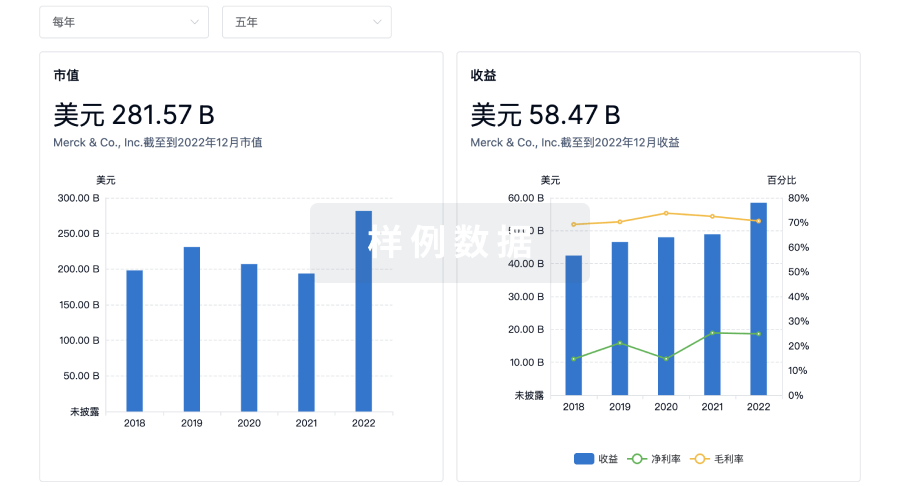
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
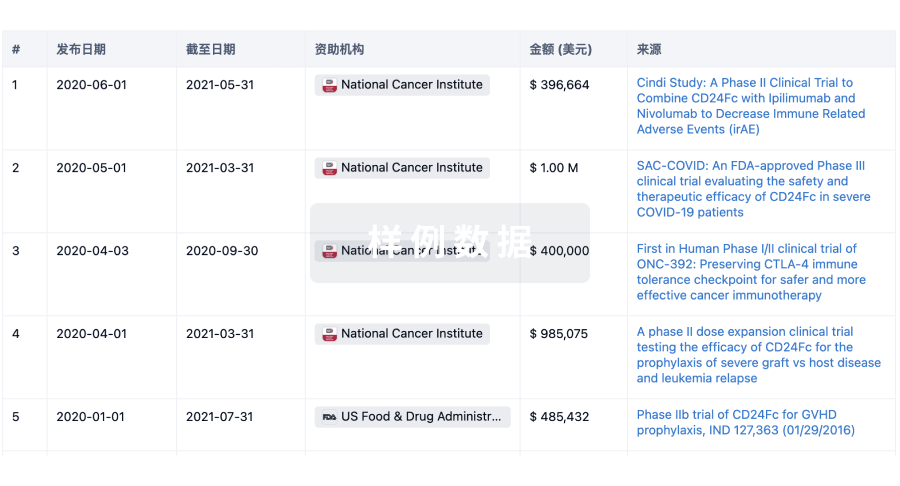
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
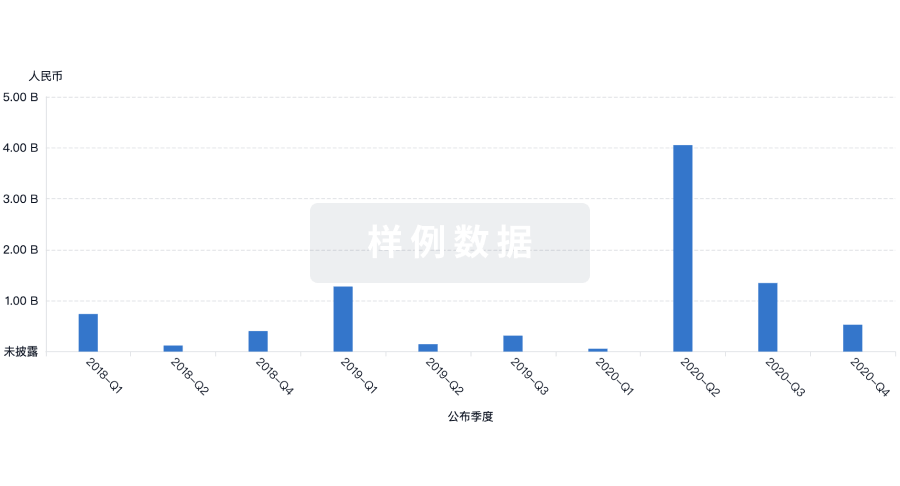
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
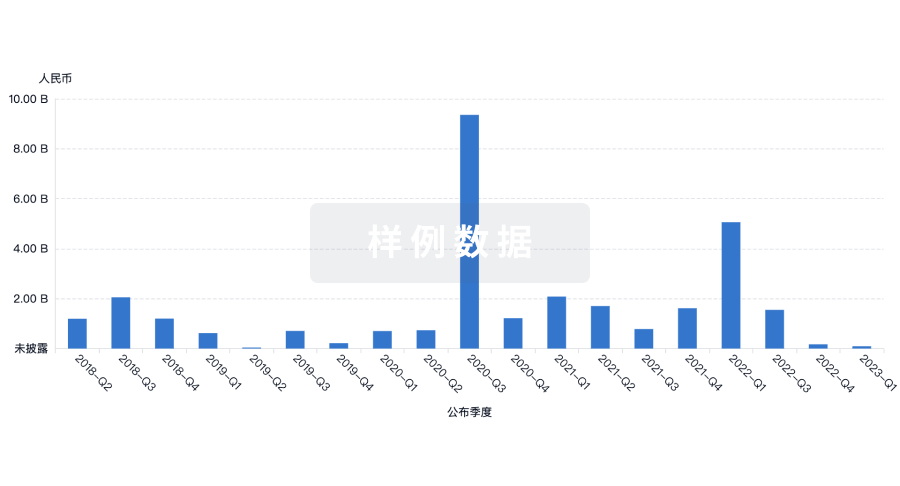
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用