预约演示
更新于:2025-05-07

Yabao Medicine Sichuan Pharmaceutical Co. Ltd.
更新于:2025-05-07
概览
标签
耳鼻咽喉疾病
呼吸系统疾病
消化系统疾病
小分子化药
关联
1
项与 亚宝药业四川制药有限公司 相关的药物靶点- |
作用机制- |
非在研适应症 |
最高研发阶段批准上市 |
首次获批国家/地区 日本 |
首次获批日期1965-11-01 |
5
项与 亚宝药业四川制药有限公司 相关的临床试验CTR20250252
布洛芬混悬液在健康参与者中的单中心、单次口服给药、随机、开放、两序列、两周期、双交叉、空腹状态下的生物等效性研究
主要研究目的:通过生物等效性研究,考察中国健康参与者在空腹条件下单次口服受试制剂布洛芬混悬液(规格:100 mL:2 g,亚宝药业四川制药有限公司研发)与参比制剂布洛芬混悬液(商品名:美林®,规格:100 mL:2 g,上海强生制药有限公司持证)后的体内药代动力学特征,评价两制剂的生物等效性。
次要研究目的:评价单次口服布洛芬混悬液100 mL:2g受试制剂及参比制剂在中国健康参与者中的安全性。
开始日期- |
申办/合作机构 |
CTR20230664
地诺孕素片在健康受试者中单中心、随机、开放、两制剂、单次给药、两周期、双交叉空腹/餐后生物等效性试验
以药代动力学参数作为主要终点评价指标,分别比较在空腹/餐后状态下口服受试制剂地诺孕素片(生产厂家:亚宝药业四川制药有限公司)与参比制剂地诺孕素片(持证商:Jenapharm GmbH & Co. KG,商品名:唯散宁®)后在健康受试者体内的药代动力学行为,评价两种制剂的生物等效性。观察受试制剂地诺孕素片和参比制剂地诺孕素片在健康受试者中的安全性。
开始日期2023-03-29 |
申办/合作机构 |
CTR20221685
孟鲁司特钠颗粒在中国成年健康受试者中的一项随机、开放、空腹和餐后单次给药、两制剂、两序列、两周期交叉的生物等效性试验
观察在空腹和餐后状态下单次口服受试制剂孟鲁司特钠颗粒T(规格:0.5g:4mg,以孟鲁司特计,亚宝药业四川制药有限公司生产)与参比制剂孟鲁司特钠颗粒R(商品名:顺尔宁®,规格:0.5g:4mg,以孟鲁司特计,Merck Sharp & Dohme Corp生产)在中国成年健康受试者体内的药代动力学特征,初步评估空腹与餐后状态下分别口服两种制剂后,T和R之间的生物等效性及个体内变异度。观察在空腹和餐后状态下单次口服受试制剂和参比制剂0.5g:4mg在中国成年健康受试者中的安全性。
开始日期2022-07-31 |
申办/合作机构 |
100 项与 亚宝药业四川制药有限公司 相关的临床结果
登录后查看更多信息
0 项与 亚宝药业四川制药有限公司 相关的专利(医药)
登录后查看更多信息
10
项与 亚宝药业四川制药有限公司 相关的新闻(医药)2025-04-28
·中国药闻
中药保护品种公告(第25号)(2025年第45号)根据《中药品种保护条例》规定,国家药品监督管理局批准北京中惠药业有限公司的五味苦参肠溶胶囊、成都华神科技集团股份有限公司制药厂的三七通舒胶囊、广州康臣药业有限公司的益肾化湿颗粒和亚宝药业四川制药有限公司的儿童清咽解热口服液为首家中药二级保护品种,保护品种编号分别为:ZYB2072025007、ZYB2072025008、ZYB2072025009、ZYB2072025011,保护期限自公告日起七年。 特此公告。国家药监局2025年4月25日
2025-04-28
根据《中药品种保护条例》规定,国家药品监督管理局批准北京中惠药业有限公司的五味苦参肠溶胶囊、成都华神科技集团股份有限公司制药厂的三七通舒胶囊、广州康臣药业有限公司的益肾化湿颗粒和亚宝药业四川制药有限公司的儿童清咽解热口服液为首家中药二级保护品种,保护品种编号分别为:ZYB2072025007、ZYB2072025008、ZYB2072025009、ZYB2072025011,保护期限自公告日起七年。 特此公告。 国家药监局 2025年4月25日
2025-03-02
·微信
统计每周仿制药一致性评价申报、上市申请(2.24-3.2)
1、仿制药上市申请获批药品名称企业名称分类受理号阿卡波糖片恒昌(广州)新药研究有限公司;南京海纳制药有限公司4CYHS2301628阿昔莫司胶囊石家庄四药有限公司4CYHS2400073艾司奥美拉唑镁肠溶胶囊广州新济药业科技有限公司;宜昌人福药业有限责任公司3CYHS2301834艾司奥美拉唑镁肠溶胶囊广州新济药业科技有限公司;宜昌人福药业有限责任公司3CYHS2301835艾司奥美拉唑镁肠溶胶囊湖南银泽华浩生物科技有限公司;双鹤药业(海南)有限责任公司3CYHS2301644艾司奥美拉唑镁肠溶胶囊湖南银泽华浩生物科技有限公司;双鹤药业(海南)有限责任公司3CYHS2301643艾司奥美拉唑镁肠溶胶囊江苏中邦制药有限公司3CYHS2301499艾司奥美拉唑镁肠溶胶囊江苏中邦制药有限公司3CYHS2301498氨甲环酸片石家庄四药有限公司4CYHS2400007氨氯地平贝那普利胶囊杭州沐源生物医药科技有限公司;新乡市常乐制药有限责任公司3CYHS2302279氨溴特罗口服溶液安盛药业有限公司;国药集团致君(深圳)坪山制药有限公司3CYHS2303179氨溴特罗口服溶液山东朗诺制药有限公司3CYHS2301242氨溴特罗口服溶液海南全星制药有限公司3CYHS2301203氨溴特罗口服溶液山西同达药业有限公司3CYHS2300730倍他米松磷酸钠注射液陕西丽彩药业有限公司;新乡市常乐制药有限责任公司3CYHS2301809苯磺顺阿曲库铵注射液海南斯达制药有限公司4CYHS2302502布洛芬混悬液福建太平洋制药有限公司4CYHS2301656蛋白琥珀酸铁口服溶液河北一品制药股份有限公司;安徽沃泰生物医药有限公司4CYHS2300152地氯雷他定口服溶液南京创迪生物技术有限公司;江苏贝佳制药有限公司3CYHS2301371地诺孕素片亚宝药业四川制药有限公司4CYHS2302418碘美普尔注射液成都倍特药业股份有限公司4CYHS2303352恩格列净二甲双胍缓释片上海汇伦江苏药业有限公司3CYHS2301338恩格列净二甲双胍缓释片乐普药业股份有限公司3CYHS2300066法莫替丁注射液成都米子生物医药科技有限公司;四川宏明博思药业有限公司3CYHS2302251法莫替丁注射液云南先施药业有限公司;江苏神龙药业有限公司3CYHS2301883非布司他片广州汇元医药科技有限公司;中山可可康制药有限公司4CYHS2400062非诺贝特片(Ⅲ)河北东圣科宇医药科技有限公司;广州玻思韬控释药业有限公司4CYHS2303347复方氨基酸注射液(18AA-Ⅶ)内蒙古白医制药股份有限公司4CYHS2302533复方醋酸钠林格注射液浙江医药股份有限公司新昌制药厂3CYHS2300622复方聚乙二醇电解质散(II)广东科泓药业有限公司;浙江国镜药业有限公司3CYHS2401130复方聚乙二醇电解质散(II)广东科泓药业有限公司;浙江国镜药业有限公司3CYHS2401129复方聚乙二醇电解质散(Ⅲ)重庆药谷制药有限公司;济川药业集团有限公司4CYHS2303243复方匹可硫酸钠颗粒苏州二叶制药有限公司3CYHS2300519复合磷酸氢钾注射液湖北科伦药业有限公司3CYHS2302126富马酸伏诺拉生片山东朗诺制药有限公司4CYHS2302609富马酸伏诺拉生片山东朗诺制药有限公司4CYHS2302610富马酸伏诺拉生片江苏万高药业股份有限公司4CYHS2301632富马酸伏诺拉生片江苏万高药业股份有限公司4CYHS2301631枸橼酸氢钾钠颗粒浙江众延医药科技有限公司;石家庄市华新药业有限责任公司4CYHS2303580骨化三醇软胶囊海南葫芦娃药业集团股份有限公司4CYHS2302755己酮可可碱注射液山西惠达林曦医药科技有限公司;山西威奇达光明制药有限公司3CYHS2302369甲磺酸仑伐替尼胶囊江苏东科康德药业有限公司;江苏华阳制药有限公司4CYHS2300534间苯三酚注射液国药集团国瑞药业有限公司4CYHS2302802间苯三酚注射液江苏东科康德药业有限公司;浙江赛默制药有限公司4CYHS2302370间苯三酚注射液呋欧医药科技(湖州)有限公司;浙江赛默制药有限公司4CYHS2302368间苯三酚注射液江苏明圣康源药业有限公司;江苏九旭药业有限公司4CYHS2302343聚普瑞锌颗粒江苏正大丰海制药有限公司3CYHS2301999拉考沙胺注射液浙江华海药业股份有限公司4CYHS2303102拉考沙胺注射液浙江兄弟药业有限公司;南京海纳制药有限公司4CYHS2302957硫酸氨基葡萄糖胶囊合肥国高药业有限公司;华益药业科技(安徽)有限公司4CYHS2303517铝碳酸镁咀嚼片湖北唯森制药有限公司4CYHS2301514氯化钾注射液北京布霖生物科技有限公司;华夏生生药业(北京)有限公司3CYHS2303251罗库溴铵注射液南京健友生化制药股份有限公司4CYHS2201910罗库溴铵注射液南京健友生化制药股份有限公司4CYHS2201909洛索洛芬钠凝胶贴膏湖南金圃医药科技有限公司;南京海纳制药有限公司4CYHS2302174马来酸氟伏沙明片石家庄四药有限公司4CYHS2401286马立巴韦片齐鲁制药(海南)有限公司4CYHS2500156吗替麦考酚酯干混悬剂杭州中美华东制药有限公司3CYHS2303280米拉贝隆缓释片江苏德源药业股份有限公司4CYHS2303421米诺地尔搽剂福元药业有限公司3CYHS2301774米诺地尔搽剂福元药业有限公司3CYHS2301775普拉洛芬滴眼液山东百诺医药股份有限公司;江西科伦药业有限公司4CYHS2303009沙库巴曲缬沙坦钠片江苏万高药业股份有限公司4CYHS2303500沙库巴曲缬沙坦钠片江苏万高药业股份有限公司4CYHS2303499缩宫素注射液裕松源药业有限公司3CYHS2301747他达拉非片广东九明制药有限公司4CYHS2303273他达拉非片广东九明制药有限公司4CYHS2303274他达拉非片广东九明制药有限公司4CYHS2303275他达拉非片重庆朗天制药有限公司;江苏华阳制药有限公司4CYHS2303188妥布霉素地塞米松滴眼液湖南明瑞制药股份有限公司;杭州国光药业股份有限公司4CYHS2500148吸入用盐酸氨溴索溶液四川普锐特药业有限公司3CYHS2401221吸入用盐酸氨溴索溶液四川普锐特药业有限公司3CYHS2401220吸入用盐酸氨溴索溶液四川普锐特药业有限公司3CYHS2401222吸入用盐酸氨溴索溶液瑞阳制药股份有限公司3CYHS2302805吸入用盐酸氨溴索溶液瑞阳制药股份有限公司3CYHS2302804西咪替丁注射液山西诺成制药有限公司3CYHS2301528腺苷钴胺胶囊北京柏雅联合药物研究所有限公司;广东华南药业集团有限公司3CYHS2301823熊去氧胆酸胶囊福建省宝诺医药研发有限公司;浙江京新药业股份有限公司4CYHS2303153盐酸氨溴索口服溶液安徽四环科宝制药有限公司3CYHS2300662盐酸氨溴索口服溶液安徽四环科宝制药有限公司3CYHS2300663盐酸奥洛他定滴眼液浙江莎普爱思药业股份有限公司4CYHS2302146盐酸丙美卡因滴眼液合肥立方制药股份有限公司;安徽省双科药业有限公司3CYHS2301065盐酸二甲双胍缓释片重庆药友制药有限责任公司4CYHS2302114盐酸胍法辛缓释片四川百利药业有限责任公司3CYHS2400473盐酸胍法辛缓释片四川百利药业有限责任公司3CYHS2400472盐酸尼卡地平注射液陕西丽彩药业有限公司;江苏九旭药业有限公司4CYHS2303327盐酸尼卡地平注射液成都地奥九泓制药厂;四川美大康佳乐药业有限公司4CYHS2302954盐酸齐拉西酮胶囊湖南九典制药股份有限公司4CYHS2302874盐酸屈他维林注射液成都倍特药业股份有限公司4CYHS2302232盐酸去氧肾上腺素注射液远大医药(中国)有限公司3CYHS2202105盐酸他喷他多片宜昌人福药业有限责任公司3CYHS2302567盐酸他喷他多片宜昌人福药业有限责任公司3CYHS2302569盐酸他喷他多片宜昌人福药业有限责任公司3CYHS2302568盐酸左布比卡因注射液山东新时代药业有限公司4CYHS2302953吲哚布芬片福安药业集团湖北人民制药有限公司3CYHS2301929吲哚布芬片福安药业集团湖北人民制药有限公司3CYHS2301928注射用利培酮微球浙江圣兆药物科技股份有限公司;吉林敖东洮南药业股份有限公司4CYHS2302328注射用利培酮微球浙江圣兆药物科技股份有限公司;吉林敖东洮南药业股份有限公司4CYHS2302327注射用两性霉素B脂质体Taiwan Liposome Company, Ltd.5.2JYHS2300035注射用尼可地尔合肥盛秦医药科技有限公司;国药集团国瑞药业有限公司3CYHS2302325注射用尼可地尔常州四药制药有限公司3CYHS2302173注射用尼可地尔常州四药制药有限公司3CYHS2302172左卡尼汀注射液浙江昂利康制药股份有限公司;浙江创新生物有限公司4CYHS2303573左氧氟沙星氯化钠注射液广东大翔制药有限公司4CYHS2303579左氧氟沙星氯化钠注射液广东大翔制药有限公司4CYHS2303578左乙拉西坦口服溶液湖南省湘中制药有限公司4CYHS2302859
注:灰色字体部分受理号结论为不批准。
2、一致性评补充申请获批药品名称企业名称受理号阿莫西林克拉维酸钾干混悬剂南京臣功制药股份有限公司CYHB2450220阿莫西林克拉维酸钾干混悬剂南京臣功制药股份有限公司CYHB2450221布洛芬缓释胶囊云鹏医药集团有限公司CYHB2450063非那雄胺片鲁南贝特制药有限公司CYHB2450085富马酸酮替芬片仁和堂药业有限公司CYHB2450210坎地沙坦酯片山西皇城相府药业股份有限公司CYHB2450167碳酸氢钠注射液海南倍特药业有限公司CYHB2350916碳酸氢钠注射液海南倍特药业有限公司CYHB2350917碳酸氢钠注射液四川太平洋药业有限责任公司CYHB2350843头孢泊肟酯片康芝药业股份有限公司CYHB2450123盐酸布比卡因注射液安徽长江药业有限公司CYHB2450185盐酸布比卡因注射液安徽长江药业有限公司CYHB2450186盐酸布比卡因注射液上海朝晖药业有限公司CYHB2350873盐酸多西环素片特一药业集团股份有限公司CYHB2450082盐酸多西环素片特一药业集团股份有限公司CYHB2450081盐酸左氧氟沙星片广州白云山医药集团股份有限公司白云山制药总厂CYHB2250121叶酸片华北制药股份有限公司CYHB2450315注射用更昔洛韦浙江亚太药业股份有限公司CYHB2450095
注:灰色字体部分受理号结论为不批准。
3、新增仿制药上市申请药品名称企业名称分类受理号奥沙利铂注射液湖北一半天制药有限公司3CYHS2500879奥沙利铂注射液湖北一半天制药有限公司3CYHS2500878奥沙利铂注射液湖北一半天制药有限公司3CYHS2500877贝美前列素涂剂海南斯达制药有限公司3CYHL2500051苯磺酸氨氯地平口服溶液山东朗诺制药有限公司3CYHS2500880比拉斯汀口崩片江苏和晨药业有限公司3CYHS2500863丙戊酸钠缓释片(Ⅰ)燃点(南京)生物医药科技有限公司;浙江京新药业股份有限公司4CYHS2500848布立西坦口服溶液江苏正大丰海制药有限公司;华益药业科技(安徽)有限公司3CYHS2500876布洛芬缓释胶囊河北山姆士药业有限公司4CYHS2500827醋酸钙口服溶液赤峰源生药业有限公司3CYHS2500871达格列净片浙江京新药业股份有限公司4CYHS2500850达格列净片浙江京新药业股份有限公司4CYHS2500849达格列净片海南倍吉康医药科技有限公司;济南高华制药有限公司4CYHS2500832达格列净片海南倍吉康医药科技有限公司;济南高华制药有限公司4CYHS2500831地奈德软膏湖南明瑞制药股份有限公司3CYHS2500829碘佛醇注射液成都天之翼尚品医药科技有限公司;北京北陆药业股份有限公司4CYHS2500841对乙酰氨基酚布洛芬片南京海纳医药科技股份有限公司;南京海纳制药有限公司3CYHS2500835多种微量元素注射液(Ⅲ)合肥市未来药物开发有限公司;广东星昊药业有限公司4CYHS2500882恩格列净片山东丹红制药有限公司;广州玻思韬控释药业有限公司4CYHS2500838二甲双胍恩格列净片(I)南昌立健药业有限公司4CYHS2500858二甲双胍恩格列净片(Ⅵ)南昌立健药业有限公司4CYHS2500857氟伐他汀钠缓释片北京四环科宝制药股份有限公司4CYHS2500859复方氨基酸注射液(17AA-Ⅲ)武汉滨湖双鹤药业有限责任公司4CYHS2500873复方氨基酸注射液(18AA-Ⅶ)湖北津药药业股份有限公司4CYHS2500826复方聚乙二醇(3350)电解质散合肥盛秦医药科技有限公司;安徽金太阳生化药业有限公司3CYHS2500872复方匹可硫酸钠颗粒山东化药医药科技有限公司;西安远大德天药业股份有限公司3CYHS2500854甘露醇山梨醇注射液南京恩泰医药科技有限公司;江苏大红鹰恒顺药业有限公司3CYHS2500870格列吡嗪控释片天津力生制药股份有限公司4CYHS2500833琥珀酸亚铁片湖南千金湘江药业股份有限公司3CYHS2500883甲磺酸沙非胺片华润赛科药业有限责任公司4CYHS2500837甲硝唑阴道凝胶华控创新(北京)药物研究院有限公司3CYHL2500053间苯三酚口崩片广州帝奇医药技术有限公司;重庆华邦制药有限公司4CYHS2500887间苯三酚口崩片广州帝奇医药技术有限公司;重庆华邦制药有限公司4CYHS2500886聚普瑞锌颗粒烟台万润药业有限公司3CYHS2500839聚乙二醇4000散(儿童型)合肥盛秦医药科技有限公司;安徽金太阳生化药业有限公司3CYHS2500885聚乙烯醇滴眼液四川好医生攀西药业有限责任公司;合肥华威药业有限公司4CYHS2500840卡格列净二甲双胍缓释片浙江华海药业股份有限公司3CYHS2500830克霉唑阴道片浙江华海药业股份有限公司4CYHL2500054利丙双卡因乳膏南京瑞捷医药科技有限公司;杭州领业医药科技有限公司4CYHS2500825联苯苄唑溶液唐山红星药业有限责任公司3CYHS2500881磷酸芦可替尼片江西科伦药业有限公司;湖南科伦制药有限公司4CYHS2500842硫酸氨基葡萄糖胶囊翎耀生物科技(上海)有限公司;上海新亚药业闵行有限公司4CYHS2500884铝镁匹林片(II)河北汇德旭盛医药科技有限公司;河北仁合益康药业有限公司3CYHS2500844氯化钾口服溶液河北华晨药业集团有限公司3CYHS2500843莫匹罗星软膏北京民康百草医药科技有限公司;赤峰赛林泰药业有限公司4CYHS2500892普拉洛芬滴眼液江苏福邦药业有限公司4CYHS2500853乳果糖口服溶液山东泽宇生物有限公司;莱阳市江波制药有限责任公司4CYHS2500875乳果糖口服溶液山东泽宇生物有限公司;莱阳市江波制药有限责任公司4CYHS2500874瑞格列奈片浙江海翔药业股份有限公司4CYHS2500856碳酸氢钠注射液江苏迪赛诺制药有限公司3CYHS2500860吸入用盐酸丙卡特罗溶液海南美康达药业有限公司;立生医药(苏州)有限公司3CYHS2500868吸入用盐酸丙卡特罗溶液海南美康达药业有限公司;立生医药(苏州)有限公司3CYHS2500869盐酸奥洛他定滴眼液亚邦医药股份有限公司4CYHS2500864盐酸贝尼地平片浙江华海药业股份有限公司4CYHS2500865盐酸丙卡特罗吸入溶液江苏万高药业股份有限公司3CYHS2500888盐酸丙卡特罗吸入溶液江苏万高药业股份有限公司3CYHS2500889盐酸毛果芸香碱滴眼液鲁南贝特制药有限公司3CYHL2500052盐酸帕罗西汀片深圳市新阳唯康科技有限公司4CYHS2500828盐酸缬更昔洛韦片仁合益康集团有限公司;河北仁合益康药业有限公司4CYHS2500836盐酸溴己新注射液重庆药友制药有限责任公司3CYHS2500847盐酸溴己新注射液湖北民康药业集团有限公司;湖北美林药业有限公司3CYHS2500834盐酸左沙丁胺醇雾化吸入溶液四川美大康华康药业有限公司3CYHS2500845盐酸左沙丁胺醇雾化吸入溶液四川美大康华康药业有限公司3CYHS2500846伊布替尼片重庆华邦制药有限公司3CYHS2500891伊布替尼片重庆华邦制药有限公司3CYHS2500890依达拉奉右莰醇注射用浓溶液九华华源药业(桂林)有限公司;广东星昊药业有限公司4CYHS2500855蔗糖羟基氧化铁咀嚼片南京正大天晴制药有限公司4CYHS2500851注射用赖氨匹林福安药业集团庆余堂制药有限公司3CYHS2500866注射用赖氨匹林福安药业集团庆余堂制药有限公司3CYHS2500867注射用硫酸多黏菌素B安徽省先锋制药有限公司3CYHS2500852注射用头孢呋辛钠山东鲁抗医药股份有限公司4CYHS2500861注射用头孢呋辛钠山东鲁抗医药股份有限公司4CYHS2500862
4、新增一致性评价补充申报药品名称企业名称受理号丁溴东莨菪碱注射液山东益健药业有限公司CYHB2550131交沙霉素片桂林南药股份有限公司CYHB2550128马来酸氯苯那敏注射液上海锦帝九州药业(安阳)有限公司CYHB2550129马来酸氯苯那敏注射液上海锦帝九州药业(安阳)有限公司CYHB2550130盐酸曲马多缓释片石药集团欧意药业有限公司CYHB2550127注射用哌拉西林钠他唑巴坦钠湘北威尔曼制药股份有限公司CYHB2550126注射用哌拉西林钠他唑巴坦钠湘北威尔曼制药股份有限公司CYHB2550125
新药动态
1、新药上市申请获批药品名称企业名称分类受理号喉喑清胶囊贵州瑞和制药有限公司1.1CXZS2400007
2、新药上市申请受理药品名称企业名称分类受理号A群C群脑膜炎球菌多糖结合疫苗北京智飞绿竹生物制药有限公司3.3CXSS2500029HR-19034滴眼液成都盛迪医药有限公司2.2CXHS2500019Tremelimumab注射液AstraZeneca AB3.1JXSS2500016Tremelimumab注射液AstraZeneca AB3.1JXSS2500015德谷胰岛素注射液杭州中美华东制药有限公司3.3CXSS2500030度伐利尤单抗注射液AstraZeneca UK 3.1JXSS2500013度伐利尤单抗注射液AstraZeneca UK 3.1JXSS2500014亮丙瑞林注射乳剂Accord BioPharma Inc5.1JXHS2500024硫酸氢司美替尼胶囊AstraZeneca UK 2.4JXHS2500025硫酸氢司美替尼胶囊AstraZeneca UK 2.4JXHS2500026泻白颗粒江苏康缘药业股份有限公司3.1CXZS2500008信迪利单抗注射液信达生物制药(苏州)有限公司2.2CXSS2500031伊匹木单抗注射液信达生物医药科技(杭州)有限公司2.2CXSS2500032
数据来源:摩熵医药
一致性评价上市批准
100 项与 亚宝药业四川制药有限公司 相关的药物交易
登录后查看更多信息
100 项与 亚宝药业四川制药有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月08日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
批准上市
1
登录后查看更多信息
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
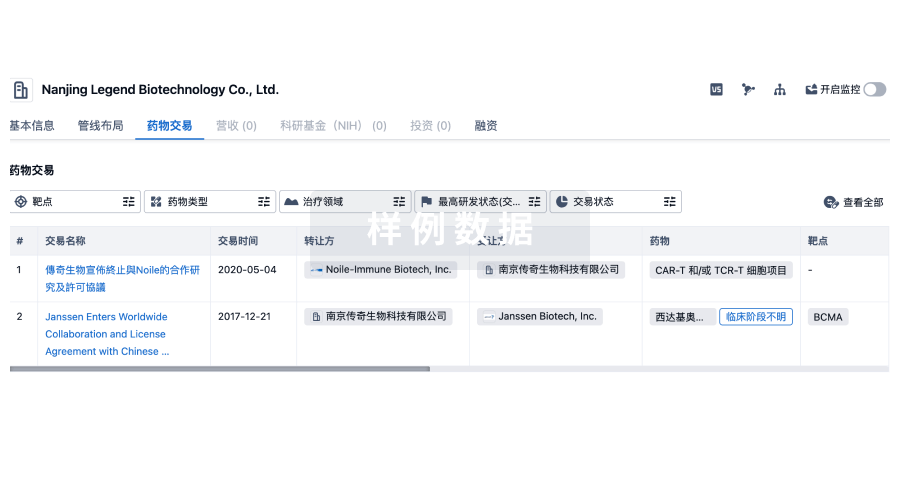
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
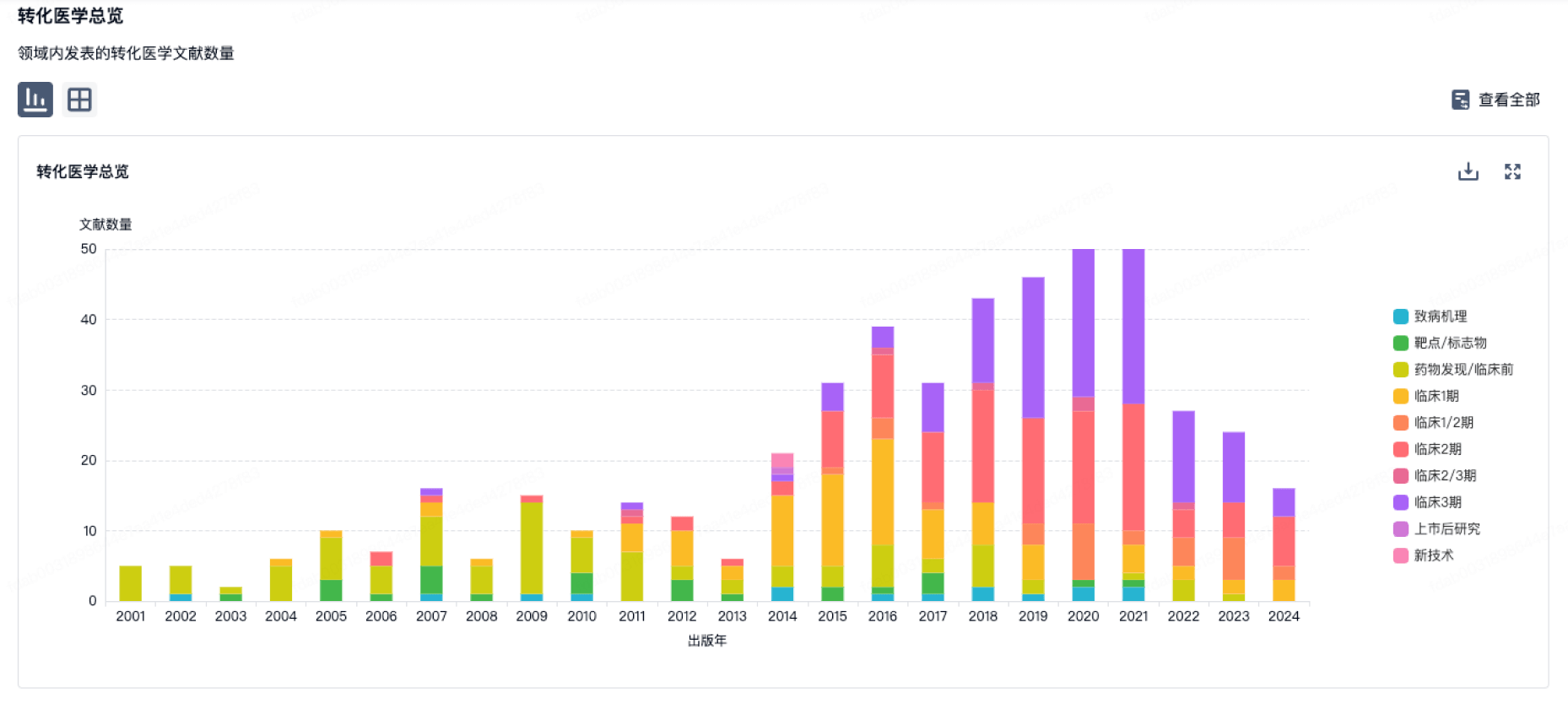
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
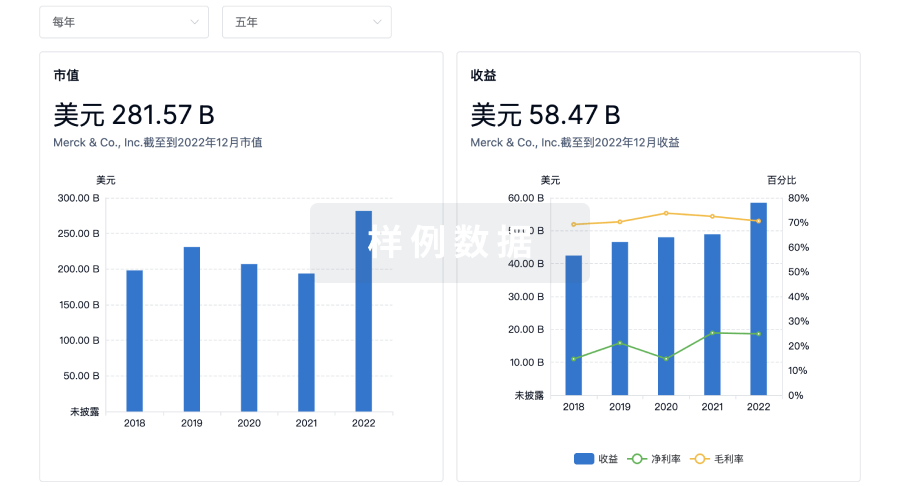
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
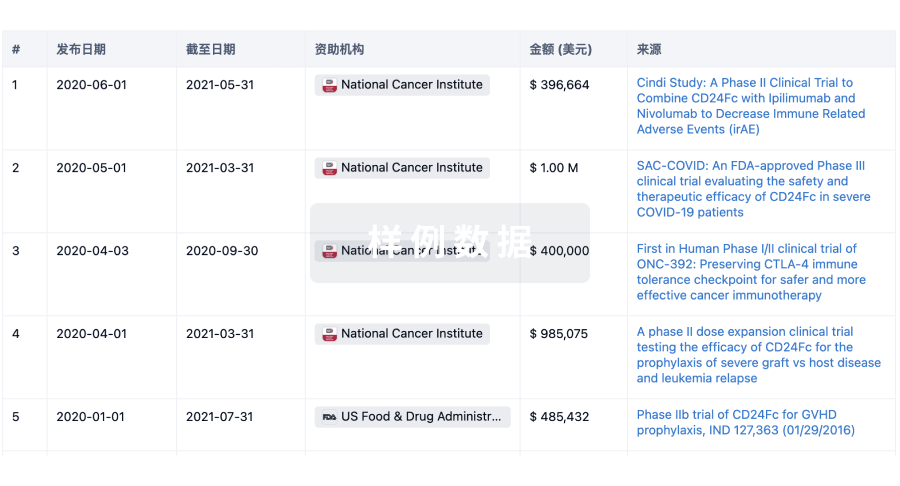
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用