预约演示
更新于:2025-05-07
PD-1 x HPV E6
更新于:2025-05-07
关联
1
项与 PD-1 x HPV E6 相关的药物作用机制 HPV E6抑制剂 [+1] |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症 |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
3
项与 PD-1 x HPV E6 相关的临床试验NCT05357027
A Phase I/II Clinical Trail of TC-E202 Targeting HPV16 E6 for Relapsed/Refractory to Standard Treatment or Metastatic Cervical Carcinoma
Background:
Cervical cancer is the most common gynecologic malignant tumor. The occurrence and progression of cervical carcinoma is firmly relevant to HPV (Human papilloma virus) infection. Cancer cells infected by HPV expressing an HPV protein called E6. E6 is the main factors of HPV 16 carcinogenesis. In TCR-T therapy, researchers take the blood of a certain patient, select T cells and insert genes into the cell that expressing a kind of protein that targeting HPV E6. The genetically engineered cells are called E6 TCR-T cells. The engineered cells are re-infused in the patients with cervical carcinoma.
Objective:
To evaluate the safety and efficacy of TCR-T cells in the treatment of cervical carcinoma.
Eligibility:
Adults aging 18-70 with relapsed/refractory to standard treatment or metastatic cervical carcinoma.
Design:
Patients will have many screening tests, including imaging procedures, heart and lung tests, and lab tests.
Patients will have leukapheresis. Blood will be removed through a needle in the arm. A machine separates the white blood cells. The rest of the blood is returned through a needle in the other arm.
Engineered T cells will be re-infused into the patients will stay in hospital and be evaluated.
Cervical cancer is the most common gynecologic malignant tumor. The occurrence and progression of cervical carcinoma is firmly relevant to HPV (Human papilloma virus) infection. Cancer cells infected by HPV expressing an HPV protein called E6. E6 is the main factors of HPV 16 carcinogenesis. In TCR-T therapy, researchers take the blood of a certain patient, select T cells and insert genes into the cell that expressing a kind of protein that targeting HPV E6. The genetically engineered cells are called E6 TCR-T cells. The engineered cells are re-infused in the patients with cervical carcinoma.
Objective:
To evaluate the safety and efficacy of TCR-T cells in the treatment of cervical carcinoma.
Eligibility:
Adults aging 18-70 with relapsed/refractory to standard treatment or metastatic cervical carcinoma.
Design:
Patients will have many screening tests, including imaging procedures, heart and lung tests, and lab tests.
Patients will have leukapheresis. Blood will be removed through a needle in the arm. A machine separates the white blood cells. The rest of the blood is returned through a needle in the other arm.
Engineered T cells will be re-infused into the patients will stay in hospital and be evaluated.
开始日期2022-08-10 |
申办/合作机构  天科雅 天科雅 [+1] |
100 项与 PD-1 x HPV E6 相关的临床结果
登录后查看更多信息
100 项与 PD-1 x HPV E6 相关的转化医学
登录后查看更多信息
0 项与 PD-1 x HPV E6 相关的专利(医药)
登录后查看更多信息
26
项与 PD-1 x HPV E6 相关的文献(医药)2024-04-01·Cancer Letters
Three-dimensional chromatin analysis reveals Sp1 as a mediator to program and reprogram HPV-host epigenetic architecture in cervical cancer
Article
作者: Wei, Juncheng ; Wei, Ye ; Zhu, Zhixian ; Huang, Xingyu ; Wu, Ping ; Lin, Da ; Zhi, Wenhua ; Huang, Xiaoyuan ; Hong, Ping ; Lin, Shitong ; Ding, Wencheng ; Sung, WingKin ; Xu, Qian ; Ma, Ding ; Cheng, Sheng ; Cao, Canhui ; Chen, Gang ; Xu, Miaochun ; Li, Guoliang ; Cao, Gang ; Peng, Ting ; Meng, Yifan ; Wu, Peng
2023-10-23·International journal of molecular sciences
A Therapeutic DNA Vaccine Targeting HPV16 E7 in Combination with Anti-PD-1/PD-L1 Enhanced Tumor Regression and Cytotoxic Immune Responses.
Article
作者: Gao, Zhixiao ; Zhang, Weifang ; Cheng, Yeping ; Wu, Shuoshuo ; Chen, Jianxing ; Han, Xuechao
2023-08-01·Journal of cancer research and clinical oncology
Molecular markers predicting the progression and prognosis of human papillomavirus-induced cervical lesions to cervical cancer.
Review
作者: Amin, Fatema Alzahraa Samy ; Un Naher, Zeba ; Ali, P. Shaik Syed
38
项与 PD-1 x HPV E6 相关的新闻(医药)2025-04-29
摘要:人乳头瘤病毒(HPV)感染是导致宫颈癌的主要原因,尽管预防性 HPV 疫苗的出现使 HPV 感染率和宫颈癌发病率有所下降,但宫颈癌仍是全球女性中常见的癌症 。本文回顾了宫颈癌疫苗的发展历程,介绍了 HPV 的特性、现有疫苗和治疗方法,以及新型疫苗的研究进展,包括 Accum™技术疫苗、DNA 疫苗、口服疫苗和 mRNA 疫苗等。同时指出,虽然宫颈癌疫苗研究取得了一定成果,但仍需进一步研究优化,以更好地治疗宫颈癌 。一、引言HPV 感染是一种常见的性传播疾病,全球每年有大量新增感染病例 。大多数 HPV 感染可在两年内自行清除,但持续感染可能引发多种疾病,其中约 90% 的宫颈癌由 HPV 感染导致 。自 2006 年预防性 HPV 疫苗在美国上市后,HPV 感染率和宫颈癌诊断率虽有所下降,但宫颈癌仍是全球女性第四大常见癌症 。在低收入和中等收入国家,由于 HPV 疫苗接种和宫颈癌筛查的可及性不足,宫颈癌发病率较高 。因此,持续研究和改进宫颈癌治疗方法至关重要 。二、HPV 的特性目前已发现 200 多种 HPV 毒株,大多数为低风险型,而高危型 HPV-16 和 HPV-18 是导致 70% 宫颈癌的主要原因 。HPV 病毒由环状双链 DNA 构成,分为早期区域(E)、晚期区域(L)和非编码长调控区域(LCR) 。早期区域的 E6 和 E7 基因在致癌过程中起关键作用,E6 抑制肿瘤抑制因子 p53,E7 抑制肿瘤抑制因子 Rb,使感染细胞逃避凋亡并发展为癌细胞 (原文 Figure 1,展示 E6 和 E7 基因抑制肿瘤抑制因子,促使细胞癌变的过程,辅助读者理解 HPV 致癌机制)。此外,HPV 感染细胞可通过上调免疫检查点蛋白(如 PD-L1),形成免疫逃逸微环境,阻碍 T 细胞等免疫细胞发挥作用 。肿瘤形成后,还会招募调节性 T 细胞(Tregs)和髓源性抑制细胞(MDSCs),进一步改变肿瘤微环境,促进肿瘤的免疫逃逸和转移 。三、HPV 疫苗现状目前,全球有六种预防性 HPV 疫苗获批使用,其中 GARDASIL® 和 Cervarix® 较为知名 (原文 Table 1,呈现不同 HPV 疫苗的目标毒株、 efficacy 和 FDA 批准情况,便于读者对比)。GARDASIL® 是四价疫苗,可预防 HPV-6、HPV-11、HPV-16 和 HPV-18 感染;Cervarix® 是二价疫苗,针对 HPV-16 和 HPV-18 。这些疫苗利用 HPV 的 L1 蛋白诱导机体产生特异性抗体,预防感染,效果显著,可降低特定 HPV 毒株感染率达 90% 。然而,它们仅能预防特定毒株,无法提供完全免疫,且需在感染前接种,推荐接种年龄通常为 11 - 12 岁,18 岁后接种效果会明显下降 。因此,即便有了预防性疫苗,宫颈癌的防治仍面临挑战,需要探索更多治疗方案 。四、当前宫颈癌的治疗手段宫颈癌的治疗方法取决于癌症的分期 。早期宫颈癌通常采用手术治疗,但手术可能导致患者生育能力丧失等不良后果 。对于晚期宫颈癌,化疗或放化疗联合是常用的治疗方式 。顺铂是治疗宫颈癌最常用的化疗药物,但化疗会带来脱发、疲劳、恶心呕吐和感染风险增加等副作用 。虽然现有治疗方法取得了一定进展,但仍存在诸多不足,如转移性宫颈癌患者的五年相对生存率仅为 19% 。因此,急需探索更有效的治疗策略 。近年来,免疫治疗药物 pembrolizumab 获批与化疗联合用于宫颈癌治疗,它是一种抗 PD1 抗体,可使 T 细胞绕过 PD-L1 免疫检查点,增强对肿瘤组织的免疫反应,改善治疗效果 。五、疫苗作为治疗手段的合理性鉴于当前宫颈癌治疗的不足,免疫疗法和疫苗治疗为攻克这一难题带来了希望 。HPV 能够抑制肿瘤抑制因子并营造免疫逃逸环境,而疫苗治疗有望针对这些特性发挥作用 。pembrolizumab 的成功应用,以及众多新的和正在进行的研究,为开发新型宫颈癌治疗方法提供了思路,让人们看到了疫苗作为治疗手段的潜力 。六、Accum™技术疫苗癌细胞会将抗体 - 药物结合物隔离在内涵体中并排出细胞,降低治疗效果 。而 Accum™技术通过胆酸和核定位信号,实现内涵体逃逸和核靶向,增加目标物质在细胞内的积累 。Bikorimana 等人研究了基于 Accum-E7(aE7)的蛋白疫苗 。在预防性研究中,给小鼠分别接种 aE7 疫苗、E7 疫苗(无 Accum™技术)和生理盐水作为对照,同时使用 Montanide™ISA720 佐剂 。结果显示,aE7 疫苗组的小鼠未出现肿瘤,而 E7 疫苗组和对照组小鼠的肿瘤持续生长,且 aE7 疫苗组在后续多次癌细胞攻击下仍能保持无瘤状态 ,表明 aE7 疫苗能引发有效的免疫反应预防宫颈癌 。在治疗性研究中,先让小鼠接种宫颈癌细胞系,待出现可触及肿瘤后,再分别用 aE7、E7 和生理盐水进行治疗,部分小鼠还同时注射抗 PD-1、抗 CTLA4 和抗 CD47 等免疫检查点抑制剂 。结果发现,aE7 能抑制肿瘤细胞生长,与抗 CD47 联合使用时效果更显著 ,且联合治疗组小鼠的生存率更高 。第三方的 GLP 研究表明,该疫苗无论剂量和性别差异,都不会引起小鼠体重变化和明显病理变化 。这一系列研究表明,Accum™技术在宫颈癌的预防和治疗方面具有很大的潜力,但还需进一步研究其对其他宫颈癌细胞系的效果以及与更多免疫检查点抑制剂联合使用的情况 。七、DNA 疫苗和腺病毒载体DNA 疫苗通过引入病毒基因组的部分改变氨基酸序列的安全抗原,引发免疫系统的保护性反应 。Han 等人设计了一种编码突变型 HPV-16 E7 的腺病毒载体(Ad-E7) 。由于人体免疫系统对某些腺病毒株(如腺病毒血清型 5)能产生大量中和抗体,使得腺病毒成为递送治疗性疫苗的理想载体 。实验中使用的突变型 HPV-16 E7 缺失了 21 - 24 位氨基酸,降低了 HPV 抑制 Rb 肿瘤抑制因子的能力 。研究人员给接种了宫颈癌细胞系的小鼠分组进行不同处理,包括对照组、Ad-E7 疫苗组、免疫检查点抑制剂(PD-1 或 PD-L1 抗体)组以及 Ad-E7 疫苗与免疫检查点抑制剂联合治疗组 。结果显示,单独使用免疫检查点抑制剂对抑制肿瘤生长没有效果,而 Ad-E7 疫苗能抑制肿瘤生长,联合免疫检查点抑制剂使用时,肿瘤缩小更为明显 。进一步对小鼠的脾脏淋巴细胞和肿瘤组织进行分析发现,Ad-E7 疫苗联合免疫检查点抑制剂能增加 CD8 T 细胞和干扰素 γ 水平,同时降低 Treg 和 MDSC 水平 。对肿瘤组织的 H&E 染色结果表明,该联合治疗还能增加肿瘤包膜厚度,降低毛细血管密度,从而抑制肿瘤生长和转移 。这一研究为 DNA 疫苗用于宫颈癌治疗提供了有力的证据,但还需研究其对其他 HPV 毒株的治疗效果 。八、宫颈癌前疫苗联合治疗DNA 疫苗 GX-188E(tirvalimogene teraplasmid)编码 HPV-16 和 HPV-18 的 E6 和 E7 蛋白,用于治疗宫颈癌前病变 。研究表明,接种该疫苗可使宫颈癌前病变患者受益,可能是因为它能增强 HPV 特异性干扰素 γ 反应 。Youn 等人研究了 GX-188E 疫苗与免疫检查点抑制剂 pembrolizumab 联合治疗复发或晚期宫颈癌的效果 。患者在第 1、2、4、7、13 和 19 周接受 GX-188E 肌肉注射,pembrolizumab 则每三周静脉注射一次,持续两年 。在第 24 周的中期评估中,42% 的患者至少有部分缓解,15% 的患者完全缓解 。虽然这只是中期评估结果且未经过集中审查,但该研究为晚期宫颈癌的治疗提供了新的方向,表明宫颈癌前疫苗联合治疗可能具有良好的应用前景 。九、乳酸杆菌口服疫苗大多数 HPV 治疗性疫苗采用肌肉注射方式,而 Kawana 等人探索了一种表达 HPV-16 E7 的乳酸杆菌口服疫苗 IGMKK16E7 。在双盲、安慰剂对照的随机试验中,选取 HPV-16 阳性的高级别宫颈上皮内瘤变 2 和 3 级的患者,分为安慰剂组、低剂量、中剂量和高剂量 IGMKK16E7 治疗组 ,在第 1、2、4、8 周给予口服治疗。结果显示,高剂量组的组织病理学恢复正常的比例比安慰剂组高 19% ,仅感染 HPV-16 的患者中,高剂量组恢复正常的比例比安慰剂组高 28% ,且恢复正常的比例呈剂量依赖性。此外,恢复较好的患者外周血中产生干扰素 γ 的细胞水平更高,而高剂量组和安慰剂组的不良事件发生率相同 。该研究表明,口服疫苗治疗宫颈癌前病变具有一定的可行性,IGMKK16E7 是首个显示出抗肿瘤效果的口服免疫治疗疫苗,为宫颈癌治疗开辟了新方向,不过相关研究还处于初步阶段,需要进一步探索 。十、mRNA 疫苗mRNA 疫苗在抗击新冠疫情中备受关注 (原文 Figure 2,展示 mRNA 疫苗进入细胞后,经核糖体翻译为蛋白,再通过 MHC 系统引发免疫反应的过程,帮助读者理解其作用机制)。此前,由于未保护的 mRNA 注入体内后易被免疫系统识别和破坏,其应用受到限制 。脂质纳米颗粒技术的出现解决了这一问题,它可以包裹和保护 mRNA,增强其向抗原呈递细胞的递送 。mRNA 疫苗具有高效、开发速度快和安全性良好等优点 。目前,虽然将 mRNA 疫苗用于癌症治疗的研究还处于初步阶段,但多项正在进行的研究显示出了一定的前景,因此有必要进一步探索其在宫颈癌治疗中的应用 。十一、需要持续推进的研究方向宫颈癌疫苗研究虽取得一定进展,但仍有许多方面需要进一步研究(原文 Table 2,总结不同疫苗策略的独特优势,为后续研究方向的讨论做铺垫)。Accum™技术作为疫苗递送工具,需要研究其对其他疫苗配方和 HPV 毒株的适用性,以充分发挥其潜力 。对于 DNA 疫苗,应进一步寻找最有效的突变氨基酸序列,提高癌症治疗效果 。目前针对 HPV 感染和宫颈癌前病变的治疗方法,作为联合治疗方案,需要探究其对晚期宫颈癌的疗效 。口服和基于细菌的疫苗研究处于起步阶段,但已展现出潜力,需要更多研究来深入挖掘 。免疫检查点抑制剂可提高宫颈癌疫苗疗效,但目前 FDA 仅批准 pembrolizumab 用于宫颈癌治疗,且并非所有宫颈癌都依赖 PD-L1 作为免疫检查点,因此需要开发针对其他免疫检查点的抑制剂 。此外,mRNA 疫苗在宫颈癌治疗中的作用也有待充分研究 。十二、结论HPV 疫苗和筛查计划的推行使宫颈癌发病率显著下降,但疫苗仍存在完善空间,且全球部分地区尚未有效实施相关计划 。只要 HPV 未被彻底消除,就需要不断改进宫颈癌的治疗方法 。鉴于 HPV 对宫颈组织的影响,疫苗治疗是一种理想的手段 。新型疫苗研究取得了一定进展,如 Accum™技术、腺病毒载体、口服疫苗和 mRNA 疫苗等,但要充分发挥宫颈癌疫苗的治疗潜力,仍需大量研究工作 。识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观不本站。
疫苗信使RNA免疫疗法
2025-01-30
一、核酸疫苗的科学基础
核酸疫苗的核心是利用基因编码技术,将肿瘤特异性抗原的遗传信息传递给人体细胞,激活免疫系统精准攻击癌细胞。与传统疫苗(如灭活病毒或重组蛋白疫苗)不同,核酸疫苗不需要体外培养抗原,而是利用人体细胞直接生产抗原,模拟自然感染过程,触发更强的免疫反应。1. DNA疫苗的工作原理
递送与表达:DNA疫苗以质粒形式递送(质粒是一种环状DNA分子),进入细胞核后,利用宿主细胞的转录机制生成mRNA,再翻译为抗原蛋白(图1)。
图示:DNA疫苗需突破细胞膜、核膜双重屏障,依赖宿主转录机制。
免疫激活路径:抗原蛋白通过蛋白酶体降解为肽段,与MHC I类分子结合后呈递至细胞表面,激活CD8+ T细胞(杀伤性T细胞),直接摧毁癌细胞。分泌型抗原还可通过MHC II类分子激活CD4+ T细胞(辅助T细胞),增强抗体产生。2. mRNA疫苗的快速响应机制
绕过细胞核:mRNA疫苗无需进入细胞核,直接在细胞质中翻译成抗原蛋白,省去转录步骤,速度更快(图2)。
图示:mRNA疫苗的简化路径使其开发周期短至数周。
天然佐剂效应:mRNA中的未修饰核苷酸可激活细胞内的TLR7/8受体,释放干扰素等信号分子,增强树突状细胞成熟和抗原呈递。
二、核酸疫苗的设计优化:从实验室到临床的关键突破
1. DNA疫苗的三大改进方向(1)质粒设计优化
启动子选择:强效启动子(如CMV)确保高表达,组织特异性启动子(如前列腺特异性抗原PSA)减少脱靶效应。案例:pTVG-HP疫苗使用CMV启动子驱动PAP抗原表达,用于前列腺癌治疗。
多抗原串联:单质粒编码多个抗原(如HPV的E6/E7蛋白),覆盖肿瘤异质性。案例:VGX-3100疫苗靶向HPV16/18的E6/E7基因,治疗宫颈癌前病变。
免疫佐剂整合:添加CpG基序(激活TLR9)或细胞因子基因(如GM-CSF),增强免疫应答。数据:含CpG的DNA疫苗在小鼠模型中抗体滴度提升10倍(Science, 2018)。(2)递送技术革新
电穿孔技术:通过短暂高压电脉冲打开细胞膜,提升DNA递送效率。设备:Inovio的CELLECTRA®系统,脉冲参数(电压、时长)可针对不同组织优化。临床数据:电穿孔使DNA疫苗免疫原性提升100倍(NCT03600350试验)。
脂质纳米颗粒(LNP):可离子化脂质(如DLin-MC3-DMA)在酸性条件下带正电,封装DNA;进入细胞后释放。案例:ZyCoV-D(COVID-19 DNA疫苗)使用LNP递送,有效性达67%。(3)联合疗法增效
免疫检查点抑制剂:PD-1/PD-L1抗体逆转T细胞耗竭,与DNA疫苗协同增效。案例:pTVG-HP联合PD-1抑制剂,客观缓解率(ORR)从12%提升至28%。
化疗/放疗:释放肿瘤抗原,增强疫苗效果。案例:WOKVAC疫苗联合紫杉醇,乳腺癌患者T细胞浸润增加3倍。2. mRNA疫苗的四大创新(1)结构工程:从稳定性到翻译效率
5'帽修饰:CleanCap®技术合成天然三磷酸帽(m7GpppN),提升翻译效率。对比:未加帽mRNA翻译效率下降90%(Nature, 2020)。
密码子优化:替换低频密码子(如CTA→CTG),匹配宿主tRNA库。案例:Moderna的mRNA-4157优化后抗原表达量提升50%。
UTR设计:借用高表达基因(如β-珠蛋白)的UTR序列,延长mRNA半衰期。数据:优化UTR使mRNA稳定性从6小时延长至72小时(Cell, 2021)。(2)递送系统:从肝靶向到肿瘤特异性
LNP配方演进:
第一代:DLin-MC3-DMA(Onpattro®),肝靶向性强,用于遗传病治疗。
第二代:SM-102(Moderna COVID-19疫苗),肺和肿瘤靶向性提升。
第三代:可降解脂质(如LP01),降低肝毒性(临床前数据)。
靶向修饰策略:
抗体偶联:抗EGFR抗体-LNP靶向实体瘤(小鼠模型显示肿瘤mRNA表达量提升10倍)。
电荷调控:阳离子脂质体靶向带负电荷的肿瘤血管。(3)个性化新抗原疫苗
设计流程:肿瘤测序→新抗原预测→mRNA合成→LNP封装→个体化接种。案例:BioNTech的iNeST平台,单疫苗编码20种新抗原,覆盖90%肿瘤克隆。
临床突破:Moderna的mRNA-4157针对34种新抗原,III期试验中黑色素瘤复发风险降低44%。(4)通用型疫苗开发
共享新抗原库:通过AI预测高频突变(如KRAS G12D、TP53 R175H),覆盖多癌种。案例:Gritstone的SLATE疫苗靶向20种公共新抗原,30%实体瘤患者适用。三、临床进展:从早期试验到III期突破1. DNA疫苗的里程碑案例(1)前列腺癌:pTVG-HP的十年征程
机制:靶向前列腺酸性磷酸酶(PAP),激活CD8+ T细胞。
II期试验(NCT01341652):
联合GM-CSF,62%患者产生PAP特异性T细胞。
中位无进展生存期(PFS)延长6个月(18 vs 12个月)。
联合PD-1抑制剂(NCT04090528):
客观缓解率(ORR)达28%,显著高于单药(12%)。(2)宫颈癌:VGX-3100的非手术革命
III期REVEAL试验:
入组193例HPV16/18阳性宫颈高级别鳞状上皮内病变(HSIL)。
结果:37%患者病灶完全消退(vs 9%安慰剂组),无需子宫切除。
优势:避免手术创伤,保留生育功能。
2. mRNA疫苗的临床突破(1)黑色素瘤:mRNA-4157的突破
KEYNOTE-942试验设计:
157例术后高危患者,随机接受mRNA-4157 + Keytruda或单药Keytruda。
终点:无复发生存期(RFS)。
结果:
联合组18个月RFS率82%(vs 64%)。
复发风险降低44%(HR=0.56)。
意义:首个获FDA“突破性疗法”认证的个性化mRNA疫苗。(2)胰腺癌:新抗原疫苗的曙光
个体化疫苗试验(NCT04161755):
16例可切除胰腺癌患者,疫苗联合化疗 + PD-1抑制剂。
结果:50%患者术后18个月无复发(历史对照<20%)。
机制:疫苗诱导的新抗原特异性T细胞浸润肿瘤微环境。
四、技术挑战与创新解决方案1. 递送效率的瓶颈(1)DNA疫苗的穿透难题
细胞核屏障:<5%的胞质DNA能进入核内。
解决方案:
核定位信号(NLS)肽段融合:SV40大T抗原NLS提升核转运效率。
微针阵列:经皮递送绕过肌肉屏障,直接靶向皮肤DC。(2)mRNA的肝靶向偏好
问题:LNP天然富集肝脏,降低肿瘤抗原表达。
策略:
电荷调控:中性LNP(如Acuitas ALC-0315)减少肝摄取。
组织特异性配体:叶酸修饰靶向肺癌(叶酸受体高表达)。2. 稳定性的现实困境(1)mRNA的热稳定性突破
冻干技术:CureVac的CVnCoV疫苗可在5°C稳定3个月。
核苷修饰:1-甲基假尿苷(m1Ψ)减少水解,半衰期延长至7天(37°C)。(2)DNA疫苗的长期储存
冻干制剂:Inovio的INO-4800(COVID-19疫苗)室温稳定1年。
超螺旋质粒优化:去除开环DNA,提升稳定性(>90%超螺旋率)。3. 肿瘤免疫抑制微环境(1)髓系抑制细胞(MDSC)的干扰
机制:MDSC分泌IL-10和TGF-β,抑制T细胞功能。
对策:
联合CSF1R抑制剂:阻断MDSC招募(临床前模型显示T细胞活性恢复70%)。
疫苗编码CD40L:激活DC,逆转免疫抑制。(2)T细胞耗竭
表观遗传重编程:DNMT抑制剂(地西他滨)恢复T细胞效应基因(如IFN-γ)表达。
代谢调控:补充谷氨酰胺增强T细胞线粒体功能。五、未来方向:从技术创新到全球可及1. 下一代技术平台(1)自扩增RNA(saRNA)
原理:借用甲病毒复制酶,低剂量(1/10常规mRNA)即可长效表达抗原。
案例:Arcturus的LUNAR-COV19疫苗,单剂免疫原性等同两剂Moderna。(2)环状RNA(circRNA)
优势:无5'/3'端,抗核酸酶降解,室温稳定。
进展:Orna Therapeutics的circRNA-LNP疫苗,临床前肿瘤模型显示持久免疫应答。2. 通用型疫苗开发(1)共享新抗原库
AI预测平台:
工具:NetMHCpan + DeepHLA预测高频新抗原(如KRAS G12D)。
案例:Gritstone的SLATE疫苗靶向20种公共新抗原,覆盖>30%实体瘤患者。(2)病毒载体整合
腺病毒载体:Oxford/AstraZeneca的ChAdOx1平台,携带多抗原表达盒。
优势:单次免疫激发强T细胞应答(如COVID-19疫苗)。3. 可及性与公平性(1)低成本生产技术
无细胞合成:酶法合成DNA(如Touchlight的doggybone DNA),避免细菌发酵。
连续流工艺:mRNA合成时间从7天缩短至8小时(如Synthego微流控系统)。(2)全球合作网络
WHO mRNA技术转移中心:南非、阿根廷等6国本地化生产mRNA疫苗。
开放专利池:MPP(药品专利池)授权中低收入国家生产COVID-19疫苗技术。六、总结:癌症治疗的新纪元
核酸疫苗通过基因编码的精准性,正在重塑癌症治疗格局。尽管面临递送效率、稳定性和成本挑战,但随着技术创新(如LNP优化、AI设计)和全球合作推进,未来十年或将实现“一针定制,终身防癌”的愿景。从实验室到病床,这场基因驱动的抗癌革命,终将让癌症从“绝症”变为可管理的慢性病。
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观,不代表本站立。
疫苗信使RNA
2025-01-29
摘要:癌症疫苗作为免疫治疗的关键组成部分,分为预防性和治疗性两类。预防性疫苗(如HPV和HBV疫苗)通过阻断致癌病毒感染显著降低癌症发病率,而治疗性疫苗通过激活树突状细胞(DC)和细胞毒性T淋巴细胞(CTL)诱导持久的抗肿瘤免疫应答。近年来,合成肽、mRNA、DNA、细胞疫苗及纳米疫苗等平台的创新显著提升了抗原递送效率和免疫激活能力。尽管美国食品药品监督管理局(FDA)已批准多款疫苗,但由于肿瘤抗原异质性、免疫抑制微环境及递送系统优化等挑战,其治疗潜力尚未完全释放。本文系统综述了癌症疫苗的分类、新抗原发现、递送平台进展、佐剂作用机制及联合疗法的协同效应,并探讨了临床转化中的关键挑战与未来方向。
癌症疫苗的研发始于19世纪末,William B. Coley观察到细菌毒素可诱导肿瘤消退,首次揭示了免疫系统与癌症的关系。20世纪80年代,BCG疫苗被用于膀胱癌治疗,成为首个获批的治疗性癌症疫苗。2010年,Sipuleucel-T的上市标志着个性化免疫治疗的突破。近年来,基因工程技术的进步(尤其是mRNA疫苗)在胶质母细胞瘤和黑色素瘤中展现出显著潜力。例如,靶向EB病毒的mRNA疫苗WGc-043和针对黑色素瘤的mRNA-4157已在临床试验中取得积极成果。然而,肿瘤抗原异质性、免疫抑制微环境及递送效率仍是主要挑战。
图1 治疗性癌症疫苗的免疫反应机制
描述:疫苗通过递送肿瘤抗原至DC,激活CTL和CD4+ Th1细胞,诱导肿瘤细胞杀伤。APC(抗原呈递细胞)通过MHC分子呈递抗原,触发T细胞受体(TCR)信号通路。预防性与治疗性疫苗预防性疫苗
HPV疫苗:覆盖HPV 16/18等高危亚型,降低宫颈癌、肛门癌及口咽癌发病率。临床数据显示,接种后宫颈癌前病变发生率下降60%-90%。需与常规细胞学筛查联合应用。
HBV疫苗:通过阻断乙肝病毒感染,降低肝细胞癌风险。全球范围内接种率提升使肝癌发病率显著下降。治疗性疫苗
治疗性疫苗需满足以下关键特性:
高效抗原递送:优先选择肿瘤特异性新抗原(如EGFRvIII、KRAS突变),避免自身免疫毒性。
克服免疫抑制微环境:TME中的调节性T细胞(Treg)和髓源性抑制细胞(MDSC)可抑制DC功能,需联合佐剂(如TLR激动剂)增强DC活性。
持续免疫记忆:通过激活记忆T细胞,防止肿瘤复发。肿瘤抗原的选择共享抗原(TAAs)
TAAs在肿瘤和正常组织中均有表达,如CEA(结直肠癌)、PSA(前列腺癌)和MUC1(乳腺癌)。早期临床试验中,CEA疫苗在结直肠癌患者中诱导免疫应答,但疗效短暂。AFP肽疫苗在肝细胞癌中部分患者实现完全缓解,提示TAAs的潜力与局限性。肿瘤特异性抗原(TSAs)
TSAs由肿瘤突变产生,如EGFRvIII(胶质母细胞瘤)、RAS突变(胰腺癌)及p53突变(多种实体瘤)。新抗原的筛选依赖于:
全外显子测序(WES)和RNA测序:识别体细胞突变及表达水平。
质谱技术(MS):精确检测免疫肽段,减少预测算法误差。
生物信息学工具:NetMHCpan等算法预测抗原与MHC结合亲和力。
表1 新抗原疫苗临床案例
疫苗平台1. 合成肽疫苗
短肽疫苗(8-15氨基酸):如gp100疫苗联合高剂量IL-2,客观缓解率(ORR)达42%。但需佐剂(如Poly-ICLC)增强免疫原性。
长肽疫苗(20-30氨基酸):如HPV E6/E7长肽疫苗在宫颈癌中耐受性良好,诱导强效T细胞应答。
多价肽疫苗:NEO-PV-01联合PD-1抑制剂在黑色素瘤中ORR达35%,显著优于单药治疗。2. 核酸疫苗
DNA疫苗:INO-5401编码hTERT和WT1抗原,联合PD-1抑制剂在胶质瘤中延长生存期。
mRNA疫苗:mRNA-4157联合Pembrolizumab在黑色素瘤III期试验中降低44%复发风险。脂质纳米颗粒(LNP)递送系统提升稳定性,如BNT122在胰腺癌中激活多克隆T细胞。3. 细胞疫苗
自体肿瘤细胞疫苗:GVAX通过分泌GM-CSF募集DC,但单药疗效有限。联合化疗或免疫检查点抑制剂可增强响应。
DC疫苗:Sipuleucel-T通过体外负载PAP抗原延长前列腺癌患者生存期(中位OS 25.8 vs 21.7个月)。DCVax-L负载肿瘤裂解物,在胶质瘤中5年生存率提升至13%。4. 病毒疫苗
溶瘤病毒:T-VEC(表达GM-CSF)在黑色素瘤中客观缓解率25.2%,中位OS 41.1个月。
病毒样颗粒(VLP):VBI-1901靶向CMV抗原,在复发性胶质瘤中中位OS达12.9个月。5. 纳米疫苗
脂质体/介孔二氧化硅:增强抗原递送至淋巴结,激活DC和CTL。如dClip-LNP/siRNA纳米疫苗通过沉默TIM-3增强抗肿瘤免疫。
自组装纳米结构:CS-TEMPO-OVA纳米疫苗联合PD-1抑制剂抑制黑色素瘤转移。
图2 纳米疫苗作用机制
描述:纳米载体共递送抗原和佐剂至淋巴结,促进DC成熟及T细胞活化。佐剂的作用机制免疫刺激剂
TLR激动剂:
TLR3激动剂(Poly-ICLC)诱导IFN-β和IL-12,增强抗原交叉呈递。
TLR4激动剂(MPL)激活NF-κB通路,促进Th1极化。
细胞因子:IL-12和GM-CSF增强T细胞增殖,但需平衡疗效与毒性(如IL-2引发毛细血管渗漏综合征)。递送系统
脂质纳米颗粒(LNP):保护mRNA免受降解,如Moderna的mRNA-5671靶向KRAS突变。
可降解聚合物(PLGA):控释抗原,延长免疫应答。
表2 佐剂分类及代表疫苗
联合疗法1. 化疗联合
化疗诱导免疫原性细胞死亡,释放肿瘤抗原。
案例:SurVaxM(靶向Survivin)联合替莫唑胺在胶质母细胞瘤中延长无进展生存期(PFS 11.4个月)。2. 放疗联合
放疗增强肿瘤抗原释放并改变TME。
案例:PSA靶向疫苗联合放疗在前列腺癌中显著提升抗原特异性T细胞数量。3. 免疫检查点抑制剂(ICI)联合
疫苗逆转T细胞耗竭,ICI阻断PD-1/PD-L1通路。
案例:mRNA-4157联合Pembrolizumab在黑色素瘤中ORR达50%,降低复发风险44%。4. CAR-T联合
疫苗增强CAR-T持久性与肿瘤浸润。
案例:CLDN6 mRNA疫苗联合CAR-T在实体瘤中实现33%客观缓解率。
图3 联合疗法机制示意图
描述:疫苗与化疗、放疗、ICI或CAR-T协同,通过多通路激活抗肿瘤免疫。临床挑战
1.抗原筛选与个性化制备:新抗原预测需结合基因组学与免疫肽组学,成本高且周期长。
动物模型局限性:人源化小鼠难以完全模拟人类免疫系统,需开发类器官或芯片替代模型。
不良反应管理:
常见:注射部位反应、发热、疲劳。
严重:细胞因子释放综合征(CRS)、自身免疫性毒性。
耐药机制:肿瘤抗原丢失或MHC下调可导致免疫逃逸。结论与展望
癌症疫苗通过多平台创新与联合策略展现出变革性潜力。未来方向包括:
精准新抗原筛选:结合AI优化预测算法,降低成本。
新型递送系统:开发靶向淋巴结或穿透血脑屏障的纳米载体。
克服免疫抑制:联合TME调控剂(如TGF-β抑制剂)或表观遗传药物。
临床转化加速:利用器官芯片替代部分动物试验,缩短研发周期。
随着mRNA技术和个性化医疗的突破,癌症疫苗有望成为“治愈性疗法”的重要组成部分,为实体瘤和血液肿瘤患者带来长期生存希望。
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观,不代表本站立。
疫苗信使RNA免疫疗法临床研究
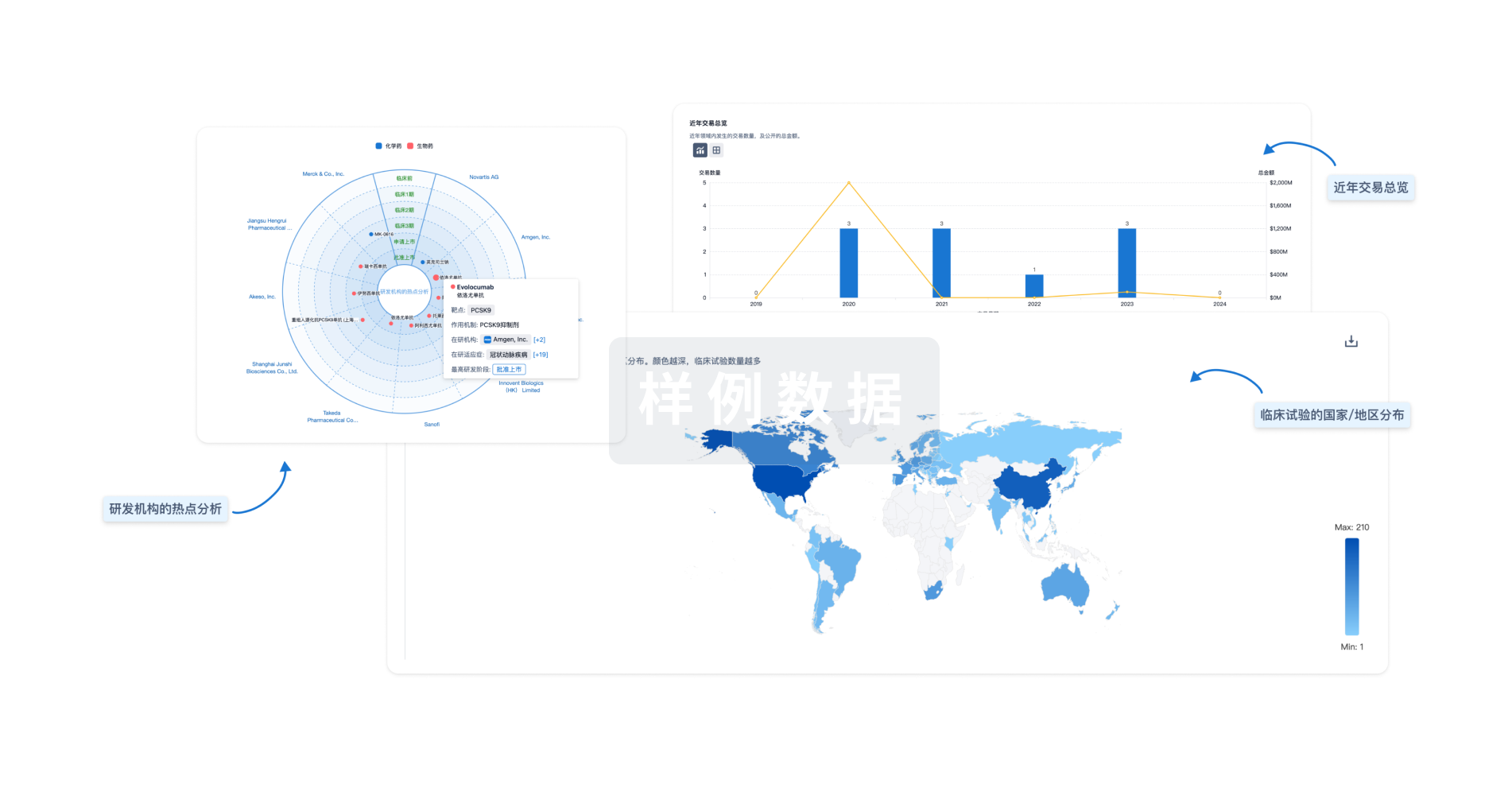
分析
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
