预约演示
更新于:2025-05-07
DNMT3B
更新于:2025-05-07
基本信息
别名 DNA (cytosine-5)-methyltransferase 3B、DNA methyltransferase 3 beta、DNA methyltransferase HsaIIIB + [3] |
简介 Required for genome-wide de novo methylation and is essential for the establishment of DNA methylation patterns during development. DNA methylation is coordinated with methylation of histones. May preferentially methylates nucleosomal DNA within the nucleosome core region. May function as transcriptional co-repressor by associating with CBX4 and independently of DNA methylation. Seems to be involved in gene silencing (By similarity). In association with DNMT1 and via the recruitment of CTCFL/BORIS, involved in activation of BAG1 gene expression by modulating dimethylation of promoter histone H3 at H3K4 and H3K9. Isoforms 4 and 5 are probably not functional due to the deletion of two conserved methyltransferase motifs. Functions as a transcriptional corepressor by associating with ZHX1. Required for DUX4 silencing in somatic cells (PubMed:27153398). |
关联
2
项与 DNMT3B 相关的药物靶点 |
作用机制 DNMT3B inhibitors |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
靶点 |
作用机制 DNMT3B inhibitors |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
100 项与 DNMT3B 相关的临床结果
登录后查看更多信息
100 项与 DNMT3B 相关的转化医学
登录后查看更多信息
0 项与 DNMT3B 相关的专利(医药)
登录后查看更多信息
2,501
项与 DNMT3B 相关的文献(医药)2025-12-31·Epigenetics
SIRT1/DNMT3B-mediated epigenetic gene silencing in response to phytoestrogens in mammary epithelial cells
Article
作者: Boycott, Cayla ; Stefanska, Barbara ; Yang, Tony ; Zhang, Jiaxi ; Ma, Yuexi ; Gomilar, Rekha
2025-12-01·Journal of Clinical Immunology
Investigation of Transcription Factor and Cytokine Gene Expression Levels in Helper T Cell Subsets Among Turkish Patients Diagnosed with ICF2 (Novel ZBTB24 gene Variant) and ICF3 (CDCA7 Variant) Syndrome
Article
作者: Kuccukturk, Serkan ; Gul, Yahya ; Reisli, Ismail ; Guner, Sukru Nail ; Karaselek, Mehmet Ali ; Sahin, Ali ; Duran, Tugce ; Keles, Sevgi
2025-06-01·Poultry Science
The landscape of RNA 5-methylcytosine modification during chicken embryonic myogenesis
Article
作者: Li, Wenwei ; Liao, Zurong ; Liu, Sanfeng ; Mao, Huirong ; Wang, Zikun ; Jiang, Hongxia ; Wang, Yuxiang ; Xiao, Xiaoyun ; Chen, Biao ; Liu, Jing ; Liang, Jingzhan ; Huang, Xvwen ; Hu, Xiaolong ; Xu, Jiguo ; Ding, Zhenxvan
20
项与 DNMT3B 相关的新闻(医药)2025-01-16
·小药说药
关注小药说药,一起成长!
前言
遗传和表观遗传变化都是癌症发生、肿瘤进展和转移的重要因素。从广义上讲,癌症的发病率与生物/遗传年龄直接相关。DNA甲基化是一种重要的表观遗传调控机制,在生命周期中不断变化,是“表观遗传衰老”过程的重要组成部分。值得注意的是,最近的研究已经证实表观遗传衰老在肿瘤发生中起主要作用。
表观遗传学改变通过影响广泛组织学中的多种致癌基因与抑癌基因途径,以及通过影响免疫细胞(如T细胞和NK细胞)的激活、分化和功能从而促进癌症的发生。事实上,最近的一项研究表明,正是组织环境诱导的表观遗传编程启动了肿瘤发生,这些发现为表观遗传药物的应用提供了强有力的理论基础,不仅可以作为癌症治疗药物,还可以用于预防癌症,因为它们可以协同靶向“正常”细胞,包括免疫细胞和癌前细胞。
基于表观遗传学的治疗旨在调节影响免疫细胞、其他正常细胞和/或癌细胞中各种信号通路的转录编程,从而影响这些细胞群体的命运。表观遗传药物是作用于细胞表观基因组以发挥其功能的化学物质,这些药物包括DNA甲基转移酶(DNMT)、DNA去甲基酶、组蛋白去乙酰化酶(HDAC)、组蛋白乙酰转移酶(HATs)、组蛋白甲基转移酶(HMT)、组蛋白去甲基酶(HDMs)和其他相关酶的抑制剂。此外,microRNA(miRNA)和长非编码RNA(lncRNAs)也是多种关键生物过程的重要表观遗传介质,包括致癌和免疫反应,这是有效癌症治疗的两个关键靶点。
表观遗传途径
DNA甲基化
DNA甲基化作为一种主要的表观遗传学标记,可通过有丝分裂遗传,并参与稳定基因转录抑制,尤其是当其位于哺乳动物基因转录起始点附近时。研究的最深入的DNA共价修饰是5-甲基胞嘧啶(5mC),这是一种由DNMT催化的标记。
在哺乳动物基因组中,5mC主要存在于CpG二核苷酸中,人类基因组中2800万CpG二核苷酸中70–80%的CpG被甲基化。在哺乳动物中,发现了三种活跃的DNMT,分别命名为DNMT1、DNMT3a和DNMT3b。
组蛋白乙酰化
组蛋白可以经历多种形式的翻译后修饰(PTMs),包括乙酰化、甲基化、磷酸化、泛素化以及ADP核糖基化、磺酰化和瓜氨酸化。这些组成所谓的“组蛋白密码”,调节染色质结构、重塑酶的募集和基因活动的调节。
组蛋白赖氨酸残基的乙酰化影响基因组的组织和功能。组蛋白H3和H4的乙酰化由两组酶决定:HATs和组HDAC。这两组酶决定组蛋白的乙酰化状态,并以可逆方式工作。
在人类中,有18种HDAC酶分为四类:Rpd3样蛋白的I类(HDAC1、HDAC2、HDAC3和HDAC8);类Hda1蛋白的II类(HDAC4、HDAC5、HDAC6、HDAC7、HDAC9和HDAC10);Sir2样蛋白的III类(SIRT1、SIRT2、SIRT3、SIRT4、SIRT5、SIRT6和SIRT7)和第四类蛋白质(HDAC11)。这些酶及其在癌症中的功能已被广泛研究。
组蛋白甲基化
组蛋白甲基化是表观遗传修饰的第三种主要类型。为了完成这一可逆过程,涉及两大类催化甲基加成的酶:蛋白质精氨酸甲基转移酶(PRMT)和组蛋白赖氨酸甲基转移酶(HKMT)。癌症环境中的关键赖氨酸和精氨酸甲基转移酶包括zeste同源物2(EZH2)、G9a、DOT1L以及PRMTs 1和5。另一组称为组蛋白去甲基酶的酶逆转这一过程。
组蛋白磷酸化
磷酸化是另一种高度动态的组蛋白PTM形式。它发生在丝氨酸、苏氨酸和酪氨酸残基上,主要发生在组蛋白N端尾部,受激酶和磷酸酶的竞争作用控制。作为“组蛋白代码”的重要组成部分,PTM在DNA损伤修复、染色质致密化、转录调控以及包括肿瘤发生和癌症进展在内的一系列生物学过程中起着关键作用。
肿瘤微环境的表观遗传调节
肿瘤微环境(TME)由多种细胞类型组成。除肿瘤细胞外,TME还包含多种非上皮细胞类型,包括构成血管系统的细胞(内皮细胞、周细胞和平滑肌细胞)、参与免疫监测的细胞(淋巴细胞、巨噬细胞和肥大细胞)以及基质细胞(即成纤维细胞),这些细胞在细胞外基质(ECM)中,分泌一系列可扩散生长因子、细胞因子和趋化因子。人们早就认识到,癌症发生促进以促血管生成生长因子表达、ECM表达改变、成纤维细胞增殖加速和炎性细胞浸润增加为特征的基质变化。
TME的表观遗传改变控制着组织缺氧状态,并在细胞对缺氧的反应和癌细胞代谢中起着关键作用。表观遗传调控因子可与缺氧诱导转录因子(HIF)家族基因协同工作,在HIF依赖性启动后很长时间内维持缺氧适应的细胞表型。表观遗传变化稳定HIF与其转录靶点的结合,从而影响直接HIF反式激活后的组蛋白去甲基化酶活性,并最终导致缺氧TME中组蛋白修饰和DNA甲基化的整体模式,JMJD1A表达的低氧上调作为信号放大器促进低氧基因表达,最终促进肿瘤生长。
巨噬细胞是TME中的关键固有免疫细胞,它们在TME中调节原发性肿瘤生长、血管生成、转移扩散和肿瘤对介入治疗的反应。在巨噬细胞中,缺氧减弱了Jumonji组蛋白去甲基化酶活性的表达,导致组蛋白H3K9甲基化增加和趋化因子表达降低,从而导致TME内免疫景观的变化。
免疫细胞的表观遗传调节
表观遗传机制在免疫细胞分化和功能中发挥关键作用,确保在不同组织微环境条件下免疫细胞中恰当的基因表达模式。重要的是,表观遗传机制在TME内的免疫细胞和基质细胞类型中起着决定性作用。
固有免疫细胞(髓系细胞和NK细胞)
髓系细胞在适应性免疫系统识别癌细胞中发挥重要作用,并协调炎症和保护性抗肿瘤免疫反应的启动。这些细胞包括粒细胞、单核细胞、巨噬细胞、中性粒细胞、DC和MDSC。
DC细胞启动并协调针对感染和疾病的适应性免疫反应,它们是免疫记忆和免疫耐受发展的核心。树突状细胞迅速整合来自其组织微环境的信号,并相应地对这些信号作出反应,这种动态变化依赖于DC细胞染色质结构的表观遗传变化。
在巨噬细胞中,其功能极化状态需要对靶基因表达进行精确的时间和情境调节。在M1和M2极化期间,表观遗传变化在改变细胞信号和特征基因图谱中发挥作用。
MDSCs在肿瘤形成过程中被诱导,它们介导有效的肿瘤促进活动。研究表明,在肿瘤相关培养基存在的情况下,MDSCs的基因组中存在广泛的去甲基化和某些特殊位点的DNA甲基化,这些和免疫抑制特征的特异性基因增加有关。此外,许多研究表明,组蛋白修饰的表观遗传途径调节MDSCs的各个方面。例如,HDAC11是一种新的表观遗传调节因子,在肿瘤相关的MDSC中调节细胞的扩增和功能。
NK细胞在免疫监视和消除应激、感染或转化细胞方面发挥着重要作用。对于NK细胞,H3K4me3去甲基化酶Kdm5a是细胞激活所必需的。此外,慢性刺激的NK细胞在被肿瘤靶点重新激发时表现出功能紊乱,这些无能的NK细胞表现出特定的表观遗传重编程模式,DNA甲基化发生全基因组改变。
CD4+T细胞
表观遗传学机制在Th1和Th2细胞的细胞分化和功能中起着关键作用。STAT4和STAT6转录因子在辅助性T细胞分化过程中的表观遗传修饰和转录调节中起着调控作用。研究发现,STAT4在促进活跃的表观遗传标记方面具有更为显著的作用,而STAT6在对抗抑制性标记方面具有更为显著的作用。
对于T滤泡辅助细胞(Tfh)细胞,已经证明VHL-HIF-1α轴在通过糖酵解表观遗传重编程启动Tfh细胞发育过程中起着重要作用。EZH2是一种HMT,催化H3K27me3并主要通过HMT活性影响Th1、Th2和Treg细胞。研究表明,EZH2敲除会损害Tfh分化和转录编程的激活。
Treg细胞
Treg细胞的发育严重依赖于FoxP3,FoxP3的表达是最佳Treg抑制活性所必需的,过去几十年的研究表明,增强子区CpG岛的DNA甲基化控制着T细胞中FoxP3的表达。此外,TET-甲基胞嘧啶双加氧酶对Treg细胞的功能稳定性也至关重要。一系列研究证明了TET在维持Treg细胞中稳定的FoxP3表达中的关键作用。
EZH2在Treg细胞中的重要性也得到了证实。EZH2对Treg的分化和T效应细胞的扩张都至关重要,通过遗传或药理学手段破坏Treg细胞中的EZH2活性,导致肿瘤浸润性Treg细胞获得促炎功能,重塑TME,增强CD8+和CD4+效应T细胞的募集和功能,从而消除肿瘤。
CD8+T细胞
基因表达的表观遗传调控在获得和维持CD8+T细胞的效应器功能,以及记忆性CD8+T细胞对抗原再激发的快速而稳健的反应中起着关键作用。表观遗传机制也影响CD8+T细胞的干性及其命运。
组蛋白乙酰化通过效应分子的差异表达促进CD8+T细胞快速而稳健的记忆反应。与原始CD8+T细胞相比,记忆CD8+T细胞中效应基因H3赖氨酸9乙酰化(H3K9Ac)显著提高。此外,HDAC3已被确定为CD8+T细胞效应器分化和细胞毒性潜能的表观遗传调节因子。
肿瘤细胞和免疫分子的表观遗传调节
癌细胞的代谢重编程是公认的癌症标志,这已成为调节抗肿瘤免疫反应的关键免疫抑制机制。代谢重编程和表观遗传重编程是相互关联的,并且在很大程度上,代谢状态决定了癌症的表观遗传学。
糖酵解或氧化磷酸化等代谢途径在炎症和组织修复过程中调节巨噬细胞功能,α-酮戊二酸通过代谢和表观遗传重编程协调巨噬细胞活化至M2表型。糖酵解增强也被确定影响骨桥蛋白基因表达的表观遗传修饰。最终,TME内的代谢条件加强了癌细胞和免疫细胞的表观遗传重编程,导致免疫抑制性微环境,然而,这些表观遗传修饰表现出可通过表观遗传调节剂纠正的可塑性。
在分子水平上,已知与免疫功能(STING)、CD8+细胞毒性T细胞(GzmB、IFN-γ、IL-2、IL-12)和FOXP3+Treg细胞相关的关键效应分子通过表观遗传途径进行调节。事实上,许多细胞因子和趋化因子在癌症中通过表观遗传途径调节。
免疫检查点分子(ICMs)包括程PD-1、CTLA-4、TIM-3、LAG-3以及TIGIT。这些分子及其受体在癌细胞和免疫细胞表面的表达,或其可溶性分泌形式,可帮助肿瘤细胞逃避免疫监视。表观遗传机制在调节TME中ICMs及其受体的表达中起着关键作用。作为一个具体的例子,LAG-3 DNA甲基化与肿瘤和免疫细胞中该免疫检查点分子的表达相关,影响透明细胞肾细胞癌中免疫细胞浸润的命运。
表观遗传靶向药物
表观遗传药物经常与其他免疫刺激剂联合使用,以实现五个目标:1)癌细胞生长停滞;2)诱导肿瘤细胞死亡(通过凋亡、坏死、自噬);3)促进肿瘤相关新抗原的表达以提高免疫细胞识别能力;4.)缺氧逆转和肿瘤血管生成抑制;以及5)TME中免疫细胞(DC、T细胞等)功能的调节。
目前,大量涉及表观遗传调控途径的小分子酶抑制剂或激活剂正被开发用于临床。许多表观遗传药物已获得监管机构批准用于治疗人类恶性肿瘤。
2004年,FDA批准5-azaC(商品名Vidaza)用于骨髓增生异常综合征(MDS)的所有五个阶段,随后于2006年批准了5-aza-dC。这两种药物目前代表了干细胞疗法不适用时MDS的一线疗法。它们也被应用于慢性粒单核细胞白血病(CMML)和AML的治疗。
一些HDAC抑制剂(HDACi)也已获得FDA批准用于临床。Vorinostat和romidepsin是这类药物中最早被批准用于治疗皮肤T细胞淋巴瘤(CTCL)的药物。SAHA,也称为Zolinza或Vorinostat,于2006年获得FDA批准,目前是CTCL患者的第三线治疗选择。Romidepsin是2009年FDA批准的第二种HDAC抑制剂。随后,Belinostat和Panobinostat以及Chidamine均被批准用于治疗复发或难治性外周T细胞淋巴瘤(PTCL)或多发性骨髓瘤。
FDA药品批准的第三波浪潮发生在过去几年中。2017年和2018年,异柠檬酸脱氢酶1和2(IDH1/2)抑制剂Enasidenib和Ivosidenib分别被批准用于治疗复发或难治性AML。最后,在2020年,FDA加速批准了tazemetostat,一种EZH2的抑制剂,用于治疗上皮样肉瘤和复发/难治性滤泡性淋巴瘤。
表观遗传药物的临床前景
到目前为止,除了少数类型的实体瘤、T细胞淋巴瘤、上皮样肉瘤和难治性滤泡性淋巴瘤外,表观遗传学药物在晚期肿瘤中通常无法证明足够的疗效,从而无法获得FDA或其他监管机构的批准。
然而,一些关于实体瘤的临床研究显现出有希望的前景。首先,Tazemetostat是第一类抑制剂的代表,对两种实体瘤有效。单药治疗显示出有临床意义的、持久的反应,并且在经多次治疗的复发性或难治性滤泡性淋巴瘤患者或晚期上皮样肉瘤患者中普遍具有良好的耐受性。
其次,两种或两种以上的表观遗传药物的组合可能是提高治疗抗肿瘤疗效的一个很好的选择。在一项研究中,证明了azacitidine和romidepsin与IFN-α的联合具有很高的治疗潜力,其靶向的是结直肠癌最具侵袭性的细胞成分(即转移细胞和癌干细胞),并调节关键的生存和死亡途径(包括肿瘤ICD)。在另一项研究中,研究人员评估了使用azacitidine和entinostat对复发性转移性非小细胞肺癌患者的联合治疗,在一些难治性NSCLC患者中显示出客观、持久的反应。
此外,在临床前研究中,已报道EZH2抑制剂可增强ICIs的抗肿瘤反应。在一个病例报告中,一名使用EZH2抑制剂(tazemetostat)治疗的SMARCB1阴性脊索瘤患者对放疗的持续全身反应超过2年。功能分析显示,CD8+ T细胞和Treg细胞的肿瘤内和间质浸润显著增加,与T细胞上PD-1和LAG-3检查点分子的表达增强有关。这些结果表明EZH2抑制促进持续的抗肿瘤免疫反应,导致免疫检查点激活。新出现的临床数据也表明,表观遗传药物和ICIs的联合疗法有望用于一系列实体癌患者。
目前,有多项表观遗传药物和ICIs联合治疗的临床试验正在进行中。
小结
令人信服的证据表明,表观遗传调控影响癌细胞、免疫细胞、基质细胞、癌细胞和免疫细胞之间的相互作用以及免疫TME的状态。因此,作为一种干预手段,表观遗传调节本身可以诱导强大的抗肿瘤免疫。
因此,进一步增强免疫治疗效果的一个合理策略是将某些表观遗传调节因子与一种或多种经典免疫治疗方案相结合,如癌症疫苗、ICIs、溶瘤病毒、CAR-T细胞、TCR-T细胞或其他新型免疫刺激剂。表观遗传药物可以诱导ICD并使肿瘤由冷变热,它们可能与其他免疫治疗方案产生协同作用。未来,这些联合治疗方案可能在临床研究中显示出良好的应用前景。
参考文献:
1.Epigenetic modulation of antitumor immunityfor improved cancer immunotherapy. Mol Cancer. 2021; 20: 171.
公众号内回复“ADC”或扫描下方图片中的二维码免费下载《抗体偶联药物:从基础到临床》的PDF格式电子书!
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
寡核苷酸核酸药物
2024-09-19
·今日头条
【导读】
放疗是前列腺癌(PCa)的治疗手段,但放疗耐药严重影响其疗效。失调的RNA剪接因子广泛参与肿瘤进展。尽管如此,剪接因子在前列腺癌放射耐药中的作用在很大程度上仍未被探索。
9月17日,中山大学研究团队在期刊《Advanced Science》上发表了研究论文,题为“PTBP1 Regulates DNMT3B Alternative Splicing by Interacting With RALY to Enhance the Radioresistance of Prostate Cancer”,本研究在多个公开的前列腺癌数据库中,识别出23个在前列腺癌和相邻正常组织之间表达差异显著的剪接因子。在这些基因中,PTBP1在前列腺癌中显著上调,与高级别临床病理特征和不良预后呈正相关。功能获得和丧失实验表明,PTBP1显著增强了基因组DNA的稳定性,从而使前列腺癌细胞在体外和体内对辐射产生耐药。机制上,PTBP1与RALY相关的异染色质核糖核蛋白(hnRNP)相互作用,并调节DNA甲基转移酶3b(DNMT3B)第5外显子的剪接,从DNMT3B-S剪接到DNMT3B-L。此外,DNMT3B-L的上调导致DUSP2的启动子甲基化,进而抑制DUSP2的表达,从而增强前列腺癌的辐射耐药性。这些发现强调了剪接因子在响应放疗时诱导异常剪接事件中的作用,并指出了PTBP1和DNMT3B-L在逆转前列腺癌辐射耐药性方面的潜在作用。
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202405997
背景知识
01
电离辐射通过引起基因组DNA损伤有效地消除肿瘤细胞。因此,放疗已成为治疗各种癌症,特别是前列腺癌(PCa)的广泛使用的致突变细胞杀伤治疗方法,前列腺癌是男性第二大肿瘤相关死亡原因。值得注意的是,放疗是局限性PCa的治愈性治疗,也已获准作为手术后的辅助治疗、生物化学复发后的补救治疗,甚至在存在远处转移的情况下作为姑息治疗。不幸的是,尽管放疗在治疗PCa方面取得了成功,但由于辐射耐药的出现,仍有近30-50%的患者在原发或转移部位长期复发或短期内病情恶化。因此,迫切需要阐明辐射耐药的分子机制。
选择性剪接(AS)是真核细胞中一种受到严格调控的转录后细胞过程,它增加了真核生物的蛋白质多样性。统计数据显示,人类超过95%的基因会发生AS,癌症中的AS事件比正常组织多达30%,这有助于产生参与肿瘤发生的多种基因变异。一般来说,AS的调控主要依赖于跨膜剪接因子,它们能够特异性地识别和结合内在的CIS元件。在多种人类恶性肿瘤中异常表达这些剪接因子会导致剪接重编程,从而促进肿瘤进展和包括放射耐受在内的治疗耐药。因此,有针对性地靶向异常剪接因子可能会开辟癌症治疗的新途径。然而,目前尚不清楚异常剪接和相应的剪接因子是否参与了前列腺癌的辐射耐药。
PTBP1增强PCa细胞体外增殖和放疗耐受性
02
为了确定PTBP1在PCa细胞中的功能作用,研究人员通过PTBP1-靶向siRNAs或慢病毒转染建立DU145和PC-3细胞的PTBP1敲低(KD)或过表达(OE)模型。CCK-8实验结果表明,PTBP1敲低显著抑制PCa细胞的细胞活力,而PTBP1过表达则表现出相反的效果。此外,克隆形成实验进一步强化了PTBP1的促增殖作用。同时,实验结果还表明,PTBP1在调控细胞群体处于S期方面发挥着重要作用。这些结果表明,PTBP1可能有助于细胞周期中DNA复制阶段的正常进展。
据报道,PTBP1参与DNA损伤修复,这是放射治疗耐药的主要原因之一。为了研究PTBP1在辐射响应中的潜在作用,研究人员将PTBP1敲除或过表达的PCa细胞暴露于不同剂量的辐射。克隆形成试验表明,PTBP1敲除显著降低了PCa细胞在辐射后的克隆形成,而PTBP1过表达增加了PCa细胞对辐射治疗的耐药。此外,当暴露于4 Gy的辐射时,PTBP1敲除显著增加了PCa细胞的凋亡比例,而PTBP1过表达PCa细胞在4 Gy辐射后的生存潜力大于对照组细胞。为了进一步研究PTBP1是否影响辐射诱导的基因组不稳定性,研究人员对PTBP1敲除或过表达的PCa细胞在辐射后0、1、24小时的DNA损伤情况进行了彗星试验。与对照PCa细胞相比,PTBP1-KD PCa细胞在24小时后呈现出更长的彗星尾,而PTBP1-OE PCa细胞在24小时后呈现出较短的彗星尾。同时,蛋白质免疫印迹实验分析显示,在4 Gy IR治疗后不同时间点,PTBP1敲除的PCa细胞中γ-H2AX蛋白水平升高,而PTBP1过表达的PCa细胞中该蛋白水平降低,与各自的对照PCa细胞相比。这些结果表明,PTBP1在促进PCa细胞增殖和放疗耐药方面发挥着重要作用。
PTBP1通过维持遗传稳定性来促进前列腺癌细胞对放疗的耐药
为了进一步阐明DNMT3B-L如何调控DUSP2,研究人员首先基于TCGA数据评估了DUSP2启动子和5'-上游区域的CpG甲基化状态。此外,体外实验表明,5-aza-2'-脱氧胞苷(5-Aza)是一种DNA甲基化抑制剂,可剂量依赖性地显著增加DUSP2的mRNA和蛋白质水平,进一步证实DUSP2表达可通过DNA甲基化进行调控。研究人员通过在线软件设计了一对覆盖三个CpG位点的甲基化和非甲基化引物。MSP实验结果却表明,DNMT3B-L KD显著减少了使用甲基化引物时产生的PCR产物数量,但相反地增加了使用非甲基化引物时产生的PCR产物数量。为了调查DUSP2是否对PTBP1和DNMT3B-L介导的辐射耐药产生不可忽视的影响,研究人员进行了挽救实验。结果显示,DUSP2 siRNAs显著恢复了PTBP1或DNMT3B-L KD细胞的辐射耐药。同时,DUSP2 KD显著减少了PTBP1或DNMT3B-L KD细胞中由IR引起的DNA损伤。总之,这些数据表明,PTBP1通过DNMT3B-L介导的DUSP2启动子甲基化促进PCa的辐射耐药。
研究小结
03
总之,研究人员通过系统性分析PCa中的剪接因子,识别出PTBP1为一种致癌蛋白。在RALY的帮助下,PTBP1能够与DNMT3B的前mRNA结合,驱动DNMT3B的致癌剪接切换,产生DNMT3B-L,进而诱导DUSP2的启动子甲基化,从而增强癌细胞对放疗的耐药性。
本研究为异常剪接因子调节PCa的放疗耐药机制提供了新的见解,并发现PTBP1是前列腺癌放疗增敏的潜在治疗靶点。
【参考资料】
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202405997
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
热门推荐活动 点击免费报名
🕓 北京|09月20日-21日
▶ 第五届单细胞技术应用研讨会暨空间组学前沿研讨会
🕓 上海|11月15日-16日
▶ 2024第一届中国类器官转化医学大会
点击对应文字 查看详情
放射疗法
2024-06-30
·生物探索
引言
从古至今,无论是秦始皇派出去寻找长生不老药的徐福,还是野史流传甚广的唐太宗李世民毒死于不老丹药,亦或是现如今科学家们对于衰老的不懈研究,长生不老或逆转衰老一直是人类亘古不变的追求。随着现代医学和生物学的发展,科学家对于衰老已经有了非常深入地认知,其中端粒和端粒酶的作用逐渐突显出来。端粒是位于染色体末端保护DNA不受降解并防止染色体黏连和重组的一段区域。当细胞发生分裂时,端粒都会略微缩短。因此,端粒的长短是细胞能否继续分裂的一个限制因素,端粒过短时导致细胞停止分裂,进入衰老状态。目前的研究发现,端粒的异常缩短与多种老年相关疾病有关,端粒功能障碍与细胞衰老、组织功能下降和机体老化密切相关【1-3】。其实,生物体也能表达端粒酶,在端粒末端添加DNA,从而对抗端粒的自然缩短。然而,在大多数体细胞中,端粒酶的活性较低或不活跃,但在干细胞、生殖细胞和癌细胞中,端粒酶通常较为活跃,有助于这些细胞保持增殖能力。由于端粒酶功能的重要性,越来越多的被看作是抗衰老研究的关键靶点。
2024年6月21日,来自美国得克萨斯大学MD安德森癌症研究中心的Ronald A. DePinho课题组在Cell上发表了研究论文TERT activation targets DNA methylation and multiple aging hallmarks。在本研究中,作者通过大规模小分子药物筛选,发现了一种化合物TAC可以高效诱导端粒酶逆转录酶TERT的表达,TAC显示出了在延缓衰老和改善神经退行中的重要临床价值。
端粒酶是一种核糖核蛋白复合物,其转录活性在正常体细胞内受到严格调控,这主要是由于端粒酶的核心催化亚基端粒酶逆转录酶(TERT)的转录抑制所致。强制表达TERT可以通过促进端粒合成和调节衰老相关基因表达来逆转衰老【4-6】。如果能筛选出诱导TERT表达的化合物,那么这种化合物很可能就是一款“长生不老药”。基于此,作者开发了一种高通量筛选方法,可以大规模筛选调节成年小鼠耳成纤维细胞中人类TERT转基因转录活性的小分子药物。通过筛选超过65万中小分子化合物,作者发现TAC(本文中命名为TERT激活剂化合物)可以最高水平的诱导TERT表达,TAC的处理可以改写TERT基因上游转录抑制状态。更加重要的是,TAC的腹腔注射可以在转基因小鼠多个组织中诱导人类TERT基因的表达,而且TAC的诱导效果在其他衰老模型中也得到的验证。这些结果表明TAC是一种可以有效激活TERT表达的小分子化合,腹腔注射和多组织高效性预示着TAC可能作为一种逆转衰老的特效药用于临床研究。
随后,为了揭示TAC诱导TERT表达的机制,作者首先使用磷酸化激酶阵列分析了激酶及其底物的磷酸化谱。研究发现,在人类原代MRC-5细胞中,ERK及其下游效应因子S6激酶的磷酸化在TAC处理后持续增加,抑制ERK激酶活性可以 TAC的诱导作用。转录组分析表明TAC处理上调了AP-1转录复合物的主要组成成分FOS基因的表达,有趣的是在TERT基因上游含有两个AP-1结合位点。当缺失这两个AP-1结合位点后,TAC的诱导作用受到了显著抑制,并且AP-1的抑制剂也显示出类似的结果。这些数据表明,TAC通过MEK/ERK/AP-1途径特异性的激活了TERT基因的转录活化。
在明确了TAC的作用机制后,作者想要继续探究TAC是否能在体外减轻自然老化小鼠的机体衰老。腹腔注射TAC后,作者分析了其在血浆中暴露水平,确定了TAC的药代动力学特性。值得注意的是,TAC在中枢神经系统中的浓度大约是血浆的两倍,说明其能有效穿透血脑屏障。对TAC处理后小鼠的多个衰老指标进行分析后发现,老化基因特征(如细胞周期停滞和PML体等)有所减少;衰老相关分泌表型(SASP)的关键驱动因子p16INK4a的表达被抑制,同时激活了生长和自然杀伤细胞活化的标志;负责p16INK4a启动子高甲基化的DNMT3b表达显著减少;SASP诱导的促炎因子IL-1β和IL-6的产生减少等。这些发现表明,TAC可能作为一中潜在的抗衰老治疗药物,通过激活TERT和改变衰老相关基因表达模式来延缓衰老。
最后,由于TAC能穿透血脑屏障,暗示了其在神经系统中可能发挥重要作用。因此,作者详细分析了TAC处理对大脑的影响。他们发现,TAC通过激活TERT不仅改善了海马依赖的认知功能,还增强了神经肌肉功能,而且没有明显的不良后果。这些研究指出了一种可能性,即通过药物手段激活TERT可以作为一种潜在的策略来延缓老化过程中的神经退行和认知衰退。
研究模式图(Credit: Cell)
总的来说,这篇文章发现了一种小分子化合物TAC可以激活TERT的表达,揭示了TAC发挥作用的分子机制,并且提出了TAC 在逆转衰老中的诸多作用。这些发现对于开发延缓甚至逆转衰老的治疗策略提供非常有价值的见解。
参考文献
1. Lo ́ pez-Otı ́n, C., Blasco, M.A., Partridge, L., Serrano, M., and Kroemer, G. (2013). The hallmarks of aging. Cell 153, 1194–1217.
2. Chakravarti, D., LaBella, K.A., and DePinho, R.A. (2021). Telomeres: history, health, and hallmarks of aging. Cell 184, 306–322.
3. Sahin, E., and DePinho, R.A. (2010). Linking functional decline of telomeres, mitochondria and stem cells during ageing. Nature 464, 520–528.
4. Bodnar, A.G., Ouellette, M., Frolkis, M., Holt, S.E., Chiu, C.P., Morin, G.B., Harley, C.B., Shay, J.W., Lichtsteiner, S., and Wright, W.E. (1998). Extension of life-span by introduction of telomerase into normal human cells. Science 279, 349–352.
5. Toma ́ s-Loba, A., Flores, I., Ferna ́ ndez-Marcos, P.J., Cayuela, M.L., Maraver, A., Tejera, A., Borra ́ s, C., Matheu, A., Klatt, P., Flores, J.M., et al. (2008). Telomerase reverse transcriptase delays aging in cancer-resistant mice. Cell 135, 609–622.
6. Bernardes de Jesus, B., Vera, E., Schneeberger, K., Tejera, A.M., Ayuso, E., Bosch, F., and Blasco, M.A. (2012). Telomerase gene therapy in adult and old mice delays aging and increases longevity without increasing cancer. EMBO Mol. Med. 4, 691–704.
https://doi.org/10.1016/j.cell.2024.05.048
责编|探索君
排版|探索君
文章来源|“BioArt”
End
往期精选
围观
一文读透细胞死亡(Cell Death) | 24年Cell重磅综述(长文收藏版)
热文
Cell | 是什么决定了细胞的大小?
热文
Nature | 2024年值得关注的七项技术
热文
Nature | 自身免疫性疾病能被治愈吗?科学家们终于看到了希望
热文
CRISPR技术进化史 | 24年Cell综述
分析
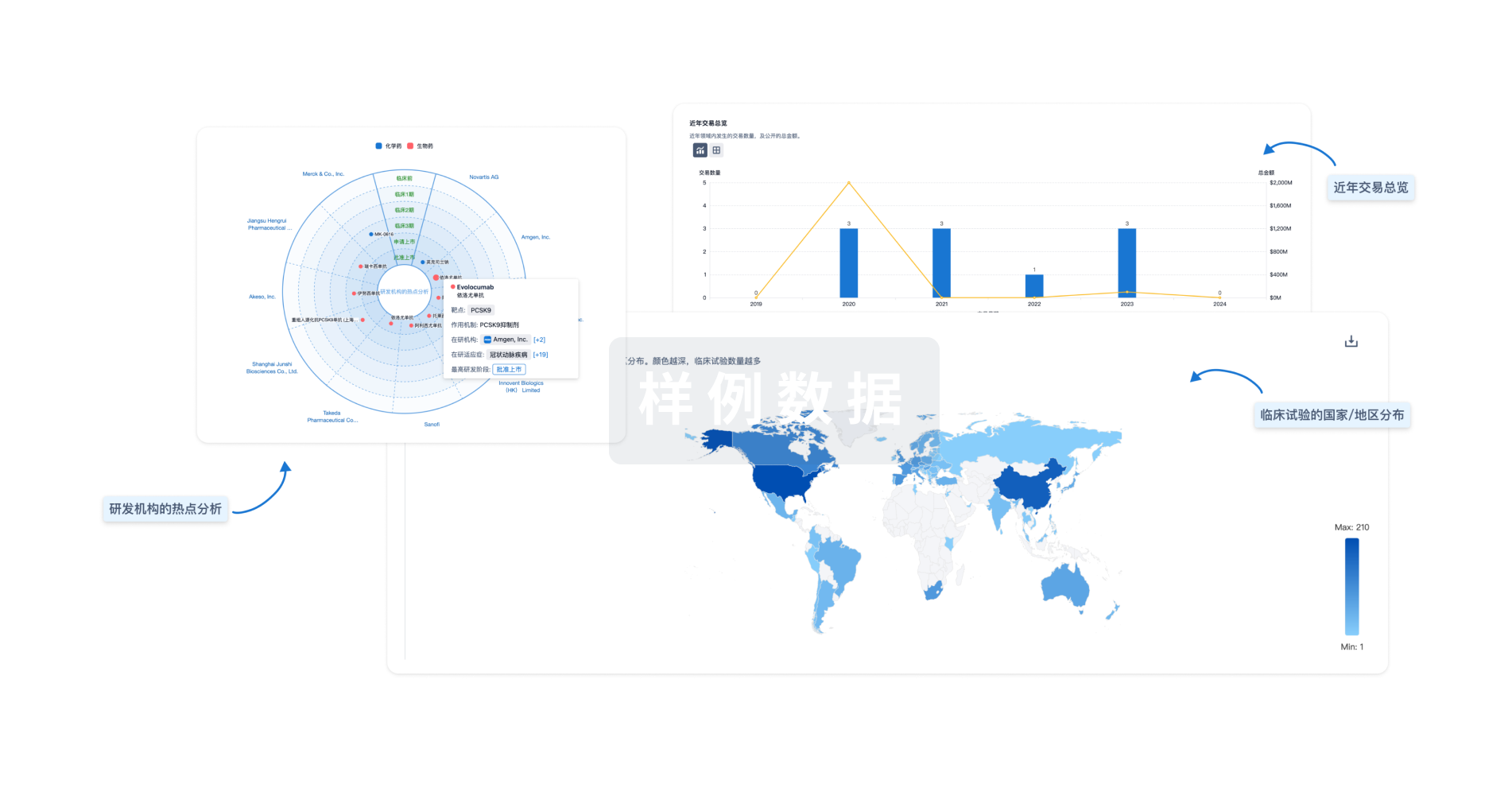
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

