索元生物基因疗法DB107临床2期试验获FDA批准,治疗神经胶质瘤
2023年8月1日,索元生物宣布,美国FDA已批准其基因疗法DB107的临床2期试验。该临床试验由全球脑瘤领域知名研究机构:加州大学旧金山分校(UCSF)、加州大学圣迭戈分校(UCSD)以及南加州大学(USC)的研究者共同发起,将验证全新生物标志物DGM7作为预测性生物标志物指导下,DB107治疗高级别神经胶质瘤(HGG)的有效性。
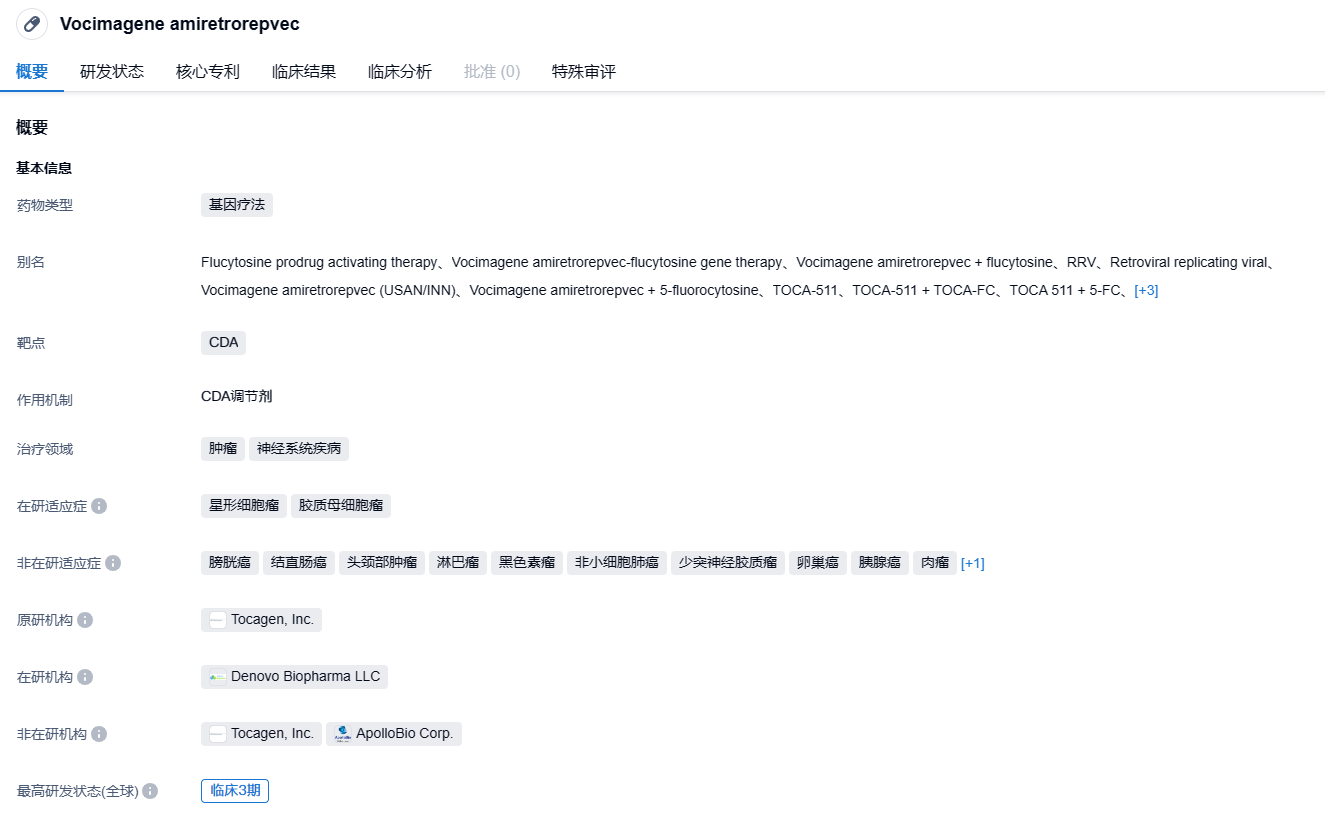
DB107是索元生物从Tocagen公司获得的一种新型组合基因疗法,它包括基因治疗载体Toca 511和小分子化疗药Toca FC。Toca 511是一种逆转录病毒复制载体(RRV),能够选择性地感染癌症细胞,将胞嘧啶脱氨酶(CD)的基因选择性地递送入癌细胞,这意味着被感染的癌细胞会选择性携带CD基因并产生CD。Toca FC是一种口服前延长释放药5-氟胞嘧啶(5-FC),当它遇到CD时,它能够转化成抗癌药物5-氟尿嘧啶(5-FU)。5-FU能直接杀死癌细胞和免疫抑制性骨髓细胞,从而激活免疫系统对抗癌症并消灭肿瘤。2020年,索元生物从Tocagen收购了DB107及其RRV基因治疗平台。经过一年多的探索,索元生物发现DGM7可作为DB107的预测性生物标志物。
研究发现,在DB107试验组中,DGM7阳性的患者的总体生存率显著优于DGM7阴性患者,同时也显著优于采用标准治疗的患者。DGM7有望作为作为伴随诊断识别出DB107的潜在获益人群,拯救这部分复发性GBM患者的生命。此前,在Tocagen使用DB107针对复发性高级别神经胶质瘤的国际3期临床试验中,DB107表现出良好的安全性及耐受性,但在整体人群中DB107并没有显现出优于标准疗法的药效。此次DB107重新进入临床阶段,如能确认DB107对DGM7生物标志物阳性患者的疗效,将使得这些患者大幅获益。
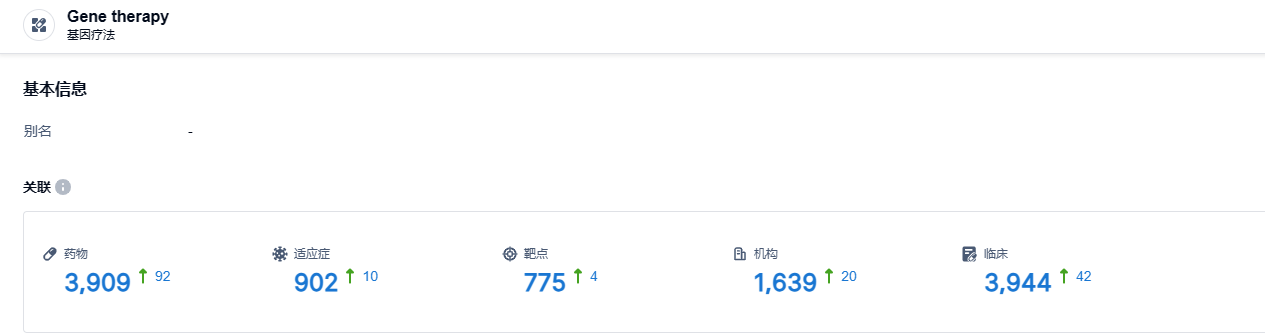
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 基因疗法 药物类型注册登录后可免费获得该药物类型下的在研药物、适应症、靶点、研发机构、临床试验等详细信息),截止到 2023 年8月3日,基因疗法这一药物类型共有在研药物3909个,包含的适应症有902种,靶点775个,在研机构1639家,涉及相关的临床试验3944件……期待DB107的后续表现。