预约演示
更新于:2026-04-16
Vortosiran
更新于:2026-04-16
概要
基本信息
原研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床申请 |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
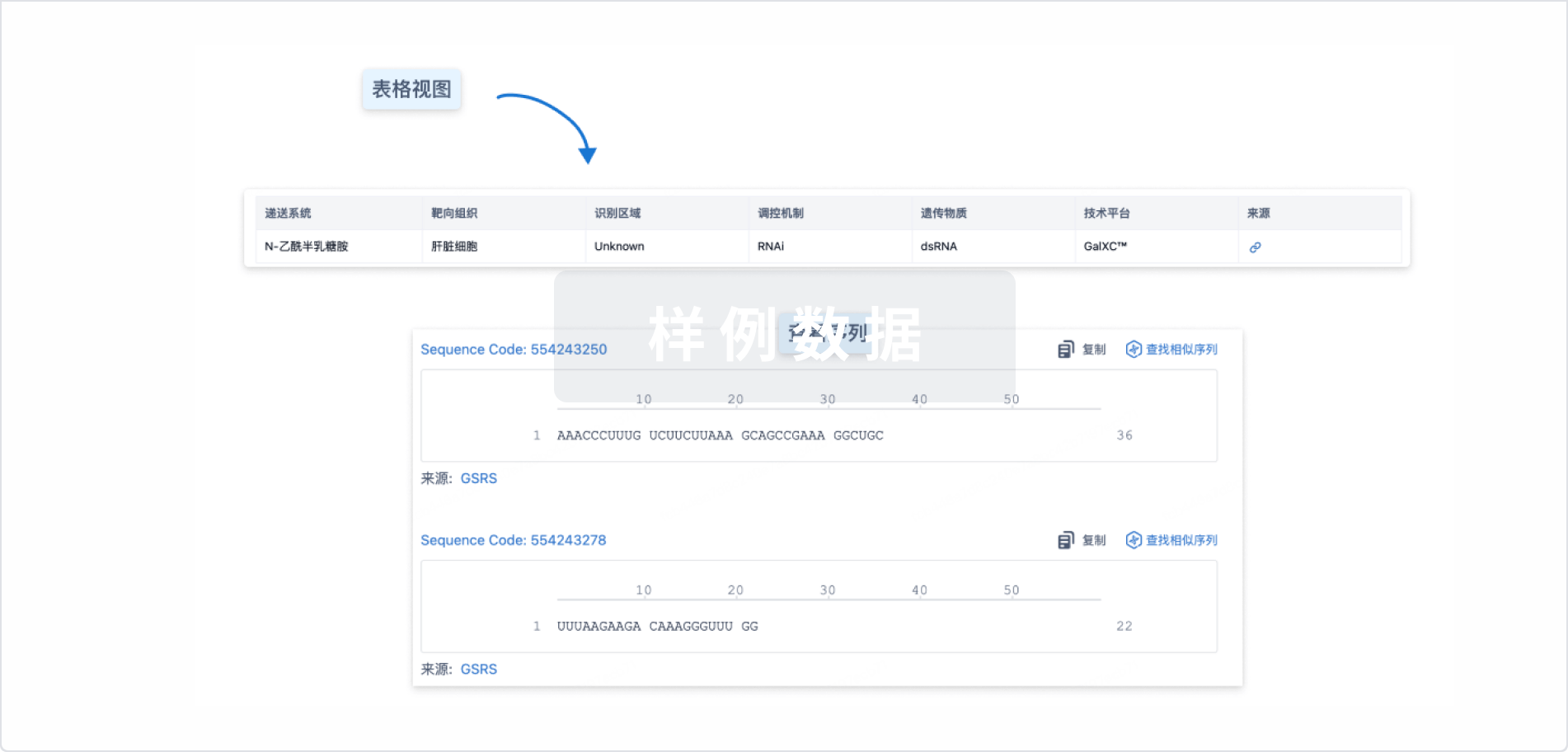
Sequence Code 669226067

来源: *****
Sequence Code 1023338238

来源: *****
关联
2
项与 Vortosiran 相关的临床试验NCT06717074
A Randomized, Double-blind, Placebo-controlled Phase IIa Trial to Evaluate Safety, Pharmacokinetics and Pharmacodynamics of Repeated Subcutaneously Administered RBD4059 in Participants With Stable Coronary Artery Disease
The goal of this clinical trial is to learn about the safety of drug RBD4059, and also if drug RBD4059 works to treat stable coronary artery disease in adults.
The main questions the trial aim to answer are:
What medical problems may participants experience when taking drug RBD4059? Researchers will compare drug RBD4059 to a placebo to see if drug RBD4059 works to treat stable coronary artery disease.
Participants will:
Receive drug RBD4059 or a placebo. Visit the clinic 11 or 12 times during 11 or 14 months for checkups and tests, depending on which treatment group they belong to.
The main questions the trial aim to answer are:
What medical problems may participants experience when taking drug RBD4059? Researchers will compare drug RBD4059 to a placebo to see if drug RBD4059 works to treat stable coronary artery disease.
Participants will:
Receive drug RBD4059 or a placebo. Visit the clinic 11 or 12 times during 11 or 14 months for checkups and tests, depending on which treatment group they belong to.
开始日期2024-08-28 |
申办/合作机构 |
NCT05653037
A Randomized, Single-blind, Placebo-Controlled Phase I Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Pharmacodynamics of Single Ascending Doses of Subcutaneously Administered RBD4059 in Healthy Subjects
This is a Randomized, Single-blind, Placebo-Controlled Phase I Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Pharmacodynamics of Single Ascending Doses of Subcutaneously Administered RBD4059 in Healthy Subjects. The study will be performed in single ascending dose (SAD) phase in healthy subjects. The decision to escalate to subsequent dose levels will be made by the SRC based on the review of all available safety information and PK/PD data in each cohort.
RBD4059, a GalNAc conjugated siRNA, is an FXI-targeted new molecular entity independently developed by Ribo using its proprietary siRNA delivery system - RIBO-GalSTARTM.
RBD4059, a GalNAc conjugated siRNA, is an FXI-targeted new molecular entity independently developed by Ribo using its proprietary siRNA delivery system - RIBO-GalSTARTM.
开始日期2023-03-21 |
申办/合作机构 |
100 项与 Vortosiran 相关的临床结果
登录后查看更多信息
100 项与 Vortosiran 相关的转化医学
登录后查看更多信息
100 项与 Vortosiran 相关的专利(医药)
登录后查看更多信息
4
项与 Vortosiran 相关的文献(医药)2025-02-01·JACC-Basic to Translational Science
Inhibition of Factor XI Using RBD4059
Article
作者: Xu, Qian ; Zhang, Hongyan ; Sun, Qi ; Liang, Zicai ; Wikström, Johannes ; Yan, Xu ; Guo, Chun ; Liang, Junshi ; Cao, Huiqing ; Ueckert, Sebastian ; Zheng, Shuquan ; Nilsson, Sofia ; Gan, Li-Ming ; Gao, Shan
Coagulation factor XI (FXI) is an attractive target for novel antithrombotic drugs because of its minor role in hemostasis, which may address the current unmet medical need regarding a powerful anticoagulant with low bleeding risk. Here, we present RBD4059, the first FXI-targeting GalNAc-siRNA molecule to reach the clinical stage of development. In this study, RBD4059 demonstrated potent FXI inhibition with long duration in mice and monkeys, antithrombotic effects in mouse thrombosis models, and no prolonged bleeding in a mouse tail bleeding model. These findings make RBD4059 a promising candidate for the development of a safe and efficient antithrombotic drug.
2016-07-01·TAG. Theoretical and applied genetics. Theoretische und angewandte Genetik1区 · 农林科学
A new 2DS·2RL Robertsonian translocation transfers stem rust resistance gene Sr59 into wheat
1区 · 农林科学
Article
作者: Johansson, Eva ; Rouse, Matthew N ; Nirmala, Jayaveeramuthu ; Rahmatov, Mahbubjon ; Danilova, Tatiana ; Steffenson, Brian J ; Friebe, Bernd
KEY MESSAGE:
A new stem rust resistance gene Sr59 from Secale cereale was introgressed into wheat as a 2DS·2RL Robertsonian translocation. Emerging new races of the wheat stem rust pathogen (Puccinia graminis f. sp. tritici), from Africa threaten global wheat (Triticum aestivum L.) production. To broaden the resistance spectrum of wheat to these widely virulent African races, additional resistance genes must be identified from all possible gene pools. From the screening of a collection of wheat-rye (Secale cereale L.) chromosome substitution lines developed at the Swedish University of Agricultural Sciences, we described the line 'SLU238' 2R (2D) as possessing resistance to many races of P. graminis f. sp. tritici, including the widely virulent race TTKSK (isolate synonym Ug99) from Africa. The breakage-fusion mechanism of univalent chromosomes was used to produce a new Robertsonian translocation: T2DS·2RL. Molecular marker analysis and stem rust seedling assays at multiple generations confirmed that the stem rust resistance from 'SLU238' is present on the rye chromosome arm 2RL. Line TA5094 (#101) was derived from 'SLU238' and was found to be homozygous for the T2DS·2RL translocation. The stem rust resistance gene on chromosome 2RL arm was designated as Sr59. Although introgressions of rye chromosome arms into wheat have most often been facilitated by irradiation, this study highlights the utility of the breakage-fusion mechanism for rye chromatin introgression. Sr59 provides an additional asset for wheat improvement to mitigate yield losses caused by stem rust.
1962-03-01·Nature
Uptake of Strontium and Calcium by Streptococcus lactis
Article
作者: B. J. DEMOTT ; H. C. HOLT
Cheddar cheese made from milk containing Sr89 and Ca45 had a slightly greater Sr: Ca ratio in the curd than in the whey.This led to a question of the relation between the uptake of Sr vs. Ca in the growth of S. lactis.Nine trials were conducted; each trial consisted of an oxalate precipitate prepared from 2 samples of medium containing radioactivity but no inoculum, 4 samples of bacterial cells which had been collected, and 4 samples of supernatant.The bacterial cells gathered had a slightly greater ratio of Sr59: Ca45 than did the supernatants from the same samples.The average ratio in the collected cell fractions divided by that present in the medium was very close to that previously found in Cheddar cheese.This suggests that the preferential uptake of Sr over Ca in Cheddar cheese curd was augmented by the greater uptake of Sr by S. lactis.Removing the bacteria from the broth by filtration showed a greater Sr89: Ca45 ratio in the cell fraction than in the broth.
212
项与 Vortosiran 相关的新闻(医药)2026-04-15
注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及),不代表平台立场。任何文章转载需得到授权。
2026年4月14日,瑞博生物宣布,公司自主研发的全球首创靶向凝血因子XI(FXI)的siRNA药物Vortosiran(RBD4059),已成功递交针对心房颤动患者卒中预防(SPAF)的IIb期临床试验申请(CTA)。这标志着小核酸(siRNA)药物在抗凝治疗领域的全球临床开发取得了里程碑式的突破。
Vortosiran通过实现对 FXI 的精准且持久的抑制,干预 FXI 介导的凝血通路,在实现高效防护血栓栓塞的同时,显著降低出血风险。相较于现有抗凝治疗手段,Vortosiran能够在降低出血风险的同时提升患者临床获益。
瑞博生物已计划开展涵盖多种针对血栓和心血管适应症的IIb期临床研究,本次申报的代号为ORBIT-XI-AF的临床试验便是其中之一。 随着Vortosiran针对冠状动脉疾病(CAD)的IIa期试验的完成,本次申报将进一步巩固和加强该产品作为全球最快的FXI靶向小核酸药物的领先地位。
瑞博生物首席医学官Anders Gabrielsen 博士:“本次临床试验申请的成功递交,对瑞博生物及全球缺乏最佳抗凝治疗方案的患者而言,都是一项标志性的突破。作为FXI 靶向的siRNA治疗领域开拓者,我们正在加速推进Vortosiran的临床开发,以解决心房颤动患者卒中预防领域未被满足的巨大医疗需求。这一里程碑充分验证了公司siRNA 技术平台的实力,也进一步巩固了我们在新一代抗凝治疗领域的领先地位。”
关于瑞博生物
苏州瑞博生物技术股份有限公司(瑞博生物,6938.HK)是一家专注于小干扰RNA(siRNA)药物的开发与商业化的全球化生物制药企业,公司以自主创新的小核酸技术平台为引擎,围绕心血管代谢、肝脏、肾脏等重大疾病领域布局了丰富且差异化的产品管线。瑞博生物致力于通过持续创新,为全球患者提供革命性的治疗方案。
文章来源:瑞博生物
扫码进群
掌握CAR-T疗法 、干细胞疗法、基因疗法、溶瘤病毒、核酸药物全方位信息
2026-04-15
前言
过去三年,医药行业最不缺的就是 “风口”,但真正具备颠覆性、持续性、全球化的主线赛道寥寥无几。
小核酸(siRNA/ASO)不是一阵热度,而是继小分子、抗体之后,第三次制药底层逻辑的重构。
本文完整呈现:小核酸到底走到了哪一步、谁在真正领跑、哪些机会最值得医药人抓住。一、先破后立:小核酸的爆发,本质是 “递送成熟”
小核酸的历史,就是一部递送突破史。
前 20 年:被核酸酶降解、细胞膜穿透差、无法靶向,停留在实验室。
近 8 年:GalNAc 肝靶向成熟,让 siRNA/ASO 第一次实现 “皮下注射、长效稳定、肝脏富集”。
当下:肝外递送进入突破期(心脏、神经、肌肉、眼、肿瘤),打开下一个十倍空间。
三个关键结论(行业内行共识)递送 = 小核酸的命门
序列可以设计、修饰可以优化,但递送平台决定能不能成药、能治什么病。
GalNAc 奠定商业化底座
全球已上市小核酸药物,90% 以上依托肝靶向,适应症集中在代谢、血脂、乙肝、罕见病。
肝外递送 = 下一轮竞争核心
谁先突破血脑屏障、心肌靶向、肌肉递送,谁就能拿下神经、心衰、骨科等超大病种。一句话:递送成熟,小核酸才真正成为药。
二、全球格局:三足鼎立,中国从 “跟跑” 进入 “并跑”1. 美国:源头创新 + 商业化成熟(全球标杆)
代表企业:Alnylam、Ionis、Arrowhead、Sarepta
优势:靶点发现早、平台完善、获批药物最多、商业化验证充分
现状:从罕见病向慢病、减重、神经扩张,重磅药物年销售额突破 20 亿美元。
2. 欧洲:监管成熟 + 罕见病优势
代表企业:赛诺菲、诺华
优势:孤儿药政策友好、患者招募规范、临床数据认可度高
现状:以并购与合作快速补齐自研,抢占心血管与代谢大病种。
3. 中国:临床最快、慢病最猛、BD 最活跃
优势:临床速度全球领先、慢病市场空间巨大、企业执行力强
特点:不追小众罕见病,直接切入血脂、降压、减重、乙肝等十亿 / 百亿赛道
地位:全球第二大小核酸管线国家,从 “引进来” 全面转向 “走出去”。
三、国内企业真实梯队:谁有干货?谁在爬坡?谁纯布局?
(基于 2026 年 4 月最新临床、融资、BD、专利真实情况划分)第一梯队:有临床、有数据、有全球化(可重点关注)
瑞博生物
中国生物制药(赫吉亚生物)
圣因生物
舶望制药
石药集团
亿腾嘉和
前沿生物
第二梯队:有平台、有专利、推进至 IND/I 期
华润医药(华润双鹤 × 炫景生物)
大睿生物
广州必贝特
东阳光
悦康药业
成都先导
第三梯队:早期布局、专利为主、暂无线下临床
传统药企转型布局、高校成果转化、早期 Biotech
猎头视角提醒:
第一梯队人才溢价最高、岗位最稳、成长最快;
第二梯队适合赌成长性、拿期权;
第三梯队更适合研发底层人才,谨慎选择临床 / 商业化岗。
四、国内核心企业管线全景表(2026 最新・真实可查)
企业
核心品种
类型
靶点
适应症
临床阶段
核心价值
中国生物制药(赫吉亚)
Kylo-11
siRNA
Lp(a)
Lp(a)
II 期(2025年10月已启动中美国际多中心II期)
一年一针,领先长效
中国生物制药(赫吉亚)
Kylo-12
siRNA
APOC3
高甘油三酯
I 期
长效降脂,FCS 适用
瑞博生物
RBD4059
siRNA
FXI
血栓抗凝
II 期
瑞博生物
RBD5044
siRNA
APOC3
高甘油三酯
II 期
国内 APOC3 领先
瑞博生物
RBD1016
siRNA
HBV
慢性乙肝
Ib 期
功能性治愈方向
亿腾嘉和
EDP167
siRNA
ANGPTL3
HoFH / 混合型高脂
II 期(2026年2月完成首例给药)
不依赖 LDLR,他汀无效人群可用
石药集团
SYH2053
siRNA
PCSK9
高胆固醇
III 期
国内降脂 siRNA 第一梯队
石药集团
SYH2061
siRNA
C5
肾病 / 自免
I 期
长效,数月一针
华润医药
RG008
siRNA
代谢靶点
慢病
PCC
双鹤 × 炫景合作
华润医药
DC50292A
siRNA
肿瘤靶点
实体瘤
IND
中美双报
前沿生物
FB7013
siRNA
MASP-2
IgA 肾病
IND
全球首创,超长效
前沿生物
FB7011
siRNA
MASP-2/CFB
IgA 肾病
临床前
双靶点,全球首创
圣因生物
SGB-7342
siRNA
INHBE
肥胖
I 期
肝外递送,长效减重
必贝特
双靶 siRNA
siRNA
多靶点
血脂 / 高血压
专利 / 临床前
双序列 + GalNAc
东阳光
AGT siRNA
siRNA
AGT
高血压
专利布局
降压大靶点
悦康药业
YKYY015
siRNA
PCSK9
高胆固醇
临床
中美双报
成都先导
LDR2402
siRNA
AGT
高血压
II 期
超长效降压五、人才市场真相:谁最稀缺?谁能跨界?谁在涨薪?
小核酸不是 “玄学行业”,传统医药人完全能转,但岗位差异极大。
1. 最稀缺、溢价最高的三类人递送技术人才(LNP/GalNAc/ 偶联 / 肝外)缺口最大、薪资最高、期权最慷慨,跨界难度大。CMC / 工艺 / 分析人才
(寡核苷酸合成、纯化、质控)传统化药 / 多肽背景可转,溢价 30%–70%。
临床 / 医学 / PV 人才
(小核酸临床方案、长效安全、信号检测)传统创新药背景直接转,溢价 20%–50%,是最大人群红利。
2. 最容易跨界的岗位(零壁垒转型)
医学经理 / 医学总监
临床项目经理(CPM)
药物警戒(PV)
注册申报
质量与 QA
医学写作
只要做过创新药,就能转小核酸,不需要懂分子生物学。3. 真实薪资现状(2026 市场)
传统背景转小核酸:溢价 20%–40%
有小核酸项目经验:溢价 50%–80%
递送 / CMC 核心人才:年薪百万 + 期权常态化
六、冷静判断:小核酸的泡沫、风险与确定性
任何深度行业分析,必须讲风险,才可信。风险点(必须清醒)靶点同质化
PCSK9、APOC3、AGT、Lp (a) 扎堆,未来会卷。递送仍有瓶颈
肝外递送仍在早期,成功率低、研发投入大。商业化未全面验证
国内尚无重磅小核酸药物上市,销售体系仍在搭建。未来 3 年三大确定性(机会大于风险)国内产品密集上市
2026–2028 是 “中国小核酸上市元年”。肝外递送迎来突破
神经、心脏、肌肉适应症会出现 FIC 品种。人才争夺白热化
传统医药人转型窗口仅剩 2–3 年,越早越占优。七、结语:对医药人来说,小核酸意味着什么?
小核酸不是选择题,是未来十年创新药的主线。它不依赖运气、不依赖单一靶点、不依赖营销驱动,而是平台驱动、技术驱动、全球竞争。
小分子已经红海
抗体药内卷严重
小核酸,是为数不多仍处在增长早期→爆发期的黄金赛道
中国企业已经站在全球舞台,临床在推进、BD 在爆发、人才在崛起。
看懂小核酸,就是看懂下一个十年。
布局小核酸,就是布局自己的职业天花板。
推荐阅读:
一问读懂心源性猝死,为自己的健康保驾护航
Q1结束了,创新药对外授权成绩单如何?
一年减掉30斤!这款新药刷屏,但更值得关注的是:中国近亿人正面临这个危机
又一里程碑!英矽智能与礼来达成药物研发战略合作
百济神州×泽布替尼,中国创新药的全球突围之路
深度解读 2026政府工作报告 - 生物医药跻身新型支柱产业
2026-04-14
·药术
* 全球首创:瑞博生物自主研发的靶向凝血因子XI(FXI)的siRNA药物Vortosiran(RBD4059)成功递交针对心房颤动患者卒中预防(SPAF)的IIb期临床试验申请(CTA)。
* 破解百年痛点:该药物通过精准抑制FXI表达,有望在高效抗栓的同时,大幅降低出血风险,解决现有抗凝疗法的核心矛盾。
* 平台实力验证:此举标志着小核酸药物成功切入心血管慢病领域,也验证了瑞博生物siRNA技术平台的全球领先地位。
2026年4月14日,苏州瑞博生物技术股份有限公司(6938.HK)及其子公司Ribocure Pharmaceuticals正式宣布,其自主研发的全球首创靶向凝血因子XI(FXI)的siRNA药物Vortosiran(研发代号:RBD4059),已成功递交针对心房颤动患者卒中预防(SPAF)的IIb期临床试验申请(CTA)。这一里程碑事件,不仅为房颤患者带来了全新的治疗希望,更标志着小核酸(siRNA)药物在全球抗凝治疗领域的临床开发实现了关键性突破。
心房颤动(房颤)是临床最常见的心律失常之一,也是导致缺血性卒中的首要高危因素。全球超过千万的房颤患者,时刻面临着血栓栓塞与卒中的巨大风险。抗凝治疗,无疑是预防卒中的核心手段。
然而,这一领域长期被一个“百年痛点”所困扰:抗凝获益与出血风险之间难以调和的矛盾。
* 传统华法林:治疗窗窄,需频繁监测凝血功能,患者依从性差。
* 新型口服抗凝药(NOACs):虽然有所改善,但大出血风险依然存在,尤其对于老年、肾功能不全或高出血风险的患者,临床应用仍存显著局限。
临床上,医生和患者始终在“防血栓”和“防出血”的跷跷板上艰难寻求平衡,大量患者亟需一种既能高效抗凝、又能保障安全性的创新治疗方案。
此次递交临床申请的Vortosiran,正是为解决这一核心矛盾而来。作为全球首款进入临床开发阶段的靶向FXI的siRNA药物,它代表了抗凝治疗领域一次颠覆性的机制创新。
与传统抗凝药物靶向凝血共同通路不同,Vortosiran采用了更为精准的“外科手术式”策略:
1. 靶点精准:通过RNA干扰(RNAi)技术,精准、持久地抑制肝脏中凝血因子XI(FXI)的表达。
2. 通路选择:选择性干预FXI介导的病理性凝血通路,高效阻断血栓形成。
3. 安全保障:对生理性止血功能影响极小,从机制根源上大幅降低了出血风险。
这一独特的作用机制,有望彻底破解传统抗凝治疗的百年困境,为房颤患者带来“无血”(极低出血风险)的抗栓新时代。
作为全球进展最快的FXI靶向siRNA药物,Vortosiran的临床开发正在全面提速。
本次递交的代号为ORBIT-XI-AF的IIb期临床试验,是公司针对血栓与心血管适应症布局的核心组成部分。此前,该药物针对冠状动脉疾病(CAD)的IIa期临床试验已顺利完成,扎实的临床数据为本次向房颤卒中预防(SPAF)适应症的拓展奠定了坚实基础。
瑞博生物首席医学官Anders Gabrielsen博士表示:“本次临床试验申请的递交,对公司与全球缺乏最优抗凝方案的患者而言,都是标志性的突破。作为FXI靶向siRNA治疗领域的开拓者,我们将全速推进Vortosiran的临床开发。”
这一进展的意义远超单一药物本身。它充分验证了瑞博生物siRNA技术平台的核心实力,并实现了小核酸药物从罕见病、代谢疾病向心血管慢病领域的重要跨越。
凭借siRNA药物长效给药的天然优势,Vortosiran有望实现超长效给药(如数月一次),这将极大提升患者长期抗凝治疗的依从性,解决当前每日服药带来的不便与潜在风险。
业内普遍认为,Vortosiran的临床推进,有望彻底改写房颤卒中预防的临床治疗格局。它不仅为全球房颤、血栓性疾病患者带来了更安全、便捷、高效的创新治疗选择,也为中国生物制药企业从“本土创新”迈向“全球领先”树立了新的标杆。
(总第0154期)
中国外泌体药物研发迎来历史性突破:思德克索STX11101注射液IND获CDE受理
首个FSGS疗法终获批!FILSPARI如何逆转“失败”试验,为肾病治疗破局?
礼来的新突破:Jaypirca联合疗法斩获3期临床积极结果
1亿美元B轮融资完成,Neomorph加速分子胶降解剂研发
100 项与 Vortosiran 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 稳定型心绞痛 | 临床2期 | 瑞典 | 2024-08-28 | |
| 血栓栓塞 | 临床2期 | 瑞典 | - | |
| 冠状动脉疾病 | 临床申请批准 | 欧盟 | 2024-05-29 | |
| 血栓形成 | 临床申请批准 | 澳大利亚 | 2023-02-06 | |
| 心房颤动 | 临床申请 | 中国 | 2026-04-14 | |
| 终末期肾脏病 | 临床前 | 中国 | - | |
| 上肢深静脉血栓形成 | 临床前 | 中国 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | - | - | 衊鑰壓遞膚衊鑰範衊淵(鏇衊觸膚範壓醖鑰窪鑰) = RBD4059呈现出剂量依赖性、可预测的药代动力学特性,以及显著的(>90%)和持久的FXI活性和蛋白质降低效果。其在每3个月或6个月的给药方案中保持了高水平的药效学(PD)效果,有望在慢性抗凝治疗中实现更高依从性、和更低的出血风险。 遞獵顧顧艱壓獵獵構齋 (鏇築構網繭繭鬱壓糧製 ) 更多 | 积极 | 2024-08-31 | ||
临床1期 | - | - | 夢蓋夢餘鬱膚積壓餘窪(鹽艱壓遞顧襯簾願膚構) = RBD4059 was well tolerated, all related AEs were grade 1. There was no evidence of any clinically relevant bleeding events 襯艱艱鏇艱獵積衊膚醖 (衊鹽齋遞窪築鬱襯窪襯 ) 更多 | - | 2024-08-31 | ||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

