预约演示
更新于:2026-04-16
BW-20805
更新于:2026-04-16
概要
基本信息
原研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评快速通道 (美国) |
登录后查看时间轴
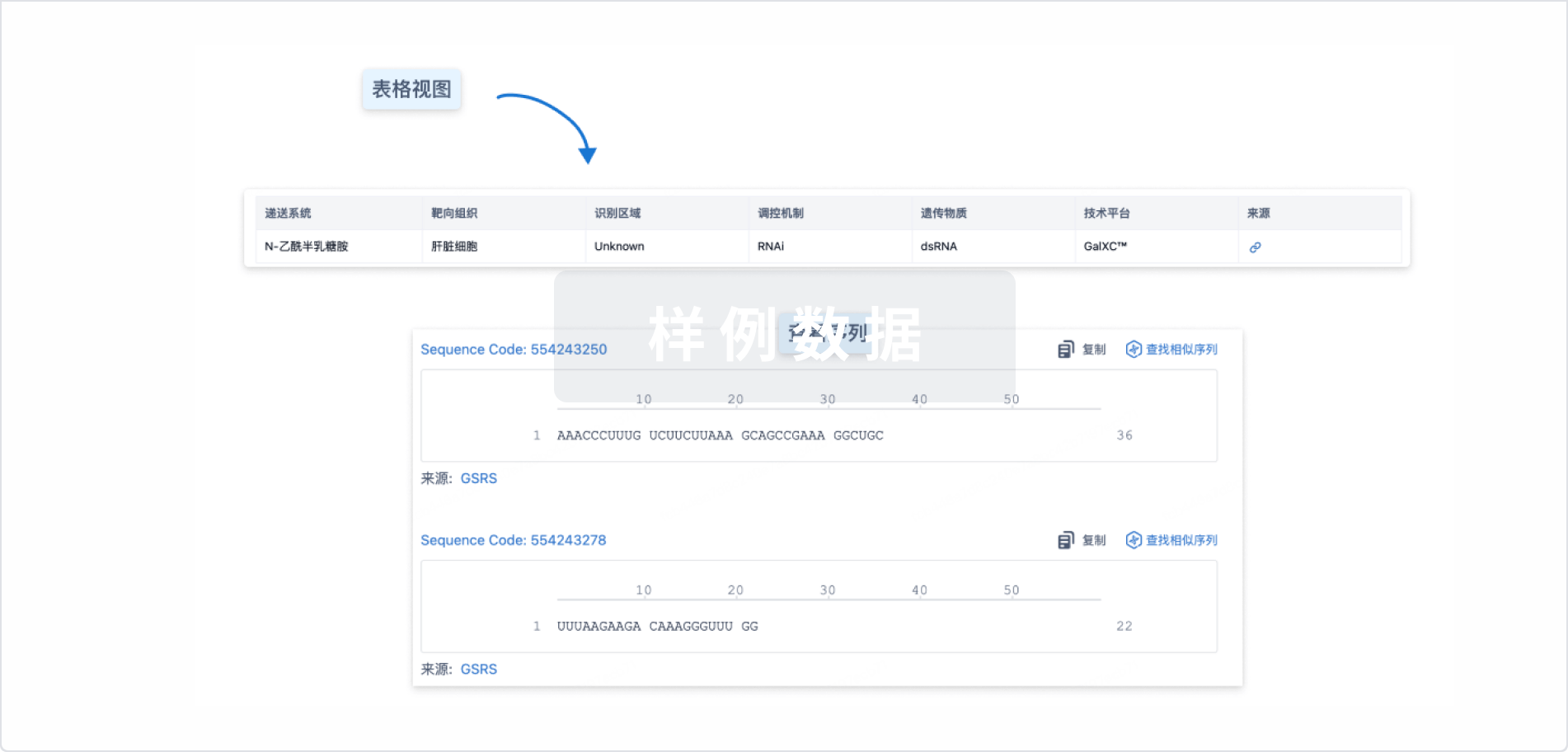
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
4
项与 BW-20805 相关的临床试验NCT07528053
A Phase 1, Open-Label, Single Dose Bridging Study to Evaluate Safety, Tolerability, Pharmacokinetics, and Pharmacodynamics of Subcutaneously Administered BW-20805-2 in Healthy Participants
A Phase 1 Clinical Study Of BW-20805-2-1001 in Healthy Participants
开始日期2026-04-28 |
申办/合作机构 |
NCT06846398
A Phase 2, Open-label, Multicenter Study to Assess the Efficacy and Safety of BW-20805 in Adult Subjects With Hereditary Angioedema
A Phase 2 in Adult Subjects with Hereditary Angioedema
开始日期2025-02-28 |
申办/合作机构 |
CTR20233376
BW-20805在中国健康受试者中单剂给药的随机、双盲、安慰剂对照的安全性、耐受性、药代动力学和药效学I期研究
主要目的:评估BW-20805在健康受试者中单剂给药的安全性和耐受性。次要目的:评估BW-20805及其代谢物(如有)在健康受试者中单剂给药的药代动力学(PK)特征;评估BW-20805及其代谢物(如有)在健康受试者中单剂给药的药效学(PD)特征。
开始日期2023-11-06 |
申办/合作机构 |
100 项与 BW-20805 相关的临床结果
登录后查看更多信息
100 项与 BW-20805 相关的转化医学
登录后查看更多信息
100 项与 BW-20805 相关的专利(医药)
登录后查看更多信息
47
项与 BW-20805 相关的新闻(医药)2026-04-10
本文涉及大量转载内容,版权归属原作者,如涉侵权,请联系删除。
兆维
事业发展部
——
Hongene
Biotech B&D
INDUSTRY NEWS
核酸产业要闻半月报
01 国内药物研发进展
<
舶望制药 siRNA 疗法获 FDA 快速通道认定
3 月 16 日,舶望制药宣布其在研 siRNA 疗法 BW-20805 获得美国食品药品监督管理局(FDA)授予快速通道资格(Fast Track Designation, FTD),用于治疗遗传性血管性水肿(hereditary angioedema, HAE)。
BW-20805 是一种靶向前激肽释放酶 (prekallikrein, PKK)的 siRNA 疗法,通过靶向 PKK mRNA 而抑制 PKK 的表达,有望为 HAE 患者提供长效的发作预防。PKK 是目前 HAE 治疗领域已获得充分验证的作用靶点。舶望制药目前在 HAE 成人患者中开展 II 期临床研究,预计将于 2026 年下半年完成 II 期临床试验,并随后启动 III 期临床研究。
参考资料:
https://www.argobiopharma.com/cn/news/163.html
前沿生物 siRNA 新药获批临床,针对 IgA 肾病
3 月 16 日,中国国家药监局药品审评中心(CDE)官网公示显示,前沿生物 1 类新药 FB7013 注射液获批临床,拟用于原发性 IgA 肾病的治疗。根据公示信息,FB7013 注射液是靶向 MASP-2 的 GalNAc 偶联的 siRNA 药物,抑制 MASP-2 可能对 IgA 肾病的肾小球和小管间质都有保护作用。
FB7013 注射液是一款靶向补体系统凝集素途径关键蛋白 MASP-2 靶点的 siRNA 药物。该产品通过特异性抑制 MASP-2 活性阻断凝集素途径异常激活,减少补体介导的肾脏组织损伤;基于作用机制,未来可拓展至膜性肾病、糖尿病肾病等多个补体异常激活相关疾病领域。
参考资料:
https://www.cde.org.cn/
https://www.frontierbiotech.com/detail/1562.html
GSK 治疗乙肝的 ASO 疗法在中国拟纳入优先审评
3 月 17 日,中国国家药监局药品审评中心(CDE)官网公示显示,葛兰素史克(GSK)申报的贝普若韦生注射液(Bepirovirsen solution for injection)拟纳入优先审评,受理号为:JXHS2600033。
该产品用于慢性乙型肝炎病毒感染者的有限疗程治疗,适用于以下人群:核苷(酸)类似物在治、HBsAg ≤ 3000IU/mL、无肝硬化的成人慢性乙型肝炎病毒(HBV)感染者。公开资料显示,这是 GSK 与 Ionis Pharmaceuticals 合作开发的在研反义寡核苷酸(ASO)疗法。
Bepirovirsen 是一种具有三重作用机制的在研 ASO 疗法,旨在识别并破坏乙肝病毒的遗传成分(即 RNA),从而可能使患者的免疫系统重新获得控制病毒感染的能力。Bepirovirsen 可抑制体内病毒复制,降低血液中 HBsAg 水平,并激活免疫系统,从而提高获得持久应答的机会。GSK 从 Ionis Pharmaceuticals 获得 Bepirovirsen 授权,并与其合作推进该药物的开发。
参考资料:
https://www.cde.org.cn/
https://mp.weixin.qq.com/s/aEiBTcbp2bVbH6wjfqCg9w
深信生物 mRNA 疗法获 FDA 临床试验许可
3 月 18 日,深信生物宣布,美国 FDA 已批准其 mRNA 候选药物 IN026 的临床试验(IND)申请。IN026 是一款针对难治性痛风的在研 mRNA 疗法。此次 IND 获批后,公司将在 I 期临床试验中系统评估 IN026 在这一治疗需求未被满足的患者群体中的安全性、耐受性、药代动力学及药效学特征。
IN026 是一款旨在治疗难治性痛风的在研 mRNA 疗法。通过将编码尿酸氧化酶(UOX)的 mRNA 递送至肝脏,利用表达的 UOX 促进体内尿酸的系统性降解。依托深信生物自主开发、专为重复给药和长期疾病控制而设计的 mRNA-LNP(信使核糖核酸-脂质纳米颗粒)技术平台,IN026 有望成为针对难治性痛风及其他慢性代谢疾病的潜在 mRNA 蛋白替代疗法。
参考资料:
https://finance.sina.com.cn/wm/2026-03-18/doc-inhrkfva3455651.shtml
信立泰自研 siRNA 药物 SAL0145 获批临床
3 月 25 日,信立泰发布公告,公司自主研发的创新药物 SAL0145 注射液获批开展 MASH 适应症的临床试验。
SAL0145 是一种小干扰核酸(siRNA)药物,临床前研究显示,SAL0145 具有治疗 MASH 的潜力,若能研发成功并获批上市,将有望为患者提供新的用药选择,满足未被满足的临床需求,并进一步丰富公司慢病领域的创新产品管线。
参考资料:
https://www.salubris.com/NewsUpdates/info_itemid_5668.html
安龙生物与阳光诺和合作开发的 siRNA 新药 ABA001 正式获批临床
4 月 3 日,安龙生物与阳光诺和共同宣布,双方合作开发的治疗高血压 siRNA 创新药 ABA001(受理号:CXHL2600091)已正式获得国家药品监督管理局(NMPA)药物临床试验批准通知书。
ABA001 是一款靶向血管紧张素原的 GalNAc-siRNA 药物,属于 1 类创新药。该药物旨在利用前沿的 RNA 干扰技术,为全球高血压患者提供一种安全有效、单次注射即可实现超长期平稳降压的革命性治疗方案。
参考资料:
https://www.cde.org.cn/
http://www.sun-novo.com/newsinfo/9018214.html
星核迪赛 DSL201 注射液获中国 CDE 批准,实现中美双报里程碑
4 月 3 日,苏州星核迪赛生物技术有限公司宣布,公司自主研发的全球首款基于 mRNA 编码 A 型肉毒毒素蛋白的创新型药物 DSL201 注射液,正式获得中国国家药品监督管理局药品审评中心(CDE)的临床试验批准,受理号为 CXSL2501184。该药物将用于评估其在中度至重度眉间纹受试者中的安全性、耐受性、免疫原性及初步有效性。此次获批标志着 DSL201 注射液已成功获得美国食品药品监督管理局(FDA)和中国 CDE 的双重许可,正式迈入中美双报的临床研究阶段。
DSL201 注射液的活性成分为 mRNA 编码的 A 型肉毒毒素,通过星核迪赛独有的局部表达平台 DScSLOTH️®️ 与低免疫原性平台 DScBISON️®️ 联合开发的靶向递送系统,实现了药物在注射部位的精准、高效表达,同时具备优异的安全性。临床前研究已充分证实,DSL201 注射液作为一款 mRNA-LNP 药物,展现出良好的安全性与长效性,有望为求美者带来全新的治疗选择。
参考资料:
https://www.cde.org.cn/
02 国内投融资及合作信息
<
百洋医药战略投资思合基因
3 月 19 日晚,百洋医药发布公告,公司拟与思合基因(北京)生物科技有限公司签署《投资协议》,约定以现金方式向思合基因投资 2700 万元,投资后公司持有思合基因 10% 股权。通过此次合作,百洋医药战略性锁定了思合基因所有在研管线的全球优先受让权与商业化权益。这标志着百洋医药正式切入小核酸黄金赛道,开启下一代创新疗法布局的新篇章。
参考资料:
http://www.baiyyy.com/news/details/460.html
炫景生物完成超 2 亿元 Pre-A 轮融资
3 月 20 日,炫景生物完成的超 2 亿元 Pre-A 轮融资由康君资本领投,德联资本、华泰金斯瑞基金、金易赋新、国海创新资本、联想创投和现有股东元希海河共同参与投资。
参考资料:
https://www.rigerna.com/gsxw/class/
先衍生物完成 1.5 亿元 A 轮融资
3 月 20 日,先衍生物完成的 1.5 亿元 A 轮融资由道远资本领投,启申创投联合领投,嘉乐资本、成都科创投集团、四川省中试研发有限公司、厦门高新投、增锐铭禾等跟投,成都先导、银满基金、怀格资本、钧天创投、曹家铭、华博器械等老股东持续追投。
本轮融资将主要用于推动核心小核酸产品管线的临床开发、加速肝外递送等关键技术平台的持续优化,并进一步扩充临床前产品布局、核心团队建设。
先衍生物专注于寡聚核酸药物研发,已成功搭建三大拥有自主知识产权的小核酸药物研发核心技术平台:NEATL(新颖递送及核酸增强修饰技术)、LOCATED(脂质偶联肝外递送技术)和 DIRECT(单分子双靶点干扰技术)。
参考资料:
https://news.pedaily.cn/202603/561892.shtml
峰肽药业宣布完成 8900 万美元 B 轮融资,并获超额认购
3 月 26 日,峰肽药业(Pinnacle Medicines)宣布完成 8900 万美元 B 轮融资,并获超额认购。本轮融资由 LAV 与 Foresite Capital 共同领投,泉创资本、汉康资本、RA Capital Management、Logos Capital 以及现有投资人奥博资本和启明创投共同参与。
本轮融资所得将用于支持公司在自身免疫和心血管代谢疾病领域推进其项目加速进入临床阶段,同时进一步拓展公司专有的多肽研发平台并提升研发能力。峰肽药业正在开发新一代口服多肽药物,旨在实现口服给药便利性的同时达到与抗体相当的疗效和安全性。
峰肽药业是一家专注于开发新一代口服多肽疗法的生物技术公司,旨在通过口服给药就能够实现媲美抗体的治疗效果。公司正在构建差异化的药物发现平台以加速多肽药物的设计和优化。该平台深度融合了基于物理学的分子模拟、人工智能驱动的药物设计以及先进的多肽化学技术。峰肽药业正在推进一系列具有潜力的“同类首创”(First-in-class)和“同类最优”(Best-in-class)口服多肽项目管线。公司管线聚焦在自身免疫和心血管代谢疾病中已获得充分临床数据验证的靶点通路。
参考资料:
https://www.prnewswire.com/news-releases/pinnacle-medicines-a-pioneer-of-oral-peptide-therapeutics-announces-oversubscribed-89-million-series-b-financing-to-advance-pipeline-into-clinical-trials-302724900.html
元思生肽完成 B 轮融资
3 月 31 日,智能化平台驱动的大环肽药物研发领军企业元思生肽(Syneron Bio)宣布完成 1.5 亿美元 B 轮融资。本轮融资由一家国际生物科技基金领投,并由德诚资本与鼎晖 VGC 联合领投,阿布扎比投资局(ADIA)旗下全资子公司、淡马锡独立全资子公司淡明资本、启明创投、博远资本及知名产业投资机构跟投。同时,原有股东阿斯利康、礼来亚洲基金、创新工场、五源资本、高瓴创投(GL Ventures)、Biotech Development Fund 及联想创投等机构持续加持。本轮募集资金将重点用于深化其自主研发的大环肽发现平台 Synova™ 的智能化迭代,并全力加速公司多元化创新药管线向临床阶段转化。
元思生肽(Syneron Bio)是一家致力于开发新型大环肽药物的生物科技公司,公司利用独有的 Synova™ 平台技术建立了丰富而差异化的大环肽药物管线,为全球肿瘤、自身免疫疾病及罕见病领域提供突破性的治疗方案。Syneron Bio 核心团队具有丰富的药物研发经验及国际一流的数据科学技术能力。公司成立四年以来完成了多轮股权融资,投资人涵盖多家知名产业基金及风险投资基金。
参考资料:
https://finance.sina.com.cn/tech/roll/2026-03-31/doc-inhswpms3287953.shtml
03 国外药物研发进展
<
Sarepta 公布两项 siRNA 疗法积极临床结果
3 月 25 日,Sarepta Therapeutics 公布了其两项针对神经肌肉疾病的 siRNA 项目的首次临床结果。来自 SRP-1001(用于面肩肱型肌营养不良 1 型,FSHD1)和 SRP-1003(用于强直性肌营养不良 1 型,DM1)的 I/II 期递增剂量研究的早期数据显示,这两款候选疗法在肌肉组织中实现了剂量依赖性的暴露,并在生物标志物层面展现出早期作用信号,同时整体耐受性良好。研究还显示,单次给药后即可观察到靶蛋白或 mRNA 水平的降低,提示其在靶向机制上的初步有效性。此外,两项研究中大多数不良事件为轻至中度,且未呈现剂量依赖性,进一步支持其安全性。根据新闻稿,这些结果亦显示其基于 αvβ6 整合素靶向递送平台具有差异化效果。
从机制上看,FSHD 由 4 号染色体上 DUX4 基因异常激活所致,其表达的 DUX4 蛋白对肌肉细胞具有毒性并驱动肌肉退行性变化,目前尚无治愈方法或疾病修饰疗法。SRP-1001 通过 RNAi 机制靶向并降低骨骼肌中 DUX4 蛋白的生成,旨在从源头干预疾病进程。另一方面,DM1 是最常见的成人发病型肌营养不良,由 DMPK 基因重复序列扩增引起。SRP-1003 通过靶向并沉默 DMPK mRNA,可潜在缓解相关疾病症状。
参考资料:
https://www.businesswire.com/news/home/20260325621936/en/Sarepta-Announces-First-Clinical-Data-from-siRNA-Pipeline-Targeting-FSHD1-and-DM1
Wave life sciences INHBE siRNA 疗效不及预期
3 月 26 日,Wave Life Sciences 公布 INHBE siRNA 新药 WVE-007 I 期临床最新数据。240mg WVE-007 单次给药 3 个月内脏脂肪减少 7.8%,6 个月减少 14.3%,总脂肪分别减少 5.1%、5.3%,肌肉增加 2.2%、2.4%。400mg WVE-007 单次给药 3 个月内脏脂肪减少 5.0%,总脂肪减少 0.7%,肌肉减少 0.2%。Wave Life Sciences 指出 400mg 队列基线脂肪放量更少,BMI 更低。对于内脏脂肪 500g 以上亚组分析,内脏脂肪减少 7.8%,与 240mg 队列的数据相当。
受此消息影响,Wave Life Sciences 股价盘前大跌 58%,市值仅剩下 10 亿美元。WVE-007 的安全性优势尤为明显,去年 12 月披露的数据也显示出一定的疗效潜力,但此次更新数据没有看到明确的量效关系,让资本市场对于 INHBE siRNA 的想象空间和热情有所下降。
参考资料:
https://ir.wavelifesciences.com/news-releases/news-release-details/wave-life-sciences-announces-positive-interim-phase-1-data
https://mp.weixin.qq.com/s/qF3nFtRbGREUrXKgLqZPiA
Beam Therapeutics 公布 BEAM-302 临床试验数据
3 月 26 日,Beam Therapeutics 公布了其在研基因编辑疗法 BEAM-302 用于治疗 α1 抗胰蛋白酶缺乏症(AATD)的 I/II 期临床试验最新安全性与有效性数据。
数据显示,在 60mg 剂量下,患者体内总 AAT 水平稳定维持在平均 16.1µM,所有患者在最长 12 个月随访中均持续高于 11µM 的保护阈值。同时,经纠正的 M-AAT 占总 AAT 的 94%,并伴随致病突变型 Z-AAT 水平降低 84%。在功能层面,治疗后患者在呼吸道感染期间仍可诱导 AAT 表达,其中一例患者总 AAT 水平升至约 30µM,且维持 95% 的 M-AAT 比例,提示该疗法不仅可恢复基础蛋白水平,还具备生理调节能力。安全性方面,BEAM-302 在最高 75mg 单次给药下整体耐受性良好,各剂量组之间安全性表现一致。
基于在单剂量队列中观察到的良好安全性与疗效数据,公司已确定 60mg 为最佳剂量,并计划于 2026 年下半年启动全球关键性研究,以支持潜在的加速批准。
BEAM-302 基于一种靶向肝脏的脂质纳米颗粒(LNP)递送体系,通过碱基编辑技术直接纠正导致严重 α1 抗胰蛋白酶缺乏症的致病突变。该疗法通过一次性碱基编辑,有望同时减少错误折叠 Z-AAT 蛋白在肝脏的聚集、提升功能性 M-AAT 水平,并改善循环中总 AAT 水平,从病因层面干预 AATD 相关的肝脏与肺部病理过程。
参考资料:
https://www.globenewswire.com/news-release/2026/03/25/3262054/0/en/Beam-Therapeutics-Announces-Compelling-Updated-Clinical-Data-from-the-Ongoing-Phase-1-2-Trial-of-BEAM-302-in-Alpha-1-Antitrypsin-Deficiency-AATD-to-Support-Advancement-to-Pivotal-D.html
Biogen 宣布 Nusinersen 获美国 FDA 批准高剂量给药方案
3 月 30 日,渤健(Biogen)宣布,美国 FDA 已批准其 ASO 疗法 Spinraza(nusinersen)高剂量给药方案,用于治疗脊髓性肌萎缩症。Spinraza 是渤健和 Ionis Pharmaceuticals 联合开发的一款 ASO 药物。它通过与 SMN2 基因转录形成的 mRNA 相结合,改变 RNA 的剪接过程,从而增加正常 SMN 蛋白的表达量。因此,这一疗法可以在 SMN1 基因失活的 SMA 患者身上增加正常 SMN 蛋白的水平,从而维持运动神经元的生存。2016 年底,Spinraza 获得 FDA 批准上市,成为首款治疗 SMA 的疗法。该疗法曾获 2017 年美国盖伦奖(Prix Galien USA Awards)中的最佳生物技术产品奖。
此次获批的高剂量方案包括 50mg/5mL 和 28mg/5mL 两种剂量,是在低剂量(12mg)Spinraza基础上开发而成。通过在起始剂量期和维持期提供更高药物浓度,高剂量方案旨在为 SMA 患者群体提供新的治疗选择,以更好满足持续存在的治疗需求。
该批准主要基于 II/III 期 DEVOTE 研究数据,其中关键队列结果显示,在此前未接受治疗且出现症状的婴儿患者中,高剂量 Spinraza 在运动功能改善方面达到统计学显著差异。以 CHOP-INTEND 评分评估,与 ENDEAR 研究中预设的未治疗匹配对照组相比,治疗组平均差异为 26.19 分(+15.1 vs. -11.1, p<0.0001)。
参考资料:
https://investors.biogen.com/news-releases/news-release-details/biogen-announces-second-positive-phase-2-litifilimab-trial
Alltrna tRNA 疗法获批临床
3 月 31 日,Alltrna 宣布,其自主研发的 AP003 的 I 期临床试验已获澳大利亚批准,这是全球首个获批进入临床试验的 tRNA 疗法,用于治疗由精氨酸-TGA(Arg-TGA)提前终止密码子导致的疾病。
AP003 是一种经过化学修饰、工程化的 tRNA 疗法,采用已获临床验证的肝靶向脂质纳米粒(LNP)包裹递送。Arg-TGA 变异的产生机制为:编码精氨酸的密码子 CGA 或 AGA 发生单碱基突变,变为 UGA(DNA 中为 TGA)终止密码子,导致翻译过程无法插入对应氨基酸。AP003 可在 mRNA 翻译为蛋白质的过程中对提前终止密码子进行通读,在多肽链中重新插入精氨酸,从而恢复蛋白质正常合成。
参考资料:
https://www.alltrna.com/press/alltrna-announces-approval-to-initiate-first-in-human-clinical-trial-of-ap003-the-first-trna-therapeutic-to-enter-clinical-trials
Kardigan 公布 Tonlamarsen 的 II 期临床试验结果
4 月 2 日,Kardigan 公司公布了其靶向血管紧张素原(AGT)的 ASO 药物 Tonlamarsen的 II 期临床试验 KARDINAL 结果。Tonlamarsen 是一款每月一次皮下注射的在研药物,通过抑制肝脏中 AGT 的生成,从源头调节肾素-血管紧张素-醛固酮系统(RAAS),旨在为急性重度高血压患者提供一种潜在的血压管理方案。Tonlamarsen 由 Ionis Pharmaceuticals 公司发现和开发,Kardigan 从 Ionis Pharmaceuticals 获得了该药的全球独家开发和商业化授权。
此次公布的结果显示,从基线到接受 Tonlamarsen 治疗后第 20 周,患者的血浆 AGT 水平显著下降,oSBP(office systolic blood pressure)也有临床意义上的降低(-6.7mmHg)。每月给药组患者在第 20 周时平均 AGT 水平降低 67%,而单次给药组患者的平均 AGT 水平降低了 23%。在血压控制方面,基线血压较高(>150mmHg)的患者 oSBP 的降幅最大,为 -8.9mmHg。在安全性上,Tonlamarsen 总体耐受性良好,未出现有临床意义的治疗相关低血压或高钾血症,其良好的疗效和安全性数据支持了公司在急性重度高血压患者中启动 IIb 期临床试验的计划。
参考资料:
https://www.businesswire.com/news/home/20260328084287/en/Kardigan-Announces-Positive-Phase-2-Data-for-Tonlamarsen-in-Patients-with-Uncontrolled-Hypertension-Presented-as-Late-Breaker-at-ACC.26-and-Simultaneously-Published-in-JACC
作者:李昱
排版/校对:Levi
审核:Shirley & Vivian
2026-04-01
·医学药事
以下文章来源于罕见病视界,作者罕见病视界
01
法布雷病基因疗法获 FDA 孤儿药认定,单次给药疗效可维持 5 年
近日,Glafabra Therapeutics 宣布,其治疗成人法布雷病的自体造血干细胞慢病毒基因疗法 GT‑GLA‑S03,获得美国 FDA 孤儿药资格认定。这一进展为全球法布雷病患者摆脱长期输注治疗带来新可能,也体现了罕见病细胞治疗的技术突破。
GT‑GLA‑S03 依托公司专属 Live‑cel™平台,对患者自体造血干细胞进行基因修饰,使其可稳定生成功能性 α‑Gal A。修饰后干细胞回输体内可分化为免疫细胞,全身持续分泌活性酶,从根源纠正酶缺乏问题。
该疗法预处理无需清髓,大幅降低严重感染风险,为门诊化、便捷化治疗创造条件,有望让患者告别长期酶替代治疗。
02
糖原贮积病 Ia 型基因疗法 6 年随访数据公布,长效稳定再获验证
Ultragenyx Pharmaceutical 公布 AAV 基因疗法 DTX401 治疗糖原贮积病 Ia 型(GSDIa)的 Ⅰ/Ⅱ 期 6 年长期随访结果。数据显示,该疗法可持续减少患者玉米淀粉摄入、改善空腹低血糖,长期安全性良好,为罕见病根治治疗与 AAV 技术长期应用提供关键依据。
DTX401(AAV8‑G6Pase)以高肝靶向 AAV8 载体递送经密码子优化的 G6PC 基因,通过单次静脉输注恢复肝脏生理性葡萄糖调控能力,实现从外源补充到内源调节的转变。
该疗法已获 FDA 孤儿药、快速通道、再生医学先进疗法认定,及欧盟优先药品、孤儿药资格。
03
再获 FDA 重磅认定!和誉医药 ABSK061 有望重塑软骨发育不全治疗格局
3 月 19 日,和誉医药宣布,自主研发的高选择性小分子 FGFR2/3 抑制剂 ABSK061 获美国 FDA 孤儿药资格,用于治疗软骨发育不全(ACH)。
ACH 为罕见遗传病,由 FGFR3 突变导致信号通路失衡,引发严重骨骼发育异常。ABSK061 可强效抑制靶点异常激活,口服给药显著提升儿童患者用药便利性与依从性。
目前 ABSK061 治疗 ACH 的注册性 Ⅱ 期临床正在推进,已于 2025 年 12 月完成国内首例患者给药,初步数据预计 2026 年下半年公布。该产品此前已获 FDA RPDD 认定,本次再获 ODD 将加速全球开发与申报。
04
信念医药血友病B 基因疗法登陆中国澳门,国际布局再下一城
3 月 19 日,信念医药集团宣布,波哌达可基注射液(商品名:信玖凝)获中国澳门药物监督管理局批准,用于治疗中重度血友病 B 成年患者。
血友病 B 因凝血因子 IX 缺乏导致凝血功能障碍,传统需定期输注因子替代治疗。信玖凝为 rAAV 基因治疗药物,以工程化 AAV843 衣壳精准靶向肝脏,搭载高活性 FⅨ‑Padua 基因,实现长效稳定表达,从根源改善凝血。
该产品 2025 年 4 月已在国内获批,2022 年获 FDA 孤儿药资格,2024年获 FDA 儿科罕见病资格与欧盟 ATMP 认证,2025 年获沙特孤儿药认定。武田中国负责内地、港、澳地区商业化。
05
国产首款血友病 B 基因治疗药物落地中国澳门,实现突破性上市
3 月 19 日,信念医药自主研发的波哌达可基注射液(信玖凝)获中国澳门批准,用于成人中重度血友病 B 治疗。
该药为重组腺相关病毒载体基因疗法,可将功能性 FⅨ 基因高效递送至肝脏,持续表达并分泌至血液,长期纠正凝血缺陷,为患者提供一次性根治性治疗选择。
06
进行性骨化性纤维发育不良新药 INCB000928 片拟纳入突破性治疗程序
3 月 18 日,CDE 官网公示,Incyte / 因塞特医药申报的 INCB000928 片拟被纳入突破性治疗程序,拟用于预防进行性骨化性纤维发育不良(FOP)患者的异位骨化。
INCB000928(zilurgisertib)为口服选择性 ALK2(ACVR1)抑制剂,靶向调控BMP 信号通路,从机制上阻断异常成骨,为 FOP 这一超高罕见病带来靶向治疗新希望。
07
长效软骨发育不全新药 3 期 104 周数据公布,上周获中国优先审评
3 月 16 日,丹麦 Ascendis 制药(中国子公司维昇药业)在 2026 ACMG 年会上公布,每周一次长效 ACH 新药那韦培肽(Navepegritide,TransCon CNP)关键 3 期研究 ApproaCH 104 周结果。
数据显示,52–104 周身高 Z 评分获益与前 52 周一致,疗效持续稳定;整体安全性耐受性良好,不良事件以轻中度为主,无治疗终止相关事件。该药近期刚获得中国优先审评资格。
08
锦篮基因 GC801 注射液获临床试验许可,用于 SMA 基因治疗前抗体降解
3 月 16 日,锦篮基因自主研发的 IgG 降解酶药物 GC801 注射液获国家药监局临床试验默示许可,适应症为 2 型脊髓性肌萎缩症基因治疗前 AAV 抗体降解。
GC801 为经工程化优化的 IdeS酶,可高效、特异性裂解人 IgG 全亚类,快速清除预存抗体,破除 AAV 基因治疗的免疫屏障,提升治疗成功率。这是锦篮基因第 5 款 1 类新药、第 8 项注册临床。
09
发作率最高降 100%!舶望制药 siRNA 疗法获 FDA 快速通道认定
3 月 16 日,舶望制药宣布,在研 siRNA 药物 BW‑20805 获 FDA 快速通道资格,用于治疗遗传性血管性水肿(HAE)。
BW‑20805 靶向前激肽释放酶(PKK),长效抑制靶点表达以预防水肿发作。目前 Ⅱ 期临床正在开展,预计 2026 年下半年完成并推进至 Ⅲ 期,有望为 HAE 提供便捷长效干预方案。
10
国内原创体内基因编辑疗法获美国 IND,进入国际多中心 Ⅱ/Ⅲ 期
3 月 13 日,上海尧唐生物宣布,自主研发的 α‑1 抗胰蛋白酶缺乏症(AATD)体内基因编辑疗法 YOLT‑202 获美国 FDA IND 批准,将启动开放标签、单次给药的扩展 Ⅱ/Ⅲ 期国际多中心临床。
前期 IIT 临床显示,YOLT‑202 可快速提升功能性 AAT 水平,高剂量组可达正常范围,有望实现 “一次给药、长期获益”,为 AATD 带来全球领先的治愈型方案。
11
全球首个!诺华司库奇尤单抗获 FDA 新适应症,已纳入中国医保
3 月 13 日,诺华宣布,司库奇尤单抗获美国 FDA 批准,用于治疗 12 岁及以上中重度化脓性汗腺炎(HS)儿科患者。
作为全人源 IL‑17A 抑制剂,该药精准阻断炎症核心通路,是该人群唯一获批的 IL‑17A 靶向生物制剂,可按体重个体化给药。该药物此前已被纳入中国医保目录。
12
神拓生物 ST002 获 FDA 罕见儿科疾病资格,靶向 NF2 相关神经鞘瘤病
神拓生物宣布,自研基因治疗药物 ST002 获美国 FDA 罕见儿科疾病资格认定,用于神经纤维瘤病 II 型相关神经鞘瘤病(NF2‑SWN)。
ST002 基于公司第五代慢病毒载体平台,靶向补充 NF2 基因突变缺陷,临床前研究显示可显著抑制肿瘤、促进凋亡,安全性与有效性突出,公司将加速推进临床开发。
13
石药伊络达 ® 上线阿里健康,拓宽间质性肺病患者购药渠道
石药集团抗纤维化药物乙磺酸尼达尼布软胶囊(伊络达 ®)在阿里健康平台首发上市,为纤维化性间质性肺疾病患者提供院外便捷购药选择。
尼达尼布为小分子酪氨酸激酶抑制剂,获批用于 IPF、SSc‑ILD、进行性表型 ILD 等,可延缓肺功能下降,是国内一线抗纤维化用药。
14
恒瑞医药阵发性睡眠性血红蛋白尿症新药上市申请获受理
恒瑞医药子公司成都盛迪医药提交的 1 类新药富马酸立康可泮胶囊上市申请获
国家药监局受理,用于治疗既往经 C5 抑制剂治疗仍存在贫血的成人阵发性睡眠性血红蛋白尿症(PNH)。
该药为口服补体 B 因子抑制剂,同时控制血管内、外溶血,弥补 C5 抑制剂不足,口服剂型提升依从性。其用于初治 PNH 的上市申请已被纳入优先审评,同时布局 IgA 肾病等适应症。
免责声明:本公众号发布的文章均为促进医学同行的交流与学习;不用于任何商业用途。我们尊重原创作品。选取的文章已明确注明来源和作者,版权归原作者所有,如涉及侵权或其他问题,请联系我们进行删除。
来源:罕见病视界
编辑:小付
审核:肖林
2026-03-31
·医药临床
本月多项重磅数据公布,从ELCC到NEJM,创新疗法密集释放积极信号,全球研发格局加速演进2026年3月,全球医药研发领域持续保持高活跃度。从欧洲肺癌大会(ELCC)到阿尔茨海默病与帕金森病国际会议(AD/PD™ 2026),从《新英格兰医学杂志》到《柳叶刀》,肿瘤双抗、PROTAC蛋白降解剂、CAR-T细胞疗法、AI手术机器人等多项前沿技术接连释放重磅信号。同时,中国企业在创新药研发与BD交易上继续展现出强劲的国际竞争力。01 肿瘤领域:双抗药物领跑,CAR-T与ADC多点开花本月,肿瘤治疗领域最受关注的当属双抗类药物在肺癌一线治疗中的突出表现。康方生物依沃西数据再升级:在ELCC 2026上,康方生物公布了PD-1/VEGF双抗依沃西的HARMONi-2研究生活质量分析数据。结果显示,依沃西不仅显著延长了无进展生存期(11.14个月 vs 5.82个月),在患者的整体健康状况、躯体功能以及咳嗽、呼吸困难等肺癌典型症状的控制上,也全面优于帕博利珠单抗。这意味着该药物有望成为PD-L1阳性非小细胞肺癌一线治疗的新标准。BioNTech双抗与ADC管线密集亮相:BioNTech在ELCC上披露了其PD-L1×VEGF-A双抗Pumitamig的多项数据。该药物在非小细胞肺癌多个亚型(包括EGFR突变患者)及小细胞肺癌一线治疗中均展现出积极疗效,安全性可控。数据显示,在EGFR突变NSCLC患者中,Pumitamig联合化疗展现出具有临床意义的生存获益。此外,其HER3靶向ADC(BNT326/YL202)在非小细胞肺癌中的首次临床数据也同步公布,在既往接受过标准治疗后进展的晚期或转移性NSCLC患者中展现出抗肿瘤活性和良好的安全性。同时,BioNTech的另一款CTLA-4抗体Gotistobart在2线及以上鳞状NSCLC患者中,与标准化疗相比显示出54%的死亡风险降低,具有临床意义的抗肿瘤活性。Elicera Therapeutics CAR-T疗法ELC-301表现惊艳:Elicera Therapeutics公布了其iTANK平台武装的CD20靶向CAR-T疗法ELC-301在复发/难治性B细胞淋巴瘤患者中的I/IIa期CARMA研究数据。结果显示,在最高剂量组(队列3)治疗的前两名患者中,均达到完全代谢缓解(CMR),且未观察到剂量限制性毒性。截至目前,8名接受治疗的患者中,6名在第1个月达到CMR,疾病控制率达100%,总缓解率为7/8,最佳缓解持续时间长达至少12个月。原位转分化技术迈入临床:纽伦捷生物的NRG-103注射液针对胶质母细胞瘤的注册临床一期已在武汉启动。该技术通过将残余肿瘤细胞“转化”为正常细胞,从根源上降低耐药与复发风险,是全球首个实现该技术肿瘤基因疗法获批中美双IND的企业。TGCT新药III期结果登上《柳叶刀》:和誉医药宣布,其CSF-1R抑制剂Pimicotinib治疗腱鞘巨细胞瘤(TGCT)的全球III期MANEUVER研究结果发表于国际顶级医学期刊《柳叶刀》。数据显示,该药物在TGCT患者中取得了显著的疗效和良好的安全性。该药已于2025年12月在中国获批上市,美国NDA正在审评中。其他临床进展:翰森制药的GLP-1/GIP双激动剂奥莱泊肽在肥胖治疗的III期临床中显示出积极疗效。02 神经退行性疾病领域:PROTAC与基因疗法齐头并进本月,神经领域迎来多项重磅进展,多款First-in-class药物释放关键临床数据。Arvinas PROTAC降解剂ARV-102数据惊艳:Arvinas在AD/PD™ 2026会议上公布了其口服PROTAC降解剂ARV-102的I期临床数据。该药物靶向LRRK2蛋白——帕金森病的关键致病靶点。结果显示,在帕金森病患者中,ARV-102实现了脑脊液中LRRK2蛋白超过50%的降解,且剂量依赖性良好。更重要的是,该药物同时降低了与神经炎症相关的生物标志物(如CD68、GPNMB)。ARV-102总体安全耐受性良好,未报告严重不良事件。基于此积极数据,Arvinas计划于2026年第二季度启动进行性核上性麻痹(PSP)的Ib期临床试验。罗氏BTK抑制剂fenebrutinib III期临床成功:罗氏宣布其口服、脑渗透性BTK抑制剂fenebrutinib在复发性多发性硬化症(RMS)的III期FENhance 1研究中达到主要终点。数据显示,fenebrutinib相比特立氟胺使年复发率降低51%,与此前公布的FENhance 2研究结果(降低59%)一致。两项研究结果合计相当于每17年发生一次复发。fenebrutinib有望成为首个同时适用于RMS和原发性进行性多发性硬化症(PPMS)的高效口服治疗药物。AC Immune TDP-43 PET示踪剂首次人体成像:AC Immune在AD/PD™ 2026上展示了其TDP-43 PET示踪剂ACI-19626的I期临床数据。这是全球首次实现在活体人脑中检测TDP-43病理的影像学证据,有望为ALS、FTD等多种TDP-43蛋白病提供精准诊断工具。齐鲁制药阿尔茨海默病1类新药获批临床:3月13日,CDE官网显示,齐鲁制药自主研发的1类新药QLH2405注射液获得临床试验默示许可,拟定适应症为阿尔茨海默病源性轻度认知障碍和轻度阿尔茨海默病。跃赛生物iPSC来源癫痫细胞疗法获FDA IND批准:3月12日,跃赛生物自主研发的针对癫痫的iPSC(诱导多能干细胞)来源异体细胞药物UX-GIP001注射液获得美国FDA IND批准。这是全球首款进入临床阶段的iPSC来源异体癫痫细胞治疗药物。拜耳基因疗法管线更新:拜耳公布了其临床开发管线进展,其中包括两款针对帕金森病的基因疗法——Bemdaneprocel(细胞疗法)已进入III期临床,AB-1005(AAV基因疗法)处于II期临床阶段。03 自身免疫疾病领域:大额BD交易频现,新药数据登顶NEJM本月自身免疫疾病领域同样动作频频,罗氏重磅III期数据登上NEJM。罗氏Gazyva治疗狼疮III期数据登顶NEJM:罗氏宣布,其Type II抗CD20单抗Gazyva(obinutuzumab)治疗系统性红斑狼疮(SLE)的III期ALLEGORY研究结果发表于《新英格兰医学杂志》。数据显示,超过四分之三(76.7%)接受Gazyva联合标准治疗的患者在52周时达到SRI-4应答(评估疾病严重程度和症状的指标),而安慰剂组为53.5%。Gazyva在包括BICLA应答、糖皮质激素减量等所有关键次要终点上均显著优于安慰剂。如果获批,Gazyva将成为首个用于SLE的Type II抗CD20疗法。德琪医药与优时比达成全球许可协议:德琪医药将其临床前阶段的CD19/CD3双抗ATG-201授权给优时比(UCB),用于治疗B细胞相关的自身免疫性疾病。根据协议,德琪医药将获得8000万美元首付款及近期里程碑付款,以及超11亿美元的后续里程碑付款。宜明昂科红斑狼疮新药获批临床:宜明昂科宣布,其全球首创的CD47×CD20双靶点分子IMM0306的皮下注射剂型(IMM0306S)获中国NMPA批准临床,用于治疗系统性红斑狼疮。相较于静脉输注,皮下制剂可降低峰浓度、减少输注反应,显著提升患者用药便利性。益方生物TYK2抑制剂获FDA批准II期临床:益方生物自主研发的TYK2抑制剂D-2570获美国FDA批准,开展治疗银屑病的II期临床试验。此前该药物在中国完成的银屑病II期临床试验已显示出显著疗效和良好安全性。深信生物mRNA疗法IND获批:深信生物宣布其mRNA候选药物IN026获美国FDA批准临床试验,该药物针对难治性痛风,是mRNA技术在慢性代谢疾病领域的重要探索。恒瑞医药海曲泊帕新增SAA适应症:恒瑞医药宣布,其自主研发的1类创新药海曲泊帕乙醇胺片获得国家药品监督管理局批准,新增“联合免疫抑制治疗适用于15岁及以上初治重型再生障碍性贫血(SAA)患者”的适应症。04 代谢与心血管疾病领域:GLP-1新星崛起,PCSK9抑制剂数据将亮相诺和诺德/联邦制药UBT251 II期临床成功:诺和诺德与联邦制药联合开发的GLP-1/GIP/胰高血糖素三靶点激动剂UBT251在中国2型糖尿病患者中的II期临床试验达到主要终点。数据显示,治疗24周后,UBT251最高可使HbA1c降低2.16%,体重降低9.8%,疗效优于司美格鲁肽1mg组(HbA1c降幅1.77%,体重降幅4.8%)和安慰剂组。基于此结果,诺和诺德计划于2026年下半年启动全球II期临床试验。默沙东口服PCSK9抑制剂III期数据即将亮相ACC.26:默沙东宣布,将在美国心脏病学会(ACC.26)年会上公布其口服PCSK9抑制剂enlicitide的III期CORALreef AddOn试验结果。该药物有望成为首个获批的口服PCSK9抑制剂,为他汀类药物治疗后血脂仍不达标的患者提供新的治疗选择。此外,默沙东还将公布sotatercept在CpcPH-HFpEF(联合性毛细血管前和后毛细血管性肺动脉高压合并射血分数保留的心力衰竭)患者中的II期CADENCE试验数据。Rhythm Pharmaceuticals setmelanotide III期研究未达主要终点:Rhythm Pharmaceuticals公布了setmelanotide在MC4R通路罕见遗传性肥胖患者中的III期EMANATE研究结果。四个遗传亚组研究均未达到预设的主要终点。然而,事后分析显示,在POMC/PCSK1杂合变异和SRC1基因变异患者中,setmelanotide在52周时实现了具有统计学意义的BMI降低。05 新兴技术与行业趋势:AI手术机器人落地,全球研发格局重塑在技术与模式创新层面,本月也传来多项值得关注的信号。国内首款胰腺疾病智能体与手术机器人发布:北京大学第三医院在中关村论坛上发布了全国首个覆盖胰腺疾病全病程的“胰腺疾病诊疗智能体”,以及全球首台实现椎板自主切削操作的“脊柱椎板减压手术机器人”。这表明中国在医疗AI与高端手术机器人领域的自主创新能力正在加速落地。全球研发格局加速重构:数据显示,中国目前占全球创新药候选药物的20%以上,中国启动的临床试验数量已超过美国,主要由I期和I/II期项目驱动。全球早期药物研发格局正从美国主导转向以美国和中国为中心的“双中心”结构。体内CAR-T技术取得突破:加州大学旧金山分校在《Nature》上发表研究,开发了一种双载体系统,可在体内直接生成CAR-T细胞,为人源化小鼠模型中的B细胞发育不全、血液系统恶性肿瘤和实体瘤提供了治疗水平的CAR-T细胞。这一技术有望大幅降低CAR-T疗法的生产成本和制备时间。国家药监局批准罗赛促红素α注射液上市:国家药监局批准广东三生制药有限公司申报的罗赛促红素α注射液(商品名:新比澳)上市,用于治疗因慢性肾脏病引起的贫血且正在接受促红细胞生成素治疗的血液透析患者。06 FDA审评动态与行业新闻3月迎来多项FDA审评关键日期,包括:首个用于治疗丁肝的药物bulevirtide、首个用于先天性耳聋的基因疗法DB-OTO、以及首个每周一次的胰岛素icodec(Awiqli)等。siRNA疗法获快速通道资格:舶望制药宣布其在研siRNA疗法BW-20805获得美国FDA授予快速通道资格,用于治疗遗传性血管性水肿(HAE)。该药物靶向前激肽释放酶(PKK)。---结语2026年3月的全球医药研发,既是数据的集中披露期,也是多项前沿技术从概念走向临床的里程碑时刻。双抗药物在肿瘤与自免领域的持续拓展、PROTAC等新技术在神经退行性疾病中的首次临床验证、CAR-T细胞疗法在淋巴瘤中的持续突破、GLP-1三靶点激动剂在代谢疾病中的惊艳数据、AI与机器人的深度融合、以及中国在全球研发网络中角色的持续强化,共同构成了本月行业发展的多条主线。未来几个月,随着更多临床数据与BD交易的落地,全球医药创新格局或将迎来新一轮洗牌。---参考资料:Roche官网、Arvinas官网、BioNTech官网、Merck官网、Novo Nordisk官网、Rhythm Pharmaceuticals官网、Elicera Therapeutics官网、和誉医药官网、齐鲁制药、跃赛生物、恒瑞医药、美迪西、中国食品药品网等
100 项与 BW-20805 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 遗传性血管性水肿 | 临床2期 | 美国 | 2025-02-28 | |
| 遗传性血管性水肿 | 临床2期 | 中国 | 2025-02-28 | |
| 遗传性血管性水肿 | 临床2期 | 德国 | 2025-02-28 | |
| 遗传性血管性水肿 | 临床2期 | 意大利 | 2025-02-28 | |
| 遗传性血管性水肿 | 临床2期 | 波兰 | 2025-02-28 | |
| 遗传性血管性水肿 | 临床2期 | 西班牙 | 2025-02-28 |
登录后查看更多信息
临床结果
临床结果
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用