9
项与 阿达木单抗生物类似药 (百奥泰生物) 相关的临床试验一项多中心、前瞻性、观察性 IV 期临床研究评估格乐立®(阿达木单抗注射液)治疗儿童及青少年重度斑块状银屑病(pPsO)的疗效和安全性 (PISCES 研究)
评估格乐立®(阿达木单抗注射液)治疗 4-18 岁儿童及青少年重度斑块状银屑病的疗效和安全性。
/ Not yet recruitingN/AIIT A Multicenter, Prospective, Observational Real World Study For the Efficacy and Safety of a Adalimumab Biosimilar (Geleli) in Rheumatoid Arthritis.
The purpose of this multicenter, prospective, Observational study is to assess the Efficacy and Safety of an Adalimumab Biosimilar (Geleli) in Rheumatoid Arthritis in the real world setting.
A Multicenter, Prospective, Post-marketing Evaluation of QLETLI (Adalimumab Injection) Treatment Clinical Study on Efficacy and Safety of Non-infectious Uveitis (UV)
This is a multicenter, prospective, post-marketing clinical study with a total of 60 uveitis (UV) subjects planned to be enrolled.
Screening period (-2
0 weeks) ,Treatment period (1-22 weeks), Follow-up period, At the same time, plasma concentration will be determined
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的临床结果
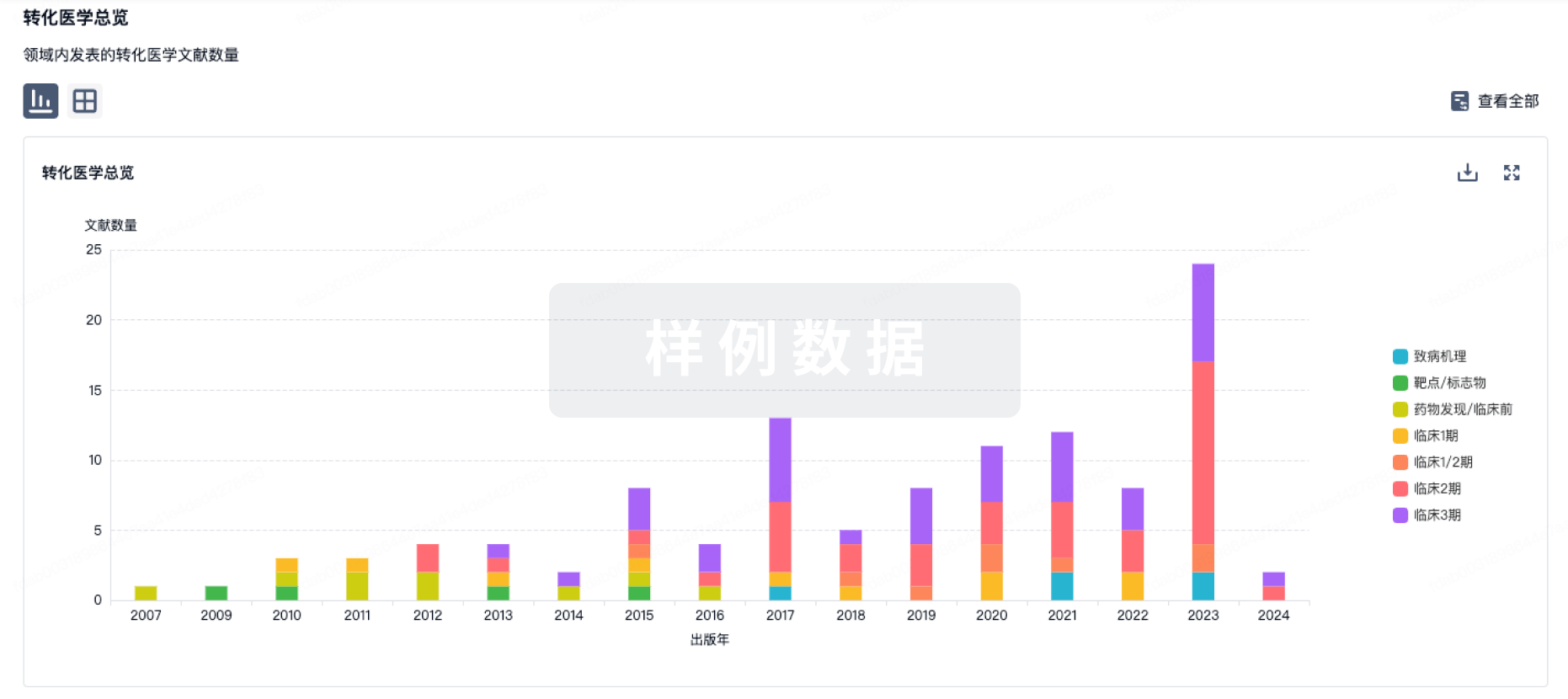
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的转化医学
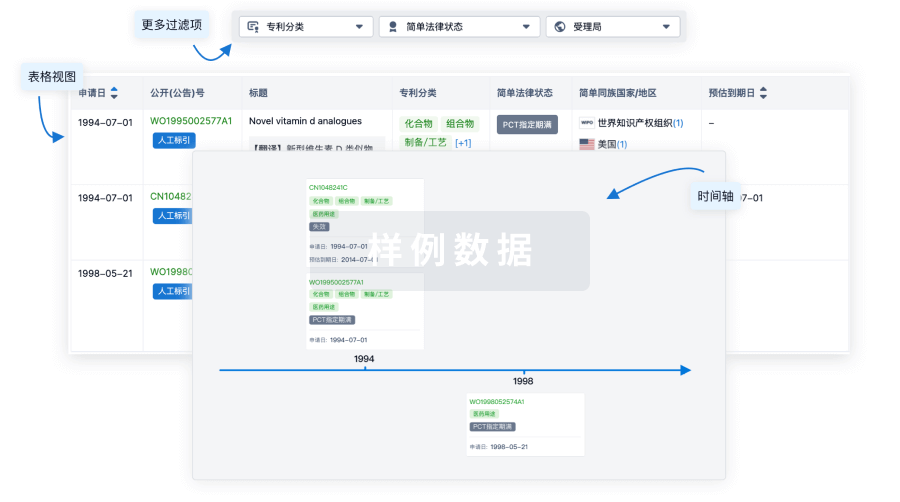
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的专利(医药)
397
项与 阿达木单抗生物类似药 (百奥泰生物) 相关的新闻(医药)百奥泰生物制药股份有限公司(证券代码:688177)是一家基于科学而创新的全球性生物制药企业(以下简称“百奥泰”或“公司”)。近日,公司在2026年欧洲风湿病学大会上(EULAR)展示了BAT2506(一款参照欣普尼®(戈利木单抗)开发的生物类似药)的临床3期研究结果。BAT2506 是一种肿瘤坏死因子α(TNF-α)的重组人源化单克隆抗体。研究概要内容可在2026年欧洲风湿病学大会(EULAR)网站上查阅,大会于2026年6月3日-6月6日同时在线上及英国伦敦现场进行。
3期临床对照试验的数据表明,BAT2506 具有与原研药等同的疗效且具有可比的安全性和免疫原性。这是一项随机、双盲、为期60周的3期国际多中心临床研究,共入组704例活动性银屑病关节炎患者。在52周的治疗期内,患者每4周接受一次BAT2506或欣普尼®(欧洲产品)的皮下注射给药,剂量为50mg。
该研究的主要终点为在第14周的ACR20反应率。第14周时,BAT2506和原研药欣普尼®(欧洲产品)组的ACR20反应率分别为79.26% vs 77.08%;在主要估计目标框架下,两组间的ACR20反应率差异均落在预先设定的等效区间内,为2.36% (90% CI (-2.91% , 7.63%); 95% CI (-3.92% , 8.64%) )。同时,两个治疗组也具有可比的戈利木单抗平均血清药物浓度、治疗相关不良事件(TEAE)发生率及抗药抗体阳性率,从而也证明两组药物在药代动力学、安全性和免疫原性上具有可比性。
主要研究者四川大学华西医院刘毅教授表示:“全球多中心3期临床试验结果证实,BAT2506 在关键疗效终点 ACR20 反应率、体内血药浓度、安全性与免疫原性上和原研戈利木单抗高度等效,充分印证这款生物类似药可满足银屑病关节炎临床规范化治疗需求。”
(EULAR大会现场--刘毅教授)
关于BAT2506临床3期试验设计
该临床试验是一项全球、随机、多中心、双盲、平行、阳性对照的3期研究。其旨在700例对活动性银屑病关节炎患者中,对照和评估BAT2506与欣普尼®在安全性、疗效、免疫原性和药代动力学方面的表现。入组的704例患者中,有92名(13.1%)来自亚洲,612名(86.9%)来自欧洲。有关BAT25063期临床试验的更多信息,包括患者入选和排除标准以及临床主要和次要终点等指标,可访问: Study Details | NCT05046431 | Comparative Study of BAT2506 With Simponi® in Participants With Active Psoriatic Arthritis | ClinicalTrials.gov
关于百奥泰
百奥泰是一家立足于广州、放眼于全球、基于科学而创新的生物制药企业。公司聚焦肿瘤、自身免疫、心血管、眼科等重大疾病,深耕创新药与生物类似药研发、产业化与全球商业化布局。公司多款产品落地海内外,托珠单抗 TOFIDENCE™是首个由中国药企研发、生产且获得美国FDA批准上市的单克隆抗体药物、IMMGOLIS™是全球首个获FDA批准上市的戈利木单抗生物类似药、阿达木单抗格乐立®是首个国产的阿达木单抗生物类似药。乌司奴单抗及贝伐珠单抗生物类似药等核心品种已先后在中国、美国、欧盟、英国、巴西、瑞士等多国获批上市。公司另有多款候选药物进入后期临床试验,其中肿瘤领域主要聚焦PD-1后时代的肿瘤免疫治疗和抗体药物偶联体(ADC)靶向药物开发。
百奥泰始终以患者的福祉作为首要核心价值,通过创新研发,为患者提供安全、有效、可负担的优质药物,以满足亟待解决的治疗需求。欲了解更多信息,请访问官网www.bio-thera.com,或关注我们的X(@bio_thera_sol)和微信公众号(百奥泰)。
百奥泰前瞻性声明
本新闻稿包含了BAT2506或百奥泰及产品线相关的前瞻性声明。由于某些重要因素可能会影响公司的实际结果,特此提醒读者注意不要过分依赖该前瞻性声明。这些前瞻性语句包括但不限于包含意愿、将要、可能、潜在性、预测、计划、估计、预期等类似陈述。它们都应被视为百奥泰基于截至本新闻稿发布之日可获得的信息的合理假设,并不保证未来的表现或发展。由于多种因素,实际结果和事件可能与前瞻性声明中包含的信息存在重大差异,这些因素包括但不限于本产品可能不会获得受理或批准,以及药物研究、开发和商业化中固有的风险和不确定性,例如临床前和临床研究的风险和不确定性以及能否获得药政部门的批准。其他风险因素包括生产、分销、营销、竞争、知识产权、药物功效和安全性方面的风险和不确定性,国家及全球财务与医疗状况的变化,公司财务状况的变化以及适用法律法规的变化等。本新闻稿中包含的任何前瞻性声明仅针对截止于作出声明之日的情况。除非法律要求,否则百奥泰没有义务更新本新闻稿中包含的任何前瞻性声明,以反映本新闻稿发布之日以后的新信息和事件,公司观点的改变或其他情况。
参考文献:
ACR20即ACR(美国风湿病学会)规定指标达到20%及以上的临床改善。
欣普尼®是强生公司的注册商标。
伊顿健康导读:银屑病的治疗已经进入靶向治疗时代,生物制剂和小分子药物的应用显著改善了患者的生活质量。我国批准上市并已用于治疗银屑病的生物制剂共6种,包括肿TNF-α抑制剂、IL-12/23抑制剂、IL-23抑制剂、IL-17A抑制剂、IL-17A/F及IL-36抑制剂;小分子口服靶向药包括PDE4抑制剂、JAK1抑制剂、JAK1/3抑制剂TYK2抑制剂4 种药物。药物的价格和医保进展几乎是每个中重度银屑病患者关心的,本文将现已在中国获批上市的生物制剂和小分子靶向药的用法用量、价格、医保进展做了汇总,供病友们参考。银屑病生物制剂IL-17A抑制剂用法用量+价格这类药起效快,对中重度斑块状银屑病效果好。司库奇尤单抗(可善挺):第0、1、2、3、4周,每次2支,之后每月2支维持。目前每支约778.65元,第1年大概32支。已进医保。依奇珠单抗(拓咨):首次注射2支,第2、4、6、8、10、12周各1支,然后1支/每月维持。每支约1218元,首年约16支。已进医保。赛立奇单抗(金立希):第0、2、4、6、8、10、12周每次2支,以后2支/每个月维持。每支756元,首年约32支。已纳入医保。夫那奇珠单抗(安达静):第0、2、4周每次2支,以后2支/每月维持。743.5元/支。第1年共需28支。已纳入医保。安沐奇塔单抗(益赛拓):有两种用药方案,第一种第0周2支,2/4/6/8/10/12周每次1支,以后1支/4周维持。第二种首次给药2支,4//8/12周每次2支,以后2支/8周维持;一般推荐第二种用药方案。1520元/支,暂未纳入医保,但药企有推出援助活动。夫那奇珠单抗(安达静):第0、2、4周每次2支,以后2支/每月维持。743.5元/支。第1年共需28支。已纳入医保。布罗利尤单抗(立美芙):第0周一支,从第2周开始,每2周1支维持。约3000-5000元/支,暂未纳入医保。IL-23抑制剂用法用量+价格这类药维持期打针间隔长,更加方便。古塞奇尤单抗(特诺雅):第0、4周每次1支,从第8周开始,每2个月1支维持。首年7针,3680元/支,已进医保。替瑞奇珠单抗(益路取):第0、4周每次1支,从第12周开始,每3个月1支维持。首年5针,4360元/针,已进医保。匹康奇拜单抗(信美悦):第0、4、8周每次2支,第20周开始,以后每3个月1支维持。首年9针,6500元/针,暂未纳入医保,但目前药企有推出援助活动。IL-23/12抑制剂用法用量+价格乌司奴单抗(喜达诺):首次和第4周各打1支,之后每3个月1支。第一年5支。4015元/支,已进医保。乌司奴单抗(赛乐信):首次和第4周各打1支,之后每3个月1支。第一年也是5支。3614元/支,已进医保。依若奇单抗(爱达罗):第0、4周每次1支,以后1支/每3个月维持。首年5支,3830元/支,已进医保。乌司奴单抗(恩益克):2026年5月22日新上市,暂未纳入医保。TNF-α抑制剂用法用量+价格这是比较经典的一类,特别是阿达木单抗,市面上品牌很多。修美乐(进口原研):第0周2支,一周后1支,往后每两周1支。1290元/支,已进医保。格乐立、汉达远、安健宁、苏立信(国产):这些国产生物类似药用法用量相同,价格都在1000元左右,均已进医保,另外也有援助活动。IL-17A/F和IL-36抑制剂用法用量+价格比奇珠单抗(倍捷乐):每4周一次,每次1支,约2500元/支,暂未纳入医保,但目前有援助活动。佩索利单抗(圣利卓):是专门针对脓疱型银屑病的生物制剂,26436元/盒,已纳入医保。小分子口服靶向药用法用量+价格对于怕打针或者想口服治疗的患者,小分子靶向药是个新选择。TYK2抑制剂,氘可来昔替尼(颂狄多):既可以治疗银屑病,又可以治疗银屑病关节炎,每天口服1次, 28片/盒,1484元/盒,已进医保。JAK1抑制剂,乌帕替尼(瑞福):也是既可以治疗银屑病,又可以治疗银屑病关节炎,每天/1片,28片/盒,1833.44元/和,也已经进入医保。JAK1/3抑制剂:托法替布(尚杰):主要用于银屑病关节炎,常释剂5mg每日2次;缓释剂11mg每日1次。785.91((5mg×28片),1999元(11mg×30片),已进医保。PDE4抑制剂,阿普米司特(欧泰乐):早晚各1次/1片,30mg×60片/盒,约847元/盒,已纳入医保。伊顿健康温馨提示上述药品价格主要参考市场信息,绝大多数主流生物制剂和口服药都已纳入国家医保,没纳入医保的药物,也有相关援助活动,患者实际自费会更低。各地医保报销比例会有差异,具体以当地医保政策为准。治疗银屑病,现在有了很多好武器,虽然依然无法治愈,但皮损清除已经不是问题。尽管如此,银屑病患者在用药前,也应该谨遵医嘱,必要的检查不可少,切勿自行用药。了解这些信息,希望能帮助你和医生一起,制定出更适合你的治疗方案。如今银屑病/强直性脊柱炎领域创新药研发均在飞速发展,银屑病临床项目包括IL-17A抑制剂,IL-23 抑制剂、TYK2 抑制剂、JAK 抑制剂等多个靶点。强直性脊柱炎临床项目包括IL-17A抑制剂、JAK抑制剂等,生物制剂与口服靶向药均有大量临床研究持续推进。感谢阅读,希望内容能对你有所帮助!本文仅做参考,不构成对任何药物或诊疗方案的推荐、推广或宣传,也不可替代专业医疗建议。如有问题,请咨询医疗卫生专业人士。材料图片等源自网络,侵删。
2026年4月14日晚上,百奥泰发了份公告。
公司要把上市不到两年的国家1类新药贝塔宁,连上市许可证、知识产权、生产技术、商业化权益,整个打包转让给乐普医疗的子公司乐普药业。
价格谈好了,4.5亿元。
一款被寄予厚望的心血管创新药,刚上场就换东家,到底发生了什么?
01
百奥泰会卖掉这款药,不是因为它做不出好药,而是因为它从一开始就没打算在心血管赛道上扎根。
2025年1月。
广州一家三甲医院心内科诊室里,有个急性冠脉综合征患者正在接受一种新药的注射。那就是贝塔宁——枸橼酸倍维巴肽注射液——第一次在全国开出正式处方。
这种场面,好多年没见过了。
一款国家1类化学新药,研发代号BAT2094,从实验室走到患者面前,走了十几年。搞研发的人看了,谁不得激动一阵子。
可谁也没想到,这个故事的转弯来得这么快。
02
那贝塔宁到底是一款什么药。
这不是什么仿制药。
是百奥泰自己研发出来的,有完整的自主知识产权,国家1类化学新药,还是国家重大新药创制科技重大专项支持的项目。
它的核心机制挺有说法的——能同时锁定两种不同的整合素受体。
一种叫αIIbβ3,是血小板聚集的关键受体。另一种叫αvβ3,跟血管壁细胞增生有关。两种都锁住,什么意思呢?
就是既能防支架内血栓,又能减少出血风险,还能抑制血管壁增生、降低再堵的几率。
简单讲,别人可能是一个靶点打天下,它是双保险。
03
数据到底怎么样。
III期临床试验的核心数据,把很多同行甩开了一个档次。
主要终点风险比值0.57。95%的置信区间0.35到0.94,P值0.026。
用人话说就是:在现有标准治疗基础上,用了贝塔宁的患者,复合终点事件发生率又降低了43%以上。
在心血管药物这个竞争已经卷到不行的赛道里,这个成绩相当能打。
I期临床数据显示,给药后10分钟,血小板聚集抑制率就超过了80%,而且恒速滴定时一直很稳定。
停药后4小时内恢复血小板功能。
口服抗血小板药起效至少得等两个小时,停药后恢复得几天。这个速度,对手术台上的人来说就是救命稻草。
04
2024年6月,国家药监局的批文下来了。
适应症瞄准的是做经皮冠状动脉介入手术的急性冠脉综合征患者。
乐普医疗公告里披露的数据说,国内一年PCI手术量大约200万例,其中因为心梗做手术的占了快三分之一。
这正是贝塔宁的核心患者群。
围手术期抗栓药物的市场空间有多大,不用多说。
手里捏着这么一张牌,按说怎么也该打出去试试。可百奥泰的选择让很多人都没想到。
05
百奥泰这家公司骨子里是个什么基因。
总部在广州,2003年成立的,2020年2月在科创板上市。
它身上的标签从成立那天起就只有两个:创新药和生物类似药。赛道始终锁在肿瘤、自身免疫性疾病、眼科、全是生物大分子领域。
到2025年8月,百奥泰手里已经有5款上市产品。包括治疗自身免疫疾病的格乐立、普贝希、施瑞立,还有就是贝塔宁。另外还有3款拿到美国FDA批准的。
仔细看这个产品列表就会发现,贝塔宁是唯一一个心血管领域的品种,其他全是生物大分子。
它在百奥泰的管线里,属于那种很好,但不太合群的存在。
06
那为啥不自己卖呢。再看一组数字就明白了。
2025年全年,百奥泰营收9.35亿元,同比增长超过25%,势头看着不错。但归母净利润亏了3.32亿元。
虽然比前一年减亏了近四成,亏损还是在持续。
更让人揪心的是负债这块。公司归属于母公司的所有者权益,从2024年末的7.08亿元,降到了2025年末的3.72亿元,直接腰斩。
资产负债率到2025年末已经83.56%以上了。
当然,公司自己在业绩说明会上解释过,这个高负债率里有很大一块是合同负债——授权项目合作收来的预付款项,7.7个亿,不能算成实打实的欠债。剔除这块,负债率是52.51%。
但不管怎么解释,账面上看,现金流压力是实打实的。
研发投入还在烧钱。
2025年研发总投入8亿元,占了营收的八成多。做创新药就是这样,一边烧钱,一边等着回血。
07
2026年4月14日晚上,百奥泰发出了那份让整个医药投资圈炸开锅的公告。
公司开完董事会第七次会议,审议通过了转让贝塔宁品种权益的议案。
连药品上市许可证、全部知识产权、生产技术、商业化权益,整个打包卖给乐普医疗的控股子公司乐普药业。
4.5亿元,含税,分五期支付。
在完成药品上市许可持有人转移和生产转移获批之后,付完全部款项。除此之外,还有个销售分成——按贝塔宁年度净销售额的个位数百分比算,最长分十年。
消息一出,议论声四起。
有人替百奥泰惋惜——舍不得啊,一款刚上市的1类新药,有潜力、有数据、有市场,就这么拱手让人了。
也有人表示理解——这恰恰是一家研发型生物药企在最合适的时机做出的战略选择。
到底怎么看这笔交易。
08
先看接盘的是谁。
乐普医疗,在心血管领域泡了二十多年。
它的产品覆盖全国1200多家心脏诊疗中心,手里握着国内最成熟的PCI全产业链解决方案——冠脉支架、结构性心脏病器械、心脏节律管理、心血管药物,配套的院内推广体系早就搭得稳稳当当。
贝塔宁作为PCI围手术期抗栓用药,使用场景和乐普现有的器械产品高度重合。
它一进乐普的系统,就能直接嵌入现有的心内科客户网络。不需要从头建渠道,不需要重新搭学术推广体系,直接在现有轨道上跑起来就行。
比起自己立项、从头搞研发、花十年才能搞出一款同类创新药,乐普这笔账算得很清楚——4.5亿元,拿下一款已经完成III期临床、已经获批上市的1类新药的全部权益,还能收未来十年的销售分成。
用最低的时间成本和研发风险,快速补强心血管药物管线。
09
那百奥泰这边呢。
4.5亿的现金一次性流进来,再加上未来十年的销售分成。
这笔钱怎么用?往BAT8008、BAT2506这些更高优先级的管线上砸。
BAT2506,戈利木单抗生物类似药,2026年5月拿到了FDA的上市批准通知,美国商品名Immgolis™。欧盟EMA也批了,还向巴西卫生监督局递交了申请,商业化授权合作覆盖了118个国家和地区。这种全球化的盘子,需要的资金量不是一个级别。
BAT8008,TROP-2 ADC,在宫颈癌、HER2阴性乳腺癌等多个适应症上势头很猛。
2026年ASCO年会上,BAT8008在宫颈癌的I期临床最新结果要做12分钟口头报告。联合BAT1308在肺癌和TNBC里的探索性研究,样本量还在扩大。
这些才是支撑百奥泰未来估值逻辑的核心骨架。
10
再往深一层看,这笔交易暴露了一个很多创新药企都得面对的现实:研发能力和商业化能力,是两套完全不同的本事。
做出来一个药是一回事,卖好一个药是另一回事。
尤其是在心血管这种高度依赖科室渠道的赛道里——得跟心脏诊疗中心深度绑定、跟介入器械协同推广、跟心内科医生建立长期学术关系。这是一套需要花好多年才能搭起来的专科渠道体系。
百奥泰擅长的,是生物类似药的工艺平台和创新生物药的临床开发。它在生物类似药领域积累的推广能力,没法简单平移到PCI围术期用药的销售场景里。这不是它有什么短板,是专业分工的现实摆在那儿。
这两年,许可合作和品种转让作为商业化工具越来越快崛起。
让研发强的公司专注搞创新,让渠道强的公司主导推广。通过清晰的价值链分工,实现各环节的效率最大化。
贝塔宁在百奥泰和乐普医疗之间的流转,就是这个逻辑最生动的写照。
11
再看百奥泰接下来的路。
BAT2506三地上市申请同步推进,说明百奥泰的生物类似药全球化布局正在进入收获期。
FDA的批文拿到了,EMA也批了,NMPA和巴西的还在评审中。
BAT8008在多个实体瘤适应症上展露的疗效信号,代表公司在ADC赛道上的深层布局开始兑现价值。
BAT8008联合BAT1308的II期临床研究在进行中,BAT8008联合BAT1006以及曲妥珠单抗在HER2阳性晚期实体瘤里的临床试验也刚拿到批文。
如果把百奥泰的管线想象成一棵大树,贝塔宁就是一根枝丫——长得挺好,但不在这棵树的生长主方向上。砍掉这根枝丫,养分就能更集中地供给主干。
12
说到底,这笔交易不是失败者的撤退,是聪明人的收拳。
拥有一款好产品,只是价值创造的起点,远远不是终点。
真正的终点,是把正确的产品交到有能力让它价值最大化的人手里。
在创新药这条赛道上,有时候放弃,比坚持更需要判断力。
不是每个好东西都得攥在手里自己干。知道自己能做什么、不能做什么,然后把有限的资源砸到最擅长的地方,这可能比埋头死磕更需要勇气。
百奥泰把贝塔宁交给乐普医疗,说不定正是在给这款药写一个更好的后半段故事。
创作来源
百奥泰关于转让药品品种权益及相关资产与业务的公告 2026年4月14日
乐普医疗关于子公司签署药品受让协议的公告 2026年4月14日
证券时报 百奥泰拟4.5亿元卖子 产品获批上市不到两年 2026年4月20日
东方财富网 百奥泰2025年年报净利润为-3.32亿元 2026年4月28日
科普 枸橼酸倍维巴肽注射液的临床研究之旅 2025年2月20日
百奥泰关于ImmgolisTM获美国FDA上市批准的公告 2026年5月19日
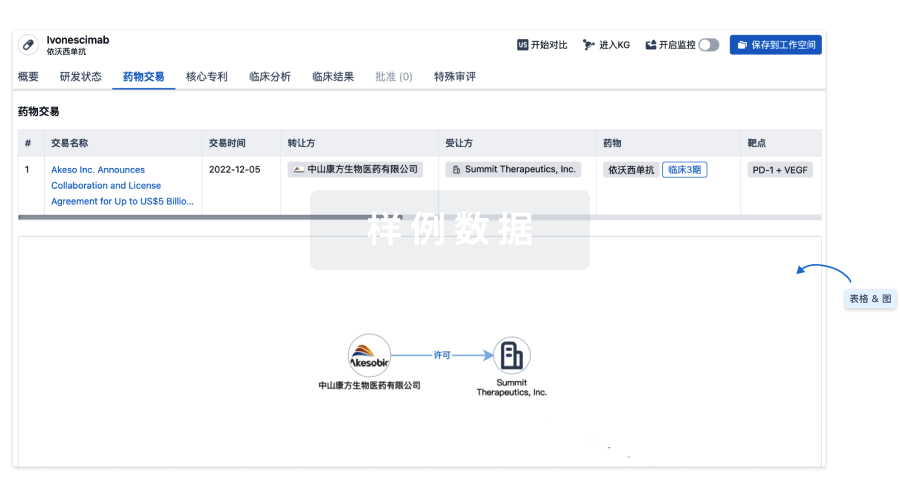
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的药物交易