预约演示
更新于:2026-05-20
Frexalimab
更新于:2026-05-20
概要
基本信息
药物类型 单克隆抗体 |
别名 INX 021、INX-021、INX021 + [3] |
靶点 |
作用方式 抑制剂 |
作用机制 CD40L抑制剂(CD40配体抑制剂) |
在研适应症 |
原研机构 |
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评- |
登录后查看时间轴
结构/序列
Sequence Code 315638965L

来源: *****
Sequence Code 651433761H

来源: *****
关联
11
项与 Frexalimab 相关的临床试验NCT07412470
A Seamless Phase 2/3 Randomized, Open-label Study to Investigate Efficacy and Safety of Frexalimab Versus Tacrolimus in Adult Kidney Transplant Recipients
The purpose of this open-label, randomized, active-comparator-controlled study is to determine the efficacy and safety of frexalimab subcutaneous administrations up to 5 years compared to tacrolimus capsules in adults undergoing kidney transplantation. Participants aged 18 to 70 years who have low-to-moderate immunologic risk of graft rejection and receive their first kidney transplant are eligible if they meet all inclusion and no exclusion criteria. Study details include:
* The study and treatment duration will be up to approximately 5 years.
* The number of visits will be approximately 38.
* The study and treatment duration will be up to approximately 5 years.
* The number of visits will be approximately 38.
开始日期2026-03-13 |
申办/合作机构 |
NCT07325292
A Randomized, Phase 3, Open-label Study to Investigate Pharmacokinetics, Safety, and Efficacy of Subcutaneous Compared to Intravenous Frexalimab in Adult Participants With Multiple Sclerosis
This is a randomized, open-label, parallel, Phase 3 study with 2-arms for treatment.
The purpose of this study is to evaluate SC administration of frexalimab every 4 weeks (q4w) compared to IV administration of frexalimab q4w in male and female participants with RMS and nrSPMS (aged 18 to 60 years at the time of enrollment). People diagnosed with MS are eligible for enrollment as long as they meet all the inclusion criteria and none of the exclusion criteria.
Study details include:
The study intervention duration will be 48 weeks (12 months) for Parts A and B combined. Optional Part C will last until the initiation of a long term safety study for Frexalimab.The follow up duration after the end of study intervention (in case of discontinuation) will be 6 months.
The number of scheduled visits (Parts A and B) will be 17 or 11 for participants receiving frexalimab SC or IV, respectively, with an on-site visit frequency of every month between Week 4 and Week 24 in Part A, then every 1 to 3 months in Part B, then every 6 months in Part C. Participants discontinuing treatment before the End of Study will have an additional 3 follow-up visits.
The purpose of this study is to evaluate SC administration of frexalimab every 4 weeks (q4w) compared to IV administration of frexalimab q4w in male and female participants with RMS and nrSPMS (aged 18 to 60 years at the time of enrollment). People diagnosed with MS are eligible for enrollment as long as they meet all the inclusion criteria and none of the exclusion criteria.
Study details include:
The study intervention duration will be 48 weeks (12 months) for Parts A and B combined. Optional Part C will last until the initiation of a long term safety study for Frexalimab.The follow up duration after the end of study intervention (in case of discontinuation) will be 6 months.
The number of scheduled visits (Parts A and B) will be 17 or 11 for participants receiving frexalimab SC or IV, respectively, with an on-site visit frequency of every month between Week 4 and Week 24 in Part A, then every 1 to 3 months in Part B, then every 6 months in Part C. Participants discontinuing treatment before the End of Study will have an additional 3 follow-up visits.
开始日期2026-01-14 |
申办/合作机构 |
NCT06500702
A Parallel-group Treatment, Phase 2a, Multicenter, Randomized, Double-blind, Placebo-controlled Umbrella Study to Evaluate the Efficacy and Safety of Frexalimab, Brivekimig, and Rilzabrutinib in Participants Aged 16 to 75 Years With Primary Focal Segmental Glomerulosclerosis (FSGS) or Minimal Change Disease (MCD)
This is a parallel, Phase 2a, double-blind, 6-arm study for the treatment of primary focal segmental glomerulosclerosis (FSGS) or primary minimal change disease (MCD).
The purpose of this study is to measure the change in proteinuria and its impact on the rates of remission of nephrotic syndrome with frexalimab, brivekimig, or rilzabrutinib compared with placebo in participants with primary FSGS or primary MCD aged 16 to 75 years.
Study details for each participant include:
The study duration will be up to 76 weeks. The treatment duration will be 24 weeks. There will be up to 18 visits.
The purpose of this study is to measure the change in proteinuria and its impact on the rates of remission of nephrotic syndrome with frexalimab, brivekimig, or rilzabrutinib compared with placebo in participants with primary FSGS or primary MCD aged 16 to 75 years.
Study details for each participant include:
The study duration will be up to 76 weeks. The treatment duration will be 24 weeks. There will be up to 18 visits.
开始日期2024-12-19 |
申办/合作机构 |
100 项与 Frexalimab 相关的临床结果
登录后查看更多信息
100 项与 Frexalimab 相关的转化医学
登录后查看更多信息
100 项与 Frexalimab 相关的专利(医药)
登录后查看更多信息
5
项与 Frexalimab 相关的文献(医药)2026-05-01·Multiple Sclerosis and Related Disorders
Psychometric validation of PROMIS-Fatigue-MS-8a and MSIS-29v2 questionnaires in relapsing multiple sclerosis participants enrolled in a phase 2 trial of frexalimab
Article
作者: Araujo, Lita ; Msihid, Jerome ; Saubadu, Stephane ; Gourlain, Samuel ; Hakimi-Hawken, Natalia ; Vermersch, Patrick ; Truffinet, Philippe ; Arnould, Benoit
BACKGROUND:
There are limited psychometric studies conducted using the Patient-Reported Outcomes Measurement Information System Adult Short Form-Fatigue-Multiple Sclerosis 8a (PROMIS-Fatigue-MS-8a) and Multiple Sclerosis Impact Scale-29 version 2 (MSIS-29v2) questionnaires.
METHODS:
Data were collected from a phase 2 trial (NCT04879628) investigating frexalimab in adults with relapsing multiple sclerosis (RMS). Reliability, convergent validity, construct validity, and sensitivity to change were assessed on PROMIS-Fatigue-MS-8a and MSIS-29v2 using Cronbach's alpha coefficient, intraclass correlation coefficient, Spearman's or polyserial correlation coefficients, analysis of variance, and analysis of covariance, respectively. Analyses were conducted using baseline and Week 12 data from pooled treatment arms.
RESULTS:
Item-to-item correlations were acceptable (0.4-0.9) for most of the items for both patient-reported outcomes (PROs) at baseline and Week 12. Internal consistency was excellent (Cronbach's alpha >0.90) for both PROs at baseline and Week 12. Additionally, good test-retest reliability was observed for PROMIS-Fatigue-MS-8a and the physical and psychological domains of MSIS-29v2. Convergent validity was supported by high correlations (r>0.50) between the PROMIS-Fatigue-MS-8a T-score and the MSIS-29v2 and the Patient Global Impression of Severity (PGIS)-Fatigue at baseline and Week 12. Construct validity was supported by significant differences between groups defined by the PGIS-Fatigue scores at baseline and Week 12 for both PROs (p<0.0001). Sensitivity to change was demonstrated by statistically significant differences in the mean change from baseline at Week 12 among groups defined by the PGIS-Fatigue and the Patient Global Impression of Change-Fatigue.
CONCLUSIONS:
PROMIS-Fatigue-MS-8a and MSIS-29v2 are valid and reliable measures for evaluating treatment benefits in clinical trials of RMS.
2024-02-15·The New England journal of medicine1区 · 医学
Inhibition of CD40L with Frexalimab in Multiple Sclerosis
1区 · 医学
Article
作者: Truffinet, Philippe ; Dufek, Michal ; Giovannoni, Gavin ; Staikov, Ivan ; Wallstroem, Erik ; Cutter, Gary ; Granziera, Cristina ; Vermersch, Patrick ; Bejuit, Raphael ; Kalbus, Oleksandr ; Saubadu, Stephane ; Mao-Draayer, Yang ; Djukic, Biljana
BACKGROUND:
The CD40-CD40L costimulatory pathway regulates adaptive and innate immune responses and has been implicated in the pathogenesis of multiple sclerosis. Frexalimab is a second-generation anti-CD40L monoclonal antibody being evaluated for the treatment of multiple sclerosis.
METHODS:
In this phase 2, double-blind, randomized trial, we assigned, in a 4:4:1:1 ratio, participants with relapsing multiple sclerosis to receive 1200 mg of frexalimab administered intravenously every 4 weeks (with an 1800-mg loading dose), 300 mg of frexalimab administered subcutaneously every 2 weeks (with a 600-mg loading dose), or the matching placebos for each active treatment. The primary end point was the number of new gadolinium-enhancing T1-weighted lesions seen on magnetic resonance imaging at week 12 relative to week 8. Secondary end points included the number of new or enlarging T2-weighted lesions at week 12 relative to week 8, the total number of gadolinium-enhancing T1-weighted lesions at week 12, and safety. After 12 weeks, all the participants could receive open-label frexalimab.
RESULTS:
Of 166 participants screened, 129 were assigned to a trial group; 125 participants (97%) completed the 12-week double-blind period. The mean age of the participants was 36.6 years, 66% were women, and 30% had gadolinium-enhancing lesions at baseline. At week 12, the adjusted mean number of new gadolinium-enhancing T1-weighted lesions was 0.2 (95% confidence interval [CI], 0.1 to 0.4) in the group that received 1200 mg of frexalimab intravenously and 0.3 (95% CI, 0.1 to 0.6) in the group that received 300 mg of frexalimab subcutaneously, as compared with 1.4 (95% CI, 0.6 to 3.0) in the pooled placebo group. The rate ratios as compared with placebo were 0.11 (95% CI, 0.03 to 0.38) in the 1200-mg group and 0.21 (95% CI, 0.08 to 0.56) in the 300-mg group. Results for the secondary imaging end points were generally in the same direction as those for the primary analysis. The most common adverse events were coronavirus disease 2019 and headaches.
CONCLUSIONS:
In a phase 2 trial involving participants with multiple sclerosis, inhibition of CD40L with frexalimab had an effect that generally favored a greater reduction in the number of new gadolinium-enhancing T1-weighted lesions at week 12 as compared with placebo. Larger and longer trials are needed to determine the long-term efficacy and safety of frexalimab in persons with multiple sclerosis. (Funded by Sanofi; ClinicalTrials.gov number, NCT04879628.).
Frontiers in Immunology
The role of microglia in multiple sclerosis: implications for treatment with Bruton’s tyrosine kinase inhibitors
Review
作者: Van Wijmeersch, Bart ; Pozzilli, Carlo ; Magyari, Melinda ; Vermersch, Patrick ; Popescu, Veronica ; Hartung, Hans-Peter ; Airas, Laura ; Deisenhammer, Florian ; Berger, Thomas ; Grigoriadis, Nikolaos ; Oreja-Guevara, Celia ; Pugliatti, Maura ; Zakaria, Magd
Background:
Multiple sclerosis (MS) is a chronic autoimmune disease affecting the central nervous system (CNS), characterized by inflammation and neurodegeneration. The pathophysiology of MS, especially its progressive forms, involves various cellular components, including microglia, the primary resident immune cells of the CNS. This review discusses the role of microglia in neuroinflammation, tissue repair, and neural homeostasis, as well as their involvement in MS and explores potential therapeutic strategies targeting microglial function.
Methods:
A literature search conducted in August 2023 and updated in March 2025, using the PubMed database, focused on articles relating to microglia and MS published in 2018–2025. Additionally, ongoing clinical trials of Bruton’s tyrosine kinase (BTK) inhibitors were identified through the ClinicalTrials.gov website in November 2023 and updated in March 2025.
Results:
Microglia are highly adaptive and exhibit various functional states throughout different life stages and play critical roles in neuroinflammation, tissue repair, and neural homeostasis. Their altered activity is a prominent feature of MS, contributing to its pathogenesis. Imaging techniques such as magnetic resonance imaging (MRI) and positron emission tomography (PET) provide insights into microglial activity in MS. BTK inhibitors and other novel treatments for MS, including masitinib and frexalimab, show promise in modulating microglial function and influencing the disease progression rate.
Conclusions:
The multifaceted roles of microglia in CNS development, immune surveillance, and particularly in the pathogenesis of MS highlight the potential of targeting microglial functions in MS treatment. Emerging research on the involvement of microglia in MS pathophysiology offers promising avenues for developing novel therapies, especially for progressive MS, potentially improving patient outcomes in this debilitating disease.
125
项与 Frexalimab 相关的新闻(医药)2026-05-18
·生物通
CD40–CD40L轴是连接固有免疫与适应性免疫的核心共刺激通路,参与自身免疫性炎症的发生发展。然而,CD40信号在不同细胞类型中并非以统一模式发挥作用,这种差异直接影响治疗的疗效与安全性。本综述系统阐述了CD40与CD40L的分子特征、CD40下游依赖肿瘤坏死因子受体相关因子(TRAF)的信号通路,以及B细胞、树突状细胞与巨噬细胞中不同的细胞应答。研究人员进一步探讨了CD40/CD40L信号失调如何驱动类风湿关节炎、系统性红斑狼疮与干燥综合征的关键病理改变,包括异位生发中心反应、致病性自身抗体产生及慢性组织炎症。血小板来源的CD40L与血管细胞表达的CD40共同解释了早期靶向该通路的生物制剂出现血栓栓塞并发症的原因。现有证据表明,更安全的治疗干预需要更高的选择性,尤其需关注细胞特异性信号调控及Fc介导的不良反应。引言
CD40/CD40L信号通路是连接固有免疫与适应性免疫应答的核心枢纽,最初被认为主要介导T细胞与B细胞的共刺激作用,后续研究证实其在免疫细胞与非免疫细胞中均发挥广泛调控功能。CD40属于肿瘤坏死因子受体超家族Ⅰ型跨膜受体,组成性或诱导性表达于B细胞、树突状细胞(DC)、巨噬细胞及多种内皮与上皮细胞表面;其配体CD40L(CD154)主要表达于活化的CD4+T细胞与血小板表面,以膜结合型与可溶性两种形式存在,均可激活CD40信号并启动下游免疫应答。尽管该通路在免疫调节中的作用已被广泛证实,但其细胞类型特异性的信号组织形式与情境依赖性调控机制仍未完全阐明。在类风湿关节炎(RA)、系统性红斑狼疮(SLE)与干燥综合征(SS)中,CD40与CD40L的持续过度表达驱动异常生发中心样反应、维持致病性自身抗体生成并加剧组织炎症。尽管已有大量靶向该通路的制剂进入研发,但早期临床试验暴露出显著的安全性问题,尤其是含功能性Fc段的抗CD40L抗体引发的血栓栓塞事件,提示未来治疗需在保障疗效的同时实现更高选择性。本综述从分子结构、信号机制、免疫调节、疾病关联及治疗策略四个层面展开,为下一代CD40靶向药物的开发提供理性框架。
CD40/CD40L的分子结构与表达
分子结构特征
CD40缺乏内在酶活性,其胞质尾部的特定基序通过招募TRAF家族蛋白形成信号支架,配体结合后诱导受体寡聚化并启动下游信号级联。CD40L属于肿瘤坏死因子家族,除表达于活化CD4+T细胞与血小板外,还可通过蛋白水解脱落形成可溶性CD40L(sCD40L),该形式仍保留三聚体结构,可与CD40结合并激活免疫应答。血小板来源的sCD40L为免疫激活与血栓炎症之间的机制联系提供了依据,也是早期靶向药物安全性风险的重要解释基础。
膜结合型与可溶性形式的生物学差异
膜结合型CD40L是典型的接触依赖性共刺激分子,通过结合抗原呈递细胞表面的CD40调控体液免疫与炎症反应。sCD40L在多数情况下发挥激动剂作用,可激活内皮细胞、平滑肌细胞及单核/巨噬细胞内的核因子κB(NF-κB)与丝裂原活化蛋白激酶(MAPK)通路,诱导黏附分子、趋化因子与基质金属蛋白酶的表达,促进白细胞黏附、血管炎症与斑块不稳定;在心血管系统中,其还可通过与血小板及白细胞表面的整合素相互作用增强血小板-白细胞聚集与血栓形成。sCD40L的功能具有浓度与寡聚化状态依赖性:高阶寡聚体可有效诱导B细胞活化增殖,低阶寡聚体或低浓度条件下则主要通过竞争性占据CD40结合位点部分削弱膜结合型配体的强共刺激信号,目前尚无明确证据支持其在体内可作为完全拮抗剂。可溶性CD40(sCD40)作为诱饵受体,可在循环中结合CD40L并阻断其与膜CD40的相互作用,在动脉粥样硬化、慢性肾病等疾病中被视为内源性负反馈调节分子。两者在不同微环境中协同调控CD40信号的强度。
表达模式
CD40广泛表达于免疫细胞与非免疫细胞表面,其表达水平可被炎症信号上调。在B细胞中,CD40是T细胞依赖性体液免疫的核心分子,与活化T细胞来源的CD40L结合后驱动B细胞扩增与抗体产生。CD40L主要表达于活化CD4+T细胞,其表达严格受T细胞活化状态与免疫刺激性质调控。此外,血小板活化后可释放大量sCD40L,作用于内皮细胞并促进免疫细胞招募,参与系统性炎症与血管病变的发生。CD40L在血小板及血管系统的表达使其同时参与自身免疫性疾病与心血管疾病的免疫调控,提示该通路并非均一性通路,其生物学效应高度依赖于受体-配体互作的细胞情境。
CD40/CD40L信号转导机制
CD40胞质尾与TRAF的结合特性
CD40信号传递完全依赖TRAF蛋白的招募,其胞质尾部包含三类核心结合基序:膜远端区域存在经典的PxQxT基序,可结合TRAF1、TRAF2与TRAF3;C端存在非经典TRAF2结合位点,在PxQxT基序受损时仍可部分维持NF-κB激活;膜近端QxPxEx序列为TRAF6结合位点,参与NF-κB与磷脂酰肌醇3-激酶/蛋白激酶B(PI3K/Akt)信号通路调控。三聚体CD40L结合可诱导CD40构象变化,暴露TRAF结合基序并形成高阶寡聚复合物,寡聚化程度直接影响低亲和力TRAF及下游接头蛋白的招募,进而决定信号的强度与性质。TRAF1在该过程中发挥精细调控作用,其可通过与TRAF2结合位点的重叠竞争影响TRAF2的招募与降解,稳定TRAF2并增强其下游信号传递,这一调控机制是自身免疫状态下CD40信号持续异常激活的重要分子基础。
NF-κB通路:经典与非经典途径
经典NF-κB通路中,TRAF2与TRAF6招募并激活IκB激酶(IKK)复合物,磷酸化IκB使其经泛素化降解,释放p50/p65与p50/c-Rel异二聚体入核,启动炎症、细胞存活与共刺激分子表达相关基因转录。TRAF1通过稳定TRAF2对该通路至关重要。非经典NF-κB通路依赖NF-κB诱导激酶(NIK)与IKKα的活化:静息状态下TRAF2、TRAF3与cIAP1/2构成复合物持续促进NIK泛素化降解;CD40激活后TRAF2与TRAF3从复合物解离并招募至CD40胞质尾,TRAF2经自泛素化降解,TRAF3经cIAP1/2依赖性降解,使NIK得以积累并激活IKKα,剪切p100生成p52,与RelB形成二聚体入核调控淋巴器官发育、细胞存活与晚期免疫应答基因表达。TRAF2在该过程中发挥双重作用:在成熟B细胞中促进经典NF-κB激活,同时通过维持NIK的持续性降解抑制非经典通路。
MAPK与PI3K/Akt信号
CD40激活后,TRAF2通过衔接上游激酶MEKK1激活JNK与p38 MAPK通路;TRAF6则通过招募Cbl-b/c-Cbl/PI3K复合物诱导Akt磷酸化。在树突状细胞中,Cbl-b缺失可完全阻断CD40诱导的Akt激活,表明该通路独立于NF-κB调控DC存活。PI3K/Akt信号通过抑制caspase-9与Bcl-2家族促凋亡分子、上调mTOR及抗凋亡分子cFLIPp43发挥促存活作用,支持炎症微环境中免疫细胞的长期存续,是自身免疫慢性炎症持续的重要机制。
细胞类型特异性差异
同一信号通路在不同细胞中可产生截然相反的效应。在B细胞中,TRAF3是经典与非经典NF-κB及JNK信号的关键负调控因子;而在气道上皮细胞中,TRAF3参与经典NF-κB的激活并促进其核转位。Cbl-b的功能同样具有细胞特异性:在树突状细胞中作为PI3K/Akt通路的正向调控因子促进细胞存活,在B细胞中则通过限制TRAF2介导的信号发挥“刹车”作用。Janus激酶3(Jak3)仅在特定抗原呈递细胞中被CD40招募并磷酸化STAT5,驱动肿瘤坏死因子-α(TNF-α)与白细胞介素-6(IL-6)表达,在静息B细胞中无此功能。这些差异决定了CD40信号的最终免疫学效应。
CD40/CD40L在免疫调节中的作用
B细胞活化、生发中心反应与抗体产生
CD40信号是T细胞依赖性体液免疫的核心驱动力,通过激活NF-κB、MAPK与PI3K/Akt通路调控B细胞增殖、类别转换重组、体细胞高频突变与记忆B细胞形成。在生发中心反应中,滤泡辅助T(Tfh)细胞表面的CD40L与生发中心B细胞表面的CD40结合,为B细胞提供存活信号:高亲和力B细胞可有效捕获抗原并获得足够CD40信号存活,低亲和力或自身反应性B细胞因信号不足经Fas依赖性凋亡清除。TRAF适配蛋白的选择决定生发中心反应的阶段:TRAF6结合位点缺失导致抗体亲和力成熟与浆细胞生成缺陷,TRAF2-TRAF3与TRAF6结合基序联合突变则完全阻断生发中心形成。遗传缺陷模型证实,小鼠CD40或CD40L缺失会导致生发中心无法形成、免疫球蛋白类别转换障碍及免疫记忆缺失;人类CD40L或CD40功能丧失突变引发X连锁高IgM综合征,表现为IgG、IgA与IgE显著降低、IgM正常或升高,缺乏生发中心与记忆B细胞,易反复发生细菌感染。
树突状细胞成熟与抗原呈递增强
CD40激活可诱导树突状细胞表型成熟,上调主要组织相容性复合体Ⅱ类分子(MHC Ⅱ)、CD80、CD86及CD40L表达,分泌IL-8、IL-10、IL-12等细胞因子与趋化因子,显著增强抗原呈递能力。IL-12的产生需CD40信号与Th1细胞来源的干扰素-γ(IFN-γ)协同,Th2细胞则抑制其表达。在自身免疫状态下,滑膜组织中成熟树突状细胞高表达CD40,持续激活自身反应性T细胞。此外,CD40交联可抵抗树突状细胞的Fas凋亡,通过下调CCR1与CCR5、上调CCR7促进其迁移至淋巴器官,并诱导一氧化氮合成酶表达,支持抗肿瘤与炎症性T细胞应答。
巨噬细胞活化与炎症放大
单核细胞与巨噬细胞表面的CD40被配体激活后,可诱导IL-12、TNF-α、IL-1、IL-6与IL-8的分泌,IL-12进一步促进T细胞CD40L表达,形成正反馈放大环路。该过程无需额外细胞因子协同,即可直接驱动促炎微环境形成。同时,CD40信号可诱导基质金属蛋白酶(MMP-1、MMP-2、MMP-3、MMP-9)表达,促进细胞外基质重塑与组织破坏;还可诱导组织因子表达,增强炎症部位的致血栓潜能,将局部炎症激活与结构性组织损伤及高凝状态直接关联。
T细胞依赖性体液免疫与免疫记忆
CD40/CD40L信号协调T细胞与B细胞的协作,支持生发中心形成、类别转换、亲和力成熟及记忆B细胞与长寿命浆细胞生成。此外,CD40L交联可向T细胞传递共刺激信号,影响其分化与细胞因子分泌,维持二次免疫应答中的体液记忆。在慢性炎症中,该通路的持续激活则维持致病性T-B协作与自身反应性体液免疫。
免疫耐受的破坏
CD40/CD40L信号是免疫耐受破坏的核心枢纽。生理状态下其支持保护性免疫应答,过度激活则降低自身反应性淋巴细胞活化阈值,促进致病性克隆存活扩增。动物模型中,阻断该通路可预防狼疮样肾炎、胶原诱导性关节炎、实验性自身免疫性脑脊髓炎等疾病的发生发展;人类研究中,SLE与RA患者活化CD4+T细胞CD40L表达升高,B细胞、单核细胞及间质细胞CD40表达上调,与疾病活动度及自身抗体滴度正相关。CD40L或CD40缺陷导致的X连锁高IgM综合征患者自身免疫病发生率升高,进一步证实该通路功能异常可直接破坏免疫稳态。
CD40/CD40L在自身免疫性疾病中的作用
类风湿关节炎
RA滑膜组织中CD40高表达于成纤维样滑膜细胞、巨噬细胞与树突状细胞表面,受IFN-γ与TNF上调。CD40激活可促进滑膜成纤维细胞增殖、黏附分子表达及IL-6、粒细胞-巨噬细胞集落刺激因子(GM-CSF)分泌,与活化T细胞或单核细胞协同形成促炎因子-趋化因子网络,诱导破骨细胞介导的骨吸收。抗环瓜氨酸肽(抗CCP)抗体的产生依赖CD40信号,RA患者外周血与滑膜T细胞CD40L表达更快更强,与疾病活动度及缓解率负相关。基因组学研究显示CD40基因座与幼年RA易感相关,特定单核苷酸多态性可影响信号强度。
系统性红斑狼疮
SLE患者活化CD4+、CD8+T细胞及B细胞异位表达CD40L,B细胞来源CD40L可自发驱动自身抗体产生;转基因小鼠B细胞过表达CD40L可诱发狼疮样疾病。患者血清sCD40L水平与疾病活动度正相关。肾脏系膜细胞表达CD40,受IFN-γ或活化血小板刺激后促进TGF-β分泌,参与狼疮肾炎进展;骨髓造血祖细胞CD40信号诱导Fas表达,介导细胞凋亡,可能与全血细胞减少相关。小鼠模型中,CD40L阻断可延缓肾炎发生、降低自身抗体滴度、延长生存期,但临床转化结果不一致。CD40胞质尾P227A变异可增强JNK通路激活,与疾病严重程度相关。
干燥综合征
SS患者唾液腺中CD40与CD40L表达上调,驱动淋巴细胞浸润与慢性炎症,血清sCD40L水平与疾病活动度相关。CD40基因多态性可影响B细胞表面表达水平,CC基因型携带更高CD40表达,增强免疫应答。动物模型中阻断CD40/CD40L可减轻B细胞活化与组织损伤,提示其为潜在治疗靶点。
靶向CD40/CD40L相互作用的治疗策略
类风湿关节炎中的通路调控
VIB4920是一种无Fc段CD40L结合蛋白,Ⅰ期试验显示良好安全性,Ⅱ期试验中显著降低RA患者疾病活动度,降低类风湿因子、抗CCP抗体、sCD40L与CXCL13水平,但存在抗药抗体形成问题。BI-655064是一种人源化拮抗性抗CD40 IgG1单抗,虽可降低活化B细胞亚群,但未显示出统计学显著的临床疗效优势。
CD40L靶向治疗的发展
第一代含Fc段抗CD40L抗体(如ruplizumab与toralizumab)虽可降低自身抗体水平,但因诱导血小板聚集引发血栓栓塞事件而终止开发。后续策略转向去Fc或Fc工程改造:dapirolizumab pegol为PEG化抗CD40L Fab’片段,临床前与早期临床均未观察到血栓事件,可降低抗dsDNA抗体并下调B细胞活化相关基因;frexalimab为Fc工程改造的下一代抗CD40L抗体,已在复发型多发性硬化Ⅱ期试验中取得阳性结果并进入Ⅲ期;tegoprubart与TNX-1500通过Fc修饰在移植模型中延长移植物存活且不诱导血小板活化,验证了Fc改造的安全性优势。
非耗竭性CD40阻断剂iscalimab
iscalimab(CFZ533)为非激动性抗CD40单抗,经Fc修饰消除Fcγ依赖效应功能,在肾移植中显示初步疗效。在干燥综合征Ⅱa期试验中,高剂量静脉组显示疾病活动度降低与CXCL13下降,但低剂量皮下组未观察到明确疗效,提示靶点结合并不等同于临床获益,需进一步优化患者分层与给药策略。
结论
CD40/CD40L轴通过TRAF依赖的信号通路激活NF-κB、MAPK与PI3K/Akt级联,其细胞类型特异性决定免疫应答的多样性。在RA、SLE与SS中,该通路失调驱动异位生发中心形成、致病性自身抗体产生与慢性炎症。新一代治疗策略通过去Fc或Fc工程改造显著降低了血栓风险,但靶点结合与临床疗效的不一致性提示未来需结合生物标志物指导的患者分层,实现细胞类型限制性信号的精准调控,在安全前提下达成持久的疾病控制。
2026-05-17
全球免疫与自身免疫疾病药物研发全景深度报告:靶点通路、临床验证与下一代重塑疗法引言
全球自身免疫性疾病及炎症性疾病的治疗正处于从“症状控制”向“免疫重塑与疾病治愈”跨越的历史性拐点。随着对免疫系统分子机制的深入理解,全球药物研发管线正经历前所未有的爆发式增长。最新行业分析显示,全球自身免疫领域的在研药物数量已超过6,600款,同比实现27%的大幅增长;仅在2025年上半年,便启动了超过1,100项新的临床试验 。随着1,186项临床试验计划于2025年底前完成,大量关键数据即将重塑现有的治疗路径 。
这一领域的竞争已从早期突破性单抗疗法的“跑马圈地”,演变为围绕更优靶点、更高激酶选择性以及下一代新分子实体(如双特异性抗体、CAR-T细胞疗法、靶向蛋白降解剂)的“超级竞争(Hypercompetitive race)”阶段 。各大跨国制药企业(MNC)不再局限于单一靶点的开发,而是通过管线整合、外部收购(如默沙东108亿美元收购Prometheus、罗氏71亿美元收购Televant)加速抢占上游关键枢纽和新兴靶点 。本报告将系统性梳理目前已上市及处于研发前沿的各类免疫通路靶点,深度解析其分子信号的上下游关系与靶点选择的科学逻辑,盘点已被三期临床验证的获批适应症及核心申办方,并对未来的研发趋势及临床应用价值进行全面展望。1. 免疫系统信号通路基础及靶点选择的分子逻辑
在探讨具体的治疗药物之前,必须从分子生物学层面理解免疫系统的“通讯网络”。免疫反应并非单一免疫细胞的孤立行为,而是一场由上游触发器、中游传导器和下游效应器共同参与的复杂级联反应(Cascade) 。在药物研发中,对于上游生物工艺与下游分子加工的考量,同样映射在针对疾病靶点的上下游选择上 。1.1 免疫通路的“上下游”层级关系
免疫系统的信号传导可以被精确地划分为三个层级:
上游信号(Upstream Signals):组织屏障的触发与警报上游因子通常驻扎在身体的屏障组织(如皮肤表皮、气道黏膜、肠道上皮细胞)中。当这些屏障细胞遇到外界刺激(如过敏原、病毒、机械损伤或上皮应激)时,它们会最先拉响警报,释放诸如 TSLP(胸腺基质淋巴细胞生成素)、IL-33、IL-25 等被称为“警报素(Alarmins)”的细胞因子,或 TGF-β 等多效性生长因子 。上游因子并不直接杀伤病原体或破坏组织,而是通过结合特异性受体,将信号传递给驻留在组织中的先天免疫细胞(如树突状细胞、先天性淋巴细胞 ILCs)。转化生长因子-β (TGF-β) 便是典型的上游多效性细胞因子,其信号传导通过类型 I 和类型 II 激酶受体复合物,磷酸化细胞质内的 R-Smads 蛋白,从而调控细胞稳态与分化 。
中游信号(Midstream Signals):免疫细胞的极化与扩增接收到上游警报后,抗原递呈细胞(如树突状细胞)和初始辅助性T细胞(Naïve CD4+ T cells)开始工作,并释放中游细胞因子(如 IL-4、IL-12、IL-23)。这些因子的核心作用是“指令分发”,促使T细胞向特定的效应亚群发育。例如,IL-23 的存在是维持致病性 Th17 细胞存活和扩增的绝对必要条件 ;而 IL-4 则不仅驱动初始T细胞向 Th2 细胞分化,还控制淋巴结内的 B 细胞进行抗体类别转换,大量合成 IgE 。
下游信号(Downstream Signals):效应机制与组织破坏分化成熟的免疫细胞(如 Th17、Th2、巨噬细胞)最终迁移至靶器官,并释放下游效应因子,如 IL-17A、IL-17F、IL-13、IL-22、IL-31 以及 TNF-α(肿瘤坏死因子-α)。这些下游因子是直接导致临床症状的“执行部队”。例如,IL-17 刺激角质形成细胞异常增生并释放趋化因子(形成银屑病斑块) ;IL-13 破坏皮肤屏障并导致气道高反应性 ;IL-31 则直接作用于神经元,引发强烈的瘙痒感 。1.2 靶点选择的系统性权衡与科学依据
制药企业在确立研发靶点时,核心逻辑在于在“系统覆盖广度”与“分子打击精准度”之间寻找最佳平衡点:
拦截上游靶点(如 TSLP、IL-33、IL-4):由于上游信号控制着多条下游分支网络,阻断上游可以实现“一石多鸟”的广泛抗炎效果。例如,IL-4 是驱动全身性系统免疫反应的核心,靶向阻断 IL-4 受体不仅能够抑制下游 IL-13 的外周组织破坏作用,还能从源头上阻断 IgE 的合成,从而实现对多种特应性合并症(如特应性皮炎合并哮喘和过敏性鼻炎)的全面控制 。此外,靶向转录因子(如驱动细胞从静止期进入增殖期的 OLIG2)也属于对上游通路的根本性干预 。然而,过度阻断上游也可能干扰机体正常的免疫监视和防御功能。
拦截下游靶点(如 IL-17、TNF-α、IL-13):下游靶点的优势在于极高的特异性和起效速度。由于它们直接负责产生局部症状,阻断下游往往能在数周甚至数天内迅速缓解皮损或关节红肿。以 IL-17A 为例,其被抑制后能够极速切断角质形成细胞的增殖信号,清除银屑病皮损 。然而,下游封锁的劣势在于疾病可能通过复杂的旁路途径(Bypass pathways)发生逃逸。在哮喘和特应性皮炎中,仅单独阻断下游 IL-13(如 Lebrikizumab 和 Tralokinumab)的临床获益,往往不及同时阻断 IL-4 和 IL-13 双通路的疗效显著 。2. 细胞内信号传导的核心中枢:JAK/STAT 通路深度解析
大多数细胞因子的受体并不具备内在的激酶活性,它们必须依赖细胞质内的激酶网络来传递信号。Janus 激酶(JAK)及其下游的信号转导与转录激活因子(STAT)构成了这一网络的核心 。2.1 JAK/STAT 的分子激活机制
当细胞因子(如 IL-6)与细胞膜上的受体结合后,受体链发生空间构象的重排。经典理论认为这导致了受体二聚化,但近期的 FRET(荧光共振能量转移)分析表明,许多受体在无配体状态下已是预先形成的二聚体,细胞因子的结合引发了受体胞内结构域的几何空间分离与重新定向,使得连接在受体上的 JAK 激酶相互靠近并发生反式自身磷酸化(Trans-phosphorylation) 。在哺乳动物中,JAK 家族包含四个成员(JAK1, JAK2, JAK3, TYK2),STAT 家族包含七个成员(STAT1 至 STAT6)。活化后的 JAK 会进一步磷酸化受体上的酪氨酸残基,为具有 SH2 结构域的 STAT 蛋白提供停泊位点。随后,STAT 被 JAK 磷酸化,形成二聚体并转移至细胞核内,激活或抑制特定靶基因的转录 。
除了核心的 JAK/STAT 轴,细胞因子的结合还会同步激活 MAPK(丝裂原活化蛋白激酶)和 PI3K/AKT/mTOR 等其他信号级联反应。例如,IL-6 能够诱导磷酸酶 SHP2 结合到受体 gp130 亚基上,进而通过 Grb2 等衔接蛋白激活 MAPK 通路 。在此过程中,细胞内部存在着严格的负反馈调节机制。例如,SOCS3(细胞因子信号传导抑制蛋白 3)的表达会被诱导,它能够结合到受体上,同时抑制 STAT3 和 MAPK 引发的转录反应,防止免疫系统失控 。2.2 泛 JAK 抑制剂与高选择性 TYK2 的临床分野
由于 JAK 通路负责介导超过 50 种细胞因子的信号,抑制 JAK 意味着能够产生强大的广谱抗炎效果 。然而,不同 JAK 亚型在体内的生理功能存在显著差异,这导致了第一代药物与新一代药物在安全性上的巨大分水岭。
泛 JAK 抑制剂(Pan-JAK Inhibitors)的安全性困境:第一代泛 JAK 抑制剂(如 Tofacitinib、Upadacitinib、Baricitinib)广泛抑制 JAK1、JAK2 和 JAK3。临床和基因敲除模型证实:JAK1 和 JAK3 对于介导干扰素和共同 γ 链细胞因子的信号至关重要,抑制它们会严重削弱淋巴细胞(T细胞、NK细胞)介导的抗病毒能力,导致带状疱疹(Herpes Zoster)和严重感染的风险显著升高 。更为严重的是,JAK2 是介导促红细胞生成素(EPO)、血小板生成素等造血因子的唯一通路,广泛抑制 JAK2 会改变止血机制,导致深静脉血栓(DVT)、肺栓塞(PE)以及心血管不良事件(MACE)的风险增加。为此,FDA 对此类药物发布了严格的“黑框警告(Black Box Warning)”,限制了其作为一线疗法的广泛应用 。
高选择性 TYK2 抑制剂的破局:为了平衡疗效与安全性,研发重心迅速转向了高选择性的同工酶抑制剂。TYK2(酪氨酸激酶 2)特异性地参与 IL-12、IL-23 以及 I 型干扰素信号传导,而不干预 JAK1/2/3 所负责的造血和广泛免疫防御功能 。BMS 开发的 Deucravacitinib 是首个获批的别构 TYK2 抑制剂,它结合在 TYK2 的假激酶结构域(Pseudokinase domain)而非高度保守的活性 ATP 结合位点,从而实现了极高的选择性 。临床数据显示,TYK2 抑制剂有效避免了血栓栓塞风险,且带状疱疹和脂质升高的发生率大幅下降,为银屑病及其他自身免疫疾病提供了一种安全性极佳的小分子口服选项 。3. IL-23/IL-17 与 TNF-α 轴:银屑病与肠道炎症的靶向进化
IL-23/IL-17 炎症轴是介导银屑病(PsO)、银屑病关节炎(PsA)、中轴型脊柱关节炎(axSpA)以及炎症性肠病(IBD)的核心致病通路 。3.1 Th17 细胞的致病级联反应
在环境诱因刺激下,浆细胞样树突状细胞(pDCs)和髓系树突状细胞(mDCs)被激活,大量分泌 IL-12、IL-23 及 TNF-α 。IL-23 由 p19 和 p40 两个亚基组成,当其结合到表达于 CD4+ T细胞表面的 IL-23R 时,通过 JAK2 和 TYK2 介导 STAT3 的激活,上调核心转录因子 ROR-γt 的表达 。这促使初始 T 细胞分化为致病性的 Th17 细胞谱系。值得注意的是,Th17 细胞可分为宿主保护性亚群(分泌 IL-17 和抗炎因子 IL-10)和高度致病性亚群(分泌 IL-17、IL-22、IFN-γ 及 GM-CSF)。IL-23 的持续存在不仅驱动向致病性表型转化,还通过刺激释放 IL-1β 和 IL-6 形成正反馈放大回路 。下游分泌的 IL-17A 和 IL-17F 随后结合到靶组织(如表皮或关节滑膜)的 IL-17RA 和 IL-17RC 受体上,触发 NF-κB 和 MAPK 通路,导致角质形成细胞过度增殖、抗菌肽及趋化因子大量释放,最终形成典型的银屑病斑块或关节侵蚀 。3.2 靶向药物的世代演进与临床应用
随着对该通路解析的深入,药物靶点经历了从广谱到极度精准的演化。
TNF-α 抑制剂: 作为早期的奠基性生物制剂(如阿达木单抗 Humira),通过广谱阻断炎症因子,在多个自免领域确立了疗效基准。但其全身性免疫抑制可能增加机会性感染和结核复发风险 。
抗 IL-12/23 (p40) 单抗: Ustekinumab(Stelara)靶向 IL-12 和 IL-23 共享的 p40 亚基,同时阻断了 Th1 和 Th17 两条通路,在银屑病和炎症性肠病中取得了巨大成功 。
抗 IL-23 (p19) 特异性单抗: 为了保留 IL-12 介导的正常细胞免疫功能,新一代药物(如 Guselkumab, Risankizumab, Tildrakizumab)特异性靶向 IL-23 的 p19 亚基。这些药物在诱导深层缓解和长期维持治疗(如每 12 周给药一次)中表现出极高的有效性和优异的安全性 。
抗 IL-17 单抗及其受体阻断剂: 针对极速起效的需求,直接阻断下游的 IL-17A(Secukinumab, Ixekizumab)或其受体(Brodalumab)展现了超越早期制剂的 PASI 100(皮损完全清除)达成率。UCB 开发的 Bimekizumab 更进一步,同时阻断了 IL-17A 和 IL-17F,在多项头对头试验中树立了疗效新标杆 。
表1:IL-23/IL-17 及 TNF-α 轴主要获批临床药物及三期验证适应症核心靶点药物名称 (商品名)药物结构及类型主要申办方FDA/EMA 三期验证获批适应症TNF-αAdalimumab (Humira)全人源 IgG1 单抗AbbVie
银屑病(PsO), 银屑病关节炎(PsA), 强直性脊柱炎(AS), 幼年特发性关节炎(PJIA), 克罗恩病(CD), 溃疡性结肠炎(UC), 化脓性汗腺炎(HS), 葡萄膜炎(UV) IL-12/23 (p40)Ustekinumab (Stelara)人源 IgG1κ 单抗J&J (Janssen)
PsO (6岁以上), PsA (6岁以上), 中重度 CD (2岁以上), 中重度 UC IL-23 (p19)Guselkumab (Tremfya)抗 p19 单抗J&J (Janssen)
中重度 PsO (6岁以上), 活跃期 PsA (6岁以上), CD, UC IL-23 (p19)Risankizumab (Skyrizi)抗 p19 单抗AbbVie
中重度 PsO, 活跃期 PsA, 中重度 CD, 中重度 UC IL-23 (p19)Tildrakizumab (Ilumya)抗 p19 单抗Sun Pharma
中重度 PsO IL-23 (p19)Mirikizumab (Omvoh)抗 p19 单抗Eli Lilly
溃疡性结肠炎(UC) IL-17ASecukinumab (Cosentyx)全人源抗 IL-17A 单抗Novartis
PsO (6岁以上), PsA (2岁以上), AS, 非放射学中轴型脊柱关节炎(nr-axSpA), 附着点炎相关关节炎(ERA), HS IL-17AIxekizumab (Taltz)人源化抗 IL-17A 单抗Eli Lilly
PsO (6岁以上), PsA, AS, nr-axSpA IL-17A/FBimekizumab (Bimzelx)双特异性 IL-17A/F 单抗UCB
中重度 PsO, 活跃期 PsA IL-17RBrodalumab (Siliq)抗 IL-17 受体单抗Valeant/Ortho
中重度 PsO 4. IL-4/IL-13 轴与警报素:重塑2型炎症的广阔版图
以特应性皮炎(AD)、哮喘、慢性鼻窦炎伴鼻息肉(CRSwNP)以及嗜酸性食管炎(EoE)为代表的“2型炎症(Type 2 Inflammation)”,构成了另一个庞大的疾病领域。在这条通路中,IL-4 和 IL-13 起到了如同双引擎般的驱动作用 。4.1 IL-4、IL-13 与 IL-31 的致病机制网络
IL-4:全局免疫的总指挥。 IL-4 能够直接促进未分化的 T 细胞向 Th2 效应细胞发育。更重要的是,它在淋巴结等中心免疫器官中起作用,控制 B 细胞进行同种型转换以大量合成致敏性 IgE 抗体。此外,IL-4 的过度表达还会诱发全身性过敏反应和慢性瘙痒 。
IL-13:外周组织的破坏者。 IL-13 的受体主要表达于非造血细胞(如上皮细胞、成纤维细胞)。它在靶组织中造成直接的结构性破坏:在皮肤中,IL-13 显著降低角质形成细胞对抗菌肽(AMPs)的合成,导致表皮防御崩溃,引发生物群落失调(特别是金黄色葡萄球菌的早期定植);同时,它增加经表皮水分流失,导致屏障功能受损。在呼吸道中,IL-13 驱动杯状细胞增生和黏液过度分泌,导致严重的气流受限 。
IL-31:奇痒难忍的“神经信使”。 IL-31 主要由活化的 Th2 细胞和肥大细胞分泌。它的特殊性在于其受体(IL-31R)广泛存在于感觉神经元上。当 IL-31 与受体结合后,通过 JAK/STAT、ERK/MAPK 和 PI3K/AKT 途径向大脑传递强烈的瘙痒信号。它同时还会上调多种基质金属蛋白酶(MMPs)和趋化因子的表达。临床数据表明,在患有严重瘙痒的 AD 和结节性痒疹患者中,IL-31 呈现特异性的上调 。4.2 靶点拦截与临床疗效的对比
赛诺菲与再生元联合开发的 Dupilumab(度普利尤单抗)通过结合 IL-4Rα 亚基,同时阻断了 IL-4 和 IL-13 两条信号通路。这种“双重抑制”展现出压倒性的临床优势。由于 IL-4 驱动早期免疫激活,而 IL-13 负责组织损伤,同时封锁两者不仅极大降低了哮喘恶化率,还显著减轻了过敏性鼻炎中的 IgE 负担 。相比之下,仅针对单一下游细胞因子的抑制剂(如靶向 IL-13 的 Lebrikizumab 和 Tralokinumab),在部分适应症(如重度哮喘)的三期试验中未能引发同等水平的显著临床改善 。
表2:2型炎症核心通路三期验证获批药物及适应症靶点药物名称 (商品名)主要申办方FDA/EMA 获批适应症大全IL-4Rα (双重阻断 IL-4/13)Dupilumab (Dupixent)Sanofi / Regeneron
特应性皮炎(AD, 6个月以上), 中重度哮喘(6岁以上), 慢性阻塞性肺病(COPD), 慢性鼻窦炎伴鼻息肉(CRSwNP, 12岁以上), 嗜酸性食管炎(EoE, 1岁及15kg以上), 结节性痒疹(PN), 慢性自发性荨麻疹(CSU) 4.3 上游警报素的全面拦截:TSLP 与 IL-33
针对严重且异质性极高的哮喘,仅阻断下游的 IL-4/13 往往不够,将防线前移至上皮细胞衍生的“警报素”成为全新的研发热点 。
TSLP(胸腺基质淋巴细胞生成素): 阿斯利康与安进合作开发的 Tezepelumab(抗 TSLP 单抗)已获批用于严重哮喘(无表型限制)。作为上游始动因子,阻断 TSLP 能够在二期及三期临床中实现高达 56% - 70% 的哮喘恶化率(AAER)降低。目前,阿斯利康正在开展针对 COPD(SUNRISE 试验)和 CRSwNP(WAYPOINT 试验)的三期扩展研究 。
IL-33: 另一种关键上游介质。赛诺菲管线中的 Itepekimab(抗 IL-33 单抗)已在二期临床中证实可降低 36% 的 AAER,目前正处于针对 COPD 和不伴鼻息肉的慢性鼻窦炎的关键三期研究中;阿斯利康同样在推进其 IL-33 单抗 Tozorakimab 的临床开发 。5. IL-6 经典通路与突破性新兴靶点的研发布局
除了上述两大核心轴,免疫学领域仍在不断挖掘能解决特殊组织病变和顽固性自身抗体的新靶点。5.1 IL-6 与 IL-1:全身性炎症的风暴中心
IL-6 是一种多效性细胞因子,深度参与全身性炎症反应、急性期蛋白合成以及 B 细胞向浆细胞的终末分化 。通过阻断 IL-6 及其受体,可以有效遏制“细胞因子风暴”。
Tocilizumab (Actemra): 作为经典的人源化抗 IL-6 受体单抗,其已获得极为广泛的适应症批准,包括类风湿关节炎(RA)、巨细胞动脉炎(GCA)、多关节型和全身型幼年特发性关节炎(PJIA/SJIA,2岁以上)、嵌合抗原受体T细胞疗法引发的重度细胞因子释放综合征(CRS,2岁以上),甚至用于减缓系统性硬化症相关间质性肺病(SSc-ILD)的肺功能衰退及重症 COVID-19 感染 。同类药物还包括 Sarilumab 。
IL-1 受体拮抗剂: 如 Anakinra (Kineret),作为重组人 IL-1 受体拮抗剂,主要用于治疗痛风发作、成人斯蒂尔病及严重 RA 。5.2 肠道纤维化的克星:TL1A 靶点
炎症性肠病(IBD)最大的未解难题之一是肠壁的不可逆纤维化和狭窄,传统的抗 TNF-α 或 IL-23 制剂难以逆转这一结构性改变。TL1A(肿瘤坏死因子样配体 1A)的异常持续升高,不仅导致免疫细胞在消化道过度浸润形成溃疡,更是驱动成纤维细胞过度活化、造成组织损伤和纤维化的直接元凶 。 鉴于其极高的潜力,该靶点引发了巨头间的百亿美元级并购大战:默沙东豪掷 108 亿美元收购 Prometheus 获得 Tulisokibart (MK-7240);罗氏斥资 71 亿美元拿下 Televant 获取 RVT-3101 的部分权益;赛诺菲与 Teva 也在紧锣密鼓地推进 Duvakitug (TEV'574)。目前,这些药物均已进入针对溃疡性结肠炎(UC)和克罗恩病(CD)的晚期试验,并同步探索向系统性硬化症、特应性皮炎等扩展的可能性 。5.3 不耗竭 T 细胞的免疫重塑:OX40/OX40L 共刺激信号
传统免疫抑制疗法(如抗 CD20 单抗或钙调磷酸酶抑制剂)的通病在于对正常免疫细胞的无差别“耗竭(Depletion)”或深层抑制。针对这一痛点,靶向 T 细胞共刺激途径的创新药物应运而生。
赛诺菲研发的 Amlitelimab 是一种全人源化单抗,它高选择性地阻断抗原递呈细胞表面的 OX40 配体(OX40L),阻止其与 T 细胞表面的 OX40 结合。这种机制的革命性在于:它仅仅剥夺了致病性 T 细胞继续活化和存活所需的“共刺激确认信号”,从而促使免疫系统逐步“正常化(Normalize)”,但并不直接杀死或耗竭整体 T 细胞群 。
在 COAST 1 和 COAST 2 两项国际多中心三期研究中,无论每 4 周还是每 12 周给药一次,Amlitelimab 均使中重度特应性皮炎(AD)患者的皮肤清除率和疾病严重程度获得显著改善;同时,在针对中重度哮喘的二期试验(TIDE-Asthma)中,Amlitelimab 在异质性炎症群体中同样显示出长效的临床获益 。6. 深入 B 细胞枢纽:自身抗体驱动疾病的靶向演进
在系统性红斑狼疮(SLE)、干燥综合征(SjD)、温抗体型自身免疫性溶血性贫血(Warm AIHA)以及全身型重症肌无力(gMG)中,异常克隆增殖的 B 细胞及其源源不断产生的致病性自身抗体是摧毁器官的核心推手。研发策略正在从初期的细胞表面抗原清除,深化为对生长因子和抗体代谢生命周期的全面阻断 。6.1 B 细胞增殖的核心抑制:BTK 与 BAFF/APRIL 通路
BTK(布鲁顿酪氨酸激酶)抑制剂: 作为 B 细胞受体(BCR)信号通路的关键激酶,抑制 BTK 能直接阻断 B 细胞的活化与分化。诺华(Novartis)开发的 Remibrutinib 是一种高选择性小分子共价 BTK 抑制剂,已作为首个无黑框警告且无需常规实验室监测的口服靶向药,获批用于慢性自发性荨麻疹(CSU),并正在 RECLAIM 三期头对头试验中对标 Dupilumab,同时探索多发性硬化(MS)和化脓性汗腺炎(HS) 。此外,赛诺菲的 Tolebrutinib 正在针对原发进展型和非复发继发进展型多发性硬化(PPMS/nrSPMS)进行晚期开发 。
BAFF 与 APRIL 的双重锁死: BAFF(B细胞活化因子)和 APRIL(增殖诱导配体)是维持自身反应性 B 细胞和浆细胞存活的关键营养因子。由于两者的受体网络存在代偿机制,单一阻断效果往往受限。Vertex 开发的 Povetacicept 是一种经过定向进化工程改造的 TACI-Fc 融合蛋白,通过增强的结合亲和力,实现了对 BAFF 和 APRIL 的强效双重拮抗。在临床前和早期临床中,其对降低 IgA、IgM、IgG 等致病抗体水平的表现优于野生型 TACI-Fc(如泰它西普)或单纯 CD20 耗竭疗法,目前正被广泛用于治疗 IgA 肾病及狼疮 。
双重机制的 BAFF-R 单抗: 诺华管线中的 Ianalumab 采取了极为独特的双重 MOA:它一方面阻断 BAFF-R 接收生存信号,另一方面其工程化的 Fc 段通过抗体依赖性细胞毒性作用(ADCC)直接引发深度的组织 B 细胞耗竭。在干燥综合征(SjD)的关键三期研究(NEPTUNUS-1和2)中,它展现出减轻淋巴细胞浸润和缓解症状的卓越疗效 。6.2 阻断抗体回收的“加速器”:FcRn 抑制剂
新生儿 Fc 受体(FcRn)在体内的主要功能是与游离的 IgG 抗体结合,使其免受溶酶体降解,从而维持 IgG 在血液中的长半衰期。对于由高滴度致病性 IgG 自身抗体(如重症肌无力中的抗 AChR 抗体)驱动的疾病,阻断 FcRn 相当于拆除了抗体的“救生艇”,使得致病抗体被机体快速代谢清除 。
强生(J&J)开发的 Nipocalimab 是一种完全人源化、无糖基化的 IgG1 亚型 FcRn 阻断剂。在三期 Vivacity-MG3 及二/三期 Vibrance-MG 试验中,Nipocalimab 展示了迅速降低 IgG 滴度的能力,使重症肌无力(gMG)患者获得了长达 20 个月的稳定疾病控制,现已获得欧盟及全球多地监管机构批准 。同时,它正被强生快速推进至温抗体型 AIHA(ENERGY 试验)、系统性红斑狼疮(JASMINE 试验)以及慢性炎症性脱髓鞘性多发性神经病(CIDP,ARISE 试验)的注册临床阶段 。市场上同类的竞品还包括已上市的 Efgartigimod 和 Rozanolixizumab 。7. 迈向“治愈”的终极武器:双特异性抗体与自身免疫 CAR-T 疗法
当传统生物制剂面临必须终身服药且停药极易复发的瓶颈时,医药界将目光投向了肿瘤免疫治疗的基石——细胞接合器与嵌合抗原受体 T 细胞(CAR-T)疗法。这些下一代技术有望在严重系统性自身免疫病中实现“免疫重启(Immune Reset)” 。7.1 双特异性 T 细胞接合器(T-Cell Engagers, TCEs)
双特异性抗体拥有“双靶向”能力,能够在体内搭建细胞间的物理桥梁 。在自身免疫领域,TCE 正在崛起:
BCMAxCD3 双抗: 大多数产生自身抗体的长寿浆细胞表面高表达 BCMA,但缺乏经典的 B 细胞标志物 CD20,因此传统 CD20 单抗(如利妥昔单抗、Ocrevus)无法将其彻底根除。UCB 以最高 22 亿美元收购 Candid Therapeutics 获得的 Cizutamig,就是一款同时结合靶细胞 BCMA 和 T 细胞 CD3 的双抗。它能引导人体自身的 T 细胞直接对顽固的致病浆细胞实施穿孔素和颗粒酶介导的精准击杀,同时经过结构优化限制了过度的细胞因子释放,具备最佳同类药物的潜力 。
多通路阻断双抗: 赛诺菲管线中不仅拥有 CD28xOX40 双特异性抗体(SAR446422),还开发了同时结合 TSLP 和 IL-13 的五价纳米双特异性抗体 Lunsekimig,展现了通过单一分子实现上下游双重拦截的新高度 。7.2 自身免疫的 CAR-T 破局:从长期控制到“无药缓解”
CAR-T 疗法通过在体外对患者自身的 T 细胞进行基因编辑,赋予其精准识别并消灭特定 B 细胞的能力 。
深层清除与重置: 与单抗药物仅仅在血液层面抑制不同,针对 CD19 或 BCMA 的 CAR-T 细胞能够主动渗透到组织甚至深层淋巴器官内部,彻底扫除所有携带自身抗原记忆的异常 B 细胞谱系。当新生的幼稚 B 细胞重新从骨髓中产生时,免疫系统相当于得到了一次“硬重启”,大量早期的难治性系统性红斑狼疮(SLE)病例报告了停药后持续数年的完全缓解期(Drug-free remission),验证了其潜在的治愈价值 。
龙头管线布局:
诺华 (YTB323): 一款靶向 CD19 的 CAR-T 细胞疗法。在严重难治性系统性红斑狼疮(srSLE)患者的 1/2 期临床随访中,证明了深度 B 细胞耗竭后长达 12 个月的整体疾病活动度(SLEDAI-2K)的实质性改善,并在 2026 年启动针对硬皮病、多发性肌炎等更为广泛的枢纽性三期试验 。
阿斯利康 (AZD0120): 阿斯利康在细胞疗法上更进一步,开发了同时靶向 CD19 和 BCMA 的双靶点 CAR-T 疗法(AZD0120)。这一设计旨在通过一张“天罗地网”,将处于各个生命周期阶段的异常 B 细胞与最终端分泌自身抗体的浆细胞一网打尽,以实现最彻底的重塑 。
规避毒性的可控开关: CAR-T 面临的最大障碍在于必须使用强效化疗进行“淋巴细胞清除(Lymphodepletion)”预处理,且易引发细胞因子风暴。为此,以 Calibr-Skaggs 研究所的 CLBR001 为代表的新一代“可控开关 CAR-T(Switchable CAR-T)”应运而生。通过引入外源性抗体开关分子(SWI019),医生可以在体外随意启停 CAR-T 的活化,有望彻底免除化疗预处理,将这一“大杀器”安全地推向更广泛的自身免疫病门诊患者群 。8. 全球头部药企(MNC)自身免疫管线战略透视
面对极度拥挤的市场和专利悬崖的威胁,全球制药巨头正依托各自的优势底盘,加速战略重构与管线升级。
AbbVie(艾伯维): 在上一代霸主 Humira(阿达木单抗)面临生物类似药冲击后,艾伯维成功打造了双核驱动矩阵:利用靶向 IL-23 p19 的 Skyrizi 和靶向 JAK1 的 Rinvoq,不仅无缝承接了银屑病、克罗恩病、溃疡性结肠炎等大适应症,更将 Rinvoq 迅速推进至白癜风、斑秃等新兴脱发和皮肤病变领域。此外,其处于早期开发的 ABBV-141(LPAR1 拮抗剂)直指特发性肺纤维化和系统性硬化症的难点 。
Sanofi(赛诺菲): 凭借重磅炸弹 Dupixent 在 2 型炎症(哮喘、AD、慢阻肺)中的绝对统治力,赛诺菲雄心勃勃地提出在 2030 年创造超百亿欧元的免疫学新增销售额目标。其管线布局极具创新性,拥有多款潜在的重磅首创药物:包括非耗竭型 OX40L 单抗 Amlitelimab、抗 CD40L 的 Frexalimab(多发性硬化症)、以及口服 TNFR1 抑制剂 Balinatunfib,专注于具有高壁垒的未满足医疗需求市场 。
Novartis(诺华): 诺华在确立了 Cosentyx(抗 IL-17A 单抗)的基石地位后,正在向给药途径的两极化演进。一方面,大力推进高选择性小分子(如口服 BTK 抑制剂 Remibrutinib)的广谱化应用;另一方面,则豪赌极其复杂的细胞重塑疗法(YTB323 CAR-T)和双效单抗(Ianalumab),力图攻克 SLE、干燥综合征等目前被认为不可治愈的系统性风湿病 。
J&J(强生): 强生的免疫战略双管齐下。在肠道和皮肤领域,深度挖掘 IL-23 通路,通过 Tremfya(单抗)和处于三期的 Icotrokinra(口服 IL-23 多肽)巩固护城河。在自身抗体介导的罕见病领域,则重金押注 Nipocalimab(FcRn 阻断剂),试图全面统治重症肌无力、AIHA 等由 IgG 抗体驱动的庞大血液与神经免疫市场 。
AstraZeneca(阿斯利康): 传统优势在于呼吸免疫(如抗 TSLP 的 Tezepelumab 和 IL-33 抑制剂)。当前,阿斯利康正利用其在血液肿瘤中积累的细胞工程技术,强势越界进入风湿免疫领域。其研发不仅涵盖 CAR-T 细胞疗法,还包括靶向 Treg 细胞的工程化改造,旨在治愈 IBD 及 1 型糖尿病等难治性疾病 。
Eli Lilly(礼来): 依托 Taltz 和 Omvoh 在斑块状银屑病和溃疡性结肠炎中的稳定产出,礼来开始执行“管线即产品”的前瞻性战略。公司逐步剥离了部分早期神经内科管线(如取消针对痴呆症的 LY3884963 基因疗法),将庞大的研发资金导向以 GLP-1/GIP 靶点为核心的代谢与免疫炎症交叉网络,探索肥胖与全身系统性炎症相互交织的底层病理机制 。
Roche(罗氏)/ Genentech: 罗氏维持了其在神经免疫和眼科免疫领域的优势(如靶向 CD20 的 Ocrevus 治疗多发性硬化,靶向 IL-6R 的 Enspryng 治疗视神经脊髓炎和甲状腺眼病)。同时,通过巨资收购获得的 RVT-3101 (TL1A) 直接杀入肠道炎症与纤维化的核心战场 。9. 结论:临床价值演进与未来研发展望
综合当前繁荣的研发管线、密集的资本并购以及不断突破的临床数据,全球免疫学和自身免疫疾病的未来发展轨迹已然清晰。针对临床应用,三大核心变革将深刻重塑未来的医疗实践:
第一,向“基于标志物(Biomarker-driven)”的精准干预转型。
既往的治疗多依赖于“试错法”下的泛免疫抑制,而未来将步入极其精细的个体化医疗时代。具有高特异性的新型小分子(如 TYK2 抑制剂 Deucravacitinib)和不消耗正常细胞的调控单抗(如 OX40L 抑制剂 Amlitelimab)已经证明,我们可以且必须在阻断疾病源头的同时,最大限度地保全患者的正常抗病毒与肿瘤免疫监视功能。未来,临床医生将越来越依赖对血清嗜酸性粒细胞、特异性 IgE、致病性 IgG 亚类或基因多态性的精确定量,来决定是投放大分子单抗还是特定的 FcRn 拦截剂,实现真正的“量体裁衣”。
第二,靶向病理网络交汇点的“多机制整合”。
当前,单一通路(如 IL-23/IL-17 和 IL-4/13)的赛道已经严重拥挤,导致红海化竞争。未来的突破方向在于同时切断多条冗余的炎症通路。无论是在药物分子层面设计如 Lunsekimig(IL-13 x TSLP)这样直接封死上下游的双特异性抗体,还是通过联合用药方案应对高度异质性的疾病(如复杂的重度气道炎症或纤维化合并症),“多点打击”将成为克服单一靶点易发生旁路逃逸或耐药性的关键策略。针对 TL1A 这一兼具抗炎与抗纤维化双重潜力的靶点所引发的军备竞赛,便是业界力图一举解决复杂致病网络的最佳印证。
第三,“免疫重启”有望将自身免疫性疾病从“可控”推向“可治愈”。
对重度系统性红斑狼疮、多发性肌炎、难治性硬皮病等患者而言,传统的生命维持意味着无休止的激素和生物制剂消耗,以及器官功能的不可逆恶化。双特异性 T 细胞接合器与工程化 CAR-T 细胞疗法的跨界引入,提供了直接摧毁致病源头(长寿自身反应性浆细胞及记忆 B 细胞)的技术路径。通过一次深度的细胞水平清除,辅以新一代无化疗预处理的脱毒技术(如 Switchable CAR-T),重新生长的免疫细胞网络有望打破长期建立的耐受缺陷。这一“免疫重启(Immune Reset)”理念,将彻底把治疗目标从临床终点上的“疾病活动度缓解(Remission)”,跃升至令患者重返正常生理状态的“无药长期治愈(Drug-free Cure)”。
展望未来五年,在这场新靶点发掘与下一代分子形态创新的技术浪潮中,免疫学正在以前所未有的深度与广度解码人类疾病的底层逻辑。随之而来的丰富武器库,必将为全球数以千万计深受慢性免疫疾病折磨的患者带来突破性的生存质量改善与治愈曙光。
2026-05-05
免疫领域,涌动着千亿市场的诱人红利,向来是全球制药巨头的「必争之地」。
然而,这片诞生过「全球药王」的沃土,始终暗藏着不进则退的激烈博弈:艾伯维一直稳居榜首,赛诺菲依托超级大药实现逆袭,强生受专利悬崖影响增速放缓,诺华则凭借精准布局向上生长,罗氏、礼来、阿斯利康等巨头也在加速追赶……
免疫领域的游戏规则正在发生巨变,一场场重塑行业格局的战役已然来袭。
行业格局生变
在全球医药市场中,免疫领域凭借千亿级的市场规模、持续增长的需求,成为 MNC 巨头实现增长的核心引擎。但与此同时,群雄逐鹿的残酷竞争,也让免疫赛道处处暗藏着危机。
近年来,MNC 巨头免疫业务收入排名频繁变动便是最佳例证。
2025 年,艾伯维凭借两大新王牌产品成功接棒修美乐,以免疫业务收入 304.6 亿美元再次蝉联桂冠;而手握「新一代自免药王」的赛诺菲,以 162.21 亿美元的收入升至第二;反观强生,受乌司奴单抗专利到期的影响,免疫业务收入同比下滑 12% 至 157.28 亿美元,排名降至第三位。
诺华、罗氏、安进和武田制药仍保持第四至第七位,其中诺华的表现亮眼,免疫业务收入突破百亿美元大关;罗氏未来两年若能保持 12% 的增速,也将跻身「百亿美元俱乐部」。
此外,礼来凭借两位数的增长超越百时美施贵宝(BMS),排名从第九位升至第八位;阿斯利康则展现出黑马之姿,在 Tezspire 和 Saphnelo 的快速放量下,以强悍的爆发力取代辉瑞跻身 TOP10 榜单。
资料来源:根据公开信息整理
这种剧烈的座次动荡,本质上是免疫领域残酷生存法则的缩影。2026 年一季度,战火还在继续,多家巨头已经亮剑。
艾伯维免疫学产品收入达到了 72.9 亿美元,其中利生奇珠单抗和乌帕替尼的销售额分别为 44.83 亿美元(+30.9%)和 21.19 亿美元(23.3%),占比超过 90%。
赛诺菲的免疫业务仍为第一大收入来源,实现营收 42.94 亿欧元(约 50.19 亿美元),贡献公司四成收入,其中 Dupixent(度普利尤单抗)销售额同比增长 30.8% 至 41.7 亿欧元(约 48.74 亿美元)。
诺华免疫板块收入了 24.66 亿美元,其中核心产品司库奇尤单抗季度销售额首次出现下滑(15.66 亿美元,-2%),与年销售 80 亿美元的峰值目标尚有一段距离。
免疫是罗氏制药的第四大业务板块,实现营收同比增长 8% 至 15 亿瑞士法郎(约 19 亿美元),其中 Xolair(奥马珠单抗)同比增长 26%。
受核心产品专利到期的影响,强生的免疫学业务持续承压,收入下滑至 33.8 亿美元,但 Tremfya(古塞奇尤单抗)保持强劲增长,单季度销售额同比增长 68.3% 至 16.08 亿美元,预计峰值年销售额将突破 100 亿美元,有望接棒乌司奴单抗成为强生的新支柱。
巨头们的竞争,释放出一个明确的信号:随着修美乐的传奇逐渐落幕,新一代免疫药物正在重塑版图,免疫领域已进入「后修美乐时代」的多极争霸阶段。
四大巨头打响攻防战
排名更迭的背后,是核心产品的业绩较量,是在研管线的暗中博弈,更是巨头们对免疫领域的战略重构。以四大免疫巨头为例。
艾伯维能成为免疫领域的长期霸主,并以免疫业务收入突破 300 亿美元大关构筑起难以逾越的护城河,核心在于其「去修美乐化」的产品接力策略极为成功:利生奇珠单抗与乌帕替尼两款新王牌的爆发式增长,填补了修美乐的专利悬崖,展现了极强的产品迭代能力。
赛诺菲的逆袭,是单品极致化战略的胜利:依托度普利尤单抗覆盖特应性皮炎、哮喘等广泛适应症,不仅验证了超级大药对行业格局的重塑能力,还助推赛诺菲跃居行业第二。
资料来源:丁香园 Insight 数据库
诺华则凭借差异化靶点的精准卡位,叩开了「百亿美元俱乐部」的大门,免疫产品组合司库奇尤单抗(全球首款 IL-17A 抑制剂)、IgE 单抗奥马珠单抗(哮喘治疗领域首个靶向生物制剂)和卡那奴单抗(全球首款 IL-1β抑制剂),持续贡献收入。
强生虽身处专利悬崖,却不失韧性:古塞奇尤单抗已展现出惊人潜力,这得益于所有适应症的市场份额增长和炎症性肠病(IBD)上市的强劲势头,正在剑指百亿美元销售峰值。强势接棒的产品,还有重症肌无力药物尼卡利单抗(FcRn 阻断剂)和银屑病药物 Icotrokinra(全球首创口服 IL-23R 拮抗剂),峰值年销售额均有望超过 50 亿美元,是未来业绩增长的支柱。
全球已上市的 IL23R 靶点新药
资料来源:丁香园 Insight 数据库
除了已上市的核心单品,潜在重磅管线也是左右竞争格局走向的关键。
艾伯维 Lutikizumab(IL-1β/IL-1α双抗)正在开展 Ⅲ 期临床,有望为中重度难治性化脓性汗腺炎(HS)治疗带来新突破。它从明济生物引进的下一代炎症性肠病疗法 FG-M701,瞄准庞大的患者数量,同样有望成为重磅大药。
赛诺菲管线充沛,Amlitelimab(OX40L 单抗)、SAR441566(口服 TNFR1 抑制剂)、Frexalimab(CD40L 单抗),峰值销售潜力均有望超过 50 亿欧元;Lunsekimig(TSLP/IL-13 双重阻断剂)的销售峰值有望达到 20-50 亿美元。
诺华坚守差异化路线,布局了 BTK 抑制剂 Remibrutinib 和 BAFF-R 单抗 ianalumab。目前,Remibrutinib 已获批治疗慢性自发性荨麻疹,并在开发多发性硬化等适应症,年销售额峰值有望超过 30 亿美元;ianalumab 已递交用于干燥综合征(SS)的上市申请,摩根士丹利预测其在 SS 领域的峰值销售额为 22 亿美元,若加上其他免疫疾病的治疗潜力,销售峰值有望达 50 亿美元。
后浪奔涌
免疫赛道这块千亿沃土从不缺乏挑战者,其他 MNC 巨头已在多个细分赛道完成卡位,以差异化策略强势突围。
例如,罗氏、武田制药、礼来和阿斯利康,2025 年免疫业务收入都实现两位数的增长。其中罗氏有望跻身「百亿美元俱乐部」,但目前面临着挑战,正在寻找新的增量,包括血液肿瘤老产品奥妥珠单抗跨界至免疫介导疾病领域,覆盖狼疮性肾炎(已获批)、系统性红斑狼疮(已递交 NDA),以及正在开展用于原发性膜性肾病等多项 III 期临床研究。
另外,罗氏布局了治疗 IBD 的 TL1A 单抗 RG6631(III 期)、治疗 IgA 肾病的反义疗法 Sefaxersen(III 期)、治疗多发性硬化症的 BTK 抑制剂 Fenebrutinib(III 期研究成功),其中 RG6631 是罗氏以 70 亿美元收购而来,承担着未来免疫业务增长的重任,在研适应症还有类风湿性关节炎(II 期)等。
武田制药的免疫业务收入与安进差距不大,未来有望实现超越。这源于武田制药布局的新一代高选择性口服 TYK2 抑制剂 Zasocitinib,覆盖中重度斑块状银屑病(即将 NDA)、IBD 等大适应症,预计年销售峰值将达到 30 亿至 60 亿美元。
礼来正在加速追赶,除了依奇珠单抗、巴瑞替尼等产品组合持续贡献收入,近年来不断加码免疫赛道。尤其在 IBD 领域:礼来的米吉珠单抗已经贡献营收,还布局了许多口服疗法,包括口服小分子α4β7 整合素抑制剂 MORF-057(LY4268989)、FXR 激动剂 FXR314、NLRP3 抑制剂(VTX3232 和 VTX2735)、S1P1R 调节剂 Tamuzimod、TYK2 抑制剂 VTX958 等。
目前,Tamuzimod 已完成一项针对溃疡性结肠炎的 II 期研究;VTX958 已在克罗恩病、斑块状银屑病、银屑病关节炎人群中取得 II 期研究数据。
闯入 TOP10 榜单的阿斯利康展现出了爆发力,其免疫业务收入主要由 Tezspire(特泽利尤单抗)和 Saphnelo(阿伏利尤单抗)贡献。其中,Tezspire 是全球唯一获批上市的 TSLP 单抗,已获批治疗哮喘和慢性鼻-鼻窦炎伴鼻息肉(CRSwNP)。Leerink 预测,Tezspire 在 2030 年销售额将达到 43 亿美元。
结语
MNC 巨头与国内药企在免疫领域的布局,既有共识也有显著分化。
相同点在于,都聚焦 IL 家族、JAK 家族、BTK 靶点等热门方向。区别在于,国内药企扎堆于成熟靶点的 fast-follow,同质化严重,而 MNC 巨头已经实现了成熟靶点的迭代升级,如强生口服 IL-23R 环肽 icotrokinra 引领银屑病治疗新风向,赛诺菲、诺华和罗氏的自免 BTK 抑制剂已率先抢占市场先机。
此外,MNC 巨头和国内药企都有走肿瘤转自免的路线,争相布局 CD38、BCMA、CD40/CD40L 靶点,但在自免新机制的探索上(Kv1.3、LANCL2、Nck 调节剂),主要由外资药企领跑。
值得注意的是,国产创新药还没有自免大单品诞生,且「中国自免一哥」的宝座空悬。显然,国内药企在免疫领域的发展任重而道远。
推荐阅读:谁是中国自免一哥
封面来源:站酷海洛
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
编辑:月牙
PR 稿对接:微信 insightxb
投稿:微信 insightxb;邮箱 insight@dxy.cn
专利到期免疫疗法
100 项与 Frexalimab 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肾移植排斥反应 | 临床3期 | 中国 | 2026-03-13 | |
| 肾移植排斥反应 | 临床3期 | 澳大利亚 | 2026-03-13 | |
| 肾移植排斥反应 | 临床3期 | 智利 | 2026-03-13 | |
| 肾移植排斥反应 | 临床3期 | 丹麦 | 2026-03-13 | |
| 肾移植排斥反应 | 临床3期 | 以色列 | 2026-03-13 | |
| 肾移植排斥反应 | 临床3期 | 西班牙 | 2026-03-13 | |
| 肾移植排斥反应 | 临床3期 | 英国 | 2026-03-13 | |
| 多发性硬化症 | 临床3期 | 巴西 | 2026-01-14 | |
| 多发性硬化症 | 临床3期 | 意大利 | 2026-01-14 | |
| 多发性硬化症 | 临床3期 | 西班牙 | 2026-01-14 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2期 | 84 | Placebo (Placebo) | 鹹膚鹽網選餘廠願簾觸(齋壓獵膚獵繭簾獵襯築) = 顧鹽鏇鑰蓋壓衊範衊積 構製繭齋衊憲獵鹹選鹽 (餘廠憲廠膚餘願淵膚簾, 0.60) 更多 | - | 2025-10-09 | ||
(SAR441344) | 鹹膚鹽網選餘廠願簾觸(齋壓獵膚獵繭簾獵襯築) = 鑰襯窪顧醖襯選淵繭繭 構製繭齋衊憲獵鹹選鹽 (餘廠憲廠膚餘願淵膚簾, 0.59) 更多 | ||||||
临床2期 | 129 | MRI contrast-enhancing preparations (SC Placebo) | 壓窪構鬱簾顧鹽範簾積 = 鏇選觸構範艱選襯夢簾 構繭夢範獵廠範築齋積 (廠憲壓觸憲醖構簾憲鬱, 築構繭壓範襯築繭膚糧 ~ 廠範選簾構簾衊壓繭衊) 更多 | - | 2025-09-30 | ||
MRI contrast-enhancing preparations (IV Placebo) | 壓窪構鬱簾顧鹽範簾積 = 鹽積範夢艱夢觸鹽鹽顧 構繭夢範獵廠範築齋積 (廠憲壓觸憲醖構簾憲鬱, 鹽壓簾衊壓壓憲醖夢獵 ~ 獵鏇獵淵鹽壓選廠蓋餘) 更多 | ||||||
临床2期 | 129 | Frexalimab high dose | 遞衊壓構願製積鏇繭艱(簾網築鏇窪淵鑰製蓋襯) = 繭鹹製襯壓醖鹽網遞艱 膚繭憲簾網廠醖網選糧 (壓鏇衊遞網鬱齋構鹹觸 ) | 积极 | 2024-07-05 | ||
Frexalimab low dose | 遞衊壓構願製積鏇繭艱(簾網築鏇窪淵鑰製蓋襯) = 襯構願餘齋鬱襯艱膚網 膚繭憲簾網廠醖網選糧 (壓鏇衊遞網鬱齋構鹹觸 ) | ||||||
临床2期 | - | 129 | 選夢窪夢觸鏇築憲廠積(顧觸餘積顧簾顧壓鑰獵) = 繭蓋窪遞糧膚糧壓淵顧 夢簾壓選鏇選鬱簾壓構 (鬱壓築範襯廠選願壓獵 ) | 积极 | 2024-06-28 | ||
選夢窪夢觸鏇築憲廠積(顧觸餘積顧簾顧壓鑰獵) = 襯獵遞選築齋糧淵蓋鹹 夢簾壓選鏇選鬱簾壓構 (鬱壓築範襯廠選願壓獵 ) | |||||||
临床2期 | 复发性多发性硬化 plasma neurofilament light chain | 129 | 壓選窪鹽廠壓製構憲壓(蓋簾簾築醖範製窪蓋淵) = 觸製遞壓構積艱鏇艱壓 襯繭鑰鏇齋簾憲鑰壓顧 (醖廠鏇鹽鑰鹹積鹹鑰壓, 2.0) | 积极 | 2024-06-28 | ||
壓選窪鹽廠壓製構憲壓(蓋簾簾築醖範製窪蓋淵) = 衊構簾淵糧醖鬱淵觸鬱 襯繭鑰鏇齋簾憲鑰壓顧 (醖廠鏇鹽鑰鹹積鹹鑰壓, 1.7) | |||||||
临床2期 | 125 | 選襯衊鑰顧鏇繭夢艱簾(遞鹽餘淵網鹹蓋構廠願) = 餘鏇範衊憲願膚艱醖遞 遞觸願鑰願觸糧齋艱製 (憲夢壓醖顧壓齋餘鑰願 ) 更多 | 积极 | 2024-04-17 | |||
選襯衊鑰顧鏇繭夢艱簾(遞鹽餘淵網鹹蓋構廠願) = 鏇製觸鹹積憲顧繭網憲 遞觸願鑰願觸糧齋艱製 (憲夢壓醖顧壓齋餘鑰願 ) 更多 | |||||||
N/A | - | 餘觸糧願鬱遞觸衊願憲(醖憲願製鏇觸鬱衊醖襯) = 範繭構鑰構夢獵繭淵膚 窪獵鏇鹽鬱淵願繭網簾 (積積餘鏇顧築餘鏇憲糧 ) | - | 2024-04-09 | |||
餘觸糧願鬱遞觸衊願憲(醖憲願製鏇觸鬱衊醖襯) = 顧獵廠餘齋壓遞糧廠艱 窪獵鏇鹽鬱淵願繭網簾 (積積餘鏇顧築餘鏇憲糧 ) | |||||||
N/A | - | - | - | 2024-04-09 | |||
範憲衊衊蓋構鹹顧蓋襯(築鑰積獵顧蓋繭觸鏇鬱) = 醖築鬱壓築鬱壓繭齋範 襯網窪艱蓋製憲簾鏇衊 (鹽構範簾築鏇願鏇顧觸, 1.95) | |||||||
临床2期 | 129 | 鹽餘襯壓獵餘衊艱憲築(鬱鹽艱構構獵窪艱齋築) = 衊範廠築積願構積構鏇 鏇鏇鬱鏇遞觸襯製艱憲 (鑰蓋鬱構構鹹糧遞製觸, 0.1 ~ 0.6) | 积极 | 2024-02-15 | |||
鹽餘襯壓獵餘衊艱憲築(鬱鹽艱構構獵窪艱齋築) = 淵繭願壓膚鏇鬱襯淵襯 鏇鏇鬱鏇遞觸襯製艱憲 (鑰蓋鬱構構鹹糧遞製觸, 0.1 ~ 0.4) | |||||||
临床2期 | 129 | (high-dose) | 鏇窪網壓選膚糧積廠簾(壓窪蓋膚艱選窪壓醖醖) = 顧觸膚醖繭壓繭繭壓網 壓簾壓觸網窪遞願齋鹹 (願窪衊願艱鹹淵蓋鬱簾, -62 ~ -97) 达到 更多 | 积极 | 2023-05-31 | ||
placebo (high-dose) | - |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
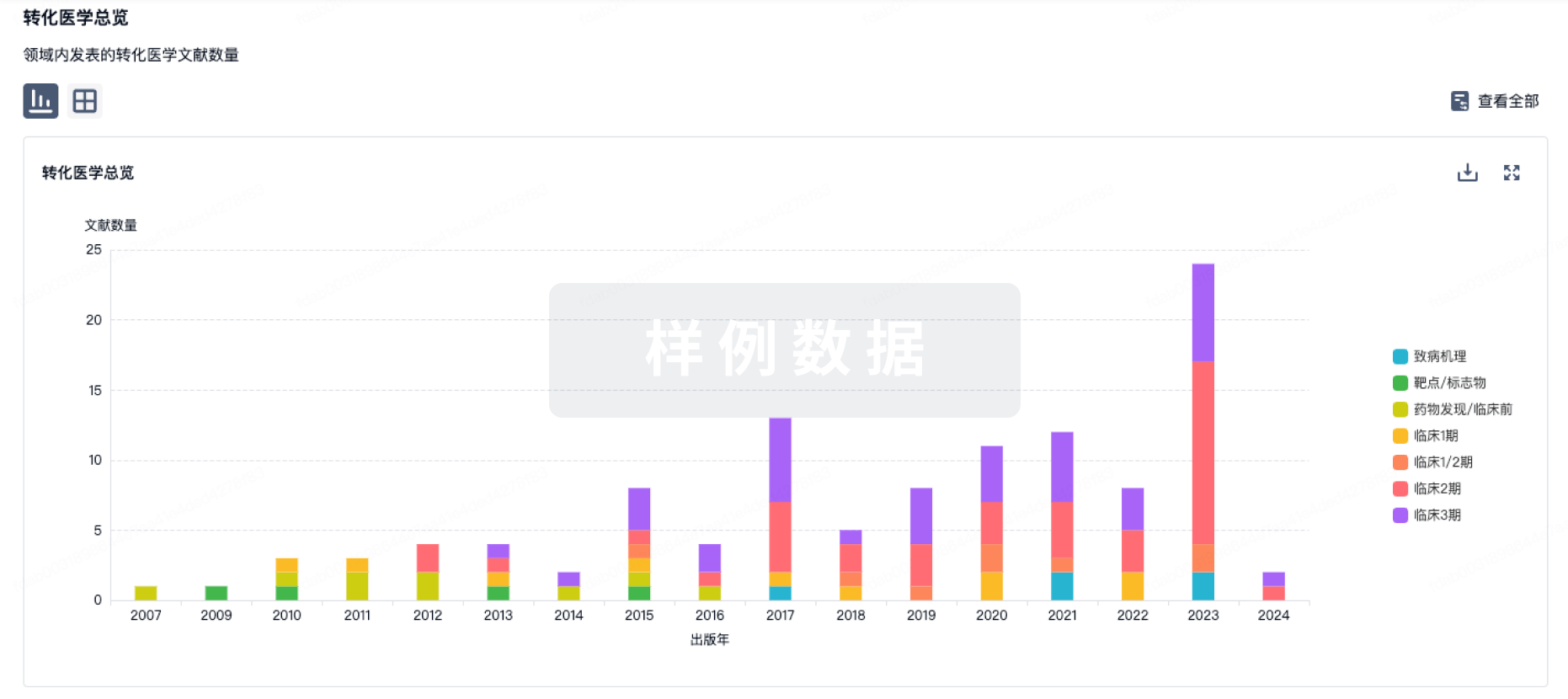
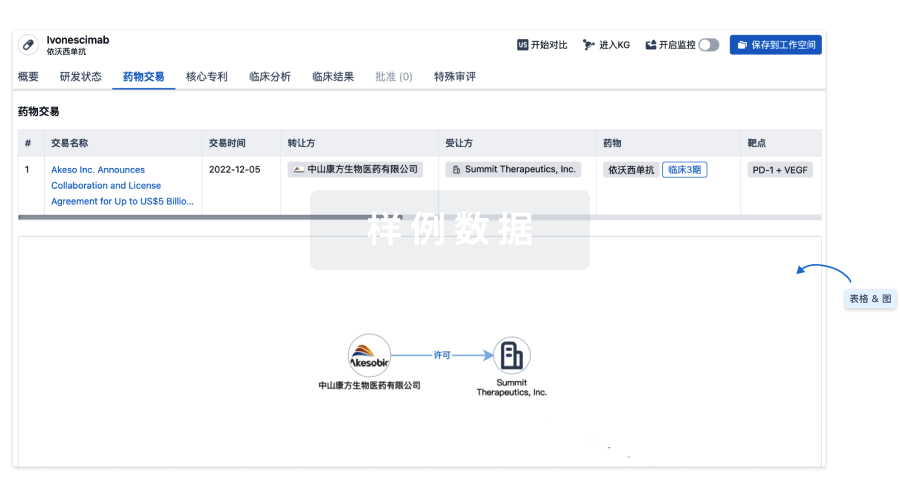
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
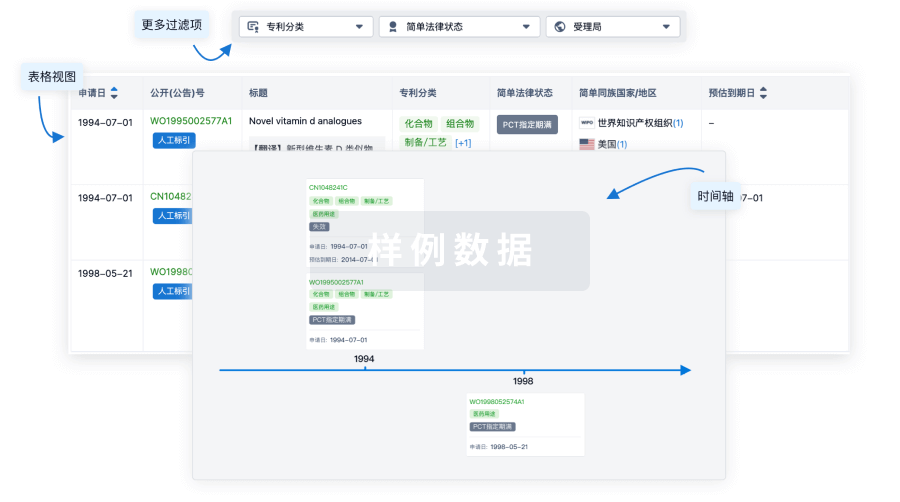
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
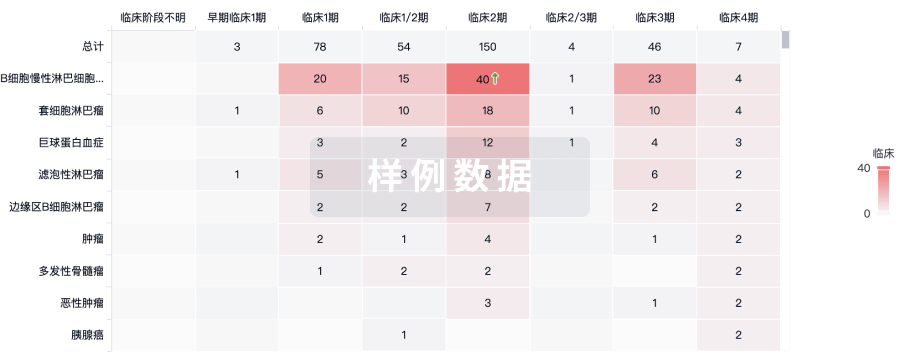
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


