2
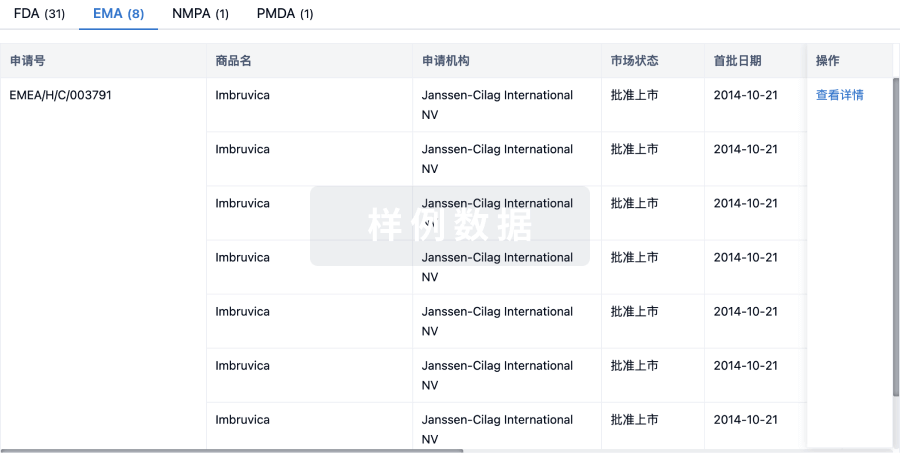
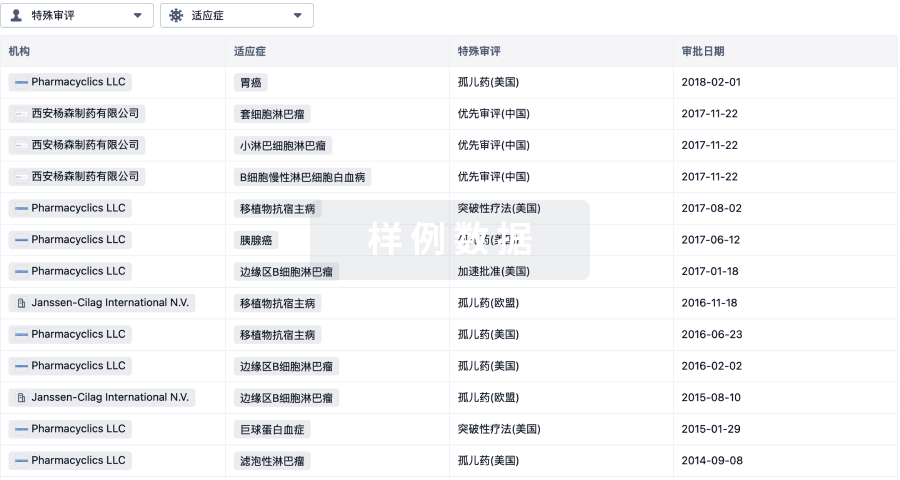
项与 靶向 CD19 非病毒 PD1 定点整合 CAR-T 细胞(上海邦耀) 相关的临床试验A Phase I/II Clinical Study of the Safety and Efficacy of CD19-targeted Non-viral PD1 Site-specific Integrated CAR-T Cell Injection (BRL-201) in the Treatment of Relapsed or Refractory B Lymphocyte Non-Hodgkin Lymphoma
This is a multi-center, single-arm, open-label clinical study, and the sample size is set to 12-18 subjects.
a Safety and Efficacy Evaluation of PD1-CD19-CART in Patients With Relapse/Refractory B-cell Lymphoma
This is an open label, single-site, dose-escalation study in up to 25 participants with relapse/refractory B-NHL. This study aims to evaluate the safety and efficacy of the treatment with PD1-CD19-CART.
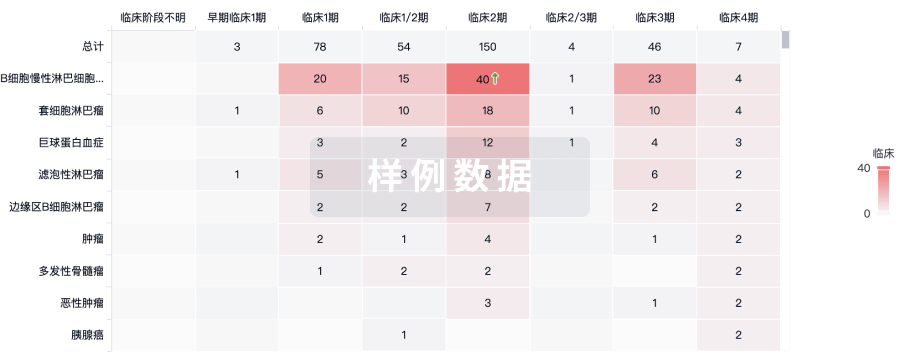
100 项与 靶向 CD19 非病毒 PD1 定点整合 CAR-T 细胞(上海邦耀) 相关的临床结果
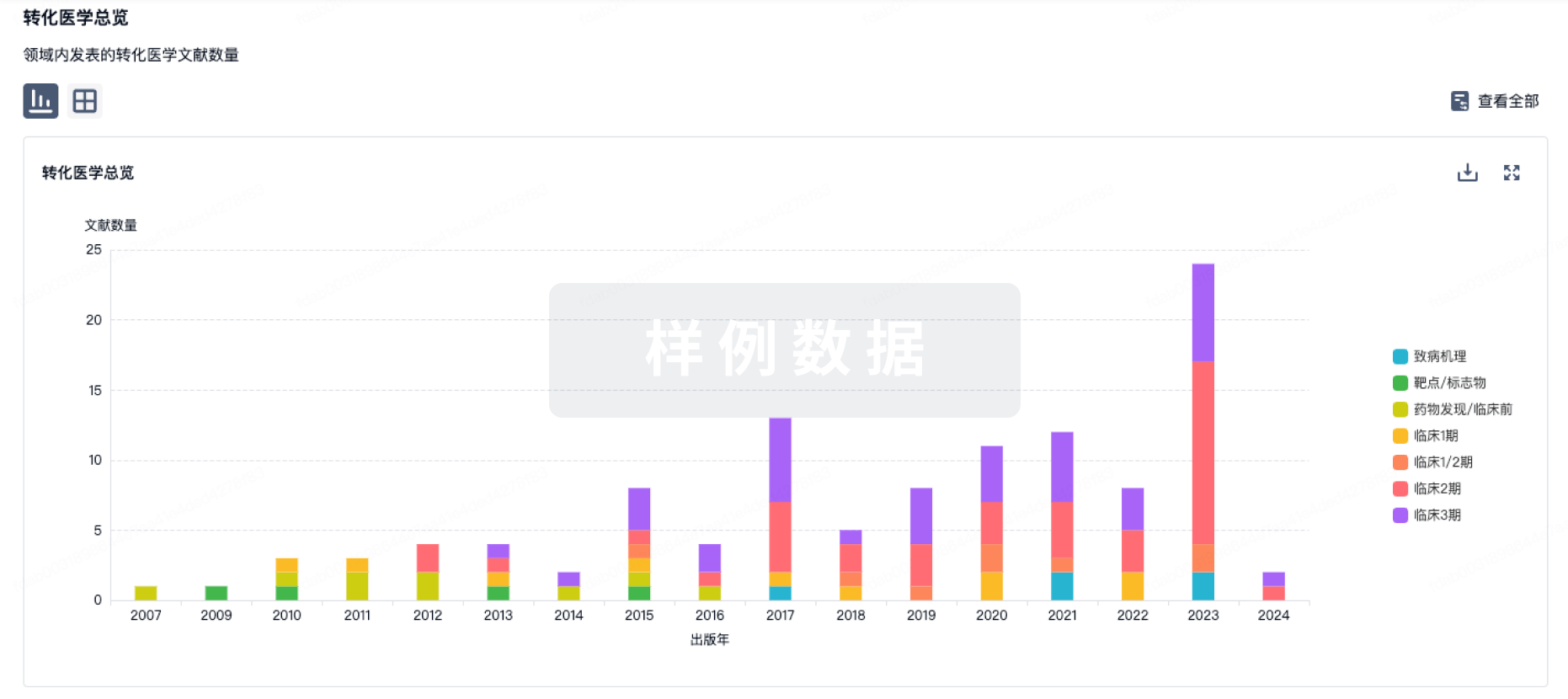
100 项与 靶向 CD19 非病毒 PD1 定点整合 CAR-T 细胞(上海邦耀) 相关的转化医学
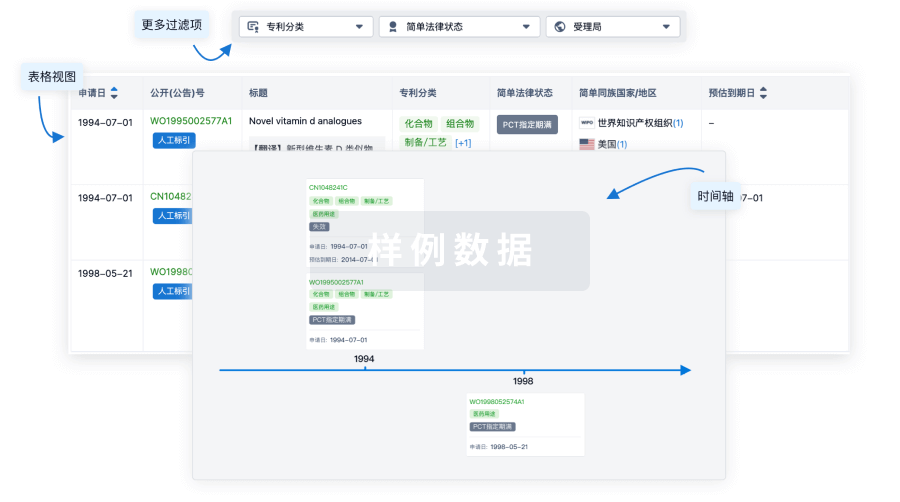
100 项与 靶向 CD19 非病毒 PD1 定点整合 CAR-T 细胞(上海邦耀) 相关的专利(医药)
52
项与 靶向 CD19 非病毒 PD1 定点整合 CAR-T 细胞(上海邦耀) 相关的新闻(医药)岁序更替,科创不止。2026年1月15日,聚焦于基因和细胞治疗的上海邦耀生物科技有限公司(以下简称“邦耀生物”)隆重举行了2025年度总结会暨2026新春年会。本次年会以“骏启新程,耀创未来”为主题,系统回顾了过去一年的科研突破与经营成果,并展望了新一年的战略方向与发展蓝图。公司凭借在基因与细胞疗法领域的持续创新,正加速推动多项全球前沿技术从实验室迈向临床,展现了引领行业变革的科技实力。
领导团队合影
年度总结会:骏启新程 · 耀创未来
2026年1月15日下午,年度总结会率先启幕。首先由邦耀生物联合创始人&副总裁李大力教授围绕基因编辑工具的最新进展与应用前景展开报告演讲,用深厚的学术积淀为企业技术创新提供了重要思路,并奠定了坚实的基础。
联合创始人&副总裁李大力教授
随后,邦耀生物首席技术官(CTO)谭炳合博士、研发副总裁张娜博士及研发总监王飞博士,分别聚焦新一代异体通用型CAR-T(管线代号:BRL-301/BRL-303)、非病毒定点整合PD1-CAR-T(管线代号:BRL-201/BRL-203)、地贫基因疗法BRL-101(管线代号:BRL-101)等几款“明星”产品管线,分享了相关管线的最新进展与未来推进计划,展现了公司在CGT药物研发上的扎实积累与稳步推进。
从左至右依次为:谭炳合博士、张娜博士、王飞博士
最后公司领导进行总结与战略指引。邦耀生物联合创始人&副总裁杜冰教授对公司2025年的一整年丰硕科研成果和多个重要里程碑事件做了全面梳理与回顾。
联合创始人&副总裁杜冰教授
邦耀生物首席执行官(CEO)向宇博士深入阐述了新一年的公司发展规划,明确了2026年加速管线临床转化、推进全球商业化的核心目标。这不仅是一份面向未来的战略蓝图,更是对邦耀生物使命愿景的坚定践行。邦耀生物将以此为目标,全力推动科学理想向现实成果转化,在全球健康领域书写新的篇章。
首席执行官(CEO)向宇博士
邦耀生物创始人&副董事长席在喜进行了一年一度富有洞见又鼓舞人心的主题分享,今年以“心之所向、善启新章”为主题,倡导用真善美引领价值观来开启邦耀下一个十年的辉煌征程,重申“以基因编辑技术引领创新,开发突破性疗法,造福全人类”的使命初心。
创始人&副董事长席在喜
邦耀生物创始人&董事长刘明耀教授在最后总结发言中,充分肯定了公司过去一年在科研与产品管线推进上取得的成就,并勉励全体邦耀人继续秉持创新精神,紧密协作,在2026年迈向新的高度。期待邦耀生物推动更多突破性疗法落地,让创新技术惠及全球患者。
创始人&董事长刘明耀教授
新春年会:欢庆佳绩,共叙温情
在当晚举行的年会现场,华灯初上,笑语欢声。新春拜年视频的播放传递着浓浓暖意,领导致辞送祝福后,晚宴正式开席。开场歌舞《鼓舞》气势磅礴,瞬间点燃现场氛围。随后晚宴穿插多轮颁奖环节,颁发了业绩飞跃奖、效率提升奖、技术能手奖等多项荣誉,对过去一年涌现出的优秀团队与个人进行了隆重表彰,充分肯定了各部门员工的卓越贡献。
首席执行官(CEO)向宇博士新春晚宴致辞
新岁启封,征途浩荡。2026年,邦耀生物将以此次年会为契机,怀揣初心、深耕技术,在基因与细胞治疗领域持续突破,以更优质的创新疗法守护人类健康,书写普惠医疗的崭新篇章。
END
关于邦耀生物
上海邦耀生物科技有限公司致力于成为新商业文明时代全球领先的细胞基因药企,邦耀生物以“以基因编辑技术引领创新,开发突破性疗法,造福全人类”为使命,依托自主研发中心及与高校共建的“上海基因编辑与细胞治疗研究中心”,目前已产生100多项专利成果,有19个项目在20余家知名医院开展临床试验,6个项目已获批IND,正式进入注册临床试验阶段,还有多个项目进入IND申报阶段。其中,基因编辑治疗β-地中海贫血症、非病毒定点整合PD1-CAR-T、以及UCAR-T等项目已经取得优异临床效果,具有全球领先性,并在Nature、Cell、Nature Medicine、Nature biotechnology等知名学术期刊上发表多篇学术论文。邦耀生物已搭建基因编辑技术创新平台、造血干细胞平台、非病毒定点整合CAR-T平台、通用型细胞平台、增强型T细胞平台、体内基因编辑CAR-T平台六大具有自主知识产权的技术平台,拥有7000平米GMP中试基地及近100人的运营团队,有力保障创新的研究成果能够快速转化与应用。邦耀生物通过患者需求和临床反馈不断推动研发产品快速更新迭代。并秉持开放、共享、共赢的态度,与全球创新生物医药生态链企业一起,加快推进创新药物的转化与落地,造福全球遗传疾病、恶性肿瘤及自身免疫系统疾病等患者!
扫码关注,解锁更多
微 信 号:bioraylab
为人类健康提供解决方案
合作、投稿、转载授权事宜请联系
邮箱:wjinfang@brlmed.com
> 一款定价仅20余万元的国产CAR-T细胞药物,在2025年12月12日正式向国家药监局药品审评中心递交了上市申请。这不仅将此前动辄百万元的CAR-T治疗费用大幅拉低,也标志着中国细胞治疗产业正从“技术验证期”加速迈向“商业化普及期”。

1. 价格屠夫入场:全产业链自主降成本
递交申请的华道生物,其首款CAR-T药物针对**难治复发性非霍奇金淋巴瘤**。公司自2017年成立便明确“让中国患者用得起CAR-T疗法”的使命,其战略核心在于**全产业链工艺优化与成本重构**。
> 华道生物创始人余学军曾坦言,CAR-T疗法的本质是‘活体药品’,其高昂价格主要来源于三方面:病毒载体成本、生产过程复杂性和质控体系要求。
通过自主研发的规模化病毒生产工艺和全自动、全封闭的无人化生产系统,华道生物将细胞药物产能提升至传统方法的**50倍以上**,位于上海松江的个性化CAR-T全自动生产基地一期年产能可达**9000人份**。这为其将价格定在20余万元区间提供了坚实基础。
2. 疗效不妥协:临床数据支撑竞争力
低价并不意味着低质。根据华道生物在2024年美国血液学会年会上公布的II期临床试验数据,其CD19 CAR-T疗法在**112例**复发/难治性非霍奇金淋巴瘤患者中,显示出与已上市产品相当的疗效和安全性。
- **客观缓解率**为82.1%
- **完全缓解率**为58.9%
- 在弥漫大B细胞淋巴瘤亚组中,中位无进展生存期达**16.3个月**
更值得注意的是,其临床试验中仅**1例患者**因细胞制备失败而未能接受输注,制备成功率高达99.1%,远低于行业平均的5-8%失败率。
3. 国产CAR-T集体爆发:多款产品数据惊艳
华道生物的进展仅是国产CAR-T近期集体突破的缩影。2025年11月至12月,多款产品取得关键进展:
- **合源生物**的纳基奥仑赛注射液于11月28日获批用于治疗复发或难治性大B细胞淋巴瘤,成为国内**唯一**同时覆盖白血病和淋巴瘤两大适应症的CAR-T产品。其关键临床研究数据显示,联合自体干细胞移植策略的**最佳总缓解率高达92%**,且无≥3级细胞因子释放综合征发生。

- **邦耀生物**在2025年ASH年会上公布的BRL-201最新长期随访数据显示,在**21例**复发/难治性B细胞非霍奇金淋巴瘤患者中,**客观缓解率达到100%**,完全缓解率为85.7%,且所有患者均未发生任何2级及以上的严重副作用。
- **精准生物**的普基奥仑赛注射液于11月7日获批,用于治疗3~21岁CD19阳性的难治或复发急性B淋巴细胞白血病,成为**中国首个**针对该儿童及青少年患者群体的CAR-T药物。
4. 支付端现曙光:从商保目录到医保门槛
高价一直是限制CAR-T疗法可及性的核心瓶颈。目前中国市场已上市的CAR-T疗法价格普遍处于**99.9万至129万元**区间。自2021年首款产品获批以来,四年间全国治疗患者总数仍不足2000人。
转机正在出现。2025年12月7日,国家医保局首次发布《商业健康保险创新药品目录》,纳入了19款创新药,其中**五款CAR-T产品**成功入选,占比超过四分之一。合源生物的纳基奥仑赛注射液正在其中。

业内分析认为,华道生物20万元级别的定价,**大概率能落在我国医保支付体系的可承受范围之内**,有望打破细胞免疫疗法在医保准入中的壁垒,使其从高端医疗选择转型为具备普惠性质的公共卫生产品。
5. 从奢侈品到普及品:行业拐点已至
国产CAR-T的集体突破,正从价格和疗效两个维度重塑市场格局。企业通过**全产业链自主创新**和**工业化生产模式**,在确保疗效的同时实现了成本的大幅下降。
随着更多临床数据的公布和支付渠道的拓宽,曾经被视为“奢侈品”的细胞免疫治疗,正在加速走向普罗大众。这不仅意味着中国生物医药创新实力的体现,更将为更多血液肿瘤患者带来重获新生的、可触及的希望。
2021年,中国首款CAR-T药物阿基仑赛注射液以120万元/针的定价震惊市场,让这款能使晚期淋巴瘤患者“绝境重生”的疗法成为少数人的“奢侈品”。短短四年后,华道生物宣布其在研CAR-T药物定价仅20余万元,磐升生物通过自动化技术将单剂成本降至20万元以内。从“天价神药”到“触手可及”,CAR-T疗法的价格跃迁,不仅是一场医药产业的革命,更是中国生物医药自主创新能力崛起的缩影。
图片内容来源于上海松江官微
一、CAR-T:改写抗癌逻辑的“活药物”
CAR-T疗法(嵌合抗原受体T细胞免疫疗法)的革命性,在于它打破了传统抗癌药物“被动杀伤”的逻辑,将患者自身的免疫细胞改造为“精准制导的杀伤武器”。其核心原理是从患者外周血中提取T细胞,通过基因工程技术为其装上识别肿瘤抗原的“导航系统”(CAR),在体外扩增培养后回输体内,实现对癌细胞的特异性杀伤。
这种“活药物”的临床价值已被充分验证。针对复发或难治性大B细胞淋巴瘤,国际首款CAR-T药物Yescarta®的客观缓解率超过80%,而国研非病毒CAR-T药物BRL-201在临床试验中更是实现了100%的客观缓解率,85.7%的患者达到完全缓解,且12个月生存率达76.2%。在血液肿瘤领域,CAR-T已从“末线治疗”逐渐向“前线治疗”推进,甚至在胰腺癌、胃癌等实体瘤治疗中展现出突破潜力,一款CEA CAR-T疗法曾让化疗耐药的胰腺癌肝转移患者生存期延长近5倍。
二、天价之困:120万背后的成本密码
120万元的定价并非企业“漫天要价”,而是由CAR-T疗法的生产特性和产业格局决定的。2021年中国上市的首款CAR-T药物阿基仑赛注射液,其定价逻辑可拆解为三重成本壁垒。
来源:国家药品监督管理局
核心技术垄断是首要壁垒。长期以来,CAR-T生产的关键设备、耗材和病毒载体被欧美企业掌控。德国美天旎的CliniMACS Prodigy全自动细胞制备系统及配套耗材单套成本就达10-15万元,而制备过程必需的病毒载体成本最高可达3万美元。依赖进口供应链不仅推高成本,更导致产能受限——国内早期CAR-T企业年产能普遍不足300人份,难以通过规模化摊薄成本。
个体化生产模式加剧了成本压力。传统CAR-T疗法需为每位患者“量身定制”,从细胞采集、基因改造到扩增培养,全流程依赖人工操作,人力成本占比高达35%,且质控采用“事后抽检”模式,容错率低导致报废成本上升。这种“手工小灶”式的生产,使得单剂CAR-T综合成本维持在80-120万元区间。
研发投入的回收需求也不可忽视。一款CAR-T药物从实验室到上市,需经历十余年研发和数亿元投入,而早期狭窄的患者群体(2021-2025年全国治疗患者不足2000人)使得企业只能通过高定价快速回收成本。多重因素叠加,让CAR-T疗法陷入“疗效卓越却无人能用”的尴尬境地。
三、破局之路:自主创新打破价格枷锁
CAR-T价格从“百万级”降至“二十万级”,本质是中国生物医药产业从“跟跑”到“领跑”的自主创新成果。这场破局之战,始于核心技术突破,成于生产模式革新。
全产业链自主化是降本的核心:华道生物自主研发“蚂蚁工坊”智能制造设备,完全替代进口系统,同时攻克一次性耗材、细胞培养试剂等关键物料的国产化难题,将病毒载体等核心成本降低90%以上。磐升生物的双智能化平台则通过“全封闭隔离器+AI视觉识别”实现全流程无人干预,人力占比从35%压缩至8%,耗材利用率提升25%。截至2025年,中国已成为全球唯一实现CAR-T全产业链自主可控的国家。
生产模式革新带来规模效应:传统人工产线年产能不足300人份,而华道生物松江基地一期年产能达9000人份,磐升设备年产量可支持5000名患者治疗,是人工产能的8-10倍。规模化生产使单位固定成本摊薄40%以上,彻底改变了“小批量、高成本”的产业困境。
技术迭代进一步降低边际成本:邦耀生物的非病毒定点整合技术,不仅使CAR-T制备周期从传统的7-14天缩短至3天,更避免了病毒载体的高昂费用,为成本控制提供了新路径。这些技术突破共同构建起“自主化+规模化+迭代化”的降本体系,让20万元定价成为可能。
四、普惠之效:抗癌门槛降低后的民生之变
20万元的价格阈值,不仅是数字的变化,更意味着CAR-T疗法从“小众奢侈品”转变为“大众可及的治疗选择”,将引发医疗生态的连锁变革。
患者可及性实现质的飞跃:按20万元定价计算,结合医保报销(假设报销比例50%-70%),患者自付费用可降至6-10万元,进入普通家庭可承受范围。以上海为例,若该价格纳入医保,预计每年受益患者将从不足500人增至5000人以上,血液肿瘤患者的5年生存率有望提升15-20个百分点。临床数据显示,CAR-T疗法可使复发难治性淋巴瘤患者的中位生存期从传统治疗的6个月延长至20个月以上,价格普惠将让更多患者获得“重生机会”。
产业生态迎来良性竞争:20万元的定价已倒逼现有企业加速降本,药明巨诺、复星凯瑞等企业纷纷宣布启动自动化产线升级,预计未来1-2年内,国内CAR-T产品价格将普遍降至30万元以下。同时,华道生物将自主技术平台开源共享,助力全行业降低创新门槛,形成“患者受益、企业发展、产业升级”的良性循环。
医疗资源配置更趋合理:此前,CAR-T治疗集中于少数顶尖医院,基层患者面临“异地就医难”问题。价格下降后,更多二级医院有望开展相关治疗,结合远程医疗指导,将形成“中心医院攻坚、基层医院普及”的诊疗网络,提升全国CAR-T治疗的均等化水平。
五、未竟之路:普惠之下的平衡之道
CAR-T疗法的普惠化并非终点,而是新的起点。在价格降低的同时,如何平衡疗效、安全与可持续性,仍是行业需要解决的课题。
疗效与安全的底线不容突破:自动化生产虽提升效率,但需建立更严格的全流程质控标准,避免“降本降质”。磐升生物将质控从“事后抽检”改为“在线100%监测”,使质量事件发生率降至0.2‰,仅为行业平均的1/20.为行业树立了标杆。未来需通过智能化质控系统、长期随访数据积累,确保普惠不“减效”。
医保支付的可持续性需要统筹:CAR-T疗法虽单价降至20万元,但患者基数扩大后,仍将对医保基金形成压力。可探索“医保+商业保险+企业援助”的多元支付模式,例如医保覆盖基础治疗费用,商业保险补充个性化需求,企业为特殊困难患者提供减免,既保障患者权益,又减轻医保压力。
技术创新的步伐不能停滞:当前CAR-T疗法仍面临实体瘤疗效不佳、副作用管理复杂等问题。普惠化带来的市场扩容,应反哺研发投入,推动CAR-T向实体瘤、自身免疫病等更广阔领域拓展,同时研发通用型CAR-T(无需依赖患者自体细胞),进一步降低成本、提升可及性。
从120万到20万,CAR-T疗法的价格跃迁,是中国生物医药产业自主创新的生动实践。它不仅改写了抗癌治疗的成本逻辑,更彰显了“让创新药惠及普通人”的产业初心。未来,随着技术的持续迭代和生态的不断完善,CAR-T疗法将真正实现“疗效卓越、价格亲民”,为更多患者带来生命的希望——这既是生物医药发展的终极目标,也是健康中国战略的生动注脚。
审核│糖晶
编辑│知风
愿生命如水螅一般永恒!
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!账号所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
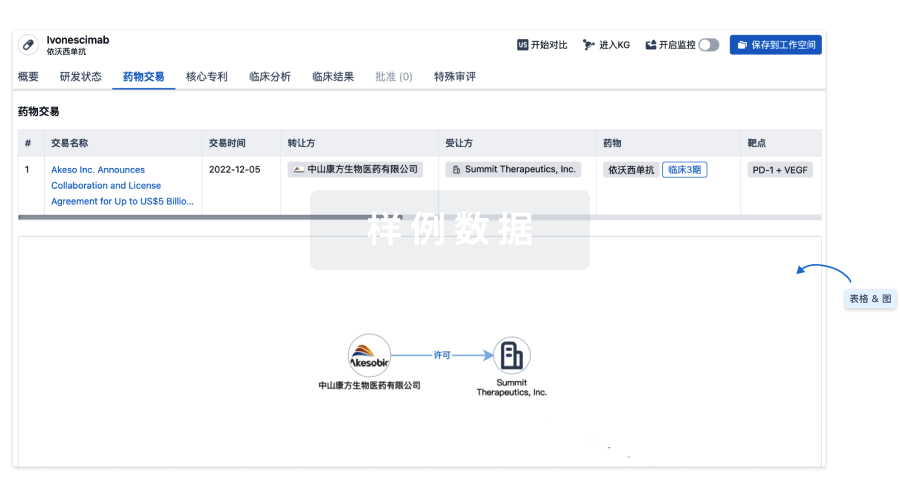
100 项与 靶向 CD19 非病毒 PD1 定点整合 CAR-T 细胞(上海邦耀) 相关的药物交易