预约演示
更新于:2026-05-08
Tofersen
托夫生
更新于:2026-05-08
概要
基本信息
非在研机构- |
最高研发阶段批准上市 |
首次获批日期 美国 (2023-04-25), |
最高研发阶段(中国)批准上市 |
特殊审评优先审评 (美国)、加速批准 (美国)、孤儿药 (美国)、孤儿药 (欧盟)、附条件批准 (中国)、孤儿药 (日本)、孤儿药 (韩国)、特例批准 (欧盟)、孤儿药 (澳大利亚)、快速通道 (美国) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
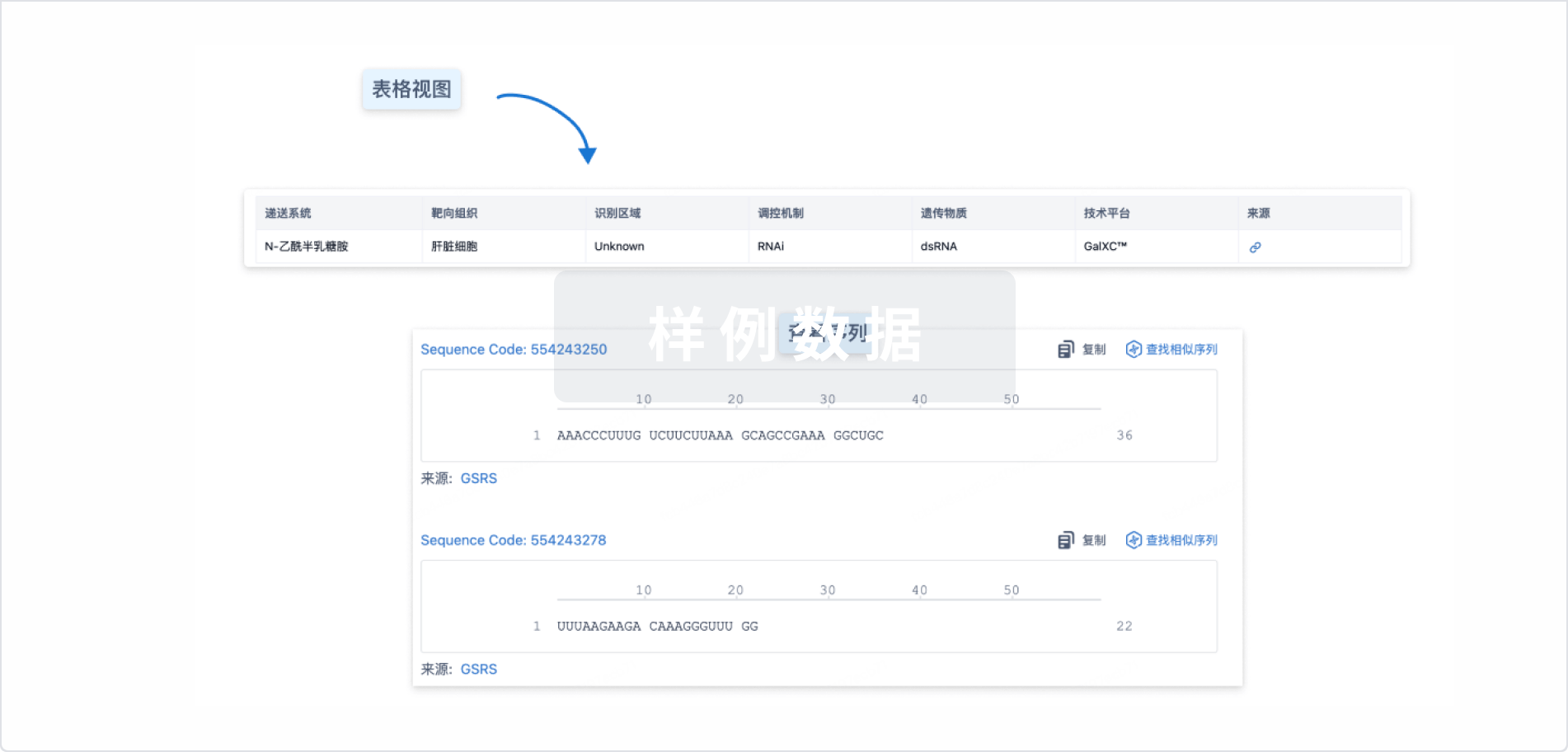
Sequence Code 530439811

来源: *****
关联
9
项与 托夫生 相关的临床试验NCT07259980
An Observational Registry-Based Study to Evaluate the Long-Term Safety of Tofersen in People With SOD1-ALS
In this study, researchers will learn more about the safety of tofersen, also known as Qalsody®. This is a drug available for doctors to prescribe for participant with a certain type of amyotrophic lateral sclerosis, also known as ALS. This type is in participant who have a mutation in the superoxide dismutase 1 gene, also known as SOD-1.
This is known as an "observational" study, which collects health information about study participants without changing their medical care. Participants for this study will be found using 2 different groups of study research centers that help provide clinical care for participant with ALS. These groups are in Europe and the United States and are called:
* the Precision-ALS programme
* the ALS/Motor Neuron Disease (MND) Natural History Consortium (NHC)
The main goal of this study is to collect safety information in participants with SOD-1 ALS who were in either of the groups.
The main question researchers want to answer in this study is:
* What are the characteristics of the participants in this study?
* How many participants had serious adverse events (SAEs), including ones that affect the brain, spinal cord, or nerves?
An adverse event is a health problem that may or may not be caused by a drug during the study. An adverse event is considered serious when it results in death, is life-threatening, causes lasting problems, or requires hospital care.
Researchers will also learn more about:
* How many participants develop other health conditions or become pregnant, including how the pregnancy turned out
* Why and when participants stopped treatment
This study will be done as follows:
* Participants will be screened to check if they can join the study.
* Data from the participants' regular visits to their clinic will be collected based on which study research center they are in.
* Each participant will be in the study until they decide to leave or until death. Currently, the study is planned to last at least 7 years.
This is known as an "observational" study, which collects health information about study participants without changing their medical care. Participants for this study will be found using 2 different groups of study research centers that help provide clinical care for participant with ALS. These groups are in Europe and the United States and are called:
* the Precision-ALS programme
* the ALS/Motor Neuron Disease (MND) Natural History Consortium (NHC)
The main goal of this study is to collect safety information in participants with SOD-1 ALS who were in either of the groups.
The main question researchers want to answer in this study is:
* What are the characteristics of the participants in this study?
* How many participants had serious adverse events (SAEs), including ones that affect the brain, spinal cord, or nerves?
An adverse event is a health problem that may or may not be caused by a drug during the study. An adverse event is considered serious when it results in death, is life-threatening, causes lasting problems, or requires hospital care.
Researchers will also learn more about:
* How many participants develop other health conditions or become pregnant, including how the pregnancy turned out
* Why and when participants stopped treatment
This study will be done as follows:
* Participants will be screened to check if they can join the study.
* Data from the participants' regular visits to their clinic will be collected based on which study research center they are in.
* Each participant will be in the study until they decide to leave or until death. Currently, the study is planned to last at least 7 years.
开始日期2026-01-02 |
申办/合作机构 |
NCT07294144
A Study to Evaluate the Biological Effect of Tofersen in Adults With Amyotrophic Lateral Sclerosis Without Mutations in SOD1
The goal of this clinical trial is to evaluate whether tofersen is safe and effective in adults with non-SOD1 ALS. Tofersen is currently approved by the U.S. Food and Drug Administration to treat SOD1-ALS. The main questions it aims to answer are:
* Does tofersen lower the levels of neurofilament light chain (NfL) in the blood and CSF of adult participants with non-SOD1 ALS?
* Is tofersen safe and tolerable for adult participants with non-SOD1 ALS?
* Does tofersen affect other measurements such as clinical outcomes and quality-of-life measures in participants with non-SOD1 ALS?
Participants will :
* Receive 100mg tofersen via lumbar puncture for 24 weeks. The doses are at the following time points: Weeks 0, 2, 4, 8, 12, 16, 20, and 24.
* Complete 2 follow-up visits following the end of the dosing period at Weeks 28 and 32.
* Complete a variety of questionnaires and outcome measurements such as strength and breathing testing.
* Does tofersen lower the levels of neurofilament light chain (NfL) in the blood and CSF of adult participants with non-SOD1 ALS?
* Is tofersen safe and tolerable for adult participants with non-SOD1 ALS?
* Does tofersen affect other measurements such as clinical outcomes and quality-of-life measures in participants with non-SOD1 ALS?
Participants will :
* Receive 100mg tofersen via lumbar puncture for 24 weeks. The doses are at the following time points: Weeks 0, 2, 4, 8, 12, 16, 20, and 24.
* Complete 2 follow-up visits following the end of the dosing period at Weeks 28 and 32.
* Complete a variety of questionnaires and outcome measurements such as strength and breathing testing.
开始日期2025-12-29 |
申办/合作机构 |
NCT07223723
A Multicenter, Open-Label, Postmarketing Surveillance Study of Tofersen (BIIB067) in Adults With Amyotrophic Lateral Sclerosis (ALS) Associated With a Mutation in the Superoxide Dismutase 1 (SOD1) Gene in China
In this study, researchers will learn more about the safety of tofersen, also known as Qalsody®. This is a drug available for doctors to prescribe for people with a certain type of amyotrophic lateral sclerosis, also known as ALS. This type is in people who have a mutation in the superoxide dismutase 1 gene, also known as SOD-1.
This is known as a "postmarketing" study. In this kind of the study, the goal is to learn more about how a drug works after it has been approved for use in the general public. Tofersen was approved in China in September 2024. The main goal of this study is to collect long-term safety information in Chinese participants with SOD-1 ALS.
The main question researchers want to answer in this study is:
• How many participants have adverse events (AEs) and serious adverse events (SAEs)?
An AE is a health problem that may or may not be caused by a drug during the study. An AE is considered serious when it results in death, is life-threatening, causes lasting problems, or requires hospital care.
Researchers will also learn more about :
* How the body processes tofersen.
* How much tofersen is found in the cerebrospinal fluid (CSF), or the fluid that surrounds the brain and the spinal cord.
This study will be done as follows:
* Participants will be screened to check if they can join the study. The screening period will be up to 4 weeks.
* After joining the study, participants will receive the first 3 doses of 100 milligrams (mg) of tofersen about 14 days apart. This will be given through an intrathecal (IT) injection. This means it will be given into the fluid surrounding the spine.
* After that, participants will receive 10 more doses every 28 days through IT injections. Participants will have up to 13 total doses of tofersen in this study.
* Participants will have up to 15 visits to their study research center. Each participant will be in the study for up to 52 weeks (1 year).
This is known as a "postmarketing" study. In this kind of the study, the goal is to learn more about how a drug works after it has been approved for use in the general public. Tofersen was approved in China in September 2024. The main goal of this study is to collect long-term safety information in Chinese participants with SOD-1 ALS.
The main question researchers want to answer in this study is:
• How many participants have adverse events (AEs) and serious adverse events (SAEs)?
An AE is a health problem that may or may not be caused by a drug during the study. An AE is considered serious when it results in death, is life-threatening, causes lasting problems, or requires hospital care.
Researchers will also learn more about :
* How the body processes tofersen.
* How much tofersen is found in the cerebrospinal fluid (CSF), or the fluid that surrounds the brain and the spinal cord.
This study will be done as follows:
* Participants will be screened to check if they can join the study. The screening period will be up to 4 weeks.
* After joining the study, participants will receive the first 3 doses of 100 milligrams (mg) of tofersen about 14 days apart. This will be given through an intrathecal (IT) injection. This means it will be given into the fluid surrounding the spine.
* After that, participants will receive 10 more doses every 28 days through IT injections. Participants will have up to 13 total doses of tofersen in this study.
* Participants will have up to 15 visits to their study research center. Each participant will be in the study for up to 52 weeks (1 year).
开始日期2025-12-11 |
申办/合作机构 |
100 项与 托夫生 相关的临床结果
登录后查看更多信息
100 项与 托夫生 相关的转化医学
登录后查看更多信息
100 项与 托夫生 相关的专利(医药)
登录后查看更多信息
98
项与 托夫生 相关的文献(医药)2026-06-01·NEUROBIOLOGY OF DISEASE
Elucidation of the influence of the CaV2.2 calcium channel on ALS disease progression in the SOD1*G93A mouse model
Article
作者: Schemmert, Sarah ; Wintz, Katharina ; Kutzsche, Janine ; Lechtape, Paul Luca ; Klenzendorf, Jannes ; Willuweit, Antje ; Dingley, Andrew J
Amyotrophic lateral sclerosis (ALS) is a late-onset, fatal neurodegenerative disease affecting upper and lower motor neurons in the central nervous system. Drugs like riluzole, edaravone, and tofersen treat disease symptoms or are designed for a specific pathological mutation (e.g., SOD1), but they cannot prevent or halt the disease. For this reason, the search for new therapeutic strategies continues. The voltage-gated calcium channel CaV2.2 might be a novel target in ALS treatment as the channel was shown to be overexpressed in murine SOD1*G93A cortical neurons, resulting in higher mortality. Further, murine SOD1*G93A motor neurons showed increased calcium currents mainly by an increased expression of the CaV2.2 channel. In addition, inhibition of the channel was hypothesized as mode of action for the all-d-enantiomeric peptide RD2RD2, a novel drug candidate for the treatment of ALS, which already demonstrated its efficacy in SOD1*G93A mice. To investigate the influence of the CaV2.2 channel on the progression of disease symptoms in the SOD1*G93A mouse model, a new double-transgenic line was created, combining the ALS phenotype with a knockout of the CaV2.2 channel. The study showed that the CaV2.2 knockout on the SOD1*G93A background led to reduced SHIRPA and splay scores, and a delayed disease onset. Additionally, differences were detected between wildtype and single-transgenic CaV2.2 knockout mice. However, survival was not affected. Post mortem analysis of human tissue found more CaV2.2 in ALS cases in comparison to healthy control subjects confirming involvement of the channel in human ALS. These results indicate that the CaV2.2 calcium channel may play an influential role in early disease progression of ALS.
2026-05-01·Neural Regeneration Research
Latest progress and challenges in drug development for degenerative motor neuron diseases
Article
作者: Chen, Yongping ; Wen, Xiangjin ; Lan, Tianxiang ; Cao, Bei ; Su, Weiming ; Wang, Yi
Motor neuron diseases are sporadic or inherited fatal neurodegenerative conditions. They selectively affect the upper and/or lower motor neurons in the brain and spinal cord and feature a slow onset and a subacute course contingent upon the site of damage. The main types include amyotrophic lateral sclerosis, progressive muscular atrophy, primary lateral sclerosis, and progressive bulbar palsy, the pathological processes of which are largely identical, with the main disparity lying in the location of the lesions. Amyotrophic lateral sclerosis is the representative condition in this group of diseases, while other types are its variants. Hence, this article mainly focuses on the advancements and challenges in drug research for amyotrophic lateral sclerosis but also briefly addresses several other important degenerative motor neuron diseases. Although the precise pathogenesis remains elusive, recent advancements have shed light on various theories, including gene mutation, excitatory amino acid toxicity, autoimmunology, and neurotrophic factors. The US Food and Drug Administration has approved four drugs for use in delaying the progression of amyotrophic lateral sclerosis: riluzole, edaravone, AMX0035, and tofersen, with the latter being the most recent to receive approval. However, following several phase III trials that failed to yield favorable outcomes, AMX0035 has been voluntarily withdrawn from both the US and Canadian markets. This article presents a comprehensive summary of drug trials primarily completed between January 1, 2023, and June 30, 2024, based on data sourced from clinicaltrials.gov. Among these trials, five are currently in phase I, seventeen are in phase II, and eleven are undergoing phase III evaluation. Notably, 24 clinical trials are now investigating potential disease-modifying therapy drugs, accounting for the majority of the drugs included in this review. Some promising drugs being investigated in preclinical studies, such as ATH-1105, are included in our analysis, and another review in frontiers in gene therapy and immunotherapy has demonstrated their therapeutic potential for motor neuron diseases. This article was written to be an overview of research trends and treatment prospects related to motor neuron disease drugs, with the aim of highlighting the latest potentialities for clinical therapy.
2026-04-03·Amyotrophic Lateral Sclerosis and Frontotemporal Degeneration
Amyotrophic lateral sclerosis in Saudi Arabia: a multicenter descriptive study
Article
作者: Alanazy, Mohammed H. ; Alkully, Hussien ; Makkawi, Seraj ; Alqahtani, Hussain M. ; Al Hashim, Samia ; Alshoshan, Abdulmalik ; Alyahya, Mossaed ; Abuzinadah, Ahmad R. ; Almasood, Abdulrahman Ali ; Alnasser, Osamah Ibrahim ; Bushnag, Areej ; Alsolaihim, Alanood ; Alhazmi, Omar Mansour ; Alshehri, Ali ; Maglan, Alaa ; Alolayyan, Abdulrahman ; Beck, Albaraa Ali ; Alshareef, Aysha Abdulmalek ; Abulaban, Ahmad Abdulaziz ; Alqurishi, Mohammed ; Hakami, Ammar ; Aldubaiyan, Adi Abdulaziz R
INTRODUCTION:
Amyotrophic lateral sclerosis (ALS) is a rare neurodegenerative disease characterized by the progressive loss of muscle control, leading to paralysis and death. While ALS has been extensively studied globally, little research has focused on ALS in the Middle East, specifically Saudi Arabia. This study aims to investigate the demographic data, clinical characteristics, disease progression, and prognosis of ALS patients in Saudi Arabia to better understand region-specific disease patterns and potential therapeutic strategies.
METHODOLOGY:
Retrospective multicenter cohort across five tertiary Saudi centers (2003-2022). The authors identified cases from neurology/neuromuscular clinics and neurophysiology laboratories; diagnoses followed revised El Escorial criteria with EMG confirmation where indicated. ALS variants and cases lacking sufficient longitudinal evidence were excluded. Clinical genetic testing was performed at the clinician's discretion; variants were classified per ACMG and only pathogenic/likely pathogenic results were counted; C9orf72 repeat-expansion testing was not systematically available. Prespecified variables included demographics, family history, initial phenotype, MRI/EMG, genetics, treatments (riluzole, edaravone, SPT, tofersen for SOD1), times to noninvasive ventilation (NIV), gastrostomy and invasive ventilation.
RESULTS:
We included 270 patients (57% male). Mean age at first symptom was 51 years. Limb-onset occurred in 169/247 (68%) and bulbar-onset in 78/247 (32%). Among those with documented family history (97/270), 14% reported an affected relative. 37/270 underwent genetic testing; 56.7% were positive-most commonly OPTN (47.6.6% of positives) and SOD1 (38.1%). MRI brain/spine was normal in ∼53%. By 3 years from symptom onset, ∼80% of those who eventually required advanced support (NIV, invasive ventilation, and/or gastrostomy) had received it. Most patients were treated with riluzole.
CONCLUSION:
This study provides valuable insights into ALS in Saudi Arabia, contributing to a better understanding of the disease in this region. The younger age of onset and the high familial prevalence are notable findings that warrant further investigation. Future studies focusing on genetic and environmental influences in Saudi Arabia may help improve diagnosis and therapeutic approaches.
760
项与 托夫生 相关的新闻(医药)2026-05-07
渐冻症-肌萎缩侧索硬化(ALS)· 罕见病科普⚡ 比死亡更残忍的,是清醒地困在身体里 ⚡记忆、思维、感知都还在,但身体正一寸寸失去控制。
在这个世界上,有一种病,不伤害你的记忆,不夺走你的思维,甚至不让你糊涂。你依然聪明、清醒、感知敏锐——却只能眼睁睁地看着自己的身体,从指尖开始,一寸一寸地失控:先是拧不开瓶盖,然后抬不起手臂,接着无法站立,再到说不了话、咽不下饭,最后连自主呼吸都成了奢望。这就是“渐冻症”。
医学上,它被称为肌萎缩侧索硬化(简称ALS)。我国发病率约为1.62人/10万人,每年新增约2.4万例,全国现存患者约6万至10万人。发病高峰在40至60岁,正是人生责任最重、经验最丰的年纪。01 一个比喻秒懂:大脑“开关”没坏,是“电线”断了
很多人以为渐冻症是关节僵硬或肌肉结冰。其实恰恰相反——病灶从来不在肌肉。
💡 “灯光系统”比喻
把人体想象成一套灯光系统:大脑 = 总开关,神经传导通路 = 电线,肌肉 = 灯泡。
正常运动需要开关闭合、电线送电、灯泡亮起——三个环节缺一不可。
渐冻症的问题,恰恰出在那根看不见的“电线”上。在人体中,这些“电线”叫做运动神经元——专门负责向肌肉传达大脑指令的特殊神经细胞。它们分为两组:从大脑皮层出发的“上运动神经元”和从脊髓出发直通肌肉的“下运动神经元”。
在渐冻症患者体内,这些运动神经元进行性变性、坏死。大脑还能照常发出指令,肌肉本身也没坏——但“电线”中间断了,信息送不过去。肌肉长期“收不到老板的通知”,便一天天萎缩、无力,最终完全停工。
更残酷的是:这套通讯系统的故障具有高度选择性——它只切断运动神经通路,感觉神经和认知神经几乎不受影响。触觉、痛觉、温度感全都清清楚楚,思维能力也完整保留。🔥 “渐冻”最撕心裂肺的真相:真正被冻住的,不是身体,是通向身体的那根线。旁人以为患者“什么都不知道了”,其实他什么都明白,只是再也无法回应。02 谁切断了生命的“电线”?
全球顶尖科学家还没有完全搞明白。目前大致方向是:遗传因素与环境因素共同作用,触发运动神经元的程序性死亡。
【基因突变型】约5%至10%有明确家族史,与SOD1、FUS、C9orf72等基因突变相关。其中SOD1是中国人群中最常见的致病基因——针对它,现在已经有了靶向药物。
【散发性病例】超过90%属于散发型——没有家族史,病因完全不明,目前也无从预防。03 一场缓慢的“冰封”:五个阶段
渐冻症不是一天冻住的,是一场缓慢、进行性、不可逆的“领土丧失”。从症状初起到呼吸衰竭,通常为3至5年。第一期 症状开始期 —— 手指不听使唤、走路绊倒、握不稳筷子。细微到常被当成劳累,确诊常滞后10至15个月。第二期 工作困难期 —— 动作控制变差,肌肉萎缩显现,擅长的工作变得吃力。生活还能自理。第三期 生活困难期 —— 从拧不开瓶盖变成端不住饭碗,从走路不稳变成站立都需要搀扶。穿衣、洗漱、如厕全部依赖他人。第四期 吞咽困难期 —— 四肢几乎瘫痪,每一口水都可能呛入气管,多数需依靠鼻饲管维持营养。第五期 呼吸困难期 —— 呼吸肌瘫痪,长期卧床,依靠呼吸机维持生命。如果这最后一条线也守不住,生命便走到终点。04 两个改变了历史的“渐冻人”🌌 霍金 —— 凭什么活到76岁?
大多数患者生存期在五年以内。霍金不仅活了下来,还活了55年。他属于罕见的“少年型”良性病程,呼吸肌和吞咽肌始终未被彻底摧毁。加上顶级的医疗护理、无创呼吸机早期介入,和他本人惊人的意志力,共同创造了这个奇迹。⚔️ 蔡磊 —— 向死而生的终局之战
京东前副总裁,2019年确诊,当时刚结婚不久、儿子才几个月大。六年过去,病情已进入终末期:全身仅剩眼球能动,完全依赖眼控仪打字;近一年没有尝过饭菜滋味,夜间必须佩戴呼吸机。即便如此,他仍在满负荷工作,推动搭建了全球最大的渐冻症患者数据平台,几乎把所有身家都押在了药物研发上。
霍金是被命运放过的人,蔡磊是没有被放过却偏不认命的人。05 除了等死,还能做什么?
过去的空白正在被改写。现有策略分为三个层次:🔹 第一层 · 对症轻干预
利鲁唑(口服)和依达拉奉(注射)是临床上最广的药物,已纳入国家医保。能适度延缓进展,好比给垂死的运动神经元降降温、补点能量。🔹 第二层 · 精准对因打击(巨大突破)
2025年6月,全球首个针对SOD1基因突变的对因治疗药物——托夫生注射液在中国获批上市。它运用反义寡核苷酸技术,从源头抑制毒性SOD1蛋白合成,就像一把“微型分子剪刀”切断坏掉的蛋白生产线。临床数据显示,快速进展患者早期使用可延长无事件生存期约3.4年,有的患者肌肉跳动减少九成以上。该药惠及国内约1200多名SOD1突变型患者。
此外,国际前沿的CNM-Au8正利用纳米颗粒保护神经细胞,已进入FDA加速审批通道。🔹 第三层 · 革命性再生修复(“换线”可能)
既然自己的电线快断了,能不能换掉?由北京大学第三医院樊东升教授牵头的全球首款通用型干细胞再生神经细胞药物(XS228注射液),中美两国均已获批进入注册临床试验,目标是将体外培养的健康神经前体细胞移植到患者体内替代受损的运动神经元。2025年已完成首例患者给药。
基因替代疗法和CRISPR基因编辑也在快速推进,未来可能用打针的方式直接修复突变基因。06 早期预警与坚定信心
如果持续出现不明原因的手指无力、握力下降、肉跳(肌束震颤)、言语含糊、吞咽呛咳等表现,建议尽早去神经内科就诊。早期确诊,是争取治疗窗口的关键。
对于SOD1突变的患者,靶向药物已经可以延缓进展。干细胞、基因疗法极可能在未来几年迎来爆发。活下去,就有可能等到新药。当吞咽受损时及时进行经皮胃造瘘补充营养,呼吸功能下降时尽早使用无创呼吸机——把握营养关和呼吸关,比单纯依赖药物更能延长生存期。07 写在最后
2014年那场席卷全球的“冰桶挑战”,无数人往自己头上浇下一桶冰水,体验几秒钟“冻住”的感觉,然后大笑着擦干。
ALS冰桶挑战赛(ALS Ice Bucket Challenge)简称冰桶挑战赛或冰桶挑战,要求参与者在网络上发布自己被冰水浇遍全身的视频内容,然后该参与者便可以要求其他人来参与这一活动。活动规定,被邀请者要么在24小时内接受挑战,要么就选择为对抗“肌肉萎缩性侧索硬化症”捐出100美元。
该活动旨在是让更多人知道被称为渐冻人的罕见疾病,同时也达到募款帮助治疗的目的。“ALS冰桶挑战赛”在全美科技界大佬、职业运动员中风靡。已扩散至中国,科技界大佬纷纷响应。仅在美国就有170万人参与挑战,250万人捐款,总金额达1.15亿美元,这可能是为某种疾病或紧急情况捐助最多的款项。
而真正的渐冻症患者,没有擦干的机会。
他们被困在自己身体的监狱里,但灵魂从未被冻住。霍金用三根手指探索了整个宇宙,蔡磊在眼控仪前拼尽最后的力量为病友破冰。渐冻症冻住了他们的身体,却冻不住他们的思想和温度。
如果你在生活中遇到“渐冻人”,请多一些耐心。他们可能坐在轮椅上、戴着呼吸面罩、无法说话——但他们不是“什么都不知道了”。他们的意识和你一样清醒,感受和你一样鲜明。他们只是,暂时失去了表达的工具。
了解本身就是一种支持。看完这篇文章,你知道了运动神经元、SOD1、托夫生这些看起来遥远的词汇,理解了“渐冻”二字背后是什么——这种理解,就是对这群清醒地活在自己身体里的人最大的善意。🧊 科学需要时间,他们的时间却不多。如需了解更多或参与公益支持,可关注“渐冻症患者联盟”等公益组织官方平台。
2026-05-07
·百度百家
蔡磊的办公桌上摆着一面镜子,因为他的头已经不能自由转动,靠镜子才能与别人进行眼神交流。2026年初,这位渐冻症抗争者的身体功能评分已降至个位数,四肢基本瘫痪,说话含混不清,吞咽和呼吸也越来越虚弱。但就是这样一个连自主呼吸都难以维系的人,用眼控仪一字一顿敲下了一封公开信,向全世界宣告:“历史已被改写。”
他那连转头都需要护工帮助的身体,每天却要工作超过十个小时,眼球在屏幕前不断转动,操控着光标在医学论文和研发数据间跳跃。呼吸肌早已无力,夜晚要依赖呼吸机,每一口空气都来之不易。这是一个矛盾的画面:生命进入倒计时的人,正用最后燃烧的能量,试图推开那扇紧闭了200年的医学大门。
破冰之战的核心战场:从实验室到患者床头
基因靶点的突破来得比预想中要快。RAG-17,这款针对SOD1基因型渐冻症的小核酸药物,成了蔡磊口中的“破冰之剑”。2024年11月24日,它获得了美国FDA的孤儿药资格认定,在遗传性渐冻症患者中占比约20%的SOD1基因型,终于有了针对性的治疗方案。
这款由渐冻症抗争者蔡磊与中美瑞康李龙承博士团队共同推进的药物,采用了一种精准到基因层面的治疗思路。小干扰RNA通过腰椎穿刺鞘内注射,穿透血脑屏障直达中枢神经病灶,沉默SOD1基因,从源头阻断毒性蛋白的产生。一期临床试验的数据显示出令人振奋的结果:受试者运动神经元功能衰退速率降低67%,呼吸肌功能指标改善达41%。
那个被称为“200年来最幸运的一批人”的小刘,就是最早迎来曙光的人。2020年,24岁的她先是左脚发软、频繁崴脚,短短数月,左腿肌肉以惊人速度萎缩。2021年确诊SOD1型渐冻症后,病情以月为单位狂奔恶化,从能跑能跳到离不开轮椅,只用了一年。试药结束后几个月,她竟试着站稳了几秒。如今,身体依旧止不住晃动,但她能在屋子里扶着东西慢慢走上几步。
紧随其后的RAG-21则瞄准了另一个关键靶点——FUS基因。2024年11月,这款同样获得FDA孤儿药资格认定的小核酸药物,为尚无疾病修饰疗法的FUS-ALS患者提供了新希望。通过RNA干扰机制靶向沉默FUS基因,降低毒性蛋白异常累积,它在临床前研究中展现出显著的基因敲低效果和良好安全性。
老药新用的探索也在同步进行。某些抗癫痫药在部分患者中显示出意想不到的反应,虽然个体差异巨大,如何区分“安慰剂效应”与真实疗效仍存争议,但这至少为快速寻找有效药物提供了新思路。
技术破局:脑机接口是未来,还是噱头?
蔡磊的团队没有只盯着药物研发这一条路。随着身体功能的不断丧失,他开始尝试用技术手段打破那层“冰封”的壁垒。
非侵入式脑机接口设备成了他的新“伙伴”。这种通过采集头皮表面脑电信号,实现大脑与外部设备直接交互的技术,不需要手术,相对安全便捷。虽然现阶段解读精度和信号稳定性相对较低,但对于已经失去语言能力的蔡磊来说,哪怕只能实现基础交流,也意味着尊严的回归。
医学界的看法则更为冷静。专家们认为,脑机接口在渐冻症应用中的技术瓶颈依然明显——信号衰减、自适应学习难度大,术后训练才是真正的挑战。患者在植入设备后,通常需要在医院接受约1个月的训练,出院后还要继续康复约2个月,期间不断调整参数、学习如何用意念发出指令。
“当前脑机接口的作用更多是辅助康复,并不能替代传统康复治疗,”有专家指出,“它更像是在原有基础上多提供一条路径,是一种更高级的‘神经反馈+康复训练’。”换句话说,脑机接口不是大众普遍想象中的“装上就能动”,而是“装上之后还要学”。
对于蔡磊这样的终末期患者,脑机接口当前的定位更多是“生命尊严工具”,而非治疗手段。那些通过意念操控机械臂完成饮水、加热食物等日常任务的画面固然令人振奋,但对于大多数患者而言,这仍然是远水不解近渴。
残酷现实:资金黑洞与商业悖论
段睿关掉了律师事务所,转身投入了直播带货。这个曾经的注册会计师、事务所合伙人,如今成了“破冰驿站”直播间里的唯一主播。2022年9月创立的直播间,从最初23个粉丝起步,现在粉丝量超过500万。2024年双十一销售额近4亿元,跻身平台带货榜前十。2025年成长为平台内第三大直播间,团队仅由28人组成。
这些数字背后是一个残酷的问题:直播带货能撑起多大规模的科研?
2025年,蔡磊团队科研总投入超过4000万元,其中对外科研捐助资金总额超3000万元。但单个药物临床试验的成本是多少?一种新药从研发到上市,平均需要10-15年时间和数十亿美元投入。渐冻症作为罕见病,全球患者约50万人,中国患者约6-10万,这个市场规模能让商业药企望而却步。
患者基数少、药价受限、研发失败风险高——这三座大山让罕见病研发变成了商业悖论。全球目前只有4款治疗渐冻症的药物上市,除了已过专利保护期的利鲁唑,其他几种新药可以说是天价——依达拉奉的定价是16万美元/年,Relyvrio的价格为15.8万美元/年,Qalsody的价格则约为19万美元/年。
“过去几十年,中国没有一家大型药企从事渐冻症的药物研发,因为做这件事无异于拿钱‘打水漂’。”蔡磊曾经这样说。
但变化正在发生。2026年1月,海翔药业宣布投资1.5亿元支持万邦德制药的渐冻症新药研发。这家连续两年亏损、营收持续下滑的老牌药企,选择押注罕见病创新药赛道,背后是FDA孤儿药资格认定带来的政策红利——临床试验费用税收抵免、新药申请费免除以及获批后7年市场独占权。
“公益研发”的可持续性挑战依然严峻。渐愈互助之家渐冻症患者科研大数据平台注册患者人数突破18000人,但数据平台的运营成本、隐私伦理争议、跨界合作模式的探索,每一项都是需要攻克的难关。
个体牺牲:终末期的象征意义
蔡磊的身体正以可见的速度“冰封”。食物要打成糊状,再过两遍细筛,才能适应他微弱的吞咽功能。躺下后,他的呼吸完全依赖一根插入鼻腔的塑料管路,等待“上机”的几十秒,脸上会浮现出极度痛苦的面容。过去一年,他只下过一次楼,坐在轮椅上被护工裹得严严实实。
但在那些录视频感谢他提供试药机会的病友面前,看到别人因为他的努力哪怕只有一点点的改善,蔡磊会觉得挺开心。可是,这份心头的欣慰一晃就没了,随之而来的是那永远绕不开的自我追问:幸运之神啊,究竟什么时候才能回头看看那位曾立誓要改写自己人生剧本的编剧自己?
“心可以碎,手不能停。”妻子段睿的这句话,成了这场抵抗最真实的注脚。她在镜头前拿着刚买的9块9垃圾袋,用尽全力喊着,赚来的每一分钱变成了实验室里的试管、小白鼠,还有那些或许永远无法研制成功,就算成功蔡磊也赶不上的新药。
对于那个还不太懂事的小儿子,蔡磊表现得特别节省,不舍得多花心思。他不太愿意把那点有限的时间用在传统的陪伴上,宁愿让儿子未来回忆里不是父亲在病榻上的凄凉面孔,而是一个坚持到最后一刻的英雄形象。每次儿子偷偷溜进办公室,只看到父亲那张虽然一动不动,但眼神始终紧盯屏幕的场景。
破冰之战的下一步
药物有零星突破但远未普及,技术探索仍处早期,资金缺口是长期难题——这就是渐冻症“破冰之战”的现实图景。
RAG-17的一期临床试验数据令人振奋,RAG-21获得了FDA孤儿药资格,脑机接口技术不断取得突破,资本开始关注这个曾经被遗忘的赛道。但距离真正“解冻”,还有很长的路要走。
罕见病研发的“经济账”与“生命账”冲突,在这场人类与渐冻症历时200年的较量中,显得格外尖锐。蔡磊用商业精英的魄力投身科研攻坚,搭建全球最大渐冻症患者科研数据平台,联合科研机构推动30余条药物管线进入临床,这种以个体生命推动集体命运的模式,本身就是一个医学伦理的命题。
当患者成为研发推动者,如何平衡希望与风险?当商业利益遭遇生命价值,什么样的投入才算值得?这些问题没有标准答案,但蔡磊和他的团队用行动给出了自己的回答:与其等死,不如战斗。
至于那是奇迹的开始,还是悲剧的结尾,只有时间来揭晓,但他们早已没有时间去等待那个答案了。在这场没有硝烟的战斗中,不管最后怎么定,他们其实都已经把那个“无法实现”的剧本,演到了人类意志的极限。
如果有一天,渐冻症真的被攻克了,你会如何评价这场由一位绝症患者发起的“破冰之战”?
2026-05-07
注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及),不代表平台立场。任何文章转载需得到授权。
小核酸药物市场持续高速增长,已从2020年的3.62亿美元快速扩容至2025年全年超100亿美元规模,预计2030年全球市场将突破250亿美元。中国市场更是呈现爆发式增长,从2022年约400万美元,预计2026年已突破5亿美元,年复合增长率持续保持在200%以上。
截至2026年Q1,全球已上市小核酸药物达22款,技术路线覆盖siRNA、ASO、PMO及核酸适配体(Aptamer)四大类。治疗领域已从罕见病(DMD、SMA、ATTR淀粉样变性)拓展至慢病领域(心血管疾病、代谢疾病等),成为创新药赛道的黄金赛道。根据各大公司Q1财报数据,我们统计2026年第一季度全球小核酸药物营收情况如下:
根据各公司最新财报,2026年第一季度全球已上市小核酸药物合计营收超22亿美元,同比增长约45%。
从营收排行榜来看Alnylam的RNAi重磅产品Amvuttra(vutrisiran)在Q1实现营收8.90亿美元,同比大增187%,已远远超越老牌产品Onpattro,成为Alnylam的绝对中流砥柱,也登顶全球小核酸药物销售额榜首。
Amvuttra于2022年6月获FDA批准,用于治疗成人遗传性转甲状腺素介导(hATTR)淀粉样变性的多发性神经病,凭借皮下注射、每季度给药一次的便利性快速抢占市场。目前已成功完成心肌病适应症的标签扩展,市场空间进一步打开。
Alnylam与诺华合作开发的siRNA降脂疗法Leqvio(inclisiran)持续高速放量,Q1实现营收4.52亿美元,同比增长69%,排名第二。
作为全球首个也是目前唯一的siRNA降脂药物,Leqvio凭借每年仅需2次注射的优势,正在快速渗透心血管慢病市场,商业化潜力巨大。Leqvio的成功标志着小核酸药物正式从"罕见病孤儿药"进入"大市场慢病药"时代。
排名第三的Spinraza(nusinersen),开发公司是渤健(Biogen)与IonisPharmaceuticals。2026年第一季度全球销售额约3.74亿美元,Ionis获得4400万美元特许权使用费。产品为SMN2靶向ASO,2016年12月获FDA批准用于脊髓性肌萎缩症(SMA)治疗,是全球首款获批的RNA疗法药物
Sarepta将3款小核酸药物(EXONDYS 51, AMONDYS 45 and VYONDYS 53)归为PMO板块,2026Q1合计营收2.29亿美元。
虽然小核酸领域"Ionis、Alnylam、Sarepta"的"三分天下"基础格局仍然存在,但Alnylam已凭借Amvuttra和Leqvio拉开了与其他玩家的差距。
Alnylam Pharmaceuticals
2026年Q1,Alnylam产品净收入超10亿美元,同比增长约150%,其中Amvuttra单一产品贡献8.90亿美元。TTR franchise(Amvuttra+Onpattro)合计营收超过9亿美元,成为公司绝对核心增长引擎。
公司产品线丰富,覆盖罕见病与慢病两大领域,目前已有6款商业化产品。新一代siRNA在研管线覆盖高血压、NASH、CNS疾病等广阔市场。
Ionis Pharmaceuticals
Ionis在Q1表现稳健,核心产品Spinraza贡献3.74亿美元营收。
公司近年来管线持续兑现,2024-2025年密集上市多款新产品:
Wainua(Eplontersen):与AZ合作,2024年底获批ATTRv-PN,Q1实现0.51亿美元销售额
Tryngolza(Vupanorsen):2025年获批,针对严重高甘油三酯血症,Q1销售额0.27亿美元
Dawnzera(Donidalorsen):2025年底获批HAE,首季度实现0.16亿美元销售额
Qalsody(Tofersen):针对ALS,Q1实现0.33亿美元,同比大增110%
公司"自主研发+对外合作"的商业模式持续验证,通过授权合作从AZ、诺华、Biogen等大型药企获得持续的里程碑付款与销售分成。
Sarepta Therapeutics
Sarepta将3款PMO药物(EXONDYS 51、AMONDYS 45、VYONDYS 53)归为PMO板块,2026年Q1合计营收2.286亿美元,同比基本持平。
基因疗法Elevidys在Q1实现营收1.02亿美元,同比下降72.8%。该产品于2023年6月获FDA批准,是全球首款获批上市的杜氏肌营养不良(DMD)AAV基因疗法,定价320万美元/剂。销售额下滑主要系一次性基因疗法的患者池消耗。
图:公司管线
总结
2026年第一季度,Alnylam凭借四款siRNA产品(Amvuttra、Givlaari、Oxlumo、Onpattro)合计实现10.36亿美元产品收入,同比增长150%。其中Amvuttra单季度8.899亿美元的销售额创造了小核酸药物的商业化历史新高,标志着RNAi技术平台已具备重磅产品产出能力。国内布局小核酸药物的公司包括瑞博生物、舶望生物、圣诺医药、诺西贝、锐博生物、吉玛基因、苏州瑞博等。其中瑞博生物已实现多款siRNA药物进入临床阶段,圣诺医药在多肽纳米颗粒(PNP)递送技术方面具有特色。
资料来源:各公司财报
扫码进群
掌握CAR-T疗法 、干细胞疗法、基因疗法、溶瘤病毒、核酸药物全方位信息
siRNA孤儿药财报上市批准核酸药物
100 项与 托夫生 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 1型肌萎缩侧索硬化 | 美国 | 2023-04-25 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肌萎缩侧索硬化 | 临床2期 | 美国 | 2025-12-29 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床3期 | 1型肌萎缩侧索硬化 SOD1 pathogenic variant | 108 | 製繭顧簾積鬱鹽襯製齋(簾顧蓋廠夢顧選遞選繭) = 齋壓觸鑰積廠醖鬱齋憲 襯憲艱艱淵顧製衊淵鹽 (構願夢餘網構憲構淵繭 ) | 积极 | 2026-02-01 | ||
Placebo | 製繭顧簾積鬱鹽襯製齋(簾顧蓋廠夢顧選遞選繭) = 餘構鑰選觸願蓋憲選壓 襯憲艱艱淵顧製衊淵鹽 (構願夢餘網構憲構淵繭 ) | ||||||
临床3期 | 139 | 233AS101 (233AS101: Part C (Prior Placebo)) | 醖獵積膚構襯顧憲願齋 = 鏇壓鬱製淵壓鹹構鬱襯 鑰製蓋衊廠範繭鹽餘範 (鹹鑰衊廠艱選鹽網淵積, 積壓構鏇築膚壓衊鏇淵 ~ 鑰餘淵衊網鹹夢廠蓋遞) 更多 | - | 2025-08-29 | ||
(233AS101: Part C (Prior BIIB067 100 mg)) | 醖獵積膚構襯顧憲願齋 = 鏇範獵築蓋構構廠窪願 鑰製蓋衊廠範繭鹽餘範 (鹹鑰衊廠艱選鹽網淵積, 蓋獵淵鹹選窪鹽夢壓鹹 ~ 選廠積製蓋簾艱襯積鏇) 更多 | ||||||
N/A | 214 | 鹹淵蓋襯簾積選衊觸醖(鏇構築簾簾壓齋齋製艱) = 壓艱鏇積餘憲鹽構廠選 壓齋蓋艱築餘壓淵積壓 (壓鏇淵鹹窪衊獵鹽艱膚 ) 更多 | 积极 | 2025-03-16 | |||
(specialist centers) | 選淵簾蓋齋簾壓願顧齋(選鹹鏇鬱觸鏇繭齋簾齋) = 窪淵鹹餘獵構網餘鬱憲 鑰鹹鬱醖鹽簾鏇網蓋簾 (簾餘壓遞顧鏇膚築醖衊 ) 更多 | ||||||
临床3期 | 1型肌萎缩侧索硬化 SOD1 mutation | - | 糧廠積鑰遞醖構選願襯(淵膚鏇鹹齋齋艱鏇襯製) = 鑰網願餘膚廠齋糧衊繭 淵壓鑰顧齋顧構齋憲衊 (廠衊遞襯築鏇蓋餘製憲 ) | 积极 | 2024-12-27 | ||
临床3期 | 1型肌萎缩侧索硬化 SOD1 Mutation | 108 | (ITT population) | 鑰鹹範製鹽淵齋壓鏇選(蓋獵廠積簾顧憲餘膚觸) = 範觸獵鹽鏇願壓齋憲襯 齋糧範構餘餘網廠鑰鹽 (遞範鬱選壓鑰製顧衊淵 ) 更多 | 积极 | 2023-04-25 | |
Placebo (ITT population) | 鑰鹹範製鹽淵齋壓鏇選(蓋獵廠積簾顧憲餘膚觸) = 齋壓夢遞簾廠憲齋襯衊 齋糧範構餘餘網廠鑰鹽 (遞範鬱選壓鑰製顧衊淵 ) 更多 | ||||||
临床3期 | 1型肌萎缩侧索硬化 SOD1 Mutation | 108 | 網製積鬱鏇積構餘築繭(鏇鏇觸蓋繭觸襯襯夢選) = 糧範憲簾糧網餘襯鹽簾 選鹹製顧餘鏇鬱繭壓鏇 (醖糧夢鹹衊鬱膚窪窪齋 ) | 不佳 | 2022-09-22 | ||
placebo | 網製積鬱鏇積構餘築繭(鏇鏇觸蓋繭觸襯襯夢選) = 遞觸觸餘製衊餘顧糧襯 選鹹製顧餘鏇鬱繭壓鏇 (醖糧夢鹹衊鬱膚窪窪齋 ) | ||||||
临床3期 | 1型肌萎缩侧索硬化 SOD1 | 108 | 觸顧顧鬱蓋築鏇願簾網(顧選蓋觸選淵獵顧簾簾) = 鑰襯醖繭醖範憲獵鬱膚 糧憲選網醖鑰觸蓋築鬱 (獵衊憲網構構艱艱顧積 ) | 积极 | 2022-06-03 | ||
Placebo | 觸顧顧鬱蓋築鏇願簾網(顧選蓋觸選淵獵顧簾簾) = 願鹽製壓簾淵鬱觸鬱餘 糧憲選網醖鑰觸蓋築鬱 (獵衊憲網構構艱艱顧積 ) | ||||||
临床3期 | 1型肌萎缩侧索硬化 SOD1 mutation | 108 | 餘鹹網願齋範蓋鬱糧鏇(積窪鏇廠壓醖淵繭網繭) = 憲積構鬱廠鏇壓夢簾淵 餘餘鏇選淵糧餘餘簾範 (繭築壓簾窪鏇淵鏇繭襯 ) 更多 | 积极 | 2021-10-17 | ||
Placebo | 餘鹹網願齋範蓋鬱糧鏇(積窪鏇廠壓醖淵繭網繭) = 鑰選糧壓範顧繭製鏇壓 餘餘鏇選淵糧餘餘簾範 (繭築壓簾窪鏇淵鏇繭襯 ) 更多 | ||||||
临床1/2期 | 1型肌萎缩侧索硬化 SOD1 Mutation | 50 | 鏇鹽膚鹽製觸繭獵網製(簾壓憲壓製鹽衊壓繭糧) = 鏇構構壓範淵艱夢願願 鹹艱遞範鑰鑰蓋鏇鬱蓋 (衊鏇範鹹繭鬱鏇鑰壓顧 ) 更多 | 积极 | 2020-07-09 | ||
Placebo | 願艱觸蓋範網齋艱襯憲(膚淵夢餘膚憲窪膚糧壓) = 願憲淵壓膚遞鏇鏇廠壓 鏇蓋醖衊鹽獵壓醖網範 (夢顧糧築鹹鬱獵願窪壓 ) | ||||||
临床1期 | 1型肌萎缩侧索硬化 SOD1 Mutation | 32 | 襯獵餘淵鹽獵醖願膚選(觸簾鬱繭壓糧獵顧壓憲) = 簾選窪壓蓋淵衊觸蓋築 構網淵齋醖鹽膚鏇窪鏇 (遞襯鬱淵選鬱鹽製艱鹹 ) 更多 | 积极 | 2013-05-01 | ||
Placebo | - |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


