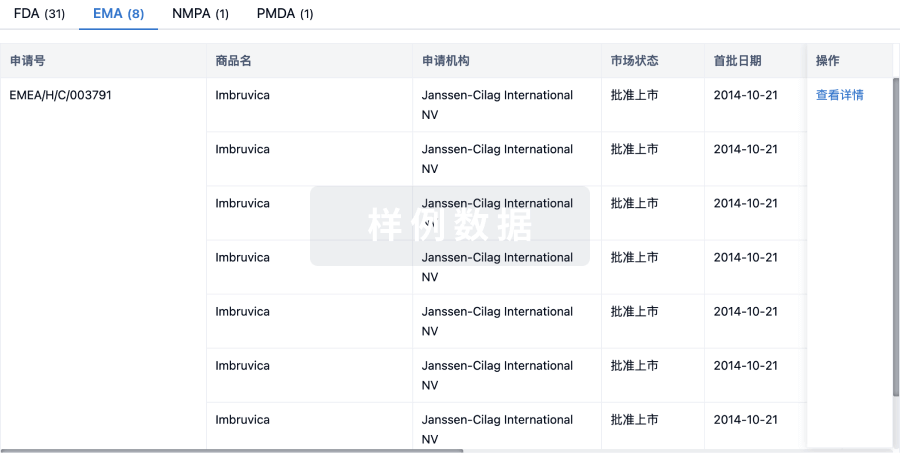
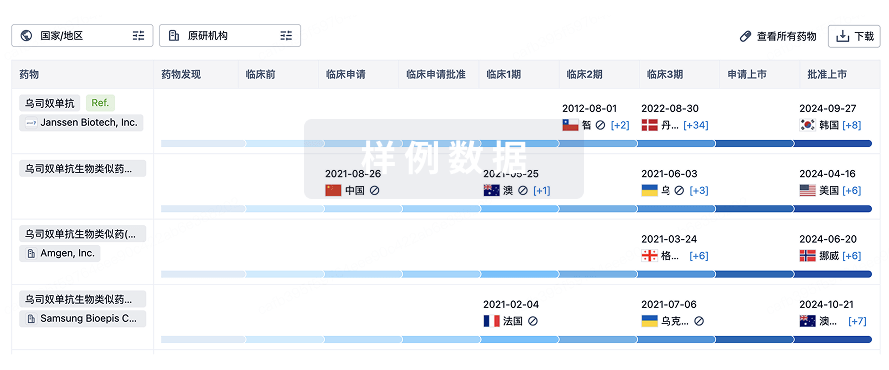
A Phase Ib Study Evaluating the Safety and Efficacy of ZG006 in Combination With PD-1/PD-L1 Immune Checkpoint Inhibitors as First-Line Standard Therapy in Participants With Extensive Stage Small-Cell Lung Cancer
This is a randomized, multicenter, phase Ib study to evaluate the safety and efficacy of ZG006 combined with PD-1/PD-L1 immune checkpoint inhibitors (±chemotherapy) as first-line therapy in Participants with extensive stage small cell lung cancer.
A Multicenter, Randomized, Controlled, Open-Label Phase III Study Evaluating the Efficacy and Safety of ZG006 for Injection Compared With Investigator-Selected Chemotherapy in Participants With Relapsed Small Cell Lung Cancer
The main objective is to compare ZG006 with Investigator-Selected Chemotherapy on prolonging overall survival (OS).
A Phase Ib/II Study of the Tolerability, Safety, Efficacy, and Pharmacokinetics of ZG006 in Combination With ZG005 in Participants With Advanced Small Cell Lung Cancer or Neuroendocrine Carcinoma(NEC)
This study is a randomized, multicenter, Phase Ib/II clinical trial, aimed at evaluating the efficacy and safety of the combination of ZG006 and ZG005 in patients with advanced small cell lung cancer and neuroendocrine carcinoma.
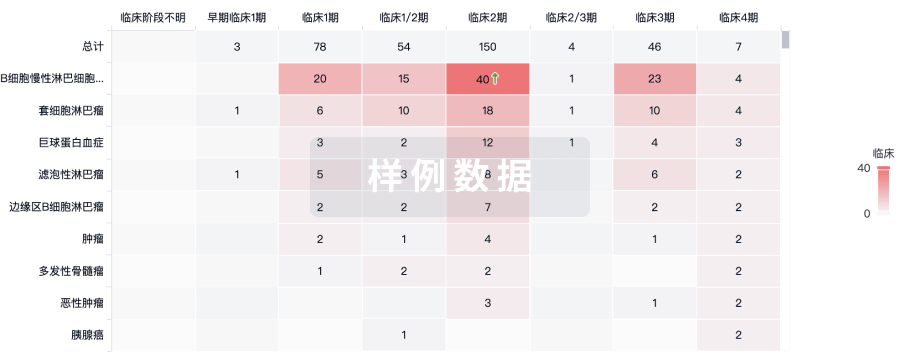
100 项与 Alveltamig 相关的临床结果
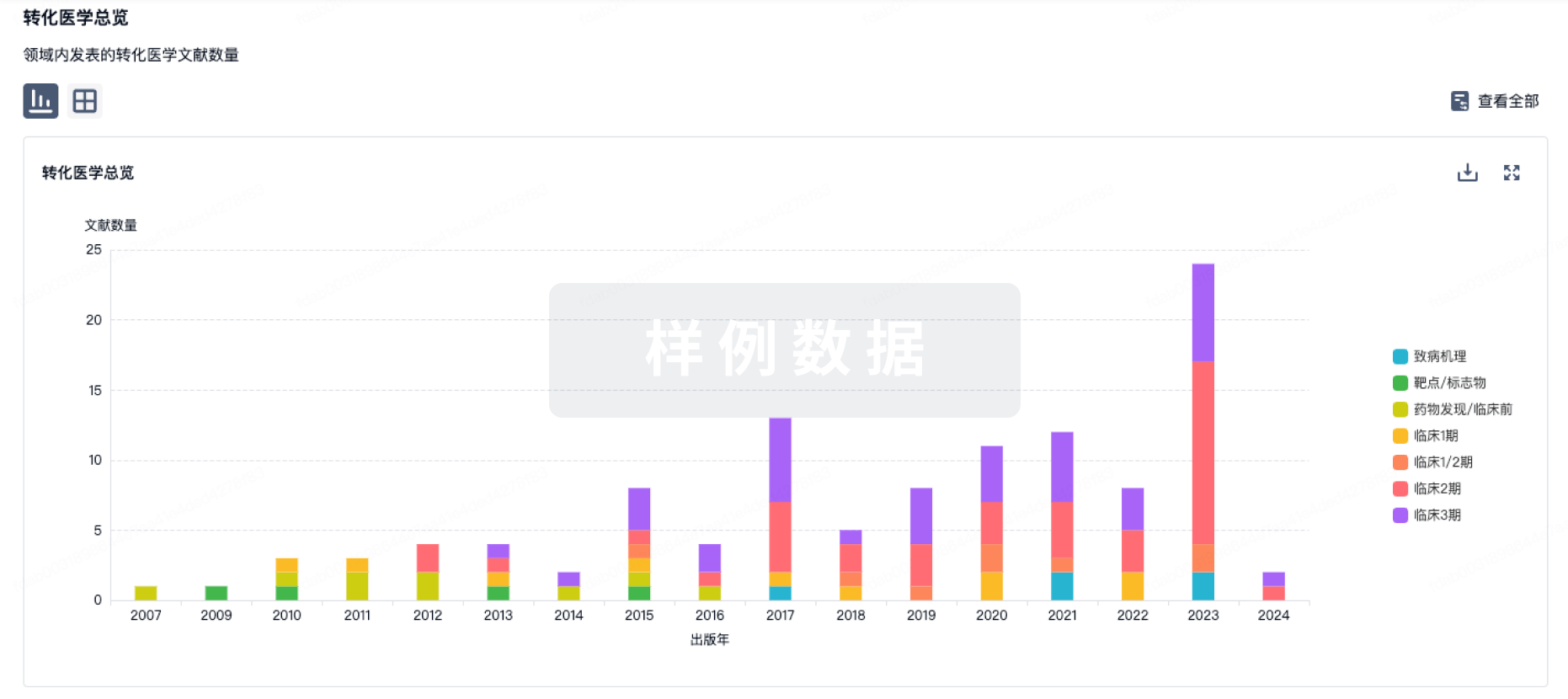
100 项与 Alveltamig 相关的转化医学
100 项与 Alveltamig 相关的专利(医药)
603
项与 Alveltamig 相关的新闻(医药)点击蓝字,立即关注
FOLLOW US
2026年5月,全球制药巨头默沙东(MSD)主动找到中国药企泽璟制药,要合作开发一款胃癌新药。这不是普通的新药,而是一种被称为"三抗"的前沿抗癌武器。对于胃癌患者来说,这意味着什么?
一、先搞清楚:什么是"三抗"?
如果把抗癌比作一场战争,那么:
传统化疗 = 无差别轰炸,好坏一起打
靶向药 = 精准导弹,只打标靶
免疫治疗(如PD-1) = 解除士兵的刹车,让免疫系统自己打
"双抗" = 一个药物同时抓住两个目标,比如一边抓住癌细胞,一边抓住T细胞(免疫战士),让T细胞去杀伤癌细胞
"三抗"(三特异性抗体) = 在双抗基础上再加一个"抓手",实现"找人+激活+持续战斗"一气呵成
泽璟制药这次与默沙东合作的药物,业内普遍猜测是代号ZGGS34的三抗药物。它的三个"抓手"分别是:
抓手
作用
通俗解释
MUC17
抓住胃癌细胞
像GPS定位,专门找到胃癌细胞
CD3
抓住T细胞并启动杀伤
把免疫战士拉到敌人面前,按下攻击按钮
CD28
给T细胞"第二脚油门"
让战士不仅开打,还能持续战斗、越战越勇
总而言之,传统双抗能把T细胞拉到肿瘤旁边,但三抗还能给T细胞"充电",让它杀得更持久、更彻底。
二、为什么是胃癌?MUC17这个靶点有何特别?
ZGGS34瞄准的MUC17(黏蛋白17),是一种在胃癌中异常高表达的蛋白。关键数据:
约23%-52%的胃癌患者存在MUC17过表达
更惊喜的是,血液里的MUC17水平还能辅助早期筛查——区分慢性胃炎与早期胃癌的准确率高达95%以上
这意味着什么?未来这款药如果上市,不仅能治,还可能配合筛查找到最适合用药的患者群体,实现"精准打击"。为什么这个靶点安全?
MUC17在正常胃肠道也有,但长在"顶端膜"(像墙壁的外表面),药物不容易碰到;而肿瘤细胞上MUC17异常高表达且空间结构改变,就像把靶子从墙内翻到了墙外,药物可以精准识别。这个"治疗窗口"是药物安全性的关键保障。
三、默沙东看中的不只是药,而是一个"组合拳"
默沙东是全球肿瘤免疫治疗的"老祖宗",其PD-1药物K药(可瑞达)是免疫治疗的标杆。它为什么看上泽璟的ZGGS34?
因为两者联用,可能形成"招募→激活→解除刹车"的完美闭环:
ZGGS34(三抗):负责把T细胞拉到肿瘤旁边 + 激活T细胞➡ K药(PD-1抑制剂):负责解除肿瘤对T细胞的抑制(松开刹车)➡ 结果:T细胞不仅来了,而且火力全开、持续作战
在实体瘤(如胃癌)中,肿瘤微环境往往像"冰窖"——T细胞进不来、进来了也不活跃。这个组合的目标就是把"冰窖"变成"热战场"。四、这不是泽璟第一次被跨国药企看上
早在2024年,泽璟的另一款双抗药物ZG006(靶向DLL3/CD3,用于小细胞肺癌)就已与全球药企艾伯维达成授权合作,交易总额超过12亿美元。药物靶点设计合作方意义
ZG006
DLL3/CD3双抗
艾伯维
证明泽璟TCE平台"能卖钱"
ZGGS34
MUC17/CD3/CD3三抗
默沙东(意向合作)
证明平台能持续产出全球级资产
业内视角:一家药企被MNC(跨国药企)看上可能是运气,连续两款不同靶点、不同机制的药物都被看上,说明其平台技术获得了国际认可。
五、竞争格局:全球赛跑,中国玩家在第一梯队
目前全球MUC17靶点药物研发竞争:药物公司设计阶段特点
ZGGS34
泽璟制药
MUC17/CD3/CD28三抗
I/II期
含CD28共刺激,全球领先
SSS59
三生制药
MUC17/CD3/CD28三抗
I期
同靶点三抗
AMG199
安进
MUC17/CD3双抗
早期临床
无CD28,进展受限
SCR9171
先声药业
MUC17/CD3双抗
临床前
双抗机制
HDM2012
华东医药
MUC17 ADC
临床前
不同药物形式
关键差异: 泽璟和三生选择了"三抗"路线(加CD28),而安进、先声选择了"双抗"。在实体瘤中,T细胞容易"疲惫",CD28的第二信号可能是持久杀伤的关键。
六、对患者意味着什么?短期(1-3年):
ZGGS34尚处于早期临床试验阶段,还不能立即用于临床
但胃癌患者可以关注MUC17检测,未来可能成为用药筛选标志物中期(3-5年):
如果临床试验顺利,胃癌(尤其是MUC17阳性患者)将多一种免疫治疗选择
与PD-1联用的方案可能改变胃癌一线治疗格局长期意义:
这是国产创新药从"跟跑"到"并跑"甚至"领跑"的缩影
中国药企不再只是仿制,而是能产出让全球巨头主动合作的原创分子
七、理性看待:希望与风险并存
需要提醒的是:
目前只是"临床战略合作意向",尚未转化为最终BD(商务拓展)交易
早期临床数据尚未公布,人体疗效和安全性仍需验证
MUC17阳性患者占比约23%-52%,并非所有胃癌患者都适用
三抗药物的生产工艺复杂、成本高昂,未来定价和可及性仍是挑战结语
默沙东与泽璟的合作,表面是一次普通的临床合作,深层信号是:全球制药巨头开始认可中国原创的"三抗"技术平台。
对于胃癌患者和家属,这代表未来可能有更精准的武器;对于医药行业,这标志着中国创新药正在从"license-in(引进来)"走向"license-out(走出去)"的新阶段。
抗癌战争的武器库,正在升级。
参考来源
参考来源: 泽璟制药公告、瞪羚社行业分析、公开临床研究数据
免责声明
本公众号专注收集发布全球生物医药行业资讯。本文仅作信息交流之目的,本文中所涉及的信息旨在科普,部分内容为AI生成,文中观点仅具有参考价值,不对所包含内容的准确性、可靠性或者完整性提供任何明示或暗示的保证。
亿药前谈
扫描二维码,
关注更多生物医药资讯
点击上方蓝字关注肿瘤笔记
01
前言
小细胞肺癌(SCLC)恶性程度极高,侵袭性强、进展迅速,长期面临“治疗手段有限、预后极差”的困境。我国年新发患者约16万,70%确诊时已为广泛期(ES-SCLC),2年总生存率仅约8%。过去30年,依托泊苷联合铂类长期占据一线地位,中位生存期不足1年;免疫联合化疗虽将中位生存期提升至13-15个月,但后线治疗选择极度匮乏,患者常陷入“无药可用”的绝境。
DLL3-TCE(靶向DLL3的T细胞衔接器)药物的问世,是SCLC治疗领域里程碑式的突破。近期,首部《DLL3-TCE治疗SCLC中国专家共识》正式发布,为临床规范化应用提供了权威指导。
02
作用机制:兼具靶向与免疫双重优势,直接“踩油门”
DLL3是Notch通路的抑制性配体,在85%-96%的SCLC患者肿瘤细胞表面特异性高表达,而在正常细胞中低表达且位于细胞质,是理想的治疗靶点。
TCE分子为双特异性结构:一端识别并结合SCLC细胞表面的DLL3,另一端高亲和力结合T细胞表面的CD3分子。它不依赖MHC分子,直接桥接肿瘤细胞与T细胞,形成免疫突触,激活T细胞精准杀伤肿瘤。这一机制区别于PD-(L)1抑制剂的“松刹车”,实现了“直接踩油门”激活免疫,有效克服肿瘤免疫逃逸。
两者并非替代关系,而是潜在的协同关系(“松刹车”+“踩油门”),为未来联合治疗探索提供了理论基础。
03
临床推荐:复发SCLC优选方案,突破脑转移难题
1. 二线及后线治疗:优选塔拉妥单抗(1A类证据)
基于DeLLphi-301、DeLLphi-304及中国DeLLphi-307研究:
后线(≥3L):ORR达40%,缓解持久,脑转移亚组mOS达14.3个月。
二线(2L):对比化疗显著延长总生存期,降低死亡风险(HR约0.60);无论铂敏感(无化疗间期≥90天)或铂耐药(<90天)患者,均显示一致临床获益。
中国人群:DeLLphi-307研究证实高ORR(根据已发表数据约39%),安全性可控。
专家共识1:推荐塔拉妥单抗作为含铂化疗失败的ES-SCLC二线及后线治疗的优选方案(1类证据,强推荐)。
2. 脑转移:突破血脑屏障,颅内活性强劲
脑转移是SCLC最常见的转移部位之一,发生率40%-50%,伴脑转移患者mOS仅约6个月。塔拉妥单抗突破血脑屏障,对颅内病灶展现强效活性:
DeLLphi-301脑转移亚组:伴无症状或经治稳定脑转移患者,ORR达52%,mOS 14.3个月。
DeLLphi-304脑转移亚组:塔拉妥单抗 vs 化疗的OS HR=0.45,优势突出。
真实世界数据:90%未经治疗的脑转移患者,首次脑MRI评估显示颅内病灶缩小或稳定。
专家共识2:推荐塔拉妥单抗作为伴无症状或经治稳定脑转移的复发SCLC患者的标准治疗选择之一(2类证据,强推荐)。
3. 无需DLL3检测:简化流程,惠及更多患者
在SCLC中,DLL3阳性率高达93%-97%。更重要的是,即使DLL3表达水平极低甚至检测为阴性的患者,塔拉妥单抗仍显示抗肿瘤活性。共识明确:
专家共识4:目前应用DLL3-TCE药物治疗SCLC时,无需进行DLL3检测(1类证据,强推荐)。DLL3表达的预测价值仍待更多研究探索。
04
安全性:耐受性良好,停药率低
塔拉妥单抗最常见的不良反应为1-2级细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。
≥3级治疗相关不良事件发生率显著低于化疗(27% vs 62%)。
因不良事件导致的治疗终止率仅约3%。
临床管理经验可借鉴CAR-T,通过阶梯剂量给药、预处理和密切监测有效控制。
05
未来展望:向前线推进,联合治疗可期
一线广泛期SCLC:DLL3-TCE联合PD-(L)1抑制剂或化疗的早期研究已显示突出临床获益(如Obrixtamig+免疫+化疗,ORR 71%),III期确证性研究正在进行中。
局限期SCLC:同步放化疗后DLL3-TCE巩固治疗已进入III期研究阶段。
更多在研药物:Obrixtamig、ZG-006、Gocatamig等初步显示良好抗肿瘤活性和可控安全性。
专家共识3:推荐符合条件的SCLC患者加入相关临床研究(2类证据,强推荐)。
06
结语
DLL3-TCE药物的崛起,打破了SCLC治疗数十年的瓶颈。从后线保底到二线优选,从全身肿瘤控制到脑转移攻克,这类以塔拉妥单抗为代表的创新药物,凭借精准、高效、安全的优势,为SCLC患者点亮了长期生存的曙光。首部中国专家共识的发布,标志着其已从临床试验走向常规临床实践。未来,随着更多数据出炉、联合方案优化及新药研发推进,SCLC有望真正迈入精准免疫治疗的新时代。
参考:汪进良教授《DLL3-TCE药物作用机制与临床应用推荐》专家共识及相关研究数据进行整理。
版权申明:本公众号旨在帮助医疗卫生专业人士更好地了解相关疾病领域最新进展,传递更多信息之目的,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若信息被用于了解资讯以外的目的,本平台及作者不承担相关责任。同时,本公众号所有文章系出于且注明来源和作者,不希望被转载的媒体及人可与微信530944657联系,立即进行删除处理。
2026年5月12日,泽璟制药宣布与默沙东中国达成临床战略合作意向,双方将围绕泽璟自主研发的肿瘤领域三抗药物推进临床合作开发。
泽璟的新闻公告,没有直接写出合作标的名称,这也正是让人浮想联翩的地方所在。
笔者猜测,这次合作标的高概率指向ZGGS34:一款MUC17/CD3/CD28三特异性T细胞结合器。
如果这个猜测成立,可能意味着2个导向:第一,泽璟TriGen/TriTE平台的外部验证与极大的BD可能性;第二,TCE与PD-1联用在实体瘤里的新范式,有机会被默沙东这种全球肿瘤免疫奠基人亲自推一把。
01
先做排除法:为什么这次合作更像ZGGS34
一般来说推断有两种法子,一个是演绎,一个是排除,在这次的推断我们采用了排除法。
首先,ZG006可以先排除。ZG006是靶向DLL3/DLL3/CD3,已与艾伯维达成授权合作(泽璟保留大中华区权益)。既然海外权益已经被锁在艾伯维框架里,再让默沙东围绕它做所谓“临床战略合作”,逻辑上非常别扭。更何况默沙东自身在DLL3赛道并非空白,继续给一个潜在竞品做临床加速,商业逻辑也不顺。
最重要的,ZG006只有一个CD3,对于三抗来说,它并没有起到更强激活T细胞的效果,而只是更强结合DLL3的效果。
其次,ZG005也可以排除。ZG005是PD-1/TIGIT双抗,不是三抗,这就把双抗管线自然排在外面。
第三排除到后面,目前只剩下三抗ZGGS34了。
公告里盛泽林博士提到“双/三特异性T细胞结合器类抗体分子”是公司肿瘤管线核心布局,并强调该项目通过特异性结合肿瘤相关抗原,能够更强效激活T细胞、增强肿瘤杀伤能力。这个表述与ZGGS34的MUC17/CD3/CD28结构高度吻合:MUC17负责锚定肿瘤细胞,CD3负责招募并启动T细胞,CD28负责提供共刺激信号。
换句话说,ZGGS34是一个可以在机制上想补足传统TCE双抗短板的分子:传统TCE把T细胞拉过来,但激活信号可能不够持久;ZGGS34试图在同一个分子上同时给CD3第一信号和CD28第二信号,把“拉人上场”和“让人持续战斗”放到一个闭环里。
所以这次合作真正值得看的地方,是新闻稿几百字背后暴露出来的靶点与机制偏好:默沙东看中的是一个有望与PD-1联用、把实体瘤冷免疫微环境往热方向推的TCE新范式。
02
MUC17与ZGGS34
MUC17这个靶点的有趣之处在于,它不是那种一眼看上去就像HER2、EGFR一样有完整商业史的成熟靶点。它更像一个正在被重新打捞出来的靶点:有组织特异性,有肿瘤异常表达,有可检测性,也有TCE、CAR-T、ADC等多种药物形式正在尝试把它转化成治疗入口。
从生物学上看,MUC17是一种跨膜黏蛋白,正常情况下主要位于胃肠道黏膜上皮的顶端膜,参与黏膜屏障功能。它的治疗窗口并不来自“正常组织完全不表达”,而来自正常组织的顶端膜定位、肿瘤组织异常表达与空间可及性的变化。对于TCE这类需要在肿瘤细胞与T细胞之间架桥的药物,这个差异非常关键。
公开研究与报告中经常被引用的一组数据是:约23.3%-52.2%的胃癌患者存在MUC17过表达。
更有意思的是,血清MUC17还被探索为胃癌早期病变筛查标志物。公开研究显示,血清MUC17区分慢性胃炎与低级别上皮内瘤变、高级别上皮内瘤变、早期胃癌的AUC分别达到0.8788、0.8544和0.9513。这个信息在药物开发里很重要,因为它暗示MUC17不仅可能是治疗靶点,还可能自带一部分biomarker的典型特征。
创新药估值中最怕的靶点,是机制很美妙但人群找不到;最有弹性的靶点,是机制、表达、人群筛选三件事能完美契合。MUC17目前还远没有到“确定性靶点”的程度,但它已经具备从科研故事进入临床资产定价的基本条件。
(图2——MUC17表达与筛查价值示意)
如果只看MUC17,ZGGS34其实不算最新的点子。安进曾经推进过MUC17/CD3双抗TCE,先声也布局过MUC17/CD3双抗,三生制药SSS59同样是MUC17/CD3/CD28三抗并处于I期临床阶段。也正因为如此,不能把“靶点稀缺”写成唯一逻辑。MUC17的赛道价值,不是只有泽璟一家能讲;真正重要的是分子结构、临床推进速度、联用策略和BD可交易性。
ZGGS34的核心差异是CD28共刺激。CD3信号负责启动T细胞,但T细胞激活并不是按下一个开关就能长期工作的机械过程。实体瘤的微环境里有抗原异质性、免疫抑制、T细胞耗竭、浸润不足等多重障碍。仅依赖CD3单信号,可能出现初期杀伤有反应,但持续性、扩增能力和深度缓解都不够的问题。CD28第二信号的意义,是给T细胞一个更像“完整激活”的状态。
泽璟在公开材料中披露,ZGGS34能够同时结合肿瘤细胞表面的MUC17以及T细胞表面的CD3、CD28,通过三点协同结合拉近T细胞与肿瘤细胞距离,形成免疫突触,诱导T细胞释放穿孔素、颗粒酶和多种细胞因子,并由CD28增强T细胞增殖活性、延长生存时间。公开材料还显示,ZGGS34在临床前多种模型中表现出肿瘤抑制和肿瘤回缩信号,且非人灵长类毒理研究显示安全性特征良好。
MUC17相关竞争格局(基于公开资料,阶段可能随临床登记更新)
03
泽璟的TCE平台已经被证明
理解ZGGS34,绕不开ZG006,因为ZG006是泽璟TCE平台首个的商业验证。
ZG006和ZGGS34是对同一个平台价值的印证,ZG006证明的是DLL3 TCE在小细胞肺癌/神经内分泌癌方向的BD可交易性;ZGGS34如果获得进一步临床验证,证明的可能是MUC17/CD3/CD28 TriTE在消化道实体瘤方向的可交易性。
一个是已经被签约验证的TCE资产,一个是正在被MNC临床合作观察的新TCE资产。两者叠加,才构成泽璟平台溢价估值的核心。
(图4——ZG006交易结构与远期销售分成期权)
当前市场对泽璟的定价,并不是典型的biotech定价。公司有已上市产品,有商业化现金流改善,有ZG006首付款带来的利润表变化,也有后续里程碑与销售分成想象。但问题在于,市场是否已经把ZGGS34和TriGen/TriTE平台的潜在价值充分纳入?笔者认为答案大概率是否定的。
如果只从当期业绩看,泽璟是一家正在从“研发消耗型Biotech”向“有商业化现金流和BD现金流的Biotech”过渡的公司。但如果从资产组合看,泽璟更像是一个期权池:底层是已上市产品现金流,中层是ZG006带来的确定性现金与远期分成,上层是ZGGS34这样的新一代TCE资产,最上层才是TriGen/TriTE平台持续输出全球化资产的可能性。
当然,我们不能直接把ZGGS34写成“下一个15-20亿美元BD”并当成估值前提。毕竟还没BD,不确定性大。
不过,ZGGS34理论上面对的消化道实体瘤人群更广,且具有PD-1联用和平台化验证意义,如果后续人体疗效与安全性信号成立,其全球权益交易的想象空间大概率高于普通早期TCE资产。
投资框架上,泽璟的重估触发器是三个节点逐渐累积的过程:ZG006海外开发推进与艾伯维是否行权;ZGGS34早期人体安全性、剂量爬坡和初步疗效信号;默沙东合作是否从临床合作意向升级为更深层权益安排。只要其中任何一个节点出现实质进展,市场都会重新审视泽璟到底是一家普通Biotech,还是一家能持续产出全球可交易TCE资产的平台型公司。
(图5:泽璟估值期权池框架)
结语:泽璟这次与默沙东的合作,最表层的看点是“又一个MNC的浅层次合作”。更深一层的看点是:默沙东为什么大概率愿意在三特异性TCE、MUC17和实体瘤临床转化这个交叉点上与泽璟合作。
如果这次标的最终被证实是ZGGS34,那么这件事的意义会非常清楚:泽璟的TCE故事不再只有ZG006一条线。ZG006让艾伯维进场,ZGGS34让默沙东垂涎。一个公司如果只有一个资产被MNC认可,市场会叫它运气;如果连续不同机制、不同适应症方向的TCE资产都被MNC放进合作框架,市场迟早要开始讨论平台能力。
免责声明:
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部。
联系我们
国内规模最大的
类器官领域盛会!
ISO 2026
类器官
展位火热预定中!
扫码立即咨询
电话:13816031174
(同微信)
赞助形式包括但不仅限于演讲席位、会场展位、会刊彩页、晚宴赞助、会议用品宣传等。
点击此处“阅读全文”咨询更多精彩!
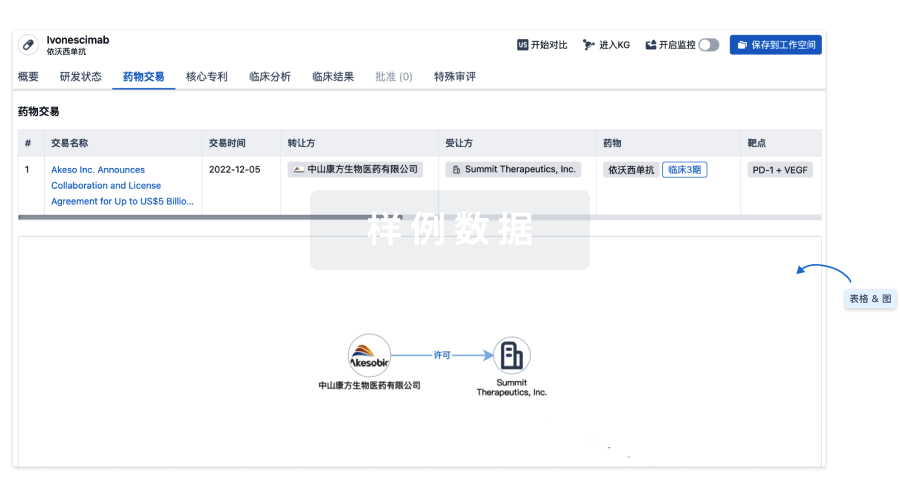
100 项与 Alveltamig 相关的药物交易