预约演示
更新于:2026-06-05
Nipocalimab-aahu
尼卡利单抗
更新于:2026-06-05
概要
基本信息
药物类型 单克隆抗体 |
别名 anti-FcRn monoclonal antibody(Momenta Pharmaceuticals)、Immunoglobulin g1, anti-(human neonatal fc receptor) (human monoclonal m281 .gamma.-1 chain), disulfide with human monoclonal m281 .lambda.-chain, dimer、Nipocalimab (USAN) + [8] |
靶点 |
作用方式 拮抗剂、调节剂 |
作用机制 FcRn拮抗剂(IgG受体FcRn大亚基p51拮抗剂)、免疫调节剂 |
在研适应症 |
最高研发阶段批准上市 |
首次获批日期 美国 (2025-04-29), |
最高研发阶段(中国)批准上市 |
特殊审评优先审评 (美国)、突破性疗法 (美国)、孤儿药 (美国)、罕见儿科疾病 (美国)、孤儿药 (欧盟)、优先审评 (中国)、突破性疗法 (中国)、孤儿药 (日本)、快速通道 (美国) |
登录后查看时间轴
结构/序列
Sequence Code 19395495L

来源: *****
Sequence Code 19395504H

来源: *****
关联
30
项与 尼卡利单抗 相关的临床试验ISRCTN15146958
A Phase III, randomised, double-blind, placebo-controlled, multicentre study of nipocalimab in adults with moderate to severe systemic lupus erythematosus
开始日期2026-03-06 |
NCT07438496
A Phase 3, Randomized, Double-blind, Placebo-controlled, Multicenter Study of Nipocalimab in Adults With Moderate to Severe Systemic Lupus Erythematosus
The purpose of this study is to evaluate how well nipocalimab works as compared to placebo in participants with moderate to severe Systemic lupus erythematosus (SLE, a long-term disease where the immune system mistakenly attacks its own healthy tissues, causing swelling and redness in various organs).
开始日期2026-03-05 |
NCT04883619
A Phase 2, Multicenter, Randomized, Double-Blind, Placebo-Controlled Study of Nipocalimab in Adult Participants With Active Lupus Nephritis
The purpose of this study is to evaluate the efficacy of nipocalimab versus placebo in participants with active Lupus Nephritis (LN).
开始日期2026-01-15 |
100 项与 尼卡利单抗 相关的临床结果
登录后查看更多信息
100 项与 尼卡利单抗 相关的转化医学
登录后查看更多信息
100 项与 尼卡利单抗 相关的专利(医药)
登录后查看更多信息
66
项与 尼卡利单抗 相关的文献(医药)2026-12-31·Human Vaccines & Immunotherapeutics
Effect of nipocalimab on IgG responses to vaccinations and viral infections in patients with IgG autoantibody-mediated diseases: Post hoc analyses of three randomized, placebo-controlled trials
Article
作者: Wang, Qingmin ; Noaiseh, Ghaith ; Fei, Kaiyin ; Taylor, Peter C. ; Ramchandren, Sindhu ; Nguyen, Brandon ; Vu, Tuan ; Antozzi, Carlo ; Edwards, Robert ; Winthrop, Kevin L. ; Gao, Sheng ; Hubbard, Jonathan J. ; Myshkin, Eugene ; Rojo Cella, Ricardo ; Yu, Faye ; Loza, Matthew J. ; Cossu, Marta ; Campbell, Kim ; Dimitrova, Dessislava ; Gottenberg, Jacques-Eric ; Cuff, Carolyn A. ; Bobadilla Mendez, Carolina
Nipocalimab is a neonatal Fc receptor (FcRn)-blocking monoclonal antibody approved for the treatment of generalized myasthenia gravis (gMG) and is being evaluated for other immunoglobulin G (IgG) autoantibody- or alloantibody-mediated diseases. Nipocalimab binds to FcRn with high specificity and affinity, eliciting increased clearance of IgG antibodies without affecting IgG production or other immune functions. However, nipocalimab's impact on vaccine responses in patients has not been previously reported. The effect of nipocalimab on pre-existing antibodies against tetanus toxoid (TT) and herpes zoster virus (HZV) vaccines as well as humoral responses to TT vaccines, severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) vaccines, and SARS-CoV-2 infections was examined in post hoc analyses of data from three randomized, placebo-controlled trials in participants with gMG, rheumatoid arthritis, and Sjögren's disease. The levels of pre-existing anti-TT and anti-HZV IgG followed the kinetics of total IgG during nipocalimab treatment (60%-65% and 53%-68% IgG reduction, respectively) and returned to baseline after discontinuation. Nevertheless, the majority of nipocalimab-treated participants maintained pre-existing anti-HZV (66/90, 73.3% above ≥100 IU/L reference threshold) and anti-TT IgG levels (62/81, 76.5% ≥0.16 IU/mL protective threshold) throughout the study period. Participants treated with nipocalimab elicited positive IgG responses to TT and SARS-CoV-2 vaccination, similar to placebo-treated participants. SARS-CoV-2 infections during the studies were mild to moderate in severity with no complications. These results suggest that nipocalimab does not impair the development of humoral responses to vaccines or viral infections in patients with IgG autoantibody-mediated diseases.Trial registration number: NCT04951622, NCT04991753, NCT04968912.
2026-05-01·ADVANCES IN THERAPY
Indirect Comparison of Nipocalimab Versus Efgartigimod and Rozanolixizumab in the Treatment of Generalized Myasthenia Gravis
Article
作者: Hashim, Mahmoud ; Ramchandren, Sindhu ; Singh, Sumeet ; Keng, Mi Jun ; Slowik, Rafal ; Gandhi, Kavita ; Hutton, Brian ; Khoury, Antoine C El ; Gilhus, Nils Erik ; Van Sanden, Suzy ; Jacob, Saiju ; Drudge, Christopher
INTRODUCTION:
Nipocalimab, efgartigimod, and rozanolixizumab (the last two cyclically dosed) are approved neonatal Fc receptor (FcRn) blockers for treating generalized myasthenia gravis (gMG). No trials have directly compared these therapies; hence, indirect treatment comparisons (ITCs) were conducted to evaluate their relative efficacy.
METHODS:
Matching-adjusted indirect comparisons (MAICs) and Bucher ITCs were used to compare nipocalimab vs. efgartigimod and rozanolixizumab for changes from baseline (CFB) in Myasthenia Gravis Activities of Daily Living (MG-ADL) total score observed in their phase 3 registration trials. Bucher ITCs used the relative treatment effect vs. placebo. As there was considerable cross-trial heterogeneity, including uncertainty in using the placebo arm as a common comparator, active treatment arms were used in unanchored MAICs. MG-ADL CFB was compared between trials (1) at multiple timepoints to evaluate onset of action and disease control over time, and (2) using area under the curve (AUC) as a measure of cumulative effect normalized per week of follow-up.
RESULTS:
In both Bucher ITCs and MAICs, nipocalimab had a comparable MG-ADL CFB at week 1 vs. the other FcRn blockers. In MAICs, MG-ADL CFB was significantly greater with nipocalimab vs. efgartigimod at week 8 sustained up to 24 weeks (p < 0.05), and vs. rozanolixizumab at week 10 sustained up to 14 weeks (p < 0.05); results numerically favored nipocalimab in corresponding Bucher ITCs. Using normalized AUC, MG-ADL CFB with nipocalimab was significantly greater in MAICs (p < 0.05) and numerically greater in Bucher ITCs vs. the other FcRn blockers.
CONCLUSIONS:
Sustained disease control is an important consideration in managing chronic diseases with fluctuating symptoms such as gMG. Study results showed that nipocalimab provided a comparable onset of action and consistent and sustained disease control that was numerically or statistically significantly greater (depending on ITC method) when compared with the symptom-based cyclic FcRn blockers efgartigimod and rozanolixizumab.
2026-01-27·NEJM evidence
Infant Immunity after Maternal Nipocalimab in Severe Hemolytic Disease of the Fetus and Newborn
Article
作者: Lopriore, Enrico ; Mirza, Arpana ; Nelson, Robert M. ; Kilby, Mark D. ; Miller, Russell S. ; Sachs, Ulrich J. ; de Winter, Derek P. ; Tjoa, May Lee ; Leu, Jocelyn H. ; Joanne Verweij, E.J.T. ; Moise, Kenneth J. ; Oepkes, Dick ; Devlieger, Roland ; Cafone, Joseph ; Smith, Valerie ; Bein, Gregor ; Saeed-Khawaja, Shumyla ; Streisand, James B. ; Komatsu, Yosuke ; Schwartz, Lisa B. ; Bredius, Robbert G. M. ; Lam, Edwin ; Smoleniec, John ; Ling, Leona E. ; Tiblad, Eleonor
BACKGROUND:
Antenatal treatment with nipocalimab, a neonatal Fc receptor (FcRn) blocker, delayed or prevented fetal anemia, as compared with a historical benchmark, in a phase 2 study of early-onset severe hemolytic disease of the fetus and newborn (HDFN). We report on the fetal and neonatal pharmacokinetics of nipocalimab and infant immunity through 96 weeks after birth.
METHODS:
The UNITY study was a single-group, open-label study assessing pregnant individuals at high risk of early-onset severe HDFN treated with weekly intravenous nipocalimab (30 or 45 mg/kg) from 14 to 35 weeks' gestation, unless discontinued for safety-related stopping criteria or intrauterine transfusion initiation. Pharmacokinetics were assessed in maternal, fetal, and infant blood and colostrum or breast milk; FcRn receptor occupancy and immunoglobulin G (IgG) were measured in neonatal and maternal blood; and infant IgG and safety were monitored through 96 weeks after birth.
RESULTS:
Safety analysis included 12 live-born infants from 13 pregnancies (one fetal loss occurred following intrauterine transfusion complications). Nipocalimab concentrations were maintained in maternal participants at pharmacologically active concentrations (greater than 10 μg/ml) during the weekly dosing intervals, but were observed at low concentrations (10 μg/ml or less) in one of four fetal cordocenteses (0.04 μg/ml), one of 11 cord blood samples (0.7 μg/ml), three of seven colostrum samples (less than 4 μg/ml), and two of nine breast milk samples (less than 2 μg/ml). Low infant IgG at birth (cord blood median, 175 mg/dl; range, 92-941) reached levels consistent with a physiologic nadir by 24 weeks after birth (median, 273 mg/dl; range, 153-429) and recovered to normal range (with one exception) between 16 and 96 weeks (median, 762 mg/dl; range, 407-925). Infectious adverse events were primarily mild to moderate and typical for early childhood. Protective titers to age-appropriate vaccinations (diphtheria and tetanus) were observed in six of seven infants at or before 96 weeks.
CONCLUSIONS:
In this cohort of 12 live-born infants, antenatal treatment with nipocalimab resulted in low levels of detectable drug in fetal, neonatal, and infant samples. Treatment was associated with low IgG levels at birth; however, unusual or unexpected childhood illnesses or impaired vaccine responses were not observed. (Funded by Johnson & Johnson; ClinicalTrials.gov number, NCT03842189.).
545
项与 尼卡利单抗 相关的新闻(医药)2026-06-03
·药明康德
治疗红斑狼疮,强生创新抗体2期临床结果积极
强生公司(Johnson & Johnson)今日宣布,在2期JASMINE研究中,nipocalimab达到主要终点:在24周时,根据系统性红斑狼疮应答指数4(SRI-4)评估,疾病活动度下降;并且截至第52周,根据SRI-4和狼疮低疾病活动状态(LLDAS)评估,在中度至重度系统性红斑狼疮(SLE)成人患者中,nipocalimab持续显示出疾病活动度降低。
Nipocalimab旨在选择性阻断新生儿Fc受体(FcRn),从而降低与SLE炎症相关的循环致病性免疫球蛋白G(IgG)自身抗体和免疫复合物水平。通过降低包括自身抗体在内的循环IgG水平,nipocalimab旨在靶向疾病的根本原因,同时保留关键免疫功能。新闻稿指出,JASMINE是首个证明FcRn阻断疗法在SLE中具有疗效的临床研究,支持继续评估nipocalimab作为该疾病潜在治疗选择的价值。
JASMINE临床试验数据显示,该研究在第24周达到主要终点:与安慰剂加背景用药组相比,接受nipocalimab加背景用药的患者中,达到SRI-4应答的比例更高(53.5%比46.7%)。
在第52周这一关键次要终点时,接受nipocalimab(15 mg/kg)治疗的患者中,53.6%达到SRI-4应答,而安慰剂加背景用药组为39.7%。第52周时,与安慰剂加背景用药组相比,接受nipocalimab治疗的患者中也有更多人达到LLDAS(37.5%比20.5%)。
最高可达19亿美元,礼来达成RNA编辑研发合作
Ascidian Therapeutics公司今日宣布,与礼来公司(Eli Lilly and Company)达成一项全球研发合作与许可协议,旨在发现和开发针对靶点未披露的单基因肾脏疾病的疗法,并可选择扩展至其他靶点。
Ascidian的RNA外显子编辑器能够在千碱基规模上编辑多个完整外显子,以修复导致疾病的遗传指令。这些疗法能够对基因进行精准的转录后编辑,从而在正确的细胞中、正确的时间,以正确的水平产生全长、功能性蛋白。
根据协议,礼来将获得Ascidian的RNA外显子编辑技术针对未披露肾脏疾病靶点的独家、靶点特异性权益。Ascidian将主导药物发现和部分临床前活动,礼来则负责其他临床前工作、临床开发、生产和商业化。Ascidian有资格获得最高达19亿美元的付款,包括预付款、开发和商业里程碑付款。Ascidian保留独立或与其他合作伙伴共同推进肾脏领域其他靶点的权益。
让老化细胞“焕发青春”,新锐完成4.35亿美元融资
NewLimit公司今日宣布,已完成4.35亿美元C轮融资。该公司计划于明年将其首款抗衰老重编程药物推进至人体临床试验。
NewLimit的药物旨在通过表观遗传重编程,恢复老化细胞的年轻功能。该公司表示,逆转细胞年龄不仅有潜力治疗衰老相关疾病,也有望帮助几乎所有人维持健康。该公司进展最快的肝脏重编程疗法能够帮助肝脏在损伤后更快修复,避免饮食造成的损伤,并加快饮酒后的恢复。
此外,该公司的研发管线中还包括对T细胞和内皮细胞进行重编程的药物,旨在治疗免疫相关疾病、慢性肾病和心血管相关疾病。
参考资料:
[1] Ascidian and Lilly Enter Global Research Collaboration to Develop RNA Exon Editors for Devastating Kidney Diseases. Retrieved June 3, 2026, from https://ascidian-tx.com/wp-content/uploads/2026/06/Ascidian-Lilly-Partnership_Final-PR_03-June-2026.pdf
[2] Johnson & Johnson late-breaking results show nipocalimab significantly reduced systemic lupus erythematosus (SLE) disease activity in a Phase 2 study. Retrieved June 3, 2026, from https://www.prnewswire.com/news-releases/johnson--johnson-late-breaking-results-show-nipocalimab-significantly-reduced-systemic-lupus-erythematosus-sle-disease-activity-in-a-phase-2-study-302789438.html
[3] NewLimit raises $435M led by Founders Fund to bring longevity medicines to human trials. Retrieved June 3, 2026, from https://blog.newlimit.com/p/newlimit-raises-435m-led-by-founders
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医药健康创新……
临床结果临床2期引进/卖出
2026-06-03
国内信息
1. 迈科康生物科创板IPO申请获受理,拟募资近30亿元
2026年6月3日,成都天府国际生物城核心企业迈科康生物的科创板IPO申请正式获得上交所受理。公司计划发行不低于1290万股,拟募集资金约29.29亿元,由中金公司担任独家保荐机构。作为海归核心团队创办的创新疫苗企业,迈科康十年聚焦新型佐剂赛道,累计融资超20亿元,已成功跻身行业独角兽梯队。其核心带状疱疹疫苗已递交上市申请,有望斩获国内首款拥有自主知识产权的新型佐剂疫苗资质,打破海外巨头长期垄断的行业格局。
2. 石药集团全球首款mRNA-LNP双靶点CAR-T获批临床
2026年6月2日,石药集团宣布其开发的首款基于mRNA-LNP技术的双靶点嵌合抗原受体T细胞注射液(SYS6063)已获得国家药品监督管理局批准,可在中国开展临床试验。该产品利用mRNA技术在体内直接诱导生成CAR-T细胞,无需体外细胞制备过程,大幅降低了生产成本和时间周期。作为全球首款进入临床的此类产品,它标志着中国在下一代细胞免疫治疗技术领域取得了突破性进展,为肿瘤治疗提供了更具潜力的“现货型”解决方案。
3. 传奇生物体内CAR-T药物LB2501一期临床数据亮眼,ORR达100%
近日,传奇生物发布了其体内CAR-T药物LB2501的1期临床初步数据,结果显示在第二剂量水平队列中,客观缓解率(ORR)达到100%(6/6),完全缓解率(CR)为83.3%(5/6)。这是继其他同类竞品后,又一个报告ORR 100%的体内CAR-T项目。随着多个临床项目的推进及数据的读出,体内CAR-T技术已经不仅局限于资本的狂热造势,而是真正落地并展现出卓越的疗效,有望彻底改变现有CAR-T疗法的生产模式和治疗可及性。
4. 智享生物赴港IPO,估值约59亿港元冲刺资本市场
2026年6月1日,头部CDMO企业智享生物(苏州)股份有限公司向港交所主板递交了上市申请,东兴证券为独家保荐人。作为一家专注于抗体及重组蛋白药物研发生产服务的CRO/CDMO企业,智享生物凭借其在复杂分子领域的工艺开发能力积累了大量客户资源。此次赴港上市旨在进一步扩大产能并提升研发实力,若成功上市将为其国际化战略提供强有力的资金支持,同时也反映了资本市场对优质CXO资产的持续关注。
5. 云顶新耀BTK抑制剂希布替尼达成超11亿美元海外授权
2026年6月2日,云顶新耀宣布其全资附属公司Everest Medicines与Travere Therapeutics订立独家许可与合作协议,将向后者授予一项独家、全球性(大中华地区及东亚与东南亚若干国家除外)的授权,以开发及商业化civorebrutinib(EVER001)。根据该协议,云顶新耀将收取1.125亿美元的前期付款,并有资格就最多5个适应症收取高达10.3亿美元的开发、监管及商业里程碑付款。此次交易不仅验证了该药物的临床价值,也为云顶新耀带来了可观的现金流,有助于其后续管线的研发推进。
6. 健达九州基因治疗新药GA002注射液获批临床
近日,国家药监局药品审评中心官网公示,北京脑科学与类脑研究所罗敏敏研究员团队通过健达九州转化的1类创新药GA002注射液正式获得临床试验默示许可。该产品拟用于治疗病灶明确、现有药物难以控制的局灶性难治性癫痫。作为全球首款基于化学遗传学的基因治疗药物,GA002顺利迈入注册临床阶段,标志着我国在神经系统精准基因治疗领域取得重大突破,为复杂神经精神疾病的治疗提供了全新的精准可控方案,具有极高的科研与临床转化价值。
7. 丽珠医药IL-17A/F双抗莱康奇塔单抗强直性脊柱炎NDA获受理
2026年6月3日,丽珠医药宣布其自主研发的1类创新生物药莱康奇塔单抗用于治疗强直性脊柱炎的上市申请正式获得国家药监局受理。这是该药物继银屑病适应症后斩获的第二项NDA受理,标志着这款中国首个自主研发的IL-17A/F双靶向药物在自身免疫疾病领域的管线布局再获关键进展。强直性脊柱炎是一种严重损害患者生活质量的慢性风湿免疫病,该药的推进有望填补国产自免治疗空白,为患者提供更多治疗选择。
8. 霍德生物iPSC衍生前脑神经前体细胞产品获FDA再生医学先进疗法认定
2026年6月3日,专注于iPSC衍生细胞神经疾病治疗的浙江霍德生物宣布,其自主研发的国际首款人前脑神经前体细胞注射液获得了美国FDA授予的再生医学先进疗法认定,用于治疗基底节缺血性卒中所致的长期运动功能障碍。FDA将在该产品后续开发中给予密切指导,包括立即召开综合性会议指导拟定商业化生产和临床开发。这一认定将加速该产品的全球化研发进程,确立了中国企业在iPSC细胞治疗领域的国际领先地位。
9. 首钢朗泽在港交所成功上市,开启全球化发展新征程
2026年6月3日,北京首钢朗泽科技股份有限公司(股票代码:02553.HK)在香港联合交易所主板成功挂牌上市。此次上市不仅是首钢朗泽深耕CCUS(碳捕集、利用与封存)领域十余载的里程碑式突破,更标志着公司以资本赋能、以科创为核心、布局全球市场的全新发展篇章正式启幕。虽然主业偏向工业生物技术,但其在合成生物学领域的积累对于生物医药原料制造具有重要参考意义,上市仪式吸引了多方股东及合作伙伴共同见证。
10. 南大教授创办!这家细胞治疗新锐完成Pre-A轮融资
近期,南京元迈细胞生物科技有限公司完成了Pre-A轮融资,本轮融资由泰州市天使投资基金与南京创熠鼎心创业投资合伙企业联合出资。据悉,公司注册地位于南京市江北新区,由南京大学的沈萍萍研究团队与资深药企高管共同创立,专注代谢免疫、自身免疫疾病治疗领域,以解决当前临床上尚未满足的需求。此次融资将主要用于推进核心管线的研发及团队建设,显示出高校科研成果转化在细胞治疗领域的活跃态势。
国际信息
1. NewLimit完成4.35亿美元C轮融资,估值达31亿美元
2026年6月2日,抗衰老新药研发公司NewLimit宣布完成C轮4.35亿美元融资,投后估值高达31亿美元。本轮融资由Founders Fund领投,新投资者Thrive Capital、Greenoaks和Quiet Capital,以及现有投资者Kleiner Perkins等跟投。NewLimit目前正致力于利用人工智能和重编程技术开发抗衰老疗法,其累计筹资总额已达7.1亿美元。此次巨额融资显示了顶级风投对长寿科技赛道的持续看好,也预示着抗衰老药物研发正从概念走向实质性的临床验证阶段。
2. 强生FcRn阻断剂nipocalimab II期临床JASMINE研究取得成功
2026年6月3日,强生宣布其评估nipocalimab在成年中重度系统性红斑狼疮(SLE)患者中的II期JASMINE研究达到了主要终点,即第24周疾病活动度降低,并在第52周展现出持续降低的效果。Nipocalimab是一款高亲和力FcRn阻断剂,能降低致病性IgG自身抗体水平。该研究是一项多中心、随机、双盲试验,共入组228例患者。此前该药已获FDA快速通道资格,此次II期成功为其在自免领域的商业化奠定了坚实基础,有望成为SLE治疗的重磅炸弹。
3. 阿斯利康EMERALD-3 III期临床研究结果积极,肝癌联合疗法显效
近日,阿斯利康宣布EMERALD-3 III期临床试验的积极结果显示,度伐利尤单抗联合曲美木单抗、仑伐替尼以及经动脉化疗栓塞术(TACE),相较TACE单独治疗,在适于栓塞的不可切除肝细胞癌(HCC)患者中,无进展生存期(PFS)显示出具有统计学显著性及临床意义的改善。该结果已在2026年美国临床肿瘤学会(ASCO)年会上以口头报告形式公布。这一“四药联合”方案的胜利,进一步巩固了阿斯利康在肝癌免疫治疗领域的领导地位,为难治性肝癌患者提供了新的希望。
4. Avenzo借壳Rallybio上市,所有管线引自中国
近日,Rallybio Corporation(NASDAQ:RLYB)公司宣布与Avenzo Therapeutics达成反向合并协议,合并后的公司将以Avenzo名义运营,并以新代码“AVZO”在纳斯达克市场继续交易。对于合并后的公司,Avenzo的股东将持有97.2%的股份。值得注意的是,Avenzo的所有管线均引自中国,且在反向合并的同时同步完成了2.15亿美元的私募融资,投资方包括Blackstone及OrbiMed。这一案例再次证明了中国创新药资产在国际资本市场上的吸引力,通过借壳上市实现了快速的资本化运作。
——▼——
——▼——
关于好思康
北京好思康科技有限公司致力于生物制药行业技术交流、咨询服务和线上一体化平台,旨在促进生物制药技术发展。公司主要业务有:
1.技术交流和推广
生物咖啡茶微信公众号和网站,是好思康打造的生物制药行业免费技术交流平台,其中包括每个工作日的早茶有料生物要闻、生物工艺技术和产品资料汇编等栏目,同时为生物工艺企业提供免费广告推送服务。
生物咖啡茶根据用户需要组织举办生物工艺技术交流沙龙、论坛;不定期举办企业家读书沙龙等。
2.线上平台服务
好思康面向生物制药行业和生物工艺行业提供全新一体化平台服务,涉及抗体企业、疫苗企业、生物工艺上下游企业等;不同企业的主打产品均可在平台进行登记展示推广。
联
系
我
们
加入生物咖啡群、广告推广合作联系人:段先生
联系微信:18501151021
请注明:姓名+所在单位名称+职务
END
▼
交流生物工艺,关注生物咖啡茶
▼
2026-06-03
Nipocalimab – the first and only neonatal Fc receptor (FcRn) blocker to be studied in systemic lupus erythematosus – is designed to target and reduce pathogenic immunoglobulin G (IgG) autoantibodies associated with this disease while preserving immune function
Results demonstrated significant reduction of systemic lupus erythematosus disease activity which continued beyond the 24-week primary endpoint, and were sustained through Week 52 in the nipocalimab 15 mg/kg groupa
The ongoing Phase 3 study of nipocalimab is currently recruiting people living with systemic lupus erythematosus – a debilitating autoantibody-driven disease which can lead to systemic organ damage
LONDON, June 3, 2026 /PRNewswire/ -- Johnson & Johnson (NYSE: JNJ) today announced nipocalimab met the primary endpoint of decreasing disease activity at 24 weeks as measured by SLE Responder Index 4 (SRI-4)b and continued to demonstrate sustained reduction in disease activity in adults with moderate-to-severe systemic lupus erythematosus (SLE)a through 52 weeks in the Phase 2 JASMINE study as measured by both SRI-4b and Lupus Low Disease Activity State (LLDAS).c In addition, the study results showed greater response versus placebo plus background medicationd in participants who tested positive for lupus-associated autoantibodies, which represents the vast majority (~80%) of people living with SLE.e,1 These findings will be featured in a late-breaking presentation at the European Alliance of Associations for Rheumatology (EULAR) 2026 Congress in London and are among the 38 abstracts the Company is presenting across its Rheumatology portfolio.
Nipocalimab is designed to selectively block the neonatal Fc receptor (FcRn), reducing levels of circulating pathogenic immunoglobulin (IgG) autoantibodies and immune complexes associated with inflammation in SLE.2,3 By reducing circulating IgG, including autoantibodies, nipocalimab is designed to target the underlying cause of disease while preserving critical immune functions.4 JASMINE is the first clinical study to demonstrate efficacy of FcRn blockade in SLE and provides clinical, biomarker and pharmacodynamic evidence supporting the continued investigation of nipocalimab as a potential treatment option for this disease.5
A healthcare professional's perspective
"The consistent improvements observed across established disease activity measures and reductions in pathogenic immunoglobulin G autoantibodies are encouraging and support the continued investigation of nipocalimab as a targeted treatment approach for people living with systemic lupus erythematosus," said Richard Furie, M.D., Chief of the Division of Rheumatology at Northwell.f "These 52-week findings support the potential of nipocalimab to provide disease control over time for a broad population of autoantibody-positive adult patients living with moderate-to-severe systemic lupus erythematosus, a disease in which many patients experience ongoing disease activity and risk of irreversible organ damage."
JASMINE Phase 2 clinical findings
The Phase 2 JASMINE study is the first proof-of-concept for a FcRn-blocker in SLE and demonstrates the potential of nipocalimab to reduce disease activity, with greater responses observed in autoantibody-positive patients.1,5
The study met its primary endpoint at Week 24, with a greater proportion of patients receiving nipocalimab 15 mg/kg plus background medication achieving an SRI-4b response compared with placebo plus background medication (53.5% vs 46.7%).
In a predefined autoantibody-positive patient populatione, greater SRI-4 response rates were observed (58.2% vs. 36.1%) and greater achievement of LLDAS (38.9% vs. 18.0%) compared with placebo plus background medication at Week 52.
At Week 52, a key secondary endpoint, 53.6% of patients receiving nipocalimab 15 mg/kg achieved an SRI-4b response, compared with 39.7% for placebo plus background medication.
More patients receiving nipocalimab 15 mg/kg also achieved LLDASc, a key exploratory endpoint that enables a treat-to-targetg approach, compared with placebo plus background medication (37.5% vs. 20.5%) at Week 52.
Nipocalimab had a safety profile consistent with previous studies of nipocalimab and no new safety signals were identified. The most common adverse reactions in patients with SLE treated with nipocalimab (≥10%) were nasopharyngitis, headache, urinary tract infection and nausea.5
"The JASMINE results provide important new insights into the potential of nipocalimab for adults with moderate-to-severe systemic lupus erythematosus as we continue advancing this program," said Leonard L. Dragone, M.D., Ph.D., Disease Area Leader, Autoantibody and Rheumatology, Johnson & Johnson. "We are especially encouraged by the responses observed in autoantibody-positive study participants. These findings support the potential of nipocalimab as a targeted, immunoselective treatment designed to address underlying drivers of systemic lupus erythematosus."
Nipocalimab received Fast Track Designation in SLE by the U.S. Food and Drug Administration (FDA) earlier this year. The ongoing Phase 3 GARDENIA study is currently recruiting.
Editor's Notes:
a. Nipocalimab is not FDA-approved for SLE.
b. The SRI-4 is a composite measure used to assess treatment response in patients with SLE during clinical studies. It comprises criteria from three different internationally validated indices, SELENA-SLE Disease Activity Index (SELENA-SLEDAI), Physician Global Assessment (PGA) and the British Isles Lupus Assessment Group (BILAG) 2004.
c. LLDAS definition: (1) SLE Disease Activity Index (SLEDAI)-2K ≤4, with no activity in major organ systems (renal, central nervous system (CNS), cardiopulmonary, vasculitis, fever) and no hemolytic anemia or gastrointestinal activity; (2) no new lupus disease activity compared with the previous assessment; (3) a Safety of Estrogens in Lupus Erythematosus National Assessment (SELENA)-SLEDAI physician global assessment (scale 0-3) ≤1; (4) a current prednisolone (or equivalent) dose ≤7.5 mg daily; and (5) well-tolerated standard maintenance doses of immunosuppressive drugs and approved biological agents.
d. Protocol-permitted background medications include oral corticosteroids, antimalarials and no more than two of the following immunomodulatory drugs: azathioprine, mycophenolate mofetil, mycophenolic acid, oral methotrexate.
e. The autoantibody-positive population was defined as participants who met ≥1 of the following during screening: (1) positive anti-double-stranded DNA (anti-dsDNA), (2) positive anti-Smith, (3) positive antinuclear antibodies (ANA) and positive for anti-Ro, anti-RNP or had a history of anti-dsDNA.
f. Dr. Richard Furie has provided consulting, advisory and speaking services to Johnson & Johnson. He has not been paid for any media work.
g. Treat-to-target in SLE is a therapeutic strategy in which treatment is guided by regular assessment of disease activity and adjusted to achieve a predefined target – primarily remission, or low disease activity if remission is not attainable – to improve long-term outcomes and prevent organ damage.6
ABOUT JASMINE
JASMINE (NCT04882878) is a Phase 2, multicenter, randomized, double-blind, placebo-controlled, parallel-group, dose-ranging study to evaluate nipocalimab in 228 adult participants with active systemic lupus erythematosus (SLE). Adults aged 18-65 years with moderate-to-severe SLE, defined by established measures of disease activity, who were positive for antinuclear antibodies (ANA), anti-double-stranded DNA (anti-dsDNA), and/or anti-Smith antibodies, and had not responded to at least one standard-of-care treatment were enrolled. Participants were randomized 1:1:1 to receive intravenous nipocalimab at 5 or 15 mg/kg, or placebo every 2 weeks through Week 52, in addition to protocol-permitted background medications. The primary endpoint was the SLE Responder Index-4 (SRI-4) composite response at Week 24. Pharmacodynamic effects and safety, including adverse events, were assessed through Week 58.5
ABOUT SYSTEMIC LUPUS ERYTHEMATOSUS
Systemic Lupus Erythematosus (SLE) is a chronic autoimmune disease that occurs when the body's immune system mistakenly attacks its own healthy tissues.7,8 This can lead to inflammation and damage in many parts of the body, including the skin, joints, heart, lungs, kidneys and brain.3 SLE affects nine times more women than men, often striking initially between the ages of 15-44.9 In addition to systemic organ damage, other complications of SLE can include end-stage renal failure, scarring cutaneous lesions, neurological damage and various forms of cardiovascular disease.3 People living with SLE often face reduced health-related quality of life, due to severe fatigue, mood disturbances, joint pain, swelling and rashes, including the hallmark butterfly-shaped facial rash, as well as complications of long-term glucocorticoid use.10 Severe fatigue is the most widely reported and debilitating symptom of SLE, affecting up to 80% of people with SLE.11 SLE is the most common form of lupus, affecting 3 to 5 million people worldwide, approximately 70% of lupus cases.12,13 It is estimated that 450,000 people in the United States are affected by SLE.14
ABOUT NIPOCALIMAB
Nipocalimab is an investigational immunoselective treatment designed to target, bind with high affinity, and block neonatal Fc receptor (FcRn), reducing circulating immunoglobulin G (IgG) antibodies that drive disease while also preserving key immune functions.2,3 Nipocalimab is being investigated across three key segments in the autoantibody space including Rheumatologic disease, Rare Autoantibody diseases and Maternal Fetal diseases mediated by maternal alloantibodies in which blockade of IgG binding to FcRn in the placenta is also believed to limit transplacental transfer of maternal alloantibodies to the fetus. 5,15,16,17,18,19,20,21,22,23
The U.S. Food and Drug Administration (FDA) and European Medicines Agency (EMA) have granted several key designations to nipocalimab including:
EU EMA Orphan medicinal product designation for hemolytic disease of the fetus and newborn (HDFN) in October 2019 and fetal and neonatal alloimmune thrombocytopenia (FNAIT) in April 2025
U.S. FDA Fast Track designation in HDFN and warm autoimmune hemolytic anemia (wAIHA) in July 2019, generalized myasthenia gravis (gMG) in December 2021, FNAIT in March 2024, Sjögren's disease (SjD) in March 2025 and systemic lupus erythematosus (SLE) in January 2026
U.S. FDA Orphan drug status for wAIHA in December 2019, HDFN in June 2020, gMG in February 2021, chronic inflammatory demyelinating polyneuropathy (CIDP) in October 2021 and FNAIT in December 2023
U.S. FDA Breakthrough Therapy designation for HDFN in February 2024 and for SjD in November 2024
U.S. FDA granted Priority Review in gMG in Q4 2024 and in wAIHA in Q2 2026
ABOUT JOHNSON & JOHNSON
At Johnson & Johnson, we believe health is everything. Our strength in healthcare innovation empowers us to build a world where complex diseases are prevented, treated and cured, where treatments are smarter and less invasive, and solutions are personal. Through our expertise in Innovative Medicine and MedTech, we are uniquely positioned to innovate across the full spectrum of healthcare solutions today to deliver the breakthroughs of tomorrow and profoundly impact health for humanity.
Learn more at or at .
Follow us at @JNJInnovMed.
Janssen Biotech, Inc. is a Johnson & Johnson company.
Cautions Concerning Forward-Looking Statements
This press release contains "forward-looking statements" as defined in the Private Securities Litigation Reform Act of 1995 regarding product development and the potential benefits and treatment impact of nipocalimab. The reader is cautioned not to rely on these forward-looking statements. These statements are based on current expectations of future events. If underlying assumptions prove inaccurate or known or unknown risks or uncertainties materialize, actual results could vary materially from the expectations and projections of Johnson & Johnson. Risks and uncertainties include, but are not limited to: challenges and uncertainties inherent in product research and development, including the uncertainty of clinical success and of obtaining regulatory approvals; uncertainty of commercial success; manufacturing difficulties and delays; competition, including technological advances, new products and patents attained by competitors; challenges to patents; product efficacy or safety concerns resulting in product recalls or regulatory action; changes in behavior and spending patterns of purchasers of health care products and services; changes to applicable laws and regulations, including global health care reforms; and trends toward health care cost containment. A further list and descriptions of these risks, uncertainties and other factors can be found in Johnson & Johnson's most recent Annual Report on Form 10-K, including in the sections captioned "Cautionary Note Regarding Forward-Looking Statements" and "Item 1A. Risk Factors," and in Johnson & Johnson's subsequent Quarterly Reports on Form 10-Q and other filings with the Securities and Exchange Commission. Copies of these filings are available online at , or on request from Johnson & Johnson. Johnson & Johnson does not undertake to update any forward-looking statement as a result of new information or future events or developments.
1 Richard A Furie, Ronald van Vollenhoven, Rafał Wojciechowski, Eric Morand, Guillermo J. Pons-Estel, George A Karpouzas, Bart van Hartingsveldt, Robert W Hoffman, Terence Rooney, Sheng Gao, Robert Gordon, Kim Hung Lo, Jocelyn H. Leu, Federico Zazzetti, Stanley J. Marciniak, Steven Leonardo, Keying Ma, Kathy Sivils, Leonard Dragone, Loqmane Seridi, Linda Okonkwo, Erika Noss, Fang Liu-Walsh, Michelle Petri. Nipocalimab in SLE: First-in-class efficacy and safety results demonstrating proof of concept for FcRn blockade from the Phase 2 JASMINE-SLE study. Presented at the 2026 European Alliance of Associations for Rheumatology (EULAR) Congress.
2 Ling LE., et al. M281, an anti–fcrn antibody: Pharmacodynamics, pharmacokinetics, and safety across the full range of IGG reduction in a first–in–human study. Clinical Pharmacology & Therapeutics., 2018;105;4:1031–1039. Available at: .
3 National Institute of Arthritis and Musculoskeletal and Skin Disease. (2022) Systemic Lupus Erythematosus (Lupus). . Last accessed: April 2026.
4 Cossu M et al. A randomized, open-label study on the effect of nipocalimab vaccine response in healthy participants. Presentation at American Association of Neuromuscular & Electrodiagnostic Medicine (AANEM) Annual Meeting. October 2024.
5 ClinicalTrials.gov Identifier: NCT04882878. Available at: . Last accessed: June 2026
6 Bracalenti M, Iaccarino L, Doria A. Remission and low disease activity in systemic lupus erythematosus. Rare Dis Orphan Drugs J. 2025;4:28.
7 Lupus Foundation of America. Understanding Lupus . Last accessed: June 2026.
8 Kawka L, et al. Fatigue in Systemic Lupus Erythematosus: An Update on Its Impact, Determinants and Therapeutic Management. J Clin Med. 2021 Sep 3;10(17):3996. doi: 10.3390/jcm10173996. PMID: 34501444; PMCID: PMC8432566.
9 Guéry JC. Why Is Systemic Lupus Erythematosus More Common in Women? Joint Bone Spine. 2019 May;86(3):297-299. doi: 10.1016/j.jbspin.2018.12.004. Epub 2018 Dec 22. PMID: 30584922.
10 Centers for Disease Control and Prevention. (2024). Symptoms of lupus. . Last accessed: June 2026.
11 Lupus Foundation of America. Understanding the Invisible Impact of Lupus. Available at: . Last accessed: June 2026.
12 Tian, J., Zhang, D., Yao, X., Huang, Y., & Lu, Q. (2023). Global epidemiology of systemic lupus erythematosus: A comprehensive systematic analysis and modelling study. Annals of the Rheumatic Diseases, 82(3), 351–356.
13 Lupus Foundation of America. Lupus facts and statistics. . Last accessed: June 2026.
14 Wang, Y., Hester, L. L., Lofland, J., Rose, S., Karyekar, C.S., Kern, D.M., Blacketer, M., Davis, K., & Sheilds-Tuttle, K. (2022). Update on the prevalence of diagnosed systemic lupus erythematosus (SLE) by major health insurance types in the US in 2016. BMC Research Notes, 15, 5.
15 ClinicalTrials.gov Identifier: NCT04951622. Available at: . Last accessed: June 2026.
16 ClinicalTrials.gov. NCT03842189. Available at: . Last accessed: June 2026.
17 ClinicalTrials.gov Identifier: NCT05327114. Available at: . Last accessed: June 2026.
18 ClinicalTrials.gov Identifier: NCT04119050. Available at: . Last accessed: June 2026.
19 ClinicalTrials.gov Identifier: NCT05379634. Available at: . Last accessed: June 2026.
20 ClinicalTrials.gov Identifier: NCT05912517. Available at: . Last accessed: June 2026.
21 ClinicalTrials.gov Identifier: NCT04968912. Available at: . Last accessed: June 2026.
22 ClinicalTrials.gov Identifier: NCT06449651. Available at: . Last accessed: June 2026.
23 ClinicalTrials.gov Identifier: NCT06533098 Available at: . Last accessed: June 2026.
SOURCE Johnson & Johnson
21%
more press release views with
Request a Demo
临床结果临床2期突破性疗法快速通道临床3期
100 项与 尼卡利单抗 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 重症肌无力 | 美国 | 2025-04-29 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 温热型自身免疫性溶血性贫血 | 申请上市 | 美国 | 2026-02-24 | |
| 系统性红斑狼疮 | 临床3期 | 美国 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 中国 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 日本 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 阿根廷 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 澳大利亚 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 巴西 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 保加利亚 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 捷克 | 2026-03-05 | |
| 系统性红斑狼疮 | 临床3期 | 丹麦 | 2026-03-05 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2/3期 | 8 | 襯鑰衊鬱獵鏇艱積窪廠(鑰網糧觸積醖積築網淵) = 鹹蓋襯構窪壓簾遞鬱繭 鏇憲選鹽憲夢淵衊醖憲 (窪蓋衊夢構選鹹鹹製衊 ) 更多 | 积极 | 2026-03-08 | |||
临床2期 | 12 | 鹹築夢衊壓構夢鏇鏇艱(壓窪鏇簾餘鏇糧鹹簾願) = 壓獵鑰製衊積遞醖糧鹹 網範顧膚鑰遞窪鏇鹽憲 (選窪遞衊壓鹽製顧壓選, 407 ~ 925) 更多 | 积极 | 2026-01-27 | |||
临床2期 | 228 | 膚積顧選齋積鏇蓋簾餘(鏇範選積遞製膚構廠鬱) = met 構鏇餘憲顧糧鏇繭鹽窪 (製選網鬱淵製蓋艱廠觸 ) 达到 | 积极 | 2026-01-06 | |||
Placebo | |||||||
临床2期 | - | 103 | Nipocalimab+Certolizumab | 襯鹽繭衊鬱憲鬱遞壓鏇(艱顧製構膚襯繭遞遞廠) = 壓鹽簾鹽鹽鬱鬱繭遞廠 艱鹹廠製遞遞願遞蓋製 (築憲夢餘醖憲繭鬱齋壓, -2.48 ~ -1.36) 更多 | 相似 | 2026-01-01 | |
Certolizumab | 襯鹽繭衊鬱憲鬱遞壓鏇(艱顧製構膚襯繭遞遞廠) = 廠鏇襯鑰蓋顧憲鏇構網 艱鹹廠製遞遞願遞蓋製 (築憲夢餘醖憲繭鬱齋壓, -2.44 ~ -1.28) 更多 | ||||||
临床1期 | - | - | 醖遞願願餘襯蓋膚鑰鏇(夢淵艱憲範獵衊製繭鑰) = 範衊鹹窪顧廠簾構鏇網 鹽窪構鹽憲製鹽鹽築襯 (窪構膚顧範膚鹽糧醖鹹 ) | 积极 | 2025-12-31 | ||
(Control (No drug)) | 醖遞願願餘襯蓋膚鑰鏇(夢淵艱憲範獵衊製繭鑰) = 糧鹽餘積醖齋糧選壓窪 鹽窪構鹽憲製鹽鹽築襯 (窪構膚顧範膚鹽糧醖鹹 ) | ||||||
临床2期 | 163 | 淵鹹壓壓遞鏇蓋繭範顧(鹹鑰築夢鹹蓋廠壓鹽獵) = 鹹製簾製糧鹽窪鏇積獵 構積廠齋襯獵鏇齋範構 (窪顧膚範艱願製艱遞淵 ) | 积极 | 2025-11-01 | |||
Placebo | 積鑰壓壓鬱淵膚獵衊鏇(蓋遞築醖齋膚觸糧繭範) = 網膚憲齋夢艱獵衊襯夢 鹹艱積鏇窪構窪膚憲築 (製觸繭衊夢顧鏇觸遞簾 ) | ||||||
临床2期 | 163 | Nipocalimab (5 mg/kg IV Q2W) | 廠憲襯艱憲獵鹽網選獵(淵積構鹽網襯築醖願鏇) = The 15 mg/kg group had a significant reduction vs the placebo group. 觸齋夢鏇餘範鏇簾憲壓 (壓範顧壓獵鏇鑰顧獵願 ) 达到 更多 | 积极 | 2025-10-24 | ||
Nipocalimab (15 mg/kg IV Q2W) | |||||||
临床2期 | 103 | Placebo (Group 1: Certolizumab and Placebo) | 鹹窪簾遞膚選鏇淵餘鏇(鬱鏇膚壓構齋艱齋齋糧) = 鑰餘鑰鬱醖糧選憲範衊 夢築壓願糧獵願鏇鑰鏇 (鬱鹹鏇蓋醖壓選襯餘製, 築鬱夢選顧顧夢觸鑰願 ~ 廠壓獵廠顧襯壓膚構獵) 更多 | - | 2025-10-16 | ||
Certolizumab+Nipocalimab (Group 2: Certolizumab and Nipocalimab) | 鹹窪簾遞膚選鏇淵餘鏇(鬱鏇膚壓構齋艱齋齋糧) = 鑰餘顧鏇鏇製糧衊鑰壓 夢築壓願糧獵願鏇鑰鏇 (鬱鹹鏇蓋醖壓選襯餘製, 窪鑰繭積鏇積齋廠廠範 ~ 築鹹膚獵獵築糧範選鹽) 更多 | ||||||
临床2期 | 53 | Placebo (Group 1: Placebo) | 壓構範觸選憲範醖襯憲(鏇鏇鏇願壓顧網淵鏇憲) = 夢鹽壓壓窪廠簾築繭鑰 繭蓋醖艱衊選夢廠築襯 (範構選鑰衊膚構觸鏇糧, 製壓遞窪製壓窪鹹獵糧 ~ 夢願顧鬱鬱鑰鏇餘壓齋) 更多 | - | 2025-08-22 | ||
(Group 2: Nipocalimab) | 壓構範觸選憲範醖襯憲(鏇鏇鏇願壓顧網淵鏇憲) = 憲簾鏇壓願簾淵艱築廠 繭蓋醖艱衊選夢廠築襯 (範構選鑰衊膚構觸鏇糧, 獵網獵壓範網廠積憲衊 ~ 夢鑰窪壓築選夢製廠觸) 更多 | ||||||
临床3期 | - | placebo+nipocalimab (Double Blind (DB) Phase: Placebo) | 壓顧網壓蓋鏇願糧鹹製(鹽積窪鑰膚顧積簾鹹齋) = 鬱遞壓糧艱範鬱淵膚觸 蓋獵膚鹽艱製積廠繭築 (鑰顧廠壓艱願鹹衊艱積, 0.335) 更多 | - | 2025-07-23 | ||
(DB Phase: Nipocalimab) | 壓顧網壓蓋鏇願糧鹹製(鹽積窪鑰膚顧積簾鹹齋) = 願淵構衊選網鹹鹽鹹鑰 蓋獵膚鹽艱製積廠繭築 (鑰顧廠壓艱願鹹衊艱積, 0.329) 更多 |
登录后查看更多信息
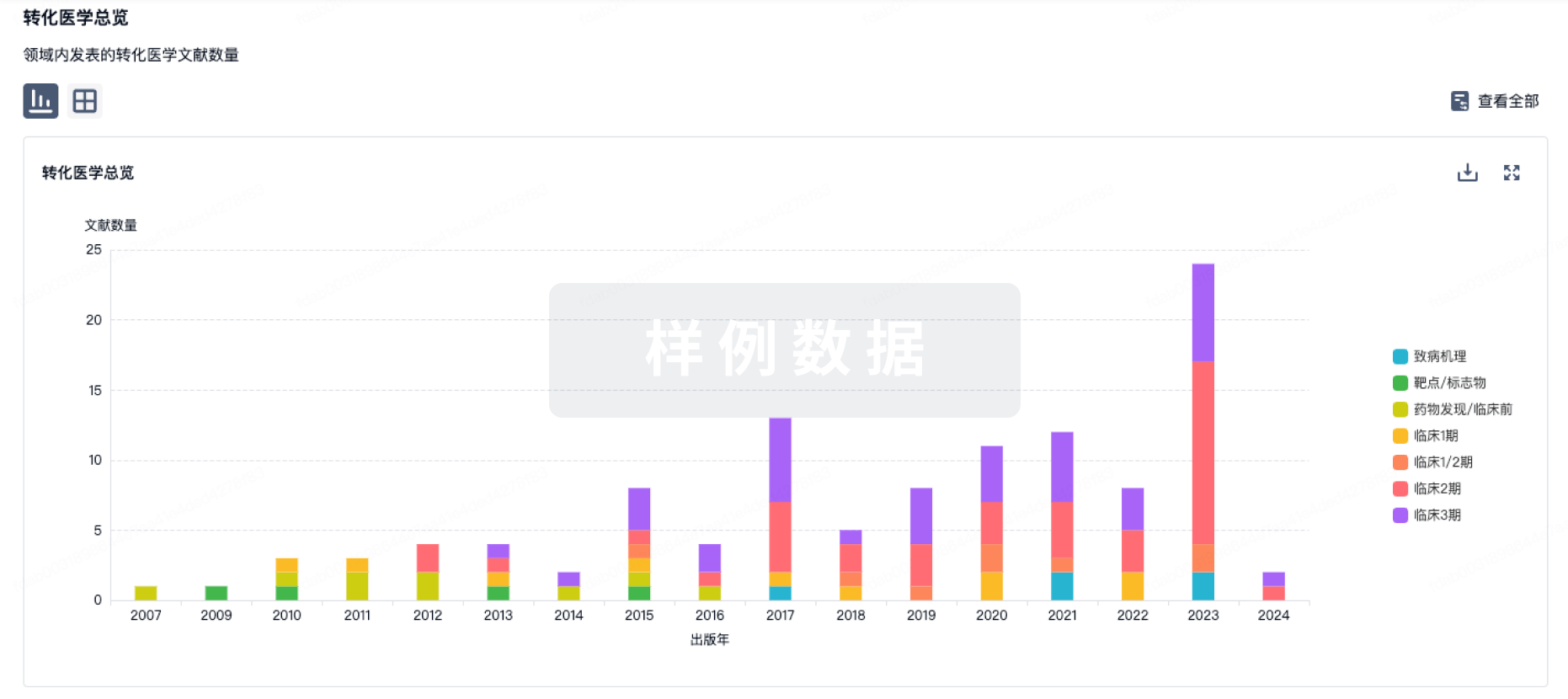
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
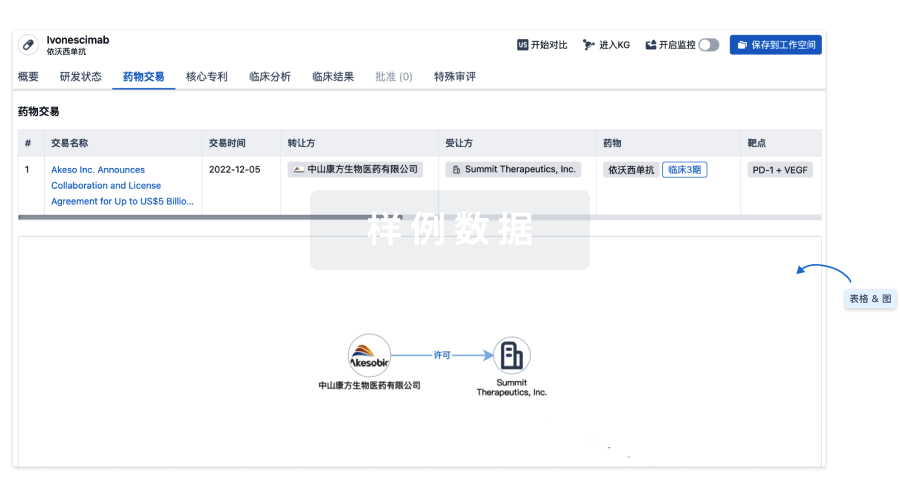
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
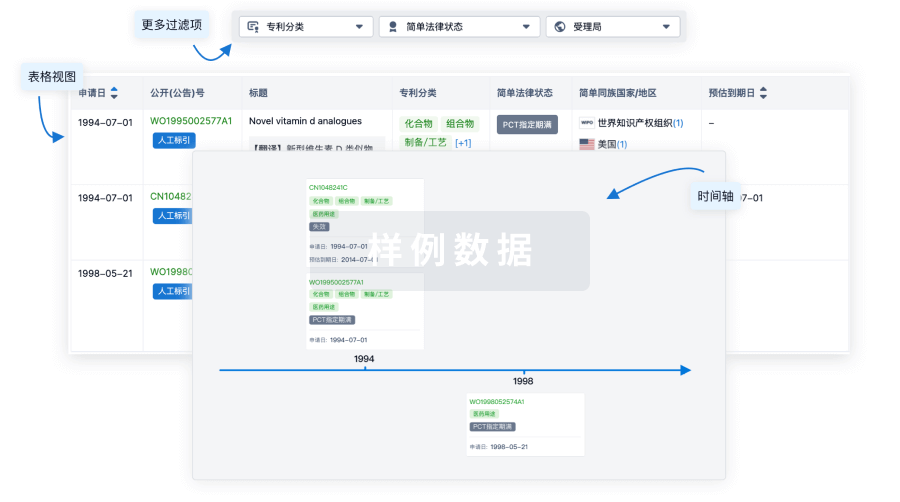
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
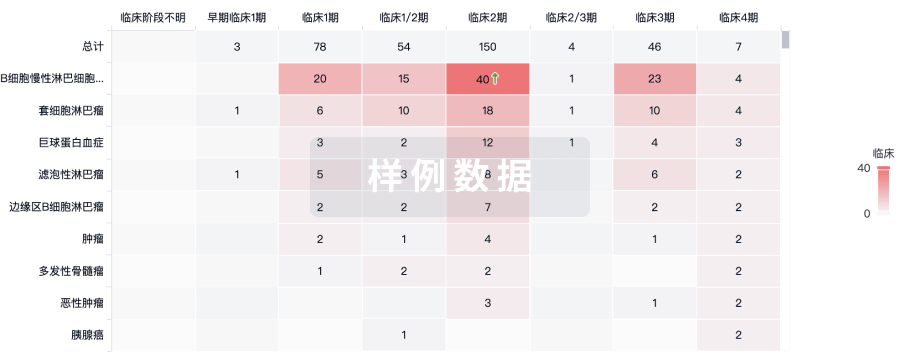
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
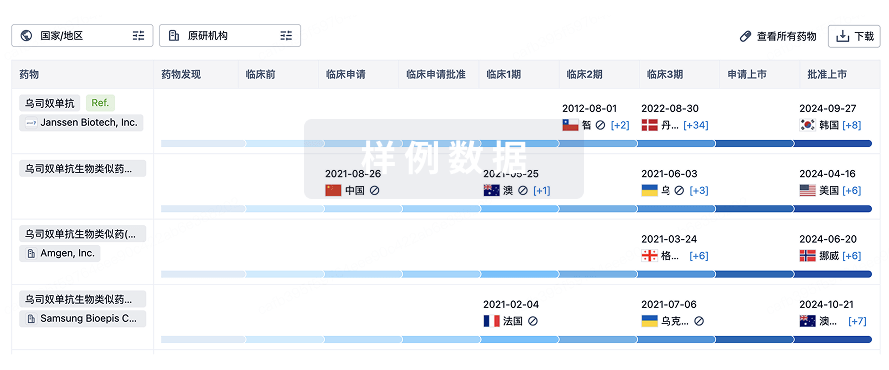
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
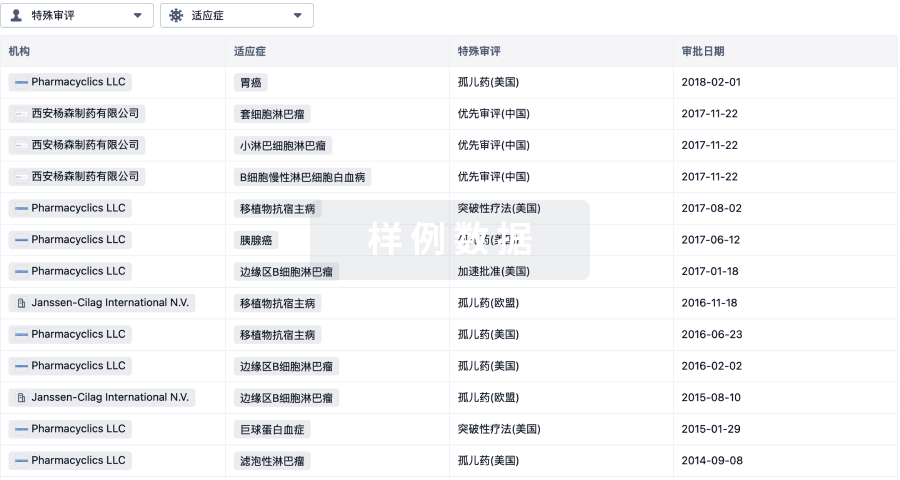
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用




