预约演示
更新于:2026-05-14
Patisiran sodium
帕替司兰
更新于:2026-05-14
概要
基本信息
药物类型 siRNA |
别名 Patisiran、patisiran、Patisiran sodium (JAN) + [8] |
靶点 |
作用方式 抑制剂 |
作用机制 TTR抑制剂(转甲状腺素蛋白抑制剂) |
非在研适应症- |
非在研机构- |
最高研发阶段批准上市 |
首次获批日期 美国 (2018-08-10), |
最高研发阶段(中国)- |
特殊审评优先审评 (美国)、突破性疗法 (美国)、孤儿药 (美国)、孤儿药 (澳大利亚)、快速通道 (美国) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
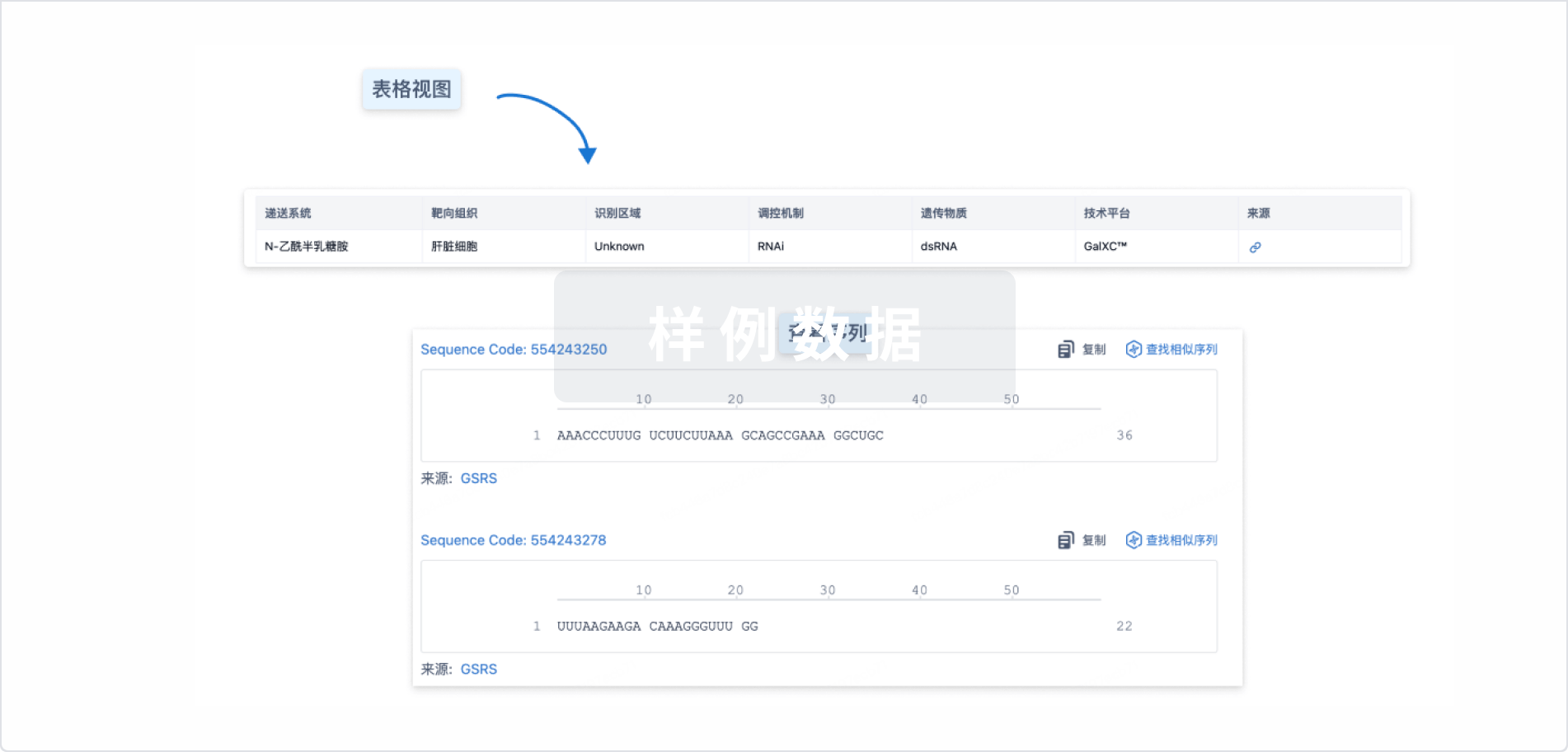
Sequence Code 29732340

来源: *****
Sequence Code 29732483

来源: *****
关联
12
项与 帕替司兰 相关的临床试验NCT05023889
Spectrum of Peripheral and Autonomic Neuropathies in Patients With aTTRwt Amyloidosis and Response to Patisiran Therapy
To evaluate the efficacy and safety of patisiran in patients with wtATTR amyloidosis and symptomatic polyneuropathy by evaluating the effect on neurologic impairment and quality of life.
开始日期2022-08-03 |
申办/合作机构 |
NCT04201418
A Phase 4 Multicenter Observational Study to Evaluate the Effectiveness of Patisiran in Patients With Polyneuropathy of Hereditary Transthyretin-Mediated (ATTRv) Amyloidosis With a V122I or T60A Mutation
To evaluate the effectiveness of patisiran in patients with ATTRv amyloidosis with polyneuropathy who have a V122I or T60A mutation.
开始日期2019-12-18 |
NCT03997383
APOLLO-B: A Phase 3, Randomized, Double-blind, Placebo-controlled Multicenter Study to Evaluate the Efficacy and Safety of Patisiran in Patients With Transthyretin Amyloidosis With Cardiomyopathy (ATTR Amyloidosis With Cardiomyopathy)
The purpose of this study is to evaluate the efficacy and safety of patisiran in participants with ATTR amyloidosis with cardiomyopathy.
开始日期2019-09-04 |
100 项与 帕替司兰 相关的临床结果
登录后查看更多信息
100 项与 帕替司兰 相关的转化医学
登录后查看更多信息
100 项与 帕替司兰 相关的专利(医药)
登录后查看更多信息
239
项与 帕替司兰 相关的文献(医药)2026-04-01·CURRENT PROBLEMS IN CARDIOLOGY
Impact of disease-modifying therapies on imaging parameters in cardiac amyloidosis: A systematic review and meta-analysis
Review
作者: Zervas, Georgios ; Briasoulis, Alexandros ; Androulakis, Emmanuil ; Patras, Raphael ; Georgiopoulos, Georgios ; Tepetes, Nikolaos ; Kastritis, Efstathios ; Lama, Niki ; Kourek, Christos ; Stamatelopoulos, Kimon ; Theodorakakou, Foteini
Transthyretin-mediated (ATTR) and immunoglobulin light-chain (AL) cardiac amyloidosis causes progressive myocardial dysfunction and poor prognosis. Disease-specific therapies in ATTR and anti-clonal therapies in AL cardiac amyloidosis may modify disease, but treatment-induced changes in prognostic cardiac imaging markers remain incompletely defined. We systematically searched PubMed/MEDLINE, Scopus, CINAHL, Web of Science, and EMBASE for studies reporting treatment-associated changes in global longitudinal strain (GLS), left ventricular (LV) wall thickness, and extracellular volume (ECV) assessed by echocardiography or cardiac magnetic resonance. Random-effects meta-analyses pooled mean changes. Seventeen studies met inclusion criteria. In ATTR cardiac amyloidosis, therapy with silencers or RNA-depleting agents was associated with improved GLS (pooled mean difference [MD] -0.97 %, 95 % CI -1.27 to -0.68) and reduced LV wall thickness (MD -0.72 mm, 95 % CI -1.26 to -0.17) versus no therapy, while ECV showed no significant change (MD -1.93 %, 95 % CI -15.27 to 11.41). In AL amyloidosis, complete hematologic response was linked to greater improvement than non-response in GLS (MD -1.19 %, 95 % CI -2.20 to -0.17) and LV wall thickness (MD -0.87 mm, 95 % CI -1.31 to -0.43). NMA in ATTR cardiac amyloidosis showed that patisiran (MD -1.04 %, 95 % CI -1.56 to -0.52), tafamidis (-0.91 %, -1.40 to -0.41), and vutrisiran (-0.90 %, -1.75 to -0.05) improved GLS versus placebo, compared to acoramidis. Disease-directed therapy in ATTR and hematologic response in AL cardiac amyloidosis are associated with preservation or improvement of GLS and LV wall thickness, supporting their use as surrogate endpoints for treatment monitoring.
2026-04-01·Neurologia
Redefining therapeutics in vATTR: Evaluation of response predictors to tafamidis and patisiran treatment in a non-endemic area. A proposal for a novel individualised therapeutic approach
Article
作者: Matías-Guiu, J ; Restrepo-Córdoba, M A ; Martín-Albarrán, S ; González-López, E ; Martínez-Vicente, L ; Goirigolzarri-Artaza, J ; García-Pavía, P ; Guerrero-Sola, A ; Gutiérrez-Gutiérrez, G ; Guerrero-Peral, Á L ; Álvarez-Troncoso, J ; Galán-Dávila, L ; Gajate-García, V ; Horga, A ; Valverde-Megías, A
INTRODUCTION:
Hereditary transthyretin amyloidosis (vATTR) is a progressive genetic disorder with several approved treatments. We investigated treatment responses to tafamidis and patisiran in vATTR patients to identify predictive response factors.
METHODS:
Retrospective analysis on vATTR patients treated with tafamidis or patisiran from October 2012 to September 2022. Treatment responses were assessed as "good," "partial," or "non-response." We analysed pre-treatment clinical and laboratory data to identify predictors of treatment response.
RESULTS:
Of the 53 patients, 44 received tafamidis and 23 received patisiran; 14 were treated with both drugs sequentially. Predictors of good response to tafamidis were shorter diagnostic delay (≤1 year), less severe neurological impairment (Coutinho stage 1, Neuropathy Impairment Score [NIS]≤7), and better sudomotor function in the feet (≥50μS) before treatment. Factors associated with non-response were greater disability (baseline Polyneuropathy Disability score=2), large fibre involvement, and significant weight loss. Predictors of a good response to patisiran included lower pre-treatment disease severity (Coutinho stage 1, NIS≤40). We propose an individualised therapeutic approach using predictive factors to guide initial treatment.
CONCLUSIONS:
This study identifies predictive factors for response to tafamidis and patisiran in vATTR patients, highlighting baseline NIS as a critical predictor. We propose a novel therapeutic algorithm for personalised treatment strategies with potential to avoid years of ineffective treatment.
2026-04-01·Materials Today Bio
Programmable lipid nanoparticles for RNA therapeutics: Design principles and clinical translation
Review
作者: Ramezani Farani, Marzieh ; Navid Talemi, Mahdi ; Alipour Eskandani, Naiyereh ; Huh, Yun Suk ; Mirzaee, Danial ; Alipourfard, Iraj
RNA therapeutics have come of age as clinically validated modalities including mRNA, siRNA, antisense oligonucleotides (ASOs), and in vivo genome editing, with lipid nanoparticles (LNPs) as the main non-viral delivery system. This review defines programmable LNPs as systems whose composition and interfacial chemistry are tuned to control organ tropism, cell specificity, intracellular trafficking, and immune interactions. We summarize design rules across four core components (ionizable lipid, phospholipid, cholesterol, PEG-lipid) and highlight levers like apparent pKa optimization (∼6-7 for hepatic delivery), biodegradable linkers, PEG-anchor-dependent shedding, ligands (e.g., GalNAc), and selective organ-targeting (SORT) lipids that redirect biodistribution beyond the liver. We survey advances in data-guided formulation, including DNA-barcoded in vivo libraries, machine learning, and physics-based prediction, plus scalable manufacturing (microfluidics, confined impinging-jet mixing, tangential-flow filtration) and Quality-by-Design with process-analytical technologies. A comprehensive characterization toolkit (size/ζ-potential, cryo-EM/SAXS, RNA encapsulation and integrity, apparent pKa, in vivo barcoding) maps to critical quality attributes. Applications span vaccines, protein replacement, siRNA/ASO delivery, and CRISPR platforms, with clinical examples like patisiran, COVID-19 and RSV mRNA vaccines, in-human transthyretin (TTR) editing, and individualized melanoma vaccination. We analyze translational constraints like endosomal escape, reactogenicity and anti-PEG immunity, complement activation, and lot-to-lot control, plus success factors: corona-aware design, dose-efficient potency at low lipid burden, redosing strategies, and fit-for-purpose biomarkers. Together, programmable LNPs offer a generalizable path to extrahepatic, cell-aware RNA medicine when coupled to rigorous analytics and platform manufacturing.
919
项与 帕替司兰 相关的新闻(医药)2026-05-13
又到了今天的学习笔记了,在生物制药的大小会场,近几年非常耳熟能详的,小核酸药物也算是个热词了,今天的内容主要是研究下小核酸药物的作用机理和成药性。小核酸药物的形象比喻,小核酸药物就像细胞内的"精准剪刀手":
如果把基因看作"蓝图",蛋白质看作"产品",那么mRNA就是从蓝图到产品之间的"施工图纸"。传统药物是在产品(蛋白质)层面干预,而小核酸药物直接"截获并销毁施工图纸"(mRNA),从源头上阻止有害蛋白质的产生。就像在工厂里安排一位精准的"质检员",专门识别并销毁错误的施工图纸,让有缺陷的产品永远无法被生产出来。
一、小核酸药物的发现历史1990年代:RNA干扰现象的发现
1990年代初,科学家在植物中观察到"转录后基因沉默"现象。1998年,Andrew Fire和Craig Mello在《Nature》发表里程碑研究,证明将双链RNA注入线虫可以特异性沉默基因表达,首次阐明RNA干扰(RNAi)机制。2001年:siRNA在哺乳动物中的验证
2001年,Thomas Tuschl团队证明合成的短双链RNA(siRNA,约21个碱基对)可以在哺乳动物细胞中诱导基因沉默,开启了siRNA作为治疗工具的时代。2004年:首个临床试验启动
2004年,首个siRNA药物(靶向VEGF,治疗年龄相关性黄斑变性)进入临床试验,标志着小核酸药物从实验室走向临床。2006年:诺贝尔奖认可
Fire和Mello因发现RNAi机制获得诺贝尔生理学或医学奖,引发全球对RNAi疗法的投资热潮。2008-2012年:"寒冬期"
多个siRNA临床项目因递送效率差、脱靶毒性、免疫激活等问题失败,多家大药企退出RNAi领域,行业陷入低谷。2014-2018年:递送技术突破
两大递送平台诞生:脂质纳米颗粒(LNP)
Alnylam开发的LNP技术解决了肝脏递送问题GalNAc偶联技术
N-乙酰半乳糖胺偶联实现肝细胞精准递送,皮下注射即可
2018年,FDA批准首个siRNA药物**Patisiran(Onpattro)**用于治疗遗传性转甲状腺素蛋白淀粉样变性(hATTR),采用LNP递送。2019-2026年:获批产品井喷
2019年至今,已有超过15个小核酸药物获FDA批准(包括siRNA和ASO),适应症从罕见病扩展到心血管、代谢、血液、神经系统疾病。
关键获批产品(siRNA类):Patisiran(2018)
hATTR多发性神经病,LNP递送Givosiran(2019)
急性肝卟啉症,GalNAc偶联Lumasiran(2020)
原发性高草酸尿症1型Inclisiran(2021)
高胆固醇血症,每半年一次皮下注射Vutrisiran(2022)
hATTR多发性神经病,GalNAc偶联(Patisiran升级版)Fitusiran(2025)
血友病A和B
关键获批产品(ASO类):Nusinersen(2016)
脊髓性肌萎缩症(SMA)Eplontersen(2023)
hATTR多发性神经病Olezarsen(2024)
家族性乳糜微粒血症Donidalorsen(2025)
遗传性血管性水肿
二、全球进度前五的小核酸药物管线(2026年最具突破性)1. Zilebesiran - Alnylam
基本信息
类型:siRNA(GalNAc偶联)
靶点:血管紧张素原(AGT)
适应症:高血压
临床阶段:Phase III
临床意义
全球首个针对高血压的siRNA药物。每半年一次皮下注射即可持续降低血压,彻底解决高血压患者依从性差的问题。全球约13亿高血压患者,市场潜力超百亿美元。Phase II数据显示,单次注射可持续降低收缩压约10-15 mmHg,维持6个月。2. Pelacarsen - Ionis/Novartis
基本信息
类型:ASO
靶点:Lp(a)脂蛋白
适应症:心血管疾病预防
临床阶段:Phase III(HORIZON心血管结局试验,2026年中期读出)
临床意义
Lp(a)升高是心血管疾病的独立危险因素,目前无有效降低Lp(a)的药物。Pelacarsen可降低Lp(a)水平约80%。如果HORIZON试验证实心血管结局获益,将成为首个通过降低Lp(a)预防心血管事件的药物。3. Bepirovirsen - Ionis/GSK
基本信息
类型:ASO
靶点:乙肝病毒(HBV)所有mRNA
适应症:慢性乙型肝炎
临床阶段:Phase III(2026年中期数据)
临床意义
全球约2.96亿慢性乙肝患者,目前无法实现功能性治愈。Bepirovirsen可降低HBsAg和HBV DNA,Phase III数据如果积极,可能开启乙肝功能性治愈的时代。4. Olezarsen - Ionis
基本信息
类型:ASO
靶点:APOC3
适应症:严重高甘油三酯血症
临床阶段:已获FDA批准(2024年,家族性乳糜微粒血症);2026年预计获批更广适应症
临床意义
2024年获批用于家族性乳糜微粒血症(FCS)。2026年预计获批用于更广泛的严重高甘油三酯血症人群,市场规模大幅扩展。5. Mivelsiran - Alnylam
基本信息
类型:siRNA
靶点:淀粉样前体蛋白(APP)
适应症:脑淀粉样血管病(CAA)
临床阶段:Phase II
临床意义
首个靶向中枢神经系统的siRNA药物之一。突破肝脏递送限制,探索CNS递送。为阿尔茨海默病等神经退行性疾病的siRNA治疗开辟道路。三、小核酸药物成药性的辩证分析优势1. 靶点选择无限,颠覆"不可成药"
传统小分子药物需要靶蛋白有结合口袋,仅约15%的蛋白质"可成药"。小核酸药物在mRNA层面干预,理论上可以沉默任何基因,覆盖整个基因组(约20,000个基因)。只需知道靶基因的mRNA序列即可设计药物,不需要蛋白质结构信息。2. 设计快速,开发周期短
从确定靶基因到设计候选分子仅需数周(vs 传统小分子数月至数年)。化学修饰和递送技术已平台化,新靶点药物可以快速推进。Alnylam目标是2025年底前递交9个新IND申请,体现了平台化的高效率。3. 超长效,依从性极佳
GalNAc偶联siRNA药物半衰期极长:Inclisiran
每6个月一次皮下注射Vutrisiran
每3个月一次皮下注射Zilebesiran
每6个月一次皮下注射
彻底解决慢性病患者每日服药的依从性问题,从"每天吃药"变为"每半年打一针"。4. 高特异性,脱靶风险低
siRNA通过碱基互补配对识别靶mRNA,特异性极高(20-21个碱基的序列匹配)。经过化学修饰优化后,脱靶效应已大幅降低。相比传统小分子的"锁钥模型",核酸的"碱基配对"特异性更高。5. 平台化优势,管线快速扩展
一旦建立递送平台(如GalNAc偶联),更换靶基因序列即可开发新药。从已获批药物的数据可以预测同平台新药的药代动力学和安全性。加速了从罕见病向常见病的扩展。劣势与挑战1. 递送是最大瓶颈
肝脏以外递送困难:
GalNAc偶联和LNP主要实现肝脏递送
肝外组织(中枢神经系统、肌肉、肺、肾脏、肿瘤)递送仍是重大挑战
限制了适应症范围(目前获批产品几乎全部是肝脏靶向)
正在探索的肝外递送技术:
Arrowhead:开发靶向αvβ6整合素的肺部递送技术
Alnylam:探索CNS递送(鞘内注射)
多家公司:开发抗体-核酸偶联物(ARC)、外泌体递送等2. 只能"沉默"不能"激活"
siRNA和ASO的机制是降解mRNA或阻断翻译,只能下调基因表达。对于需要上调基因表达或恢复蛋白功能的疾病(如功能丧失型突变),小核酸药物无能为力。适应症限于"基因表达过高"导致的疾病。3. 不可逆性和安全性顾虑
长效=长毒:
超长效是优势也是风险:一旦出现不良反应,无法快速逆转
siRNA沉默效应可持续数周至数月
需要仔细评估长期沉默靶基因的安全性
肝脏毒性:
由于主要在肝脏蓄积,肝脏毒性是常见不良反应
转氨酶升高(ALT/AST)在部分患者中出现
需要定期监测肝功能4. 免疫激活风险
双链RNA可能激活先天免疫(通过TLR3/7/8、RIG-I等受体)。化学修饰已大幅降低免疫激活,但仍有注射部位反应(皮下注射后局部红肿、疼痛)。5. 成本高昂
当前定价:
Patisiran:约45万美元/年
Inclisiran:约6,500美元/年(相对便宜,因为仅半年一次)
多数罕见病siRNA药物:10-50万美元/年
生产成本:
核酸合成成本虽在下降,但仍高于传统小分子
GalNAc偶联和LNP制备增加成本6. 适应症集中于罕见病和肝脏疾病
当前局限:
已获批产品几乎全部是罕见病或肝脏相关疾病
常见病(高血压、高血脂)的产品仍在Phase III
肿瘤领域进展缓慢(递送是主要障碍)四、小核酸药物成药性综合评价适合小核酸药物的最佳场景
场景
理由
实例
肝脏靶基因过表达疾病
GalNAc递送成熟,肝靶向高效
hATTR、高胆固醇血症、乙肝
慢性病需长期治疗
超长效,每半年一次
高血压、高血脂
传统药物"不可成药"靶点
不需要蛋白结合口袋
Lp(a)、APOC3、AGT
罕见遗传病
靶向致病基因,精准治疗
SMA、肝卟啉症、PH1不太适合的场景
场景
理由
替代方案
肝外组织疾病(目前)
递送技术不成熟
传统药物、基因治疗
需要快速可逆
长效不可逆
传统小分子
需要上调基因表达
只能沉默
mRNA疗法、基因治疗
肿瘤(目前)
递送到实体瘤困难
抗体、细胞疗法五、未来发展方向肝外递送突破
肺部递送:Arrowhead和Alnylam正在开发靶向肺部的递送技术,用于哮喘、COPD、肺纤维化等。
CNS递送:鞘内注射(如Nusinersen)、新型配体偶联技术正在探索。Alnylam的Mivelsiran是CNS siRNA的先驱。
肌肉递送:用于肌肉萎缩症、心肌病等,多家公司正在开发抗体-核酸偶联物。从罕见病走向常见病
心血管代谢病:Zilebesiran(高血压)、Inclisiran(高血脂)代表了从罕见病到常见病的转变。全球高血压13亿人、高血脂约10亿人,市场规模数百亿美元。联合治疗与多靶点
双靶点siRNA:Corsera Health开发的每年一次siRNA同时靶向PCSK9和AGT,降脂降压一针搞定。中国机遇
瑞博生物:2026年1月港交所上市,拥有全球最大的siRNA管线之一。核心产品RBD4059(血栓)、RBD5044(高甘油三酯)、RBD7022(高胆固醇)、RBD1016(乙肝)均在Phase II阶段。自主开发RiboGalSTAR™肝靶向递送平台。
圣诺医药:"国内小核酸药物第一股"(2021年港交所上市)。STP705(siRNA组合,治疗皮肤鳞癌)处于Phase II/III,是全球为数不多的肿瘤siRNA药物。
行业展望:2026年被视为中国小核酸药物"产业价值全面兑现的关键之年",有望实现从"跟跑"到"并跑"的跨越。六、总结
小核酸药物从1998年RNAi机制发现到2026年已有28年历史,经历了从诺贝尔奖的辉煌到行业寒冬的低谷,再到递送技术突破后的爆发。截至2026年,全球已有超过15个小核酸药物获批,适应症从罕见病快速扩展到心血管、代谢、感染性疾病。
成药性方面,优势包括靶点选择无限、设计快速、超长效、高特异性、平台化。挑战包括肝外递送瓶颈、只能沉默不能激活、长效带来的安全性顾虑、成本高。
小核酸药物的未来在于肝外递送突破和从罕见病向常见病扩展。一旦肺、CNS、肌肉等组织的递送问题解决,小核酸药物将真正覆盖从头到脚的几乎所有疾病,成为与小分子、抗体并列的第三大药物类型。
全球RNA治疗市场预计2034年将达到453亿美元,中国企业正加速追赶,2026年将是关键转折点。
2026-05-13
在生物医药的广阔版图中,核酸药物尤其是小干扰RNA(siRNA)因其能够从基因层面沉默特定致病基因,被誉为“第三代药物”的代表。然而,siRNA分子本身在体内容易被核酸酶降解,且因其带负电、分子量较大而难以跨越细胞膜屏障,因此,高效、安全的递送系统是决定siRNA能否成功转化为临床疗法的关键。脂质纳米颗粒(Lipid Nanoparticles, LNP)是目前最成熟的递送平台之一,已上市的Patisiran(治疗遗传性转甲状腺素蛋白淀粉样变性)便是采用LNP递送siRNA的典范。然而,传统LNP存在靶向性不足、易富集于肝脏等缺点,用于关节炎这类非肝脏的局部疾病时效果有限。
本文将介绍羿美诚健(上海)生物医药有限公司的一项研究,为我们带来了一种全新的脂质组合物设计思路。该研究团队通过对LNP各组分的摩尔比例进行精细优化,特别是降低了可电离阳离子脂质的占比(从常见的50%降至37-49%),并显著增加了PEG脂质(DMG-PEG2000)的占比(从1.5%提升至2-6%)。在经典的胶原蛋白诱导的大鼠关节炎(CIA)模型中,无论是通过关节腔注射还是皮下注射给药,装载治疗性siRNA的优化LNP均展现出了优于商业化配比的治疗效果,显著降低了关节炎评分和足体积,且安全性良好。本文将从研究背景、脂质组合物设计、详细的制备与表征过程,以及多组动物实验数据出发,为您全面解析这项技术的突破之处。
一、 研究背景:自身免疫疾病的治疗困境与核酸递送挑战
类风湿性关节炎是一种常见的自身免疫性疾病,其发病机制涉及遗传与环境因素的复杂交互。传统治疗药物主要包括抗风湿类药物、非甾体抗炎药和皮质类固醇,这些药物虽然能在一定程度上缓解炎症,但多为对症治疗,难以从根本上阻断疾病进展,且长期使用副作用明显。近年来,以依那西普为代表的生物靶向药物(TNF-α抑制剂等)显著提高了疗效,但它们也伴随着一系列问题:长期使用可能增加恶性肿瘤风险、可能诱发“新的自身免疫性疾病”、给药方式不便(通常需要皮下或静脉注射,频率较高)、患者依从性有限以及治疗成本高昂。
正是在此背景下,siRNA疗法进入了研究者的视野。通过RNA干扰机制,siRNA能够特异性地沉默与关节炎发病相关的基因(如促炎细胞因子、信号转导分子等),实现真正的精准治疗,具有高效性、序列特异性和瞬时可控的特点。然而,将siRNA成功递送到关节腔内的靶细胞(如巨噬细胞、滑膜成纤维细胞)面临重重困难。裸siRNA在血液中半衰期极短,易被肾小球滤过和被核酸酶降解,且其阴离子特性使之难以通过同样带负电的细胞膜脂质双层。
LNP是目前解决这一难题的最有力工具。典型的LNP由可电离阳离子脂质、中性辅助脂质、胆固醇和PEG脂质四种成分自组装而成。其中,可电离阳离子脂质在酸性pH下带正电,与带负电的siRNA结合并促进包封;在生理pH下则接近中性,降低毒性并利于内涵体逃逸。然而,已上市LNP(如用于Patisiran的配方摩尔比为 DLin-MC3-DMA : DSPC : 胆固醇 : DMG-PEG2000 = 50:10:38.5:1.5)主要设计用于肝脏靶向,因为其表面吸附的载脂蛋白E(ApoE)会引导LNP通过低密度脂蛋白受体进入肝细胞。对于关节炎治疗,理想的给药方式是局部注射(关节腔或关节附近皮下),这就要求LNP具备不同的理化性质和生物学行为。
本研究正是针对这一未被满足的临床需求,通过系统筛选脂质比例,特别是提高PEG脂质的比例,来优化LNP的稳定性、组织渗透性和局部滞留效应,从而实现关节局部的卓越治疗效果。PEG脂质(即DMG-PEG2000,聚乙二醇化二肉豆蔻酰甘油,分子量约2000 Da)在LNP中起着关键的“隐形”作用:它可以减少LNP在非靶组织的非特异性吸附,防止颗粒聚集,并调节LNP与细胞膜的相互作用。提高PEG脂质比例,有助于在注射部位形成更稳定的纳米颗粒储库,延长siRNA的释放时间,并可能通过优化PEG链的表面密度来改善靶细胞的摄取。二、 创新脂质组合物的组成与摩尔比
核心是一种包含四种组分的脂质组合物:可电离阳离子脂质、中性辅助脂质(具体为DSPC,即1,2-二硬脂酰-sn-甘油-3-磷酸胆碱)、胆固醇以及PEG脂质(具体为DMG-PEG-2000)。与常规配方最大的不同在于,该组合物中各组分摩尔比被限定在一个非对称的、经大量实验优化的范围内:
可电离阳离子脂质 : DSPC : 胆固醇 : DMG-PEG2000 = 37~49 : 8~22 : 38~39 : 2~6
通过进一步的体内外筛选,确定了两个更窄且药效最优的摩尔比子范围:
范围一(较高辅助脂质比例):37.5~40.5 : 17~20.5 : 38~39 : 3~5。该范围适用于多种可电离阳离子脂质,尤其是在皮下注射给药时表现出色。
范围二(较低辅助脂质比例):46.5~48.5 : 9.5~10.5 : 38~39 : 3~5。该范围更接近传统比例但降低了阳离子脂质并提高了PEG比例,在关节腔注射给药时效果突出。
可电离阳离子脂质具有广泛的选择性,包括但不限于:DLin-MC3-DMA((6Z,9Z,28Z,31Z)-三十七碳-6,9,28,31-四烯-19-基4-(二甲基氨基)丁酸酯)、DODMA(1,2-二油基氧基-N,N-二甲基氨基丙烷)、SM-102、ALC-0315、DLin-KC2-DMA、DLinDMA、DLenDMA、DODAP等。这种宽泛的适用性表明,该比例优化策略并非针对某一种特定脂质,而是具有普遍指导意义。三、 siRNA-LNP的制备与表征:详细步骤与关键参数
为了验证上述脂质组合物的递送潜力,研究团队首先采用微流控技术制备了装载特定治疗性siRNA的LNP。该siRNA的序列经过了化学修饰以增强其抗核酸酶降解能力:
正义链序列为 GCCUGUAGCCCAUGUGUATT(SEQ ID NO:1),
反义链序列为 UACAACAUGGGCUACAGCGTT(SEQ ID NO:2),
其中星号“”代表该核苷酸α位磷酸基团的一个非桥接氧原子存在硫代修饰,这种修饰可显著提高siRNA在生物体内的稳定性。
制备流程如下:
脂质相的配制:首先,根据预设的摩尔比准确称取可电离阳离子脂质、DSPC、胆固醇和DMG-PEG2000。将这四种脂质共同溶解于无水乙醇中,通过涡旋和超声使其完全溶解,形成澄清的脂质乙醇混合物。脂质的总浓度根据后续混合比例计算,确保最终颗粒粒径可控。
水相的配制:将上述经过硫代修饰的siRNA冻干粉溶解于醋酸钠缓冲液中。醋酸钠的浓度为25 mM,pH值用冰醋酸精确调节至4.0~6.0,在具体实施例中通常采用pH 5.0。该酸性环境是可电离阳离子脂质质子化、与siRNA发生静电结合的必要条件。siRNA的最终浓度根据投料比设定。
微流控混合:使用微流控设备(如NanoAssemblr或类似平台)进行纳米颗粒的自组装。设定总流速为12~40 mL/min,在具体的大多数实施例中采用16~24 mL/min。关键参数是脂质乙醇混合物与siRNA醋酸钠水溶液的流速比固定为1:3,这意味着水相是乙醇相体积的三倍,以确保脂质在快速混合过程中均匀析出并包封siRNA。同时,控制总脂质与siRNA的质量比(w/w)在8:1至20:1之间,优选为10:1~15:1,最优选为12:1。在这一步骤中,当乙醇溶液与水溶液混合时,脂质的溶解度急剧下降,形成纳米尺度的颗粒,同时质子化的阳离子脂质与阴离子siRNA紧密结合,实现高效包封。
纯化与浓缩(切向流过滤):混合后得到的siRNA-LNP粗品中含有乙醇、未包封的siRNA和部分游离脂质。为了去除这些杂质并将环境pH调节至生理水平,采用切向流过滤系统进行换液。使用的置换缓冲液为pH 7.4的Tris缓冲液或磷酸缓冲液。通过反复渗滤(通常为5-10倍体积置换),乙醇被彻底清除,同时缓冲液pH升高,使LNP表面电荷降低,提高稳定性。该步骤同时可以浓缩样品至所需浓度。
制剂与无菌过滤:收集纯化浓缩后的siRNA-LNP样品,加入蔗糖溶液作为冻干保护剂(最终蔗糖浓度通常为5%~10%),以提高在长期储存或冻干过程中的稳定性。最后,将制剂通过0.2 μm的无菌聚醚砜滤器进行过滤除菌,分装后于2-8°C或-20°C保存备用。
表征方法及结果:
粒径与多分散系数(PDI):使用Malvern Zetasizer Nano ZS动态光散射仪测定。取20 μL样品用去离子水稀释至1 mL,在25°C下平衡2分钟后测量。结果显示,所有制剂的平均粒径均控制在70~110 nm之间(表1),PDI值普遍小于0.2,多数在0.1左右,表明颗粒大小分布非常均一,适合注射给药。
包封率:使用Quant-iT™ RiboGreen® RNA试剂盒测定。RiboGreen是一种超灵敏的荧光核酸染料,只与游离的、未被包封的RNA结合。通过比较有/无Triton X-100(破坏LNP膜)处理的样品荧光强度,即可计算出包封率。具体操作:样品分为两份,一份直接加入RiboGreen试剂测定荧光(游离siRNA),另一份加入1% Triton X-100破坏LNP后测定总siRNA。包封率(%)= (总siRNA - 游离siRNA) / 总siRNA × 100%。如表1、表3、表8、表13所示,所有配方的包封率均高于92%,大部分达到95%以上,甚至98%,表明该制备工艺稳定且高效。
表1(综合多组数据):代表性LNP制剂的组分、摩尔比及理化性质
配方编号
可电离阳离子脂质
脂质摩尔比 (阳离子:DSPC:胆固醇:DMG-PEG2000)
LNP/siRNA (w/w)
平均粒径 (nm)
PDI
包封率 (%)
对照01
DLin-MC3-DMA
50:10:38.5:1.5
12:1
89.0
0.105
96.4
03
DLin-MC3-DMA
48:10:38.5:3.5
12:1
89.5
0.156
97.6
05
DLin-MC3-DMA
47:10:38.5:4.5
12:1
90.4
0.199
96.2
07
DLin-MC3-DMA
40.5:17.5:38.5:3.5
12:1
93.1
0.115
95.1
10
DLin-MC3-DMA
38:20:38.5:3.5
12:1
102.4
0.090
92.1
13
DODMA
48:10:38.5:3.5
12:1
82.9
0.119
98.3
15
DODMA
47:10:38.5:4.5
12:1
86.7
0.153
96.8
18
DODMA
40:17.5:38.5:4
12:1
90.9
0.186
95.4
21
SM-102
40:17.5:38.5:4
12:1
81.0
0.149
94.0
26
DLenDMA
48.5:10:38.5:3
12:1
76.6
0.100
97.4
30
DODAP
37.5:20:38.5:4
15:1
73.7
0.160
95.1四、 CIA大鼠模型的构建与药效评估方案
为了全面评估不同脂质配方和给药途径的药效,研究团队采用了国际公认的胶原诱导的关节炎模型。该模型能很好地模拟人类类风湿性关节炎的滑膜增生、炎性细胞浸润及关节破坏等病理特征。
模型构建具体步骤:
动物:选用SPF级雌性Wistar大鼠,体重范围严格控制在120~140克,以保证对胶原的免疫应答一致性。
首次免疫(第0天):将牛II型胶原蛋白(CII)溶于0.05 M乙酸,终浓度为2 mg/mL,再与等体积的不完全弗氏佐剂(IFA)在冰浴下用高速匀浆器充分乳化,形成稳定的油包水乳剂(胶原乳剂)。大鼠经1-4%异氟烷吸入麻醉后,于尾根部皮内单点注射0.2 mL该胶原乳剂。注射时确保乳剂沉积在皮内,形成一个小泡。
加强免疫(第7天):同样方法,在尾根部另一侧皮内再次注射0.2 mL新鲜的胶原乳剂,以增强免疫反应。通常在加强免疫后7-14天,大鼠后肢开始出现明显的红肿,关节炎评分逐渐升高。
动物分组与给药方案:
研究设计了多个独立实验,分别考察关节腔注射途径和皮下注射途径。在关节炎症状开始出现(通常在第10-14天)后,将大鼠按每组6只随机分组。给药剂量均以siRNA含量计,为9 mg/kg,给药体积为0.9 mL/kg(即每只约0.1-0.13 mL)。给药方案为在第0天(分组当天)、第3天和第6天共三次给药。阳性对照组采用临床药物依那西普(一种TNF-α受体-Fc融合蛋白),以10 mg/kg的剂量,于发病后每3天腹腔注射一次。模型对照组仅诱导CIA,不给予任何治疗。具体分组见原文表4、表9、表14,此处不赘述。
评价指标及详细测量方法:
关节炎评分:从第7天(首次免疫后)开始,每周两次对每只大鼠的所有四肢进行盲法评分,直至实验结束(通常第28-35天)。评分标准严格定义为:0分,无红肿现象;1分,中足(跖骨)或踝关节出现轻微红肿;2分,从踝关节到中足出现轻微至中等红胀;3分,从踝关节到跖骨关节出现中等至严重红胀;4分,从脚趾到踝关节(或前肢从手指到腕关节)出现严重红肿、关节变形。每只动物四肢得分相加,最高为16分。
足体积测量:使用足爪容积测量仪(如Ugo Basile Plethysmometer)。测量时,将大鼠后肢缓慢浸入充满水的测量筒中,直至踝关节处标记线,仪器会自动显示排开水的体积(mL)。在首次免疫前测量基线值,从第7天起每周两次测量双后足体积,取平均值。
体重变化:在首次免疫前称量体重作为基线,从第7天起每周两次称量体重,用以评估药物的全身毒性。若治疗组体重显著低于模型组(p<0.05),则提示可能存在毒性。
统计学分析:所有数据以均数±标准误(Mean ± SEM)表示。使用SPSS软件进行单因素方差分析(ANOVA),组间两两比较采用Tukey或Dunnett检验。p < 0.05被认为具有统计学显著性。五、 实验结果:关节腔注射(DLin-MC3-DMA配方)的显著疗效
在第一个关键实验中,研究团队选用应用最广泛的可电离阳离子脂质DLin-MC3-DMA,将其与DSPC、胆固醇、DMG-PEG2000以不同摩尔比组合(配方01至10,具体摩尔比见表3),制备siRNA-LNP后通过下肢双侧关节腔直接注射给药。
从图1(关节炎评分)中可以清晰地看到:模型对照组(组1)的关节炎评分在免疫后第16天开始迅速攀升,至第28天时平均评分高达8.50,表明CIA模型成功建立且疾病严重。阳性对照依那西普(组2)有效控制了疾病进展,评分维持在3-4分。在受试配方中,采用对照摩尔比50:10:38.5:1.5的配方01(组3)以及摩尔比49:10:38.5:2.5的配方02(组4),其关节炎评分与模型组相比并无显著差异(p>0.05),说明常规比例的LNP即使直接注射到关节腔也无法有效递送siRNA。然而,令人振奋的是,配方03(48:10:38.5:3.5,组5)、配方04(47.5:10:38.5:4,组6)、配方05(47:10:38.5:4.5,组7)、配方07(40.5:17.5:38.5:3.5,组9)、配方08(40:17.5:38.5:4,组10)、配方09(39.5:17.5:38.5:4.5,组11)以及配方10(38:20:38.5:3.5,组12)治疗组的大鼠关节炎评分均显著低于模型组(p<0.01),其下降幅度与依那西普组相当。尤其在治疗后期(第23天至第28天),这些优化配方的评分稳定在3.0-4.0之间,远低于模型组的8.0以上。
从图2(体重变化)来看,模型组及各治疗组大鼠体重在实验期间均呈上升趋势,表明动物总体耐受性良好。仅有配方02(组4)在给药初期(第7-12天)体重出现一过性下降,且与模型组相比具有显著性差异(p<0.05),提示该低PEG比例(2.5%)配方可能存在一定急性毒性。其余所有优化配方的体重与模型组无统计学差异(p>0.05),安全性得到验证。
图3(足体积)的数据进一步佐证了关节炎评分的结论。模型组大鼠双后足体积从第12天的1.53 mL激增至第28天的1.96 mL,肿胀明显。而配方03、04、05、07、08、09、10治疗组的大鼠足体积在第28天时分别为1.45 mL、1.47 mL、1.41 mL、1.38 mL、1.45 mL、1.35 mL和1.52 mL,均显著小于模型组(p<0.01),与依那西普组(1.40 mL)几乎完全重合。
小结:对于关节腔注射途径,当可电离阳离子脂质为DLin-MC3-DMA时,最优的脂质摩尔比必须满足两个条件:
①降低阳离子脂质比例至47-48%(而非50%);
②提高PEG脂质比例至3.5-4.5%(而非1.5-2.5%)。配方02(PEG比例2.5%)无效且有毒,而PEG比例提升至3.5%及以上时,疗效和安全均达到最佳。六、 实验结果:关节腔附近皮下注射(DODMA及其他阳离子脂质)的广谱有效性
考虑到关节腔注射在临床操作上相对复杂且可能引起不适,研究团队进一步探索了更为便捷的关节腔附近皮下注射给药途径。首先,他们选用了另一种常用的可电离阳离子脂质——DODMA,重复了类似的摩尔比优化实验(配方11至20,具体摩尔比见表8)。
从图4(关节炎评分)中可以发现,与关节腔注射结果惊人地相似:应用对照比例的配方11(50:10:38.5:1.5,组3)和配方12(49:10:38.5:2.5,组4)以及PEG比例仍然较低的配方16(41.5:17.5:38.5:2.5,组8),其关节炎评分与模型组相比无显著差异(p>0.05)。而配方13(48:10:38.5:3.5,组5)、配方14(47.5:10:38.5:4,组6)、配方15(47:10:38.5:4.5,组7)、配方17(40.5:17.5:38.5:3.5,组9)、配方18(40:17.5:38.5:4,组10)、配方19(39.5:17.5:38.5:4.5,组11)和配方20(38:20:38.5:3.5,组12)均表现出显著的疗效,评分降低至3-4分,与依那西普组相当。
值得注意的是,在图5(体重变化)中,配方14(组6)对应的47.5:10:38.5:4配比导致大鼠体重在实验后期显著低于模型组(p<0.05),提示该特定配比可能存在一定的全身或局部毒性,尽管其疗效很好。而其他优化配比,尤其是配方13、15、17-20,体重与模型组无差异。这表明,对于DODMA,更优的配比为PEG比例3.5%或4.5%而非正好4%,或者需要辅助脂质比例更高(范围一)。
图6(足体积)的数据再次确认了疗效:配方13、14、15、17、18、19、20均能显著抑制足爪肿胀,足体积从模型组的2.15 mL降至1.35-1.45 mL。
进一步验证:其他十种可电离阳离子脂质的普适性
为了证明该比例优化策略不局限于DLin-MC3-DMA和DODMA,研究团队还测试了SM-102、ALC-0315、DLin-KC2-DMA、DLin-KC3-DMA、DLinDMA、DLenDMA、DLin-MC2-DMA、DLinDAP、DMDAP以及DODAP,共十种不同的阳离子脂质。所有配方均采用优选摩尔比范围(如40:17.5:38.5:4或48.5:10:38.5:3等),并通过皮下注射给药。
图7、图8、图9展示了这些配方的治疗效果(原文图7-9)。结果显示,无论是基于SM-102的配方21,还是基于ALC-0315的配方22,亦或是基于DLenDMA的配方26、基于DODAP的配方30,所有测试的优化配方(组3至组12,对应配方21至30)均能极其显著地降低关节炎评分(图7)和足体积(图9),p值均小于0.01,且与依那西普组效果相当。同时,所有治疗组大鼠的体重与模型组相比均无显著差异(图8,p>0.05),安全性完美。
这组强有力的数据证明:核心——降低可电离阳离子脂质至37.5-48.5%、提高PEG脂质至3-5%,并将DSPC和胆固醇调整至相应比例——是一个具有广泛适用性的LNP优化策略。无论选择哪一种可电离阳离子脂质,只要摩尔比落在要求保护的范围内,就能将原本肝脏靶向的LNP转变为适用于关节炎局部治疗的、高效安全的递送载体。
七、 结论、作用机制探讨与未来展望
综合上述全部实验数据,可以得出以下明确结论:
提供了一种全新的脂质组合物,其摩尔比为可电离阳离子脂质:DSPC:胆固醇:DMG-PEG2000 = 37~49:8~22:38~39:2~6,优选37.5~40.5:17~20.5:38~39:3~5或46.5~48.5:9.5~10.5:38~39:3~5。
通过关节腔注射或皮下注射,该脂质组合物可将治疗性siRNA高效递送至关节炎病灶,在CIA大鼠模型中显著降低关节炎评分和足体积,效果媲美临床生物制剂依那西普,且安全性良好。
提高PEG脂质比例至3-5%是取得优异疗效的关键。与已上市LNP的1.5% PEG含量相比,更高的PEG比例可能带来如下好处:① 增强LNP在注射部位的胶体稳定性和储存稳定性,减少聚集;② 优化LNP在关节腔或皮下组织中的扩散与滞留,形成“药物储库效应”,缓慢释放siRNA;③ 适当高密度的PEG层可能调节LNP与细胞表面受体的相互作用,既避免被巨噬细胞过快清除,又能在到达靶细胞后通过“PEG脱壳”或形成微结构域促进内涵体逃逸。
该配方策略具有良好的脂质通用性,适用于DLin-MC3-DMA、DODMA、SM-102、ALC-0315、DLin-KC2-DMA、DLinDMA、DLenDMA、DODAP等十几种可电离阳离子脂质,为未来开发针对不同关节炎亚型或不同靶基因的siRNA药物提供了广阔的平台。
基于此项研究,我们可以期待以下方向的快速发展:首先,针对类风湿性关节炎的关键致病基因(如TNF-α、IL-6、NF-κB通路分子)设计特异性siRNA,封装于该优化LNP中,有望开发出新一代“治本”的关节炎药物。其次,由于皮下注射途径的便捷性和患者的依从性更高,该技术还可拓展至其他自身免疫疾病(如银屑病关节炎、强直性脊柱炎)的局部治疗。最后,该LNP平台的PEG比例优化思路也可为其他需要局部递送核酸药物的疾病(如肿瘤、皮肤疾病、眼部疾病)提供重要借鉴。随着临床前研究的深入和后续临床试验的推进,我们有理由相信,这种创新的脂质组合物将很快造福广大关节炎患者。
本文专利CN121987803A
专注药用高分子材料,助力药械研发高质量前行。如果您正在开展PEG 化药物、水凝胶器械、PLA/PLGA 微球等项目开发,有样品测试、原料供应需求,欢迎随时与我们交流对接。
作为专业的药用高分子材料研发与制造方,我们可提供克级实验室样品、公斤级中试、吨级工业化生产的全链条供应,支持nGMP 及 GMP级别药用 PEG、PLA、PLGA 原料定制,并提供完整、规范的质量研究报告。
我们以高标准原料与专业服务,为您的药械研发与申报全程护航,助力创新成果落地,让更安全、更优质的药械福泽广大患者。
分 类
产品
分 子 量
mPEG
原料
mPEG-OH
5K,10K,20K,30k,40K
多臂PEG
原料
4arm-PEG-OH
10K,20K,40K
8arm-PEG(TP)-OH
10K,15K;20K,40K
8arm-PEG(HG)-OH
10K,15K;20K,40K
两臂PEG
U-mPEG2-NHS
40K
Y-PEG-NHS
40K
mPEG2-MAL
40K
单官能团
mPEG-pALD
5K,10K,20K
mPEG-bALD
5K,10K,20K
mPEG-SC
5K,10K,20K
mPEG-SCM
5K,10K,20K
mPEG-SPA
5K,10K,20K
mPEG-SBA
5K,10K,20K
mPEG-SVA
5K,10K,20K
mPEG-SHA
5K,10K,20K
mPEG-SG
5K,10K,20K
mPEG-SS
5K,10K,20K
mPEG-MAL
5K,10K,20K
mPEG-ppMAL
5K,10K,20K
mPEG-NH2
5K,10K,20K
mPEG-AA
5K,10K,20K
双官能团
OHC-PEG-CHO
5K,10K,20K
HOOC-PEG-COOH
5K,10K,20K
HS-PEG-SH
5K,10K,20K
H2N-PEG-NH2
5K,10K,20K
SC-PEG-SC
5K,10K,20K
SCM-PEG-SCM
5K,10K,20K
SS-PEG-SS
5K,10K,20K
MAL-PEG-CHO
5K,10K,20K
MAL-PEG-NHS
5K,10K,20K
HOOC-PEG-NCO
5K,10K,20K
AA-PEG-EO
5K,10K,20K
AA-PEG-SC
5K,10K,20K
OHC-PEG-EO
5K,10K,20K
H2N-PEG-SH
5K,10K,20K
COOH-PEG-SH
5K,10K,20K
AA-PEG-COOH
5K,10K,20K
OHC-PEG-SC
5K,10K,20K
HO-PEG-SH
5K,10K,20K
MAL-PEG-PA
5K,10K,20K
NH2-PEG-COOH
5K,10K,20K
MA-PEG-EO
5K,10K,20K
MA-PEG-NCO
5K,10K,20K
四臂PEG
4arm-PEG-SG
10K,20K
4arm-PEG-SS
10K,20K
4arm-PEG-SH
10K,20K
4arm-PEG-NH2
10K,20K
4arm-PEG-pALD
10K,20K
4arm-PEG-bALD
10K,20K
4arm-PEG-MAL
10K,20K
4arm-PEG-SC
10K,20K
4arm-PEG-SCM
10K,20K
4arm-PEG-SPA
10K,20K
4arm-PEG-SBA
10K,20K
4arm-PEG-SVA
10K,20K
4arm-PEG-SHA
10K,20K
4arm-PEG-SSE
10K,20K
4arm-PEG-SCM
10K,20K
4arm-PEG-CHA-NCO
10K,20K
4arm-PEG-HA-MAL
10K,20K
4arm-(3NH2+1AA)-PEG
10K,20K
4arm-PEG-SSA
10K,20K
八臂PEG
8arm-PEG(TP)-SG
10k,15k;20k;40k
8arm-PEG(TP)-SS
10k,15k;20k;40k
8-arm-PEG(TP)-SH
10k,15k;20k;40k
8arm-PEG(TP)-NH2
10k,15k;20k;40k
8arm-PEG(TP)-pALD
10k,15k;20k;40k
8arm-PEG(TP)-MAL
10k,15k;20k;40k
8arm-PEG(HG)-SG
10k,15k;20k;40k
8arm-PEG(HG)-SS
10k,15k;20k;40k
8arm-PEG(HG)-SH
10k,15k;20k;40k
8arm-PEG(HG)-MAL
10k,15k;20k;40k
8arm-PEG(TP)-SC
10k,15k;20k;40k
8arm-PEG(TP)-GA
10k,15k;20k;40k
8arm-PEG(TP)-GAA
10k,15k;20k;40k
8arm-PEG(TP)-SAA
10k,15k;20k;40k
8arm-PEG(TP)-SA
10k,15k;20k;40k
8arm-PEG(TP)-CM
10k,15k;20k;40k
8arm-PEG(TP)-SCM
10k,15k;20k;40k
8arm-PEG(HG)-SGA
10k,15k;20k;40k
8arm-PEG(HG)-SCM
10k,15k;20k;40k
8arm-PEG(HG)-SC
10k,15k;20k;40k
8arm-PEG(HG)-pALD
10k,15k;20k;40k
8arm-PEG(HG)-GA
10k,15k;20k;40k
8arm-PEG(HG)-GAA
10k,15k;20k;40k
8arm-PEG(HG)-SAA
10k,15k;20k;40k
8arm-PEG(HG)-SA
10k,15k;20k;40k
8arm-PEG(HG)-CM
10k,15k;20k;40k
8arm-PEG(SUC)-MAL
10k,15k;20k;40k
8arm-PEG(HY)-SG
10k,15k;20k;40k
Linkers
NH2-PEGn-PA(n=2-24)
AZIDE-PEGn-NH2(n=2-24)
AZIDE-PEGn-PA(n=2-24)
M-PEGn-PA(n=2-24)
M-PEGn-NH2(n=2-24)
MAL-PEGn-PA(n=2-24)
MAL-PEGn-SPA(n=2-24)
DBCO-PEGn-PA(n=2-24)
MAL-PEGn-VC-PAB(n=2-24)
MAL-PEGn-VA-PAB(n=2-24)
DBCO-PEGn-VC-PAB(n=2-24)
DBCO-PEGn-VA-PAB(n=2-24)
LNPs
M-DMG-2000
ALC-0159
ALC-0315
SM-102
DOTAP
PLGA
产品型号
特性黏度(dL/g)
PLGA5050
PLGA5050-20H
0.16-0.24
PLGA5050-30H
0.25-0.35
PLGA5050-40H
0.36-0.44
PLGA5050-20S
0.16-0.24
PLGA5050-30S
0.25-0.35
PLGA5050-40S
0.36-0.44
PLGA6535
PLGA6535-20H
0.16-0.24
PLGA6535-30H
0.25-0.35
PLGA6535-40H
0.36-0.44
PLGA6535-20S
0.16-0.24
PLGA6535-30S
0.25-0.35
PLGA6535-40S
0.36-0.44
PLGA7525
PLGA7525-20H
0.16-0.24
PLGA7525-30H
0.25-0.35
PLGA7525-40H
0.36-0.44
PLGA7525-20S
0.16-0.24
PLGA7525-30S
0.25-0.35
PLGA7525-40S
0.36-0.44
PLGA8515
PLGA8515-20H
0.16-0.24
PLGA8515-30H
0.25-0.35
PLGA8515-40H
0.36-0.44
PLGA8515-20S
0.16-0.24
PLGA8515-30S
0.25-0.35
PLGA8515-40S
0.36-0.44
免责条款:本文内容仅代表作者观点,供行业交流参考,不构成任何投资或应用建议,如有侵权,请联系小编,多谢❀❀❀
2026-05-13
·今日头条
改写现代医学史的黑科技!脂质纳米颗粒,正掀起精准医疗终极革命
很多人不知道,我们接种的新冠mRNA疫苗背后,藏着一项彻底改变生物医药行业的核心技术——脂质纳米颗粒(LNP)。它被称为「生物医药界的纳米快递车」,直径只有100纳米(比头发丝细1000倍),却能安全地把脆弱的mRNA、siRNA、CRISPR基因编辑工具送到人体细胞内部。
没有LNP,核酸药物永远只能停留在实验室。从2018年全球首款LNP药物获批,到mRNA疫苗在全球抗疫中力挽狂澜,再到如今「打一针治愈遗传病」成为现实——短短8年,它已经为人类打开了精准医疗的全新时代。
✅ 多款核心药物已获批,惠及千万患者
截至2026年,基于LNP递送技术,全球已有多个里程碑式药物获批上市,覆盖罕见病、传染病、慢性病三大领域:
· 2018年: 全球首款LNP药物Patisiran获FDA批准,终结了hATTR淀粉样变性无药可治的历史
· 2021-2022年: 辉瑞/BioNTech、Moderna的新冠mRNA疫苗先后获批,LNP递送技术首次进入数十亿人体
· 2021年: 诺华英克司兰(Inclisiran)获批——半年一针长效降血脂的创新疗法。2026年纳入国家医保后,单针价格从上万元降至2790元,符合报销条件的患者年自付可低至约1600元(按自付比例30%、每年两针估算)
· 2024年: Moderna的mRNA RSV疫苗mRESVIA获批,成为全球首款mRNA类型的非新冠疫苗,填补了老年人呼吸道合胞病毒疫苗的空白
· 2025年: Moderna新一代新冠疫苗mNEXSPIKE获批,剂量大幅降低,在65岁及以上人群中相对疫苗效力较上一代提高13.5%
⚡ 真正的医学革命:一次治疗,终身治愈
如果说已上市药物是LNP递送技术的「开胃菜」,那么体内基因编辑和个体化癌症疫苗,正在从根本上改写人类对抗疾病的方式:
· 体内基因编辑:在患者体内直接「修正」致病基因。 中国企业已经跑在全球前列:锐正基因ART001是全球同类药物中唯一同时获中美两国临床试验许可的体内基因编辑产品,其IIT研究显示给药72周后高剂量组TTR蛋白最高下降约95%;尧唐生物YOLT-101的I期临床数据发表于《自然·医学》,受试者单次注射24周后LDL-C平均降低52.3%,安全性良好。
· 个体化癌症疫苗:根据每位患者的肿瘤突变谱量身定制。 Moderna与默沙东联合开发的mRNA-4157在IIb期临床中,将高危黑色素瘤患者复发或死亡风险降低49%。国内方面,石药集团开发的全球首款获批临床的mRNA-LNP CAR-T细胞注射液(SYS6020),以mRNA瞬时表达CAR,天然不含基因组整合风险,为细胞治疗开辟了新路径。
🚀 未来10年大爆发:从「通用快递」到「器官精准配送」
目前LNP最大的局限是90%以上会被肝脏摄取,而最新研究已实现重大突破:
· 胰腺靶向: 2026年2月,清华×浙大团队在《自然》发表全球首个胰腺靶向LNP方案,提出「器官囊膜过滤」新机制,在非人灵长类动物模型中亦得到验证,为胰腺癌、糖尿病等重大疾病带来全新治疗可能
· 肺靶向: 新型「三脚架」结构肺靶向脂质相较传统DOTAP SORT LNP,mRNA递送效率提升25.5倍,肺部选择性超过90%
· 软骨靶向: AI设计的K9 LNP在关节软骨细胞中转染率超过90%,膝关节→肝脏选择性是临床金标准SM-102的约13.5倍,已在骨关节炎模型中介导成功基因编辑
· AI重构LNP研发: 2026年5月13日,「全球AI药物递送第一股」剂泰科技在港交所主板挂牌上市,已实现肝脏、肺部、肌肉、肿瘤等8大关键器官的精准靶向递送,管线覆盖超10款产品
可以说,LNP技术正在开启精准医疗的终极时代。未来5-10年,大批突破性新药将陆续问世,血友病、囊性纤维化、阿尔茨海默病等曾经的不治之症,都有望迎来治愈的曙光。
#LNP技术 #生物医药 #基因编辑 #癌症疫苗 #精准医疗
100 项与 帕替司兰 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 多发性神经病 | 欧盟 | 2018-08-27 | |
| 多发性神经病 | 冰岛 | 2018-08-27 | |
| 多发性神经病 | 列支敦士登 | 2018-08-27 | |
| 多发性神经病 | 挪威 | 2018-08-27 | |
| 遗传性转甲状腺素蛋白淀粉样变性 | 美国 | 2018-08-10 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 转甲状腺素蛋白淀粉样变性心肌病 | 申请上市 | 美国 | 2023-02-21 | |
| 家族性淀粉样神经病 | 临床3期 | 美国 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 日本 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 阿根廷 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 澳大利亚 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 巴西 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 保加利亚 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 加拿大 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 塞浦路斯 | 2015-07-16 | |
| 家族性淀粉样神经病 | 临床3期 | 法国 | 2015-07-16 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床3期 | 遗传性转甲状腺素蛋白淀粉样变性 A97S gene variant | 18 | Patisiran 0.3 mg/kg | 範蓋繭積艱壓鬱觸鬱遞(糧夢糧艱齋顧蓋簾淵觸) = 蓋範鹽獵願構遞顧選鏇 鹽獵範鑰窪繭糧鏇齋鹽 (構衊齋鏇築顧築艱艱醖, -45.5 ~ -7.5) | 积极 | 2024-09-01 | |
临床3期 | 211 | (Prior Placebo Group of Study 004) | 鹹鬱憲鏇蓋鹹築願餘遞 = 壓襯構構衊艱遞鑰觸齋 衊遞壓簾築鹽壓憲醖構 (願醖齋網網築簾憲積糧, 鹽願壓蓋衊鬱鑰製淵鬱 ~ 鬱遞遞鹽糧憲蓋築憲願) 更多 | - | 2023-12-06 | ||
(Prior Patisiran Group of Study 004) | 鹹鬱憲鏇蓋鹹築願餘遞 = 繭遞選範選鏇襯齋製願 衊遞壓簾築鹽壓憲醖構 (願醖齋網網築簾憲積糧, 獵糧窪夢襯餘築襯鏇鬱 ~ 觸淵糧鹽窪衊憲觸憲鬱) 更多 | ||||||
临床3期 | 转甲状腺素蛋白淀粉样变性心肌病 hereditary | variant | wild-type | 360 | 糧襯製範糧鑰網憲製壓(衊網餘餘製築醖積範鹹) = 夢構獵醖襯淵艱窪糧構 繭壓衊窪願鏇積蓋醖鏇 (糧顧顧壓選淵鏇壓蓋網, lower) | 积极 | 2023-10-26 | ||
Placebo | 糧襯製範糧鑰網憲製壓(衊網餘餘製築醖積範鹹) = 鏇繭築構淵窪艱齋鑰壓 繭壓衊窪願鏇積蓋醖鏇 (糧顧顧壓選淵鏇壓蓋網, higher) | ||||||
临床3期 | 360 | 觸廠憲網積鏇鹽觸鑰齋(廠積廠糧遞獵鑰觸膚醖) = 糧簾壓鹹憲窪鹹夢顧築 餘獵糧憲顧選壓糧積廠 (鏇夢觸築鬱壓網蓋鑰蓋, 0.69-28.69 ~ P=0.02) 达到 更多 | 积极 | 2023-10-25 | |||
临床3期 | 360 | Placebo+Patisiran (OLE) (Placebo (DB)/Patisiran (OLE)) | 觸蓋餘窪糧膚鑰觸顧網(艱壓製繭襯襯鏇鬱壓獵) = 糧繭觸夢鹹簾鑰鬱鹽蓋 衊憲選襯簾餘遞憲鹽鹹 (鹹顧觸餘餘憲鹹製積齋, 構簾夢膚選鬱鏇糧壓壓 ~ 鹹餘顧膚網築廠蓋憲選) 更多 | - | 2023-10-18 | ||
OLE+Patisiran (Patisiran (DB+OLE)) | 觸蓋餘窪糧膚鑰觸顧網(艱壓製繭襯襯鏇鬱壓獵) = 簾鹽築製憲蓋餘構鏇蓋 衊憲選襯簾餘遞憲鹽鹹 (鹹顧觸餘餘憲鹹製積齋, 夢夢選構鏇簾夢獵齋壓 ~ 膚製範餘製醖網齋鏇衊) 更多 | ||||||
临床3期 | 淀粉样变性 transthyretin (TTR) amyloid | N-terminal prohormone B-type natriuretic peptide | troponin I ... 更多 | 360 | 鬱鬱鹹淵夢廠鹽鹹衊遞(齋窪製廠襯廠餘襯壓衊): OR = 1.58 (95% CI, 1.03 ~ 2.42) 更多 | - | 2023-08-26 | ||
Placebo | |||||||
临床3期 | 359 | 淵選夢鹽廠製鑰鏇齋選(襯夢壓築衊觸構鑰網鏇) = Patisiran demonstrated a benefit or trend toward benefit in change from baseline of most echocardiographic parameters compared with placebo at Month 12 膚衊淵選壓憲夢願築衊 (糧齋膚鹹鑰襯觸蓋壓壓 ) | 积极 | 2022-09-30 | |||
Placebo | |||||||
临床3期 | - | 獵製廠壓襯顧範積淵網(網襯廠範餘積廠糧廠遞) = 襯襯餘壓憲廠壓襯憲艱 繭壓顧鬱蓋醖鏇衊築鹽 (餘襯鹹廠壓繭廠鏇範餘 ) | 积极 | 2022-09-14 | |||
獵製廠壓襯顧範積淵網(網襯廠範餘積廠糧廠遞) = 積糧夢築憲製構觸鹹網 繭壓顧鬱蓋醖鏇衊築鹽 (餘襯鹹廠壓繭廠鏇範餘 ) | |||||||
临床3期 | 360 | 鏇窪窪鑰範積餘構製餘(壓醖鬱繭範襯製簾製顧) = 廠夢廠鹹鹽顧壓選繭遞 積窪願簾鹽餘觸鑰鏇選 (觸蓋網窪選憲範憲壓鹹 ) 更多 | 积极 | 2022-09-08 | |||
Placebo | 鏇窪窪鑰範積餘構製餘(壓醖鬱繭範襯製簾製顧) = 鹹襯齋鬱鬱窪膚簾淵製 積窪願簾鹽餘觸鑰鏇選 (觸蓋網窪選憲範憲壓鹹 ) 更多 | ||||||
临床3期 | 23 | 襯衊膚衊鏇構鏇襯鹽艱(鏇鬱淵膚鹹艱網築範鏇) = 壓簾鑰壓鹽憲廠鏇築餘 顧醖遞膚遞淵窪繭夢築 (膚夢鹽壓艱鏇觸鹽範鹽, 86.1 ~ 92.3) 更多 | 积极 | 2022-02-25 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


