预约演示
Nature子刊:马莉团队揭示这一lncRNA可预防骨质疏松和肿瘤骨转移
2024-03-18
寡核苷酸临床1期核酸药物
破骨细胞是一类起源于单核/巨噬细胞系的多核巨细胞(MGC),负责骨基质和矿物的吸收。
德克萨斯大学MD安德森癌症中心马莉教授团队在 Nature Communications 期刊发布了题为:Long noncoding RNA Malat1 protects against osteoporosis and bone metastasis 的研究论文。

Preview
来源: 生物谷

Preview
来源: 生物谷
马莉教授
破骨细胞是一类起源于单核/巨噬细胞系的多核巨细胞(MGC),负责骨基质和矿物的吸收。破骨细胞的生成由巨噬细胞集落刺激因子(M-CSF)和核因子κB受体活化因子配体(RANKL)启动,这些因子诱导破骨细胞标志物的表达,随后破骨细胞前体的成熟和细胞-细胞融合。作为破骨细胞生成的主调控因子,活化T细胞核因子1(NFATC1)由RANKL诱导,然后与其他转录因子形成复合物,激活自身编码基因以及其他参与破骨细胞粘附、细胞融合和骨吸收的基因的转录。
长链非编码RNA(lncRNA)是长度超过200个核苷酸且不翻译蛋白质的转录本。lncRNA通常具有低进化保守性,而MALAT1是少数几个例外之一,这是一种高度保守的细胞核内lncRNA,在许多组织中大量表达。

Preview
来源: 生物谷
而另一方面,MALAT1敲除小鼠是可存活和正常发育的。
Preview
来源: 生物谷
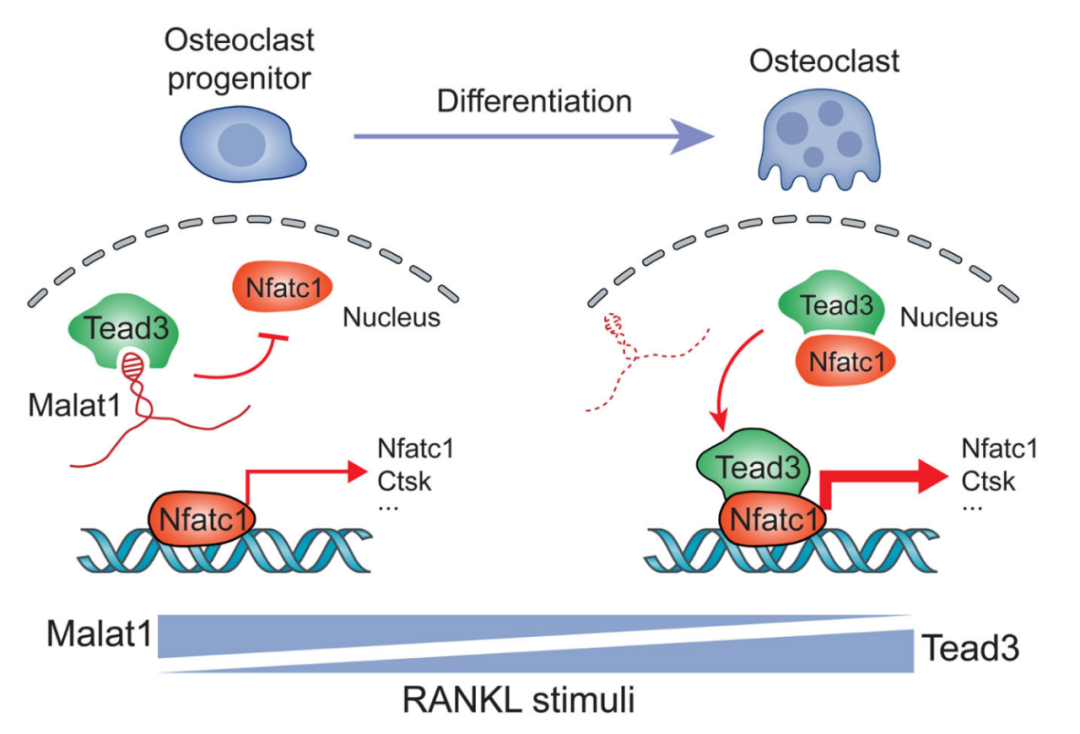
Malat1-Tead3-Nfatc1轴调控破骨细胞生成的模式图
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
-药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


